Область техники
Изобретение относится к области медицины, конкретно к перевязочным материалам для лечения гнойных и инфицированных ран, трофических язв и для профилактики нагноений инфицированных ран.
Уровень техники
В медицинской практике известно использование протеолитических ферментных препаратов для лечения гнойно-воспалительных заболеваний. Однако ферментные препараты дороги и дефицитны и, несмотря на высокую лечебную эффективность, не стойки по отношению к ингибиторам, содержащимся в раневом отделяемом (продуктах развития раневого процесса), к изменениям pH и температуры. При поступлении в рану ферменты быстро инактивируются, в связи с чем в процессе лечения требуется большой расход ферментов.
Для снижения расхода ферментов при лечении гнойных и инфицированных ран были созданы терапевтические перевязочные материалы, в том числе раневые повязки, как с раноочищающим, так и антимикробным действием (см., например, патенты RU №2142818 и №2357753).
В изобретении по патенту RU №2357753, который выбран в качестве ближайшего аналога заявляемого изобретения, предложена раневая повязка с антимикробными свойствами.
По данному изобретению раневая повязка с антимикробными свойствами содержит текстильный носитель на основе диальдегидцеллюлозы с иммобилизированными на ее волокнах после водной обработки протеолитическим ферментом и антимикробным препаратом.
Для получения раневой повязки с антимикробными свойствами используют целлюлозосодержащий текстильный носитель, предпочтительно медицинскую марлю на основе хлопковой целлюлозы. Названный текстильный носитель активируют, предпочтительно, с использованием раствора периодата натрия, выдерживают в данном растворе, отмывают водой и высушивают с получением диальдегидцеллюлозы.
В результате модификации исходного материала до диальдегидцеллюлозы изменяется молекулярная структура волокон целлюлозы с формированием реакционно-способных альдегидных групп, к которым присоединяются аминогруппы боковых цепей используемого фермента, предпочтительно, трипсина.
В качестве антимикробного препарата в раневой повязке по данному изобретению используют бактериолитический фермент - лизоцим.
Однако известный бактериолитический фермент имеет ограниченный спектр антимикробного действия. Лизоцим эффективен против грамположительных бактерий и вследствие своего специфического действия не оказывает влияния на грамотрицательные бактерии и на грибковые микроорганизмы, которые могут находиться в мягких тканях с гнойным воспалением, в гнойном экссудате.
В результате ухудшается лечебная эффективность перевязочного материала с протеолитическим ферментом - трипсином, обеспечивающим очищение ран от гнойно-некротических масс.
Исследования данной раневой повязки показали наличие значительной остаточной микробной обсемененности при ее применении.
Известно, что в медицинской практике значительное внимание уделяется антимикробным препаратам, содержащим в своем составе такие металлы, как Ag, Au, Pt, Pd, Сu и Zn (см. Н.Е.Morton, Pseudomonas in Disinfection, Sterilisation and Preservation, ed. S.S.Block, Lea and Febider 1977 и N.Grier, Silver and Its Compounds in Disinfection, Sterilisation and Preservation, ed. S.S.Block, Lea and Febider, 1977).
В частности, в известном техническом решении (см. патент RU №2361029) предложено использование антисептического препарата на основе природных минеральных компонентов, отвечающих требованиям экологичности и безопасности.
В данном техническом решении в качестве антисептического препарата для обработки целлюлозосодержащих материалов используют наноструктурированный порошок бентонита, интеркалированный ионами металлов Ag+ или/и Сu2+.
Известное техническое решение используется при изготовлении бумажной продукции, в том числе санитарно-гигиенического назначения, для улучшения антибактериальных и противогрибковых свойств.
Однако из данного технического решения не следует:
- целесообразность использования данного антисептического препарата для перевязочных материалов, в том числе раневых повязок на основе диальдегидцеллюлозы с иммобилизированным протеолитическим ферментом;
- целесообразность использования данного антисептического препарата в составе названных перевязочных материалов для улучшения их лечебных свойств и уменьшения микробной обсемененности гнойно-некротических ран.
Раскрытие изобретения
Технический результат изобретения состоит в создании раневой повязки с антимикробными свойствами на основе биологических и минеральных компонентов, синергетическое взаимодействие которых улучшает лечебные свойства перевязочного материала и его антимикробную активность в отношении широкого спектра грамположительных, грамотрицательных бактерий и грибковых микроорганизмов при обработке ран с признаками гнойно-воспалительного процесса.
Для решения поставленной технической задачи предложена раневая повязка с антимикробными свойствами, содержащая текстильный носитель на основе диальдегидцеллюлозы (ДАЦ) с иммобилизированными протеолитическим ферментом и антимикробным препаратом, согласно изобретению в качестве антимикробного препарата используют наноструктурированный порошок бентонита, интеркалированный ионами металлов Ag+, или/и Сu2+, или/и Zn2+, при этом раневая повязка имеет следующее содержание в ней компонентов, мас.%:
Согласно изобретению смесь порошков бентонита, интеркалированных ионами Ag+ и ионами Сu2+, имеет соотношение, как 0,5:1,0 (вес.ч.);
смесь порошков бентонита, интеркалированных ионами Ag+ и ионами Zn2+, имеет соотношение, как 0,5:1,0 (вес.ч.);
смесь порошков бентонита, интеркалированных ионами Сu2+ и ионами Zn2+, имеет соотношение, как 1,0: 1,0 (вес.ч.);
смесь порошков бентонита, интеркалированных ионами Ag+, ионами Сu2+ и ионами Zn2+, имеет соотношение, как 0,5:1,0:1,0 (вес.ч.).
Согласно изобретению в качестве протеолитического фермента используют трипсин.
Согласно изобретению диальдегидцеллюлоза, с иммобилизированными трипсином и антимикробным препаратом, имеет влажность не более 10%.
Согласно изобретению размер частиц наноструктурированного порошка бентонита - не более 100 нм.
Согласно изобретению наноструктурированные порошки бентонита содержат 2,0-6,0 мас.% названных выше металлов, интеркалированных в бентонит.
Согласно изобретению для иммобилизации антимикробного препарата на диальдегидцеллюлозе используют гидрозоль, содержащий 5,0-10,0 мас.%, наноструктурированного порошка бентонита, интеркалированного ионами названных металлов.
При реализации изобретения улучшаются лечебные свойства раневой повязки и ее антимикробная активность в отношении широкого спектра грамположительных, грамотрицательных бактерий и грибковых микроорганизмов.
Достигаемый в изобретении технический результат объясняется:
- использованием при создании раневой повязки с антимикробными свойствами биологических и минеральных компонентов, синергетическое взаимодействие которых способствует достижению указанного результата;
- использованием для изготовления раневой повязки диальдегидцеллюлозы, молекулярная структура волокон которой обеспечивает как химическую иммобилизацию к ним функциональных групп протеолитического фермента, так и эффективное сорбционное взаимодействие с антибактериальным препаратом на основе наноструктурированного порошка бентонита, интеркалированного ионами названных металлов;
- использованием антибактериального препарата в виде наноструктурированного порошка бентонита, интеркалированного ионами металлов Ag+, Cu2+, Zn2+, обеспечивающего большую площадь контакта с бактериальной средой и эффективное пролонгирующее воздействие на патогенную микрофлору в отношении широкого спектра грамположительных, грамотрицательных бактерий и грибковых микроорганизмов;
- использованием минерального антибактериального препарата, содержащего ионы металлов Ag+, Cu2+, Zn2+, участвующих в реакциях ионного замещения и не оказывающих отрицательного действия (аллергического, отечного) на обрабатываемые зоны тканей живого организма;
- использованием антибактериального препарата в виде наноструктурированного порошка бентонита, интеркалированного ионами Zn2+, обладающего как антимикробными, противогрибковыми свойствами, так и регенерирующим, ранозаживляющим эффектом (свойственным металлу Zn). Названные свойства цинка широко используются в медицинской практике для изготовления антисептических, регенерирующих и ранозаживляющих средств при дерматитах, гнойно-воспалительных заболеваниях кожи;
- технологическим решением раневой повязки (перевязочного материала) на основе компонентов биологически совместимых с тканями живых организмов.
При реализации заявляемого изобретения, благодаря иммобилизации на раневой повязке антимикробного препарата на основе смеси наноструктруированных порошков бентонита, интеркалированных ионами названных металлов, улучшаются антимикробные свойства повязок. Данные обстоятельства объясняются широким спектром биоцидных свойств указанных металлов, которым традиционно свойственны биоактивные, антибактериальные, фунгицидные (антигрибковые) свойства, что определяет их применение в продукции санитарно-гигиенического и медицинского назначения, предназначенной для контактного использования с кожными покровами.
Использование при иммобилизации на раневую повязку антимикробного препарата в виде гидрозоля, содержащего указанные выше наноструктурированные порошки бентонита, улучшает процесс распределения данного препарата на раневой повязке, уменьшает затратную часть по его применению.
При анализе известного уровня техники не выявлено технических решений с совокупностью признаков, соответствующих заявляемому изобретению и реализующих вышеописанный результат по антимикробному и противогрибковому воздействию на обрабатываемые раневые зоны с признаками гнойно-воспалительного процесса, с гнойной экссудацией.
Приведенный анализ известного уровня техники свидетельствует о соответствии заявляемого технического решения критериям - «новизна», «изобретательский уровень».
Заявляемое техническое решение может быть промышленно реализовано для получения раневых повязок с антимикробными свойствами для обработки раневых, ожоговых, язвенных зон кожных покровов.
Для реализации изобретения используют медицинское и лабораторное оборудование, товарные продукты, в том числе:
терапевтический материал, который изготовлен по технологическому процессу, описанному в изобретении по патенту RU №2142818.
В соответствии с данным техническим решением для получения диальдегидцеллюлозы использовали целлюлозосодержащий текстильный носитель, предпочтительно, медицинскую марлю на основе хлопковой целлюлозы.
Названный текстильный носитель активировали раствором периодата натрия. На волокнах диальдегидцеллюлозы после водной обработки иммобилизировали протеолитический фермент - трипсин. Для водной обработки диальдегидцеллюлозы использовали трипсин в фосфатном буферном растворе при pH 5.5.
Для реализации заявляемого изобретения использовали:
6,0 г йодной кислоты на 3,3 л дистиллированной воды; 1,0 г едкого натра на 3,3 л дистиллированной воды для получения раствора периодата натрия с pH 5,0, которым обрабатывали 1 кг медицинской марли. В результате был получен текстильный носитель на основе диальдегидцеллюлозы.
На полученную диальдегидцеллюлозу иммобилизировали протеолитический фермент - трипсин. Для приготовления раствора трипсина в фосфатном буферном растворе с pH 5,5 использовали 3,3 л дистиллированной воды.
Были получены 0,01%; 0,007%; 0,03% растворы трипсина, которыми обрабатывали активированные текстильные материалы. Были получены терапевтические материалы (раневые повязки) с содержанием в них протеолитического фермента соответственно 0,02; 0,03, 0, 09 мас.% на массу диальдегидцеллюлозы.
Из полученных терапевтических материалов были изготовлены образцы повязок размером 10 см × 10 см и весом - 1,9 г каждая.
Количественное содержание в раневой повязке протеолитического фермента, заданного по изобретению, оптимально и обосновано клиническими исследованиями этих терапевтических материалов, уменьшение его количества снижает терапевтическую эффективность раневой повязки по процессу очищения ран от гнойных и некротических масс, а увеличение повышает затратную часть на изготовление повязки.
Ковалентно связанный с реакционно-способными группами диальдегидцеллюлозы трипсин обладает выраженным некролитическим действием, ускоряет очищение ран от гнойных и некротических масс, оказывает эффективное противовоспалительное, противоотечное действие, что ускоряет гранулирование и заживление ран.
При создании раневой повязки могут быть использованы и родственные трипсину ферменты, например, химотрипсин, также обладающий протеолитической активностью.
Для изготовления раневой повязки по заявляемому изобретению использовали также антисептический препарат, обладающий антимикробными и противогрибковыми свойствами (см., например, патенты RU №2361029 и RU №2330673).
Данный препарат был получен следующим образом.
1-й этап. Изготовление полуфабрикатов порошков бентонита, предварительно обогащенных катионами натрия Na+.
Бентонит (монтмориллонит) Na-формы в количестве 5 г заливали 5% водным раствором NaCl, выдерживали в данном растворе, осуществляя обогащение бентонита ионами натрия, затем производили многократную промывку для удаления анионов хлора, последующую фильтрацию и сушку.
2-й этап. Получение наноструктурированных порошков бентонита, интеркалированных ионами металлов: Ag+, Zn2+, Cu2+.
На данном этапе из полуфабрикатов бентонита, изготовленных на 1-м этапе, получают интеркалированные ионами указанных металлов наноструктурированные бентонитовые порошки (наночастицы бентонита), не содержащие солей натрия, по следующим примерам.
Пример 1.
Очищенный от кислотных анионов полуфабрикат высушивали и модифицировали 10-20% водным раствором нитрата серебра (при красном освещении). Предпочтительно, использовали 15% водный раствор нитрата серебра (AgNO3). Полученный модифицированный полуфабрикат многократно промывали для удаления солей натрия, фильтровали и сушили.
Расход водных растворов на обработку 5 г полуфабриката (1-й этап) составил - бентонит:водный раствор, как 1:20 (вес.ч.). После сушки продукт подвергали измельчению до получения дисперсного порошка бентонита.
В результате получен не содержащий солей натрия интеркалированный ионами Ag+ порошок бентонита. Полезный выход продукта - 4,8 г.
Пример 2.
Те же материалы и технологические приемы, что и в Примере 1, но при модификации бентонита, обогащенного ионами натрия Na+, использовали 15% водный раствор сульфата меди (CuSO4).
Получен не содержащий солей натрия интеркалированный ионами Сu2+ бентонитовый порошок. Полезный выход продукта - 4,8 г.
Пример 3.
Те же материалы, технологические приемы, что и в Примере 1, но при модификации полуфабриката бентонита, обогащенного ионами натрия, использовали 15% водный раствор неорганической соли цинка, предпочтительно, хлорида цинка (ZnCl2). Возможно также использование сульфата цинка (ZnSO4).
Получен не содержащий солей натрия интеркалированный ионами Zn2+ бентонитовый порошок. Полезный выход продукта - 4,8 г.
Для реализации технологических этапов 1 и 2 (указанных выше) используется деионизованная вода.
Процесс измельчения полученных по Примерам 1-3 продуктов до заданных по изобретению размеров частиц порошка бентонита осуществляют во всех примерах следующим образом.
Полученные продукты после интеркалирования (модификации) ионами указанных металлов, их очистки от солей натрия и сушки суспендируют (интенсивно перемешивают) в большом количестве воды, дают отстояться в течение некоторого времени и декантируют надосадочную жидкость.
После добавления воды снова суспендируют осадок, отстаивают, декантируют. Этот процесс проводится многократно. Фильтрацией из декантированной жидкости выделяют наноструктурированный продукт, сушат его и размалывают в планетарных мельницах. При таком способе получения порошков наноструктурированного бентонита расходуется большое количество деионизованной воды, процесс достаточно длителен.
Для снижения трудоемкости названные продукты по Примерам 1-3 вводили в деионизованную воду при соотношении (вес.ч.): продукт (Примеры 1-3): растворитель, как 1:10, и осуществляли их наноструктурирование (ультрадиспергирование) до размера частиц не более 100 нм с использованием ультразвукового диспергатора, ускоряющего процесс наноструктурирования бентонитовых порошков. Процесс осуществляли с использованием диспергатора Bandelin Sonoplus HD2070 при мощности 40 Вт в течение 5-10 мин.
Полученные коллоидные системы наносились на подложку и после испарения воды проводились измерения размеров частиц наноструктурированного порошка бентонита методами микроскопии. Исследования показали, что наноструктурированные порошки бентонита имеют размеры частиц: 20-30 нм - 30% от количества порошка; 100 нм - остальное.
Наноструктурированные порошки бентонита (по Примерам 1-3) исследовались для определения в них мас.% содержания серебра, меди, цинка методом титриметрического анализа.
Титриметрический анализ по определению количества металлов в порошках бентонита осуществлялся с использованием индикаторов, фиксирующих точку эквивалентности титрования.
В результате проведенных исследований было установлено, что порошки бентонита, интеркалированные ионами названных металлов, в зависимости от количества активирующих и модифицирующих (интеркалирующих) реагентов, могут содержать от 2,0 до 8,0 мас.% серебра, или меди, или цинка.
Указанное мас.% содержание металлов в интеркалированном (промодифицированном) бентонитовом порошке оптимально. Увеличение мас.% содержания металлов приводит к возрастанию затратной части используемых реагентов на получение наноструктурированных бентонитовых порошков. Уменьшение мас.% содержания названных металлов в бентонитовых порошках снижает их антимикробную и фунгицидную активность.
По результатам титриметрических анализов количественное содержание металлов (Ag, Сu, Zn) в наноструктурированных бентонитовых порошках (в продуктах по примерам 1-3), составило порядка 2,0-6,0 мас.%.
На раневые повязки, содержащие иммобилизованный на диальдегидцелллюлозу протеолитический фермент - трипсин, наносили антисептические препараты в виде наноструктурированных порошков бентонита, интеркалированных ионами металлов Ag+, Cu2+, Zn2+.
Нанесение антимикробных препаратов осуществляли при обработке повязок в 5-10% гидрозолях на основе наноструктурированных порошков бентонита.
Заданное по изобретению мас.% содержание порошка бентонита в гидрозоле оптимально. Уменьшение количества бентонитового порошка в водной системе приводит к ухудшению его сорбции на волокна диальдегидцеллюлозы, что ухудшает антимикробные свойства раневой повязки. Увеличение количества бентонитового порошка в водной системе повышает затратную часть на изготовление раневой повязки.
Для реализации изобретения были изготовлены 6,0% гидрозоли, содержащие наноструктурированный порошок бентонита и деионизованную воду.
Полученные после обработки гидрозолем материалы подвергались сушки до исходной влажности не более 10 мас.%.
Заданная по изобретению влажность получаемой раневой повязки оптимальна по условиям ее хранения. При уменьшении влажности повязки ухудшаются ее эксплуатационные характеристики, а увеличение исходной влажности получаемой раневой повязки приводит к необходимости создания специальной упаковки, что повышает затратную часть.
В соответствии с описанным технологическим процессом были получены раневые повязки с антимикробными свойствами при следующем содержании в них компонентов, мас.%:
Пример 4.
Пример 5.
Пример 6.
Пример 7.
Пример 8.
Раневые повязки с антимикробными свойствами, имеющие иммобилизированные на диальдегидцеллюлозу протеолитический фермент - трипсин и антимикробный препарат, на основе указанных по изобретению наноструктурированных порошков бентонита соответствуют заданному по изобретению содержанию компонентов в них.
Заявленное по изобретению мас.% содержание компонентов в раневой повязке оптимально по ее терапевтическому действию при обработке ран с признаками гнойно-воспалительного процесса.
Уменьшение мас.% содержания в раневой повязке, иммобилизированного на диальдегидцеллюлозу указанного антимикробного препарата, снижает антимикробное влияние ионов металла на патогенную микрофлору.
Увеличение мас.% содержания в раневой повязке антимикробного препарата повышает затратную часть на ее изготовление.
Из полученных по Примерам 4-8 раневых повязок изготавливали испытываемые образцы, которые оценивали по их действию на сроки очищения гнойно-некротических ран и на клинические штаммы.
Для сопоставимости полученных результатов в качестве контрольных образцов использовали раневые повязки по следующим примерам.
Пример 9.
Раневая повязка, изготовленная по патенту №2142818, содержащая следующие компоненты, мас.%:
Пример 10.
Раневая повязка, изготовленная по патенту №2142818, на которую иммобилизирован бактериолитический фермент - лизоцим (патент RU №2357753), содержащая, мас.%:
Пример 11.
Раневая повязка с антимикробными свойствами, содержащая, мас.%:
Оценку сроков очищения гнойно-некротических ран осуществляли по следующей методике.
Белым крысам средней массой 173,0 г под эфирным наркозом удаляли полнослойный лоскут ткани между лопаток площадью 400 мм2, в образовавшийся дефект вшивали тефлоновое кольцо. На поверхность раны нанесен 1 мл микробной взвеси, содержащей золотистый стафилококк. Поверхность тефлонового кольца закрыта перфорированной полиэтиленовой крышкой. Через 2-е суток установлено: края раны гиперемированы, на ране фибринозный налет, желтоватый экссудат.
Фрагментами повязок (двухслойными), размером 2×2 см по Примерам 4-8, закрывали раны.
Функциональные свойства раневых повязок оценивали по срокам очищения гнойно-некротических ран, сопровождающихся уменьшением отека и гиперемии мягких тканей.
Результаты испытаний приведены в Таблице 1 «Сроки очищения гнойно-некротических ран при лечении раневыми повязками».
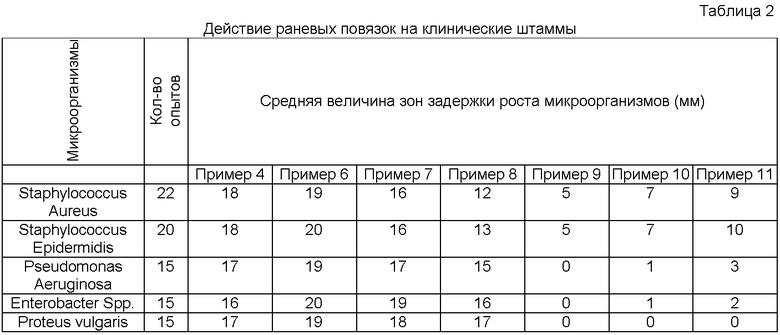
Оценку испытываемых образцов по антимикробным свойствам осуществляли в отношении различных клинических штаммов: грамположительных (Staphylococcus Aureus, Staphylococcus Epidermidis) и грамотрицательных (Pserdomonas Aeruginosa, Enterobacter Spp., Proteus vulgaris) бактерий.
Для испытаний были использованы:
- стерилизованная дистиллированная вода;
- мембранные фильтры;
- чашки Петри (D до 120 мм) с сухими средами: соевый агар (Soyabean Casein Digest Medium) для подсчета общего числа микроорганизмов; среда Чапмена- Стоуна (Chapman Stone Medium) для выделения и подсчета стафилококков; среда ECO (ЕСО Medium) для выделения и подсчета кишечной палочки и других колиформных микроорганизмов.
Испытания проводились в течение 2-5 суток при температуре культивирования 35-37°С, что при указанных параметрах инкубирования приводило к резкому росту различных микроорганизмов, грибов.
При испытаниях каждый исследуемый образец повязки замачивался в емкости со стерилизованной дистиллированной водой, которые затем закрывали крышками, образцы выдерживали в течение 24 часов в обычных условиях при комнатной температуре.
Полученные после выдержки образцов смывы профильтровывали через мембранные фильтры с последующим их размещением (рабочей поверхностью вверх) на поверхность восстановленной питательной среды в чашках Петри. При исследовании определялась величина зон задержки роста микроорганизмов (мм).
Результаты исследований сведены в Таблицу 2 «Действие раневых повязок на клинические штаммы».
Представленные в Таблице 1 и 2 данные по выбранным для исследования образцам в достаточной мере подтверждают и обосновывают целесообразность композиционного состава раневой повязки с антимикробными свойствами по заявляемому изобретению.
Проведенные исследования подтверждают:
- высокие антимикробные свойства раневой повязки по изобретению в отношении широкого спектра грамположительных, грамотрицательных бактерий для обработки и лечения ран с признаками гнойно-воспалительного процесса различной этиологии;
- особенную эффективность раневой повязки при первичном закрытии ран с высокой микробной обсемененностью;
- эффективность использования в композиционном составе раневой повязки по изобретению биологических и минеральных компонентов, синергетическое взаимодействие которых улучшает лечебные свойства перевязочного материала.
Предлагаемая по изобретению раневая повязка проста и удобна в применении, может находиться на ране в течение 2-х суток без потери функциональных свойств, обладает пролонгированным антимикробным и протеолитическим действием.
Область применения раневой повязки - первая помощь раненым и пострадавшим, медицина, гигиена, косметика.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ повышения реакционной способности левана и формирования белково-полисахаридных пленок | 2022 |
|
RU2813119C1 |
| СОСТАВ ДЛЯ АНТИСЕПТИЧЕСКОЙ ОБРАБОТКИ ТКАНЫХ МАТЕРИАЛОВ | 2010 |
|
RU2426560C1 |
| НАНОСТРУКТУРНАЯ КОМПОЗИЦИЯ БИОЦИДА | 2009 |
|
RU2407289C1 |
| ПРОФИЛАКТИЧЕСКИЙ БАКТЕРИЦИДНЫЙ ЛАК ДЛЯ ОБРАБОТКИ НОГТЕЙ | 2010 |
|
RU2432158C1 |
| АНТИСЕПТИЧЕСКАЯ МАЗЬ НАРУЖНОГО ПРИМЕНЕНИЯ (2 ВАРИАНТА) | 2009 |
|
RU2429820C2 |
| СОСТАВ ДЛЯ ПРОФИЛАКТИКИ И УХОДА ЗА ДИАБЕТИЧЕСКОЙ СТОПОЙ | 2010 |
|
RU2427379C1 |
| ПРОФИЛАКТИЧЕСКАЯ МАЗЬ ДЛЯ ДИАБЕТИЧЕСКОЙ СТОПЫ | 2010 |
|
RU2426525C1 |
| Способ получения гелевых антибактериальных раневых повязок с бактериоцинами | 2022 |
|
RU2784400C1 |
| ГИГИЕНИЧЕСКОЕ ИЗДЕЛИЕ С АНТИМИКРОБНЫМИ И ПРОТИВОГРИБКОВЫМИ СВОЙСТВАМИ | 2010 |
|
RU2419455C1 |
| ПОЛИУРЕТАНОВАЯ СИСТЕМА ДЛЯ ИЗГОТОВЛЕНИЯ ЭЛАСТИЧНЫХ ИЗДЕЛИЙ С УЛУЧШЕННЫМИ САНИТАРНО-ГИГИЕНИЧЕСКИМИ СВОЙСТВАМИ | 2010 |
|
RU2447098C1 |
Изобретение относится к области медицины, конкретно к перевязочным материалам для лечения гнойных и инфицированных ран, трофических язв и для профилактики нагноений инфицированных ран. Раневая повязка с антимикробными свойствами содержит текстильный носитель на основе диальдегидцеллюлозы (ДАН) с иммобилизированными протеолитическим ферментом и антимикробным препаратом. В качестве антимикробного препарата используют наноструктурированный порошок бентонита, интеркалированный ионами металлов Ag+, или/и Cu2+, или/и Zn2+. Раневая повязка имеет следующее содержание в ней компонентов, мас.%: протеолитический фермент - 0,03-0,1, наноструктурированный порошок бентонита, интеркалированный ионами Ag+, или/и Сu2+, или/и Zn2+ - 2,0-10,0, диальдегидцеллюлоза - остальное. Раневая повязка имеет высокие антимикробные свойства в отношении широкого спектра грамположительных, грамотрицательных бактерий для обработки и лечения ран с признаками гнойно-воспалительного процесса различной этиологии. Синергетическое взаимодействие используемых в композиционном составе раневой повязки биологических и минеральных компонентов улучшает лечебные свойства перевязочного материала. 6 з.п. ф-лы, 2 табл.
1. Раневая повязка с антимикробными свойствами, содержащая текстильный носитель на основе диальдегидцеллюлозы с иммобилизированными протеолитическим ферментом и антимикробным препаратом, отличающаяся тем, что в качестве антимикробного препарата используют наноструктурированный порошок бентонита, интеркалированный ионами металлов Ag+ или/и Сu2+, или/и Zn2+, при этом раневая повязка имеет следующее содержание в ней компонентов, мас.%:
2. Раневая повязка по п.1, отличающаяся тем, что смесь порошков бентонита, интеркалированных ионами Ag+ и ионами Сu2+, имеет соотношение, как 0,5:1,0, вес.ч.;
смесь порошков бентонита, интеркалированных ионами Ag+ и ионами Zn2+ имеет соотношение, как 0,5:1,0, вес.ч.;
смесь порошков бентонита, интеркалированных ионами Сu2+ и ионами Zn2+, имеет соотношение, как 1,0:1,0, вес.ч.;
смесь порошков бентонита, интеркалированных ионами Ag+, ионами Сu2+ и ионами Zn2+, имеет соотношение, как 0,5:1,0:1,0, вес.ч.
3. Раневая повязка по п.1, отличающаяся тем, что в качестве протеолитического фермента используют трипсин.
4. Раневая повязка по п.1, отличающаяся тем, что диальдегидцеллюлоза с иммобилизированными трипсином и антимикробным препаратом имеет влажность не более 10%.
5. Раневая повязка по п.1, отличающаяся тем, что размер частиц наноструктурированного порошка бентонита - не более 100 нм.
6. Раневая повязка по п.1, отличающаяся тем, что наноструктурированные порошки бентонита содержат 2,0-6,0 мас.% названных выше металлов, интеркалированных в бентонит.
7. Раневая повязка по п.1, отличающаяся тем, что для иммобилизации антимикробного препарата на диальдегидцеллюлозу используют гидрозоль, содержащий 5,0-10,0 мас.% наноструктурированного порошка бентонита, интеркалированного ионами названных металлов.
| МАТЕРИАЛ, ОБЛАДАЮЩИЙ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2005 |
|
RU2357753C1 |
| СПОСОБ ПОЛУЧЕНИЯ БУМАГИ С БИОЦИДНЫМИ СВОЙСТВАМИ | 2008 |
|
RU2361029C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРЕВЯЗОЧНЫХ МАТЕРИАЛОВ "САЛФЕТКИ ФИЛАТОВА-РЫЛЬЦЕВА" | 1998 |
|
RU2142818C1 |
Авторы
Даты
2011-08-20—Публикация
2010-06-21—Подача