Изобретение относится к области нефтехимического синтеза, а именно к способу получения циклических гомо- и содимеров стирола и α-метилстирола.
Циклические димеры стирола и α-метилстирола применяются в качестве пластификаторов оргстекла, сырья для получения реактивных топлив, присадок к смазочным материалам, высокотемпературных теплоносителей [Патент США 3161692; Патент США 3792096; Патент США 4442027; Пат. США 20040242441; АС СССР 1036727; Maier G.Angew. Chem. Im. Ed. 1998, 37, p.2960-2974].
Синтез циклических гомо-димеров стирола и α-метилстирола осуществляют с использованием различных кислотных катализаторов.
Известны способы получения циклического димера α-метилстирола-1.1,3-триметил-3-фенилиндана (ЦДМС) димеризацией α-метилстирола в присутствии серной кислоты [1. Патент Великобритании 1507600. 2. Патент РФ 2088561]. Используют Н2SO4 концентрированную или концентрацией 80-90% в количестве 0,05-100 мас.% на α-метилстирол. Температура реакции 35-60°С [2] или более высокая, до 225°С [1].
Обязательным условием осуществления реакции согласно [2] является непрерывная продувка азотом с объемной скоростью не менее 100 л/ч, перемешивание мешалкой с линейной скоростью не менее 80 см/с и непрерывная дозировка серной кислоты со скоростью 0,3-0,5 мас.ч./ч.
Существенным недостатком данных способов является многостадийность, связанная с использованием минеральной кислоты. Целевой продукт ЦДМС при температурах ниже 53°С (температура плавления ЦДМС) находится в кристаллическом состоянии, отделить от него полностью серную кислоту декантацией (особенно, если катализатор используется в небольших количествах) практически невозможно, поскольку кислота может оставаться между крупными кристаллами продукта. Поэтому для получения чистого продукта потребуются операции растворения ЦДМС в органическом растворителе, нейтрализация серной кислоты, ее отделение, промывка органического слоя, его осушка и отгонка растворителя. Возможны также потери сырья за счет образования побочных продуктов с серной кислотой. Кроме того, серная кислота вызывает коррозию оборудования.
Предложен способ получения ЦДМС димеризацией α-метилстирола на обработанном кислотой монтмориллоните или алюмосиликате [Патент США 3161692]. Катализаторы используют в количестве 1-15 мас.%, температура реакции 140-150°С. В присутствии алюмосиликата конверсия α-метилстирола составляет 84-94,6 мас.%, выход ЦДМС - 86-89%. Монтмориллонит для повышения каталитической активности обрабатывают серной кислотой, на нем конверсия α-метилстирола выше - 94-98,8 мас.%, выход ЦДМС - 88-97%. Более высокого выхода ЦДМС достигают также при проведении реакции в растворителе (ксилоле).
Недостатки указанного способа - использование серной кислоты для пропитки глины, так как она постепенно смывается с катализатора во время реакции; использование растворителя в больших количествах (до 500%), что усложняет стадию выделения продукта. Кроме того, в описании отмечается, что реакция на предлагаемых катализаторах протекает высокоэкзотермично, температура резко повышается от комнатной до 200°С, т.е. процесс практически нерегулируем.
Описано получение ЦДМС димеризацией α-метилстирола в присутствии цеолитов типа морденит и СаХ в среде растворителей - нитробензола или нитрометана [А.с. СССР №829606]. Содержание растворителя составляет 41-45 об.%, содержание катализатора 18-19 мас.% на шихту (или 35-40% катализатора на α-метилстирол); температура реакции 80°С, время - 2-2,5 ч. Выход ЦДМС оставляет 99,0 мас.%. Конверсия α-метилстирола не указана, но поскольку в описании говорится о том, что при выделении ЦДМС отгоняют непрореагировавший α-метилстирол, то можно сделать вывод о неполном превращении мономера.
Известен способ получения ЦДМС димеризацией α-метилстирола в присутствии цеолитсодержащего катализатора крекинга Ц-10 в количестве 5-50 мас.% при температуре 60-150°С.
Конверсия α-метилстирола достигает 100 мас.%, выход ЦДМС составляет 92-98,8% [Патент РФ 2223937].
К недостаткам этого способа можно отнести использование катализатора крекинга Ц-10, технология приготовления которого сложна и многостадийна. Кроме основного активного вещества - цеолита типа Y - для изготовления катализатора Ц-10 применяются другие компоненты (аморфный алюмосиликат, глина и др.).
Для получения ЦДМС катализатор используют в больших количествах - до 50%. Это снижает эффективность процесса, т.к. уменьшается съем продукта с 1 кг катализатора. Возрастают потери продукта с катализатором.
Известен процесс циклодимеризации α-метилстирола в 1,1,3-триметил-3-фенилиндан, в котором в качестве катализатора используют цеолит типа Beta в Н-форме. Процесс димеризации осуществляют в присутствии 1-5 мас.% катализатора при температуре 60-90°С. Конверсия α-метилстирола составляет 100 мас.%, выход ЦДМС - 97,5% [Патент РФ 2317969].
Примером димеризации стирола с целью получения циклических димеров цис- и транс-1-метил-3-фенилинданов (ЦДС) может быть способ, описанный в патенте [Патент Великобритании 1343 445]. Стирол добавляют к фосфорной кислоте (98%-ной) в соотношении 1:1 (мас.) и перемешивают при 100°С в течение 40 мин. Димеры экстрагируют из реакционной массы метиленхлоридом, а затем перегоняют. Выход димеров стирола составляет 67-84%. В димерной фракции содержится 9-14% линейного димера и 86-91% ЦДС.
К недостаткам данного способа можно отнести использование большого количества минеральной кислоты, необходимость применения экстрагента, который затем необходимо отделять и регенерировать.
Чтобы избежать недостатков, присущих минеральным кислотам, авторы [B.B.Corson, Ju. Dorsky, J.E.Nickels. J. Org. Chem. 1954, v.19, p.17-26] предлагают использовать при димеризации стирола фосфорную кислоту, нанесенную на уголь. Раствор стирола в этилбензоле пропускают через катализатор с объемной скоростью 0,9 ч-1 при температуре 140°С. Из полученного продукта выделяют 72,8% димерной фракции. Соотношение ЦДС: линейный димер составляет 90:10.
В то же время авторы отмечают, что используемый ими в качестве растворителя этилбензол не является инертным соединением, а в присутствии сильных кислот взаимодействует со стиролом, образуя продукты алкилирования. Следовательно, полученная «димерная фракция» является смесью продуктов алкилирования (1-этилфенил-1-фенилэтанов) и димеров стирола.
Известен способ получения ЦДС с использованием катионообменной смолы H-Nafion [Hasegawa H., Higashimura Т. Polim. J., 1979, 11, p.737]. Димеризацию стирола проводят в растворителе ССl4 при температуре 50°С в течение 2 ч. Получают реакционную массу следующего состава (мас.%): димеры - 22, тримеры -18, более высокомолекулярные соединения - 60.
К недостаткам этого процесса можно отнести низкий выход димеров стирола.
В работе [Kuroki Т., Ogawa Т., Sekiguchi J. at al. Ind. and Eng. Chem. Prod. Res. and Dev., 1983, 22, №2, p.234-237] изучена парофазная димеризация стирола в присутствии алюмосиликатного катализатора. Реакцию проводят в кварцевой трубке в среде азота в интервале температур 200-300°С. Получают продукт состава (мас.%): этилбензол - 37,3-49, олигомеры - 5-21, кокс - 35-45. Отношение линейный димер: циклический димер = 15:85.
Недостатками этого способа является очень низкий выход димеров, большое количество кокса, высокие температуры реакции.
Известен способ получения ЦДС в присутствии цеолитов Y и Beta. Реакцию проводят в растворителе CCl4, количество которого составляет от 227 до 454 объемных частей на 1 об. часть стирола. Катализатор используют в количестве 500-1000 мас.% в расчете на стирол. Температура реакции 72°С, время - 3 ч. Селективность образования ЦДС на цеолите Бета составляет 84-90% при конверсии стирола 95 мас.% [Benito A., Corma A., Garcia H. Appl. Catal. A: General. 1994, 116, p.127-135].
К недостаткам этого способа можно отнести:
1. Использование катализатора в больших количествах - 500-1000 мас.% (в расчете на стирол), что снижает эффективность процесса.
2. Применение дорогостоящего растворителя в больших объемах (от 227 до 454 об. частей на 1 об. часть стирола), что ведет к нерациональному использованию оборудования.
3. Метод может использоваться только как препаративный.
Усовершенствование способа получения ЦДС в присутствии цеолитов Бета и ZSM-12 предложено в патентах [Патент РФ 2354639; 2350592; 2354638].
Димеризация стирола в присутствии 18-25% цеолита Н-Бета в хлорбензоле при соотношении стирол:хлорбензол=1:4 и 115-130°С проходит с образованием 79-82 мас.% ЦДС. Конверсия стирола достигает 100% [Патент РФ 2354639].
Использование цеолита ZSM-12 при димеризации стирола позволяет получать ЦДС с высоким выходом (80,2-85,4 маc.%) как в среде растворителя (хлорбензол) [Патент РФ 2350592], так и без него [Патент РФ 2354638]. Количество катализатора составляет 20-30 мас.%, температура реакции 120-120°С.
В отличие от широко изученной гомодимеризации стирола и метилстирола их совместное взаимодействие исследовано мало.
Описана совместная олигомеризация стирола с метилстиролом под действием фосфорной кислоты с получением смеси циклических гомо- и содимеров [Р.Н.Волков, Ю.С.Цыбин, В.В.Кузенков. Нефтехимия, 1970, т.Х, №4, с.541-545]. При мольном соотношении стирол: метилстирол=1:1 выход димеров составляет 80%. Реакцию проводили, добавляя 150 г смеси мономеров к 150 мл упаренной фосфорной кислоты, постепенно поднимая температуру от 130 до 155°С, в течение 3 ч. В составе димеров идентифицированы ЦДМС, ЦДС и два циклических содимера - 1,1-диметил-3-фенилиндан и 1,3-диметил-3-фенилиндан.
К недостаткам данного способа относится использование большого количества агрессивного, коррозионноактивного реагента - фосфорной кислоты, сложность ее отделения от продуктов реакции (необходимость в нейтрализации, отмывке, осушке органической части перед перегонкой), появление большого количества стоков.
Задачей настоящего изобретения является разработка малостадийного, экологически безопасного способа совместной олигомеризации стирола и α-метилстирола с получением циклических гомо- и содимеров.
Решение поставленной задачи достигается тем, что способ получения циклических гомо- и содимеров стирола и α-метилстирола осуществляют взаимодействием стирола и α-метилстирола в присутствии цеолитов типа Y и Beta. Реакцию проводят в хлорбензоле при мольном соотношении стирол: α-метилстирол=1:1, температуре 80-130°С и количестве катализатора 5-30 мас.% (в расчете на смесь мономеров). Начальная концентрация мономеров в хлорбензоле составляет 2-8 моль/л.
Цеолиты Y и Beta используют как в водородной форме НY и H-Beta (степень обмена Na+ на Н+ составляет более 90 мас.%), так и в катион-декатионированной форме - РЗЭНУ, РЗЭ-Beta, которую получали путем ионного обмена цеолита HY или цеолита H-Beta (степень обмена 96%) в растворе солей РЗЭ.
Сравнительный анализ заявляемого решения с прототипом показывает, что заявляемый способ отличается от прототипа тем, что в процессе содимеризации стирола и α-метилстирола в смесь циклических гомо- и содимеров в качестве катализаторов используют цеолиты типа Y или Beta. Процесс содимеризации осуществляют в присутствии 5-30 мас.% катализатора при температуре 80-130°С. Конверсия стирола и α-метилстирола достигает 97-100 мас.%. Выход димеров в присутствии цеолита HY составляет 56,3-66,5%, в присутствии цеолита Beta -72,9-81,2%. В составе димеров образуются циклические димеры стирола (ЦДС), α-метилстирола (ЦДМС) и циклический содимер (ЦСД) - 1,1-диметил-3-фенилиндан. Содержание содимера в димерной фракции достигает 56 маc.%.
Схема реакции:
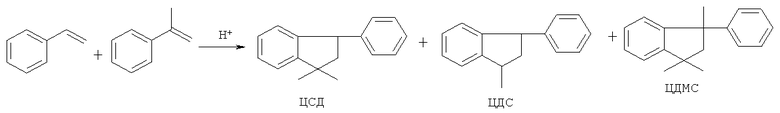
Катализаторы легко отделяются фильтрованием и могут использоваться многократно без потери активности.
Предлагаемый способ осуществляют следующим образом. Катализатор цеолит HY получали из цеолита NaY с мольным соотношением SiO2/Al2O3=6,0, синтезированного по методике, описанной в [13]. Декатионированием из раствора NH4NO3 и последующим прокаливанием при 540°С цеолит NaY переводили в Н-форму со степенью декатионирования ионов Na+ на H+ 90-96% (последний обозначен как 0,96 HY). Ионным обменом цеолита 0,96HY получали цеолит РЗЭ-HY (степень обмена = 0,96).
Катализатор цеолит Beta синтезируют в ОАО "Ангарский завод катализаторов и органического синтеза" в аммонийной форме (ДК 04-21303-008-2004). Мольное отношение SiO2/Al2O3 составляет 18,0; степень кристалличности 95%.
Для осуществления содимеризации стирола и α-метилстирола катализатор из аммонийной формы переводят в Н-форму. Для этого цеолит NH4-Beta прокаливают в атмосфере воздуха 4 ч при 540°С. Цеолит РЗЭ-Beta получали ионным обменом цеолита H-Beta.
Соолигомеризацию проводят в периодическом термостатированном реакторе, в присутствии 5-30 мас.% катализатора, при 80-130°С в среде хлорбензола. Реакционную массу перемешивают при температуре реакции в течение определенного времени. После окончания реакции реакционную массу отделяли от катализатора фильтрованием. Степень превращения исходных виниларенов и состав димерной фракции определяют методом газожидкостной хроматографии. Состав образующихся олигомеров анализируют методом высокоэффективной жидкостной хроматографии. Для калибровки выделяли вакуумной перегонкой димерную и тримерную фракции.
ГЖХ-анализ выполняли на хроматографе HRGS 5300 Mega Series ("Carlo Erba") с пламенно-ионизационным детектором (капиллярная колонка 25 м, фаза SE-30, программирование нагревания от 50 до 280°С со скоростью подъема 8°С/мин, температура детектора 250°С, температура испарителя 300°С, газ-носитель - гелий, 30 мл/мин). ВЭЖХ-анализ выполняли на хроматографе HP-1090 с рефрактометрическим детектором и полистирольной колонкой Plgel 100 А, элюент-толуол, скорость подачи толуола 0,8 мл/мин, скорость ленты 1,5 см-1.
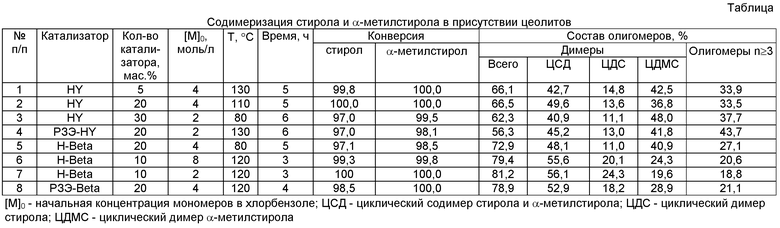
Предлагаемый способ иллюстрируется следующими примерами (таблица).
ПРИМЕР 1. В стеклянный обогреваемый реактор с мешалкой, обратным холодильником и термометром помещали смесь 5,2 г (0,05 моля) стирола и 5,9 г (0,05 моля) α-метилстирола в 25 мл хлорбензола. При 130°С прибавляли 0,55 г цеолита HY и перемешивали при этой температуре 5 ч. После охлаждения от реакционной смеси отфильтровывали катализатор, затем при пониженном давлении удаляли растворитель и непрореагировавшие виниларены. Получали 6,2 г олигомеров состава, мас.%: димеры - 66,1; тримеры - 20,5; n>4. В составе димеров содержится (мас.%): ЦДС -14,8, ЦЦМС - 42,5; ЦСД - 42,7.
1,1-Диметил-3-фенилиндан. Спектр ЯМР 1H (δ, м.д.): 1.36 (с, 3Н, СН3), 1.40 (с, 3Н, СН3), 1.79 (м, 1Н, СН2); 2.06 (м, 1Н, СН2); 4.43 (т, 1Н, СН). Спектр ЯМР 13С (δ, м.д.): 29.70 (-СН3); 29.10 (-СН3); 46.64 (-С(СН3)2); 49.04 (CPh); 52.79 (-СН2-). Масс-спектр, m/z: 222; индекс Ковача 1713.
ПРИМЕРЫ 2-8 приведены в таблице аналогично примеру 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ЛИНЕЙНЫХ И ЦИКЛИЧЕСКИХ ГОМО- И СОДИМЕРОВ СТИРОЛА И АЛЬФА-МЕТИЛСТИРОЛА | 2010 |
|
RU2428407C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ЛИНЕЙНЫХ И ЦИКЛИЧЕСКИХ ГОМО- И СОДИМЕРОВ СТИРОЛА И АЛЬФА-МЕТИЛСТИРОЛА | 2010 |
|
RU2424221C1 |
| Способ получения гомо- и соолигомеров α-метилстирола и изопентенов в присутствии иерархического цеолита H-Ymmm | 2020 |
|
RU2735666C1 |
| Способ получения гомо- и соолигомеров α-метилстирола и изопентенов в присутствии мезопористого алюмосиликатного катализатора ASM | 2020 |
|
RU2759627C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНЫХ ДИМЕРОВ α-МЕТИЛСТИРОЛА | 2006 |
|
RU2322429C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИМЕРОВ СТИРОЛА | 2007 |
|
RU2354639C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИМЕРОВ СТИРОЛА | 2007 |
|
RU2350592C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,1,3-ТРИМЕТИЛ-3-ФЕНИЛИНДАНА | 2006 |
|
RU2317969C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНОГО ДИМЕРА СТИРОЛА | 2007 |
|
RU2350591C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНЫХ ДИМЕРОВ α-МЕТИЛСТИРОЛА | 2006 |
|
RU2316531C1 |
Изобретение относится к способу получения циклических гомо- и содимеров стирола и α-метилстирола совместной олигомеризацией стирола и α-метилстирола в присутствии кислотных катализаторов, характеризующемуся тем, что в качестве катализатора используют цеолиты типа Y и Beta в Н-форме или катион-декатионированной форме РЗЭ-HY, РЗЭ-Beta, реакцию проводят в хлорбензоле при мольном соотношении стирол: α-метилстирол=1:1, температуре 80-130°С и количестве катализатора 5-30 мас.% (в расчете на смесь мономеров). Применение данного способа позволит упростить получение циклических гомо- и содимеров стирола и α-метилстирола. 2 з.п. ф-лы, 1 табл.
1. Способ получения циклических гомо- и содимеров стирола и α-метилстирола совместной олигомеризацией стирола и α-метилстирола в присутствии кислотных катализаторов, отличающийся тем, что в качестве катализатора используют цеолиты типа Y и Beta в Н-форме, или катион-декатионированной форме РЗЭ-HY, РЗЭ-Beta, реакцию проводят в хлорбензоле при мольном соотношении стирол: α-метилстирол=1:1, температуре 80-130°С и количестве катализатора 5-30 мас.% (в расчете на смесь мономеров).
2. Способ по п.1, отличающийся тем, что степень обмена Na+ на Н+ в цеолитах HY и HBeta составляет более 90 маc.%.
3. Способ по п.1, отличающийся тем, что начальная концентрация мономеров в хлорбензоле составляет 2-8 моль/л.
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИМЕРОВ СТИРОЛА | 2007 |
|
RU2354639C1 |
| Р.Н.ВОЛКОВ, Ю.С.ЦЫБИН, В.В.КУЗЕНКОВ | |||
| НЕФТЕХИМИЯ, 1970, Т.Х, №4, с.541-545 | |||
| US 4198535 А, 15.04.1980. | |||
Авторы
Даты
2011-09-27—Публикация
2010-01-11—Подача