Изобретение относится к области нефтехимического синтеза, а именно к способу получения линейных и циклических гомо- и содимеров α-метилстирола и изоамиленов.
Главными потребителями данных содимеров являются полимерная, химическая, парфюмерная и другие отрасли промышленности.
Олигомеры амиленов - продукты с высокой добавленной стоимостью, которые после гидрирования используются в качестве компонентов бензинового (димеры) либо дизельного топлива (тримеры и более высокомолекулярные) [I.Cruz V.J.Jzquierdo J.F., Cunill F.,Tejero J.Jborra M., Fite' C. React. Funct. Polym. 2005. V. 65. P. 149], присадок [2. Kulkarni A., Kumar A., Goldman A.S., Celik F.E. Catalysis Communications. 2016. V. 75. P. 98-102] или растворителей [3. US Pat. 4,335,009. 1982]. Кроме того, димеры амиленов - изодецены - являются промежуточными продуктами в производстве эпоксидов, аминов, алкилированных ароматических соединений и синтетических жирных кислот [4. Ceska J., Zilkova N., Nachtigall P. Industrial Studies in Surface Science and Catalysis. 2005. V. 158. P. 1201-1212]. Разветвленные димеры изоамиленов находят применение в парфюмерной и пищевой промышленности [5. US Pat. 4,374,053, 1983; 6. US Pat. 4,391,999. 1983].
Циклические и линейные гомо-димеры α-метилстирола используются в качестве регуляторов молекулярной массы различных полимеров, сырья для получения топлив, компонентов синтетических масел и смазочных материалов, растворителей для лакокрасочных материалов, высокотемпературных теплоносителей, пластификатора оргстекла, мономеров для получения полимерных газоразделительных мембран, диэлектрических жидкостей, основ для синтетических масел [6-11. Патенты США 3161692, 3792096, 3994816, 4302618, 4442027, 20040242441; А.С. СССР 1036727; 12-15. Патенты РФ 2071460, 2129043, 2149862; Maier G.Angew. Chem. Im. Ed. 1998, 37, р. 2960-2974].
Продукты содимеризации α-метилстирола с изоамиленами (1,1,2,3,3-пентаметилиндан и 3-этил-1,1,3-триметилиндан) являются интермедиатами циклических соединений изохромановых мускусов, использующихся в парфюмерии. Например, 1,3,4,6,7,8-гексагидро-4,6,6,7,8,8-гексаметил-циклопента-γ-2-бензопиран, известный под торговым названием Галаксолид, - это самый крупнотоннажный мускусный макроцикл, объем производства которого достигает 8000 тонн в год [16. Т. Sekiguchi, S. Nakagawa and Y. Fujikura, Preparation of polyalkylindans as intermediates for musk fragrance, Jpn. Pat, 0344337 (1991); C. A., 115 (1991) 28920].
Кроме того, известно, что соединения, содержащие индановый цикл, используются в качестве пластификаторов, растворителей, масел широкого спектра применения [17. Rudnik L.R. Synthetics, Mineral Oils, and Bio-based Lubricants. Chemistry and technology. Taylor&Francis. 2006. p. 894].
Продукты гомо- и содимеризации α-метилстирола и изопентенов: 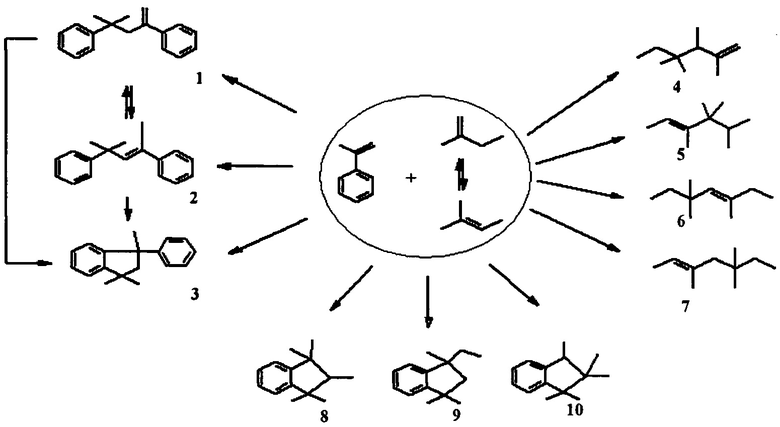
Синтез гомо-димеров α-метилстирола проводят с использованием различных кислотных катализаторов: минеральных или органических кислот [18. Патент Великобритании 1507600; 19. патент РФ 2088561], катионообменных смол [20 В. Chaudhuri, М.М. Sharma. Ind. Eng. Chem. Res. 1989, v.28, N12, p. 1757-1763; 21. M. Fujiwara, K. Kuraoka, T. Yazawa. Chem. Commun. 2000, p. 1523-1524], обработанных кислотой глин [22. Патент США 3161692, 1964]. В зависимости от условий реакции и природы катализатора основными продуктами реакции являются линейные (ЛДМС, 1, 2) или циклический димер α-метилстирола (ЦДМС, 3).
Эффективными катализаторами для получения линейных димеров α-метилстирола являются цеолиты и цеолитоподобные материалы. В работе [23. Я.И. Исаков, Х.М. Миначев, В.З. Шарф и др. Нефтехимия, 1999, т.39, №4, с. 278-283] описан способ получения линейных димеров α-метилстирола в присутствии кристаллических алюмофосфатов. На катализаторе, полученном из немодифицированного кристаллита AlPO4-8, при атмосферном давлении, 75-100°С и объемной скорости 1,5 ч-1 конверсия α-метилстирола составляет 80-83%, селективность образования линейных димеров 93,6-96,3%.
Авторы [24. В.П. Талзи, В.П. Доронин, Т.П. Сорокина. ЖПХ, 2000, т.13, №5, с. 787] осуществили димеризацию α-метилстирола на цеолите Y в среде метиленхлорида при 25-40°С. Конверсия α-метилстирола составляет 98,4-99,9% мас., селективность образования линейных димеров достигает 76,1-87,0% мас.
В патентах приведены способы получения линейных димеров α-метилстирола без растворителя в присутствии цеолитов HNaY [25-27. Патенты РФ №2189963, 2189964, 2313511], Beta [28. Патент РФ №2322429], ZSM-12 [29. Патент РФ №2312095].
Для синтеза циклического димера α-метилстирола-1,1,3-триметил-3-фенилиндана (3) использовали цеолиты типа морденит и СаХ в среде растворителей - нитробензола или нитрометана [30. А.с. СССР №829606. 1979, БИ 1981, №18]. Содержание растворителя составляет 41-45 об. %, содержание катализатора 18-19 мас. % на шихту (или 35-40% катализатора на α-метилстирол); температура реакции 80°С, время - 2-2,5 ч. Выход 3 составляет 99,0 мас. %. Конверсия α-метилстирола не указана, но поскольку в описании говорится о том, что при выделении 3 отгоняют непрореагировавший α-метилстирол, то можно сделать вывод о неполном превращении мономера.
Известен способ получения 3, осуществляемый путем димеризации α-метилстирола в присутствии цеолитсодержащего катализатора крекинга Ц-10 в количестве 5-50 мас. % при температуре 60-150°С. Конверсия α-метилстирола достигает 100 мас. %, выход ТМФИ составляет 92-98,8% [31. Патент РФ 2223937]. Столь же успешно 3 может быть получен в присутствии цеолита Beta [32. Патент РФ 2327969].
Разработаны катализаторы олигомеризации низших олефинов (преимущественно С3-С4) на основе цеолита ZSM-5. Для получения качественного дизельного топлива необходимо проводить процесс в реакторах периодического действия со стационарным слоем катализатора при невысоких температурах (200-300°С) и высоком давлении (3-10 МПа) (процесс MOGD фирмы Mobil Oil). [33. US Pat. №4504693. 1983; 34. Guann R.J., Green L.A., Tabak S.A., Krambeck F.J. // Ind. Eng. Chem. Res. 1988, V. 27, P. 565-570;35. Tabak S.A., Krambeck F.J., Garwood W.E. AIChE J. 1986. V. №9. P. 1526-1531].
Недостатки описанных методов: высокое давление реакции, большое количество побочных продуктов реакции. Кроме того, при использовании изопентенов процесс закоксовывания катализатора ускоряется по сравнению с олигомеризацией пропена за счет уменьшения возможности диффузии продуктов из пор и полостей цеолита ZSM-5.
В патенте фирмы UOP [36. US Pat. №9567267. 2017] предложен способ олигомеризации фракции олефинов С4-С5 с установки каталитического крекинга. Олигомеризацию алкенов проводят в две стадии: исходную смесь С4-С5 подвергают олигомеризации, затем фракционируют и возвращают С4 и С5+ на вторую стадию олигомеризации. Катализатором первой ступени является твердая фосфорная кислота. Катализатором второй стадии процесса являются одномерные цеолиты с 10-членной пористой структурой (МТТ, MTW, MFI). Процесс проводят при давлении 2,1-10,5 МПа и температуре 150-300°С. Скорость подачи сырья варьируется от 0,5 до 5 ч-1. Суммарная конверсия олефинов по данному методу составляет 95%. Содержание бензиновой фракции в продукте может быть около 40%, выход дизельной фракции достигает 56-78% в зависимости от состава сырья.
Недостатками указанного выше способа являются многостадийность; использование на первой стадии фосфорнокислотного катализатора; использование гранулированных цеолитных катализаторов, полученных путем гранулирования смеси цеолита со связующим веществом, снижающим активность катализаторов.
В работе [37. Schmidt R., Welch М.В., Randolph В.В. Energy and Fuels. 2008. V. 22. P. 1148-1155] изучали олигомеризацию модельной смеси пентана и пентенов (содержание последних не превышало 10%) и фракции С5 с установки крекинга в присутствии цеолитных катализаторов MOR, MFI, ВЕА в Н-форме. Скорость подачи сырья варьировали от 1,4 до 2,2 ч-1. Температуру реакции изменяли от 75-125°С. Показано, что при олигомеризации смеси олефинов в присутствии кислотных цеолитных катализаторов следующих структурных типов: ВЕА (Si/Al=25), Ni-BEA (Si/Al=25, содержание Ni=17,6% мас.), MFI (Si/Al=50 и 90), MOR (Si/Al=14, 40, 90 и 130), в качестве связующего в которых использовали бентонит, конверсия в расчете на пент-1-ен изменялась от 7 до 55% в зависимости от типа цеолита и выбранных условий процесса. Селективность по продуктам составляла: фракция С9 - 1-3%, С10 - 80-86%, С12+ - 18-39%. Катализатор MOR (Si/Al=90) работал стабильно при постоянной температуре в течение 600 часов.
Недостатками метода являются низкая активность образцов катализаторов в условиях процесса, использование при приготовлении гранулированных образцов связующего вещества бентонит, что приводит к уменьшению активности цеолитного компонента.
В работе авторов [38. Granollers М., Izquierdo J.F., Tejero J., Iborra M., Fife' С, Bringue' R., Cunill F. Ind. Eng. Chem. Res. 2010. V. 49. P. 3561-3570] приведены результаты олигомеризации смеси изоамиленов (6 мас. % 2-метил-бут-1-ена и 94 мас. % 2-метил-бут-2-ена) в присутствии цеолитов: Н-BEA (Si/Al=25), H-FAU-6, H-FAU-30 и H-MOR-20. Реакцию проводили в периодическом реакторе с магнитным перемешиванием (500 rpm) в интервале температур от 60 до 100°С, при давлении 0,2 МПа. Загрузку катализаторов изменяли от 0,5-6 г сухого образца. Показано, что конверсия изоамиленов достигает 98-99,5%, селективность по димерам составляет 65-75,6% (цеолит Н-ВЕА-25) и 32,8-51,3% (H-FAU-30), по тримерам - 19-28,9% (Н-ВЕА-25) и 43-44% (H-FAU-30), а по продуктам крекинга (С6-С9 и С11-С14) - 6% (Н-ВЕА-25) и 23,5%(H-FAU-30).
В отличие от широко изученной гомодимеризации α-метилстирола и изопентенов, их совместная димеризация исследована мало.
Известны способы получения индановых производных реакцией п-диметилстирола, а-метилстирола с С4-С6-спиртами/олефинами, включая изоамилены, в присутствии серной, фтористоводородной, фосфорной, уксусной кислоты, оксида фосфора (V), хлорида алюминия в среде насыщенных углеводородов в качестве растворителя или без него.
Описаны способы синтеза индановых производных амилена, преимущественно 1,1,2,3,3-пентаметилиндана (8) и 3-этил-1,1,3-триметилиндана (9), реакцией трет-амилового спирта с п-кумолом в присутствии серной кислоты или соолигомеризацией стирола и соответствующего олефина. [39. D.B. Spoelstra, S.H. Weber and R.J.C. Kleipool, New musk odor ants. IV. Aldehydes derived from polyalkylindans, Rec. Tray.Chim. Pays-Bas, 76 (1957) 205; 40.SB. Spoelstra, S.H. Weber and RJ.C. Kleipool, New musk odorants. V. A new synthesis of polyalkylindanes starting from styrenes, Rec. Tray. Chim. Pays-Bas, 82 (1963) 1100]. Состав образующейся смеси полиметилинданов: 41% 1,1,2,3,3,5-гексаметилиндана, 23% 3-этил-1,1,3,5-тетраметилиндана (9) и 12% 1,1,3,3,5-пентаметилиндан (8). Кроме того, были синтезированы 1,2,3,3,5-пентаметилиндан и 1,1,2,3,5-пентаметилиндан.
Авторами [41. Т. Sekiguchi, S. Nakagawa and Y. Fujikura, Preparation of polyalkylindans as intermediates for musk fragrance, Jpn. Pat., 0344337 (1991); С A., 115(1991) 28920] предложен способ получения инданов взаимодействием α-метилстирола (α-МС) с изопентенами (мольное соотношение α-МС : изопентены=1:4) при добавлении к ним смеси серной и уксусной кислот при 20-30°С в течение 3 ч и дальнейшем перемешивании в течение 1 ч.
В патенте [42. R.L. Cobb, Acid-catalyzed reactions of monovinylaromatic compounds, U.S. Pat., 4596896 (1986); C. A., 105 (1986) 114706.] сообщается о получении 1,1,2,3,3-пентаметилиндана (8) (63%) и 1,1,3-триметил-3-этилиндана (9) (18%) реакцией α-метилстирола и изопентенов в сульфолане в присутствии серной кислотой. Конверсия α-метилстирола достигает 90%.
Было установлено [43. R.L. Cobb, Metal oxide, acid-, and sulpholanecatalyzed Sulpholanecatalyzed cycloalkylation of vinylaromatics by olefins, U.S. Pat., 5034562 (1991); С.A., 115 (1991) 158 748], что добавление оксидов металлов, таких как CeO2, Na2MoO4 или Na2WO4, к смеси кислота-сульфолан повышает селективность образования продуктов на 10-15% при одновременном сокращении времени реакции.
Авторы [44. G. J. Ferber and P.J. Goddard, Indans, isochromans and indan precursors, Eur. Pat., 61267 (1982); C. A., 98 (1983) 71 725] получали 1,1,2,3,3-пентаметилиндан (8) и 3-этил-1,1,3-триметилиндан (9) реакцией α-метилстирола с 2-метил-2-бутеном (наличие примеси 2-метил-1-бутена) в присутствии 90%-ной фосфорной кислоты в качестве катализатора при 25-27°С. Селективность образования 8 и 9 составила 55% и 8%, соответственно. Продукты реакции в дальнейшем превращали в изохроман по реакции с алкеноксидом и формальдегидом.
В патенте [45. Е. Henkes, К. Halbritter, Н. Mayr, W. Striepe and R. Pock, D.E. Pat., 3626227 (1986): C.A., 108 (1988) 167129] предложено получать соединение 8 взаимодействием 2-метил-2-бутена (25 моль) с кумилхлоридом (10 моль) при -5°С в присутствии TiCl4. Выход соединения 8 достигает 92,5%.
Предложен [46. N. Hirowatali, Т. Kishiba, Н. Nakamuro and Н. Nanbu, Polyalkylindans, Jpn. Pat, 7659846 (1976); С.A., 85 (1976) 177129] способ получения инданов 8 и 9 соолигомеризацией α-метилстирола и изоамиленов в присутствии смеси 60% серной кислоты и оксида фосфора (V) в гексане при 30°С.
В работе [47. Obiefuna С.Okafor, Sunitha Tadepalli, Geatesh Tampy, Adeniyi Lawal Microreactor Performance Studies of the Cycloaddition of Isoamylene and α-Methylstyrene // Ind. Eng. Chem. Res. 2010, 49, 5549-5560] описан способ олигомеризации α-метилстирола и смеси двух изопентенов (2-метил-1-бутена (15%) и 2-метил-2-бутена (85%)) под действием серной кислоты с получением смеси гомо- и содимеров. Реакцию проводили в микропроточной установке при температуре 30-35°С, с объемной скоростью подачи сырья 0,1-10 мл/мин, при атмосферном давлении. Выход содимеров составляет 18-34%, Конверсия при 35°С выше 95%.
Суммарный выход димеров составляет 80% при мольном соотношении α-метилстирол : изопентены=1:1. В составе димеров присутствуют три димера α-метилстирола, четыре основных димера изопентенов и содимеры - диметил-3-фенилиндан и 1,3-диметил-3-фенилиндан.
К недостаткам данного способа относится низкий выход содимеров, использование большого количества агрессивного реагента - серной кислоты (70-90% мас.), наличие высоковязкой двухфазной системы, затрудненный тепло и массообмен, сложность выделения продуктов реакции (необходимость в нейтрализации, отмывки, осушке органической части перед перегонкой), появление большого количества стоков, трудности при масштабировании реакции.. Кроме того, в продуктах реакции присутствуют соединения, возникающие в результате распада гомо- и содимеров α-метилстирола и изопентенов.
Разработан [48. D.E. Boone, E.J. Eisenbraun, P.W. Flanagan and R.D. Grigsby, The acid-catalyzed alkylation andcyclialkylation of the cymenes with isobutylene and related olefins, J. Org. Chem., 36 (1971) 2042] метод получения 1,1,3,3,5-пентаметилиндана реакцией между п-цимолом и изобутиленом в присутствии ионообменной смолы.
В работе Wiegers [49. W.J. Wiegers, М.А. Sprecker, Н. Watkins, US Pat. №4398412 (1981); 50. W.J. Wiegers, Flavouring with indane alkanols and tricyclic isochromans, US. Pat. №4315951 (1982)] описан способ получения продуктов совместной димеризации α-метилстирола и изопентенов (мольное соотношение 1: 1,13) - 1,1,2,3,3-пентаметилиндана (8) и 3-этил-1,1,3-триметилиндана (9) в присутствии глин (SPA-2 и Filtrol) при 125°С. В качестве растворителей использовались октан, нонан, 2,4,4-триметилпентан и другие. Соотношение катализатора и реагентов может варьироваться от 0,1 до 8% от общего веса используемого альфа-метилстирола и изоамилена. Давление для проведения этой реакции зависело от температуры реакции и могло варьироваться от 3 атм до 20 атм. Реакция может быть проведена периодически, непрерывно или в полу-периодическом режиме в течение 2-10 часов. Общее содержание содимеров 8 и 9 в продукте достигает 66%. Выход 5% от теоретического на α-метилстирол.
В работе [51. Naresh F. Shah, Mahalaxmi S. Bhagwat and Man Mohan Sharma Cross-dimerization of α-methylstyrene with isoamylene and aldol condensation of cyclohexanone using a cation-exchange Reactive Polymers, 22 (1994) 19-34] для синтеза гомо- и содимеров α-метилстирола с изоамиленами использовали макропористую катионообменную смолу Amberlyst 15 и обработанную кислотой глину F-24 (фирма Engelhard, США). Все эксперименты проводились в автоклаве при следующих условиях реакции: содержание катализатора 5% мас., соотношение α-метилстирола к изопентенам=1:1,2, температура 100°С, автодавление, время реакции 2,5 ч после достижения заданной температуры. Максимальная конверсия α-метилстирола достигает 90%. Селективность по содимерам (8,9) на катионообменной смоле Amberlyst-15 достигает 39-61% (доля от смеси с димерами альфа-метилстирола) и 38-62% (доля от смеси с димерами изопентенов) после 4 ч реакции. На кислотной глине (F-24) эти значения соответственно равны 34-66% и 80-20%.
Недостатками использования ионообменных смол [52. Antunes В.М., Rodrigues А.Е., Lin Z., Portugal I., Silva C.M. Fuel Processing Technology. 2015. V. 138 P. 86-99] являются: 1) температурные ограничения их использования (120°С); 2) дезактивация при повышении температуры и необратимая деактивация при повышенных температурах, и, как следствие, невозможность реактивации; 3) быстрая дезактивация из-за наличия примесей в реакционной массе (например, NaOH); 4) необходимость добавления стадии гидрирования в случае наличия в сырье диенов (бутадиена), для того, чтобы избежать дезактивации; 5) выход содимеров α-метилстирола и изопентенов ограничивается 40%, в том числе, из-за появления в реакционной массе продуктов распада гомо- и содимеров α-метилстирола и изопентенов.
Задачей настоящего изобретения является разработка малостадийного, экологически безопасного способа получения гомо- и содимеров α-метилстирола и изопентенов, позволяющего получать олигомеры с высоким выходом в мягких условиях, в периодическом реакторе.
Решение поставленной задачи достигается тем, что способ получения смеси гомо- и содимеров α-метилстирола и изопентенов осуществляют взаимодействием α-метилстирола и изопентенов в присутствии иерархического цеолита Y в Н-форме (цеолит H-Yммм).
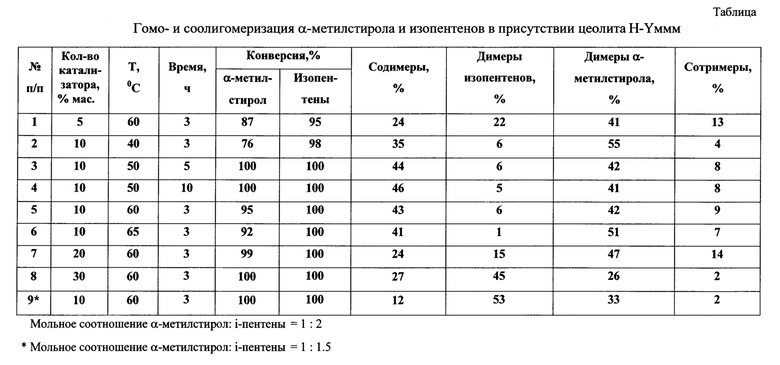
Содержание катализатора составляет 5-30% мас. в расчете на смесь мономеров. Реакцию проводят в хлорбензоле при мольном соотношении α-метилстирол : i-пентены=1:1,5-2, при 40-65°С в течение 3-10 ч. Конверсия α-метилстирола и алкенов до 100%, селективность образования содимеров достигает 46%, гомодимеров изопентенов - 1-53, гомодимеров α-метилстирола - 26-55%, количество сотримеров - 2-14% мас.
Цеолит Y-ммм синтезирован в виде гранул без связующих веществ; его гранулы представляют собой единые сростки цеолитных кристаллов и обладают близкой к 100% степенью кристалличности. Пористая структура гранул состоит из микропористой структуры самого цеолита Y, а также мезо- и макропористой структуры, сформировавшейся между сростками кристаллов. Применение цеолита Y-ммм в синтезе соолигомеров альфа-метилстирол и изопентенов неизвестно.
Существенным преимуществом цеолита H-Ymmm перед высокодисперсными (порошкообразными) цеолитами является то, что он синтезируется в гранулах. Гранулированный катализатор обладает лучшими физическими свойствами: не пылит, не слеживается, легко рассеивается и легко отделяется от реакционной массы фильтрованием (в отличие от высокодисперсного, который быстро забивает фильтр или проходит через полотно фильтра).
Кроме того, известно, что при глубоком декатионировании микропористых цеолитов Y (до степени ионного обмена катионов Na+ на Н+ выше 90-95%) происходит их частичная аморфизация и степень кристалличности уменьшается. Иерархическая кристаллическую структура цеолита H-Yммм высокостабильна и не разрушается в процессе декатионирования.
Преимуществом катализатора H-Yммм перед гранулированными цеолитами является отсутствие в составе конечной гранулы связующих материалов. Гранулы катализатора H-Yммм на 100% состоят из цеолита Y с иерархической пористой структурой.
Традиционный способ получения сформованных цеолитных катализаторов осуществляют следующим образом [Мухленов И.П., Добкина Е.И., Дерюжкина В.И., Сороко В.Е. / Под ред. д.т.н. проф. Мухленова И.П. Технология катализаторов. Производственное издание. Л. Химия. 1989. 137 с.]: смешивают высокодисперсный цеолит (в этой форме их обычно синтезируют) со связующим веществом (алюмосиликатом, оксидом алюминия, оксидом кремния), увлажняют эту смесь до получения пасты, формуют пасту в гранулы, в таблетки и т.д.; сушат полученные гранулы, таблетки. Полученный таким образом гранулированный катализатор представляет собой смесь цеолита и связующего вещества, что снижает эффективность действия катализатора.
Преимущества предлагаемого метода:
1. Позволяет снизить энерго- и материалоемкость процесса олигомеризации, поскольку синтез олигомеров проходит при более низкой температуре (40-65°С), чем в известных способах (100°С);
2. Получение гранулированного иерархического цеолита H-Yммм проводят прямым синтезом, без постобработок с использованием кислот или щелочей.
3. Синтез олигомеров проходит с практически полной конверсией исходных мономеров, хорошим выходом гомо- и соолигомеров α-метилстирола и изопентенов.
4. Полученные продукты реакции не подвергаются деструкции в ходе реакции.
5. Состав олигомеров можно варьировать, изменяя условия реакции.
Предлагаемый способ соолигомеризации α-метилстирола и изопентенов осуществляют следующим образом.
В качестве катализатора используют иерархический цеолит H-Yммм, синтезированный в Na-форме по методу, приведенному в [Патент РФ №2456238, 2012]. Декатионированием из раствора NH4NO3 и последующим прокаливанием при 540°С цеолит Na-Yммм переводят в Н-форму со степенью декатионирования ионов Na+ на H+ - 93-95%. В процессе ионного обмена с промежуточными термообработками аморфизация кристаллического каркаса цеолита не происходит. Удельная поверхность образцов по данным низкотемпературной адсорбции-десорбции азота составляет 735-798 м2/г, а объем микро-, мезо- и макропор - 0,28 см3/г, 0,15 см3/г, 0,14-0,15 см3/г, соответственно. Перед опытами катализатор прокаливают в атмосфере воздуха про 350°С в течение 4 ч.
В качестве источника изопентенов используют фракцию амиленов производства ОАО "Синтез-Каучук" (г.Стерлитамак), следующего состава, % масс.: β-транс-бутен - 0,03; β-цис- бутен- 0,05, изо-пентан - 0,84, н-пентан - 3,37, 3-метилбутен-1 - 3,00, пентен-1 - 0,93, 2-метилбутен-2 - 57,44, транс-пентен-2 - 2,98, цис-пентен-2 - 1,32, 2-метилбутен-1 - 29,36, пентадиен-1,3 - 0,68.
Реакцию проводят в хлорбензоле при мольном соотношении α-метилстирол : изопентены=1:1,5-2, температуре 40-65°С и количестве катализатора 5-30 мас. % (в расчете на смесь мономеров). В реактор помещают хлорбензол, катализатор и мономеры. Перемешивают при температуре реакции в течение определенного времени. После окончания реакции реакционную массу отделяют от катализатора фильтрованием. Степень превращения исходных алкенов и состав олигомеров анализируют методами газожидкостной и высокоэффективной жидкостной хроматографии, хроматомасс-спектрометрии.
В указанных условиях реакции α-метилстирол образует гомодимеры: линейные 2,4-дифенил-4-метилбутен-1 (1) и 2,4-дифенил-4-метилбутен-2 (2) или циклический 1,1,3-триметил-3-фенилиндан (3) и небольшое количество тримеров. Изопентены (преимущественно,  превращаются в димеры (2,3,4,4-тетраметил-1-гексен, Е- 3,5,5-триметил-2-гептен, 3,4,5,5-тетраметил-2-гексен, 3,5,5-триметил-3-гексен) и тримеры С15Н30.
превращаются в димеры (2,3,4,4-тетраметил-1-гексен, Е- 3,5,5-триметил-2-гептен, 3,4,5,5-тетраметил-2-гексен, 3,5,5-триметил-3-гексен) и тримеры С15Н30.
Индановые продукты содимеризации α-метилстирола и изопентенов - 1,1,2,3,3-пентаметилиндан (8) и 3-этил-1,1,3-триметилиндан (9). Содержание содимеров в димерной фракции достигает 50% мас.
Катализатор иерархический цеолит H-Yммм легко отделяется фильтрованием. Может использоваться многократно без потери активности.
Предлагаемый способ иллюстрируется следующими примерами.
ПРИМЕР 1.
В реактор периодического действия загружают 0,5 мл альфа-метилстирола (1 моль), 0,84 мл (2 моль) изопентенов в 1 мл хлорбензола и 0,1 г иерархического цеолита H-Yммм (5% мас. на смесь олефинов). Колбу герметично закрывают и помещают на магнитную мешалку. Реакцию проводят при 60°С в течение 3 ч при непрерывном перемешивании. После окончания синтеза реакционную массу охлаждают, отделяют от катализатора фильтрованием и анализируют. Гомо- и содимеры выделяют при помощи перегонки.
Состав олигомеров (% мас.): содимеры - 24%; димеры изопентенов - 22%; димеры α-метилстирола - 41%; сотримеры - 13%. Конверсия α-метилстирола - 87%, изопентенов - 95%.
Остальные примеры приведены в таблице.
ПРИМЕРЫ 2-9. Аналогично примеру 1. Условия и результаты примеров представлены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гомо- и соолигомеров α-метилстирола и изопентенов в присутствии мезопористого алюмосиликатного катализатора ASM | 2020 |
|
RU2759627C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ГОМО- И СОДИМЕРОВ СТИРОЛА И АЛЬФА-МЕТИЛСТИРОЛА | 2010 |
|
RU2430079C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ЛИНЕЙНЫХ И ЦИКЛИЧЕСКИХ ГОМО- И СОДИМЕРОВ СТИРОЛА И АЛЬФА-МЕТИЛСТИРОЛА | 2010 |
|
RU2428407C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ЛИНЕЙНЫХ И ЦИКЛИЧЕСКИХ ГОМО- И СОДИМЕРОВ СТИРОЛА И АЛЬФА-МЕТИЛСТИРОЛА | 2010 |
|
RU2424221C1 |
| Способ получения олигомеров изопентенов | 2022 |
|
RU2783680C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОМЕРОВ ПЕНТ-1-ЕНА В ПРИСУТСТВИИ ИЕРАРХИЧЕСКОГО ЦЕОЛИТА Н-Y | 2019 |
|
RU2709818C1 |
| Способ получения олигомеров пентена | 2022 |
|
RU2783661C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОМЕРОВ ПЕНТ-1-ЕНА В ПРИСУТСТВИИ АМОРФНОГО МЕЗОПОРИСТОГО АЛЮМОСИЛИКАТА ASM | 2019 |
|
RU2697885C1 |
| Способ олигомеризации изопентена | 2022 |
|
RU2794999C1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕНАСЫЩЕННЫХ ДИМЕРОВ α-МЕТИЛСТИРОЛА | 2001 |
|
RU2189963C1 |
Изобретение относится к способу каталитического получения гомо- и соолигомеров α-метилстирола и изопентенов. Способ характеризуется тем, что в качестве катализатора используют иерархический цеолит H-Yммм, реакцию проводят в хлорбензоле при мольном соотношении α-метилстирол : изопентены = 1:1.5-2, количестве катализатора 5-30% мас. на смесь исходных непредельных соединений, при 40-65°С, атмосферном давлении, в течение 3-10 ч. Технический результат: эффективный способ получения смеси гомо- и соолигомеров α-метилстирола с изопентенами, позволяющий получать целевые соединения с хорошим выходом, в мягких условиях. 1 табл., 9 пр.
Способ каталитического получения гомо- и соолигомеров α-метилстирола и изопентенов, отличающийся тем, что в качестве катализатора используют иерархический цеолит H-Yммм, реакцию проводят в хлорбензоле при мольном соотношении α-метилстирол : изопентены = 1:1.5-2, количестве катализатора 5-30% мас. на смесь исходных непредельных соединений, при 40-65°С, атмосферном давлении, в течение 3-10 ч.
| Naresh F | |||
| Shah, Mahalaxmi S | |||
| Bhagwat and Man Mohan Sharma, Cross-dimerization of a-methylstyrene with isoamylene and aldol condensation of cyclohexanone using a cation-exchange resin and acid-treated clay catalysts, Reactive Polymers, 22 (1994), 19-34 | |||
| Способ получения димеров или содимеров -олефинов | 1976 |
|
SU658119A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОМЕРОВ ПЕНТ-1-ЕНА В ПРИСУТСТВИИ ИЕРАРХИЧЕСКОГО ЦЕОЛИТА Н-Y | 2019 |
|
RU2709818C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНЫХ ДИМЕРОВ α-МЕТИЛСТИРОЛА | 2006 |
|
RU2316531C1 |
| Antunes В.М., | |||
Авторы
Даты
2020-11-05—Публикация
2020-02-17—Подача