Изобретение относится к способам получения водорода при взаимодействии металла с водой методом электролиза и к активации пассивных алюминиевых сплавов.
Прототипом настоящего изобретения может быть патент РФ №2032611, где активация металла осуществляется, как утверждают авторы, путем снятия окисной пленки алюминия в растворе галогенида щелочного или щелочно-земельного металла при пропускании постоянного электрического тока в режиме 1,5-0,3 В. Режим по току не приводится - значит он соответствует стандартной величине 2000 А/м2 (см. Ж.Биллитер. Промышленный электролиз водных растворов, стр.42, М. 1959 г.).
В цитируемом изобретении при электролизе применяется раствор поваренной соли, т.е. NaCl непонятной концентрации «17» (то ли в грамм-молях, то ли в кг/л, то ли в г/л). Известно (см. там же - стр.355-357), что при электролизе раствора поваренной соли на аноде образуются различные соединения хлора и сам хлор, что совершенно не желательно при производстве водорода. И если использовать выработанный на борту этим способом водород, например, на экологически чистом транспортном средстве, например на автомобиле, то куда девать при этом соединения хлора?
В предлагаемом нами способе с целью экономии энергозатрат и улучшения экологии используется обычная водопроводная вода, а в качестве катода, на котором выделяется при ее электролизе водород, самый распространенный сплав дюральалюминия Д16, имеющий состав: Cu 3,8-4,9%; Mg 1,2-1,8%; Mn 0,3-0,9%; Fe 0,5%; Si 0,5%; Ni 0,1%; остальное Al - по ГОСТ 4784-74).
Сущность способа заключается в следующем. Для процесса выделения водорода в основном использовались образцы в виде «сигары» d 17,7 и длиной 135 мм с эффективной реакционной поверхностью S=76 см кв. и в виде цилиндра d 16 мм и длиной 25 мм и S=16,5 см кв.
Газопроизводительность подсчитывалась по формуле:
q=V/(S·t) л/(м2·мин),
где V - объем выделившегося водорода, мл или л,
t - время выделения водорода, мин,
S - реакционная поверхность образца, см2.
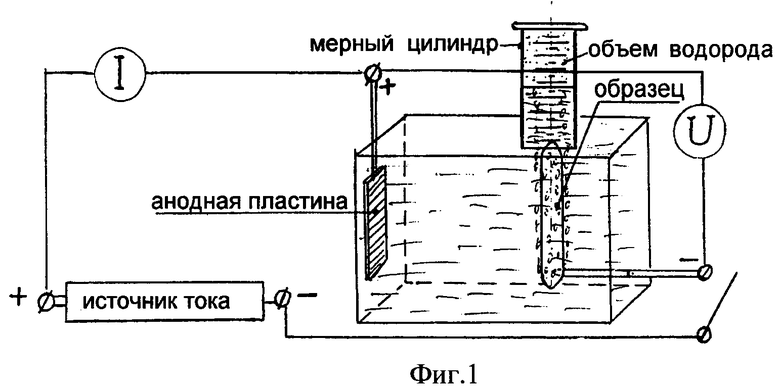
Опыты проводились в емкости из прозрачного оргстекла с внутренними размерами 137×137×90 мм (см. фиг.1) в обычной водопроводной воде. Исследуемый образец служил катодом и располагался в случае «сигары» вертикально, когда происходил замер газопроизводительности, или горизонтально, когда исследовалась равномерность выделения водорода по длине образца. Электролиз осуществлялся непосредственно от источника постоянного тока U=30 В или от сети переменного тока в 220 В через диод Д 245, в результате чего на расстоянии между электродами 40 мм получали U эф. = 110 В и ток I=200-300 мА в зависимости от размеров исследуемого образца. В дальнейшем для распространения данного способа было подтверждено выделение водорода и при 12 В. В качестве анода использовалась медная пластина.
Газопроизводительность измерялась методом вытеснения воды из мерного цилиндра объемом 200 мл и с ценой деления шкалы 0,5 мл. Схема установки представлена на фиг.1.
В опытах также подсчитывалась плотность тока: i=I/S, мА/см2.
Замер температуры воды осуществлялся термометром с точностью 1°С. В опытах использовались, кроме основного сплава Д 16, образцы из АД-1М (чистый Al), сплав AП (Zn 4-6%, Ti, Zr, T1 до 0,1% в сумме, Fe 0,1%, Cu 0,01% и Si 0,1%, остальное Al), алюминиевый сплав №90, где кроме Al-In и Ga по 3% (ВАМИ) с увеличенной газопропроизводительностью по сравнению со сплавом АП, сплав Al-Mg (АМГ6, где 5,8-6,9% Mg; 0,5-0,8% Mn, остальное Al), Fe и др.
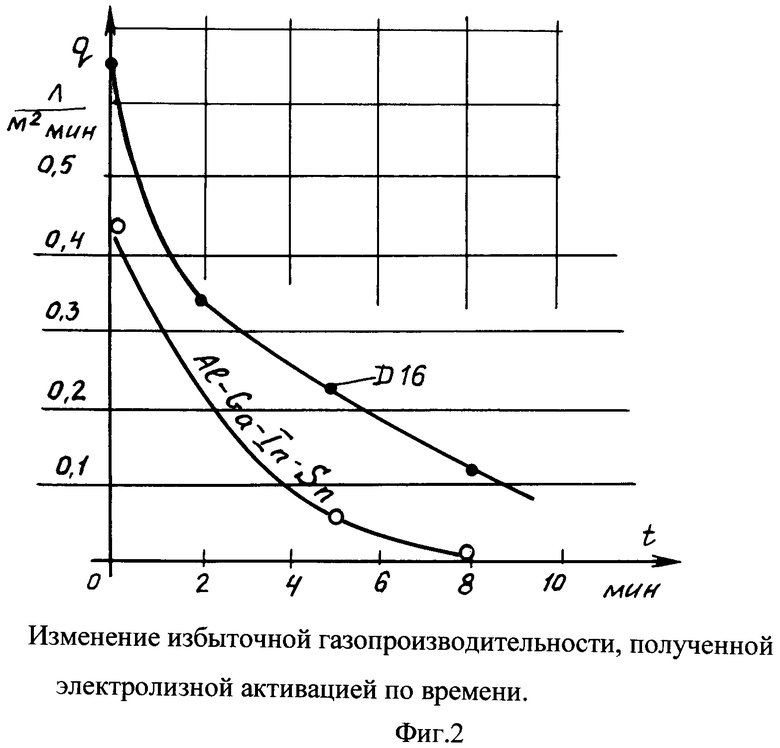
Результаты экспериментов занесены в таблицу 1 и показаны на фиг.2. Из представленных экспериментальных результатов наиболее интересны опыты, когда выделение водорода можно осуществлять в обычной воде, используя инертный сплав Д16, активируя его электрическим током в электролизной ячейке, например, в течение 20 мин с плотностью тока всего 4 мА/см2 при напряжении 30-110 В, затем ток отключается на 5-10 мин, в течение которых выделяется водород. Далее активация идет в каждом последующем цикле в течение более короткого промежутка времени 1-10 мин, и процесс выделения водорода идет с постепенным ослаблением. Т.е., создавая различные режимы активации электрическим током, можно получать различные графики подачи водорода в сеть потребителя.
Как показали опыты, другие исследуемые материалы при исследуемых параметрах электролиза активации почти не поддавались, т.е при снятии напряжения выделение водорода тут же прекращалось или было незначительным (см. табл.1).
В работе Григорьева В.П., Гонтмахера Н.М., Кравченко В.М., Гершановой И.М. Влияние температуры на дифференц-эффект для Al марки АД-1М. Защита металлов. №3, том X1, 1975 г. авторы изучали дифференц-эффект на Al, специально подготовленном в различных растворах, марки АД-1М, где получена газопроизводительность по водороду 0,005 мл/см2 мин при плотности тока 4 мА/см2. При такой же плотности тока в наших опытах на сплаве Д16 было получено 0,066 мл/(см2 мин), т.е. в 13 раз выше.
Чем этот сплав отличается от исследованных в этих опытах различных металлов и сплавов, где после отключения тока процесс выделения водорода прекращался. Тем, что он содержит два основных элемента Al и Cu, образующих при определенных условиях неустойчивые гидриды и хорошую гальванопару, и то, и другое создает самоподдерживающийся процесс генерации водорода.
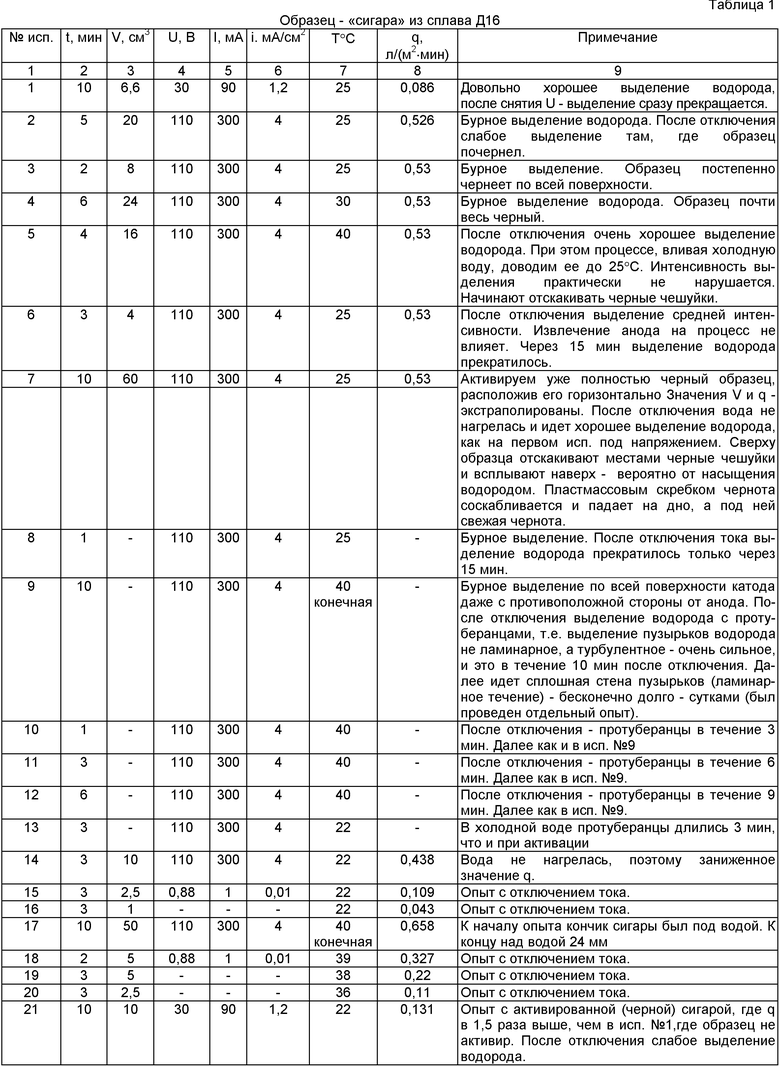
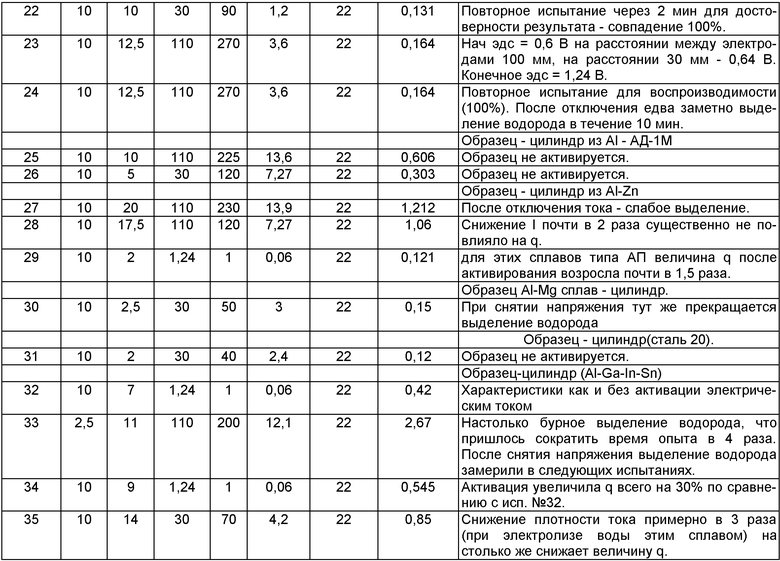
Пояснения к таблице 1
При составлении формулы изобретения первое испытание было пробным при использовании маломощного источника постоянного тока и поэтому при составлении формулы изобретения не рассматривалось. Учитывались испытания №21-22 уже активированного Al. Главное в электролизе - плотность тока. Поэтому, используя бытовое напряжение сети 220 В, через простейший выпрямитель добивались плотности тока 4 мА/см2. Как показывают проведенные эксперименты, чем выше плотность тока, тем значительнее эффект. 20-минутное активирование - это суммарное время испытаний №2 - №6.
Для каждого образца время, указанное в столбце №2, - это последовательные промежутки времени, следующие друг за другом (но только для одного образца).
На фиг.2 для сплава Д16 приведены данные испытаний №№17-20, и для сравнения показано падение избыточной газопроизводительности на сильноактивированном образце №90 по времени при тех же условиях. Сам образец без активации электрическим током показал q=0,42 л/(м2·мин) (исп.№32).
Исп.23 и 24 проведены на свежем (неактивированном) образце из Д16 с целью определить, как меняется эдс в начале испытания (ток еще не подавали) и в конце испытания после активации электрическим током в течение 10 мин, т.е после снятия напряжения. Проведено сравнение с испытанием №32. Нейтральный образец из Д16 имел после активации электрическим током такое же значение эдс как и сильно активированный образец №90, у которого в воде постоянно нарушена окисная пленка.
Как указывалось выше в прототипе, плотность тока составляет 200 мА/см2 при напряжении 1,5-2 вольта, т.е. 0,4 Вт в нашем изобретении мощность та же самая, но она подается не все время, а циклически, за счет чего достигается экономия энергозатрат при производстве водорода. Кроме того, получаемую при этом эдс = 1,24 В можно использовать в батареях таких электролизеров как дополнительный источник энергии. Кроме того, растворяющийся при этом катод из Д16 образует нерастворимый в воде осадок - Al2O3 (этот окисел при восстановлении относится к возобновляемым источникам энергии), которого по весу почти в 2 раза больше исходного Al, а стоимость его в 3-4 раза выше исходного Al.
С точки зрения экологии разложение воды, не содержащей галогенидов щелочных металлов, и образование безвредной окиси Al не нарушает экологию окружающей среды.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ И ХРАНЕНИЯ АТОМАРНОГО ВОДОРОДА | 2013 |
|
RU2570436C2 |
| СПОСОБ И УСТРОЙСТВО ПОЛУЧЕНИЯ ВОДОРОДА | 2012 |
|
RU2532561C2 |
| КАТОД ЭЛЕКТРОЛИЗЕРОВ ДЛЯ РАЗЛОЖЕНИЯ ВОДЫ С ВЫСОКИМИ РАБОЧИМИ ХАРАКТЕРИСТИКАМИ | 2009 |
|
RU2505624C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА | 2015 |
|
RU2602905C2 |
| СПОСОБ ОЧИСТКИ ПРИРОДНЫХ ВОДОЕМОВ ОТ СЕРОВОДОРОДА | 2017 |
|
RU2671724C1 |
| Способ амальгамирования металлов и сплавов,слабовзаимодействующих с ртутью | 1983 |
|
SU1133311A1 |
| СПОСОБ И УСТРОЙСТВО НАСЫЩЕНИЯ ЖИДКОСТИ ГАЗОМ | 2007 |
|
RU2378202C2 |
| ВОДА, ПОЛУЧЕННАЯ ОБРАБОТКОЙ ЭЛЕКТРОЛИЗОМ В КАТОДНОЙ КАМЕРЕ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2000 |
|
RU2220108C2 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОВ И/ИЛИ СПЛАВОВ ИЗ МАЛОРАСТВОРИМЫХ И НЕРАСТВОРИМЫХ СОЕДИНЕНИЙ | 2012 |
|
RU2517090C1 |
| Способ рециклинга алюминия электролизом расплава его лома и устройство для осуществления этого способа | 2022 |
|
RU2796566C1 |
Изобретение относится к области химии и может быть использовано при получении водорода электролизом. В качестве электролита используют водопроводную воду. В качестве анода используют пластину из меди, а в качестве катода - сплав Д16 - дюральалюминий. При напряжении в электролизной ячейке 30-110 В, плотности тока 4 мА/см2 сплав активируется 20 мин. Затем ток отключается на 5-10 мин, после чего активацию при каждом последующем цикле проводят в течение 1-10 мин. Изобретение позволяет снизить энергозатраты и улучшить экологию. 2 ил., 1 табл.
Способ получения водорода методом электролиза, отличающийся тем, что в качестве электролита используют водопроводную воду, в качестве анода - пластину из меди, а в качестве катода - сплав Д16 - дюральалюминий, при напряжении в электролизной ячейке 30-110 В, плотности тока 4 мА/см2 сплав активируется 20 мин, затем ток отключается на 5-10 мин, после чего активацию при каждом последующем цикле проводят в течение 1-10 мин.
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА | 1991 |
|
RU2032611C1 |
| Способ получения водорода | 1957 |
|
SU111165A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА | 2006 |
|
RU2314253C1 |
| JP 57013187 A, 23.01.1982 | |||
| Зонд | 1985 |
|
SU1417880A1 |
| US 2008245673 A1, 09.10.2008 | |||
| US 4466868 A, 21.08.1984. | |||
Авторы
Даты
2012-01-10—Публикация
2009-04-06—Подача