Изобретение относится к медицине, а именно к созданию нового ксеногенного биоматериала, используемого в качестве тканевого трансплантата для регенеративной хирургии.
Решаемая задача сводится к разработке нового доступного биоматериала с высокими показателями модуля упругости и предела прочности на линейное растяжение и сжатие, хорошей моделируемостью и прочностью шовной фиксации. Подобные биоматериалы востребованы при замещении объемных дефектов тканей, пластики сухожилий и связок, а также создании трансплантатов с фиксирующими, каркасными и мембранными (ограничительными) свойствами.
Для выполнения подобных восстановительных операций на структурах опорно-двигательного аппарата, замещении подкожных дефектов используются различные виды аллогенных трансплантатов: сухожильные, фасциальные, дермальные, жировые и т.д. (Коваленко П.П. Основы трансплантологии. - Ростов-на-Дону: Изд. Ростовского университета. - 1975, - 180 с.).
Однако следует учитывать, что сырьем для данного биоматериала служат аллогенные ткани трупа-донора, требующие строгой морфологической и биомеханической селекции и тестирования на этапах забора и физико-химической обработки материала. Кроме того, в последние годы серьезно осложнились социальные проблемы, сопровождающие донорство. Имеются в виду юридические, исторические, культурные и религиозные ограничения в получении донорских тканей как в нашей стране, так и зарубежом. Поэтому, разрабатывая новые источники трансплантационного материала, методы его доклинической обработки, нами учитывались следующие факторы:
- достаточная сырьевая база для получения донорских тканей;
- унифицированный источник, обеспечивающий высокую степень стандартизации трансплантационного материала;
- технологичность на этапах обработки и стерилизации тканей, гарантирующая получение изделия, полностью соответствующего медико-техническим требованиям;
- отсутствие социальных ограничений в заборе донорского материала.
Указанным требованиям могут отвечать трансплантаты, получаемые из органов животных.
Известен ксеногенный биоматериал для регенеративной хирургии, представляющий собой коллагенную волокнистую ткань, получаемую из органов и кровеносных сосудов животных, обработанную путем промывки, дезинфекции, удаления внутренней мембраны, внешней серозной оболочки и других активных элементов, вызывающих иммунную реакцию (CN 1249935, МПК A61K 35/12, A61L 27/00, опубл. 12.04.2000 г.).
Недостатком известного ксеногенного биоматериала является видоспецифичность его состава с преимущественным содержанием коллагеновых белков. Такие трансплантаты вызывают выраженную иммунную реакцию со стороны организма реципиента, приводящую к рубцеванию, отторжению или инкапсуляции (П.П.Коваленко. Клиническая транплантология. Ростовское книжное издательство. - 1975 г. - с 25-26).
Известен биоматериал для пластики связок коленного сустава с преимущественным содержанием в его структуре эластина, получаемый из выйной связки человеческого трупного материала (аллогенный биоматериал).
Однако существующие ограничения по использованию аллогенных тканей не отвечают назначению изобретения - созданию нового доступного биоматериала для регенеративной хирургии. К тому же у человека выйная связка - это тоненькая ленточка, которую можно использовать для восстановления только одной связки.
Наиболее близким к предложенному является биоматериал Аллоплант для регенеративной хирургии с широким спектром морфогенетических и пластических свойств (Патент РФ №2189257, МПК A61L 27/00, опубл. 20.09.2002 г.).
Недостатком данного материала, как и любого другого аллогенного, являются описанные выше ограничения.
Задачей изобретения является создание доступного биоматериала для регенеративной хирургии с предельно низкими антигенными свойствами при сохранении биопластических и физико-механических свойств исходных донорских тканей.
Поставленная задача решается биоматериалом для регенеративной хирургии, состоящим из консервированной донорской соединительной ткани, очищенной и обработанной с целью удаления антигенов, в которой на 80-90% разблокированы химические связи протеогликанов и гликопротеинов, структурированных в пучках соединительно-тканных волокон, и частично элиминированы из пучков волокон гликозаминогликаны до остаточного содержания ≥50%, в котором в отличие от прототипа в качестве донорской соединительной ткани используют выйную связку животных с содержанием эластина более 75%.
Согласно изобретению для регенерации рыхлой волокнистой соединительной ткани вводят инъекционно диспергированную форму, измельченную до порошкообразного состояния.
Основным отличием используемой донорской ткани является соотношение коллагена и эластина. Основная доля белков выйной связки приходится на эластин. Известные ксеногенные трансплантаты готовятся на основе тканей с абсолютным доминированием коллагена. В таблице приведен химический состав выйной связки быка в сравнении с наиболее часто используемым для изготовления трансплантата ахилловым сухожилием (А.И.Кононский. Биохимия животных. М., 1992 - с.442).
Как следует из приведенных данных, соотношение коллагена и эластина в сравниваемых материалах существенно различается. Как было показано выше, преимущественное содержание каллогена в ксеногенной трансплантируемой ткани вызывает иммунную реакцию со стороны организма человека. В то время как эластин, обладая более выраженными по сравнению с другими структурами морфогенетическими свойствами, способствует формированию функционально адекватного регенерата.
Для приготовления ксеногеннного биоматериала соединительную ткань - выйную связку животных, обрабатывают по известной технологии, применяемой для получения биоматериала Аллплант (Патент РФ №2189257, МПК A61L 27/00, опубл. 20.09.2002 г.) Выйную связку освобождают от жировой клетчатки и мышечной ткани, затем последовательно обрабатывают анионными и катионными детергентами с целью мембранолиза. Одновременно осуществляют контроль за разблокированием связей протеогликонов и гликопротеинов в пучках кологеновых волокон и элиминацией гликозаминогликанов. Контроль проводят гистохимическим методом. По достижении 80-90%-ного разблокирования связи протеогликанов и гликопротеинов и не более 50%-ной элиминации гликозаминогликанов обработку прекращают. Биоматериал отмывают от реагентов, фасуют в стеклянные флаконы, заливают консервантом и проводят радиационную стерилизацию с использованием ускорителя электронов. Полученный материал подвергают бактериологическому и хирургическому контролю.
Авторами были проведены экспериментальные исследования по подкожной пересадке биоматериалов, полученных из выйной связки крупного рогатого скота и подвергнутых стерилизации и консервации по известной технологии, описанной выше.
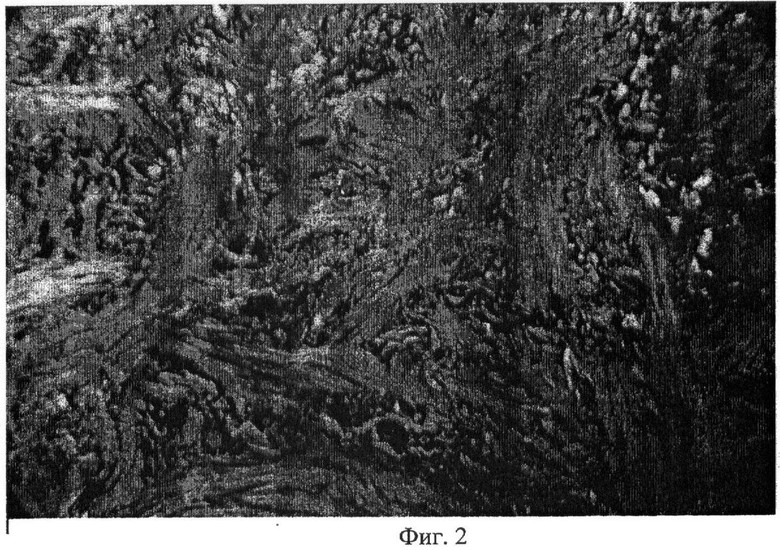
Для этого были поставлены две серии опытов. В первой серии подкожно в области голени имплантировался описанный биоматериал в виде пластины размерами 10,0×5,0×1,5 мм. Во второй серии готовился диспергированный биоматериал на основе выйной связки (размеры частиц до 120 мкм). После разведения в физиологическом растворе в соотношении 1:10 подкожно вводилось 0,5 мл биоматериала. Гистологические исследования проводились на 7, 14, 30, 120 и 360 сутки. При подсадке трансплантата в виде пластины (первая серия опытов) происходит медленная инвазия биоматериала макрофагальными недифференцированными соединительно-тканными клетками. Последние начинают синтезировать коллаген реципиента с их последующей агрегацией между эластиновыми волокнами трансплантата (фиг.1). При этом эластиновые волокна трансплантата выполняют формообразующую роль, и вновь синтезированный коллаген ориентируется вдоль волокон эластина, то есть юкстаппозиционно. Подобная морфогенетическая роль эластина хорошо прослеживается и на биопсийном клиническом материале. Последний был получен при выполненной двухэтапной операции через 2 месяца после подкожной пересадки трансплантата (фиг.2). На рисунке хорошо прослеживаются пучки новообразованных коллагеновых волокон между эластиновыми структурами. При этом формируется регенерат по типу плотной оформленной волокнистой соединительной ткани.
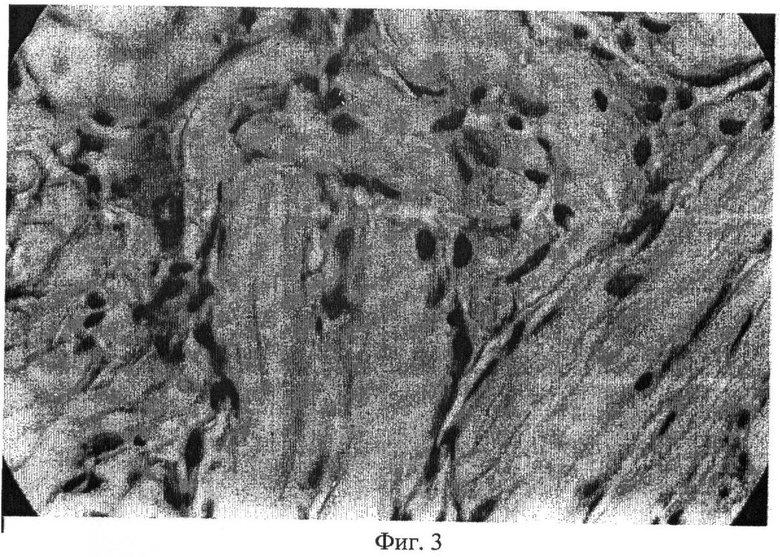
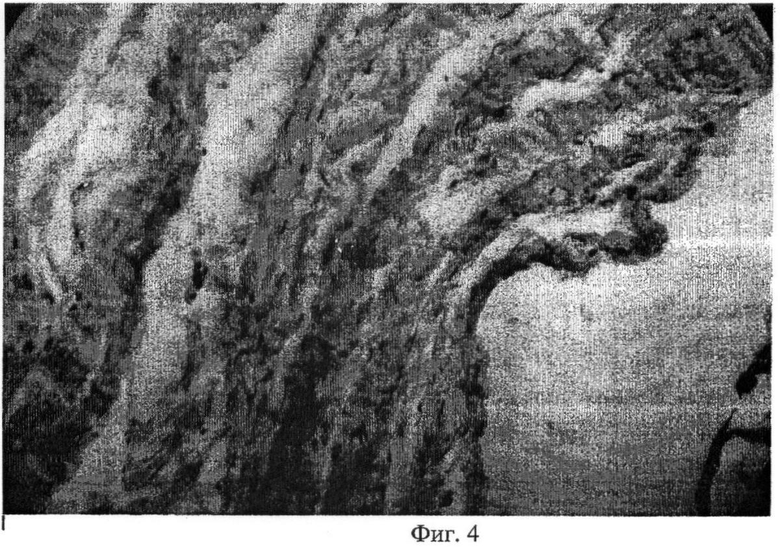
Во второй опытной серии происходит ранняя (7-14 сутки) инвазия диспергированного биоматериала клетками макрофагального дифферона (фиг.3). Клетки при этом занимают межпучковые пространства. В толще пучки эластиновых волокон свободны от мигрирующих клеток. Постепенно состав клеток становится полиморфным. Появляются гигантские многоядерные клетки, недифференцированные соединительно-тканные клетки. Уже на 30 сутки картина мозаичная - незначительных размеров фрагменты биоматериала чередуются с зонами резорбции и замещения. В области формирования регенерата имеются богатое сосудистое русло, жировые включения. В целом регенерат можно определить как относительно рыхлую волокнистую соединительную ткань. Аналогичная динамика морфогенетических процессов при трансплантации диспергированного эластина получена и в клинике (фиг.4).
Таким образом, используя различные структурные формы ксеногенного эластинового трансплантата, возможно моделирование функционально необходимого регенерата. Однако при этом следует учитывать, что спектр реконструктивных операций с использованием данного биоматериала достаточно ограничен. Его структура и биопластические свойства позволяют изготовлять трансплантаты для каркасной и фиксирующей пластики, замещения объемных дефектов, а также при необходимости использовать диспергированные формы.
Анатомические размеры выйной связки взрослого животного (2 доли каждая размером 55×8×1 см) позволяют моделировать из нее различные виды трансплантационных материалов с учетом задач хирургического вмешательства:
- лентовидный биоматериал - для фиксирующей пластики;
- пластинчатый биоматериал - для каркасной пластики;
- шаровидный биоматериал - для замещения объемных дефектов;
- мембранный биоматериал - для создания мембранных ограничителей;
- диспергированный биоматериал - для инъекционного введения.
Таким образом, предложенное изобретение позволяет использовать выйную связку животных для получения ксеногенного биоматериала для регенеративной хирургии с низкими антигенными свойствами, значительным модулем упругости и пределом прочности, адекватной моделируемостью и высоким уровнем стандартизации.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ДЕФЕКТОВ ПЕРЕДНЕЙ БРЮШНОЙ СТЕНКИ | 2009 |
|
RU2417763C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ДЕФЕКТОВ МЯГКИХ ТКАНЕЙ ЛИЦА С ИСПОЛЬЗОВАНИЕМ КСЕНОТРАНСПЛАНТАТА | 2009 |
|
RU2421154C1 |
| БИОМАТЕРИАЛ ДЛЯ ХИРУРГИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2780831C1 |
| БИОМАТЕРИАЛ АЛЛОПЛАНТ ДЛЯ РЕГЕНЕРАТИВНОЙ ХИРУРГИИ | 2001 |
|
RU2189257C1 |
| СПОСОБ ПОЛУЧЕНИЯ КСЕНОГЕННОГО БИОМАТЕРИАЛА ИЗ АОРТЫ СЕВЕРНОГО ОЛЕНЯ | 2023 |
|
RU2810102C1 |
| Биологически активная композиция Акваплант | 2019 |
|
RU2726001C1 |
| Способ увеличения толщины десны в области дентального имплантата при одномоментной установке дентального имплантата | 2024 |
|
RU2822326C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОЙ РЕГЕНЕРАЦИИ СУХОЖИЛИЙ И СВЯЗОК | 2005 |
|
RU2284768C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ АЛЛОГЕННЫХ ТРАНСПЛАНТАТОВ ПРИСЕРДЕЧНЫХ СОСУДОВ С КЛАПАНАМИ | 2010 |
|
RU2445940C1 |
| МИКРОНАНОСТРУКТУРИРОВАННЫЙ БИОПЛАСТИЧЕСКИЙ МАТЕРИАЛ | 2012 |
|
RU2481127C1 |

Изобретение относится к созданию нового биоматериала, используемого в качестве тканевого трансплантата для регенеративной хирургии. Ксеногенный биоматериал для регенеративной хирургии состоит из выйной связки животных с преимущественным содержанием эластина, очищенной и обработанной с целью удаления антигенов, в которой на 80-90% разблокированы химические связи протеогликанов и гликопротеинов, структурированных в пучках соединительно-тканных волокон, и частично элиминированы из пучков волокон гликозаминогликаны до остаточного содержания ≥50%. Изобретение позволяет создать доступный ксеногенный биоматериал для регенеративной хирургии с предельно низкими антигенными свойствами при сохранении биопластических и физико-механических свойств исходных донорских тканей. 1 з.п. ф-лы, 1 табл., 4 ил.
1. Биоматериал для регенеративной хирургии, состоящий из консервированной донорской соединительной ткани, очищенной и обработанной с целью удаления антигенов, в которой на 80-90% разблокированы химические связи протеогликанов и гликопротеинов, структурированных в пучках соединительно-тканных волокон, и частично элиминированы из пучков волокон гликозаминогликаны до остаточного содержания ≥50%, отличающийся тем, что в качестве донорской соединительной ткани используют выйную связку животных с содержанием эластина более 75%.
2. Биоматериал по п.1, отличающийся тем, что для регенерации рыхлой волокнистой соединительной ткани вводят инъекционно диспергированную форму, измельченную до порошкообразного состояния.
| БИОМАТЕРИАЛ АЛЛОПЛАНТ ДЛЯ РЕГЕНЕРАТИВНОЙ ХИРУРГИИ | 2001 |
|
RU2189257C1 |
| Способ пластики связок коленного сустава | 1987 |
|
SU1498475A1 |
| СПОСОБ ПОЛУЧЕНИЯ СУХОГО ГИДРОЛИЗАТА ЭЛАСТИНА | 2003 |
|
RU2245078C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛАСТИНА | 1995 |
|
RU2092071C1 |
| CN 1249935 А, 12.04.2000. | |||
Авторы
Даты
2012-01-20—Публикация
2009-12-21—Подача