Изобретение относится к медицине, а именно к оториноларингологии, и может применяться для функционально сохранного хирургического лечения рака гортани, в том числе, с негативными последствиями предшествующей лучевой терапии.
Гортань - анатомически и морфологически сложный орган, сочетающий функции коммутатора пищевого и дыхательного трактов, совершенного речевого и самого благозвучного в природе музыкального аппарата. Ее нормальное функционирование обеспечивает, таким образом, главные физиологические процессы организма, социальную интегрированность человека, его духовную жизнь. Эти обстоятельства предписывают особую деликатность действий хирурга и применение передовых технологических средств для максимальной сохранности функций гортани.
Созданию предлагаемого способа предшествует длительная история решения задачи адекватного замещения прочностного элемента гортани после обширной резекции по поводу опухолей.
Известен ряд органосохраняющих способов хирургического лечения рака гортани с вариацией имплантатов, протезирующих формообразующие структуры гортани, действий и приемов пластики образованного дефекта В способе [Быстренин В.А., Белый О.Н. К вопросу о гортанно-трахеальных протезах/ Вестник отоларингологии. 1981, №3, с.81-84] используют Т-образную трубку из резины, пластмассы или биологической ткани. Примитивизм протеза, низкая биосовместимость материалов приводят к недостаткам способа с точки зрения хирурга (сложность операции) и больного (низкое качество жизни), к низкой состоятельности лечения.
Более надежны способы с использованием для замещения удаленного хряща полимерных имплантатов [Ольшанский В.О., Битюцкий П.Т., Дарьялова С.Л. Современное состояние лечения рака гортани/ Вопросы онкологии, Т. XXXIII, 1989, с.41-47]. Способы позволяют сохранить объемную анатомию гортани, реабилитировать дыхательную и акустическую функции гортани. Однако низкая биосовместимость полимеров приводит к воспалительным последствиям, рубцовым стенозам, некрозам и отторжениям имплантатов.
Благоприятную возможность по критерию биосовместимости обеспечивает новый класс медицинских материалов - сплавы на основе никелида титана. Пластические операции с использованием никелид-титановых имплантатов более состоятельны.
Известен способ хирургического лечения рака гортани с использованием пластинчатого имплантата из проницаемо-пористого никелида титана [Патент РФ №2160564] в качестве протеза фрагмента щитовидного хряща.
Зияющий дефект щитовидного хряща, образованный в результате удаления местнораспространенной опухоли закрывают, во-первых, имплантатом из данного материала, надлежащим образом сформованным по анатомии щитовидного хряща и размерам дефекта, и парагортанными тканями - поверх. Способ для известного уровня техники высокосостоятелен и эффективен. Недостатки способа обусловлены открытой для внутренней среды гортани пористой поверхностью имплантата, которая служит сорбентом бактериальной воспалительной флоры в течение длительного срока реэпитализации.
В известном способе [Патент РФ №2359621] вышеуказанный недостаток умерен подстиланием имплантата с внутренней стороны аутотканью для изоляции и ускорения реэпитализации. Способ осуществляют следующим образом.
После трахеостомии выполняют доступ, мобилизацию щитовидного хряща и его рассечение на участке внешней окраины проекции опухоли на его поверхность. Верхнюю надхрящницу щитовидного хряща отсепаровывают на ножке и отводят до противоположного участка внешней окраины опухоли. Местнораспространенную опухоль удаляют вместе с прилежащим фрагментом щитовидного хряща. Укрытие образованного зияющего дефекта с соблюдением объемных размеров и анатомической формы гортани (формирование неогортани) начинают отсепарованной верхней надхрящницей, поверх которой устанавливают с опорой на края дефекта сформованный пластинчатый имплантат из проницаемо-пористого никелида титана. Фиксация имплантата происходит за счет естественной адгезии шероховатой поверхности материала к мягким тканям краев раны (эффект «липучки»). Операцию завершают штатными действиями дренирования и ушивания раны. Повышенная, по сравнению с предыдущим аналогом, состоятельность операции оставляет необходимость дальнейшего совершенствования способа.
По наибольшему сходству данный аналог выбран в качестве прототипа.
Технический результат предлагаемого изобретения - повышение состоятельности операции при лечении рака гортани в осложненных условиях гиперемии и отека парагортанных тканей.
Указанный технический результат достигается тем, что в способе хирургического лечения рака гортани, включающем наложение трахеостомы, осуществление доступа, выделение щитовидного хряща и выполнение в нем тиреофиссуры, удаление местнораспространенной опухоли, пластику образованного дефекта и формирование неогортани с использованием никелид-титаного каркаса, послойное ушивание раны, доступ осуществляют поперечным полулунным разрезом по нижней шейной складке, отсепаровывают с отведенным кверху кожно-жировой лоскут, отсепаровывают с отведением вбок лоскут подкожной мышцы шеи на ножке.
В качестве каркаса неогортани используют лоскут никелид-титановой ткани, сформированной по топографии щитовидного хряща и размерам образованного дефекта. Пластику образованного дефекта и формирование неогортани выполняют последовательным послойным укрытием дефекта лоскутом на ножке из подкожной мышцы шеи, каркасом неогортани и кожно-жировым лоскутом на ножке, причем каркас неогортани фиксируют к надкостнице подъязычной кости, перстневидному хрящу и краевым тканям образованного дефекта.
Достижимость технического результата обусловлена, главным образом, использованием иного, по сравнению с прототипом, материала каркаса неогортани, другим его расположением и отдельными действиями, связанными с осуществлением способа.
Никелид-титановая ткань, подобно, пористому литью, относится к материалам со сквозной проницаемостью. Обладая высокой биосовместимостью, эти материалы энергично, надежно и, в большой степени, органично интегрируются с живыми тканями. Тканевая структура используемого имплантата обладает, кроме того, эластичной и мягкой деформационной способностью. Это свойство позволяет технологически легко (особенно важно, интраоперационно) и функционально корректно изготавливать объекты нерегулярной и сложной формы, подобно фрагменту щитовидного хряща. Мягкая структура материала обеспечивает меньшую конфликтность с совмещаемыми аутотканями на опорных и трудносопрягаемых участках. Это снижает возможность постоперационных осложнений, отторжения имплантата, сокращает сроки реконвалесцении.
Исследованиями авторов предложения показана актуальная возможность высокоэффективной интеграции никелид-титанового материала с гиперемированными тканями гортани, подвергшимися дооперационной лучевой терапии.
Успеху интеграции имплантата и зависящего от этого общего репарационного процесса способствует выбранная структура слоистого укрытия образованного после удаления опухоли зияющего дефекта гортани. Внутренняя поверхность первого по расположенности подкожно-мышечного слоя легче других парагортанных тканей реэпитализируется, обеспечивая тем самым нормальную работу гортани в ее вышеупомянутой комбинированной функции. Внешняя поверхность этого лоскута соприкасается с тканью имплантата и через ее просветы - с жировым слоем следующего, кожно-жирового лоскута. Таким образом, имплантат, кроме формообразующей роли каркаса неогортани, благодаря его высокой и универсальной биосовместимости, служит соединительным, а в отдаленные сроки армирующим элементом образованного слоистого блока тканей. Повышению состоятельности операции также служит конструктивный прием - выполнение дубликатуры по периметру и центру лоскута никелид-титановой ткани, которая, образуя ребра жесткости, дополнительно стабилизирует заданную форму, улучшая каркасную функцию имплантата.
Сочетание указанных положительных свойств приводит к техническому результату. Соответствуют ему также, связанный со структурой материала, более удобный для хирурга и менее травматичный для больного доступ к операционному полю через полулунный разрез по нижней шейной складке. Прием фиксации имплантата к надкостнице подъязычной кости и перстневидному хрящу наиболее надежен и безопасен для голосовых связок.
Новая совокупность технических средств и хирургических действий при осуществлении операций, неочевидность логических связей признаков с техническим результатом свидетельствуют о соответствии предложения критерию «изобретательский уровень».
На иллюстрациях представлено:
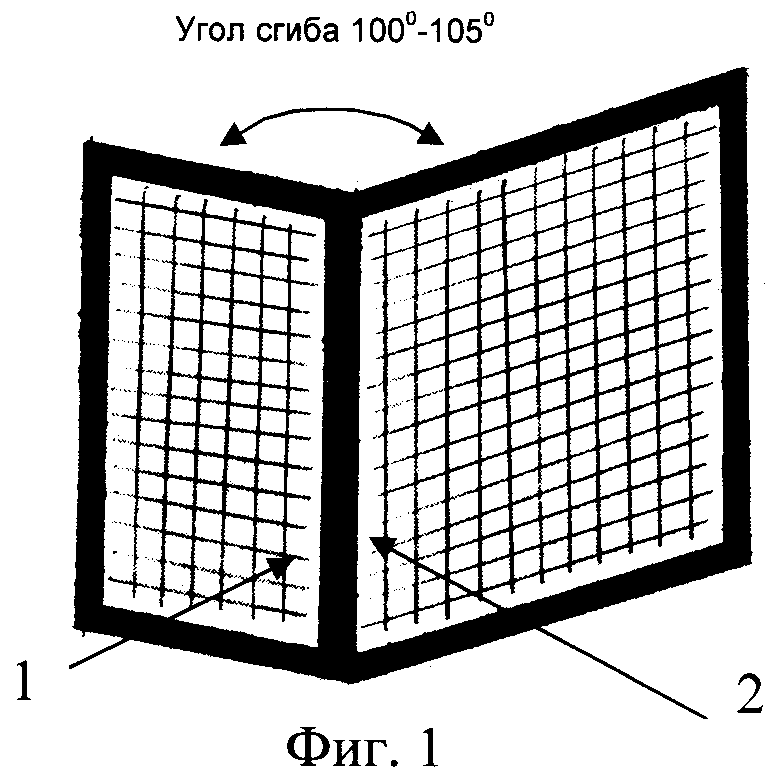
Фиг.1. Внешний вид каркаса неогортани. 1 - текстильная ткань из никелид-титановой нити, 2 - дубликатура центрального участка.
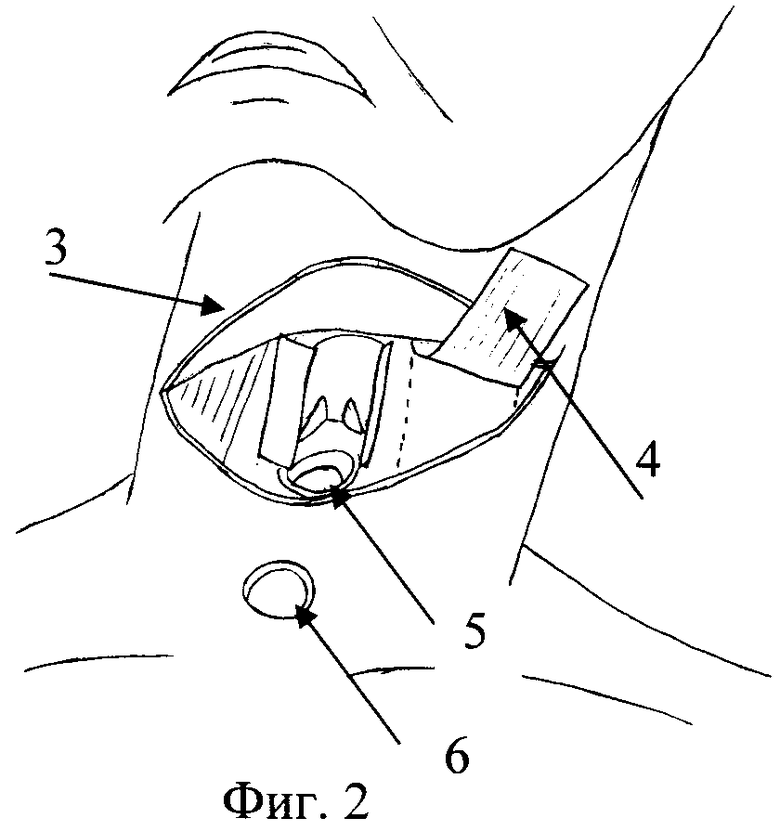
Фиг.2. Фрагмент операции. Вскрытие операционного поля. 3 - кожно-жировой лоскут, 4 - лоскут подкожной мышцы шеи, 5 - тиреофиссура щитовидного хряща, 6 - трахеостома.
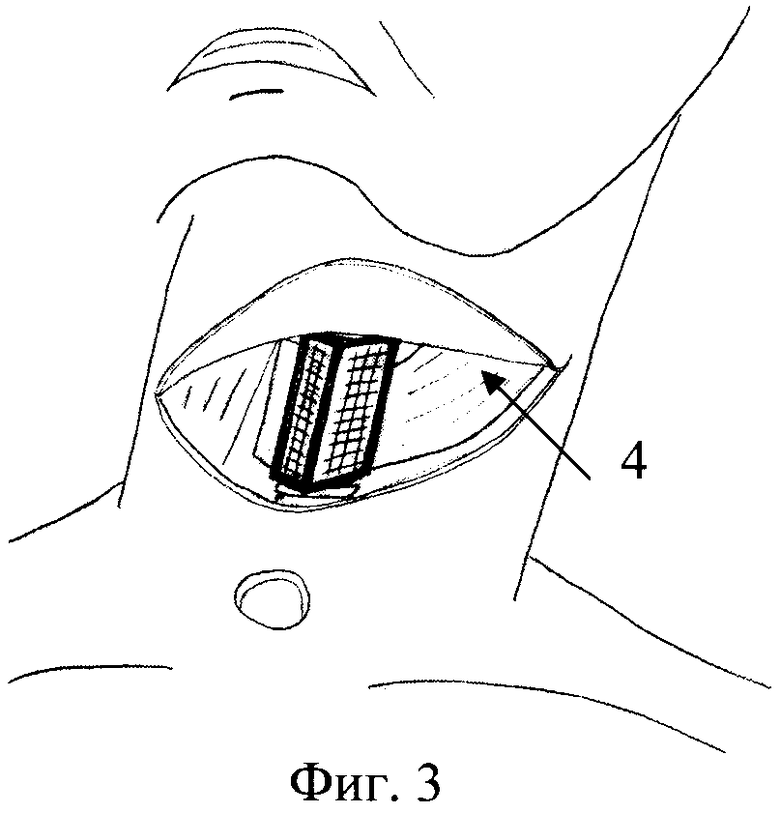
Фиг.3. Фрагмент операции. Установка каркаса неогортани.
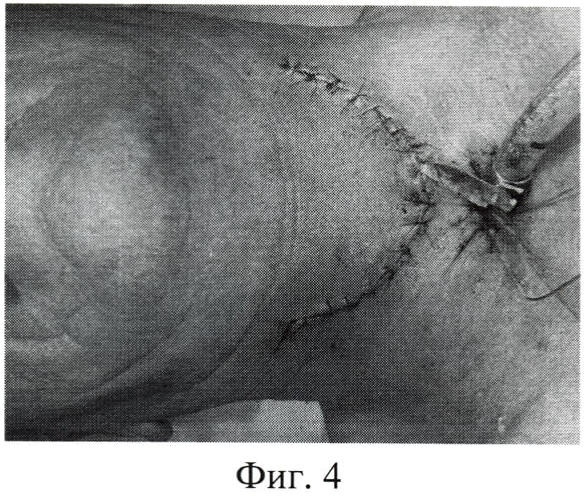
Фиг.4. Внешний вид раны после ушивания.
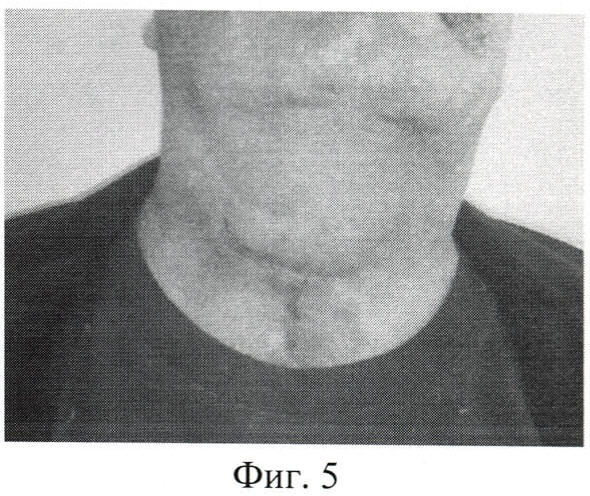
Фиг.5. Внешний вид больного после операции.
Достижимость технического результата подтверждена конкретными клиническими примерами лечения рака гортани в НИИ онкологии СО РАМН (г.Томск).
Пример 1. Больной М., 53 лет. Диагноз заболевания: умеренно-дифференцированный, неороговевающий плоскоклеточный рак гортани T1NOMO. Состояние продолжительного роста после дистанционной гамма-терапии СОД 60 Гр.
Опухоль занимает левую голосовую складку с распространением на переднюю комиссуру.
Больному выполнено хирургическое лечение по методике предлагаемого способа, который осуществлен следующим образом.
По предварительным обмерам объема предстоящей резекции изготовлен имплантат (фиг.1) из никелид-титановой ткани для каркасного армирования комплекса неогортани. Центральный участок 1 имплантата в соответствии с анатомией щитовидного хряща изогнут под углом около 100°. Жесткость этого участка и краевых участков по периметру усилена дубликатурой ткани. Толщина никелид-титановой нити ткани 300 мкм; текстура ткани текстильная, слаборазреженная.
Под местной анестезией наложена трахеостома 6 (фиг.3). Доступ осуществлен горизонтальным полулунным разрезом по нижней шейной складке. Кожно-жировой лоскут 3 с участка проекции опухоли на поверхности отсепарован на интактной ножке и отведен кверху с выделением щитовидного хряща, лоскут подкожной мышцы 4 отсепарован и отведен вбок. Резекция щитовидного хряща в едином блоке с опухолью выполнена в границах: слева - на 1 см от заднего края, справа - на 1,5 см от угла щитовидного хряща, сверху - по щитоподъязычной связке, ближе к подъязычной кости, снизу - по конической связке, ближе к перстневидному хрящу. При резекции сохранена фиксация констрикторов глотки к задним отделам щитовидного хряща. Произведен интраоперационный цитологический контроль по линии резекции. Выполнен тщательный гемостаз. В полость гортани установлен обтуратор. Зияющий дефект укрыт послойно лоскутом подкожной мышцы с шовной фиксацией его к краям раны, далее - изготовленным и простерилизованным имплантатом (фиг.1) и репонированным кожно-жировым лоскутом. При этом шовная фиксация имплантата произведена никелид-титановой нитью к надкостнице подъязычной кости, перстневидному хрящу и мягким тканям краев образованного дефекта. Послеоперационная рана ушита наглухо (фиг.4).
Заживление раны в послеоперационный период проходило первичным натяжением (фиг.5). Проводилась интенсивная антибактериальная терапия и санация полости неогортани через обтурацию, которой впоследствии, на 14-е сутки удален. Деканюляция осуществлена через 4 недели. По субъективным оценкам и данным инструментального обследования на 14-е и 30-е сутки репарационные процессы проходили ускоренно. К концу периода наблюдений поверхность неогортани покрылась розовой слизистой оболочкой. Просвет неогортани достаточно широкий, фоническая функция сохранена.
Пример 2. Больной М., 48 лет, поступил на лечение в НИИ онкологии г.Томска после комплексной, в том числе лучевой терапии в Забайкальском КОД (г.Чита) с верифицированным диагнозом заболевания: плоскоклеточный рак умеренной дифференцированности (номер гистологии 47728-29) с объективными данными: гиперемия черпало-надгортанных складок и надгортанника. Первая голосовая складка заполнена мелкобугристой опухолью с распространением на гортанный желудочек. Первая комиссура интактна. Подвижность правой голосовой складки при фонации ограничена.
Больному выполнено оперативное лечение по методике предлагаемого способа с вариацией действий, связанной с локализацией опухоли. Результаты лечения, по состоянию больного и данным контрольных обследований, при выписке из клиники свидетельствуют об успешности операции и достижимости технического результата, предлагаемого способа.
Техническая готовность и методическая отработанность способа на данный момент соответствуют критерию изобретения «промышленная применимость».
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2007 |
|
RU2359621C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2012 |
|
RU2487681C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2011 |
|
RU2475194C1 |
| Способ хирургического лечения местно-распространенного рака гортани и гортаноглотки | 2020 |
|
RU2736614C1 |
| СПОСОБ ПЛАСТИКИ ЗИЯЮЩИХ ДЕФЕКТОВ ТРАХЕИ | 2011 |
|
RU2456930C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 1999 |
|
RU2160564C1 |
| СПОСОБ ПЛАСТИКИ ЗИЯЮЩИХ ДЕФЕКТОВ ТРАХЕИ | 2010 |
|
RU2453281C1 |
| Способ реконструкции языка и дна полости рта после выполнения глоссэктомии | 2024 |
|
RU2826853C1 |
| СПОСОБ СОЗДАНИЯ ТРАХЕОСТОМЫ | 2002 |
|
RU2226991C2 |
| СПОСОБ РЕКОНСТРУКЦИИ ГОРТАНИ | 2001 |
|
RU2197906C1 |
Изобретение относится к области медицины, а именно к оториноларингологии, и может найти применение при хирургическом лечении рака гортани, в том числе с осложнениями от предшествующей лучевой терапии. Сущность способа состоит в наложении трахеостомы, осуществлении доступа, выделении щитовидного хряща и выполнении в нем тиреофиссуры, удалении местнораспространенной опухоли, пластике образованного дефекта и формировании неогортани с использованием никелид-титанового каркаса, послойном ушивании раны. При этом доступ осуществляют поперечным полулунным разрезом по нижней шейной складке. Отсепаровывают с отведением кверху кожно-жировой лоскут на ножке. Отсепаровывают с отведением вбок лоскут подкожной мышцы шеи на ножке. В качестве каркаса неогортани используют лоскут никелид-титановой ткани. Лоскут формируют по топографии щитовидного хряща и размерам образованного дефекта. Затем формируют ужестчающую дубликатуру по центру и периметру лоскута. Пластику образованного дефекта и формирование неогортани выполняют последовательным послойным укрытием образованного дефекта лоскутом на ножке подкожной мышцы шеи, каркасом неогортани и кожно-жировым лоскутом на ножке. Причем каркас неогортани фиксируют к надкостнице подъязычной кости, перстневидному хрящу и краевым тканям образованного дефекта. Использование данного изобретения позволяет повысить качество операции, сохранить функции гортани, включая фоническую. 5 ил., 2 пр.
Способ хирургического лечения рака гортани, включающий наложение трахеостомы, осуществление доступа, выделение щитовидного хряща и выполнение в нем тиреофиссуры, удаление местнораспространенной опухоли, пластику образованного дефекта и формирование неогортани с использованием никелид-титанового каркаса, послойное ушивание раны, отличающийся тем, что доступ осуществляют поперечным полулунным разрезом по нижней шейной складке, отсепаровывают с отведением кверху кожно-жировой лоскут на ножке, отсепаровывают с отведением вбок лоскут подкожной мышцы шеи на ножке, в качестве каркаса неогортани используют лоскут никелид-титановой ткани, сформированный по топографии щитовидного хряща и размерам образованного дефекта с формированием ужестчающей дубликатуры по его центру и периметру, пластику образованного дефекта и формирование неогортани выполняют последовательным послойным укрытием образованного дефекта лоскутом на ножке подкожной мышцы шеи, каркасом неогортани и кожно-жировым лоскутом на ножке, причем каркас неогортани фиксируют к надкостнице подъязычной кости, перстневидному хрящу и краевым тканям образованного дефекта.
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2007 |
|
RU2359621C1 |
| Способ лечения хронического рубцового стеноза гортани | 1990 |
|
SU1806634A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 1999 |
|
RU2160564C1 |
| ЧОЙНЗОНОВ Е.Л | |||
| и др | |||
| Рак гортани | |||
| Современные аспекты лечения и реабилитации | |||
| - Томск: Изд-во научно-техн | |||
| лит-ры, 2006, с.93-111 | |||
| КУЛЬБАКИН Д.Е | |||
| и др | |||
| Метод комбинированной реконструкции гортани после обширных резекций у онкологических больных | |||
| Сборник статей по | |||
Авторы
Даты
2012-03-20—Публикация
2010-10-12—Подача