Изобретение относится к медицинской технике хирургического лечения заболеваний трахеи.
Пластику зияющих дефектов трахеи - незакрывающихся послеоперационных трахеостом, травматических повреждений или иного генеза - выполняют послойным закрытием мягкими тканями шеи, мобилизованными оттянутыми со смежных с дефектом участков. Такая реконструкция стенки трахеи достаточно функциональна при поперечных размерах дефекта, не превышающих 10 мм. При больших размерах задача усложняется. Растянутые заменяющие мягкие ткани, не имеющие должной плотности и необходимой для стенки трахеи жесткости подвержены баллотированию в условиях форсированного дыхательного или кашлевого напряжения. Решение задачи наиболее актуально в детской хирургии вследствии того, что в детском возрасте мягкие ткани шеи находятся в стадии формирования, поэтому они нежнее и тоньше, чем у взрослых. Для парирования явления пролапса, а в экстремальных случаях - разрыва или перекрытия просвета стенки трахеи используют дополнительные элементы жесткости в виде арматуры в мягких слоях аутотканей. Их выполняют из биосовместимых, деформационно циклоустойчивых материалов, соответствие которых определяет состоятельность операции. Таким образом, совершенствование этой области хирургии напрямую связано с успехами материаловедения.
В уровне техники хронологически предшествуют остео- или хондропластика. В качестве материала опорных элементов используют аллогенные фрагменты костей или хрящей, взятых из большой берцовой кости, ребер или коленной чашечки. [Д.Богомильский. Применение марлекса при пластическом устранении послеоперационных ларинго трахеостом у детей, С.8.], аутогенные лоскуты из фиброзного слоя слизистой оболочкой нижней носовой раковины [Горбунов В.А., Вахмянин А.П., Викторова Г.И., Лекишвили М.В. Новые материалы в реконструктивной ларинготрахеопластике / 16-й съезд оториноларингологов. Россия: Тез. докл. - М, 2000. С.464-466] и другие аутотрансплантаты.
Ряд трудностей забора алло- и ауто-трансплантатов их низкая приживаемость, а следовательно, состоятельность всего хирургического вмешательства ограничили использование этих аналогов и понудили поиск более совершенных материалов и методик лечения. Успеху способствовали синтетические материалы, общим достоинством которых являются исключение операции (дополнительной травматизации больного) в донорской области и неограниченный ресурс материала для имплантации. Известен способ пластики послеоперационных трахеостом с использованием сетчатого марлекса. Марлекс достаточно плотен и умерено эластичен, настолько, что позволяет решать задачу даже в деликатной детской хирургии. [Вышеупомянутый аналог Д.Богомильского, с.86]. В отдаленные сроки имплантат прорастает соединительной тканью, увеличивая прочность реконструированной стенки.
Методическая биосовместимость полимеров проявляющаяся в химической нестойкости в агрессивных средах организма, повышенной вспомогательной и аллергической активности, ограничивают их применение в хирургии, в частности в пластике трахейных повреждений.
Прогрессу в этой области хирургии способствовали медицинские материалы на основе никелида титана. Их широкий успех обусловлен высокий биосовместимостью и отсутствием недостатков, отмеченных в вышеприведенных аналогах. Известен способ пластики зияющих дефектов трахеи, образованных в результате обширных резекций опухолей гортани и трахеи [Шинкарев С.А., Мухаммедов М.Р. и др. Клинический способ использования материала на основе пористого никелида титана в хирургическом лечении распространенного рака щитовидной железы / Материалы с памятью формы и новые технологии в медицине // Под ред. В.Э.Гюнтера, Томск., НИИ ММ. 2007. с.118]. В нем выполнено эндопротезирование резецированной стенки трахеи пластиной из пористого никелида титана с фиксацией ее лоскутом из левой кивательной мышцы. Для общего успеха сложной операции обусловлена реализацией вышеотмеченных достоинств пористого никелида титана в функционально обособленной задаче закрытия зияющих дефектов в трахеи. Объективный анализ результатов операции выявил также в качестве недостатка способа длительность приживления имплантата и общей реконвалесценции пациента.
Технический результат предлагаемого способа - сокращение сроков интеграции имплантата и повышение состоятельности операции.
Указанный технический результат достигается тем, что в способе пластики зияющих дефектов трахеи, включающем послойное закрытие зияющего дефекта местными тканями в сочетании с арматурной пластиной из проницаемо-пористого никелида титана, арматурную пластину предварительно внедряют между кожей и фасцией на участке шеи, смежном с зияющим дефектом, и выдерживают для вживления в течение 3-5 месяцев, выделяют на ножке кожно-фасциальный лоскут с вживленной арматурной пластиной и закрывают им предварительно освеженный зияющий дефект с ориентацией кожного слоя указанного лоскута внутрь трахеи.
Предпочтительно деэпидермизировать кожный слой выделенного кожно-фасцильного лоскута на краях, контактирующих с краями зияющего дефекта. Достижимость технического результата доминантно обусловлена предварительной дооперационной подготовкой имплантата, а именно консолидирующей интеграцией его с паратрахеальными тканями. В дальнейшем процесс заживления дефекта происходит быстрее, чем с одномоментным разрозненным закрытием дефекта аутотканями и интактным имплантатом. Интерпретация выявленного в ходе предварительных исследований свойства, возможно, сводится пролонгированному характеру иммунно-интеграционной реакции организма и временному распределению этих процессов в общих случаях.
Интервал выдержки имплантата для вживления, т.е. прорастания его соединительной, а впоследствии функциональной тканью выявлен для различного состояния больных. Для организма, ослабленного болезнью или предыдущими лечебными процедурами (например, лучевой терапией) необходим большой - до 5 месяцев - срок выдержки. Расположенность выделенного лоскута кожным слоем внутрь трахеи предохраняет имплантат от депонирования в нем болезнетворной флоры и ускоряет реэпитализацию.
Деэпидермизация контактных участков лоскута освежает ткань для быстрейшего срастания, эпилирует волосяные фолликулы, могущие функционировать и создавать помехи репарации.
Научно-исследовательский характер поиска, результаты которого доведены до технического решения задачи свидетельствует о его неочевидности, т.е. о соответствии критерию патентоспособности «изобретательский уровень»
На иллюстрации представлено:
Фиг.1. Внешний вид арматурной пластины.
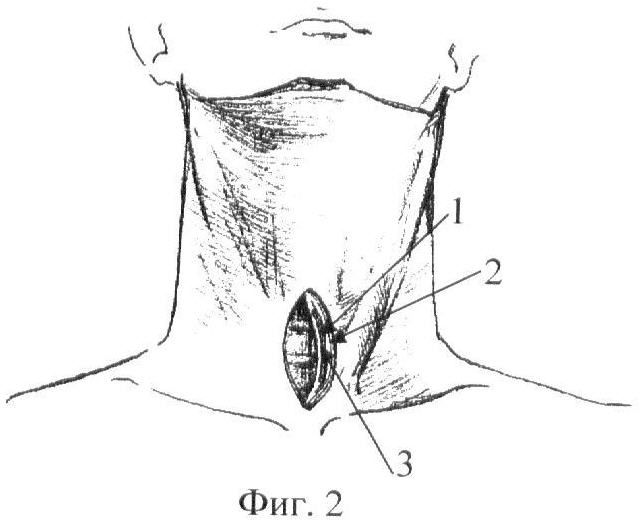
Фиг.2. Зияющий дефект трахеи - незарастающая трахеостома: 1 - арматурная пластина, 2 - слой кожи, 3 - фасция.
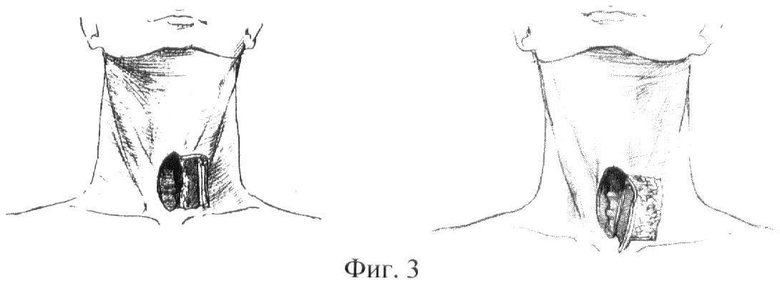
Фиг.3. Момент операции. Закрытие трахеостомы.
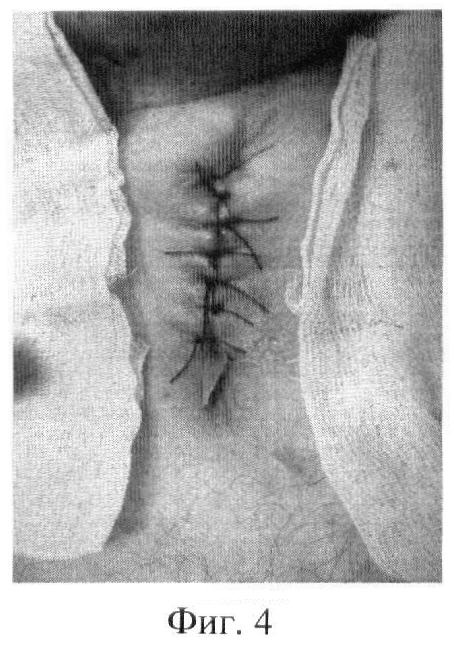
Фиг.4. Внешний вид больного после операции.
Подтверждением достижимости технического результата являются примеры клинического применения способа в органосохранных операциях на гортани в отделении опухолей головы и шеи НИИ онкологии Томского научного центра СО РАМН.
Пример 1. Больная Р., 48 лет. Диагноз заболевания - хронический (более 4-х лет) рубцовый стеноз гортани, развивающийся после проведения длительных реанимационных мероприятий, связанных с тяжелой черепно-мозговой травмой. После реконструктивной операции на гортани и длительной дилатации просвет гортани восстановлен. Незарастающая бесканюльная трахеостома размером 15×20 мм закрыта предлагаемым способом, который осуществлен следующим образом: на участке шеи, вдоль левого края трахеостомы выполнен кожно-фасцильный тоннель, в который внедрена пластина 1 (фиг.2) из проницаемо-пористого никелида титана с размерами 18×23×1,0 мм. После 3-месячной экспозиции и повторной госпитализации больной, выделен на ножке кожно-фасцильный лоскут по контуру вживленной пластины и проведена трахеопластика. Для этого края стомы освежены, а контактные края кожного слоя 2 лоскута деэпидермизированы ложкой Фолькмана. Лоскут наложен на края закрываемого дефекта с обращением кожного слоя внутрь трахеи (фиг.3). Кожная рана ушита с натяжением. Проведены протокольные мероприятия по выхаживанию больной. Больная выписана при восстановлении свободного дыхания через естественные пути. При последующем наблюдении в течение 1 года баллотирование восстановленного участка передней гортанно-трахеальной стенки отсутствовало, отторжение имплантата не произошло.
Пример 2. Больной И., 58 лет. Диагноз заболевания - рак гортани T2N0M0. Незарастающая бесканюльная трахеостома после комбинированной терапии и органосохранного хирургического лечения. Размеры трахеостомы 10×15 мм. Пластика трахеостомы (фиг.4) проведена по методике предыдущего примера с выдержкой армирующей пластины в кожно-фасциальном туннеле на смежном с дефектом участке в течение 3,5 месяцев. Восстановление свободного дыхания через естественные пути. Отсутствие баллотирования закрытого дефекта стенки в месте дефекта, свидетельствующее о работоспособности способа, сокращение до 40% периода реконвалесценции являются подтверждением заявленного технического результата. Клиническая отработанность способа, доступная для широкого использования техническая оснащенность соответствуют критерию изобретения «промышленная применимость»
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЛАСТИКИ ЗИЯЮЩИХ ДЕФЕКТОВ ТРАХЕИ | 2011 |
|
RU2456930C1 |
| СПОСОБ СОЗДАНИЯ ТРАХЕОСТОМЫ | 2002 |
|
RU2226991C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2010 |
|
RU2445014C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2011 |
|
RU2475194C1 |
| СПОСОБ ЗАКРЫТИЯ ДЕФЕКТА ТРАХЕИ И УСТРОЙСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ ПЕРВОГО ЭТАПА СПОСОБА | 2002 |
|
RU2230529C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2007 |
|
RU2359621C1 |
| СПОСОБ ИЗМЕРЕНИЯ ПЛОЩАДИ ЗИЯЮЩИХ ДЕФЕКТОВ ТРАХЕИ | 2011 |
|
RU2484759C2 |
| СПОСОБ УШИВАНИЯ ГЛОТКИ | 2002 |
|
RU2229850C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2012 |
|
RU2487681C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2010 |
|
RU2438599C2 |

Изобретение относится к области медицины, а именно к оториноларингологии. Сущность способа состоит в том, что послойно закрывают зияющий дефект местными тканями в сочетании с арматурной пластиной из проницаемо-пористого никелида титана. При этом арматурную пластину предварительно внедряют между кожей и фасцией на участке шеи, смежном с зияющим дефектом. Ее выдерживают для вживления в течение 3-5 месяцев. После этого выделяют на ножке кожно-фасциальный лоскут с вживленной арматурной пластиной. Закрывают лоскутом предварительно освеженный зияющий дефект с ориентацией кожного слоя лоскута внутрь трахеи. Перед закрытием зияющего дефекта кожный слой выделенного лоскута деэпидермизируют на краях, контактирующих с краями зияющего дефекта. Использование данного изобретения позволяет закрыть дефект трахеи, сократить сроки интеграции имплантата и повысить состоятельность операции. 2 пр., 1 з.п. ф-лы, 4 ил.
1. Способ пластики зияющих дефектов трахеи, включающий послойное закрытие зияющего дефекта местными тканями в сочетании с арматурной пластиной из проницаемо-пористого никелида титана, отличающийся тем, что арматурную пластину предварительно внедряют между кожей и фасцией на участке шеи, смежном с зияющим дефектом, и выдерживают для вживления в течение 3-5 месяцев, выделяют на ножке кожно-фасциальный лоскут с вживленной арматурной пластиной и закрывают им предварительно освеженный зияющий дефект с ориентацией кожного слоя указанного лоскута внутрь трахеи.
2. Способ по п.1, отличающийся тем, что перед закрытием зияющего дефекта кожный слой выделенного кожно-фасциального лоскута деэпидермизируют на краях, контактирующих с краями зияющего дефекта.
| ШИНКАРЕВ С.А | |||
| и др | |||
| Клинический способ использования материала на основе пористого никелида титана в хирургическом лечении распространенного рака щитовидной железы | |||
| Материалы с памятью формы и новые технологии в медицине | |||
| / Под ред | |||
| В.Э.ГЮНТЕРА | |||
| - Томск: НИИ ММ, 2007, с.118 | |||
| СПОСОБ ЗАКРЫТИЯ ДЕФЕКТА ТРАХЕИ И УСТРОЙСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ ПЕРВОГО ЭТАПА СПОСОБА | 2002 |
|
RU2230529C2 |
| СПОСОБ ПЛАСТИКИ ДЕФЕКТА ПЕРЕДНЕЙ СТЕНКИ ТРАХЕИ | 2005 |
|
RU2295923C1 |
| СПОСОБ УСТРАНЕНИЯ ДЕФЕКТА СТЕНКИ ТРАХЕИ И ГОРТАНИ | 2005 |
|
RU2296520C1 |
Авторы
Даты
2012-06-20—Публикация
2010-12-03—Подача