Область техники
Настоящее изобретение относится к применению гидролизованных белков яиц для индуцирования оральной толерантности к интактным белкам яиц у млекопитающих, могущих иметь аллергию на яйца.
Предшествующий уровень техники
Пищевые аллергии, из которых наиболее часто встречающейся является аллергия к коровьему молоку, вызываются в большинстве случаев реакцией на содержащиеся в пище белки. В первые годы жизни иммунная система еще находится в состоянии развития и может быть не в состоянии распознавать и проявлять толерантность к таким пищевым белкам. Результатом оказывается то, что ребенок или детеныш животного относится к пищевому белку как чужеродному веществу и вырабатывает к нему аллергическую реакцию. Пищевые аллергии могут поражать не только людей, но также и других млекопитающих, таких как собаки и кошки.
Центральную роль в адаптивном иммунитете играют хелперные Т-клетки. Клетки Th1 являются жизненно важными для клеточно-опосредованных иммунных реакций, а клетки Th2 стимулируют гуморальный иммунитет. Ответы Th1 и Th2 являются противорегулирующими, то есть продуцируемые клетками Th1 цитокины ингибируют функцию Th2 и наоборот. Показано, что смещенный в сторону Th2 иммунный ответ является исключительно важным для обеспечения успешной беременности, а также он преобладает при родах и в первые месяцы жизни. Постнатальное воздействие микробных антигенов предпочтительно вызывает Th1-ответы, которые, как было предположено, уравновешивают Th2-ориентированное продуцирование цитокина у новорожденных. В случае недостаточного раннего микробного воздействия продуцирование цитокинов Th2-типа (IL-4, IL-5 и IL-13) продолжается далее, приводя к продуцированию IgE и вследствие этого к аллергическому заболеванию. Однако быстро выяснилось, что эта Th2-модель оказалась недостаточной для объяснения общей иммунопатологии аллергического заболевания, и недавно была высказана гипотеза о том, что начальные стадии аллергических заболеваний могут являться следствием ошибочной активации регулирующих Т-клеток (Treg), а не увеличенной активности Th2. Treg-клетки представляют собой небольшие группы Т-клеток, способные индуцировать иммунную толерантность. Описано несколько частично совпадающих подгрупп клеток Treg (Th3, Tr1, CD4+, CD25+), экспрессирующих супрессорные цитокины (IL-10, TGF-β).
Эффект оральной толерантности является возможностью, с помощью которой введение антигенов пероральным путем может предотвращать последующие системные иммунные ответы на тот же самый антиген, представленный в иммуногенной форме. Если механизм оральной толерантности не развивается достаточным образом или если имеются нарушения в физиологическом состоянии устойчивости к определенным антигенам, это может приводить к развитию реакций гиперчувствительности. Этот механизм может быть объяснен следующим образом: после первого контакта с аллергеном продуцируются антитела IgE, которые мигрируют к поверхности тучных клеток и базофилам, где они связываются со специфическими рецепторами. При повторном контакте с аллергеном поверхностные IgE оказываются перекрестно сшитыми на тучных клетках или базофилах, что приводит к активации клетки и высвобождению химических медиаторов, включая гистамин. Это явление ведет к патологическим эффектам, таким как местная или системная вазодилятация.
Обычно пищевая аллергия появляется только после того, как восприимчивый младенец, ребенок или детеныш животного впервые сталкивается с новой пищей. Первые пищевые белки, с которыми, как правило, сталкиваются человеческие младенцы, являются, по меньшей мере, белками коровьего молока и, как отмечено выше, аллергия на коровье молоко является наиболее часто встречающейся пищевой аллергией. Общепризнано, что младенцы с установившейся аллергией к коровьему молоку имеют увеличенный риск развития аллергий к другим пищевым белкам, таким как яичные и зерновые белки, но даже у младенцев с успешно развившейся оральной толерантностью к белкам коровьего молока впоследствии могут развиться аллергии к другим пищевым белкам, таким как яичные и зерновые белки, при их введении в рацион в ходе отлучения от груди.
С диетической точки зрения существуют два способа лечения развившейся аллергии: необходимо либо полностью избегать пищевых продуктов, содержащих аллерген, либо пищевые продукты нужно обрабатывать для снижения их аллергенного потенциала, например, подвергать гидролизу. Для этой последней цели производятся смеси для детского питания, содержащие сильно гидролизованные белки коровьего молока (пептиды, состоящие из не более чем пяти аминокислот).
Однако существует потребность в продуктах, которые помогают снижать риск развития аллергии и стимулируют развитие толерантности к интактным белкам, в особенности у детей, которые рассматриваются как подверженные такому риску (например, если у ребенка есть, по меньшей мере, один страдающий от аллергии член семьи). Например, для индукции у младенцев оральной толерантности к белкам коровьего молока было предложено кормление частично гидролизованными белками коровьего молока. Fritsche и др. (J. Allergy Clin. bnmunol, том 100, №2, страницы 266-273) с использованием экспериментальных моделей на животных показали, что ферментативные гидролизаты белков коровьего молока со степенью гидролиза 18% оказались способными индуцировать оральную толерантность к интактным белкам коровьего молока, тогда как гидролизаты со степенью гидролиза 28% такой способности не продемонстрировали. Результаты этих экспериментов показали, что профилактическое кормление крыс рецептурой с таким умеренно гидролизованным коровьим молоком, аллергенность которой была снижена более чем в 100 раз по сравнению со стандартной рецептурой, подавляло выделение из тучных клеток кишечника специфического IgE и медиатора, оба из которых являются факторами аллергической реакции немедленного типа. Эта работа продемонстрировала, что для белков коровьего молока возможно определение степени ферментативного гидролиза, при которой поддерживается способность пептидов индуцировать оральную толерантность и в то же время их аллергенность существенно снижается.
Были предложены и другие различные способы улучшения индукции оральной толерантности к белкам коровьего молока, включая введение пробиотиков, как предложено в WO 2003/099037, или введение соединения, способного увеличивать активность циклооксигеназы-2 (СОХ-2), как предложено в WO 02/051437. Однако индукции толерантности к другим часто вызывающим аллергические реакции пищевым белкам, таким как белки яиц, было уделено относительно небольшое внимание. На самом деле, с учетом того, что аллергия к белкам коровьего молока обычно исчезает самопроизвольно в возрасте от двух до пяти лет, тогда как аллергия к белкам яиц исчезает, как правило, медленнее и может даже сохраняться на протяжении всей жизни, необходимость в этом может быть даже более высокой. Поэтому целью настоящего изобретения является обеспечение способа индуцирования оральной толерантности к белкам яиц.
Краткое описание изобретения
Настоящее изобретение обеспечивает применение гидролизованных ферментативным способом белков яиц со степенью гидролиза от 15% до 28% в производстве композиции для индукции у млекопитающих оральной толерантности к белкам яиц.
Изобретение распространяется на способ индуцирования оральной толерантности к белкам яиц посредством предоставления нуждающемуся в этом млекопитающему композиции, содержащей терапевтическое количество гидролизованных белков яиц со степенью гидролиза от 15% до 28%.
Краткое описание чертежей
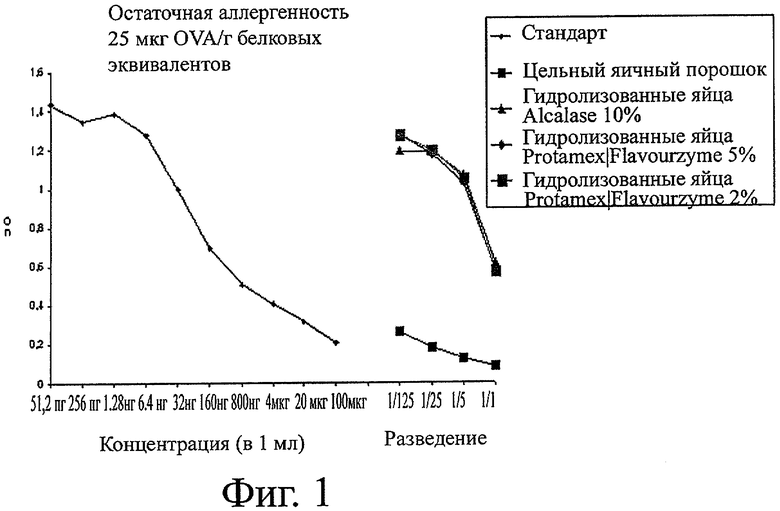
Фигура 1 показывает остаточную OVA-специфическую антигенность яичных гидролизатов.
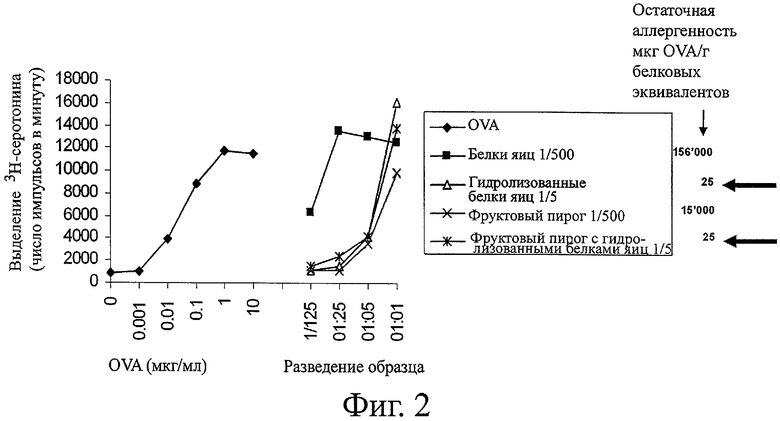
Фигура 2 показывает снижение аллергенности в функциональном исследовании стимуляции тучных клеток.
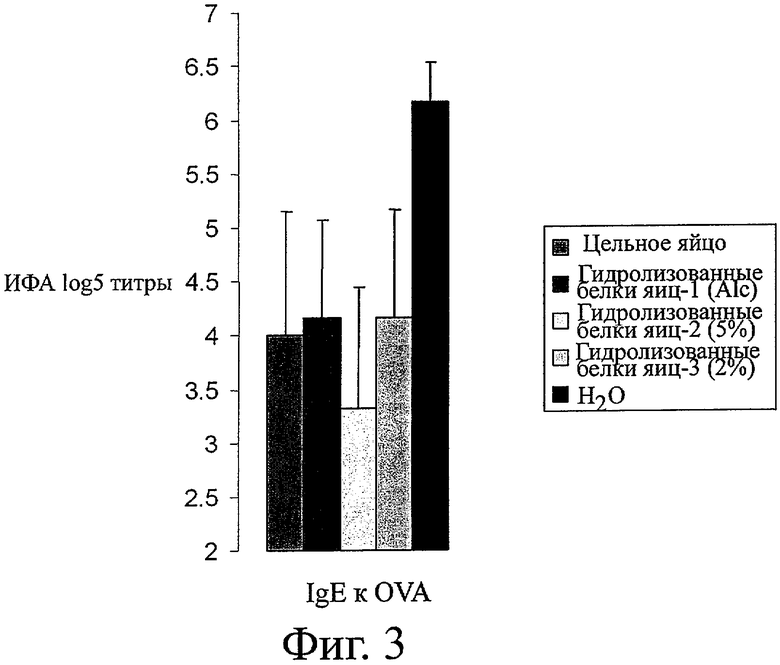
Фигура 3 показывает способность различных гидролизатов белка яиц подавлять ответ специфического к белкам яиц IgE.
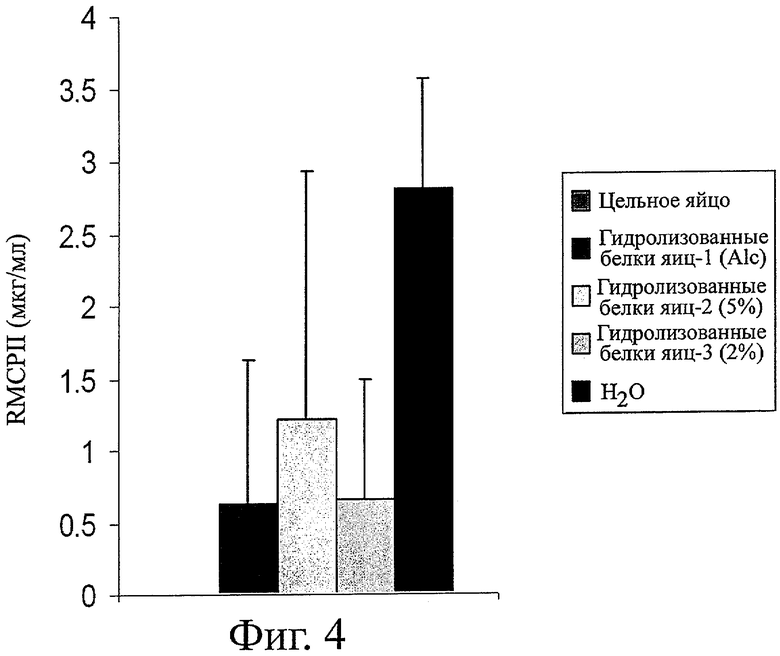
Фигура 4 показывает способность различных яичных гидролизатов подавлять стимуляцию тучных клеток кишечника.
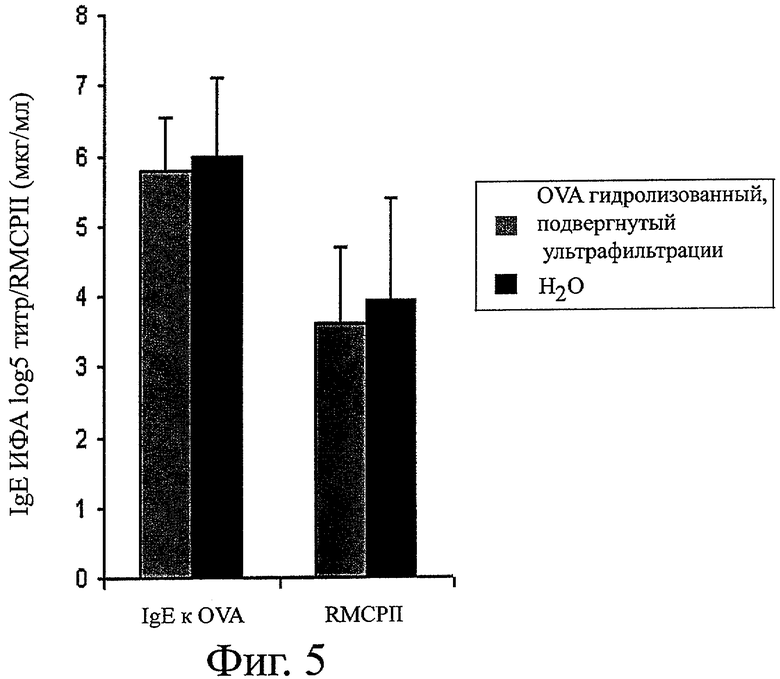
Фигура 5 демонстрирует, что сильно гидролизованные белки яиц являются неспособными подавлять ответ специфического к белкам яиц IgE или подавлять стимуляцию тучных клеток кишечника.
Подробное описание изобретения
В данном описании следующие термины имеют следующие значения.
«Степень гидролиза» или «DH» белка означает количество азота в несвязанных NH2-rpynnax, деленное на общее количество азота (NH- и NН2-группы), выраженное в процентах.
«Оральная толерантность» означает активное состояние иммунологической гипореактивности к антигенам, поступающим оральным путем.
Все указания на проценты, если не оговаривается иного, представлены массовыми процентными долями.
Предпочтительно степень гидролиза составляет от 18% до 25%, более предпочтительно от 23% до 25%.
Для успешной индукции оральной толерантности к интактным белкам яиц с использованием гидролизованных белков яиц требуется установление равновесия между остаточной антигенностью гидролизованных белков и их способностью индуцировать оральную толерантность. В целом остаточная антигенность гидролизованных белков должна быть, по меньшей мере, в 100 раз ниже, чем у интактных белков.
Согласно оценке с помощью методики, описанной Fritsché и др. (Int. Arch. Aller and Appi Imm., 93, 289-293, 1990), обнаруживается, что гидролизованные белки яиц со степенью гидролиза от 20% до 28% имеют аллергенность, сниженную по сравнению с интактными белками яиц, по меньшей мере, в 100 раз.
Белки яиц могут быть ферментативно гидролизованными с помощью любого подходящего, известного в данной области способа. Одним примером подходящего способа гидролизации является двухстадийный ферментативный гидролиз пастеризованной яичной массы из цельных яиц. Яичная масса в течение около 10 минут нагревается до температуры в диапазоне от 60 до 65°С, а затем охлаждается до около 55°С. Прибавляется протеаза, такая как субтилизин бактериальной сериновой эндопротеазы (например, предлагаемая в продаже под торговой маркой Alcalase®), и смесь выдерживается в течение, по меньшей мере, двух часов при температуре около 55°С для прохождения частичного гидролиза. Затем температура смеси поднимается до 70-75°С и поддерживается на этом уровне около 10 минут. Смесь опять охлаждается до около 55°С и добавляется следующая порция фермента. Смесь выдерживается при около 55°С в течение, по меньшей мере, еще двух часов для достижения требуемой степени гидролиза. Затем температура поднимается до величины от 85°С до 95°С и поддерживается на этом уровне в течение периода времени до 30 минут для инактивирования ферментов и прекращения гидролиза. Полученная гидролизованная яичная масса может по усмотрению использоваться либо в данном состоянии, либо она может быть подвергнута распылительной сушке для получения порошкообразного продукта.
Композиция, подходящая для применения в настоящем изобретении, может быть любым пищевым продуктом, в состав которого традиционно включаются цельные яйца, при этом цельные яйца заменяется гидролизованными яйцами, в которых белки яиц имеют степень гидролиза от 20% до 28%. Получаемый описанным выше способом гидролизованный яичный порошок, может, например, использоваться вместо цельного яичного порошка в таких рецептах, как десерты из запеченного английского крема, пироги с заварным кремом, крем-карамель. В качестве варианта гидролизованный яичный порошок может разводиться в воде и использоваться для приготовления таких блюд, как омлеты и яичница-болтунья. Гидролизованный яичный порошок является особенно подходящим ингредиентом для пищевых продуктов, предназначаемых для младенцев и маленьких детей, в частности, для пищевых продуктов, пригодных для использования на ранних стадиях отлучения ребенка от груди. Кроме того, гидролизованный яичный порошок может применяться вместо яичного порошка, традиционно используемого для приготовления таких продуктов.
Как отмечалось выше, аллергии к пищевым белкам не ограничиваются людьми, и способ настоящего изобретения может также применяться для индуцирования оральной толерантности к белкам яйца у других млекопитающих, в частности, у животных-компаньонов, таких как собаки и кошки. Так, гидролизованные белки яиц со степенью гидролиза от 15% до 28% могут также использоваться в качестве замены для цельных яиц в пищевых продуктах для животных-компаньонов, в частности, в пищевых продуктах, предназначенных, например, для недавно переставших получать грудное вскармливание щенков и котят.
Далее изобретение описывается на основании нижеследующих примеров.
Сведения, подтверяодающие возможность осуществления изобретения
Приготовление яичных гидролизатов
Исходным материалом являлась пастеризованная яичная масса из цельных яиц FT/OVO/0105 ABCD S.A., Avicole Bretonne Cecab Distribution (Ploermel, Франция).
Пример 1
30 кг яичной массы из цельных яиц нагревалось при 65°С в течение 10 минут при перемешивании со скоростью 250 об/мин. После охлаждения до 55°С было добавлено 2% ферментов Protamex® (партия PW2A1006, NOVOZYMES A/S Bagsvaerd, Дания) и смесь выдерживалась при 55°С в течение 2 часов. После этого первого этапа гидролиза было добавлено 1% ферментов Flavourzyme® 1000 L (партия 400904, NOVOZYMES A/S Bagsvaerd, Дания) и смесь нагревалась в течение 10 мин при 75°С. Затем смесь охлаждалась до 55°С, добавлялись следующие 1% ферментов Flavourzyme и смесь выдерживалась при 55°С в течение 2 часов. После этого второго этапа гидролиза смесь нагревалась в течение 30 минут при 90°С и затем высушивалась распылением для получения гидролизованного яичного порошка, который сохранялся в поддерживающем свежее состояние продукта фольгированном алюминием пакете.
Пример 2
35 кг яичной массы из цельных яиц нагревалось при 65°С в течение 10 минут при перемешивании со скоростью 250 об/мин. После охлаждения до 55°С было добавлено 5% ферментов Protamex® (партия PW2A1006, NOVOZYMES A/S Bagsvaerd, Дания) и смесь выдерживалась при 55°С в течение 2 часов. После этого первого этапа гидролиза было добавлено 1% фермента Flavourzyme® 1000 L (партия 400904, NOVOZYMES A/S Bagsvaerd, Дания) и смесь нагревалась в течение 10 мин при 75°С. Затем смесь охлаждалась до 55°С, после чего добавлялось еще 4% ферментов Flavourzyme и смесь выдерживалась при 55°С в течение 2 часов. После этого второго этапа гидролиза смесь нагревалась в течение 30 минут при 90°С и затем высушивалась распылением для получения гидролизованного яичного порошка, который сохранялся в поддерживающем свежее состояние продукта фольгированном алюминием пакете.
Пример 3
30 кг яичной массы из цельных яиц нагревалось при 65°С в течение 10 минут при перемешивании со скоростью 250 об/мин. После охлаждения до 55°С было добавлено 10% ферментов Alcalase®2.4L (партия 500357, NOVOZYMES A/S Bagsvaerd, Дания) и смесь выдерживалась при 55°С в течение 2 часов. После этого первого этапа гидролиза смесь нагревалась в течение 10 мин при 75°С. Затем смесь была охлаждена до 55°С, после чего было добавлено еще 10% ферментов Alcalase и смесь выдерживалась при 55°С в течение 2 часов. После этого второго этапа гидролиза смесь нагревалась в течение 30 минут при 90°С и затем высушивалась распылением для получения гидролизованного яичного порошка, который сохранялся в поддерживающем свежее состояние продукта фольгированном алюминием пакете.
Продукты, содержащие гидролизованное цельные яйца
Пример 4
Пример ингредиентов для сладкого яичного пудинга, содержащего гидролизованные яйца, состоит в следующем:
Такой пудинг может быть приготовлен любым известным в данной области подходящим способом.
Пример 5
Пример ингредиентов для пикантного яичного пудинга, содержащего гидролизованные яйца, состоит в следующем:
Такой пудинг может быть приготовлен любым известным в данной области подходящим способом.
Пример 6
Пример ингредиентов для яичных макаронных изделий, содержащих гидролизованные яйца, состоит в следующем:
Такие макаронные изделия могут быть приготовлены любым известным в данной области подходящим способом.
Остаточная антигенность яичных гидролизатов
Остаточная антигенность альбумина яичного белка (OVA) в гидролизатах примеров 1, 2 и 3 определялась ингибированием с поликлональной кроличьей антисывороткой с антителами к белку OVA с помощью иммуноферментного анализа (ИФА, ELISA). В лунки планшет для микротитрования добавлялись 100 мкл раствора OVA с концентрацией 50 мкг/мл в карбонатно-бикарбонатном буфере и выдерживались 24 часа при 4°С. Планшеты четырежды промывались PBS-Tween-буфере и их свободные участки блокировались добавлением в каждую такую лунку по 200 мкл рыбного желатина (0,5% в PBS-Tween). Планшеты выдерживались 1 час при комнатной температуре (RT) и снова 4 раза промывались в PBS-Tween.
В отдельных пробирках в течение 1 часа при комнатной температуре инкубировались 1 часть стандартного препарата OVA или образца для испытаний с 1 частью кроличьих антител к белку OVA (разведение 1:20000). После инкубации 100 мкл этой ингибирующей смеси прибавлялось к вышеупомянутым покрытым и блокированным лункам и выдерживалось в течение 2 часов при комнатной температуре. Планшеты четырежды промывались в PBS-Tween. Затем прибавлялся козий антикроличий меченый пероксидазой конъюгат (0,1 мл раствора с разведением 1:2000), планшеты выдерживались в течение 1 часа при комнатной температуре и промывались 4 раза в PBS-Tween. Добавлялся хромогенный субстрат (0,1 мл о-фенилендиамина). После инкубации в течение 15 минут с помощью многоканального ИФА-спектрофотометра определялась оптическая плотность при 492 нм.
Результаты представлены на фигуре 1, из которой видно, что OVA-специфическая антигенность гидролизатов из примеров 1-3 по сравнению с интактным белком яиц была снижена более чем в 10000 раз.
Остаточная аллергенность яичных гидролизатов
Для определения IgE-зависимой аллергенности антигенной молекулы (OVA) было проведено in vitro функциональное исследование выделения меченого тритием серотонина из сенсибилизированных тучных клеток крысы согласно ранее описанному в литературе (Fritsche и др. J. Allergy Clin. Immunol, №2, том 100, стр.266-273). Вкратце, тучные клетки были получены от нормальных крыс линии Спраг-Доули перитонеальными промывками в модифицированной Дульбекко среде Игла, содержащей 10% эмбриональную телячью сыворотку. Клетки промывались в этой среде и выдерживались в течение ночи при 4°С. После двух промывок в фосфатно-НЕРЕ8-рыбно-желатиновом буфере (PHG) с рН 7,0 клетки повторно суспендировались в том же самом буфере в концентрации 5×105 клеток в 1 мл и разбавлялись одним объемом богатой IgE-антителами к OVA крысиной сыворотки, содержащей 5 мкКи/мл 3H-серотонина. После инкубации в течение 2 часов при 37°С клетки далее трижды промывались в PHG и повторно суспендировались в PHG при концентрации 2,5×105 клеток в 1 мл. Сенсибилизированные тучные клетки распределялись по планшетам для микротитрования (по 0,1 мл в каждой лунке) и смешивались с 0,05 мл последовательных разведении гидролизованных белков яиц, полученных согласно примеру 2 (1/10 начиная от 10 мг/мл). Смесь выдерживалась 60 минут при 37°С и центрифугировалась. Аликвота (0,05 мл) супернатанта смешивалась с 2 мл сцинтилляционной жидкости и с помощью счетчика β-излучения фирмы Packard измерялось испускание 3Н.
Результаты показаны на фигуре 2, из которой видно, что гидролизованные яйца имели сильно сниженную аллергенность (25 мкг OVA/г белковых эквивалентов) и что эта низкая величина сохранялась при включении гидролизованных яиц в десерт типа пирога с фруктами.
Индукция оральной толерантности к белкам яиц посредством кормления гидролизатом белка яиц
Была исследована in vivo способность к индуцированною оральной толерантности к яичным продуктам с использованием крыс в качестве модельных объектов. Шести группам крыс линии Спраг-Доули (по 6 животных в группе), содержащихся на не содержащей белков яиц диете, в течение с 1 по 19 день эксперимента давались ad libitum различные экспериментальные жидкие яичные белки/яичные гидролизаты или вода (контроль), помещаемые в их поилки, и твердая диета в виде не содержащих белка яиц гранул. Животным давались следующие продукты:
Группа А: цельный яичный порошок (20 г/л);
Группа В: гидролизованный яичный порошок из примера 3 (120 г/л), DH 25%;
Группа С: гидролизованный яичный порошок из примера 2 (120 г/л), DH 23%;
Группа D: гидролизованный яичный порошок из примера 1 (120 г/л), DH 20%;
Группа Е: подвергнутый ультрафильтрации гидролизованный яичный порошок из примера 3(120 г/л), DH 31%;.
Группа F: H2O (контроль).
Даваемый группе Е подвергнутый ультрафильтрации гидролизованный яичный порошок был получен следующим образом. Субстрат полученной в примере 3 гидролизованной яичной массы был подвергнут микрофильтрации с помощью фильтрационного модуля Sefiltec FBF 0102 с мешочный фильтром на 100 мкм (PGF 51 Е 02). После этого этапа микрофильтрации фильтрат подвергался ультрафильтрации с помошью самостоятельно изготовленного ультрафильтрационного модуля с мембранами на 4000 Дальтон (ES404, PES, 4000 MWCO производства PCI Membrane Systems). Затем фильтрат был подвергнут сублимационной сушке.
Общий азот в гидролизатах определялся по методике Дюма (способ Карло Эрба). Степень гидролиза измерялась способом TNBS согласно AdIer-Nissen (J. Agric. Food. Chem. 1979 27: 1256-1262).
Все крысы иммунизировались в 5 день эксперимента подкожной инъекцией 0,1 мг яичного альбумина +0,2 мл 3% Аl(ОН)3. В 19 день все животные были умерщвлены. Кровь выпускалась и сыворотка анализировалась на специфические IgE-антитела (антиовальбумин) ранее описанным в литературе (Fritsche R, Bonzon M. hit Arch Allergy Appi Immunol 1990; 93: 289-93) методом ИФА. Вкратце, планшеты микротитратора покрывались OVA в течение 24 часов при 4°С. Планшеты промывались PBS Tween 20 и в течение 1 часа блокировались рыбным желатином. После добавления последовательных разведении исследуемой сыворотки (1/2) и инкубации в течение 2 часов прибавлялась овечья антисыворотка к IgE крысы. После инкубации 1 час при комнатной температуре добавлялось второе меченое пероксидазой антитело, вслед за которым через 1 час прибавлялся субстрат (о-фенилендиамин). Оптическую плотность при 492 нм разбавленного 1:5 пула нормальной крысиной сыворотки рассматривали как неспецифический фон. Концентрации специфических антител выражались как максимальные разбавления исследуемой сыворотки, превышающие эту величину.
Протеаза тучных клеток крысы (RMCPII) выделяется в кровь после IgE-опосредованной стимуляции тучных клеток кишечника. Пероральный стимул, приводящий к выделению RMCPII, является критерием IgE-сенсибилизации или толеризации на уровне тучной клетки кишечника. Уровни RMCPII определялись с помощью коммерчески доступного комплекта для ИФА (Moredun Animal Health Ltd., Эдинбург, Шотландия), основывающегося на принципе сэндвич-анализа, при котором выполняется покрытие планшеты моноклональным антителом к RMCPII, вслед за чем добавляется исследуемая сыворотка и второе овечье поликлональное антитело к RMCPII, конъюгированное с пероксидазой хрена.
Результаты представлены на фигурах 3, 4 и 5. Из фигуры 3 видно, что гидролизаты белка яиц из примеров 1-3 способны подавлять ответ специфического к белкам яиц IgE при кормлении ими животных в течение 19 дней ad libitum по сравнению с нетолеризованной контрольной Группой F), в которой индуцировались высокие уровни антител IgE против белков яиц. Более точно, уровни антител IgE к OVA (выраженные в виде логарифма титра антител) были следующими: Группа А: 4+/-1,1; Группа В: 4,1+/-0,9; Группа С: 3,3+/-1,1; Группа D: 4,1+/-2,0; Группа F: 6,1+/-0,3. При сравнении групп видно значительное отличие (р<0,05) групп А-D от группы F (контроль).
Фигура 4 показывает также, что стимуляция тучных клеток кишечника оказывается подавленной в Группах А, В, С и D, но не в Группе F (контроль). Показатели величин RMCPII, выраженные в мкг/мл, являются следующими: Группа А: 0+/0,0; Группа В: 0,6+/-1,0; Группа С: 1,2+/-1,7; Группа D: 0,6+/-0,8; Группа F: 2,8+/-0,7. При сравнении групп видно значительное отличие (р<0,05) групп А-D от группы F (контроль).
Фигура 5 показывает, что скармливаемые Группе Е сильно гидролизованные белки яиц не индуцировали оральной толерантности к OVA, что оценивалось по супрессии ответа специфического к белкам яиц IgE или по подавлению стимуляции тучных клеток кишечника.
Уровни RMCPII и антител IgE к OVA не отличаются от величин, полученных для контрольной группы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИДРОЛИЗОВАННЫЕ ЯИЧНЫЕ БЕЛКИ | 2007 |
|
RU2460310C2 |
| СТИМУЛИРОВАНИЕ ПЕРОРАЛЬНОЙ ТОЛЕРАНТНОСТИ ГЛИКОЗИЛИРОВАННЫМИ БЕЛКАМИ | 2006 |
|
RU2440129C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ШТАММЫ BIFIDOBACTERIUM LONGUM И ОСЛАБЛЯЮЩАЯ СИПТОМЫ ПИЩЕВОЙ АЛЛЕРГИИ, ОСОБЕННО У МЛАДЕНЦЕВ И ДЕТЕЙ | 2010 |
|
RU2539514C2 |
| ПРЕДОТВРАЩЕНИЕ АЛЛЕРГИИ ПРИ ОТЛУЧЕНИИ РЕБЕНКА ОТ ГРУДИ | 2008 |
|
RU2489888C2 |
| ПИЩЕВОЙ БУТИРАТ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ АЛЛЕРГИЧЕСКОГО РАССТРОЙСТВА | 2019 |
|
RU2809650C2 |
| ПРИМЕНЕНИЕ LGG ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ АЛЛЕРГИЙ | 2006 |
|
RU2435598C2 |
| СПОСОБЫ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ АЛЛЕРГИИ | 1996 |
|
RU2174012C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЯБЛОЧНЫЙ ЭКСТРАКТ И СНИЖАЮЩАЯ СИМПТОМЫ ПИЩЕВОЙ АЛЛЕРГИИ, ОСОБЕННО У ДЕТЕЙ | 2010 |
|
RU2536916C2 |
| ВНОВЬ ИДЕНТИФИЦИРОВАННЫЕ ПЕПТИДЫ ДЛЯ ПРИМЕНЕНИЯ ПРИ ИНДУКЦИИ ТОЛЕРАНТНОСТИ ПРИ ПЕРОРАЛЬНОМ ВВЕДЕНИИ У МОЛОДЫХ МЛЕКОПИТАЮЩИХ | 2013 |
|
RU2668155C1 |
| ИНДУЦИРОВАНИЕ ТОЛЕРАНТНОСТИ | 2001 |
|
RU2283665C2 |
Изобретение относится к пищевой промышленности и может быть использовано для предотвращения пищевой аллергии. Гидролизованные ферментативным способом белки яиц со степенью гидролиза от 15% до 28% применяют при производстве пищевых композиций. Изобретение обеспечивает толерантность к яичному белку в пищевых продуктах у млекопитающих. 4 з.п. ф-лы, 5 ил., 6 пр.
1. Применение гидролизованных ферментативным способом белков яиц со степенью гидролиза от 15% до 28% в производстве композиции для индукции у млекопитающих оральной толерантности к белкам яиц.
2. Применение по п.1, в котором млекопитающее является человеком.
3. Применение по п.2, в котором композиция является пищевым продуктом для отлучаемых от груди детей.
4. Применение по п.1, в котором млекопитающее является домашним животным, таким как кошка или собака.
5. Применение по любому из предшествующих пунктов, при котором степень гидролиза составляет от 23% до 25%.
| US 20020037357 A1, 28.03.2002 | |||
| СПОСОБЫ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ АЛЛЕРГИИ | 1996 |
|
RU2174012C2 |
| Гидрораспределитель механизированной крепи | 1975 |
|
SU629350A1 |
Авторы
Даты
2012-03-27—Публикация
2007-06-14—Подача