Область техники
Настоящее изобретение относится к области микробиологии, в частности к применению пробиотиков, особенно штаммов Bifidobacterium longum, в производстве питательной композиции, предназначенной для ослабления симптомов аллергии у аллергических пациентов, когда они подвергаются воздействию аллергенов.
Уровень техники
Аллергии принадлежат к наиболее часто встречающимся проблемам со здоровьем, воздействующим на жизнь пациентов любого возраста. Аллергические заболевания в настоящее время признаны Всемирной организацией здравоохранения (WHO, ВОЗ) в качестве эпидемии. Показано, что распространенность аллергий за прошедшие десятилетия возросла. Современный образ жизни, особенно в городах, ассоциируется с высокой распространенностью и более значительной серьезностью аллергических проявлений.
Показано, что аллергическая сенсибилизация в детстве, особенно в раннем детстве и особенно к аллергенам пищевых продуктов, является критически важной и вызывает самый пристальный интерес с точки зрения развития «аллергического фенотипа», или «атопии», способствующей последующей сенсибилизации и к другим аллергенам. Следовательно, аллергии в детстве могут явиться первоначальным этапом аллергического каскада, приводящего к множественным аллергиям в более старшем возрасте - процессу, который обычно именуется «атопическим маршем». Например, в человеческих популяциях было продемонстрировано, что у детей с устойчивой пищевой аллергией на ранних сроках жизни имеется резко увеличенный риск развития аллергического ринита (поллиноз) или астмы в более позднем детском возрасте (Ostblom и др. 2008). Дети с более умеренными формами пищевой аллергии также подвержены увеличенному риску развития респираторной аллергии, но в меньшей степени, чем дети с устойчивой пищевой аллергией. Поэтому ослабление тяжести пищевой аллергии может оказать критически важное значение в сдерживании «аллергического марша».
В этом контексте контроль аллергических приступов и профилактика аллергий в детстве и младенчестве имеют самую высокую значимость.
Иммунная система младенцев активно развивается на протяжении всех первых нескольких лет жизни. Посредством предупреждения, профилактики, контроля, ослабления или модуляции аллергических реакций у таких молодых пациентов оказывается возможным влиять не только на их краткосрочный аллергический профиль, но также и на более отдаленный в более старшем возрасте.
Профилактика аллергий может обеспечиваться на различных уровнях.
«Первичная профилактика» является действиями по предупреждению или ослаблению риска сенсибилизации к аллергенам пациентов, отличающихся отсутствием или сниженными уровнями аллерген-специфических антител IgE. Профилактика или ослабление сенсибилизации ведут к отсутствию или ослаблению аллергических симптомов при подвергании воздействию того же самого аллергена. Модулированием пути, посредством которого пациент становится чувствительным в отношении одного аллергена или одной группы аллергенов (первичная профилактика), также может быть обеспечено модулирование и последующей аллергической реакции.
«Вторичная профилактика» является действиями по модулированию аллергических симптомов, то есть проявлений или интенсивности аллергической реакции у пациента, уже ставшего чувствительным к одному или нескольким аллергенам, когда пациент повторно подвергается воздействию указанного аллергена(-ов). Модулированием проявлений или интенсивности аллергических симптомов (вторичная профилактика), минимизируются ассоциируемые с аллергиями неудобства.
Принимая во внимание эти различные концепции предупреждения аллергии, можно предположить, что, основываясь на присущих им механизмам действия, некоторые соединения могли бы воздействовать только на один или на оба этих определенных уровня профилактики. Некоторые могут, например, только ослаблять сенсибилизацию к конкретному аллергену (первичная профилактика), в то время как другие соединения могут оказывать эффект только на вторичную профилактику и снижать тяжесть аллергических реакций. Другие соединения могут быть способны влиять и на сенсибилизацию, и на симптомы, и, таким образом, являться эффективными в осуществлении первичной и вторичной профилактики.
Пищевые аллергены относятся к первым аллергенам, с которыми младенцы сталкиваются на самых ранних этапах их жизни: для младенцев, не получающих исключительно грудное вскармливание, достаточно типичной является встреча с белками коровьего молока. Молочные белки фактически относятся к числу наиболее часто наблюдаемых причин пищевой аллергии в младенчестве, за которыми следуют белки яиц и пшеничные белки. В целом, пищевые аллергии у младенцев и маленьких детей могут иметь кожные проявления (высыпания, экзема, другие) и желудочно-кишечные симптомы (колики в животе, боли, особенно в брюшной полости, рвота). Дальнейшая сенсибилизация и аллергические приступы могут также появиться, когда младенец/маленький ребенок испытывает воздействие нового пищевого продукта, такого как злаки, овощи, фрукты, орехи или рыба.
Штаммы Bifidobacterium longum (B.longum) были описаны как играющие важную роль в кишечной микробиоте и ассоциируемые с положительными эффектами на состояние здоровья. Их присутствие в больших количествах в кишечной микробиоте является типичным для здоровых вскармливаемых грудью детей. Они могут содействовать эффективному перевариванию, усиливать иммунную систему и продуцировать молочную и уксусную кислоту, которые регулируют уровень pH в кишечнике. Эти бактерии могут также ингибировать рост Candida albicans, Е.coli и других обладающих патогенными свойствами бактерий. В. longum в целом или отдельные штаммы B.longum могут быть согласно определению ВОЗ отнесены к пробиотикам.
Имеют указания на то, определенные штаммы B.longum до некоторой степени обладают антиаллергенным действием. Например, пациенты, страдающие от аллергического ринита вследствие поллиноза на японский кедр, показали снижение аллергических симптомов после употребления B.longum ВВ536 в течение нескольких недель до и во время сезона пыльцы (Xiao JZ, Kondo S, Yanagisawa N, Takahashi N, Odamaki T, Iwabuchi N, Miyaji K, Iwatsuki K, Togashi H, Enomoto K, Enomoto T. Probiotics in the treatment of Japanese cedar pollinosis: a double-blind placebo-controlled trial («Пробиотики в терапии поллиноза на японский кедр: двойное слепое плацебо-контролируемое испытание»). Clin Exp Allergy. 2006 Nov; 36(11): 1425-35. Xiao JZ, Kondo S, Yanagisawa N, Takahashi N, Odamaki T, Iwabuchi N, Iwatsuki K, Kokubo S, Togashi H, Enomoto K, Enomoto T. Effect of probiotic Bifidobacterium longum BB536 [corrected] in relieving clinical symptoms and modulating plasma cytokine levels of Japanese cedar pollinosis during the pollen season. A randomized double-blind, placebo-controlled trial («Действие пробиотика Bifidobacterium longum BB536 в смягчении клинических симптомов и модулировании плазменных уровней цитокинов при поллинозе на японский кедр во время сезона пыльцы. Рандомизированное двойное слепое плацебо-контролируемое испытание»). J Investig Allergol Clin Immunol. 2006; 16(2):86-93.)
Помимо этого было описано действие на иммунную систему аллергиков различных культур пробиотиков или смесей пробиотиков, например, EP 1858336 (WO 2006697949), описывает смесь пробиотиков, которая способна снизить риск развития аллергий на пшеничный альбумин муки и глобулины. JP 2006028050 описывает супрессивные свойства по отношению к кожной аллергии композиций, содержащих такие пробиотические бактерии, как Lactobacillus и Streptococcus. В публикации WO 2009072889 (Jan knoll и др.) описываются Bifidobacterium, которые могу применяться для улучшения легочной функции у субъектов, страдающих от аллергии на пылевого клеща. В JP 10309178 указывается, как выделенные у человека Bifidobacterium могут содействовать излечению пищевой аллергии или стимулированию пероральной иммунной толерантности.
Тем не менее все еще сохраняется необходимость в том, чтобы иметь возможность определенным образом ослаблять аллергические реакции и симптомы в популяциях маленьких детей и младенцев. Это является особенно важным в отношении созревания как кишечной, так и иммунной систем у маленьких детях, с учетом того множества новых аллергенов, действию которых подвергаются маленькие дети, особенно в период отлучения ребенка от груди.
Проблема аллергических реакций пищевого происхождения в молодом возрасте еще больше осложняется особыми пищевыми потребностями младенцев и маленьких детей. Потребление калорий, плотность калорий, многообразие желательных питательных веществ, содержание белка и качество белка - все эти факторы относятся к числу играющих важную роль в обеспечении наиболее подходящего для младенцев и маленьких детей питания. Также важно наличие питательных микроэлементов, таких как витамины и минеральные вещества, особенно когда их концентрация ограничивается определенными рекомендованными диапазонами, соответствующими возрасту целевых пациентов. В этой связи матрицы, обеспечивающие доставку пищевого продукта маленьким детям и младенцам, по своей природе являются сложными, но при этом их разнообразие невелико: например, младенцам, даже потенциально склонным к аллергиям, обычно требуется определенный белковый баланс в матрице белков, получаемых из молока. Наличие таких многочисленных питательных веществ может потенцировать действие пищевых аллергенов. В таких сложных матрицах слабые пищевые аллергены, сами по себе неспособные вызвать аллергические проявления, затем могут стать более мощными в инициировании аллергической реакции. Аналогичным образом можно наблюдать снижение или исчезновение действия в таких сложных пищевых матрицах соединений, способных нейтрализовать аллергены или проявляющих профилактический по отношению к аллергии эффект. В частности, нельзя предсказать будут ли соединения, обычно признаваемые в качестве обладающих профилактическим действием против аллергии, сохранять такую активность и в какой степени, в таких сложных матрицах, как питательные композиции для младенцев или маленьких детей.
Имеется необходимость в ослаблении симптомов пищевых аллергий в группах младенцев и маленьких детей, которые имеют в анамнезе аллергические эпизоды и/или являются аллергиками.
Существует потребность в полноценной питательной композиции, которая не только обеспечивала бы поставку различных питательных веществ, но также снижала бы тяжесть аллергических реакций.
Имеется необходимость в обеспечении питательной композиции, модулирующей аллергические реакции у молодых пациентов, страдающих аллергиями от легкой до умеренной степени тяжести, поскольку такие пациенты имеют особые потребности, продиктованные неполной зрелостью их кишечной и иммунной систем.
Существует также потребность в том, чтобы модулировать аллергические реакции у маленьких детей, которые не обладают переносимостью к сильнодействующим фармацевтическим препаратам, например, с помощью пищевого вмешательства, такого как включение в режим питания на регулярной основе иммуномодуляторов.
Имеется потребность в обеспечении питательной композиции, модулирующей аллергическую реакцию у молодых пациентов в ходе и в ближайшее время после отлучения ребенка от груди, когда его кишечник подвергается существенным преобразованиям и когда происходит поступление новых твердых пищевых продуктов, потенциально содержащих новые аллергенные белки, и, следовательно, пациент оказывается особенно уязвимым в отношении сенсибилизации к пищевым аллергенам.
Имеется необходимость в облегчении аллергических симптомов посредством предоставления эффективной композиции, возможно, при уменьшении подверженности воздействию интактных аллергенов, даже притом, что такая композиция может не снижать сенсибилизацию к аллергенам непосредственно.
Существует необходимость в композиции, которая оказывала бы положительное воздействие при вторичной профилактике аллергии, не обязательно проявляя эффект воздействия на те же самые аллергии при первичной профилактике.
Наконец, существует необходимость в композиции, в наибольшей степени подходящей для молодых пациентов, которая посредством ослабления симптомов могла бы содействовать минимизации «аллергического фенотипа» и, таким образом, могла бы снизить сенсибилизацию к новым аллергенам в более старшем возрасте. Имеется необходимость в сдерживании атопического марша.
Сущность изобретения
В первом объекте настоящее изобретение обеспечивает полноценную питательную композицию, предназначенную для ослабления симптомов аллергий, инициируемых пищевыми продуктами у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами, особенно у молодых пациентов, маленьких детей и младенцев.
Во втором объекте настоящее изобретение обеспечивает композицию, которая значительно содействует вторичной профилактике аллергических реакций, вызываемых пищевыми аллергенами, возможно не оказывая воздействия на первичную профилактику против тех же самых аллергенов.
В третьем объекте настоящее изобретение обеспечивает композицию, которая содержит пробиотики, в частности, принадлежащие к роду Bifidobacterium.
В еще одном объекте изобретения композиция изобретения является особенно эффективной для младенцев/маленьких детей в период отлучения ребенка от груди.
Данное изобретение, кроме того, распространяется на снижение сенсибилизации к другим аллергенам в более старшем возрасте.
Краткое описание чертежей
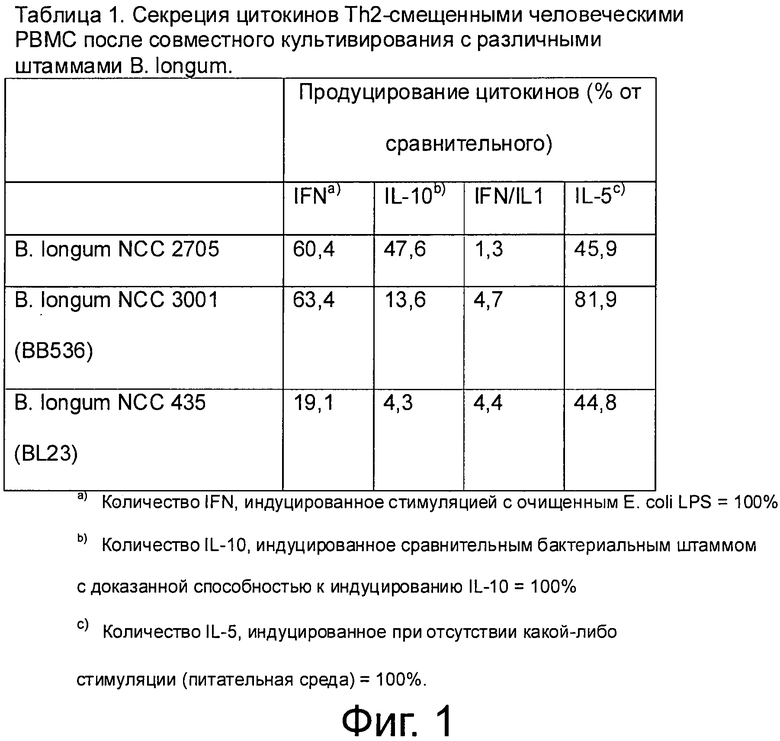
Фигура 1/Таблица 1. Цитокиновый профиль Th2-смещенных мононуклеаров периферической крови (РВМС) человека после совместного культивирования с B.longum NCC 2705, зарегистрированного Nestec SA как CNCM-I2618, или с другими штаммами.
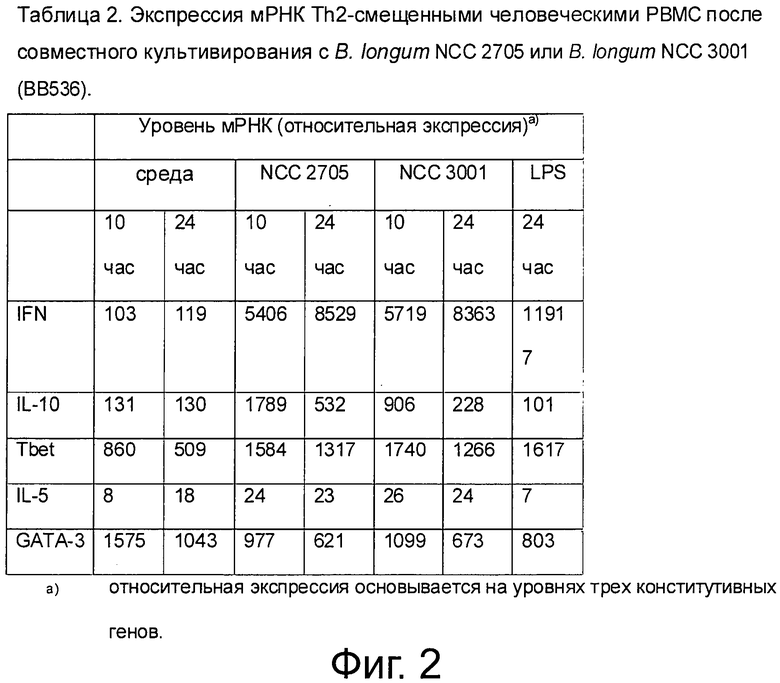
Фигура 2/Таблица 2. Профиль мРНК Th2-смещенных мононуклеаров периферической крови человека после совместного культивирования с B.longum или с другими штаммами.
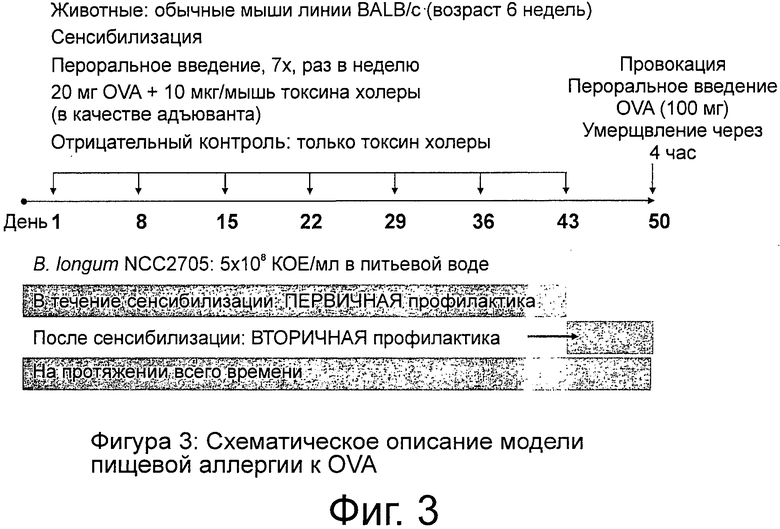
Фигура 3. Схематическое описание пищевой аллергии к альбумину яичного белка (OVA) в модели на мышах.
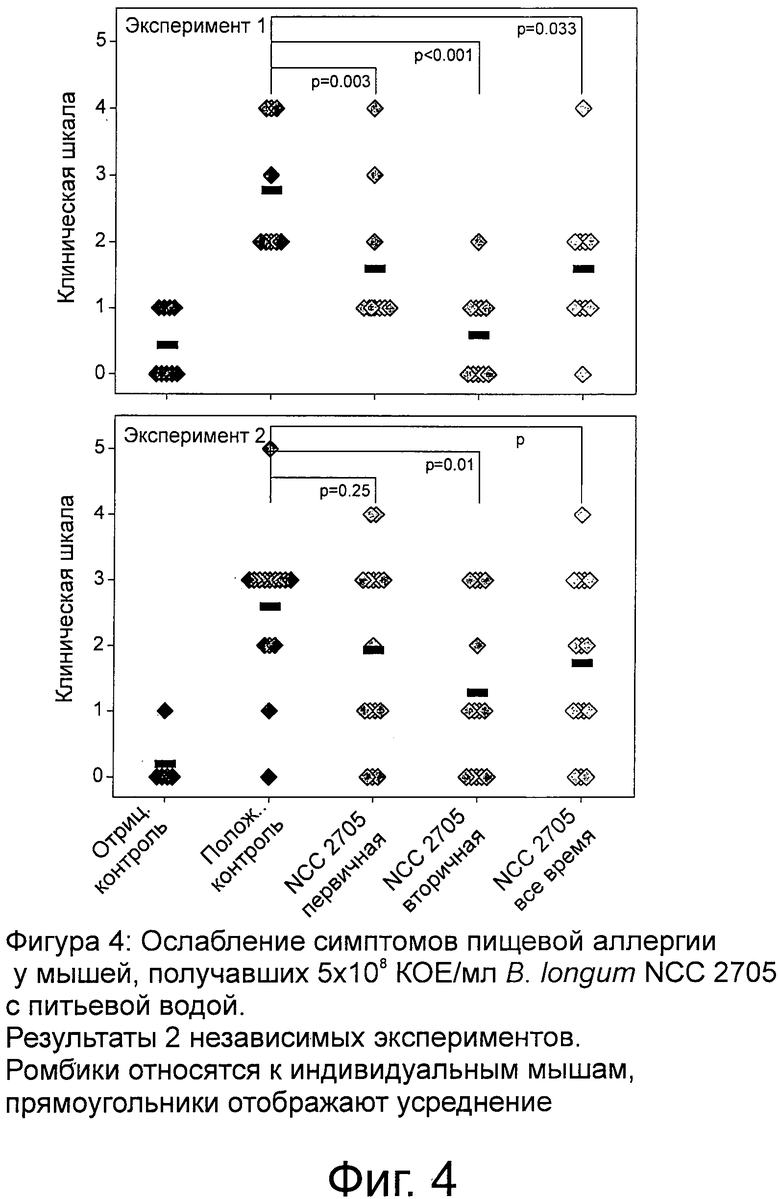
Фигура 4. Представление выражаемого в баллах клинического показателя, демонстрирующего ослабление симптомов пищевой аллергии у мышей, получавших 5×108 КОЕ/мл B.longum NCC 2705 с питьевой водой.
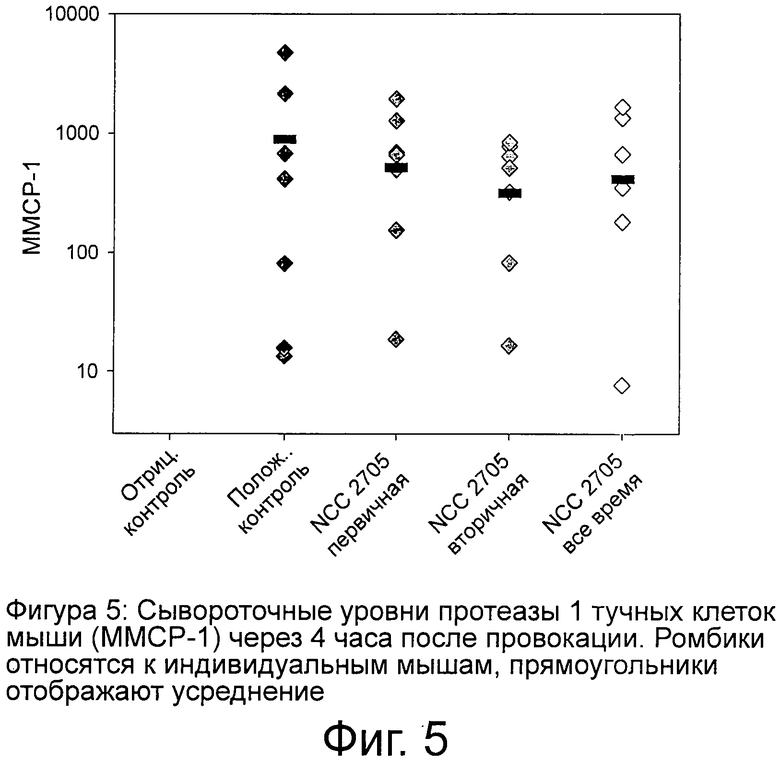
Фигура 5. Сывороточные уровни протеазы 1 тучных клеток мыши (ММСР-1).
Фигура 6/Таблица 3. Выработка цитокинов брыжеечными лимфоцитами LN и спленоцитами, повторно стимулируемыми ex vivo.
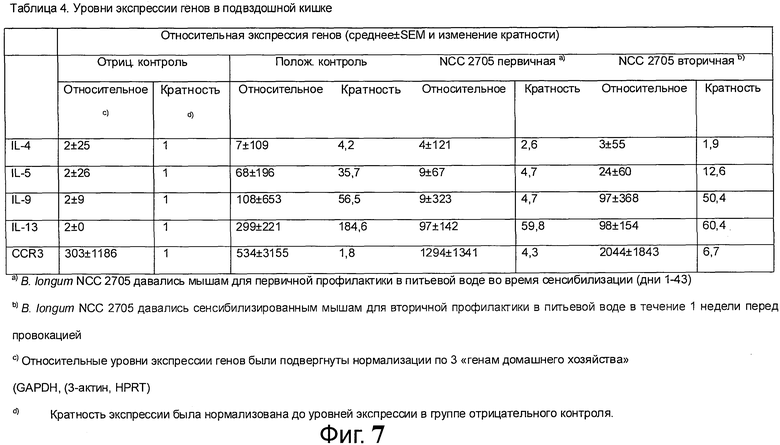
Фигура 7/Таблица 4. Уровни экспрессии генов в подвздошной кишке
Раскрытие изобретения
Определения.
В данном описании следующие термины имеют следующие значения
«Полноценная питательная композиция». Для целей данного документа полноценной питательной композицией является композиция, которая содержит значительное количество, обычно 20% или более, основных пищевых питательных веществ, рекомендованных для данного возраста. Такие основные питательные вещества обычно обеспечиваются в таких количествах и соотношениях, чтобы соответствовать 20% или более рекомендованной для данного возраста дозировки конкретного питательного вещества при использовании в количестве, адекватном для обеспечения рекомендованного для данного возраста потребления калорий. Полноценная питательная композиция обычно содержит источник белков, источник липидов, источник углеводов в сбалансированной пропорции, которая отвечает общей рекомендации для данного возраста. Обычно она также включает питательные микроэлементы, такие как витамины и минеральные вещества, а также источник незаменимых аминокислот и источник незаменимых жирных кислот. Однако понимается, что полноценная питательная композиция может не содержать ни всех конкретных питательные веществ, ни всех рекомендованных количеств, удовлетворяющих всем пищевым потребностям младенца или маленького ребенка. Полноценная питательная композиция исключает композиции, содержащие только Bifidobacterium, или те, в которых Bifidobacterium находятся в преобладающей доле содержания.
«Симптомы аллергий» в основном включают симптомы, вызываемые аллергенами. Такие симптомы включают кожные (покраснение кожи, высыпания, зуд, дерматит, экзема), глазные (зуд и слезотечение), желудочно-кишечные (конгестия, боли в животе, судороги, рвота, диарея), респираторные (зуд в носу, заложенность носа, ринит, астма) и в тяжелых случаях системные (головокружение, спутанность сознания, анафилаксия) проявления.
«Первичная профилактика аллергий» означает все меры, направленные на предотвращение или ослабление аллергической (иммунологической) сенсибилизации, например профилактика или снижение уровней специфических IgE-антител.
«Вторичная профилактика аллергий» означает профилактику или ослабление развития аллергических заболеваний/аллергических симптомов у сенсибилизированных индивидуумов.
«Период отлучения от груди» является периодом, в течение которого младенцы адаптируются от питания чистой жидкостью к твердой или полутвердой пище и приспосабливаются к переходу от пищи квази-индивидуального типа (обычно материнского молока или смеси для питания младенцев) к разнообразию пищевых продуктов.
«Сенсибилизация» означает индукцию/развитие аллерген-специфических IgE-антител.
«Пробиотик» обозначает препарат микробиологических клеток или компоненты микробиологических клеток, обладающие благотворным воздействием на состояние здоровья или самочувствие организма-хозяина (C Salminen, Ouwehand A. Benno Y. и др. "Probiotics: how should they be defined" («Пробиотики: как их следует определять») Trends Food Sci. Technol. 1999:10 107-10). Такое определение пробиотиков является широко принятым и находится в соответствии с определением ВОЗ. Пробиотик может содержать единственный штамм микроорганизма, смесь различных штаммов и/или смесь бактерий различных видов и родов. Тем не менее и в случае смесей может использоваться термин в форме единственного числа «пробиотик», применяемый для обозначения пробиотической смеси или препарата. Для целей настоящего изобретения в качестве пробиотиков рассматриваются микроорганизмы рода Bifidobacterium.
«Пребиотик», как правило, означает неусвояемый компонент пищевого продукта, который благотворно воздействует на организм реципиента, выборочно стимулируя рост и/или активность микроорганизмов, присутствующих в кишечнике организма-хозяина, и тем самым содействует улучшению состояния здоровья организма.
Штамм Bifidobacterium longum (B.longum) NCC 2705 (номер 2705 в собрании Nestle) является штаммом B.longum, имеющим международный идентификационный номер CNCM-I2618 (Collection Nationale de Cultures de Microorganismes в Институте Пастера, Париж, Франция).
Авторы изобретения продемонстрировали, что аллергическая реакция и симптомы могут быть облегчены, когда сенсибилизированные молодые млекопитающие обеспечиваются полноценной питательной композицией, которая содержит B.longum NCC 2705. Это определяет позитивное воздействие при вторичной профилактике аллергий.
Это воздействие сопровождается небольшим, но значимым уменьшением сенсибилизации молодых млекопитающих к аллергенам (то есть наблюдалась первичная профилактика аллергий).
Эффект композиции.
Изобретение относится к применению микроорганизмов рода Bifidobacterium, более конкретно Bifidobacterium longum (B.longum), и еще более конкретно, штамма B.longum NCC 2705 для получения полноценной питательной композиции, предназначенной для ослабления симптомов у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами. Авторы изобретения показали, что употребление Bifidobacterium longum вообще и B.longum NCC 2705, в частности, привело к ослаблению симптомов пищевой аллергии в группе мышей, получавших питательную композицию, содержащую указанный штамм Bifidobacterium. Это было доказано при индуцировании аллергической реакции (провокация) после сенсибилизации. Модель имитирует пищевую аллергию у человека, когда люди (обычно младенцы/маленькие дети) естественным образом становятся чувствительными к пищевым аллергенам, а в дальнейшем подвергаются воздействию указанных аллергенов повторно. При этом бактериальный штамм B.longum NCC 2705 показал протективное действие.
В одном воплощении данного изобретения эффектом композиции более конкретно является эффект действия при вторичной профилактике аллергий. В модели на мышах симптомы аллергий были действительно значительно снижены, что иллюстрируется более низкими показателями по клинической шкале тяжести аллергических проявлений. Как правило, могут включаться все симптомы или же отбираются общепризнанные симптомы аллергий.
В одном воплощении изобретения симптомы содержат диарею, кожные раздражения или респираторные симптомы, или же их комбинации.
В одном воплощении изобретения симптомы могут сопровождаться высвобождением биохимических медиаторов, таких как триптаза, химаза, гистамин, лейкотриены.
В одном воплощении изобретения композиция также оказывает воздействие на сенсибилизацию пациентов к аллергенам. На практике с помощью содержащей B.longum NCC 2705 композиции, по-видимому, достигается небольшая, но значимая по своему действию первичная профилактика аллергий. Животные демонстрировали более низкую сенсибилизацию к пищевым аллергенам. Эффект применения данной композиции представляет большой интерес в том отношении, что он проявляется и в ослаблении симптомов, и в снижении сенсибилизации, то есть в уменьшении риска появления последующих симптомов при повторном подвергании воздействию аллергенов.
В одном воплощении данная композиция снижает сенсибилизацию к другим аллергенам в более старшем возрасте. Предполагается, что данная композиция стимулирует (или по меньшей мере не блокирует) естественные процессы иммунного созревания и, следовательно, способна обладать долговременным действием снижения сенсибилизации к тем же самым аллергенам или к другим аллергенам (снижение сенсибилизации в более старшем возрасте). Делается предположение, что, снижая симптомы аллергии (вторичная профилактика) и краткосрочную сенсибилизацию (как часть первичной профилактики), композиция изобретения может при этом допускать прохождение естественного иммунного созревания, что и обеспечивает такой долговременный благоприятный эффект.
Композиция согласно изобретению или предназначенная для применения в изобретении.
Композиция изобретения может являться полноценной питательной композицией, такой как смесь для питания младенцев, или же может составлять существенную часть общей диеты. Предпочтительно композиция является полноценной питательной композицией, которая обеспечивает все или почти все пищевые потребности целевого организма при ее применении в качестве единственного источника питательных веществ. В одном воплощении композиция содержит предназначенные для младенцев каши. В другом воплощении, таком как продукт детского питания, композиция составляет одну часть полной диеты, предпочтительно 50% или более, или 20%, или более (количественно и качественно). В одном воплощении композиция содержит предназначенные для младенцев каши. В одном воплощении композиция может являться жидкой композицией для детей, содержащей каши или продукт детского питания.
Используемый пробиотик относится к роду Bifidobacterium. Хотя авторы изобретения не могут исключать того, что и другие пробиотики имели бы подобное или близкое действие, экспериментальные данные, способные доказать, что другие рода или штаммы пробиотиков одинаково эффективны, отсутствуют, за исключением наблюдаемых для Lactococcus lactis NCC 2287 (SL131) CNCM 1-4154 и Lactococcus lactis NCC 2180 (SL60) CNCM 1-4199, описанных в другой, одновременно находящейся на рассмотрении заявке этих же авторов.
В одном воплощении изобретения пробиотик является штаммом B.longum NCC 2705 CNCM-I2618.
В одном воплощении изобретения композиция содержит между 104 и 1011 колониеобразующих единиц (КОЕ) в 1 г сухой композиции. Когда композиция является смесью для питания младенцев, количество пробиотика в смеси для питания младенцев может составлять между 105 и 108 КОЕ на 1 г смеси для питания младенцев. В одном воплощении композиция содержит между 105 и 5×107 КОЕ/г, что является дозой, демонстрирующей наличие физиологического действия. В одном воплощении было определено, что пробиотики в низкой дозировке могут обладать благоприятным воздействием, в частности, когда композиция также содержит пребиотики и белки в определенном ограниченном количестве. В таком воплощении пробиотики присутствуют в композиции в количестве между 103 и 105 КОЕ/г. Пребиотики могут быть олигосахаридами и/или белками, которые могут присутствовать в количестве, не превышающем 4 г/100 ккал или менее 2 г/100 ккал, или менее 1,8 г/100 ккал, или менее 1,5 г/100 ккал композиции.
Пробиотик может быть смешан с сухой или влажной композицией изобретения. Могут быть применены специальные способы или режимы обработки в целях улучшения стабильности или жизнеспособности пробиотиков в композиции. Пробиотик может применяться в сухой или во влажной форме. После смешивания пробиотика с композицией смесь может быть обработана способом, который не оказывает серьезного воздействия на жизнеспособность пробиотиков. В еще одном воплощении пробиотики во время или после смешивания частично или полностью инактивируются. В одном воплощении пробиотики до применения в композиции изобретения были переведены в инактивированное и/или неспособное к репликации состояние. Это может быть достигнуто, например, тепловой обработкой или другими описанными способами обработки.
В одном воплощении изобретения композиция содержит пребиотики. Известно, что пребиотики содержат углеводы и, более конкретно, олигосахариды. Помимо этого, известно, что они широко применяются в качестве ингредиентов функциональных продуктов питания. Они противостоят гидролизу ферментами пищеварительного тракта человека и могут достигать толстой кишки в нерасщепленном состоянии, обеспечивая углеводный материал, особенно подходящий для роста бифидобактерий или других пробиотиков. Олигосахариды могут быть получены из, например, глюкозы, галактозы, ксилозы, мальтозы, сахарозы, лактозы, крахмала, ксилана, гемицеллюлозы, инулина или их смесей. Очищенные предлагаемые в продаже пребиотические продукты, такие как фруктоолигосахариды, содержат более около 95% сухих веществ в форме олигосахаридов.
Предпочтительно одно воплощение данной композиции является питательной композицией, которая содержит по меньшей мере один пребиотик.
Предпочтительно одно воплощение пребиотика содержит олигосахариды, полученные из глюкозы, галактозы, ксилозы, мальтозы, сахарозы, лактозы, крахмала, ксилана, гемицеллюлозы, инулина или их смесей. Более предпочтительно олигосахарид содержит фруктоолигосахарид. Наиболее предпочтительно пребиотик содержит смесь фруктоолигосахарида и инулина. Предпочтительно эта смесь содержит PREBIO1® или смесь коммерчески доступных RAFTILOSE® и RAFTILINE®.
Предпочтительно одно воплощение пребиотического компонента композиции содержит от около 50% до около 90% фруктоолигосахарида. Более предпочтительно оно содержит от около 60% до около 80% фруктоолигосахарида. Наиболее предпочтительно содержание около 70% фруктоолигосахарида. Предпочтительно одно воплощение пребиотика содержит от около 10% до около 50% инулина. Более предпочтительно оно содержит от около 20% до около 40% инулина. Наиболее предпочтительно оно содержит около 30% инулина. В одном воплощении пребиотический компонент может представлять между около 0,1% и 10% композиции.
В одном воплощении композиция изобретения содержит, кроме того, яблочный экстракт, содержащий полифенолы. Яблочный экстракт может способствовать ослаблению симптомов аллергий к пищевым продуктам у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами. Как таковой яблочный экстракт действует синергетическим образом с пробиотиком Bifidobacterium, модулируя при этом, понижая или ослабляя аллергические проявления у больных, страдающих пищевыми аллергиями. В одном воплощении такая композиция применяется для продукта детского питания и/или предназначенной для младенцев каши, которые естественным образом представляют подходящий носитель для композиции. В следующем воплощении продукты детского питания или предназначенные для младенцев каши содержат яблочные экстракты или полученный из яблок материал. В одном воплощении изобретения яблочный экстракт является белковым экстрактом, промышленно выпускаемым Val de Vire Bioactives (Conde sur Vire, Франция) под названием "Pomactiv HFV". В одном воплощении яблочный экстракт является подобным или получаемым из указанного Pomactiv HFV и обладает подобным действием.
Предполагаемый механизм действия.
За последние десятилетия непрерывно увеличивается распространенность аллергических заболеваний и в настоящее время они рассматриваются ВОЗ в качестве эпидемических. В общих чертах, аллергия, как полагают, является следствием дисбаланса между иммунными ответами Th1 и Th2, приводящего к сильному сдвигу в сторону продуцирования медиаторов Th2. Поэтому, не претендуя на теоретическую глубину, предполагается, что аллергия может быть смягчена, подавлена или предотвращена посредством восстановления надлежащего соответствия между Th1 и Th2 компонентами иммунной системы. Это подразумевает необходимость в снижении Th2-ответов или усилении, по меньшей мере временном, ответа Th1. Первый из них может отличаться сниженной выработкой цитокинов Th2, таких как IL-5, последний может отличаться увеличенным продуцированием таких Th1 цитокинов, как IFNγ. В качестве варианта у сенсибилизированных индивидуумов наиболее желательным может быть общий противовоспалительный эффект, например, через индукцию Т-регуляторных (Treg) клеток, способных к понижающему регулированию действия как Th1, так и Th2 клеток. Это может отображаться через способность к стимулированию секреции IL-10.
В одном воплощении изобретения композиция содержит гидролизованные или частично гидролизованные белки. Питательная композиция, основанная на (частично) гидролизованных белках, особенно подходит для иммунной системы и желудочно-кишечного тракта младенцев/маленьких детей, поскольку гидролизованные белки легче поддаются перевариванию и имеют сниженную аллергенность по сравнению с интактными белками. Помимо этого, не претендуя на теоретическую глубину, можно предположить, что гидролизованные белки могут являться предпочтительным субстратом для пробиотиков или кишечных бактерий (особенно демонстрирующих разнообразие пептидазной активности) по сравнению с интактными белками, приводя к усиленному действию штамма пробиотика и, таким образом, к синергизму между гидролизованными белками и пробиотиками. Это представляет наиболее подходящую композицию для иммунной системы и желудочно-кишечного тракта младенца/маленького ребенка, подверженного пищевой аллергии. В таком случае комбинация B.longum NCC 2705 с гидролизованными белками имеет самую высокую применимость для изобретения.
В одном воплощении гидролизованные белки являются гидролизованными белками сыворотки и/или казеина. В одном воплощении гидролизованные белки получают в результате действия на белки (например, на сывороточные белки) трипсина и/или химотрипсина. В одном воплощении гидролизованные белки содержат соевые белки или/и белки яиц. В одном воплощении гидролизованные белки получают в результате действия протеаз, таких как Protamex® и/или Flavourzyme® (Novozyme, Дания). В одном воплощении белки композиции, предпочтительно гидролизованные белки, содержат белки яиц или злаков. В одном воплощении гидролизованные белки получают в результате действия алкалазы. Композиция изобретения может содержать смесь из двух или более упомянутых источников белка.
Целевая группа.
Композиция изобретения наиболее подходящим образом нацелена на применение относительно молодыми пациентами, хотя ее действие на взрослых не исключено или возможно. Предпочтительно такие пациенты в действительности достаточно молоды для того, чтобы у них еще проходила фаза созревания иммунной системы и желудочно-кишечного тракта. У таких пациентов эффект композиции может быть более интенсивным или более быстрым. В одном воплощении композиция является смесью для питания младенцев, предназначенной для младенцев кашей и/или продуктом детского питания. Предпочтительно композиция адресуется молодым людям в возрасте менее 6 лет, в возрасте между моментом рождения и 3 годами или между рождением и моментом отлучения ребенка от груди. В одном воплощении композиция является стартовой смесью или смесью для прикорма младенцев. Предпочтительно питательная композиция содержит подавляющее большинство питательных веществ, необходимых для питания молодых людей.
В одном воплощении питательная композиция является композицией каши, предназначенной для младенцев/маленьких детей в возрасте 1-4 лет. Композиция может более определенно предназначаться для введения в период прекращения грудного вскармливания и/или вплоть до 12 месяцев после этого. Период отлучения от грудного вскармливания действительно важен для изобретения, поскольку младенцы в период отлучения подвергаются воздействию разнообразия пищевых продуктов, при этом все еще претерпевая созревание и реорганизацию своей иммунной системы и желудочно-кишечного тракта. Эффективное управление аллергическими реакциями имеет поэтому в этот период времени особое значение.
В отношении применения композиции изобретения дети, маленькие дети или младенцы могут быть аллергическими детьми. Аллергические дети - это такие дети, маленькие дети или младенцы, которые подвергались по меньшей мере одному приступу аллергической реакции (легкому, умеренному или тяжелому) к пищевому аллергену. В одном воплощении изобретения дети, маленькие дети или младенцы признаются имеющими тяжелые аллергии к пищевым аллергенам и/или испытавшими более одного умеренного или тяжелого приступа пищевой аллергии. Симптомы аллергий могут включать различные известные симптомы, такие как кожное раздражение или покраснение, желудочно-кишечные симптомы или респираторные симптомы.
Пищевые аллергены, охватываемые настоящим изобретением, могут включать все типы встречающихся в природе аллергенов или обычно встречающихся в пищевых продуктах, особенно в пищевых продуктах для молодых людей (например, младенцев, маленьких детей, детей).
Экспериментальные результаты.
Пробиотики, преимущественно принадлежащие к родам Lactobacillus и Bifidobacterium, были проверены в испытаниях на человеке и животных на их способность препятствовать аллергической сенсибилизации или развитию аллергических симптомов у сенсибилизированных индивидуумов. Здесь анализируется, обладает ли определенный штамм B.longum, а именно B.longum NCC 2705, потенциалом для смягчения развития аллергической сенсибилизации или симптомов.
На начальном этапе была разработана и применена in vitro система, основанная на человеческих лимфоцитах крови, для определения цитокиновых профилей, индуцированных различными штаммами B.longum. Предполагалось, что наблюдаемые профили будут прогностическими для выработки цитокинов, индуцируемой in vivo теми же самыми штаммами, и таким образом, для биологических эффектов, сообщаемых указанными штаммами.
Клетки аллергического индивидуума или индивидуума, предрасположенного к развитию аллергии, отличаются их склонностью к выработке цитокинов Th2. Для частичной имитации такого состояния in vitro была разработана модель клеточной культуры Th2-смещенных мононуклеарных клеток периферической крови (РВМС) человека в качестве альтернативного варианта для применения РВМС аллергических доноров. Th2-сдвиг был вызван культивированием РВМС с интерлейкином (IL)-4+анти-CD40-антителами (подробнее в разделе «Методики»); после 3 дней культивирования, чтобы вызвать Th2-сдвиг, на дополнительные 48 часов были добавлены бифидобактерии, приводя к общей продолжительности культивирования в 5 дней. Основными определяемыми показателями были цитокины IFNg, IL-10 и IL-5 по данным измерений ИФА (иммуноферментный анализ) в супернатанте клеток, стимулируемых B.longum.
Фигура 1/Таблица 1 показывает что B.longum NCC 2705 индуцировал подобные количества IFNg и IL-10, приводя к соотношению IFNg/IL-10, составляющему 1,3. Другие штаммы В. longum, исследовавшиеся параллельно, такие как B.longum NCC 3001 (ВВ536; заявленный Morinaga как АТСС ВАА-999 и B.longum NCC 435 (BL23, АТСС 15707), имели показатели соотношения IFNg/IL-10, в большей степени сдвинутые к IFNg. Помимо этого, B.longum NCC 2705 оказался эффективным ингибитором секреции IL-5. Эти данные означают, что B.longum NCC 2705 в условиях Th2-сдвига является мощным продуцентом IL-10 и поэтому может обладать антиаллергическим действием через противовоспалительную активность.
Фигура 2/Таблица 2 демонстрируют подтверждение этих результатов на уровнях мРНК для B.longum NCC 2705 по сравнению с B.longum ВВ536 и (из Е.coli). Уровни экспрессии различных генов анализировались спустя 10 и 24 часа после начала совместного культивирования Th2-смещенных человеческих РВМС с различными стимулами.
Культивирование Th2-смещенных РВМС с B.longum NCC 2705 или NCC 3001 (ВВ536) ведет к умеренной индукции IFNg по сравнению с LPS, известным мощным индуцирующим фактором IFNg. Уровни экспрессии мРНК IL-10, индуцированной Blongum NCC 2705, были более высоки, чем индуцированной Blongum ВВ536. Уровни мРНК IL-5 не изменялись, тогда как GATA-3 несколько снижались после инкубации с любым из штаммов. В целом эти обнаружения подтверждают результаты, полученные для уровней содержания белка (Табл.1.)
Эффект Blongum NCC 2705 in vivo был исследован в модели пищевой аллергии на мышах (OVA Food Allergy Mouse Model), поясняемой на Фиг.3.
Мыши линии BALB/c сенсибилизировались через недельные интервалы яичным альбумином (OVA)+токсин холеры, вводимых пероральным путем на протяжении 7 недель. В этой модели пероральная провокация высокой дозой OVA в конце периода сенсибилизации приводит к таким клиническим симптомам, как диарея, расчесывание, вздыбленная шерсть, цианоз и потеря подвижности.
NCC 2705 давался мышам с питьевой водой (5×108 ОЕ/мл; ad libitum) либо в течение фазы сенсибилизации со дня 1 по 43 (первичная профилактика), во время последней недели экспериментов (дни 43 - 50; вторичная профилактика), или же на протяжении всего периода испытаний (дни 1 - 50, все время).
Фигура 4 отображает клинические симптомы, наблюдавшиеся в двух независимых экспериментах.
У мышей, подвернутых терапии с Blongum NCC 2705, после провокации развивались значительно менее тяжелые клинические симптомы, чем у сенсибилизированных животных, не подвергавшихся такой обработке (положительный контроль). Наиболее выраженным эффект был при вторичной профилактике, но он также оставался значительным и при первичной профилактике, и когда Blongum NCC 2705 давался на протяжении всего времени (эксперимент 1, верхняя диаграмма). Во втором эксперименте был подтвержден протективный эффект во вторичной профилактике при наблюдавшейся тенденции к проявлению эффекта в первичной профилактике или в течение всего времени наблюдения (эксперимент 2, нижняя диаграмма).
Как показано на Фигуре 5, в дополнение к шкале клинических показателей в качестве критерия активации интестинальных тучных клеток после провокации аллергеном были определены серологические уровни протеазы-1 тучных клеток мыши (ММСР-1). Провокация OVA приводила к значительному увеличению серологических уровней ММСР-1 в группе положительного контроля по сравнению с отрицательной контрольной группой. У мышей, подвергнутых обработке NCC 2705, по сравнению с группой положительного контроля наблюдалась тенденция к модулированию серологических уровней ММСР-1 (хотя и незначительная).
Фигура 6/Таблица 3 показывает продуцирование цитокинов повторно стимулируемыми ex vivo лимфоцитами. С этой целью после выполнения провокации отбирались лимфоциты из брыжеечных лимфатических узлов (MLN), повторно стимулировались 1 мг/мл OVA и культивировались в течение 72 часов. С помощью мультиплексного анализа (Mesoscale®) были измерены уровни IL-1, IL-2, IL-4, КС, TNFa, IFN-γ, IL-5 и IL-10. MLN-лимфоциты мышей, обработанные NCC 2705 при первичной профилактике, продуцировали меньше IL-2, IL-4, TNFa, IFNg, IL-5 и IL-10 в сравнении с положительным контролем.
Уровни экспрессии в кишечнике различных ассоциируемых с аллергическими проявлениями генов определялись количественной полимеразной цепной реакцией (ПЦР) в реальном времени (qRT-PCR - см. способ ниже). Оценка экспрессии генов выполнялась на тканях подвздошной кишки для группы положительного контроля, группы отрицательного контроля и группы, получавшей Blongum NCC 2705 во время периода сенсибилизации (первичная профилактика) и на протяжении последней недели перед провокацией (вторичная профилактика). Фигура 7/Таблица 4 представляет полученные результаты: сенсибилизация приводила к повышающей регуляция транскрипции мРНК для типичных цитокинов Th2, таких как IL-4, IL-5, IL-9 и IL-13 (отрицательный контроль против положительного контроля), а также IL-10. Обработка с NCC 2705 (первичная или вторичная профилактика) приводила к выраженной понижающей регуляции этих маркеров.
Таким образом, эксперименты продемонстрировали понижающую регуляцию иммунных ответов через ослабление экспрессии релевантных генов, когда животные получали Blongum NCC 2705 (первичная и вторичная профилактика). Это, как полагают, вносит вклад в антиаллергическое действие исследуемого штамма Bifidobacterium при ослаблении пищевой аллергии в данной модели.
Выводы.
Эти данные показывают, что употребление Blongum NCC 2705 сенсибилизированном животным приводит к ослаблению аллергических симптомов при его подвергании воздействию сенсибилизирующего аллергена. Аналогично, хотя и менее выраженно, потребление В. longum NCC 2705 обеспечивало протективное действие во время фазы сенсибилизации (первичная профилактика). Это обнаружение соответствовало сниженной секреции цитокинов клетками брыжеечных лимфатических узлов, а также сокращенной экспрессии ключевых, соотносимых с аллергией генов в кишечнике, позволяющими предполагать, что модулирование компонентов иммунной системы способствует протективному действию.
Аналитические определения.
Реактивы и бактериальная биомасса.
Бактериальная биомассу получали культивированием каждого штамма под оптимальными условиями в жидкой питательной среде. Была определена кинетика роста для каждого штамма и в соответствии с ней биомасса отбиралась через 3 час после достижения фазы зрелости. В такой момент времени культуры дважды промывались в холодном PBS (физиологический раствор с фосфатным буфером) и замораживались в PBS с 20% глицерином при -80°C в 50 мкл аликвотах. LPS (липополисахарид из Е. coli) был закуплен у компании Sigma (Buchs, Швейцария).
Выделение и культивирование Th2-смещенных человеческих РВМС.
Мононуклеарные клетки периферической крови (РВМС) человека были выделены из фильтров, полученных от "Centre de Transfusion of the CHUV". Захваченные фильтрами клетки смывались обратно в мешок для взятия крови 90 мл сбалансированного солевого раствора Хэнкса (HBSS) (Sigma). Клетки разбавлялись 1:2 HBSS и РВМС выделялись центрифугированием по градиенту плотности на Histopaque 1077 (Sigma). Клетки отбирались в интерфазе и дважды промывались с HBSS. РВМС ресуспендировались в среде Дульбекко, модифицированной по способу Исков (cIMDM, Sigma), дополненной 10% эмбриональной бычьей сыворотки (Bioconcept, Париж, Франция), 1% L-глютамина (Sigma), 1% пенициллина/стептомицина (Sigma) и 0,1% гентамицина (Sigma). Клетки культивировались в 48-луночном планшете (Milian, Meyrin, Швейцария) с 1,5×106 клеток/мл в присутствии 50 нг/мл IL-4 (Bioconcept) и 1 мкг/мл анти-СО40-антител (R&D Systems, Abington, Англия) в cIMDM для индуцирования цитокинов фенотипа Th2. LPS использовался в концентрации 1 мкг/мл. После 3 дней культивирования добавлялись пробиотики в количествах 107, 106 и 105 КОЕ/мл. После добавления ингредиентов культивирование РВМС было продолжено в течение дополнительных 48 час, приводя к общей продолжительности культивирования в 5 дней.
ИФА цитокинов.
С помощью комплектов DuoSet от R&D systems в соответствии с инструкциями изготовителя измерялись уровни цитокинов IFN-γ человека, IL-5 человека, IL-10 человека, IFN-γ мыши, IL-13 мыши и IL-10а мыши.
Оценка результатов ИФА.
Величины OD (оптическая плотность) преобразовывались в пг/мл с использованием стандартных кривых перевода. Чтобы согласовать значительные колебания от донора к донору, как правило, наблюдаемые для РВМС, получаемых от различных людей-доноров, данные были стандартизированы согласно условному внутреннему стандарту. Величина IFN-γ в пг/мл, полученная для каждого донора при стимуляции с LPS, приравнивалась к 100%. При нормализации величин IL-10 за 100% принималось количество IL-10a, индуцируемое штаммом B.lactis NCC 2818 (депонирован Nestec SA как CNCM-I3446). Наконец, за 100% было принято количество IL-5a, индуцируемое IL-4 и антителом анти-СБ40 исключительно в чистой питательной среде (то есть при отсутствии пробиотиков).
Количественное определение экспрессии генов с помощью ПЦР в масштабе реального времени.
РВМС (1,5×106 клеток/мл) культивировались в cIMDM с IL-4 (50 нг/мл) и анти-CD40 (1 мкг/мл) в течение 3 дней. После этого к РВМС добавлялись ингредиенты и спустя 10 час и 24 час отбирались клетки. Тотальная РНК извлекалась из подвергнутых стимуляции РВМС с использованием комплекта "SV Total RNA Isolation System" (Promega, Wallisellen, Швейцария), включая обработку ДНК-азой согласно инструкциям изготовителя. Тотальная РНК определялась количественно с помощью использующего краситель ribogreen комплекта для количественных определений РНК (Molecular Probes, Базель, Швейцария). Была выполнена обратная транскрипция на 1 мкг тотальной РНК с помощью комплекта "Multiscribe Reverse Transcriptase kit" (Applied Biosystems, Foster City, CA, США). Тотальная РНК была смешана с 50 мкмоль случайных гексамеров, 0,5 ммоль дНТФ, 20 E ингибитора РНК-азы (Applied Biosystems), 62,5 Е обратной транскриптазы MultiScribe, IX RT буфером и 5,5 ммоль MgCl2 в конечном объеме 100 мкл. Человеческие IFNg, IL-10, IL-5, Tbet, GAT A3, FoxP3 (Applied Biosystems) количественно определялись ПЦР в масштабе реального времени (Applied Biosystems, ABI PRISM 7900HT) с использованием набора для оценки уровня экспрессии генов Taqman. Количественные показатели были подвергнуты нормализации по трем «генам домашнего хозяйства»: (β-актину, GAPDH и HPRT (Applied Biosystems).
Исходя из полученных величин порогового цикла (Ct) для каждого гена с помощью ACt были определены относительные и нормализованные показатели экспрессии мРНК. Величина Ct для каждого гена была скорректирована по среднему Ct трех «генов домашнего хозяйства». Результаты в выражении относительной экспрессии вычислялись по формуле: 2-ΔCt×K.
Модель пищевой аллергии к OVA на мышах.
Все исследования были одобрены внутренним Комитетом по этике компании Nestec и Ветеринарной службой кантона Vaud, Швейцария (разрешение №1970). Шестинедельные самки мышей линии BALB/c (Harlan Laboratories, Франция) сенсибилизировались пероральным путем (чреззондовое питание) через еженедельные интервалы 20 мг яичного альбумина (OVA) от Fluka (Buchs, Швейцария)+10 мкг/мышь токсина холеры (примененное в качестве адъюванта; List Biologicals, приобретен у LuBioscience, Люцерн, Швейцария), на протяжении 7 недель. Спустя одну неделю после последней сенсибилизации выполнялась пероральная провокация 100 мг OVA. На различных фазах эксперимента осуществлялось пищевое вмешательство с B.longum NCC 2705 (5×108 КОЕ/мл в питьевой воде); для первичной профилактики - в ходе периода сенсибилизации, для вторичной профилактики - начиная с конца фазы сенсибилизации, или же на протяжении всего времени испытания (Фиг.3). Через 30 минут после выполнения провокации мыши в течение 30 мин наблюдались индивидуально. Клинические симптомы регистрировались и количественно определялись следующим образом (оценка тяжести аллергии в баллах): 0: никаких симптомов, менее 4 эпизодов расчесывания; 1: 4-10 эпизодов расчесывания вокруг носа и головы, диарея отсутствует; 2: более 10 эпизодов расчесывания или вздыбливания шерсти и отсутствие подвижности или мягкий стул; 3: диарея, или затрудненное дыхание, или цианоз; 4: диарея в комбинации с неподвижностью после подталкивания, вздыбливание шерсти, затрудненное дыхание или цианоз; 5: анафилаксия. Спустя четыре часа после провокации мыши умерщвлялись (смещение шейных позвонков), отбирались кровь и последний сантиметр подвздошной кишки и замораживались в жидком азоте. Сывороточная ММСР-1.
Протеаза-1 тучных клеток мышей (ММСР-1) определялась количественно в сыворотке мыши средствами метода ИФА, приобретенными у Moredun Scientific (Penicuik, Шотландия), согласно инструкциям изготовителя. Данные по концентрации ММСР-1 были получены преобразованием величин OD в пг/мл с помощью полиномиальной кривой перевода.
Выделение и культивирование клеток брыжеечных лимфатических узлов.
Брыжеечные лимфатические узлы (MLN) гомогенизировались поршнем шприца в стрейнере для клеток (BD Falcon, Milian, Meyrin Швейцария). Клетки центрифугировались и дважды промывались в среде RPMI (Sigma), дополненной 10% эмбриональной бычьей сыворотки FBS (Bioconcept, Париж, Франция), 1% L-глютамина (Sigma), 1% пенициллина/стептомицина (Sigma), 0,1% гентамицина (Sigma), 0,1% β-монотиогликоля (Sigma). Клетки культивировались в 96-луночном плоскодонном планшете (Corning, Milian) при отсутствии или наличии OVA (1 мг/мл) с 3×106 клеток/мл. Через 72 час культуральные плашки замораживались.
Цитокины в супернатанте культур MLN.
С помощью комплекта для мультиплексного анализа 9 аналитов Th1/Th2 мыши (Meso Scale Discovery, Gaithersburg, MD, США) в соответствии с инструкциями изготовителя были измерены уровни мышиных IL-4, IL-5, IL-10, IFN-γ, IL-1β, IL-2, IL-8, TNF-α, IL-12T.
Анализ экспрессии генов в кишечнике с использованием микрочипов низкой плотности.
Выделение и количественные определения РНК.
Общие рибонуклеиновые кислоты (РНК) были выделены из подвздошной кишки согласно протоколу изготовителя при помощи комплекта "SV Total RNA isolation System kit", приобретенного у Promega (Dubendorf, Швейцария). РНК была определена количественно согласно протоколу изготовителя с использованием комплекта "quant-IT Ribogreen Reagent kit", предоставленного Promega (Dubendorf, Швейцария).
Обратная транскрипция.
Обратная транскрипция была выполнена на 1 мкг тотальной РНК с помощью комплекта "Multiscribe Reverse Transcriptase kit" от Applied Biosystems (Foster City, CA, США). Тотальная РНК была смешана с 50 мкмоль случайных гексамеров, 0,5 ммоль дНТФ, 20 Е ингибитора РНК-азы (Applied Biosystems), 62,5 E обратной транскриптазы MultiScribe, IX RT буфером и 5,5 ммоль MgCl2 в конечном объеме 50 мкл. Обратная транскрипция проводилась на термоциклере Т3 (Biometra, Gottingen, Германия) по следующей программе цикла: 10 мин при 25°С, 30 мин при 48°C, 5 мин при 95°С с завершением при 4°С.
Анализ на микрочипах низкой плотности (Low Density Array, LP А).
План проведения LDA был разработан в режиме онлайн на вебсайте Applied Biosytems (http://www3.appliedbiosystems.com/index.htm). Загрузка, ход исполнения и анализ были выполнены согласно протоколу изготовителя на устройстве для количественных измерений "ABI-Prism 7900НТ".
Количественные результаты были подвергнуты нормализации по трем «генам домашнего хозяйства»: β-актину, GAPDH и HPRT. Исходя из полученных величин порогового цикла (Ct) для каждого гена с помощью ΔCt были определены относительные и нормализованные показатели экспрессии мРНК. Величина Ct для каждого гена была скорректирована по среднему Ct трех «генов домашнего хозяйства». Результаты рассчитывались в виде относительной экспрессии по формуле 2-ΔCt×K, где K является множителем 106. Кратность увеличения результатов экспрессии была нормализована до уровней экспрессии в группе отрицательного контроля.
Пример 1
Ниже представлен пример композиции смеси для питания младенцев согласно настоящему изобретению. Эта композиция приводится исключительно в иллюстративных целях. Источник белка представляет собой обычную смесь сывороточного белка и казеина.

Изобретение относится к области микробиологии. Предложено применение штамма Bifidobacterium longum NCC 2705 (CNCM-I2618) для получения полноценной питательной композиции, предназначенной для ослабления симптомов аллергий к пищевым продуктам у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами. При этом указанная композиция обеспечивает существенную вторичную профилактику против аллергических реакций, вызываемых указанными пищевыми аллергенами. 15 з.п. ф-лы, 7 ил., 1 пр.
1. Применение штамма Bifidobacterium longum NCC 2705 (CNCM-I2618) для получения полноценной питательной композиции, предназначенной для ослабления симптомов аллергий к пищевым продуктам у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами, при этом указанная композиция обеспечивает существенную вторичную профилактику против аллергических реакций, вызываемых указанными пищевыми аллергенами.
2. Применение по п.1, где указанная композиция обладает способностью воздействовать на сенсибилизацию указанных пациентов к указанным аллергенам.
3. Применение по п.1, где указанный штамм Bifidobacterium longum является пробиотиком.
4. Применение по п.1, где указанная композиция содержит 105-108 КОЕ в 1 г сухой композиции.
5. Применение по п.1, где указанная композиция содержит по меньшей мере один пребиотик, предпочтительно содержащий фруктоолигосахарид.
6. Применение по п.1, где указанная композиция содержит яблочный экстракт, содержащий полифенолы, и где указанный яблочный экстракт способствует ослаблению симптомов аллергий к пищевым продуктам у больных, страдающих аллергиями, вызываемыми пищевыми аллергенами.
7. Применение по п.1, где указанная композиция содержит гидролизованные белки.
8. Применение по любому из предшествующих пунктов, где указанная композиция снижает сенсибилизацию к другим аллергенам в более старшем возрасте.
9. Применение по п.1, где указанные симптомы являются желудочно-кишечными, кожными или респираторными, или их комбинацией.
10. Применение по п.1, где указанная композиция содержит зерновые белки.
11. Применение по п.1, где указанная композиция является смесью для питания младенцев, предназначенной для младенцев кашей, жидкой композицией для детей, содержащей зерновые, или продуктом детского питания.
12. Применение по п.1, где указанная композиция является композицией каши, предназначенной для младенцев в возрасте 1-4 лет.
13. Применение по п.1, где указанная композиция предоставляется младенцам в период прекращения грудного вскармливания и/или вплоть до 12 месяцев после этого.
14. Применение по п.1, где указанные пациенты являются маленькими детьми в возрасте менее шести лет, предпочтительно в возрасте между моментом рождения и 3 годами.
15. Применение по п.1, где указанные симптомы сопровождаются высвобождением биохимических медиаторов, таких как триптаза, химаза, гистамин, лейкотриены.
16. Применение по любому из пп.1, 3 или 4, где указанный штамм Bifidobacterium подвергается инактивации так, чтобы сделать его нереплицируемым.
| WO 2007093619 A1, 23.08.2007 | |||
| JP 2006273852 A, 12.10.2006 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| EP 1854468 A1, 14.11.2007 | |||
| JP 2009060800 A, 26.03.2009 | |||
| MENARD O et all: “Gnotobiotic mouse immune response induced by Bifidobacterium sp | |||
| strains isolated from infants”, APPLIED AND ENVIPONMENTAL MICROBIOLOGY, 2008, vol | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Льновыдергивающая машина | 1923 |
|
SU660A1 |
| Устройство для мойки корнеклубнеплодов | 1984 |
|
SU1227152A1 |
Авторы
Даты
2015-01-20—Публикация
2010-08-11—Подача