Изобретение относится к способу получения новых гетероциклических кислородсодержащих соединений, а именно эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот, которые могут быть использованы в качестве прекурсоров для получения биологически активных веществ, флуоресцирующих материалов и для синтеза фталоцианинов.
Из уровня техники нам не известны способы получения данных соединений, поэтому задачей изобретения является разработка способа получения эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот структурной формулы
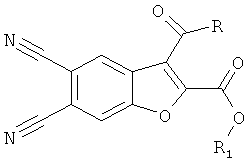
где a) R=4-СН3С6Н4; b) R=4-СН3О-С6Н4; с) R=2-тиенил; R1=СН3, С2Н5.
Поставленная задача достигается тем, что в качестве исходных реагентов для синтеза эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот (схема 1) использовались высокоактивный субстрат - 4-бром-5-нитрофталонитрил (1) и натриевые соли производных 2,4-диоксобутановых кислот (2), полученные конденсацией Кляйзена из коммерчески доступных ацетофенонов и этилового (метилового) эфира щавелевой кислоты.
Взаимодействие указанных реагентов протекает при температуре 75…85°С и мольном соотношении (1):(2)=1:2 в течение 18-24 часов в растворе ДМФА и не требует дополнительного использования катализаторов. Затем реакционную массу разбавляют десятикратным избытком воды с Т=0…25°С. Выделившийся смолистый осадок экстрагируют хлористым метиленом, тщательно промывают водой, хроматографируют на силикагеле. Элюент (растворитель) упаривают, выпавший осадок (3) отфильтровывают, перекристаллизовывают из спирта.
Схема 1:
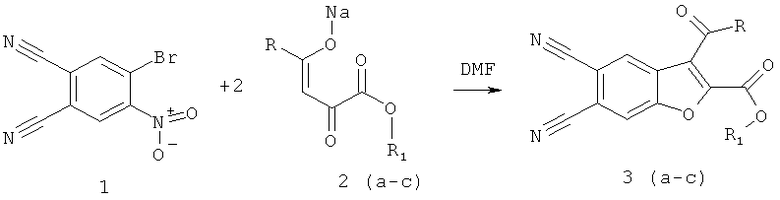
где a) R=4-СН3С6Н4; b) R=4-СН3О-С6Н4; с) R=2-тиенил; R1=СН3, C2H5.
Строение полученных соединений подтверждено методами ИК, ЯМР Н1, ЯМР С13, NOESY спектроскопией и масс-спектрометрией.
Изобретение иллюстрируется следующими примерами.
Пример 1. Метиловый эфир 5,6-дициано-3-(4-метилбензоил)бензофуран-2-карбоновой кислоты (3а).
К раствору 0,002 моль 4-бром-5-нитрофталонитрила в 5 мл ДМФА прибавляют 0,004 моль соединения (2а), перемешивают при температуре 75…85°С и мольном соотношении (1):(2а)=1:2 в течение 18-24 часов в растворе ДМФА. Затем реакционную массу разбавляют десятикратным избытком воды с Т=0…25°С. Выделившийся смолистый осадок экстрагируют хлористым метиленом, тщательно промывают водой, хроматографируют на силикагеле. Элюент (растворитель) упаривают, выпавший осадок (3а) отфильтровывают, перекристаллизовывают из спирта, сушат при температуре 60-80°С. Получают 0,32 г (47% от теории) метилового эфира 5,6-дициано-3-(4-метилбензоил)бензофуран-2-карбоновой кислоты - порошок белого цвета, т. пл.=210-212°С.
Примеры 2 и 3. Другие замещенные 5,6-дицианобензофуран-2-карбоновые кислоты получают аналогично примеру 1. Физико-химические характеристики замещенных 5,6-дицианобензофуран-2-карбоновых кислот приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ БЕНЗОФУРАН-5,6-ДИКАРБОНИТРИЛОВ | 2009 |
|
RU2429235C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 4-НИТРО-5-(2-ОКСОЭТИЛ)ФТАЛОНИТРИЛОВ | 2010 |
|
RU2443681C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЗАМЕЩЕННЫХ 1,2-БЕНЗИЗОКСАЗОЛ-5,6-ДИКАРБОНИТРИЛОВ | 2010 |
|
RU2446164C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 4-[ЦИАНО(ФЕНИЛ)МЕТИЛ]-5-НИТРОФТАЛОНИТРИЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2428413C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИ-3-R-ИНДОЛ-5,6-ДИКАРБОНИТРИЛОВ | 2013 |
|
RU2534988C1 |
| Способ получения 3-ацилзамещенных 2-арил(гетерил)-1Н-индол-5,6-дикарбонитрилов | 2017 |
|
RU2640351C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 4-ГИДРОКСИ-3-ОКСО-3,4-ДИГИДРО-2Н-1,4-БЕНЗОКСАЗИН-6,7-ДИКАРБОНИТРИЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2425047C9 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЗАМЕЩЕННЫХ 2-АМИНО-1-ГИДРОКСИ-5,6-ДИЦИАНОИНДОЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2425031C1 |
| Способ получения 2-замещенных 1-гидроксипирроло[3,4-f]индол-5,7-(1Н,6Н)-дионов | 2015 |
|
RU2613582C1 |
| Способ получения 2,3-дизамещенных 1-гидрокси-1H-индол-5,6-дикарбонитрилов | 2017 |
|
RU2641006C1 |
Изобретение относится к способу получения эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот общей формулы

где a) R=4-CH3C6H4; b) R=4-СН3О-С6H4; с) R=2-тиенил; R1=СН3, С2Н5, которые могут быть использованы в качестве прекурсоров для получения биологически активных веществ, флуоресцирующих материалов и для синтеза фталоцианинов. Способ включает получение эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот на основе реакции взаимодействия 4-бром-5-нитрофталонитрила и натриевых солей производных 2,4-диоксобутановых кислот, взаимодействие указанных реагентов протекает при температуре 75…85°С и мольном соотношении 1:2 соответственно в течение 18-24 часов в растворе ДМФА, затем реакционную массу разбавляют десятикратным избытком воды с Т=0…25°С, выделившийся смолистый осадок экстрагируют хлористым метиленом, тщательно промывают водой, хроматографируют на силикагеле, элюент (растворитель) упаривают, выпавший осадок отфильтровывают, перекристаллизовывают из спирта. 1 табл.
Способ получения эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот общей формулы

где а R=4-СН3С6Н4; b R=4-СН3О-С6Н4; с R-2-тиенил; R1=СН3, CH2H5,
заключающийся в том, что в качестве исходных реагентов для синтеза эфиров замещенных 5,6-дицианобензофуран-2-карбоновых кислот используют 4-бром-5-нитрофталонитрил и натриевые соли производных 2,4-диоксобутановых кислот, взаимодействие указанных реагентов протекает при температуре 75-85°С и мольном соотношении 1:2 соответственно, в течение 18-24 ч в растворе диметилформамида, затем реакционную массу разбавляют десятикратным избытком воды с Т=0-25°С, выделившийся смолистый осадок экстрагируют хлористым метиленом, тщательно промывают водой, хроматографируют на силикагеле, элюент (растворитель) упаривают, выпавший осадок отфильтровывают, перекристаллизовывают из спирта.
| US 6211203 В, 03.04.2001 | |||
| WO 2005099684 A1, 27.10.2005 | |||
| Соединительная линия для связи телефонных станций шаговой системы с телефонными станциями системы Ц.Б. | 1934 |
|
SU45958A1 |
| Способ получения 3-бензофурилуксусных кислот | 1977 |
|
SU639884A1 |
Авторы
Даты
2012-03-27—Публикация
2010-05-19—Подача