Изобретение относится к области медицины, а именно инфекционных болезней взрослых, и может быть использовано для лечения больных острыми формами вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D).
Вирусные гепатиты относятся к наиболее массовым инфекциям современности. Некоторые специалисты считают, что мы живем в период пандемии вирусных В и С гепатитов [1]. По данным ВОЗ, проблема вирусных гепатитов - проблема общественного здравоохранения в глобальном масштабе: в мире насчитывается около 2000 миллионов человек, инфицированных вирусом гепатита В, из которых более 350 миллионов инфицированы хронически и от 500000 до 700000 человек ежегодно умирают от инфекции вируса гепатита В. Около 130-170 миллионов человек хронически инфицируются вирусом гепатита С. Приблизительно 57% случаев цирроза печени и 78% случаев первичного рака печени обусловлены инфекцией вируса гепатита В или С [2, 3]. Гепатиты вирусной этиологии входят в число десяти заболеваний, определяющих летальность в США [4]. В первом десятилетии двадцать первого столетия заболеваемость вирусными гепатитами в целом по России и по ее отдельным регионам продолжает оставаться высокой. Уровень заболеваемости вирусными гепатитами с парентеральным механизмом передачи инфекции ассоциирован с распространенностью в стране внутривенной наркомании. Значимо и то, что растет число трудно поддающихся традиционной терапии форм заболеваний, вызванных двумя-тремя вирусами (микст-гепатитов), а также сочетанных поражений печени (вирусных + токсических). Нередко болезнь приобретает затяжное течение.
Вопросы лечения вирусных гепатитов далеки от разрешения. На протяжении многих лет терапевтические мероприятия в значительной мере сохраняются в неизменном виде и еще во многом соответствуют устаревшим представлениям о сущности развивающихся при гепатите патологических процессов и путях их коррекции. В связи с этим актуальным является разработка эффективных способов терапии заболеваний печени вирусной этиологии, обеспечивающих сокращение сроков и повышающих качество лечения.
Патогенетическая терапия острых форм вирусных гепатитов проводится по следующим направлениям: неспецифическая дезинтоксикация, гепатопротекция, иммунокоррекция, витаминотерапия, а также применение антигипоксических и антигеморрагических средств.
Методы лечения различных форм вирусных гепатитов в нашей стране регламентированы приказами: Министра здравоохранения СССР 1989 г. №408, Минздравсоцразвития Российской Федерации 2004 г. №260, 2005 г. №618, 621, 634, 2006 г. №571 [5-10]. Согласно регламентирующим документам, лечение острых вирусных гепатитов должно проводиться в стационарных условиях и заключаться в назначении всем больным базисной терапии, состоящей из охранительного режима, диеты №5, обильного питья (2-3 литра в сутки), приема поливитаминов. Лечение легких форм острых вирусных гепатитов ограничивается базисной терапией.
При среднетяжелом и тяжелом течении острого вирусного гепатита В показана противовирусная терапия препаратами интерферона (реаферона) по 1 млн ЕД 2 раза в сутки внутримышечно в течение 5-6 дней, затем по 1 млн ЕД 1 раз в сутки еще 5 дней. При отсутствии препаратов интерферона назначают рибоксин внутрь по 0,2 г 4 раза в сутки на протяжении 10 дней, цитохром С по 10 мг/сут внутримышечно, кверцетин внутрь по 0,04 г 3 раза в день в течение 10-14 дней. Базисная терапия при этом усиливается внутривенными вливаниями 5% раствора глюкозы, раствора Рингера по 500-1000 мл/сут с 10 мл 5% аскорбиновой кислоты, гемодеза по 200-400 мл/сут, 10-20% раствора альбумина по 50-100 мл/сут. При этом срок пребывания больных с тяжелыми формами вирусных гепатитов в отделении реанимации и интенсивной терапии (ОРИТ) составляет от 7 до 20 суток и более, а средняя длительность лечения в стационаре - 60-85 суток. Экономические затраты на одного стационарного больного данной нозологической формой в ценах декабря 2009 г. составляют примерно 120 тыс. рублей (данные Санкт-Петербургского городского гепатологического центра).
Известны способы лечения тяжелых форм вирусных гепатитов, основное содержание которых заключается в проведении неспецифической дезинтоксикации: посредством введения кристаллоидных и коллоидных плазмозаменителей, альбумина, плазмы (1,5-3 л/сут); назначении энтеросорбентов; осуществлении сеансов оксигенобаротерапии, эфферентной терапии (гемосорбции, плазмофереза, плазмосорбции, ультрафильтрации); применении глюкокортикоидов, рибоксина, эссенциале, витаминов [11-15].
Известны способы лечения заболеваний печени вирусной этиологии путем использования составов, обладающих гепатопротективным действием, основными активными компонентами которых являются различные аминокислоты и их производные: композиция, включающая L-аспарагиновую кислоту, L-аргинин и углевод (например, сорбит) [16]; составы, содержащие производные гидроксипролина [17], оротовой кислоты [18], валин, лейцин, изолейцин (препарат «Фолькамин») [19]; смеси, состоящие из аминокислот, нуклеотидов и фермента [20]. Известна гепатопротективная активность урсодеоксихолевой кислоты [21], предшественников аминокислоты L-цистеин [22], холинового эфира тиоктовой кислоты [23], человеческого альфа-фетопротеина [24].
Общими недостатками перечисленных препаратов-гепатопротекторов, предлагаемых для лечения вирусных гепатитов, являются отсутствие у них противовирусных эффектов, недостаточная противовоспалительная активность и низкая эффективность. Некоторые из перечисленных препаратов не зарегистрированы в Российской Федерации в качестве лекарственных средств.
Известны способы этиотропного лечения вирусных гепатитов, заключающиеся в монотерапии интерфероном или интерфероном и рибавирином, клиническая эффективность которых верифицирована [25-33]. Из всех интерферонов наиболее широко используемым препаратом является интерферон альфа [34]. Однако высокая стоимость препаратов наряду с недостаточной эффективностью и обилием побочных эффектов (лихорадка, лейкопения, нейтропения, тромбоцитопения, анемия, миалгия, аутоиммунный синдром, диспепсические явления и депрессия), усиливающих типовые иммунологические реакции при острых вирусных гепатитах [35], ограничивают их применение в клинической практике [36].
При лечении вирусных гепатитов широкое применение находят препараты, обладающие иммунокорригирующим действием: индукторы интерферона [37]; средства, стимулирующие гуморальные иммунные реакции [38]; препараты, увеличивающие функционально-метаболическую активность макрофагов [39] и стимулирующие продукцию антител [40]. Общими недостатками всех препаратов, обладающих иммунокорригирующим действием, применяемых при лечении вирусных гепатитов, являются их низкая эффективность, частое возникновение побочных эффектов.
Значимую роль в формировании цитолитического синдрома при острых вирусных гепатитах играет оксидативный стресс [41]. Наиболее интенсивно процессы неферментативного окисления проявляются при HBV-гепатитах [42]. А в качестве фактора, каталитически мультиплицирующего продукцию свободных радикалов, выступают ионы железа, выделяющиеся из трансферрина и ферритина при повреждении гепатоцитов [43,44]. В присутствии ионов металлов переменной валентности антиоксиданты (α-токоферол, аскорбиновая кислота) превращаются в продуценты гидроксильного радикала (реакция Фентона) [45]. Ионы железа не только стимулируют свободнорадикальное повреждение гепатоцитов, но и значимо ускоряют процесс репликации вирусов гепатита В и С [46-48], предопределяют эффективность интерферонотерапии [49]. С целью коррекции данных патогенетически значимых процессов при лечении вирусных гепатитов назначают антиоксиданты [50] и комплексоны железа [51]. Однако эффективность этих назначений низкая, поскольку антиоксиданты назначаются не в комплексе с тиолами, а ионы железа в составе используемых комплексонов не теряют каталитической активности.
Известно средство, представляющее собой эмульсию перфторуглеродов, используемое для лечения и профилактики патологического разрастания соединительной ткани в паренхиматозных органах [52].
В качестве прототипа, как наиболее близкий по технической сущности, выбран способ лечения осложненных форм вирусных гепатитов, предусматривающий введение эмульсии перфторуглеродов перфторан дополнительно к базисной терапии, обеспечивающий снижение ферментемии и уровня билирубина [53]. Недостатком способа-прототипа является недостаточно высокая эффективность.
Цель изобретения заключается в повышении эффективности лечения больных с острыми формами вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D), сокращении продолжительности и снижении экономических затрат на лечение данной категории больных.
Указанная цель достигается за счет комплексного назначения перфторана и фармакологических средств патогенетической терапии в дополнение к базисной терапии.
Заявляемый способ лечения больных с острыми формами вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D) заключается в том, что дополнительно к базисной терапии и введению перфторана назначают фармакологические средства патогенетической терапии: новокаин, комплекс антиоксидантов и восстанавливающих их тиолов (аскорбиновая кислота, α-токоферол, N-ацетилцистеин, ретинол и унитиол), мексидол (эмоксишша сукцинат) и витамин D3.
Перфторуглеродная эмульсия перфторан (ПФ) обладает рядом свойств, которые могут благоприятно отразиться на течении инфекционного процесса, в том числе при вирусных гепатитах. К числу этих свойств относятся: газотранспортное, противоишемическое, дезинтоксикационное, мембраностабилизирующее действие [54], способность индуцировать ферментные и неферментные антиоксидантные системы [55], иммуномодулирующие и противовирусные эффекты [56, 57]. Таким образом, перфторан - полифункциональное средство, обладающее потенциалом воздействия на различные звенья патогенеза вирусных гепатитов.
Перфторан производится ОАО НПФ «Перфторан» (Россия, г.Пущино Московской обл.). Препарат представляет собой смесь двух перфторуглеродов: перфтордекалина и перфторпараметилциклогексилпиперидина (2:1), эмульгированных с помощью поверхностно-активного вещества проксанол-268, с размером частиц эмульсии 0,03-0,15 мкм. Препарат внесен в Реестр лекарственных средств России и разрешен к клиническому применению с 1992 г. в качестве плазмозаменителя с газотранспортной функцией при шоковых состояниях, больших кровопотерях, множественных травмах, ожогах больших поверхностей тела, состояниях клинической смерти, а также в трансплантологии при пересадке органов [58].
Заявляемый способ лечения, включающий комплексное применение перфторана и патогенетических средств, реализовывали следующим образом:
- больным при поступлении их в ОРИТ дополнительно к базисной терапии назначали перфторан в дозе по 400 мл 1-2 раза в день в течение 2-3 дней внутривенно, капельно (800-2400 мл на курс). Дозу регулировали в зависимости от массы тела и тяжести состояния больного;
- в качестве индуктора интерферона назначали гидрохлорид β-диэтиламино-этилового эфира пара-аминобензойной кислоты, т.е. новокаин. Новокаин в биосредах организма быстро гадролизуется с выделением пара-аминобензойной кислоты, обладающей выраженным интерферон-индуцирующим действием [59]. Новокаин также представляет собой высокоактивный индуктор интерферона в культуре клеток и организме людей, отличающийся хорошей переносимостью и мягким спазмолитическим действием [60];
- фармакологическая коррекция проявлений оксидативного стресса эффективна только при комплексном применении водо-, жирорастворимых антиоксидантов, восстанавливающих их тиолов и комплексонов (хелаторов) металлов переменной валентности [61-63]. Исходя из этого, для достижения цели изобретения использовали аскорбиновую кислоту, α-токоферол и унитиол. Для восполнения пула эндогенного глутатиона перорально назначали N-ацетилцистеин. В протекции биологических мембран от повреждающего действия прооксидантов, в кооперации с α-токоферолом (формируя в липидном биослое мембран динамичные сенсорно-проводящие комплексы, защищающие 300-500 молекул фосфолипидов [64]), участвует и ретинол (витамин А), усиливающий антиоксидантные эффекты витамина Е [65], который также использовали при лечении острых форм вирусных гепатитов. В качестве комплексона металлов переменной валентности назначали мексидол (эмоксипина сукцинат), который достаточно давно известен и с успехом применяется в терапии критических состояний [66]. Данный лекарственный препарат имеет широкий спектр фармакологической активности: является антигипоксическим, стресспротективным, ноотропным, противосудорожным и анксиолитическим средством, эффективно ингибирующим свободнорадикальное окисление липидов. Столь широкий диапазон фармакологической активности мексидола обусловлен способностью препарата стимулировать сукцинатокидазное окисление (компенсаторный путь синтеза АТФ [67]), фосфорилироваться в биологических системах, приобретая свойства ингибитора сериновых, металлозависимых протеиназ [68] и комплексона металлов переменной валентности [69], что проявляется цитопротективными эффектами;
- только в последние годы стало обращать на себя внимание иммуномодулирующее действие 1,25-дигидроксивитамина D3 (активная форма витамина D3). Иммуномодудирующая активность витамина D3 опосредуется специфическими рецепторами и факторами транскрипции NF-AT и NF-kB, либо реализуется при его взаимодействии с воспринимающими витамин D3 элементами промоторных регионов генов (экспрессия, по крайней мере, нескольких сотен генов контролируется витамином D3 [70]), Для реализации заявляемого способа лечения острых форм вирусных гепатитов значимо то, что в присутствии активной формы витамина D3 супрессируется экспрессия провоспалительных цитокинов [71]. Витамин D3 назначали перорально.
Возможность достижения цели изобретения доказывается результатами проведенных экспериментальных исследований на моделях острого гепатита и клинических испытаний способа при лечении больных с острыми формами вирусного гепатита В и микст-гепетитов (В+С, В+D, В+С+D) представленными в следующих примерах.
Пример 1. Экспериментальные исследования с целью определения возможности применения заявляемого способа для лечения гепатита выполнены на белых беспородных крысах массой 180-200 г.
Использованы две модели острого гепатита: токсический и аутоагрессивный.
Острый токсический гепатит воспроизводили путем однократного внутрижелудочного введения крысам 1% аллилового спирта в дозе 15 мл/кг.
Острый аутоагрессивный гепатит воспроизводили последовательным внутривенным введением крысам вначале 1 мл взвеси трехдневной культуры Propyonibacterium acnes (1010 КОЕ/мл физиологического раствора натрия хлорида), а через 6 суток - брюшнотифозного эндотоксина ty-4446 серии 158 производства Санкт-Петербургского НИИ вакцин и сывороток в дозе 1,5 мг/кг.
Введение препаратов осуществляли в следующем порядке:
- перфторан вводили внутрибрюшинно в дозе 10 мл/кг;
- новокаин вводили внутрижелудочно в дозе 1,5 мг/кг;
- мексидол вводили внутрижелудочно в дозе 10 мг/кг;
- N-ацетилцистеин вводили внутрижелудочно в дозе 10 мг/кг совместно с новокаином и мексидолом;
- ретинол вводили внутрижелудочно в дозе 70 мг/кг через 30 мин после новокаина;
- витамин D3 вводили внутрижелудочно в дозе 30 МЕ/кг совместно с ретинолом;
- аскорбиновую кислоту вводили подкожно в дозе 30 мг/кг;
- унитиол вводили внутримышечно в дозе 50 мг/кг;
- α-токоферол вводили внутримышечно в дозе 25 мг/кг.
Перфторан вводили однократно через 1 сутки после отравления животных. Остальные препараты также начинали вводить через сутки после отравления животных и осуществляли это один раз в день. Их введение повторяли через двое, трое, четверо и пять суток после начала эксперимента. Дозировка антиоксидантов оптимизирована в предварительных полнофакторных экспериментах [72].
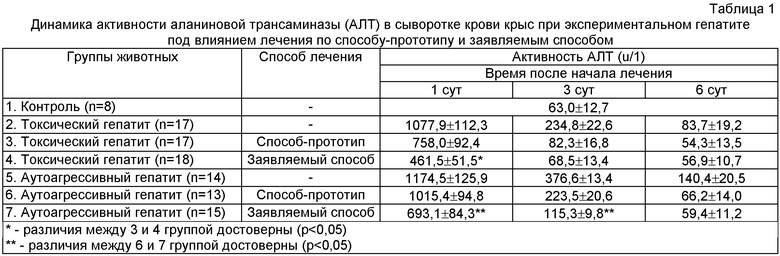
Эффективность фармакологической коррекции проявлений острых форм гепатитов при лечении перфтораном в дополнение к базисной терапии (способ-прототип) и заявляемым способом оценивали по активности аланиновой трансаминазы (АЛТ) в сыворотке крови животных через 1, 3 и 6 суток после введения препаратов. Активность фермента определяли с помощью биохимического анализатора «Spectrum». Полученные данные представлены в таблице 1.
Как видно из представленных данных, лечение заявляемым способом обеспечивает более быструю нормализацию уровня АЛТ в сыворотке крови животных как при токсическом, так и при аутоагрессивном гепатите.
В указанные выше сроки проведена также оценка интенсивности процессов перекисного окисления липидов в печени крыс по уровню активности прооксидантных ферментов: ксантиноксидазы и миелопероксидазы клеток Купфера и некоторым показателям состояния антиоксидантной системы: содержанию восстановленного глутатиона, активности каталазы, глюкозо-6-фосфатдегидрогеназы в гепатоцитах.
Активность ксантиноксидазы (КСО) оценивали спектрофотометрически по скорости изменения концентрации мочевой кислоты в среде инкубации и выражали в мкМ мочевой кислоты/мг белка в 1 минуту.
Активность миелопероксидазы (МП) определяли гистохимическим методом в криостатных (-20°С) срезах печени толщиной 15 мкм и выражали в условных единицах.
Концентрацию восстановленного глутатиона (GSH) устанавливали фотоколоро-метрически по методу, основанному на восстановлении нитропруссида натрия глутатионом в щелочной среде с образованием окрашенного соединения и выражали в мкМ GSH/1 г ткани печени.
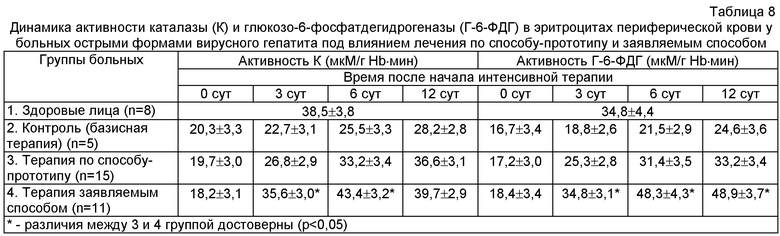
Активность каталазы (К) измеряли спектрофотометрически по скорости убыли пероксида водорода в среде инкубации и выражали в мкМ Н2О2/мг белка в 1 минуту.
Оценку активности глюкозо-6-фосфотдегидрогеназы (Г-6-ФДГ) проводили также спектрофотометрически по скорости изменения содержания НАДФН в среде инкубации. Активность энзима выражали в мкМ НАДФН/мг белка в 1 минуту.
Полученные результаты подвергали статистической обработке. Достоверность различий между группами оценивали по критерию Стьюдента.
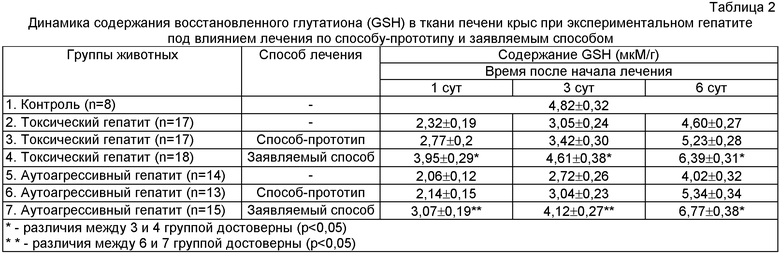
Результаты экспериментальных исследований представлены в таблицах 2, 3 и 4.
Как видно из представленных данных, динамика проявлений токсического и аутоагрессивного гепатитов развивалась параллельно с ростом активности в ткани печени ксантиноксидазы и миелопероксидазы. В группах животных, лечение которых проводили заявляемым способом, наблюдалась достоверно более быстрая нормализация активности указанных ферментов.
Обратная картина отмечена со стороны показателей состояния биоантиокислителей, В разгар экспериментальных гепатитов наблюдалось снижение содержания восстановленного глутатиона, активности каталазы и глюкозо-6-фосфатдегидрогеназы в ткани печени животных. Лечение заявляемым способом обеспечивало более быстрое восстановление этих показателей антиоксидантной системы у животных с обоими вариантами экспериментальных гепатитов.
Таким образом, экспериментальные исследования показали возможность и целесообразность применения заявляемого способа лечения в клинике для терапии острых форм вирусных гепатитов.
Пример 2. Клинические исследования проводились на базе Санкт-Петербургского городского гепатологического центра и 442 окружного клинического военного госпиталя Ленинградского военного округа (г.Санкт-Петербург).
Заявляемый способ применялся при терапии 20 больных с диагнозами: острый гепатит В (8 чел.), острый микст-гепатит В+D (3 чел.), острый микст-гепатит В+С (7 чел.), острый микст-гепатит В+С+D (2 чел.).
Способ-прототип применялся при терапии 19 больных с диагнозом: острый гепатит В (6 чел.), острый микст-гепатит B+D (2 чел.), острый микст-гепатит В+С (10 чел.), острый микст-гепатит В+С+D (1 чел.).
Контрольная группа в количестве 15 человек получала только базисную терапию, состоящую из охранительного режима, диеты №5, обильного питья (2-3 л/сут), приема поливитаминов, внутривенных вливаний 5% раствора глюкозы, раствора Рингера по 500-1000 мл/сут с 5 мл рибоксина, гемодеза по 200-400 мл/сут, 10-20% раствора альбумина по 50-100 мл/сут.
Все больные - мужчины от 17 до 40 лет. Состав групп идентичен по диагнозу и возрасту. У всех больных наблюдалась желтушная форма с холестатическим синдромом, тяжелое течение.
В ходе лечения по способу-прототипу пациенты дополнительно к базисной терапии получали перфторан, который вводили внутривенно капельно в дозе по 400 мл 1-2 раза в день в течение 2-3 дней. Доза перфторана регулировалась в зависимости от массы тела и тяжести состояния больного и составляла 800-2400 мл на курс.
При проведении лечения заявляемым способом пациенты дополнительно к базисной терапии и назначению перфторана получали:
- новокаин в виде 0,5% раствора в дозе 20-25 мл (из расчета 1,5 мг/кг) внутривенно капельно один раз в день;
- аскорбиновую кислоту в виде 5% раствора в дозе 2 мл внутримышечно два раза в день;
- α-токоферол в виде 10% масляного раствора в дозе 1 мл внутримышечно два раза в день;
- унитиол в виде 5% раствора в дозе 5 мл внутримышечно два раза в день;
- N-ацетилцистеин в дозе из расчета 10 мг/кг внутрь два раза в день;
- ретинол по 5000 ME в капсулах внутрь после еды два раза в день;
- мексидол (эмоксипина сукцинат) в виде 5% раствора в дозе 2 мл внутривенно два раза в день;
- витамин D3 по 1000 ME внутрь два раза в день.
Все перечисленные препараты назначали в течение 10 дней.
Эффективность заявляемого способа лечения острых форм вирусных гепатитов оценивали по содержанию в сыворотке крови больных билирубина и активности аланиновой трансаминазы (АЛТ) через 3, 6 и 12 суток после начала терапии. Активность АЛТ определяли по унифицированному динитрофенилгидразиновому методу Райтмана-Френкеля.
Начальные показатели билирубина и АЛТ, при которых назначалось лечение заявляемым способом, составили 428±38 мкМ/л и 31,3±3,2 мМ/час·л, соответственно, при норме до 20 мкМ/л и 0,68 мМ/час·л, соответственно.
Динамика указанных показателей под влиянием лечения заявляемым способом у больных острыми формами вирусных гепатитов за период их пребывания в ОРИТ в сравнении с аналогичной группой пациентов, получавших лечение по способу-прототипу, представлена в таблице 5.
Как видно из представленных данных, заявляемый способ лечения острых форм вирусных гепатитов способствует достоверно более быстрой нормализации уровня билирубина и активности трансаминазы в сыворотке крови больных.
В целях доказательства антиоксидантной эффективности заявляемого способа лечения острых форм вирусных гепатитов проведены исследования его влияния на интенсивность процессов пероксидации по показателям активности миелопероксидазы в нейтрофильных гранулоцитах периферической крови, содержанию восстановленного глутатиона, активности каталазы и глюкозо-6-фосфатдегидрогеназы в эритроцитах вышеуказанными методами. При острых гепатитах динамика прооксидантных систем нейтрофилов отражает таковую клеток Купфера, а динамика антиоксидантных систем эритроцитов в целом соответствует таковой в гепатоцитах [73].
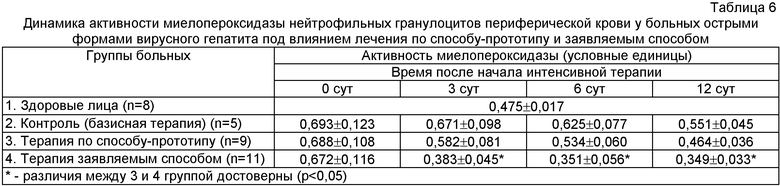
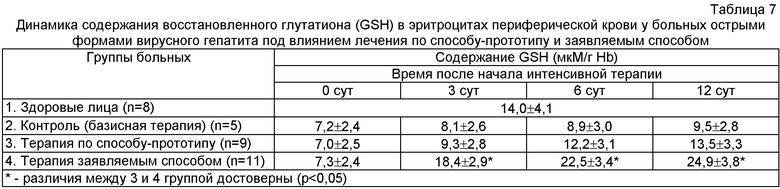
Полученные результаты представлены в таблицах 6, 7 и 8.
Как видно из представленных данных, реализация заявляемого способа лечения острых форм вирусных гепатитов сопровождается отчетливыми антиоксидантными эффектами, выражающимися в достоверном снижении активности прооксидантного энзима миелопероксидазы нейтрофилов и стимуляции антиперекисных факторов эритроцитов (содержание восстановленного глутатиона, активность каталазы и глюкозо-6-фосфатдегидрогеназы).
Продолжительность лечения в ОРИТ больных с острыми формами вирусных гепатитов при применении заявляемого способа составила 4,6±0,3 суток против 6,2±0,5 суток при лечении по способу-прототипу (p<0,05). Сроки дальнейшего лечения в стационаре при этом сократились с 27,2±3,5 суток (способ-прототип) до 17,6±2,9 суток (заявляемый способ) (p<0,05). В результате лечения острых форм вирусных гепатитов заявляемым способом экономические затраты снизились на 22 тыс. рублей.
Таким образом, применение заявляемого способа лечения острых форм вирусных гепатитов в лечебной практике инфекционных стационаров страны обеспечит высокую эффективность лечения больных с острыми формами вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D), позволит существенно сократить продолжительность лечения в ОРИТ и дальнейшего пребывания в стационаре, в результате чего добиться значительного снижения экономических затрат на лечение данной категории больных.
Заявляемое изобретение удовлетворяет критерию «новизна», так как впервые для лечения острых форм вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D) рекомендуется в дополнение к базисной терапии и введению перфторуглеродной эмульсии перфторан назначение фармакологических средств патогенетической терапии (новокаин, комплекс антиоксидантов и восстанавливающих их тиолов (аскорбиновая кислота, α-токоферол, N-ацетилцистеин, ретинол и унитиол), мексидол (эмоксипина сукцинат) и витамин D3).
Заявляемое изобретение удовлетворяет критерию «изобретательский уровень», так как из ранее известных свойств новокаина, аскорбиновой кислоты, α-токоферола, унитиола, N-ацетилцистеина, ретинола, мексидола и витамина D3 не вытекает с очевидностью возможность их комплексного использования для воздействия на различные звенья патологического процесса при острых вирусных гепатитах, то есть возможность применения данного комплекса фармакологических средств для лечения острых форм вирусного гепатитов В и микст-гепатитов (В+С, В+D, В+С+D).
Соответствие критерию «пригодность для промышленного применения» доказывается тем, что все лекарственные средства, рекомендуемые для реализации заявляемого способа лечения острых форм вирусного гепатита В и микст-гепатитов (В+С, В+D, В+С+D), выпускаются отечественной промышленностью в готовой к использованию форме и широко применяются в клинической практике при лечении различных категорий больных. Возможность применения заявляемого способа лечения острых форм вирусного гепатита В и микст-гепатитов (В+С, B+D, B+C+D) в клинической практике доказана результатами экспериментальных исследований на моделях острого гепатита и клинических испытаний при лечении больных с острыми формами вирусных гепатитов.
Источники информации
1. Bonkovsky H.L., Banner B.F., Rothman A.L. Iron and chronic viral hepatitis. Hepatology. 1997; 25(3): 759-768.
2. Всемирная организация здравоохранения. Шестьдесят вторая сессия Всемирной ассамблеи здравоохранения. Доклад секретариата: Вирусный гепатит. 16.04.2009. Документ А62/22.
3. Всемирная организация здравоохранения. 23.01.2010. Документ EB126/SR/13.
4. Thomas A.R., Zaman A., Bell В.Р. Deaths from chronic liver disease and viral hepatitis, Multnomah County, Oregon, 2000. J. Clin. Gastroenterol. 2007; 41(9): 859-862.
5. Приказ МЗ СССР от 12.07.1989 г. «О мерах по снижению заболеваемости вирусным гепатитом в стране».
6. Приказ Минздравсоцразвития РФ от 23.11.2004 г. №260 «Об утверждении стандарта медицинской помощи больным хроническим гепатитом В, хроническим гепатитом С».
7. Приказ Минздравсоцразвития РФ от 06.10.2005 г. №619 «Об утверждении стандарта медицинской помощи больным с хроническим активным гепатитом в сочетании с первичным склерозирующим холангитом».
8. Приказ Минздравсоцразвития РФ от 06.10.2005 г. №621 «Об утверждении стандарта медицинской помощи больным с хроническим активным гепатитом в сочетании с первичным биллиарным церрозом».
9. Приказ Минздравсоцразвития РФ от 13.10.2005 г. №634 «Об утверждении стандарта медицинской помощи больным с хроническим активным гепатитом в сочетании С хроническим гепатитом С».
10. Приказ Минздравсоцразвития РФ от 21.07.2006 г. №571 «Об утверждении стандарта медицинской помощи больным хроническим вирусным гепатитом».
11. А.с. СССР 1678373.
12. А.с. СССР 1685453.
13. Соринсон С.H. Вирусные гепатиты. СПб.: Теза. 1996; 314 с.
14. Соринсон С.H. Вирусные гепатиты в клинической практике. СПб.: Теза, 1996; С.69-191.
15. Вирусные гепатиты. Указания по диагностике, лечению и профилактике в ВС РФ. СПб. 1999. 155 с.
16. FR Patent 2305977.
17. US Patent 6635620.
18. FR Patent 2494113.
19. Радченко В.Г., Шабров A.B., Зиновьева Е.Н. Основы клинической гепатологии. СПб.: Диалект. 2005. 864 с.
20. Патент РФ 2293572.
21. Рейзис А.Р., Матанина Н.В. Урсодеоксихолевая кислота и ее применение при вирусных гепатитах у взрослых и детей. Клинич. персп. гастроэнтерол., гепатол. 2005; 6: 11-15.
22. US Patent 4868114.
23. Patent WO/2008/120070.
24. Патент РФ 2369403.
25. А.с. СССР 1680200.
26. А.с. СССР 1897828.
27. А.с. СССР 1885458.
28. Ивашкин В.Т., Маевская М.В. Новый шанс победить гепатит С.Клинич. перспек. гастроэнтерол., гепатолог. 2002; 2: 25-28.
29. Ивашкин В.Т. (Ред.) Болезни печени и желчевыводящих путей. М.: Изд. Дом М-Вести. 2002; 432 с.
30. Горбаков В.В., Абдуллаев Х.И., Раков А.Л., Урсов Р.Р. Современные представления о хронической HBV-инфекции. Эксперимент, клин, гастроэнтерол. 2003; 2: 54-60.
31. Perrillo R.P. Overview of treatment of hepatitis B: key approaches and clinical challenges. Simin. Liver Dis. 2004; 24(1): 23-29.
32. Gupta V., Jamil-Ul-Hussain, Vijay S. Hepatitis-B: recent treatment. JK Science. 2006; 8 (1): 9-13.
33. McHutchison J.G., Lawitz E.J., Shiffman M.L. et al. Peginterferon alpha-2b and alpha-2a with ribavirin for treatment of hepatitis С infection. N. Engl. J. Med. 2009; 361: 580-593.
34. National Institute of Health Consensus development conference statement: Management of hepatitis С 2002. Hepatology. 2002; 36 (5) Suppl.l.: 3-9.
35. Лобзин Ю.В., Жданов K.B., Волжанин В. М., Гусев Д.А. Вирусные гепатиты: клиника, диагностика, лечение. СПб.: Фолиант. 2003; 23 с.
36. Радченко В.Г., Зиновьева Е.Н., Соловьева О.М. и др. Побочные действия интерферонотерапии при лечении больных хроническими вирусными гепатитами. Актуальные вопросы внутренних болезней. СПб. 2004; С.29-44.
37. Петров В.А., Заболотная Г.А. Индукторы интерферона в лечении и профилактике вирусных инфекций. Новые лекарства и новости фармакотерапии. 2000; 8:7-12.
38. Патент РФ 2322975.
39. Патент РФ 2306934.
40. Патент РФ 2279280.
41. Koike К., Miyoshi Н. Oxidative stress and hepatic С viral infection. Hepatol. Res. 2006; 34: 65-73.
42. Riza E.A., Ayse E., Nucran B. et al. Change in plasma concentrations of lipid peroxidation products in patients with acute viral hepatitis. Turkish J. Gastroenterol. 1999; 10(1): 4-6.
43. Bonkovsky H., Banner В., Rothman A.L. Iron and chronic viral hepatitis. Hepatology. 1997; 25(3): 759-768.
44. Choi J., Ou J.-H. Mechanisms of liver injury. III. Oxidative stress in the pathogenesis of hepatitic С virus. Am. J. Physiol. Gastrointest. Liver Physiol. 2006; 290: G847-G951.
45. Beuttner G.R., Jurkiewicz B.A. Catalytic metals, ascorbate and free radicals: combination to avoid. Radiat. Res. 1996; 145: 532-541.
46. Lustbader E.D., Harm H.L., Blumberg B.S. Serum ferritin as a predictor of host response to hepatitis В virus infection. Science. 1983; 220:423-425.
47. Kakizaki S., Takagi H., Horiguchi N. et al. Iron enhances hepatitis С virus replication in cultured human hepatocytes. Liver. 2000; 20: 125-128.
48. Theurl I., Zoller H., Obrist P. et al. Iron regulates hepatitis С virus translation via stimulation of expression of translation initiation factor 3. J. Infect. Dis. 2004; 190: 819-825.
49. Van Thiel D.H., Friedlander L., Faginoli S. et al. Response to interferon alpha therapy is influenced by the iron content of the liver. J. Hepatol. 1994; 20:410-415.
50. Gabbay E., Zigmond E., Pappo O. et al. Antioxidant therapy for chronic hepatitis С after failure of interferon: Results of phase II randomized, double-blind placebo controlled clinical trial. World J. Gastroenterol. 2007; 13(40): 5317-5323.
51. Patent WO/2006/130532.
52. Патент РФ 2146133.
53. Светлов B.H., Палагин В.А. Применение перфторана при осложненных формах вирусного гепатита (предварительное сообщение). В кн.: физиологическая активность фторсодержащих соединений (эксперимент и клиника). Пущино. 1995:224-226.
54. Крылов Н.Н., Мороз Б.В., Белоярцев Ф.Ф. Применение фторуглеродного заменителя крови - перфторана - в клинике. Воен. - мед. журн. 1985; 8: 38-40.
55. Плужников Н.Н., Софронов Г.А. Фармакологическая коррекция состояния антиоксидантной системы организма. Патофизиология экстремальных состояний. СПб. 1993:108-113.
56. Плужников Н.Н., Лобзин Ю.В., Ковеленов А.Ю. и др. Иммунологические эффекты перфторана. Эксперим. и клин, фармакол. 1998; 61(5): 34-38.
57. Терешина Е.В., Афонин Н.Н., Новохатский А.С. Противовирусная активность эмульсий перфторорганических соединений. В кн.: Физиологически активные вещества на основе перфторуглеродов в экспериментальной и клинической медицине. СПб.: ВМедА. 1999: 90-91.
58. Инструкция по применению «Перфторана». Утверждена Фармакологическим комитетом МЗ РФ 24.08.1999 г.
59. Патент РФ 2132681.
60. Патент РФ 2116788.
61. Плужников Н.Н., Чиж С.И., Юзвинкевич Л.С. и др. Оксидативный стресс. Фундаментальные и прикладные проблемы. В кн.; Актуальные проблемы и перспективы развития военной медицины: Научн. тр. НИИЦ (МБЗ) ГНИИИВМ МО РФ. СПб. 2000; т.2: 193-223.
62. Патент РФ 2281092.
63. Патент РФ 2167638.
64. Плужников Н.Н., Бакунина Л.С., Легеза В.И. и др. Некоторые аспекты антирадикальной защиты биомембран. В кн.: Актуальные проблемы и перспективы развития военной медицины. Научн. тр. НИИЦ (МБЗ) ГНИИИВМ МО РФ. СПб.2003; т.4:123-139.
65. Tesoriere L., Bongiorno A., Pintaudi А.М. et al. Synergistic interactions between vitamin A and vitamin E against lipid peroxidation in phosphatidylcholine liposomes. Arch. Biochem. Biophys. 1996; 326(1): 57-63.
66. Верижникова E.B., Шоломов И.И., Дорошенко Л.М. Применение препарата «мексидол» в интенсивной терапии пациентов с мультиорганной недостаточностью. Бюлл. Эксперимент. Биол. Мед. 2006; прил.1: 104-107.
67. Лукьянова Л.Д. Биоэнергетическая гипоксия: понятие, механизмы и способы коррекции. Бюлл. Эксперимент. Биол. Мед. 1997; 124(9): 245-254.
68. Золотов Н.Н., Смирнов Л.Д., Кузьмина В.И. и др. Производные 3-оксипиридина как ингибиторы протеолитических ферментов. Хим.-фарм. журн. 1989; 23(2): 133-135.
69. Клебанов Г.И., Любицкий О.Б., Ильина С.Е. и др. Антиоксидантная активность ингибиторов свободнорадикальных реакций, используемых в перевязочном материале для лечения ран. Биол., Мед., Фармац. Химия. 2006; 52(1): 69-82.
70. Van Etten Е., Mathieu С.Immunoregulation by 1,25-dihydroxyvitarnin D3: basic concepts. J. Steroid. Biochem. Nol. Biol. 2005; 97(1-2): 93-101.
71. Schauber J., Dorschner R.A., Coda A.B. et al. Injury enhances TLR2 function and antimicrobial peptide expression through a vitamin D dependent mechanism. J. Clin. Invest. 2007; 117(3): 803-811.
72. Бакунина Л.С Фармакологическая коррекция проявлений оксидативного стресса при гнойно-воспалительных заболеваниях среднего уха (клинико-экспериментальное исследование): Дисс. … Доктора мед. наук. СПб., 2002; 260 с.
73. Бондаренко И.Г. Молекулярные механизмы формирования цитолиза в печеночной паренхиме при острых вирусных гепатитах: Дисс. … канд. мед. наук. Л., 1988; 135 с.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОМПЛЕКСНОЙ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ ОСТРЫХ ФОРМ ВИРУСНОГО ГЕПАТИТА В И МИКСТ-ГЕПАТИТОВ (В+С, В+D, В+С+D) | 2010 |
|
RU2440128C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ВИРУСНОГО ГЕПАТИТА B | 2001 |
|
RU2207135C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ГЕПАТИТА В ИЛИ С ТЯЖЕЛОГО ТЕЧЕНИЯ | 2015 |
|
RU2599037C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВИРУСНЫХ ГЕПАТИТОВ В И С | 2002 |
|
RU2217153C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ГЕПАТИТОВ B И C | 2002 |
|
RU2223070C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА | 2004 |
|
RU2265447C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ВИРУСНОГО ГЕПАТИТА В | 2003 |
|
RU2240824C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ГЕПАТИТА С И СПОСОБ ЛЕЧЕНИЯ ГЕПАТИТА С | 2010 |
|
RU2447899C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ВИРУСНОГО ГЕПАТИТА B | 1996 |
|
RU2122425C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ХРОНИЧЕСКИМ ВИРУСНЫМ ГЕПАТИТОМ C | 2002 |
|
RU2212248C1 |
Изобретение относится к медицине и предназначено для лечения больных острыми формами вирусного гепатита В и микст-гепатитов (В+С, B+D, B+C+D). Проводят базисную терапию. Вводят эмульсию перфторуглеродов перфторан внутривенно капельно. Доза 400 мл 1-2 раза в день в течение 2-3 дней, на курс 800-2400 мл. Дополнительно назначают следующий комплекс средств патогенетической терапии. Новокаин 0,5% р-р 20-25 мл внутривенно капельно один раз в день; аскорбиновая кислота 5% р-р 2 мл внутримышечно два раза в день; α-токоферол 10% масляный р-р 1 мл внутримышечно два раза вдень; унитиол в виде 5% раствора 5 мл внутримышечно два раза в день; N-ацетилцистеин 10 мг/кг внутрь два раза в день; ретинол по 5000 ME в капсулах внутрь после еды два раза в день; мексидол в виде 5% раствора 2 мл внутривенно. Продолжительность 10 дней. Способ позволяет повысить эффективность терапии, сократить сроки стационарного лечения, снизить экономические затраты. 1 з.п.ф-лы, 2 пр., 8 табл.
1. Способ лечения острых форм вирусного гепатита В и микст-гепатитов В+С, B+D, B+C+D, включающий базисную терапию и назначение перфторуглеродной эмульсии перфторан внутривенно капельно в дозе по 400 мл 1-2 раза в день в течение 2-3 дней при дозе перфторана на курс, составляющей 800-2400 мл в зависимости от массы тела и тяжести состояния больного, отличающийся тем, что дополнительно к базисной терапии и введению перфторана назначают следующие фармакологические средства патогенетической терапии:
- новокаин в виде 0,5%-ного раствора в дозе 20-25 мл (из расчета 1,5 мг/кг) внутривенно капельно один раз в день;
- аскорбиновую кислоту в виде 5%-ного раствора в дозе 2 мл внутримышечно два раза в день;
- α-токоферол в виде 10%-ного масляного раствора в дозе 1 мл внутримышечно два раза в день;
- унитиол в виде 5%-ного раствора в дозе 5 мл внутримышечно два раза в день;
- N-ацетилцистеин в дозе из расчета 10 мг/кг внутрь два раза в день;
- ретинол по 5000 ME в капсулах внутрь после еды два раза в день;
- мексидол в виде 5%-ного раствора в дозе 2 мл внутривенно два раза в день;
- витамин D3 по 1000 МБ внутрь два раза в день.
2. Способ лечения острых форм вирусного гепатита В и микст-гепатитов В+С, B+D, B+C+D по п.1, отличающийся тем, что фармакологические средства патогенетической терапии назначают в течение 10 дней.
| RU 98121034, 10.09.2000 | |||
| DE 4447588, 20.11.1997 | |||
| СВЕТЛОВ В.Н | |||
| и др | |||
| Применение Перфторана при осложненных формах вирусного гепатита (предварительное сообщение), «Физиологическая активность фторсодержащих соединений, эксперимент и клиника» | |||
| Пущино, 1995, с.224-226 | |||
| Общая терапия | |||
| Гепатиты, текстовый документ, официальный сайт РГМУ, 2002, |
Авторы
Даты
2012-04-10—Публикация
2010-03-25—Подача