ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к агенту десульфуризации для жидкофазной адсорбционной десульфуризации и к способу десульфуризации, который использует агент десульфуризации.
УРОВЕНЬ ТЕХНИКИ
С точки зрения предотвращения загрязнения окружающей среды, улучшения эффективности использования топлива для двигателей, адаптирования системы топливного элемента для транспортных средств в будущем и тому подобного, имеется потребность в дальнейшем уменьшении концентрации серы в жидких топливах, таких как бензин, керосин, легкий газойль и тому подобное. Соответственно, установление технологий для десульфуризации жидких топлив является важной проблемой.
Хотя так называемое не содержащее серы топливо, имеющее концентрацию серы примерно 10 млн.д., уже поставляется в качестве коммерческого продукта, в настоящее время имеется потребность в технологии для дальнейшего уменьшения концентрации серы. В частности, рассматривается необходимость того, что концентрация серы в топливе для топливных элементов составляет 0,1 млн.д. или меньше. Заметим, что в настоящем описании выражение "млн.д." для концентрации серы указывает млн.д. массовые. 1 млн.д. относится к случаю, когда 1 мкг серы содержится в виде элемента в 1 г жидкого нефтяного топлива.
В качестве способа уменьшения концентрации серы в жидком топливе, в способе получения жидкого топлива используют исключительно способ гидродесульфуризации, который использует катализатор на основе кобальта-молибдена. Однако среди различных соединений серы, содержащихся в жидком топливе, дибензотиофен имеет относительно низкую химическую активность при гидрировании и, таким образом, имеет отрицательную тенденцию оставаться в жидком топливе даже после обработки гидродесульфуризацией. В частности, 4,6-диметилдибензотиофен и тому подобное, имеющие алкильные группы рядом с атомом серы дибензотиофена, имеют плохую химическую активность на поверхности катализатора из-за стерического затруднения и считаются соединениями, которые сложно удалить. Соответственно, делаются попытки улучшить катализаторы гидродесульфуризации, и другие способы, такие как окислительная десульфуризация и адсорбционная десульфуризация, также исследуются в настоящее время.
Способ жидкофазной адсорбционной десульфуризации представляет собой способ адсорбирования и удаления соединения серы посредством создания контакта между жидким топливом и агентом десульфуризации, при этом способ может осуществляться с помощью простого устройства. Однако после того как агент десульфуризации достигает адсорбционного насыщения, десульфуризация не может больше осуществляться, и после замены используемый адсорбент не может использоваться повторно. Это создает проблему генерирования большого количества промышленных отходов. Таким образом, желательной является регенерация и повторное применение используемых агентов десульфуризации; однако по отношению к агентам адсорбционной десульфуризации для тиофеновых соединений нет известных агентов, которые могут удовлетворять таким свойствам.
Материалы, которые в настоящее время считаются возможными агентами для жидкофазной адсорбционной десульфуризации, могут классифицироваться на четыре категории: материал на основе активированного угля, материал на основе оксида металла, материал на основе цеолита и материал на основе металла (см. NPL 1). Из них активированный уголь может широко использоваться в качестве распространенного адсорбента. Его удельная площадь поверхности является очень большой (1000 м2/г или более), и он имеет хорошую способность к адсорбированию органических материалов в целом; однако селективной адсорбции при исключительном адсорбировании органических материалов, содержащих серу, ожидать нельзя. Кроме того, хотя термическая регенерация активированного угля осуществляется повсеместно, часть самого активированного угля, к сожалению, разлагается во время регенерации. Если протоколы обеспечения безопасности являются неадекватными, активированный уголь может возгореться, и может произойти случайное отравление из-за образования монооксида углерода во время разложения адсорбируемого вещества.
Материалы, такие как оксид железа, оксид цинка и тому подобное, вводятся в практическое использование как агенты десульфуризации на основе оксидов, поскольку они адсорбируют сероводород. Однако ни один из них, согласно сообщениям, не демонстрирует достаточных рабочих характеристик в качестве агента для адсорбирования соединений серы на основе тиофенов.
Агенты десульфуризации на основе цеолитов имеют большую удельную площадь поверхности (500 м2/г или более), являются термически стойкими и имеют свойства, которые могут легко изменяться посредством модификации, такой как ионный обмен и тому подобное. Соответственно, использование агентов десульфуризации на основе цеолитов, в качестве агентов адсорбционной десульфуризации, является объектом исследования. Например, цеолит Y-типа, подвергаемый ионному обмену с Cu или Ce (Cu-Y, Ce-Y), как сообщается, должен быть пригодным для использования в качестве адсорбента для соединений на основе тиофенов (см. PTL 2 и 3 ниже). Однако о способе регенерации адсорбентов после десульфуризации никогда не сообщалось. Эксперименты авторов настоящего изобретения подтверждают, что регенерация и повторное использование адсорбентов не могут быть достигнуты с помощью обычной операции нагрева.
По отношению к агентам десульфуризации на основе металлов, те типы соединений серы, которые могут эффективно адсорбироваться и удаляться, являются различными, в зависимости от типов используемых металлов, и известно, что агенты десульфуризации на основе Ni демонстрируют превосходные рабочие характеристики для соединений на основе тиофенов. Однако операция десульфуризации с использованием агента десульфуризации на основе Ni является очень сложной, поскольку адсорбция должна осуществляться при нагреве до температуры примерно 200°C после того, как агент подвергается восстановлению водородом при высоких температурах и специальной стабилизационной обработке. Кроме того, после того как Ni образует стабильный сульфид, регенерация является очень сложной (см. PTL 1 ниже).
Материал, для которого наночастицы благородных металлов наносятся на поверхность оксида металла в качестве носителя, как известно, имеет высокую активность при различных химических реакциях и используется в качестве катализатора для различных химических реакций. Известно, что когда используется такой катализатор на основе благородного металла, соединение серы обычно адсорбируется на активном центре катализатора на основе благородного металла и становится ядом для катализатора. Соответственно, имеется немного сообщений об исследовании катализаторов на основе благородных металлов, таких как Pt, Pd и тому подобное, для цели десульфуризации, по сравнению с количеством сообщений о катализаторе на основе кобальта-молибдена. Однако недавнее сообщение показывает, что система, в которой платину наносят, например, на цеолит, демонстрирует активность при гидродесульфуризации (см. NPL 4 ниже). Кроме того, хотя имеется сообщение о попытке регулировать рабочие характеристики платинового катализатора при гидродесульфуризации посредством добавления к нему золота, о материале, содержащем только золото в качестве благородного металла, никогда не сообщалось как о катализаторе десульфуризации.
Среди соединений серы алкантиолы (RSH) являются особенно известными как регулярно адсорбирующиеся на поверхности золота и образующие самособирающийся монослой (SAM). Со временем сообщения Gao et al. в 1995 г. об образовании SAM полиалкилтиофеном (см. NPL 5 ниже), множество исследователей также подтверждают экспериментально, что тиофен образует SAM. Поскольку тиофеновый полимер мог бы использоваться как проводящий полимер для электронных устройств и тому подобное, это становится активной областью исследования. По отношению к простому тиофену или алкилтиофену явление адсорбции на поверхности Au и это применение исследовались, как описано выше. Однако монокристаллы Au используются исключительно для целей использования монослоя в качестве SAM, и они не используются в качестве агентов адсорбционной десульфуризации, поскольку величина адсорбции является малой. Нет никаких сообщений об адсорбции дибензотиофеновых соединений, которые являются важными в качестве объектов для десульфуризации жидкого топлива.
СПИСОК ЛИТЕРАТУРЫ
Патентная литература
PTL 1: Публикация нерассмотренной заявки на патент Японии № 11-169601.
Непатентная литература
NPL 1: Japan Petroleum Energy Center, Engineering Planning Division, PETROTECH, 11(2005), pp. 835-840.
NPL 2: Osamu Chiyoda, Shokubai (Catalysts & Catalysis), 47 (2005), p. 568.
NPL 3: M. Xue et al., J. Colloid Interf. Sci., 298 (2006), pp. 535-542.
NPL 4: M. Sugioka et al., J. Jpn. Petrol. Inst., 45 (2002), pp. 342-354.
NPL 5: Z. Gao et al., Synthetic Metalls, 75 (1995), pp. 5-10.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая проблема
Настоящее изобретение проделано с точки зрения описанных выше обычных технических проблем. Его главной задачей является создание агента для десульфуризации посредством жидкофазной адсорбции, который является эффективным для соединений серы, содержащихся в жидком топливе. Более конкретно, оно предусматривает новый агент десульфуризации, где агент может удалять соединения серы на основе тиофенов, которые сложно удалять в достаточной степени с помощью обычных способов, до такой степени, что концентрация серы ниже, чем 10 млн.д., и агент может затем делаться повторно используемым с помощью простого способа после обработки десульфуризацией.
Решение проблемы
Авторы настоящего изобретения осуществили широкие исследования для достижения описанной выше задачи. В результате они обнаружили, что оксид металла, на который наносятся наночастицы золота, который известен в качестве катализатора для различных химических реакций, действует в качестве адсорбента с хорошей селективностью для органических соединений, содержащих серу в жидком топливе. В частности, они обнаружили, что соединения серы на основе тиофенов, которые сложно удалять с помощью обычных способов до такой степени, когда их концентрация является достаточно низкой, также могут адсорбироваться и удаляться до такой степени, когда их концентрация является достаточно низкой. Кроме того, они обнаружили, что после адсорбционной обработки адсорбированные соединения серы могут эффективно удаляться с помощью простой термической обработки, и таким образом, катализатор может повторно использоваться в качестве адсорбента. Настоящее изобретение осуществляется на основе этих данных.
Конкретно, настоящее изобретение предусматривает агент десульфуризации для жидкофазной адсорбционной десульфуризации и способ десульфуризации с использованием агента десульфуризации, как описано ниже.
1. Агент десульфуризации для жидкофазной адсорбционной десульфуризации, содержащий оксид металла с нанесенными на него наночастицами золота, имеющими средний размер частиц 50 нм или меньше.
2. Агент десульфуризации в соответствии с пунктом 1, который имеет удельную площадь поверхности 1 м2/г или более.
3. Агент десульфуризации жидкофазной адсорбционной десульфуризации, где оксид металла с нанесенными на него наночастицами золота в соответствии с пунктом 1 фиксируется на элементе носителя.
4. Агент десульфуризации в соответствии с пунктом 1, где целью обработки является жидкое топливо, содержащее органическое соединение, содержащее серу.
5. Способ десульфуризации, включающий приведение агента десульфуризации в соответствии с пунктом 1 в контакт с жидкостью, содержащей органическое соединение, содержащее серу.
6. Способ десульфуризации в соответствии с пунктом 5, где целью обработки является жидкое топливо, содержащее органическое соединение, содержащее серу.
7. Способ десульфуризации в соответствии с пунктом 6, где жидкое топливо, служащее в качестве объекта обработки, содержит органическое соединение, содержащее тиофеновое кольцо.
8. Способ десульфуризации в соответствии с пунктом 7, где органическое соединение, содержащее тиофеновое кольцо, представляет собой, по меньшей мере, одно соединение, выбранное из группы, состоящей из соединений дибензотиофена и алкилдибензотиофена.
9. Способ регенерирования агента десульфуризации, включающий термическую обработку агента десульфуризации после обработки десульфуризацией, осуществляемой с помощью способа в соответствии с пунктом 5, для удаления органического соединения, содержащего серу, адсорбированного на агенте десульфуризации.
10. Способ десульфуризации, включающий приведение агента десульфуризации, который подвергается обработке регенерацией с помощью способа в соответствии с пунктом 9, в контакт с жидкостью, содержащей органическое соединение, содержащее серу, с помощью способа в соответствии с пунктом 5.
Агент десульфуризации по настоящему изобретению, способ его получения и способ его использования подробно описываются ниже.
Агент десульфуризации
Агент десульфуризации по настоящему изобретению имеет структуру, в которой наночастицы золота, имеющие средний размер частиц 50 нм или меньше, наносятся на оксид металла.
Оксид металла с нанесенными на него наночастицами золота, описанный выше, как известно, демонстрирует высокую активность в качестве катализатора для различных химических реакций, включая окислительное удаление монооксида углерода или формальдегида; понижение уровня NOx в выхлопных газах углеводородов; реакцию синтеза метанола посредством гидрирования монооксида углерода или диоксида углерода; реакцию конверсии водяного пара, в которой диоксид углерода и водород генерируются из монооксида углерода и воды; реакцию синтеза пропиленоксида посредством селективного окисления пропилена; и тому подобное. Однако действие селективной адсорбции оксида металла на соединения серы в жидкой фазе является неизвестным.
В соответствии с настоящим изобретением теперь обнаружено, что материал, имеющий описанную выше структуру, в которой наноразмерные мелкодисперсные частицы золота наносятся на оксид металла, имеет действие селективной адсорбции на различные органические соединения, содержащие серу, в жидкой фазе, и что такой материал является эффективным в качестве агента десульфуризации.
Агент десульфуризации по настоящему изобретению предпочтительно имеет структуру, в которой наноразмерные частицы золота однородно нанесены на поверхность носителя на основе оксида металла. Частицы золота, нанесенные на оксид металла, находятся в наноразмерном, то есть в ультрамелкодисперсном состоянии. Соответственно, площадь поверхности золота, необходимая для адсорбции, является очень большой и позволяет демонстрировать превосходные рабочие характеристики адсорбции. Кроме того, активный центр для горения, необходимый для регенерации адсорбента после десульфуризации, как считается, формируется на границе связывания между золотом и оксидом металла, и, таким образом, размер частицы предпочтительно является настолько малым, насколько это возможно для создания настолько большого количества центров связывания, насколько это возможно. Конкретно, средний размер частиц для частиц золота может находиться в пределах от размера атома золота примерно до 50 нм, предпочтительно, примерно от 1 до 10 нм. Заметим, что в настоящем описании средний размер частиц для частиц золота представляет собой среднее для значений, измеренных с помощью способа с использованием трансмиссионного электронного микроскопа, или представляет собой размер кристаллитов золота, вычисленный с помощью уравнения Шеррера по данным измерений рентгеноструктурного анализа. Эти значения, как подтверждено, являются по существу одинаковыми в случае катализатора на основе наночастиц золота.
Оксиды, которые содержат следующие элементарные металлы, могут использоваться, например, в качестве оксида металла с нанесенными на него частицами золота: бериллий, магний, алюминий, кремний, кальций, скандий, титан, ванадий, хром, марганец, железо, кобальт, никель, медь, цинк, галлий, германий, стронций, иттрий, цирконий, кадмий, индий, олово, барий, лантаноидные элементы и тому подобное. Эти оксиды металлов могут представлять собой оксиды одного металла, в которых содержится только один из указанных выше элементарных металлов; или смешанные оксиды, в которых содержатся два или более из указанных выше элементарных металлов. Среди этих оксидов металлов оксид металла, содержащий один или несколько элементарных металлов, выбранных из титана, марганца, железа, кобальта, никеля, цинка, циркония, лантана, церия и тому подобного, является особенно предпочтительным. Описанные выше оксиды одного металла и смешанные оксиды могут также смешиваться для использования при необходимости. Заметим, что, когда используется любой элемент из бериллия, магния, кальция, стронция и бария, которые представляют собой элементы Группы 2 периодической системы, агент десульфуризации может также содержать гидроксид, основной карбонат и тому подобное, в дополнение к соответствующему оксиду, в зависимости от способа получения. В настоящем изобретении "оксид", на который нанесено золото в форме наночастиц, может включать их гидроксид, основной карбонат и тому подобное.
В агенте десульфуризации по настоящему изобретению, содержащем оксид металла с нанесенными на него наночастицами золота, содержание золота в нем не является как-либо ограниченным постольку поскольку агент десульфуризации может быть приготовлен таким образом, что золото может поддерживаться в состоянии наночастиц. Например, посредством соответствующего выбора оксида металла, используемого в качестве носителя, и способа получения, можно получить агент десульфуризации, имеющий содержание золота примерно от 0,1 до 60% мас., по отношению к общей массе наночастиц золота и оксида металла.
Форма агента десульфуризации по настоящему изобретению, то есть оксида металла, с нанесенными на него наночастицами золота, может выбираться соответствующим образом в соответствии с целью его использования. Например, он может использоваться в форме порошка. Он может также использоваться посредством формирования его в гранулированной форме, в форме таблеток и тому подобном. Кроме того, он может использоваться в форме продукта на подложке посредством фиксирования оксида металла, с нанесенными на него наночастицами золота, на элементе носителя. Форма элемента носителя не является как-либо ограниченной постольку поскольку оксид металла с нанесенными на него наночастицами золота, на его поверхности, может фиксироваться на элементе носителя. Элемент носителя может находиться в любой форме, такой как плоская форма, параллелепипед, волокно, сетка, сфера, соты и тому подобное. Например, когда элемент носителя используют в форме сот, агент десульфуризации, приготовленный в форме порошка, может приклеиваться к поверхности структуры сот для использования, или оксид может фиксироваться на поверхности структуры сот заранее, и наночастицы золота могут непосредственно наноситься на эту поверхность с использованием описанного ниже способа отложения-осаждения или чего-либо подобного. Материал элемента носителя также не является как-либо ограниченным постольку, поскольку он является стабильным при условиях, при которых наносятся наночастицы золота, и при условиях десульфуризации. Например, может использоваться различная керамика.
Удельная площадь поверхности оксида металла в состоянии, в котором на него наносятся наночастицы золота, предпочтительно составляет примерно от 1 до 2000 м2/г, более предпочтительно примерно от 5 до 1000 м2/г, как величина, измеренная с помощью способа БЭТ. Для получения такого оксида, с нанесенными наночастицами золота, может использоваться оксид металла, имеющий достаточную удельную площадь поверхности, в описанных выше пределах, например, для нанесения на него наночастиц золота.
Способ изготовления агента десульфуризации
Способ нанесения золота в виде наноразмерных частиц на оксид металла не является как-либо ограниченным. Например, могут использоваться следующие известные способы получения.
(a) Способ совместного осаждения (публикация нерассмотренной заявки на патент Японии № 60-238148, и тому подобное).
(b) Способ отложения-осаждения (публикация нерассмотренной заявки на патент Японии № 3-97623, и тому подобное).
(c) Способ коллоидного смешивания (Tsubota S. et al., Catal. Lett., 56 (1998), p. 131).
(d) Газофазная прививка (публикация нерассмотренной заявки на патент Японии № 9-122478).
(e) Жидкофазная прививка (Okumura M. et al., Chem. Lett., (2000), p. 396).
В описанных выше способах, водорастворимые соединения золота (например, золотохлористоводородная кислота), соединения, которые испаряются при нагреве, такие как комплекс ацетилацетоната золота, и тому подобное, могут использоваться в качестве предшественника золота для осаждения мелкодисперсных частиц золота в соответствии с используемым способом.
Например, нитратные соли, сульфаты, ацетаты, хлориды и тому подобное различных металлов могут использоваться в качестве исходных материалов для оксида металла в соответствии с используемым способом нанесения. Конкретно, могут использоваться нитратные соли, такие как нитрат церия, нитрат циркония, и тому подобное; сульфаты, такие как сульфат титана, и тому подобное; и хлориды, такие как хлорид церия, трихлорид титана, тетрахлорид титана, и тому подобное.
В способе совместного осаждения (a), сначала, предшественник оксида и предшественник золота одновременно осаждают в щелочных условиях. Затем, полученный таким образом осадок смеси гидроксида золота и гидроксида предшественника оксида фильтруют, промывают водой, сушат и подвергают термической обработке, как описано ниже, получая при этом оксид с нанесенными на него наночастицами золота.
В способах получения (b)-(e), предшественник оксида должен формироваться в виде оксида или гидроксида до нанесения золота. С самого начала может использоваться коммерчески доступный оксид или гидроксид. Его форма не является как-либо ограниченной. Может использоваться продукт в форме порошка, сфер, гранул или сот. Оксид необязательно может представлять собой оксид, имеющий однородный состав, и может также использоваться продукт, например, в котором оксид титана покрывает поверхность керамической сотовой структуры. Предшественник золота наносят с помощью способов (b)-(e) на поверхность оксида или гидроксида, как описано выше, с последующим фильтрованием, промывкой водой и сушкой, если это необходимо. Затем, продукт подвергают термической обработке, получая при этом оксид с нанесенными на него наночастицами золота.
В случае способа совместного осаждения и способа отложения-осаждения, среди описанных выше способов получения, добавление цитрата магния в течение получения является эффективным при уменьшении размера частиц золота, как описано, например, в публикациях нерассмотренных заявок на патент Японии №№ 5-325 и 6-29137. Этот способ используется особенно эффективно, когда наносится большое количество золота.
В описанных выше известных способах получения, для конечного преобразования золота в металлическое состояние, термическая обработка может осуществляться в различных атмосферах, например в атмосфере, содержащей кислород, в атмосфере восстанавливающего газа, в атмосфере инертного газа и тому подобное. В качестве атмосферы, содержащей кислород, может использоваться атмосфера воздуха или атмосфера смешанного газа, в которой кислород разбавляется азотом, гелием, аргоном или чем-либо подобным. В качестве восстанавливающего газа может использоваться, например, примерно 1-10% объемных газообразного водорода, газообразного монооксида углерода, и тому подобное, разбавленного газообразным азотом, и тому подобное. В качестве инертного газа может использоваться, например, азот, гелий, аргон, и тому подобное.
Температура термической обработки может соответствующим образом выбираться из диапазона известных условий для получения металлического золота и обычно, предпочтительно, находится в пределах примерно от комнатной температуры примерно до 600°C. Диапазон примерно от 200°C до 400°C является более предпочтительным для получения стабильных и мелкодисперсных частиц золота. Время термической обработки может составлять, например, примерно от 1 до 12 часов.
Объект обработки десульфуризации
Агент десульфуризации по настоящему изобретению может применяться в способе адсорбирования и удаления различных органических соединений, содержащих серу в жидкой фазе. Примеры таких органических соединений, содержащих серу, включают тиол (R-SH), сульфид (R-S-R), дисульфид (R-S-S-R), тетрагидротиофен, соединения на основе тиофена и тому подобное. Термин "соединения на основе тиофена", используемый в настоящем документе, относится к группе соединений, имеющих тиофеновое кольцо. Примеры их включают тиофен, алкилтиофен, бензотиофен, алкилбензотиофен, дибензотиофен, алкилдибензотиофен, диалкилдибензотиофен и тому подобное.
Агент десульфуризации по настоящему изобретению эффективно используется для адсорбционной десульфуризации органического соединения, содержащего серу, в частности соединения на основе тиофена, остающегося в жидком топливе. Соединение на основе тиофена, такое как 4,6-диметилбензотиофен, у которого концентрация серы не может быть уменьшена ниже 10 млн.д. с помощью обычного способа, может адсорбироваться и удаляться до такой степени, когда концентрация серы станет ниже чем 10 млн.д., с использованием агента десульфуризации по настоящему изобретению.
Тип жидкого топлива, которое должно обрабатываться, не является как-либо ограниченным и может представлять собой любое топливо из бензина, керосина, осветительного масла, легкого газойля, тяжелой нефти и тому подобное. Концентрация серы, содержащейся в жидком топливе до обработки, также не является как-либо ограниченной; однако, с точки зрения того факта, что будет необходимо большое количество агента десульфуризации, когда непосредственно обрабатывается жидкое топливо, имеющее высокую концентрацию серы, концентрация серы предпочтительно заранее понижается до 50 млн.д. или меньше, более предпочтительно до 10 млн.д. или меньше, с помощью такого способа, как гидродесульфуризация и тому подобное.
Способ десульфуризации
С помощью способа десульфуризации, который использует агент десульфуризации по настоящему изобретению, десульфуризация может осуществляться посредством приведения жидкости, которая должна быть десульфуризована, например жидкого топлива, в контакт с агентом десульфуризации и тем самым адсорбирования органического соединения, содержащего серу в жидкости. Имеются два распространенных способа: загрузочная технология и проточная технология.
С помощью загрузочной технологии может использоваться, например, способ добавления агента десульфуризации в контейнер, содержащий жидкое топливо, и перемешивание смеси. Хотя адекватное количество агента десульфуризации, которое должно использоваться, изменяется в зависимости от типа агента десульфуризации, агент десульфуризации, например, предпочтительно используется в пределах от 1 до 500 г на литр жидкого топлива, а более предпочтительно, используется в пределах от 10 до 100 г на литр жидкого топлива. Температура обработки не является как-либо ограниченной постольку, поскольку она поддерживается в таких пределах, где топливо, которое должно обрабатываться, может поддерживать свое жидкое состояние. Например, обработка может осуществляться при комнатной температуре. Давление также не является как-либо ограниченным. Хотя обработка может осуществляться при повышенном давлении, обычно она может осуществляться при атмосферном давлении.
По прохождении определенного периода времени после добавления агента десульфуризации, жидкость и агент десульфуризации разделяются, и при этом могут быть получены агент десульфуризации и жидкость, имеющая пониженное количество органических соединений, содержащих серу. Хотя время обработки нельзя определить в общем виде, поскольку оно изменяется в зависимости от концентраций соединений серы и количества используемого агента десульфуризации, обработка может осуществляться, например, в пределах примерно от 1 часа до нескольких дней, пока не будет получен желаемый эффект десульфуризации.
Отделенный агент десульфуризации может регенерироваться, например, с помощью описанного ниже способа, в котором агент десульфуризации сушат, а затем нагревают на воздухе, и использоваться повторно.
В случае проточной технологи жидкость, которая должна обрабатываться, может проходить при постоянной скорости потока через трубчатый контейнер, в котором агент десульфуризации размещают в форме слоя. Объемная часовая скорость жидкой фазы (LHSV) в этом случае может устанавливаться, например, в пределах примерно от 0,01 до 100 час-1, предпочтительно примерно от 0,01 до 1 час-1. Условия, такие как температура, давление и тому подобное, для десульфуризации не являются как-либо ограниченными, постольку, поскольку они находятся в пределах, где топливо представляет собой жидкость, как и в случае загрузочной технологии. Когда нет внешнего источника тепла, обработка может осуществляться при комнатной температуре. Когда жидкое топливо подается в предварительно нагретом состоянии, адсорбционная десульфуризация может осуществляться при температуре предварительного нагрева.
Способ регенерации
После того как жидкость десульфуризуют путем адсорбирования органического соединения, содержащего серу, в жидкости в соответствии с рассмотренным выше способом агент десульфуризации подвергают термической обработке, удаляя тем самым органическое соединение, содержащее серу, адсорбированное на агенте десульфуризации, и делая возможными регенерацию и повторное использование агента десульфуризации. Заметим, что по отношению к термической обработке агента десульфуризации, агент десульфуризации предпочтительно нагревают после промывки растворителем или чем-то подобным и сушат, если это необходимо.
Термическая обработка может осуществляться в различных атмосферах, таких как инертный газ, разбавленный кислород, воздух, водяной пар, разбавленный водород и тому подобное.
Оксид металла с нанесенными на него наночастицамии золота, который составляет агент десульфуризации по настоящему изобретению, как известно, имеет каталитическую активность для любой из следующих реакций: реакция между O2 и углеводородом, таким как метан, пропан и тому подобное (реакция горения); реакция между H2O и соединением углерода, таким как CO и тому подобное (реакция конверсии); и реакция между H2 и соединением углерода, таким как CO, CO2, альдегид и тому подобное (реакция гидрирования). Соответственно, осуществление термической обработки в атмосфере, содержащей любой газ из O2, H2O, и H2, позволяет эффективное удаление адсорбированного органического соединения, содержащего серу, посредством использования реакции, такой как каталитическая реакция, между этими молекулами и органическим соединением, содержащим серу, которое адсорбируется на поверхности агента десульфуризации, или реакции горения органического соединения, содержащего серу.
Диапазон концентраций O2, H2O, H2 и тому подобного в атмосфере не является как-либо ограниченным; однако, в особенности, когда содержится H2, концентрация должна регулироваться так, чтобы не образовывалась взрывчатая композиция. По отношению к условиям давления может использоваться обычное давление в случае реакции горения. Однако, в случае реакции гидрирования или чего-либо подобного, приложение давления 10 МПа или меньше может благоприятно ускорить реакцию. Температура нагрева может выбираться из диапазона примерно от 50°C до 500°C, предпочтительно примерно от 100°C до 400°C, более предпочтительно примерно от 150°C до 400°C. Когда температура нагрева является слишком высокой, наночастицы золота легко агрегируют, вызывая неблагоприятное ухудшение рабочих характеристик адсорбции после регенерации.
[Преимущественные эффекты изобретения]
Агент десульфуризации по настоящему изобретению имеет действие селективной адсорбции на органические соединения, содержащие серу, в жидкой фазе. В частности, концентрация соединения серы в жидком топливе может понижаться до уровня, который не может быть достигнут с помощью обычных технологий.
Агент десульфуризации по настоящему изобретению может использоваться при различных применениях посредством использования превосходных рабочих характеристик для адсорбционного удаления органического соединения, содержащего серу, как описано выше. Например, после понижения концентрации органического соединения, содержащего серу, посредством использования обычного способа гидродесульфуризации, органическое соединение, содержащее серу, адсорбируется и удаляется с использованием адсорбционной колонны, заполненной агентом десульфуризации по настоящему изобретению. Таким путем, концентрация серы в жидком топливе может понижаться до 10 млн.д. или меньше. Кроме того, концентрация серы может также понижаться до 0,1 млн.д. или меньше, то есть до концентрации, желаемой для топлива для топливного элемента.
Кроме того, в качестве примера того, как использовать настоящее изобретение, таким же способом, как описано в описанном выше NPL 1, колонна, заполненная агентом десульфуризации по настоящему изобретению, может устанавливаться между топливным танком и бензиновым насосом на заправочной станции, с тем чтобы осуществлять десульфуризацию, в то же время подавая топливо в транспортное средство.
Краткое описание чертежей
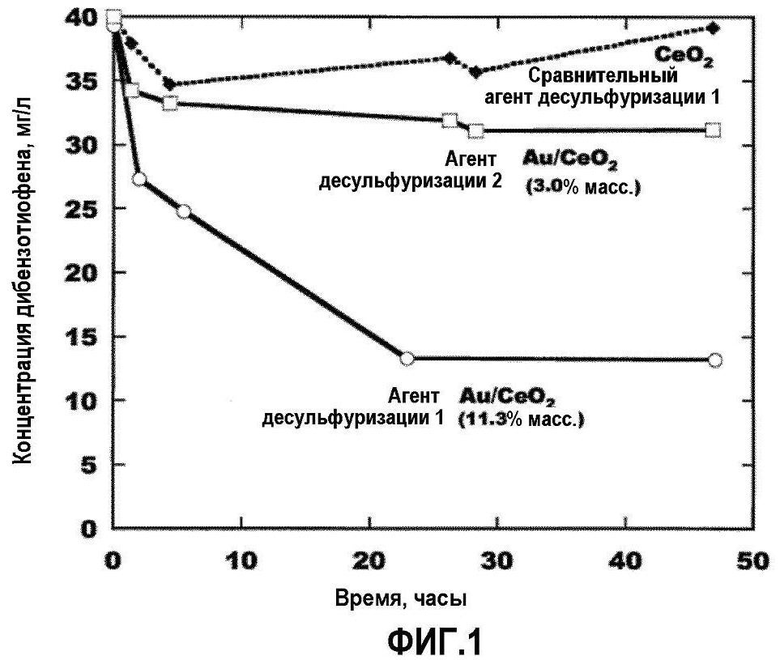
[Фиг.1] Фиг.1 представляет собой график, показывающий временной ход изменения концентрации дибензотиофена в растворе в Примере исследования 1.
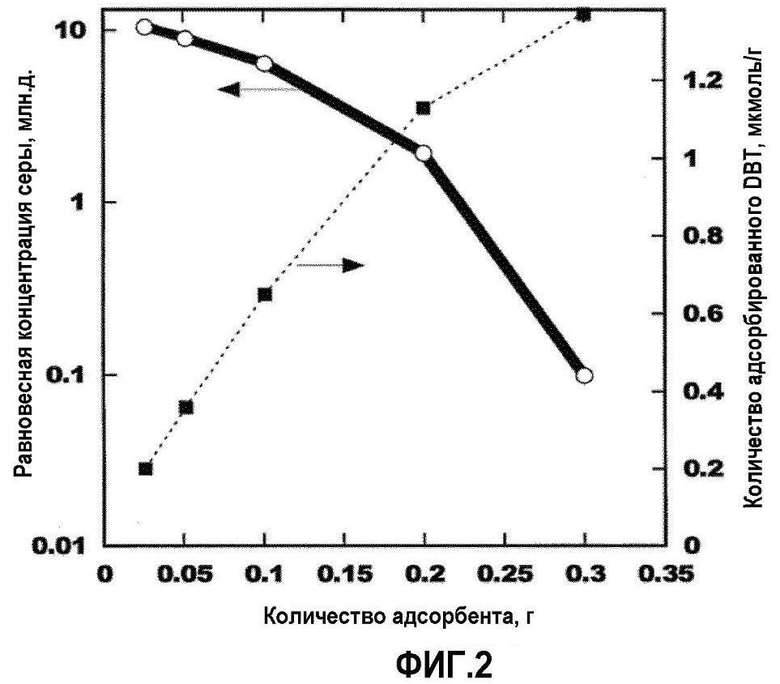
[Фиг.2] Фиг.2 представляет собой график, показывающий концентрацию серы (преобразованную из аналитического значения концентрации дибензотиофена), которая остается в растворе после достижения адсорбционного равновесия, и количество дибензотиофена, адсорбируемого на агенте десульфуризации, когда количество агента, используемого для десульфуризации, изменяется, в Примере исследования 2.
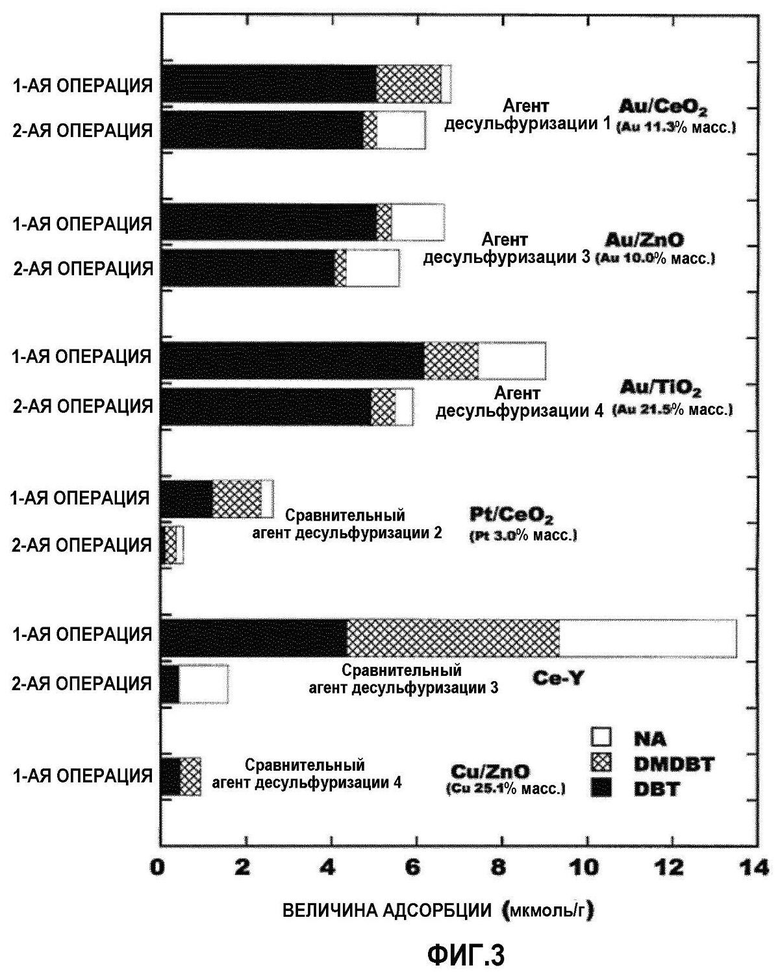
[Фиг.3] Фиг.3 представляет собой диаграмму, показывающую величину насыщения адсорбции дибензотиофена (DBT), 4,6-диметилдибензотиофена (DMDBT) и нафталина (NA), полученную посредством первой операции адсорбции (перед регенерацией) и второй операции адсорбции (после регенерации) с использованием каждого образца в Примере исследования 3.
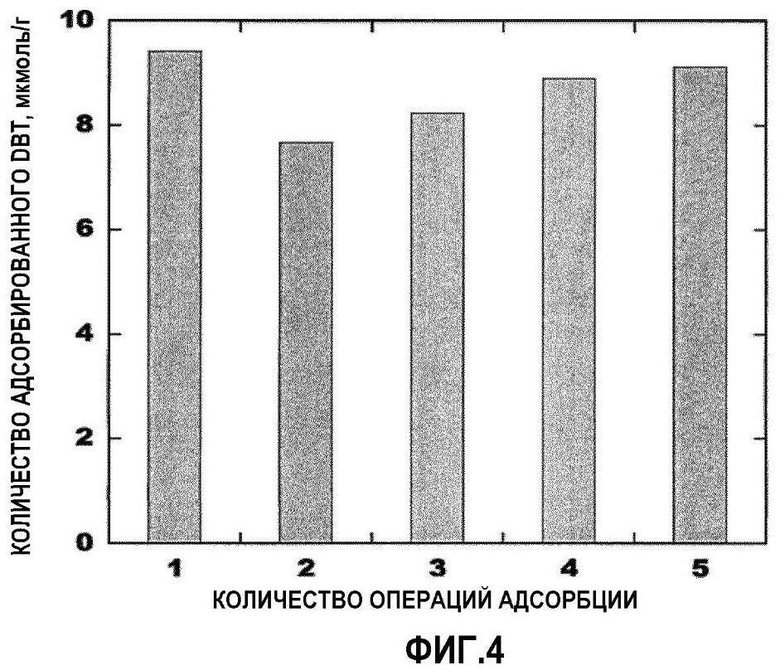
[Фиг.4] Фиг.4 представляет собой диаграмму, показывающую величину насыщения адсорбции дибензотиофена (DBT), полученную с помощью каждой операции адсорбции, когда адсорбция и регенерация чередуются, в Примере исследования 4.
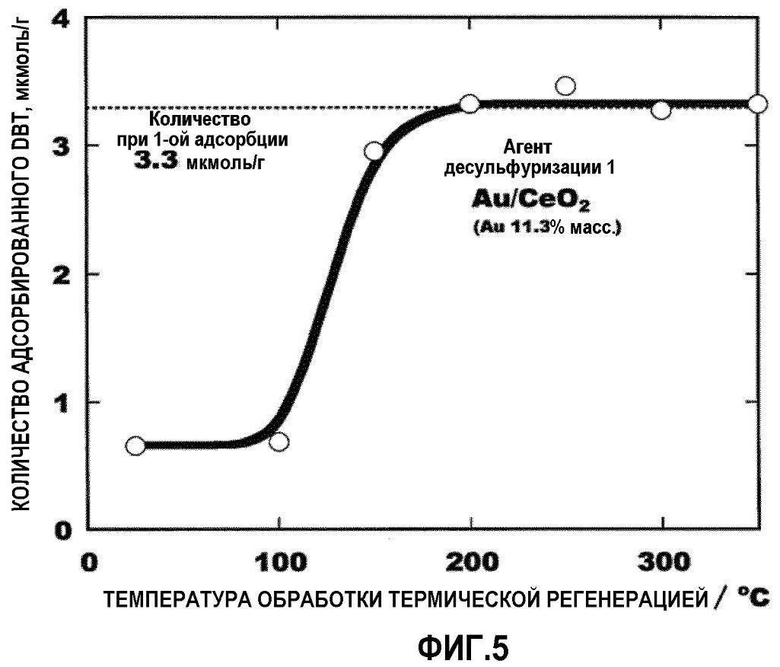
[Фиг.5] Фиг.5 представляет собой график, показывающий соотношение между температурой нагрева во время обработки регенерации и величиной насыщения адсорбции дибензотиофена (DBT) на образце после регенерации, в Примере исследования 5.
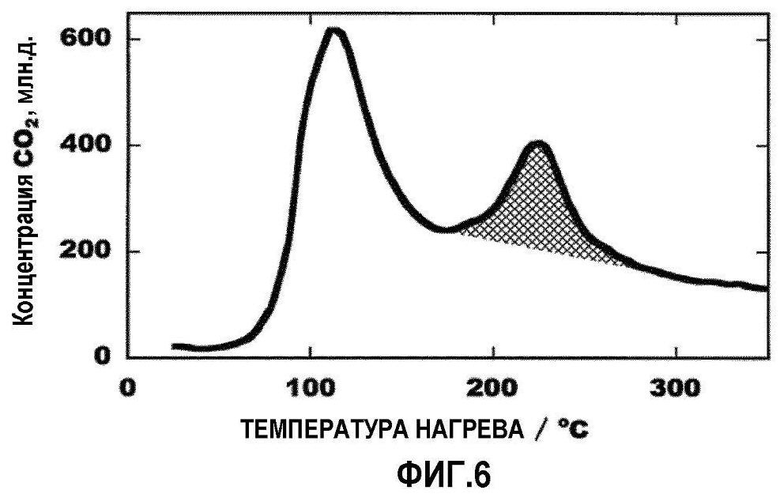
[Фиг.6] Фиг.6 представляет собой график, изображающий количество CO2, образующегося во время увеличения температуры, как функцию температуры, когда обработку термической регенерации осуществляют при 350°C, в Примере исследования 5.
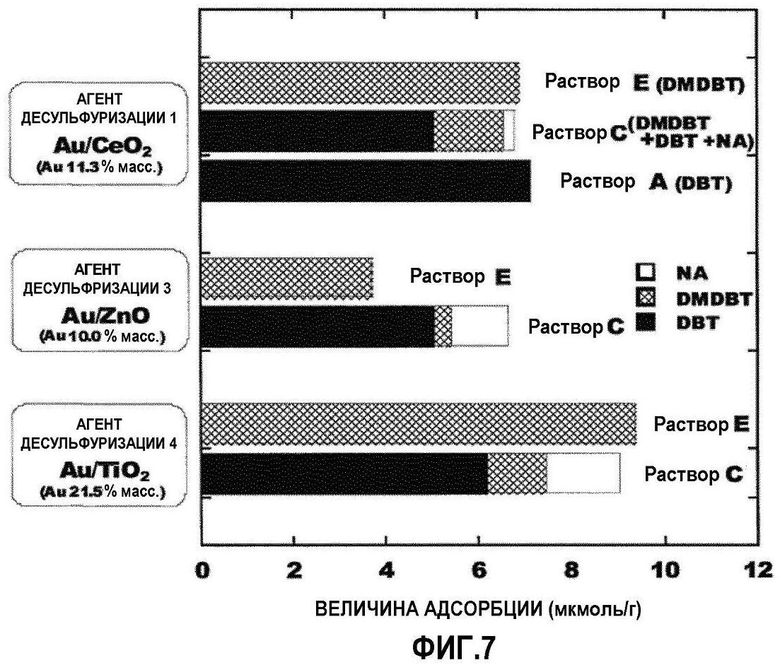
[Фиг.7] Фиг.7 представляет собой диаграмму, показывающую величину насыщенной адсорбции 4,6-диметилдибензотиофена (DMDBT) в каждом образце из исследуемого раствора E, по сравнению с величиной адсорбции DBT, DMDBT и NA из исследуемых растворов A и C.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение описывается более подробно со ссылкой на примеры ниже.
Пример 1
(1) Получение агента десульфуризации
Агент десульфуризации 1: золото/оксид церия (Au/CeO 2 )
Водный раствор (1000 мл) золотохлористоводородной кислоты [HAuCl4·4H2O] (5 ммоль/л) нагревают до 70°C и добавляют к нему по каплям KOH для доведения pH до 7. Порошок оксида церия (7,7 г) добавляют к нему, а затем добавляют к нему раствор (370 мл) цитрата магния (10 ммоль/л). Смесь перемешивают в течение 1 часа, фильтруют, промывают водой и сушат, и полученный таким образом порошок кальцинируют в течение 4 часов на воздухе при 400°C, получая тем самым агент десульфуризации 1 (Au/CeO2), имеющий структуру, в которой наночастицы золота, имеющие средний размер частиц 5,5 нм, нанесены на поверхность оксида церия (количество нанесенного Au: 11,3% мас.). Заметим, что средний размер частиц для наночастиц золота в Примерах представляет собой размер кристаллитов золота, вычисленный с помощью уравнения Шеррера из данных измерения дифракции рентгеновского излучения на порошках.
Агент десульфуризации 2: золото/оксид церия (Au/CeO 2 )
Агент десульфуризации 2 (Au/CeO2), имеющий структуру, в которой наночастицы золота, имеющие средний размер частиц 4,9 нм, нанесены на поверхность оксида церия (количество нанесенного Au: 1,0% мас.), приготавливают с помощью такого же способа получения, как и для агента десульфуризации 1, за исключением того, что уменьшают используемое количество золотохлористоводородной кислоты и не добавляют цитрата магния.
Агент десульфуризации 3: золото/оксид цинка (Au/ZnO)
Водный раствор, в котором карбонат натрия Na2CO3 (8 г) растворен в воде (200 мл), нагревают до 70°C. Водный раствор, в котором нитрат цинка (14,2 г) и золотохлористоводородную кислоту (1,1 г) растворяют в воде (200 мл), добавляют к нему при 70°C, и образуется осадок. После перемешивания в течение 1 часа осуществляют фильтрование, промывку водой и сушку. Полученный таким образом порошок кальцинируют в течение 4 часов на воздухе при 400°C, получая тем самым агент десульфуризации 3 (Au/ZnO), имеющий структуру, в которой наночастицы золота, имеющие средний размер частиц 5,8 нм, нанесены на поверхность оксида цинка (количество нанесенного Au: 10,0% мас.).
Агент десульфуризации 4: золото/оксид титана (Au/TiO 2 )
Водный раствор (1000 мл) золотохлористоводородной кислоты (5 ммоль/л) нагревают до 70°C и добавляют к нему по каплям KOH для доведения pH до 7. Порошок оксида титана (3,6 г) добавляют к нему, а затем к нему добавляют раствор (400 мл) цитрата магния (10 ммоль/л). Смесь перемешивают в течение 1 часа, фильтруют, промывают водой и сушат, и полученный таким образом порошок кальцинируют в течение 4 часов на воздухе при 400°C, получая тем самым агент десульфуризации 4 (Au/TiO2), имеющий структуру, в которой наночастицы золота, имеющие средний размер частиц 4,0 нм, нанесены на поверхность оксида титана (количество нанесенного Au: 21,5% мас.).
Сравнительный агент десульфуризации 1: оксид церия (CeO 2 )
Порошок оксида церия, используемый для получения агентов десульфуризации 1 и 2, используют как есть.
Сравнительный агент десульфуризации 2: платина/оксид церия (Pt/CeO 2 )
Водный раствор (500 мл) платинохлористоводородной кислоты [H2PtC6·6H2O] (2 ммоль/л) нагревают и к нему добавляют по каплям KOH для доведения pH до 7. Порошок оксида церия (6,5 г) добавляют к нему. Смесь перемешивают в течение 1 часа, фильтруют, промывают водой и сушат, и полученный таким образом порошок кальцинируют в течение 4 часов на воздухе при 400°C. Затем, температуру повышают до 350°C в потоке смешанного газа из H2 (3%) + He (остаток) для восстановления Pt, получая тем самым сравнительный агент десульфуризации 2 (Pt/CeO2), в котором платина, имеющая средний размер частиц 2,0 нм или меньше, нанесена на поверхность оксида церия (количество нанесенного Pt: 3,0% мас.).
Сравнительный агент десульфуризации 3: цеолит Y-типа, подвергаемый ионному обмену с церием (Ce-Y)
Порошок цеолита Y-типа (0,75 г) добавляют к водному раствору (30 мл) нитрата церия [Ce(NO3)3·6H2O] (0,2 моль/л) и смесь перемешивают посредством встряхивания в течение 3 дней. Смесь фильтруют, промывают водой и сушат, и полученный таким образом порошок кальцинируют в течение 2 часов на воздухе при 400°C, получая тем самым сравнительный агент десульфуризации 3, содержащий цеолит Y-типа, подвергаемый ионному обмену с церием (Ce-Y).
Сравнительный агент десульфуризации 4: медь/оксид цинка (Cu/ZnO)
Водный раствор, в котором карбонат натрия Na2CO3 (7,6 г) растворяют в воде (200 мл), нагревают до 70°C. Водный раствор, содержащий нитрат цинка (12,5 г) и нитрат меди (4,3 г), растворяют в воде (300 мл) добавляют к нему при 70°C, и образуется осадок. После перемешивания в течение 1 часа осуществляют фильтрование, промывку водой и сушку. Полученный таким образом порошок кальцинируют в течение 4 часов на воздухе при 400°C. Затем, температуру повышают до 400°C в потоке смешанного газа из H2 (3%) + He (остаток) для восстановления Cu, получая тем самым сравнительный агент десульфуризации 4 (Cu/ZnO), в котором медь, имеющая средний размер частиц 3,3 нм, нанесена на поверхность оксида цинка (количество нанесенного Cu: 25,1% мас.).
(2) Исследование десульфуризации
Готовят следующие исследуемые растворы для A, B, C, D, и E.
Исследуемый раствор A
Используя н-декан (производится Kishida Chemical Co., Ltd., специальное качество) в качестве растворителя, готовят раствор, содержащий следующие компоненты: дибензотиофен (39,9 мг/л) (производится Kanto Chemical Co., Inc., специальное качество) в качестве органического соединения серы и н-тетрадекан (39,5 мг/л) (производится Kishida Chemical Co., Ltd., специальное качество) в качестве внутреннего стандарта для анализа раствора. Концентрация серы в этом растворе соответствует 9,5 млн.д.
Исследуемый раствор B
Используя н-декан в качестве растворителя, как в исследуемом растворе A, готовят раствор, содержащий дибензотиофен (51,2 мг/л) в качестве органического соединения серы. Концентрация серы в этом растворе соответствует 12,2 млн.д.
Исследуемый раствор C
Используя н-декан (производится Kishida Chemical Co., Ltd., специальное качество) в качестве растворителя, готовят раствор, содержащий следующие компоненты: дибензотиофен (22,7 мг/л) (производится Kanto Chemical Co., Inc., специальное качество) и 4,6-диметилдибензотиофен (23,1 мг/л) (производится Wako Pure Chemical Industries, Ltd., специальное качество) в качестве органических соединений серы, нафталин (22,1 мг/л) (производится Wako Pure Chemical Industries, Ltd., специальное качество) в качестве не содержащего серы ароматического органического соединения и н-тетрадекан (26,5 мг/л) (производится Kishida Chemical Co., Ltd., специальное качество) в качестве внутреннего стандарта для анализа раствора. Общая концентрация серы в этом растворе составляет 10,2 млн.д., при этом дибензотиофен составляет 5,4 млн.д. и 4,6-диметилдибензотиофен составляет 4,8 млн.д.
Исследуемый раствор D
Используя н-декан в качестве растворителя, как в исследуемом растворе A, готовят раствор, содержащий дибензотиофен (43,2 мг/л) в качестве органического соединения серы и н-тетрадекан (69,3 мг/л) в качестве внутреннего стандарта для анализа раствора. Концентрация серы в этом растворе соответствует 10,3 млн.д.
Исследуемый раствор E
Используя н-декан (производится Kishida Chemical Co., Ltd., специальное качество) в качестве растворителя, готовят раствор, содержащий следующие компоненты: 4,6-диметилдибензотиофен (46,7 мг/л) (производится Wako Pure Chemical Industries, Ltd., специальное качество) и н-тетрадекан (45,3 мг/л) (производится Kishida Chemical Co., Ltd., специальное качество) в качестве внутреннего стандарта для анализа раствора. Концентрация серы в этом растворе соответствует 9,7 млн.д.
Способы исследования адсорбции и регенерации
Пример исследования 1
Образцы порошков агентов десульфуризации 1 и 2 и сравнительного агента десульфуризации 1, приготовленного с помощью описанного выше способа, нагревают на воздухе при 300°C в течение 30 минут для удаления адсорбированной воды, а затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель. 100 мг каждого образца взвешивают и помещают в отдельные бутылки с крышками на резьбе, и добавляют исследуемый раствор A (5 мл) в каждую бутылку, которую затем закрывают крышкой. Этот момент времени считается началом адсорбции. Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Хотя температуру раствора повышают до 60°C, в один момент времени, между 8,5 часами и 24 часами в агенте десульфуризации 1, и в один момент времени, между 27 часами и 47 часами в агенте десульфуризации 2 и в сравнительном агенте десульфуризации 1, в отдельном эксперименте подтверждается, что это почти не влияет на адсорбцию в экспериментальных условиях настоящих примеров исследования. После начала адсорбции, примерно 0,1 мл раствора извлекают с использованием пипетки каждые несколько часов, и композицию раствора анализируют с использованием FID-GC (газофазной хроматографии с пламенно-ионизационным детектором). Фиг.1 показывает временной ход изменения концентрации дибензотиофена в растворе.
Фиг.1 показывает, что агенты десульфуризации 1 и 2, в которых наночастицы золота нанесены на оксид церия, адсорбируют большее количество дибензотиофена, по сравнению со сравнительным агентом десульфуризации 1, содержащим только оксид церия, и, в частности, агент десульфуризации 1, в котором количество нанесенного золота велико (11,3% мас.), адсорбирует очень большое количество дибензотиофена. Кроме того, наблюдается явление, при котором величина адсорбции становится стабильной, после того как проходит, по меньшей мере, 24 часа, в случае агентов десульфуризации 1 и 2, в то время как величина адсорбции уменьшается, после того как проходит 5 часов, в случае сравнительного агента десульфуризации 1, содержащего только оксид церия.
Описанные выше результаты ясно показывают, что использование агентов десульфуризации 1 и 2, в которых наночастицы золота нанесены на оксид церия, позволяют эффективную адсорбционную десульфуризацию дибензотиофена, для которого концентрация серы в деканом растворе составляет приблизительно 10 млн.д.
Пример исследования 2
Образец порошка агента десульфуризации 1, приготовленного с помощью описанного выше способа, нагревают на воздухе при 300°C в течение 30 минут для удаления адсорбированной воды, а затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель. Затем, 26 мг, 51 мг, 101 мг, 200 мг и 300 мг этого образца взвешивают и помещают в пять бутылок с крышками на резьбе, по отдельности. Исследуемый раствор B (5 мл) добавляют в каждую бутылку с крышкой на резьбе, которую затем закрывают крышкой. Этот момент времени считается началом адсорбции. Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Через 74 часа или позже после начала адсорбции (подтверждается достижение адсорбционного равновесия) раствор извлекают с использованием пипетки и анализируют. Известное количество 2,8-диметилдибензотиофена (производится Tokyo Chemical Industry Co., Ltd.) добавляют в качестве внутреннего стандарта в каждый анализируемый раствор и анализируют композицию с помощью FPD-GC.
Фиг.2 представляет собой график, показывающий соотношение между массой используемого агента десульфуризации и концентрацией серы, остающейся в растворе данного примера исследования после адсорбции, и количеством дибензотиофена (DBT), адсорбированного с помощью агента десульфуризации. Отметим, что концентрация серы в исследуемом растворе, показанном на фиг.2, получается посредством преобразования концентрации DBT в концентрацию серы.
Фиг.2 ясно показывает, что общее количество адсорбированного дибензотиофена (DBT) увеличивается, а количество оставшегося DBT в растворе уменьшается, когда количество используемого агента десульфуризации увеличивается. В частности, когда используют 300 мг агента десульфуризации, адсорбируется 1,37 мкмоль DBT, что близко к начальному количеству DBT (1,38 мкмоль) в исследуемом растворе (5 мл), и концентрация серы, которая составляла перед адсорбцией 12,2 млн.д., понижается до 0,1 млн.д.
Пример исследования 3
Используя агенты десульфуризации 1, 3 и 4 и сравнительные агенты десульфуризации 2-4, приготовленные с помощью описанного выше способа, эксперименты по адсорбции и регенерации осуществляют с помощью процедур (1)-(3), описанных ниже.
(1) Первая адсорбция
Каждый агент десульфуризации нагревают на воздухе при 300°C в течение 30 минут для удаления адсорбированной воды, а затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель. 100 мг каждого агента десульфуризации взвешивают и помещают в отдельные бутылки с крышками на резьбе и исследуемый раствор C (5 мл) добавляют в каждую бутылку, которую затем закрывают крышкой. Этот момент времени считается началом адсорбции. Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, примерно 0,1 мл раствора извлекают с использованием пипетки и композицию раствора анализируют с использованием FID-GC.
(2) Регенерация
После осуществления эксперимента по адсорбции с помощью описанного выше способа, каждый агент десульфуризации разделяют посредством фильтрования, промывают с помощью гексана и сушат при комнатной температуре. После сушки порошок агента десульфуризации помещают в кварцевую реакционную трубку и фиксируют с помощью кварцевой ваты, помещенной в трубке по обе стороны от агента. В то время прохождения смешанного газа из He (80%) + O2 (20%) через реакционную трубку при скорости потока 100 мл/мин температуру повышают до 350°C при 10°C/мин, а затем ее поддерживают при 350°C в течение 10 мин. С помощью этой операции компоненты, адсорбированные на поверхности каждого агента десульфуризации, удаляются с помощью термической десорбции или каталитического горения, и каждый агент десульфуризации регенерируется. Ход этого процесса наблюдают посредством мониторинга газа, выходящего из реакционной трубки.
(3) Вторая адсорбция
После регенерации каждого агента десульфуризации с помощью описанного выше способа порошок агента десульфуризации, который приводится опять к комнатной температуре, взвешивают и помещают в отдельные бутылки с крышками на резьбе. Поскольку имеется уменьшение количества каждого агента десульфуризации, извлекаемого после обработки регенерации, к нему добавляют исследуемый раствор C в пропорции 5 мл на 100 мг порошка агентов десульфуризации, так что отношение исследуемого раствора к агенту десульфуризации является таким же, как и при исследовании адсорбции в (1), описанном выше, и каждую бутылку с крышкой на резьбе закрывают крышкой. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, примерно 0,1 мл раствора извлекают с использованием пипетки и композицию раствора анализируют с использованием FID-GC.
Количество дибензотиофена (DBT), 4,6-диметилдибензотиофена (DMDBT) и нафталина (NA), адсорбируемого на 1 г порошка агентов десульфуризации, вычисляют из результатов анализа композиции раствора. Фиг.3 показывает результаты.
Фиг.3 показывает, что использование агентов десульфуризации 1, 3 и 4, в которых наночастицы золота, нанесенные на оксид металла, позволяют селективную адсорбцию дибензотиофенов (DBT + DMDBT) и, в частности, очень селективную адсорбцию DBT. По отношению к сравнительным агентам десульфуризации 2, содержащим цеолит Y-типа, подвергаемый ионному обмену с церием (Ce-Y), хотя общая величина первой адсорбции на нем была больше по сравнению с агентами десульфуризации 1, 3 и 4, он адсорбирует по существу эквимолярные количества DBT, DMDBT и NA, показывая отсутствие способности к селективной адсорбции органических соединений, содержащих серу.
Кроме того, даже во втором исследовании адсорбции, агенты десульфуризации 1, 3, и 4 способны адсорбировать дибензотиофены (DBT + DMDBT) в количестве, которое составляет, по меньшей мере, 70% от количества, адсорбируемого в первом исследовании адсорбции, четко демонстрируя особенно высокую долю адсорбции после регенерации, по сравнению со сравнительными агентами десульфуризации 2 и 3.
По отношению к Cu/ZnO (сравнительный агент десульфуризации 4), который является эффективным в качестве адсорбента для сероводорода, адсорбент содержит большое количество Cu, которая, как и Au, представляет собой элемент группы IB, количество адсорбируемых дибензотиофенов является малым, оно показывает плохие рабочие характеристики в качестве адсорбентов для органических соединений, содержащих серу.
Пример исследования 4
Адсорбцию дибензотиофена (DBT) и регенерацию агента десульфуризации подвергают повторяющемуся исследованию с помощью способов (1)-(3), описанных ниже. Отметим, что это исследование осуществляют с помощью модификации способа обработки во время регенерации для предотвращения уменьшения количества агента десульфуризации, извлеченного после регенерации.
(1) Первая адсорбция
100 мг агента десульфуризации 1 взвешивают и помещают в 20-мл колбу в форме груши (изготовленную из термостойкого стекла). Колбу помещают в электрическую печь, нагревают при 350°C на воздухе в течение 30 минут для удаления адсорбированной воды, а затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель. Непосредственно после того как колбу вынимают из десикатора, колбу герметизируют с помощью крышки из Teflon (зарегистрированное торговое наименование) и ее массу измеряют для определения количества агента десульфуризации после термического дегидратирования. К нему добавляют исследуемый раствор D (5 мл) и колбу герметизируют с помощью крышки из Teflon (зарегистрированное торговое наименование). Этот момент времени считают началом адсорбции. Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, перемешивание останавливают и колбе позволяют стоять спокойно, чтобы позволить седиментацию порошка агентов десульфуризации. Раствор супернатанта извлекают с использованием пипетки и композицию раствора анализируют с использованием FID-GC.
(2) Регенерация
После осуществления эксперимента по адсорбции с помощью указанного выше способа колбе позволяют стоять спокойно для седиментации порошка агентов десульфуризации. Колбу осторожно наклоняют, чтобы слить оставшийся раствор супернатанта без вытекания порошка агента десульфуризации, и добавляют в нее примерно 5 мл гексана. Операцию добавления гексана и сливания раствора супернатанта повторяют в целом три раза. Затем, через колбу продувают газообразный азот, чтобы позволить испарение гексана. Колбу помещают в электрическую печь и нагревают при 350°C на воздухе в течение 30 минут для термической регенерации агента десульфуризации. После нагрева колбу охлаждают до комнатной температуры в десикаторе, содержащем силикагель. Непосредственно после извлечения колбы из десикатора колбу герметизируют с помощью крышки из Teflon (зарегистрированное торговое наименование) и измеряют ее массу для определения количества агента десульфуризации после регенерации. Как описано выше, регенерацию осуществляют без извлечения порошка адсорбента из колбы. В результате, даже после четвертой регенерации сохраняется, по меньшей мере, 99% мас. изначального используемого адсорбента.
(3) Вторая и последующие адсорбции и регенерации
После регенерации агента десульфуризации с помощью способа, описанного выше, исследуемый раствор D добавляют в колбу в пропорции 5 мл на 100 мг порошка агентов десульфуризации, помещенного в колбу, и затем колбу герметизируют с помощью крышки из Teflon (зарегистрированное торговое наименование) (начало второй адсорбции). Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, перемешивание останавливают и колбе позволяют стоять спокойно, чтобы позволить седиментацию порошка агента десульфуризации. Раствор супернатанта извлекают с использованием пипетки и композицию раствора анализируют с использованием ГХ. После этого операции регенерации и адсорбции повторяют таким же способом, как описано выше. Когда повторяют регенерацию, порошок адсорбента прилипает к стенке верхней части колбы, что приводит к ухудшению контакта с раствором. Таким образом, для четвертой и последующих операций адсорбции, после того как раствор для адсорбции помещают в колбу и колбу герметизируют с помощью крышки из Teflon (зарегистрированное торговое наименование), колбу погружают в воду в ультразвуковом устройстве для очистки, которое работает в течение от 10 секунд до нескольких минут, в начале адсорбции, для улучшения диспергирования порошка адсорбента, и при этом контакт с раствором восстанавливается.
Количество адсорбированного дибензотиофена (DBT) на 1 г порошка агентов десульфуризации вычисляют из результатов анализа композиции раствора в конце адсорбции каждый раз. Фиг.4 показывает результаты.
Фиг.4 ясно показывает, что нет никакого значительного уменьшения величины адсорбции, даже когда адсорбцию и регенерацию повторяют. По отношению к небольшому уменьшению величин второй и третьей адсорбции контакт между адсорбентом и раствором, как считается, слегка ухудшается, поскольку первая-третья адсорбции осуществляются без операции использования ультразвукового устройства для очистки в начале адсорбции для улучшения диспергируемости адсорбента. При четвертой и пятой адсорбции величина адсорбции становится стабильной, и она остается при 95% или более от величины первой адсорбции.
Описанные выше результаты ясно показывают, что агент десульфуризации по настоящему изобретению, в котором наночастицы золота нанесены на оксид металла, является превосходным по рабочим характеристикам селективного адсорбирования органических соединений, содержащих серу, в частности соединений дибензотиофена, и что агент десульфуризации может демонстрировать достаточные рабочие характеристики адсорбции после обработки регенерации с помощью нагрева и может повторно использоваться в качестве агента десульфуризации.
Пример исследования 5
Используя агент десульфуризации 1, приготовленный с помощью описанного выше способа, адсорбцию и регенерацию осуществляют с помощью процедур (1)-(3), описанных ниже, для исследования влияния температуры нагрева во время регенерации.
(1) Первая адсорбция
100 мг агента десульфуризации 1 взвешивают и помещают в 7 отдельных бутылок с крышками на резьбе. Каждую бутылку нагревают на воздухе при 350°C в течение 30 минут для удаления адсорбированной воды, затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель, и оставляют стоять в течение ночи, чтобы позволить поглощение влажности в десикаторе, где относительную влажность доводят 85% с использованием насыщенного раствора хлорида калия. Отметим, что, поскольку целью Примера исследования 5 является исследование влияния температуры нагрева во время регенерации на количество адсорбированного дибензотиофена (DBT), условия стандартизуются так, что каждый образец адсорбирует влажность при конкретных условиях перед началом адсорбции DBT, для устранения влияния различия в количестве остающейся влажности на адсорбцию DBT.
Исследуемый раствор A (5 мл) добавляют в каждую бутылку с крышкой на резьбе, которую затем закрывают крышкой. Этот момент времени считается началом адсорбции. Раствор перемешивают при комнатной температуре с использованием устройства для перемешивания. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, с использованием пипетки извлекают примерно 0,1 мл раствора и композицию раствора анализируют с использованием FID-GC.
(2) Регенерация
После осуществления эксперимента по адсорбции с помощью описанного выше способа раствор, остающийся в каждой бутылке с крышкой на резьбе, выливают с помощью такой же операции, как в Примере исследования 4, и внутренность бутылки с крышкой на резьбе промывают гексаном и сушат. Одну бутылку с крышкой на резьбе оставляют стоять в течение ночи в десикаторе, содержащем силикагель, при комнатной температуре (25°C). Пять бутылок с крышками на резьбе по отдельности помещают в электрические печи, с температурами, установленными при 100, 150, 200, 250 и 300°C соответственно, и нагревают на воздухе в течение 30 минут. По отношению к одной оставшейся бутылке с крышкой на резьбе порошок агента десульфуризации извлекают из нее, помещают в изготовленную из кварца реакционную трубку и фиксируют с помощью кварцевой ваты, помещенной в трубке по обе стороны от агента. Во время прохождения смешанного газа из He (80%) + O2 (20%) через реакционную трубку при скорости потока 100 мл/мин температуру повышают до 350°C при скорости 10°C/мин, а затем поддерживают при 350°C в течение 30 мин. Концентрацию CO2, образующегося в ходе повышения температуры, измеряют с использованием масс-спектрометра и Photoacoustic Multi-gas Monitor (производится INNOVA).
Агент десульфуризации подвергают термической обработке при температуре 25, 100, 150, 200, 250, 300°C или 350°C, как описано выше, затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель, и оставляют стоять в течение ночи, чтобы позволить поглощение влажности в десикаторе, где относительную влажность доводят до 85% с использованием насыщенного раствора хлорида калия.
(3) Вторая адсорбция
К агенту десульфуризации, который адсорбирует влажность после обработки термической регенерации, при каждой температуре, с помощью описанного выше способа добавляют исследуемый раствор A в пропорции 5 мл на 100 мг порошка агента десульфуризации и каждую бутылку закрывают крышкой. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, с использованием пипетки извлекают примерно 0,1 мл раствора и композицию раствора анализируют с использованием FID-GC.
Количество адсорбированного дибензотиофена (DBT) на 1 г порошка агента десульфуризации вычисляют из результатов анализа композиции раствора. При первой адсорбции все образцы в 7 бутылках с крышками на резьбе, подвергаемые адсорбции при одинаковых условиях, поглощают DBT в количестве 3,3±0,1 мкмоль/г·катализатора. По отношению к количеству DBT, адсорбируемого посредством второй адсорбции, после регенерации с помощью термической обработки при каждой температуре, соотношение между температурой термической обработки и количеством адсорбированного DBT показаны на фиг.5. Из фиг.5 ясно, что по отношению к агенту десульфуризации 1 (Au/CeO2), когда температура термической обработки равна 100°C или ниже, величина второй адсорбции существенно уменьшается по сравнению с первой адсорбцией, показывая, что температура термической обработки является недостаточной. Далее, когда температура термической обработки равна 200°C или выше, величина второй адсорбции является по существу такой же, как для первой адсорбции, показывая, что агент десульфуризации полностью регенерирован.
Фиг.6 представляет собой график, изображающий количество CO2, производимого во время нагрева, как функцию температуры, при нагреве до 350°C. Пики концентрации CO2 наблюдаются при двух температурах: 115 и 225°C. Среди них пик на стороне низких температур наблюдается также для образца Au/CeO2, который не адсорбирует DBT. В этом случае, вероятно, адсорбируется CO2 из воздуха. Пик со стороны высоких температур наблюдается только после адсорбции DBT. В этом случае, вероятно, адсорбированный DBT сгорает на каталитической поверхности и преобразуется в CO2. Количество CO2, которое соответствует заштрихованной части на фиг.6, составляет 37,2 мкмоль/г·катализатора. Это замечательно соответствует количеству CO2 (39,6 мкмоль/г·катализатора), определяемому на основе предположения, что DBT (3,3 мкмоль/г·катализатора), адсорбируемый при первой адсорбции, полностью сгорает до CO2.
Пример исследования 6
Посредством использования исследуемого раствора E (раствора, который содержит только 4,6-диметилдибензотиофен в качестве соединения дибензотиофена) агенты десульфуризации 1, 3 и 4, приготовленные с помощью описанного выше способа, подвергаются эксперименту по адсорбции с помощью процедур, описанных ниже.
Каждый агент десульфуризации нагревают на воздухе при 350°C в течение 30 минут для удаления адсорбированной воды, а затем охлаждают до комнатной температуры в десикаторе, содержащем силикагель. 100 мг каждого агента десульфуризации взвешивают и помещают в отдельные бутылки с крышками на резьбе и исследуемый раствор E (5 мл) добавляют в каждую бутылку, которую затем закрывают крышкой. Этот момент времени считается началом адсорбции. Раствор перемешивают с использованием устройства для перемешивания при комнатной температуре. Когда проходит, по меньшей мере, 24 часа и достигается адсорбционное равновесие, с использованием пипетки извлекают примерно 0,1 мл раствора и композицию раствора анализируют с использованием FID-GC.
Количество 4,6-диметилдибензотиофена (DMDBT), адсорбированного на 1 г порошка агента десульфуризации, вычисляют из результатов анализа композиции раствора. Фиг.7 показывает результаты. Фиг.7 также показывает результаты исследования адсорбции, полученные из Примера исследования 1 и Примера исследования 3, в которых используются исследуемый раствор A (раствор, который содержит только DBT) и исследуемый раствор C (смешанный раствор, содержащий DBT, DMDBT и NA) соответственно. Отметим, что композиции исследуемых растворов A, C и E показаны в Таблице 1, ниже.
В соответствии с результатами, показанными на фиг.7, результаты исследования адсорбции, в которых используют исследуемый раствор C, содержащий DBT, DMDBT и NA, показывают, что количество адсорбированного DBT выше, чем количество адсорбированного DMDBT для всех агентов десульфуризации 1, 3 и 4. Это, вероятно, связано с тем фактом, что DBT и DMDBT конкурентно адсорбируются на центре адсорбции, и DBT, не содержащий метильных групп и имеющий низкое стерическое затруднение, адсорбируется более селективно.
С другой стороны, количество адсорбированного DMDBT, которое получают при исследовании адсорбции, в котором используют исследуемый раствор E, который представляет собой раствор, содержащий только DMDBT, значительно выше, чем количество DMDBT, адсорбированного из исследуемого раствора C, который представляет собой смешанный раствор. По отношению к агенту десульфуризации 1 (Au/CeO2), сравнение между количеством DMDBT, адсорбированным из раствора, содержащего только DMDBT (исследуемый раствор E), и количеством DBT, адсорбированным из раствора, содержащего только DBT (исследуемый раствор A), показывает, что количество адсорбированного DMDBT соответствует примерно 97% от количества адсорбированного DBT. Это подтверждает тот факт, что адсорбент по настоящему изобретению демонстрирует превосходные рабочие характеристики адсорбции DMDBT.
По отношению к не содержащему серы топливу, которое поставляется в настоящее время, 4,6-диметилдибензотиофен, который исключительно трудно удалять с использованием современной технологии, составляет относительно большую часть соединений дибензотиофена, остающихся в топливе. Результаты, показанные на фиг.7, показывают, что агент десульфуризации по настоящему изобретению имеет свойства, пригодные для удаления малых количеств оставшегося 4,6-диметилдибензотиофена.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМИЧЕСКИ МОДИФИЦИРОВАННЫЙ ПЛАНАРНЫЙ ОПТИЧЕСКИЙ СЕНСОР, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СПОСОБ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ С ЕГО ПОМОЩЬЮ | 2015 |
|
RU2572801C1 |
| СПОСОБ ГЛУБОКОЙ ОКИСЛИТЕЛЬНО-АДСОРБЦИОННОЙ ДЕСУЛЬФУРИЗАЦИИ ЖИДКИХ УГЛЕВОДОРОДНЫХ ТОПЛИВ И СОРБЕНТЫ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2482162C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ОТРАБОТАННОГО АДСОРБЕНТА | 2014 |
|
RU2551361C1 |
| Способ адсорбционной десульфуризации нефти и нефтепродуктов: бензина, дизельного топлива с использованием композиционного адсорбента на основе минералов природного происхождения | 2020 |
|
RU2743291C1 |
| ОКИСЛИТЕЛЬНАЯ ДЕСУЛЬФУРИЗАЦИЯ С ИСПОЛЬЗОВАНИЕМ КАТАЛИЗАТОРА НА ОСНОВЕ ТИТАНА (IV) И ОРГАНОГИДРОПЕРОКСИДОВ | 2011 |
|
RU2581473C2 |
| Состав и способ изготовления композиции из минералов природного происхождения для адсорбционной десульфуризации нефти и нефтепродуктов | 2020 |
|
RU2751874C1 |
| КАТАЛИЗАТОРЫ СУЛЬФООКИСЛЕНИЯ И СПОСОБЫ И СИСТЕМЫ ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2472841C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ ДИСУЛЬФИДА МОЛИБДЕНА НА НОСИТЕЛЕ ИЗ ДИОКСИДА ТИТАНА | 2016 |
|
RU2720181C1 |
| СПОСОБ ДЕСУЛЬФУРИЗАЦИИ УГЛЕВОДОРОДНОЙ НЕФТИ | 2004 |
|
RU2335528C2 |
| СПОСОБ ОЧИСТКИ БЕНЗИНА | 2017 |
|
RU2742646C2 |
Изобретение относится к агентам десульфуризации и их использованию. Описан агент десульфуризации для жидкофазной адсорбционной десульфуризации, содержащий оксид металла с нанесенными на него наночастицами золота, имеющими средний размер частиц 50 нм или меньше. Описан агент десульфуризации для жидкофазной адсорбционной десульфуризации, где описанный выше агент десульфуризации фиксируется на элементе носителя. Описан способ десульфуризации, включающий приведение описанного выше агента десульфуризации в контакт с жидкостью, содержащей органическое соединение, содержащее серу. Описан способ регенерации агента десульфуризации, включающий термическую обработку агента десульфуризации после осуществления десульфуризации для удаления органического соединения, содержащего серу, адсорбированного на агенте десульфуризации. Описан способ десульфуризации, включающий приведение агента десульфуризации, который подвергается обработке и регенерации с помощью описанного выше способа регенерации, в контакт с жидкостью, содержащей органическое соединение, содержащее серу. Технический результат - описанный агент десульфуризации позволяет удалять соединения серы на основе тиофенов, до концентрация ниже 10 млн.д. 5 н. и 5 з.п. ф-лы; 1 табл.; 7 ил.; 6 пр.
1. Агент десульфуризации для жидкофазной адсорбционной десульфуризации, содержащий оксид металла с нанесенными на него наночастицами золота, имеющими средний размер частиц 50 нм или меньше.
2. Агент десульфуризации по п.1, который имеет удельную площадь поверхности
1 м2/г или более.
3. Агент десульфуризации для жидкофазной адсорбционной десульфуризации, где оксид металла с нанесенными на него наночастицами золота по п.1 фиксируется на элементе носителя.
4. Агент десульфуризации по п.1, в котором объектом обработки является жидкое топливо, содержащее органическое соединение, содержащее серу.
5. Способ десульфуризации, включающий приведение агента десульфуризации по п.1 в контакт с жидкостью, содержащей органическое соединение, содержащее серу.
6. Способ десульфуризации по п.5, в котором объектом обработки является жидкое топливо, содержащее органическое соединение, содержащее серу.
7. Способ десульфуризации по п.6, в котором жидкое топливо, служащее в качестве объекта обработки, содержит органическое соединение, содержащее тиофеновое кольцо.
8. Способ десульфуризации по п.7, в котором органическое соединение, содержащее тиофеновое кольцо, представляет собой, по меньшей мере, одно соединение, выбранное из группы, состоящей из соединений на основе дибензотиофена и алкилдибензотиофена.
9. Способ регенерации агента десульфуризации, включающий термическую обработку агента десульфуризации после осуществления обработки десульфуризации, которая осуществляется с помощью способа по п.5, для удаления органического соединения, содержащего серу, адсорбированного на агенте десульфуризации.
10. Способ десульфуризации, включающий приведение агента десульфуризации, который подвергается обработке и регенерации с помощью способа по п.9, в контакт с жидкостью, содержащей органическое соединение, содержащее серу, с помощью способа по п.5.
| УПЛОТНЕННАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ОКСИДА МЕТАЛЛА | 2001 |
|
RU2292948C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ КАТАЛИТИЧЕСКИХ ГИДРОДЕСУЛЬФУРИЗАЦИИ, ГИДРОДЕНИТРОГЕНИЗАЦИИ, РЕФОРМИНГА, ГИДРИРОВАНИЯ-ДЕГИДРИРОВАНИЯ И ИЗОМЕРИЗАЦИИ УГЛЕВОДОРОДНОГО СЫРЬЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ, АКТИВАЦИИ, РЕГЕНЕРАЦИИ И ИСПОЛЬЗОВАНИЯ | 1995 |
|
RU2146171C1 |
| US 2006102522 A1, 18.05.2006 | |||
| Биокаталитический реактор | 1990 |
|
SU1792967A1 |
| WO 2004022224 A1, 18.03.2004 | |||
| Конвейер | 1985 |
|
SU1270069A1 |
Авторы
Даты
2012-04-27—Публикация
2009-03-05—Подача