Настоящее изобретение относится к новым азолам, к новому противовирусному активному компоненту, фармацевтической композиции, противовирусному лекарственному средству, способу профилактики и лечения вирусных заболеваний, особенно вызываемых вирусами гепатита С (HCV).
Вирусные инфекции могут вызывать множество заболеваний, что создает серьезную угрозу для здоровья и жизни человечества. За последние 20 лет обнаружено не менее 30 совершенно новых возбудителей инфекционных болезней: СПИДа, вирусных гепатитов, острых и хронических диарей, геморрагических лихорадок (Эбола, венесуэльской, бразильской, долины Рифт) [a) Lednicky J.A., Rayner J.O. Uncommon respiratory pathogens. Curr. Opin. Pulm. Med. 2006, 12(3), 235-239. b) Hayden F.G. Respiratory viral threats. Curr. Opin. Infect. Dis. 2006, 19(2), 169-178]. В частности, особую тревогу вызывает возможность заболевания человека так называемым «птичьим гриппом» [a) Liu J.P. Avian influenza--a pandemic waiting to happen? J. Microbiol. Immunol. Infect. 2006, 39(1), 4-10. b) Henter J.I.; Chow C.B.; Leung C.W., Lau Y.L. Cytotoxic therapy for severe avian influenza A (H5N1) infection. Lancet. 2006 367(9513), 870-873. Review]. Согласно статистическим данным 60-65% эпидемических инфекций имеют вирусную этиологию. Из-за сложности взаимодействия в триаде «вирус - организм хозяина - лекарство» большинство современных противовирусных препаратов в процессе терапии проявляют побочные эффекты и формируют резистентные вирусные штаммы [Jain R., Clark N.M., Diaz-Linares M., Grim S.A. Limitations of current antiretroviral agents and opportunities for development. Curr. Pharm. Des. 2006, 12(9), 1065-1074]. В настоящее время количество противовирусных лекарственных препаратов, которые могут быть использованы в клинической практике, чрезвычайно ограничено - всего 43 низкомолекулярных вещества [http://integrity.prous.com/integrity], что далеко не удовлетворяет потребностям профилактики и лечения вирусных заболеваний. Кроме того, существует значительное число вирусных инфекций, вызывающих заболевания, для лечения которых в настоящее время не существует химиотерапевтических средств. Это относится, например, к заболеваниям, вызываемым вирусами папилломы, аденовирусам, герпеса-6, оспы, синдрома SARS, геморрагических лихорадок, лихорадки Западного Нила, птичьего гриппа и т.д. [De Clercq E. Recent highlights in the development of new antiviral drugs. Curr Opin Microbiol. 2005, 8(5), 552-560].
Вирус гепатита С относится к Флавивирусам (genus Flaviviridae) наряду с другими важными патогенами человека, такими как вирус желтой лихорадки, вирус West Nile, вирус Денги (Dengue) и вирус гепатита (GBV-C). Флавивирусы обладают сходной организацией генома, в том числе наличием гена, кодирующего неструктурный белок NS5A. NS5A играет важную роль в репликации вирусного РНК-генома, являясь структурным компонентом вирусного репликационного комплекса. Поскольку данный белок в настоящее время валидирован в клинических испытаниях как мишень для разработки лекарственных средств против хронического гепатита С, NS5A представляется перспективной мишенью и для других клинически важных флавивирусов, перечисленных выше.
Таким образом, большое значение имеет изыскание новых противофлавовирусных препаратов, в особенности, обладающих высокой активностью и низкой токсичностью.
В патентной литературе имеются публикации, посвященные различным производным 2-пирролидин-2-ил-1Н-имидазолов, которые являются лигандами неструктурного белка NS5A и подавляют вирус гепатита С (HCV) [WO 2008021927 А2, WO 2009020825 A1, WO 2009020828 A1, WO 2010065668 A1, WO 2010065681 A1, WO 2010096302 A1, WO 2010096462 A1, WO 2010096777 A1, WO 2010111534 A1, WO 2010111673 A1, WO 2010117635 A1, WO 2010117977 A1].
Однако поиск новых высокоэффективных противофлавивирусных лекарственных препаратов в настоящее время по-прежнему является одним из основных направлений создания новых фармакологических средств для лечения широкого и разнообразного круга вирусных инфекций, в том числе HCV.
В этой связи актуальным является синтез новых соединений и использование их в качестве противовирусных активных компонентов для фармацевтических композиций и лекарственных средств, в том числе HCV.
Ниже приведены определения терминов, которые использованы в описании этого изобретения.
«Алифатический» радикал означает радикал, полученный удалением атома водорода от неароматической С-Н связи. Алифатический радикал может дополнительно содержать заместители - алифатические или ароматические радикалы, определенные в данном разделе. Представители алифатических радикалов включают алкил, алкенил, алкинил, циклоалкил, циклоалкенил, гетероциклил, гетероцикленил, аралкенил, аралкилоксиалкил, аралкилоксикарбонилалкил, аралкил, аралкинил, аралкилоксиалкенил, гетероаралкенил, гетероаралкил, гетероаралкилоксиалкенил, гетероаралкилоксиалкил, гетероаралкенил, аннелированные арилциклоалкил, аннелированные гетероарилциклоалкил, аннелированные арилциклоалкенил, аннелированные гетероарилциклоалкенил, аннелированные арилгетероциклил, аннелированные гетероарилгетероциклил, аннелированные арилгетероцикленил, аннелированные гетероарилгетероцикленил.
«Алифатический» бирадикал означает бирадикал, полученный удалением атома водорода от С-Н связи алифатического радикала, определение которого дано выше.
«Алкенил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 7 атомов углерода и включающую по крайней мере одну углерод-углеродную двойную связь. Разветвленная означает, что к линейной алкенильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил, гетроаралкилоксикарбонил или 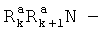 ,
, 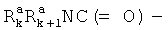 ,
, 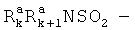 , где
, где 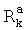 и
и  независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или
независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или 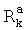 и
и  вместе с атомом N, с которым они связаны, образуют через
вместе с атомом N, с которым они связаны, образуют через 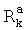 и
и  4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил и циклогексилбутенил.
4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил и циклогексилбутенил.
«Алкенилокси» означает алкенил-O-группу, в которой алкенил определен в данном разделе. Предпочтительными алкенилокси группами являются аллилокси и 3-бутенилокси.
«Алкенилоксиалкил» означает алкенил-O-алкил группу, в которой алкил и алкенил определены в данном разделе.
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил,
гетероаралкилоксикарбонил или 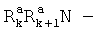 ,
, 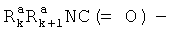 ,
,  ,
, 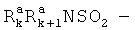 , где
, где 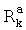 и
и 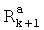 независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или
независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или 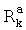 и
и 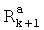 вместе с атомом N, с которым они связаны, образуют через
вместе с атомом N, с которым они связаны, образуют через 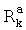 и
и 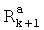 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или
4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или 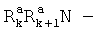 ,
, 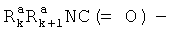 , аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкинил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 12 атомов углерода и включающую по крайней мере одну углерод-углеродную тройную связь.
Разветвленная означает, что к линейной алкинильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или 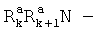 ,
, 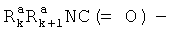 ,
, 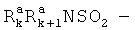 , где
, где 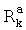 и
и 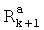 независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или
независимо друг от друга представляют собой «заместители амино группы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или 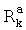 и
и 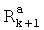 вместе с атомом N, с которым они связаны, образуют через
вместе с атомом N, с которым они связаны, образуют через 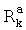 и
и 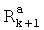 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил, бута-1,3-диин и гекса-1,3,5-триин.
4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил, бута-1,3-диин и гекса-1,3,5-триин.
«Алкинилоксиалкил» означает алкинил-O-алкил группу, в которой алкил и алкинил определены в данном разделе.
«Алкокси» означает алкил-O-группу, в которой алкил определен в данном разделе. Предпочтительными алкилокси группами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси.
«Алкилоксиалкил» означает алкил-O-алкил группу, в которой алкильные группы независимы друг от друга и определены в данном разделе.
«Алкилоксиалкиленоксиалкил» означает алкил-O-(CHR)n-O-алкил группу, в которой R представляет собой атом водорода или алкил, а n>2, предпочтительно 2, 3 или 4.
«Алкилоксиарил» означает алкил-O-арил группу, в которой алкил и арил определены в данном разделе.
«Алкенилоксиарил» означает алкенил-O-арил группу, в которой алкенил и арил определены в данном разделе.
«Алкинилоксиарил» означает алкинил-O-арил группу, в которой алкинил и арил определены в данном разделе.
«Алкилтио» означает алкил-S группу, в которой алкил группа в определена данном разделе.
«Алкилтиоалкил» означает алкил-S-алкил группу, в которой алкильные группы независимы друг от друга и определены в данном разделе.
«Алкилтиоарил» означает алкил-S-арил группу, в которой алкил и арил определены в данном разделе.
«Алкенилтиоарил» означает алкенил-S-арил группу, в которой алкенил и арил определены в данном разделе.
«Алкинилтиоарил» означает алкинил-S-арил группу, в которой алкинил и арил определены в данном разделе.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимущественно от 6 до 10 атомов углерода. Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть аннелирован с неароматической циклической системой или гетероциклом.
«Арилокси» означает арил-О-группу, в которой значение арил определено в данном разделе. Представителями арилокси групп являются фенокси и 2-нафтилокси.
«Арилтио» означает арил-S-группу, в которой значение арил определено в данном разделе.
Представителями арилтио групп являются фенилтио и 2-нафтилтио.
«Бирадикал» означает радикал, полученный удалением двух атомов водорода из двух С-Н связей молекулы.
«Гидрат» означает сольват, в котором вода является молекулой или молекулами растворителя.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы».
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Низший алкил» означает линейный или разветвленный алкил с 1-4 атомами углерода.
«Терапевтический коктейль» представляет одновременно администрируемую комбинацию двух и более лекарственных препаратов, обладающих различным механизмом фармакологического действия и направленных на различные биомишени, участвующие в патогенезе заболевания.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких содей дано в Berge S.M. et al., "Pharmaceutical Salts" J.Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия.
Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Предметом данного изобретения являются новые замещенные азолы общей формулы 1А и 1В и их фармацевтически приемлемые соли.
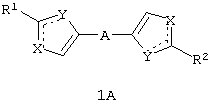
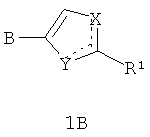
где: сплошные линии с сопровождающими их пунктирными линиями 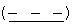 представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь;
представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь;
Х и Y необязательно принимают разные значения и представляют собой атом азота, кислорода, серы или группу NH;
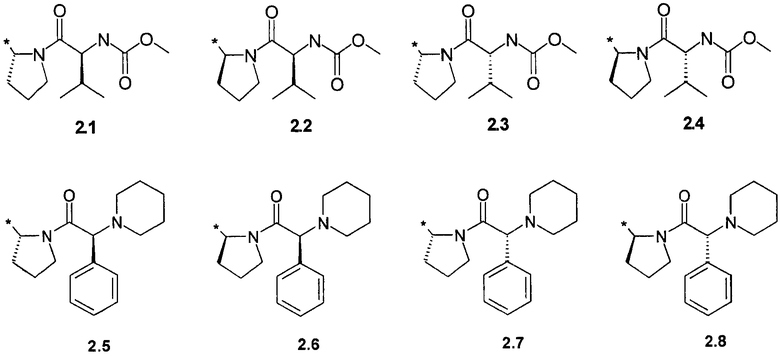
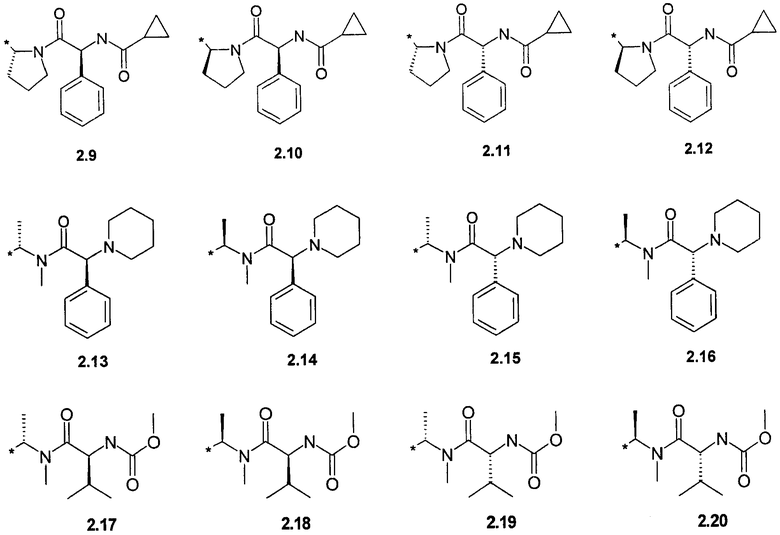
R1 и R2 представляют собой необязательно одинаковые радикалы, выбранные из 2.1-2.20, в которых звездочкой (*) указаны места присоединения к азольным фрагментам;
А представляет собой:
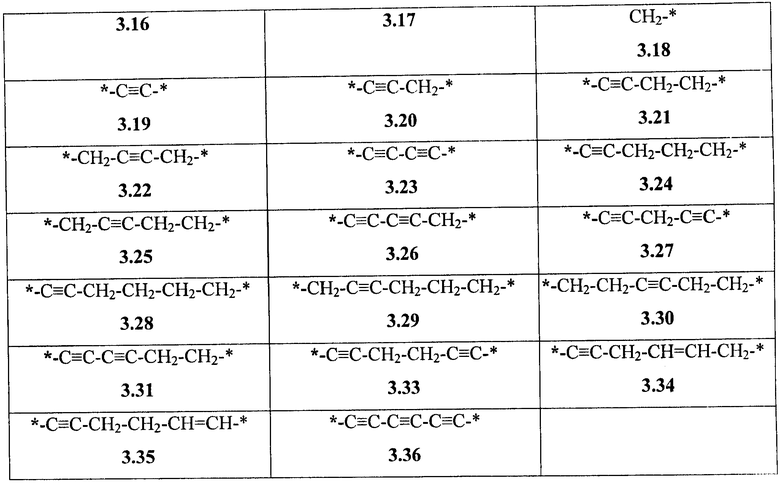
- алифатический C2-C8 бирадикал, выбранный из бирадикалов 3.1-3.36, в которых звездочкой (*) указаны места присоединения азольных фрагментов;

- диоксановый, цикло- и бициклоалифатический бирадикал, выбранный из бирадикалов 3.37-3.47, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
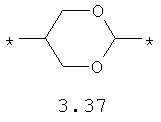
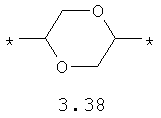
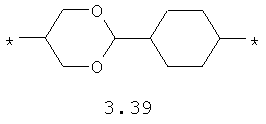
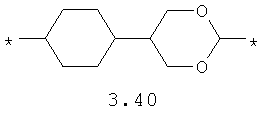
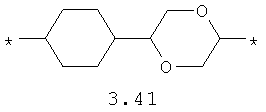
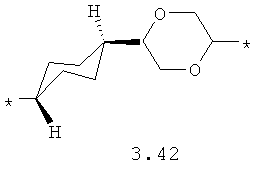
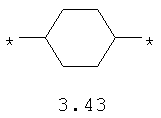
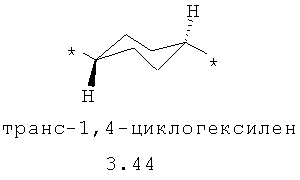

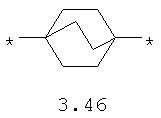
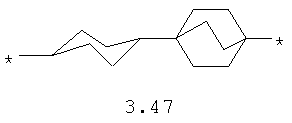
- алкилоксиалкильный, алкенилоксиалкильный, алкинилоксиалкильный бирадикалы и их тиоаналоги, предпочтительно формулы 3.48-3.56, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
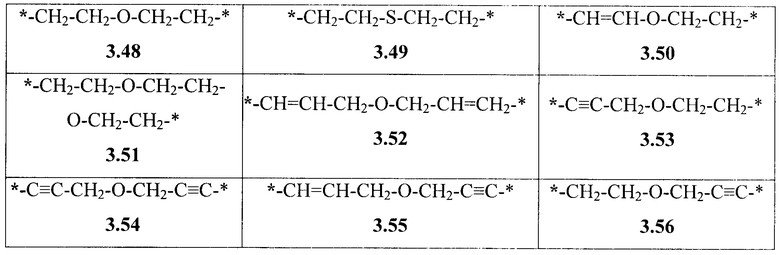
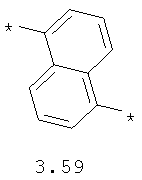
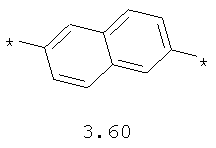
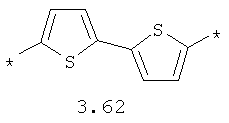
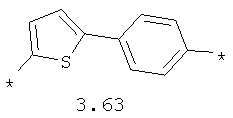
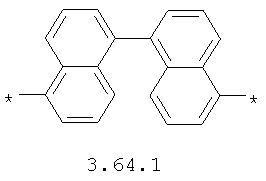
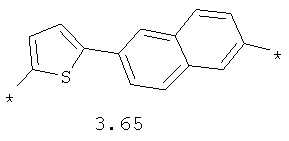
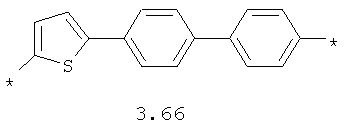
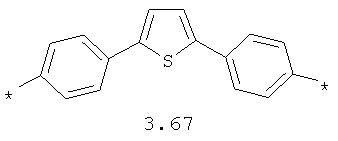
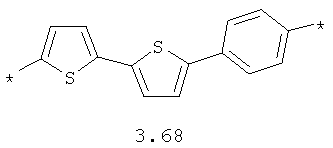
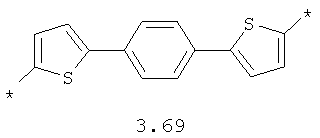
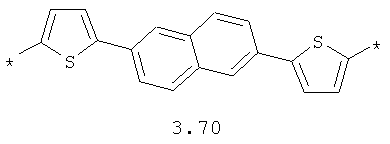
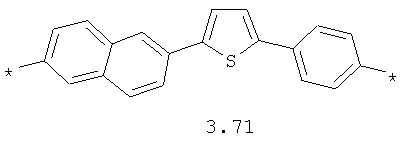
- арильный и тиофеновый бирадикалы, выбранные из бирадикалов 3.57-3.71, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
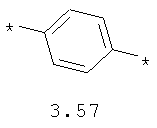



- алкинилциклоалкильный, алкинилдиоксановый, алкиниларильный, алкилтиофеновый, алкенилтиофеновый и алкинилтиофеновый бирадикал, выбранный из бирадикалов 3.72-3.129, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
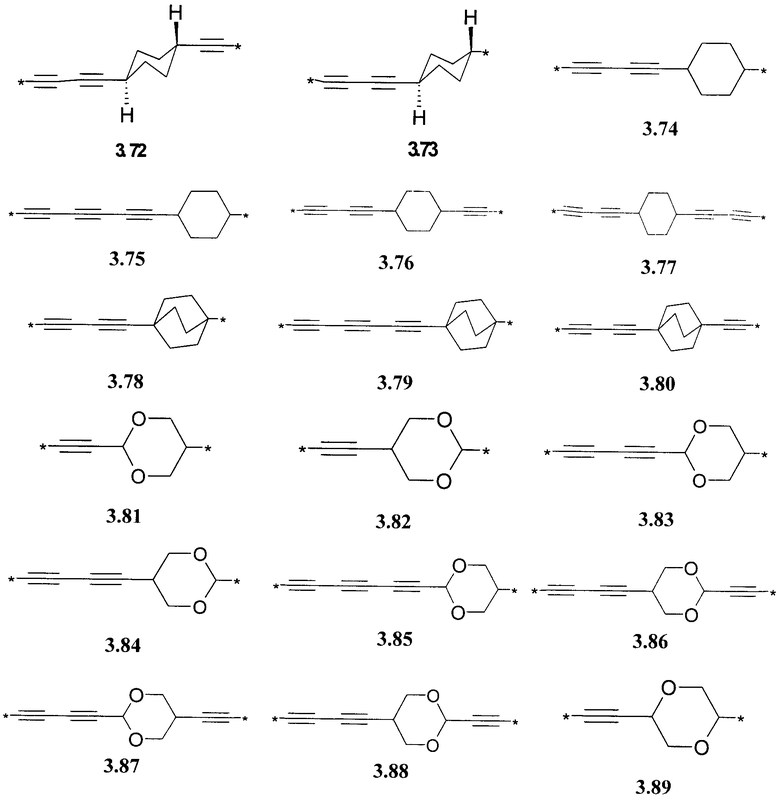
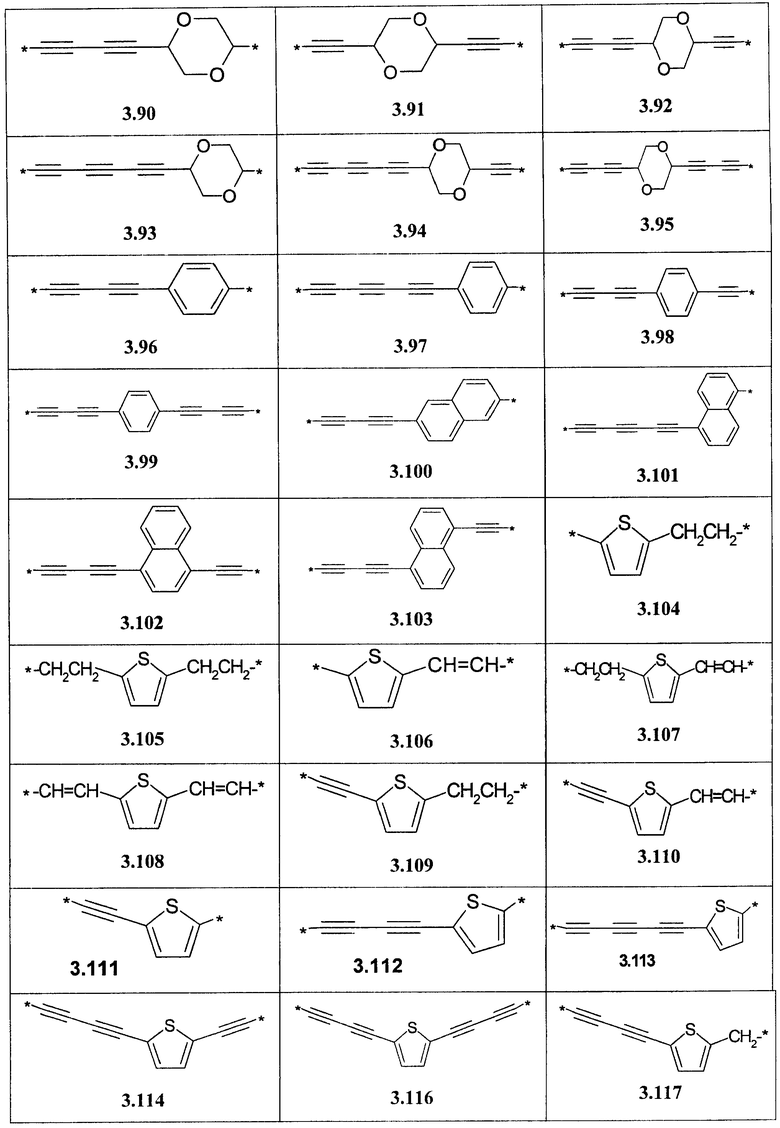
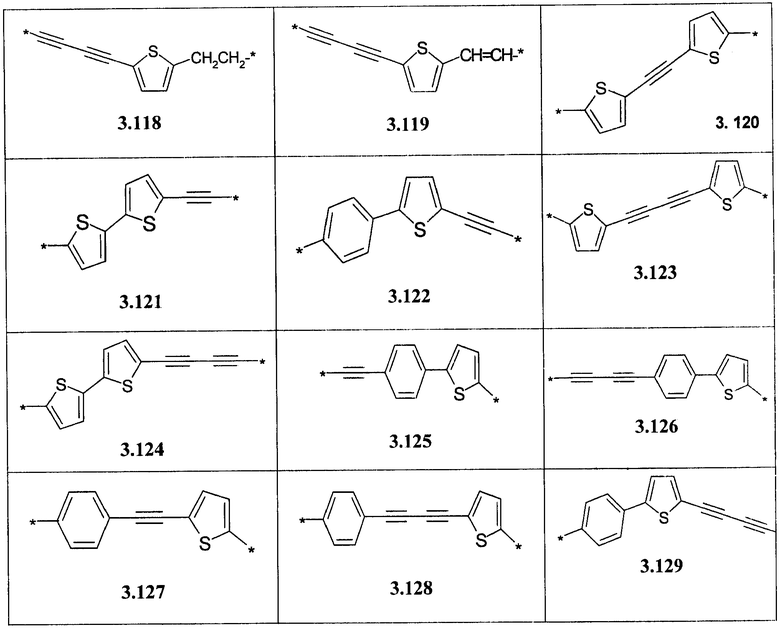
- алкилоксиарильный, алкенилоксиарильный, алкинилоксиарильный бирадикал, выбранный из бирадикалов 3.130-3.136, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
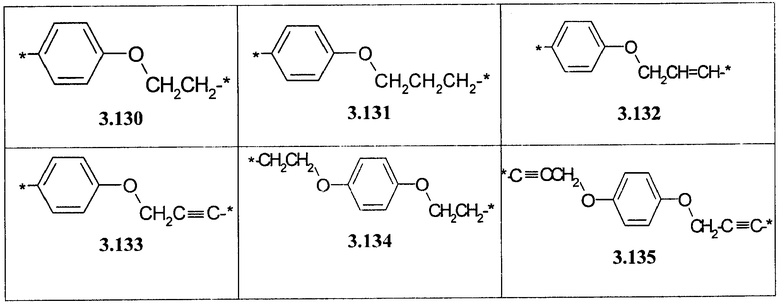
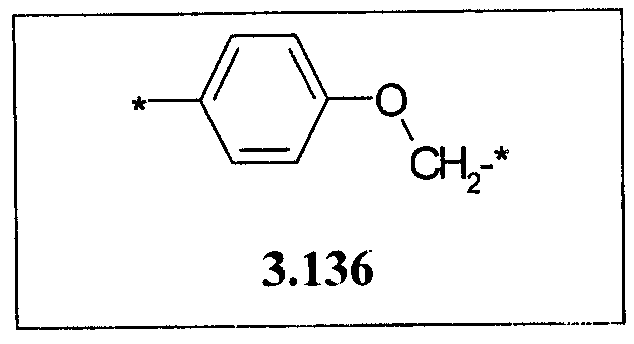
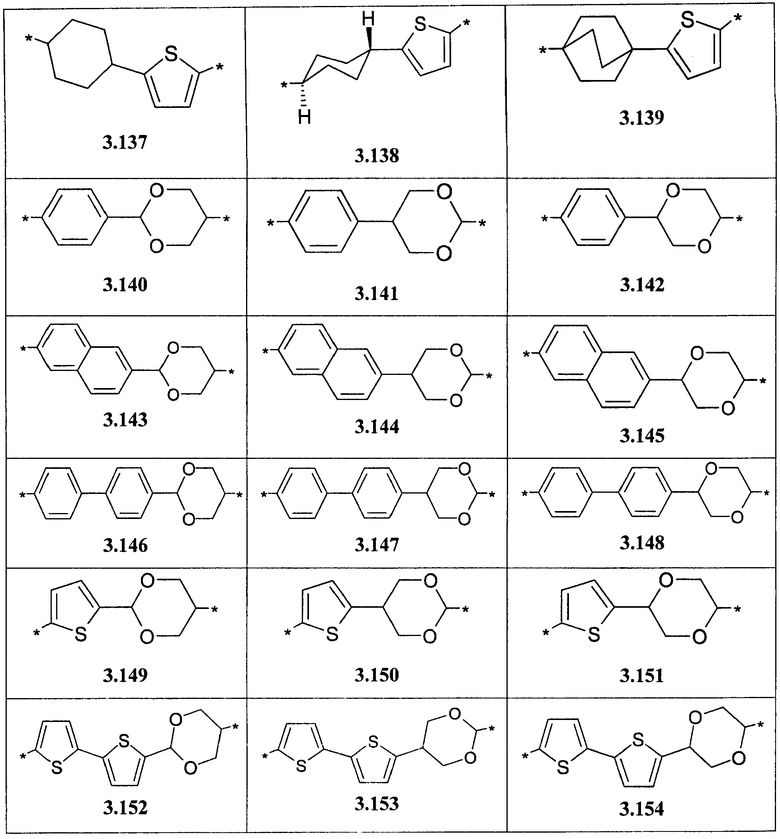
- циклоалкилтиофеновый, арилдиоксановый и тиофендиоксановый бирадикал, выбранный из бирадикалов 3.137-3.154, в которых звездочкой (*) указаны места присоединения азольных фрагментов,
а также
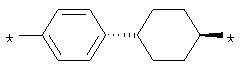
при условии, что в одном из азольных колец Y=NH, а в другом Y=О, R1=R2=2.3.
В представляет собой:
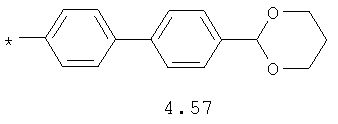
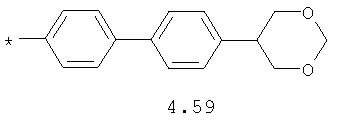
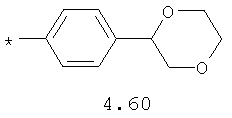
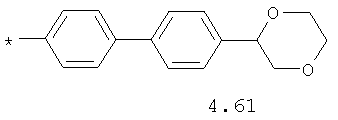
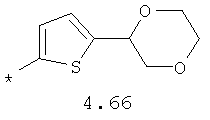
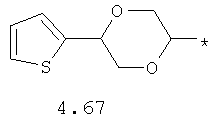
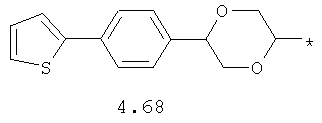
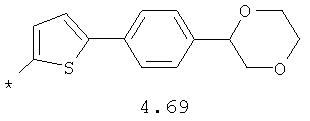
- алифатический C2-C8 радикал, выбранный из радикалов 4.1-4.12, в которых звездочкой (*) указано место присоединения азольного фрагмента;


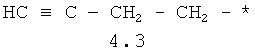
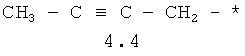

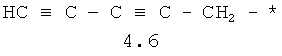
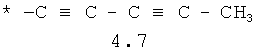
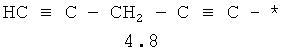
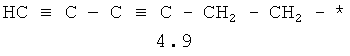
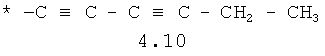

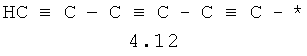
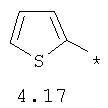
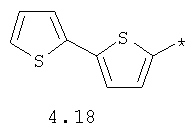
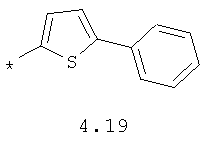
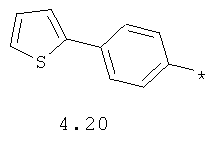
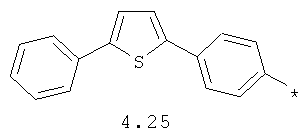
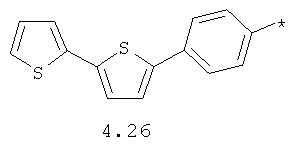
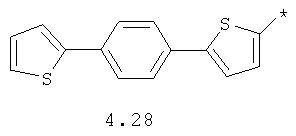
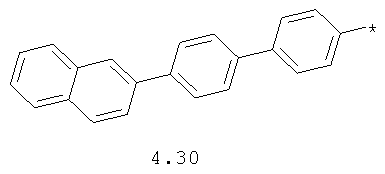
- арильный и тиофенильный радикал, выбранный из радикалов 4.13-4.30, в которых звездочкой (*) указано место присоединения азольного фрагмента;
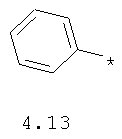
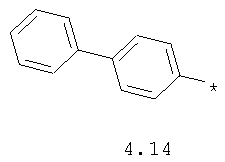
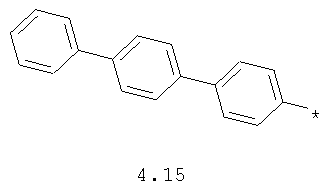
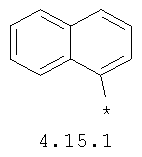

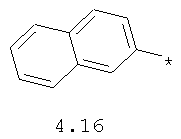
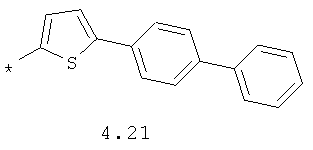
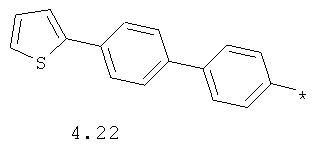
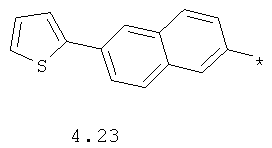
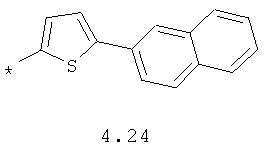


- алкинилциклоалкильный, алкиниларильный, алкилтиофеновый и алкинилтиофеновый радикал 4.31-4.47, в которых звездочкой (*) указано место присоединения азольного фрагмента;
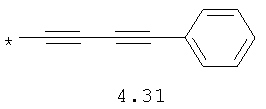
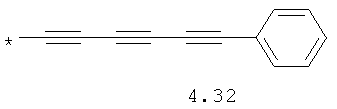
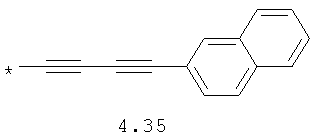
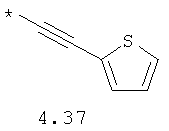

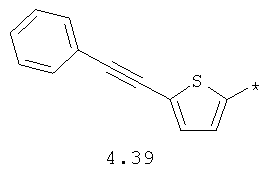
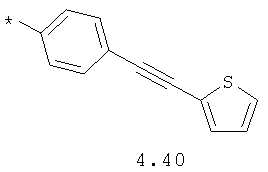

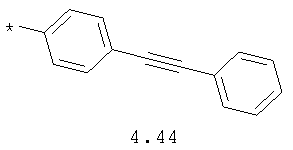
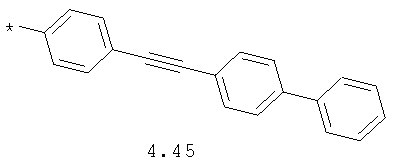
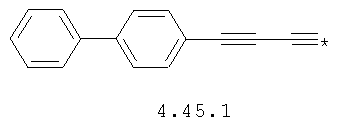
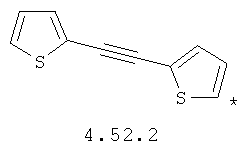


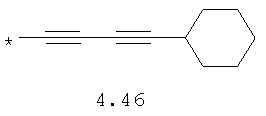
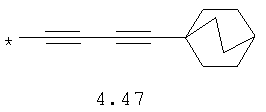
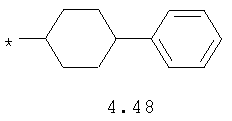
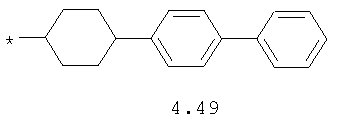
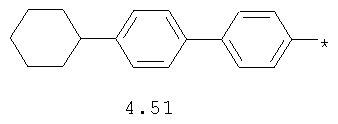
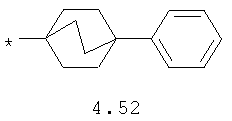
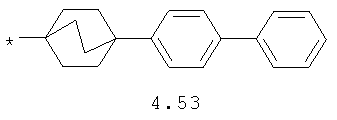
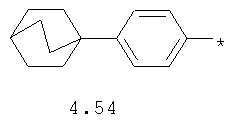
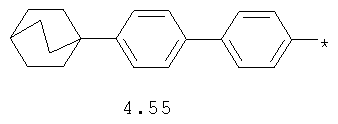
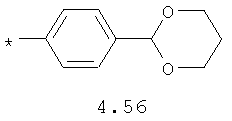
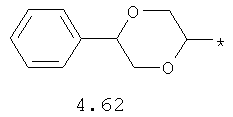
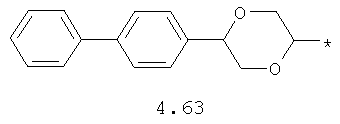
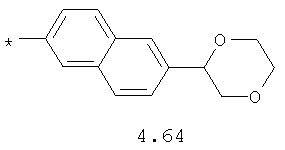
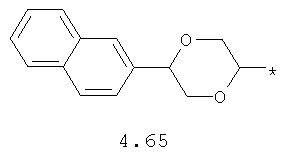
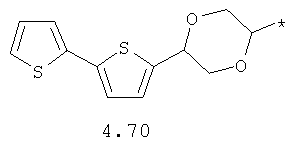
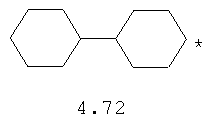
- циклоалкилбензольный, 4-циклоалкилбифенильный, (бициклооктан)бензольный, 4-(бициклооктан)бифенильный, арилдиоксановый и тиофендиоксановый радикал, выбранный из радикалов 4.48-4.72, в которых звездочкой (*) указано место присоединения азольного фрагмента.



Исключая:
((R)-1-{(R)-2-[5-(4-{2-[(R)-1-((R)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-бута-1,3-диинил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил]-карбаминовая кислота метиловый эфир;
((S)-1-{(S)-2-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-фенил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовая кислота метиловый эфир дигидрохлорид;
((S)-1-{(S)-2-[5-(6-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-2-ил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовая кислота метиловый эфир дигидрохлорид;
[(S)-1-((S)-2-{5-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-фенил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовая кислота метиловый эфир;
диметил (2S,2'S)-1,1'-((2R,2'R)-2,2'-(5,5'-(4,4'-(тиофен-2,5-диил)бис(4,1-фенилен))бис(1Н-имидазол-5,2-диил))бис(пирролидин-2,1-диил))бис(3-метил-1-оксобутан-2,1-диил)дикарбамат.
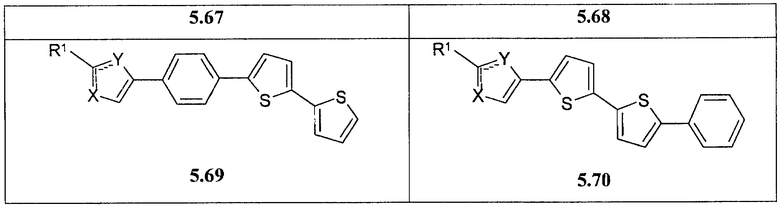
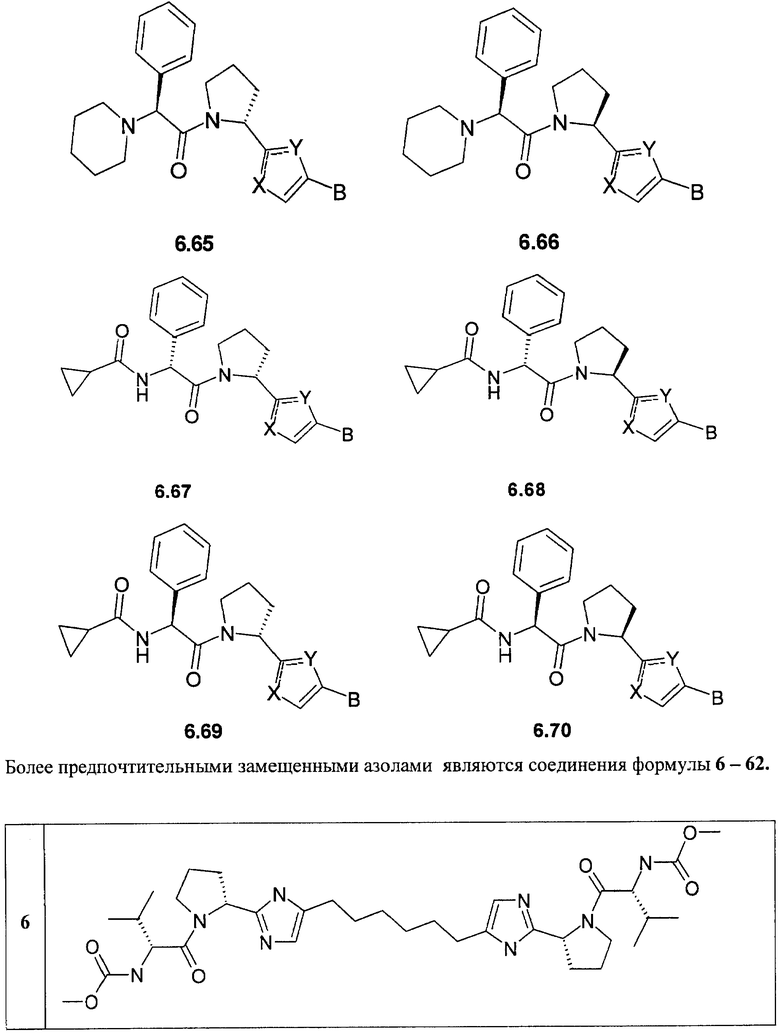
Более предпочтительными замещенными азолами являются соединения общей формулы 5.1-5.70, в которых X, Y, R1, R2 и сплошные линии с сопровождающими их пунктирными линиями 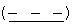 имеют вышеуказанное значение.
имеют вышеуказанное значение.
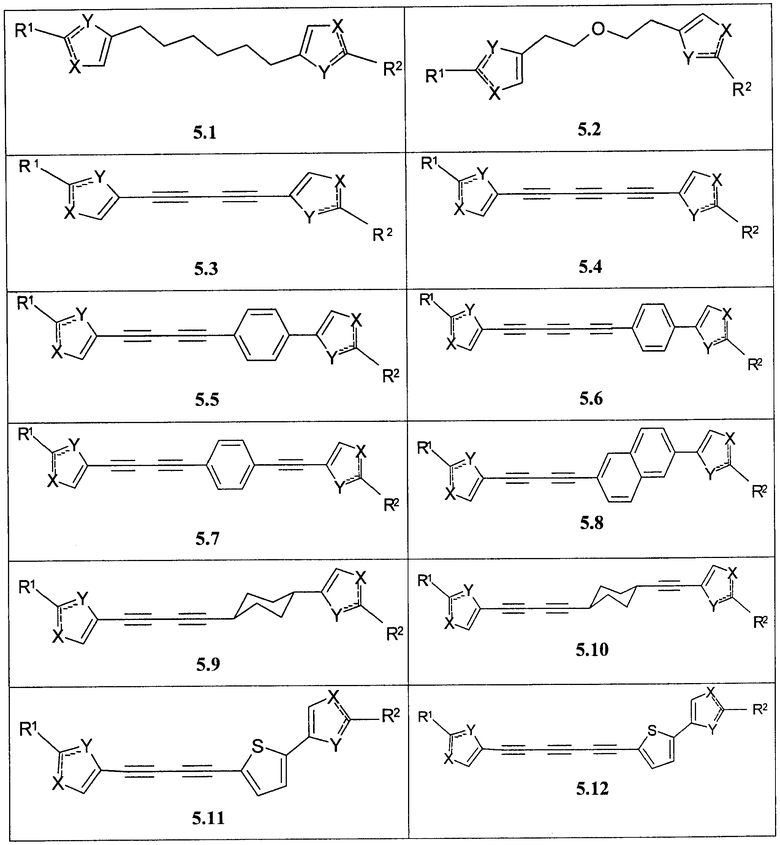
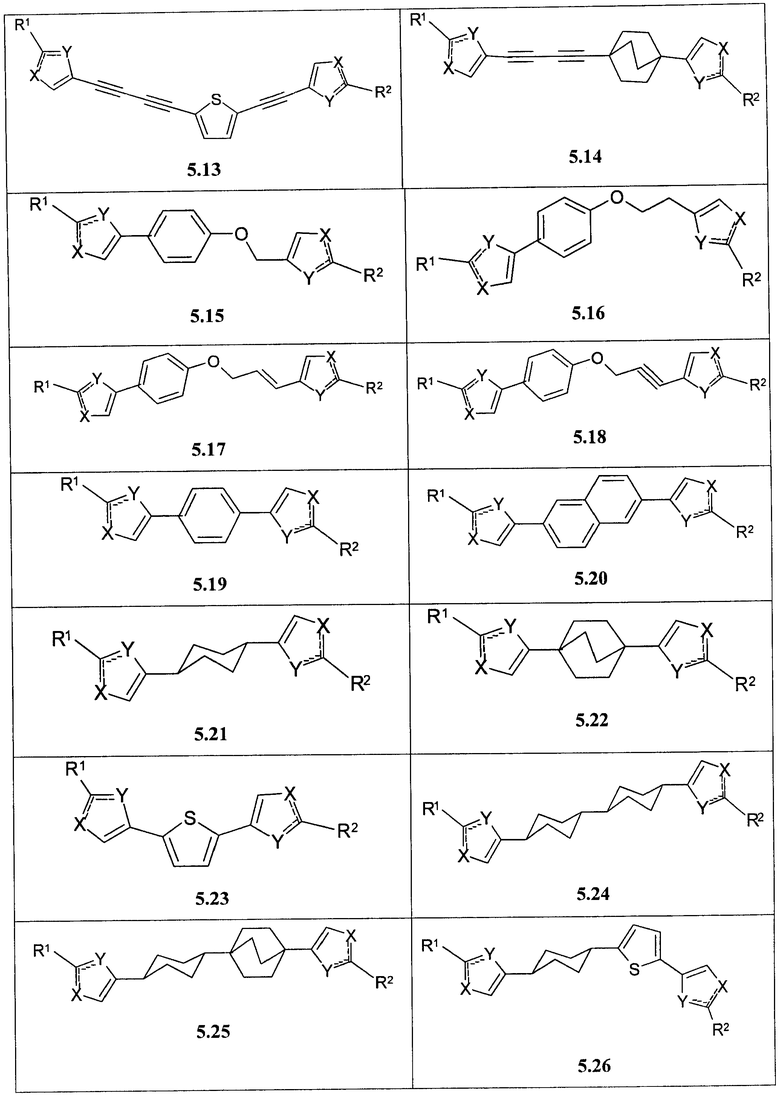
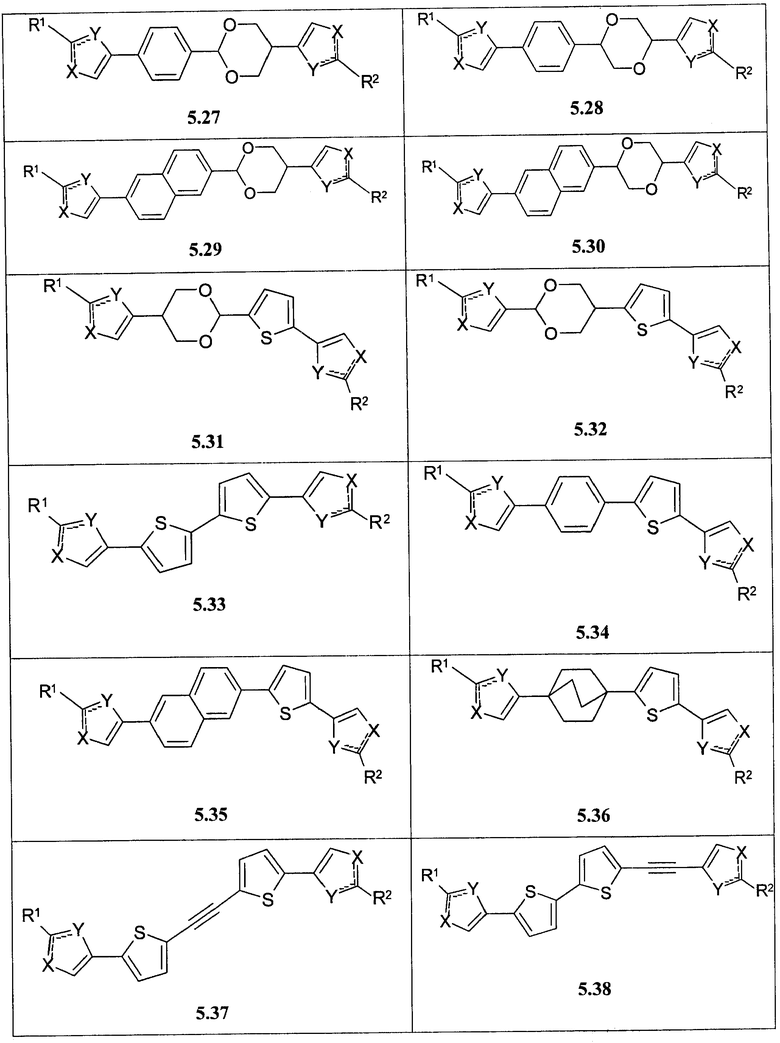
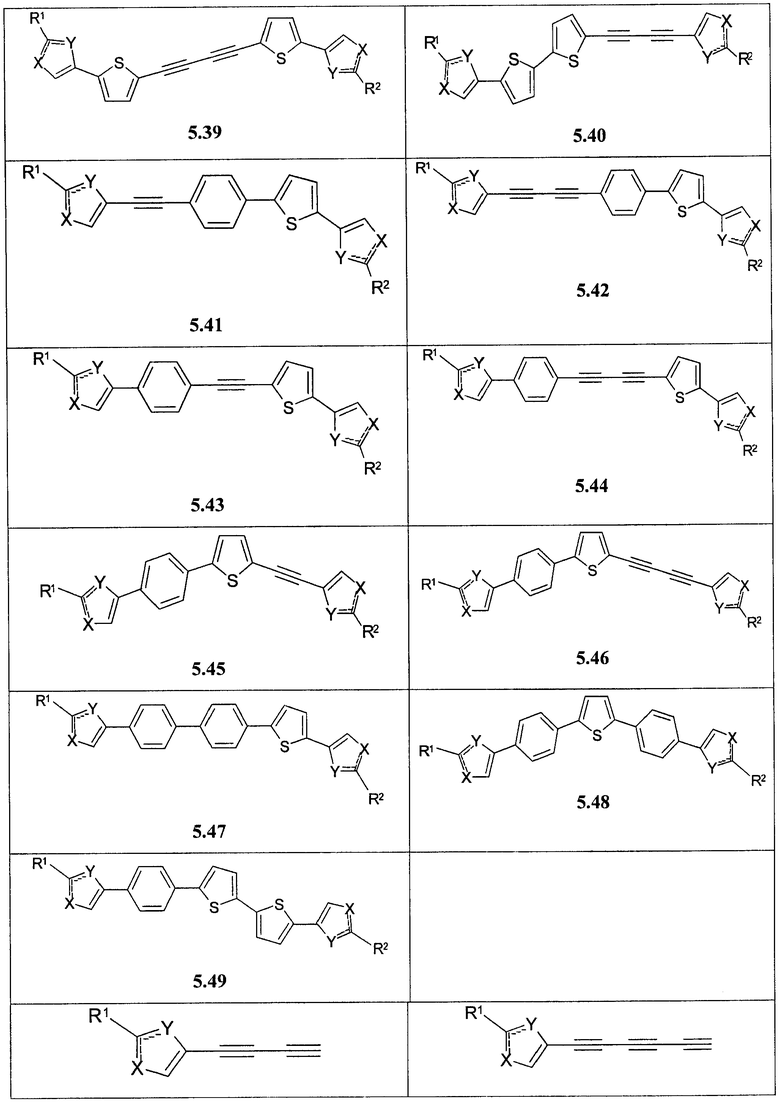
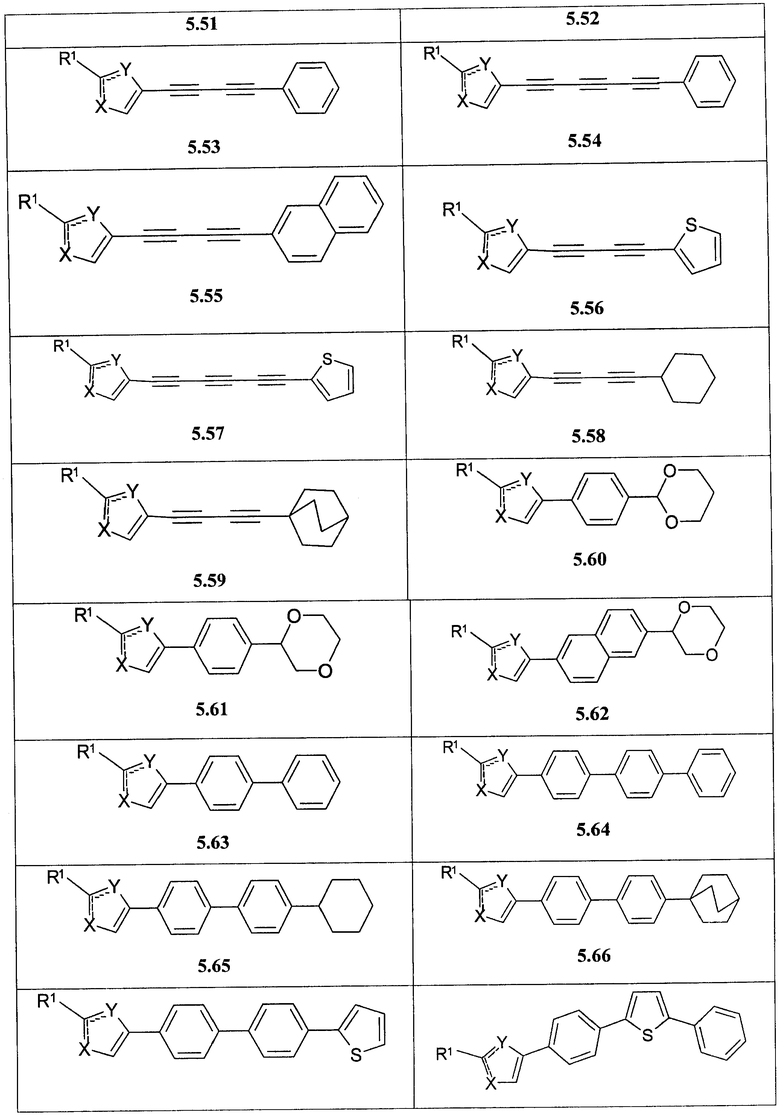
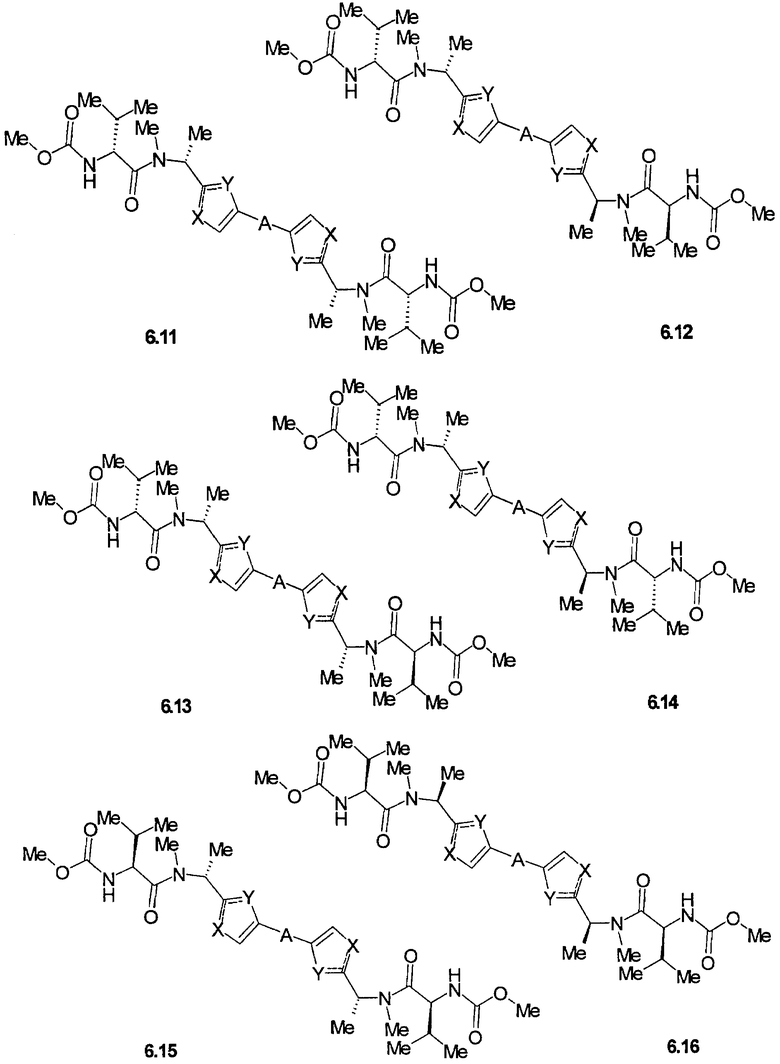
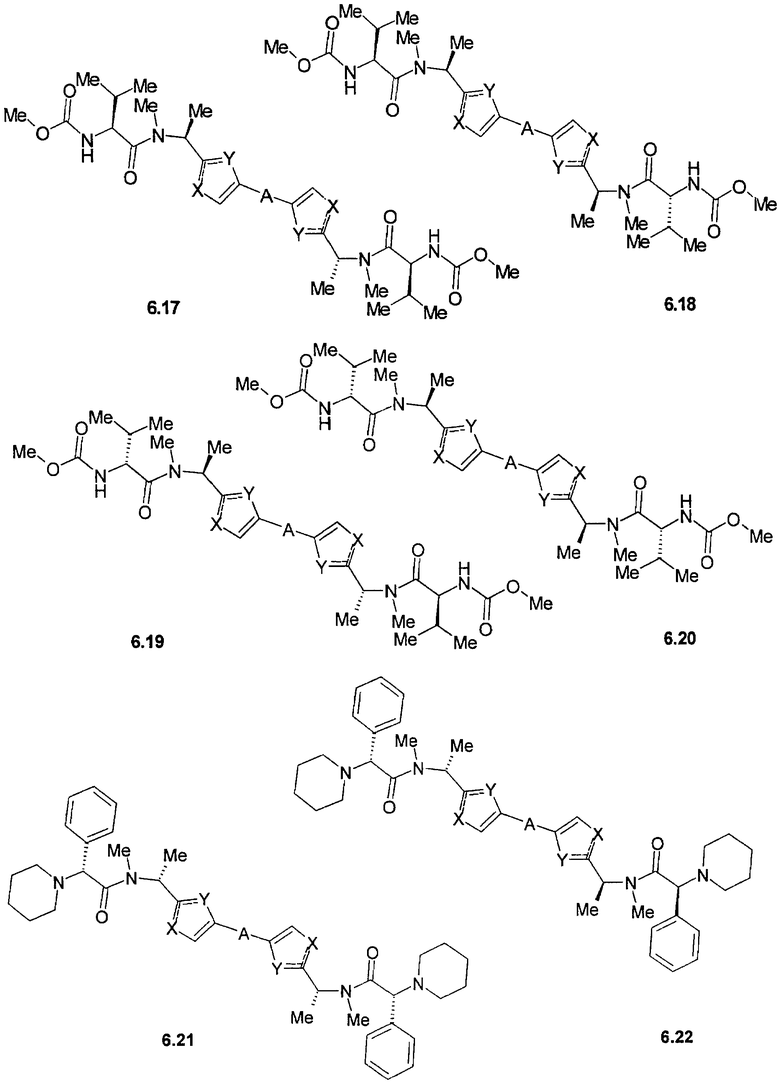
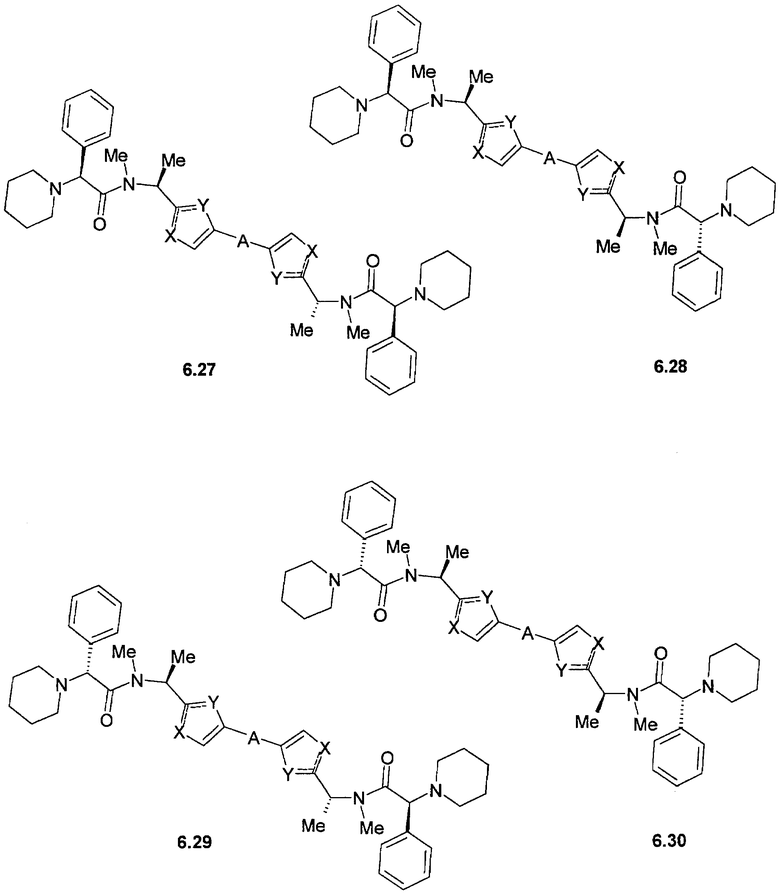
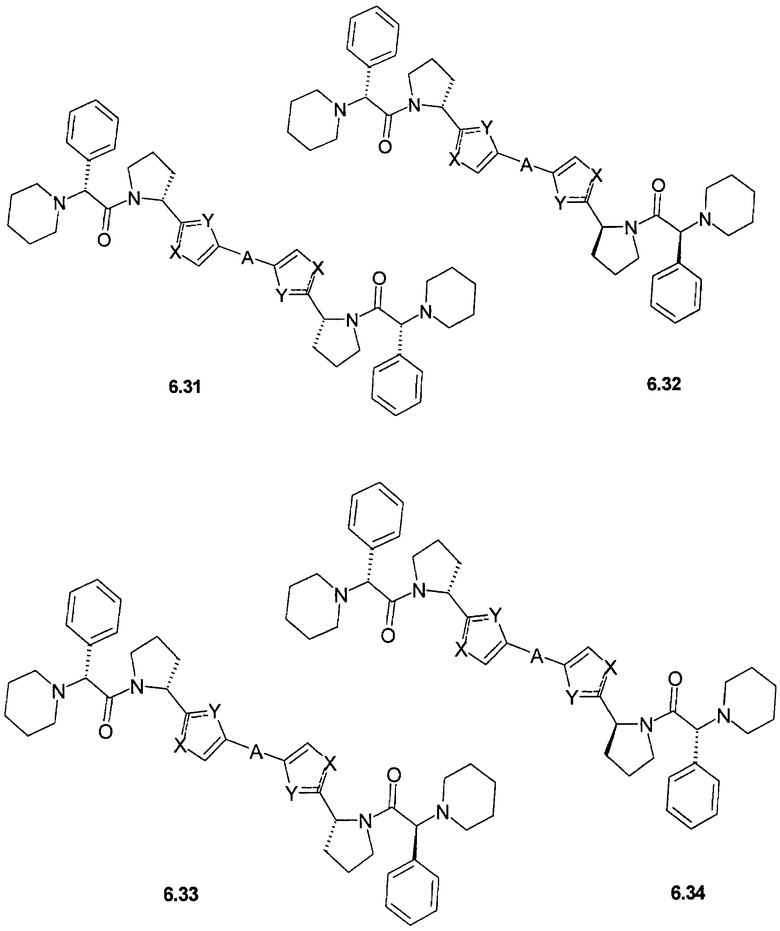
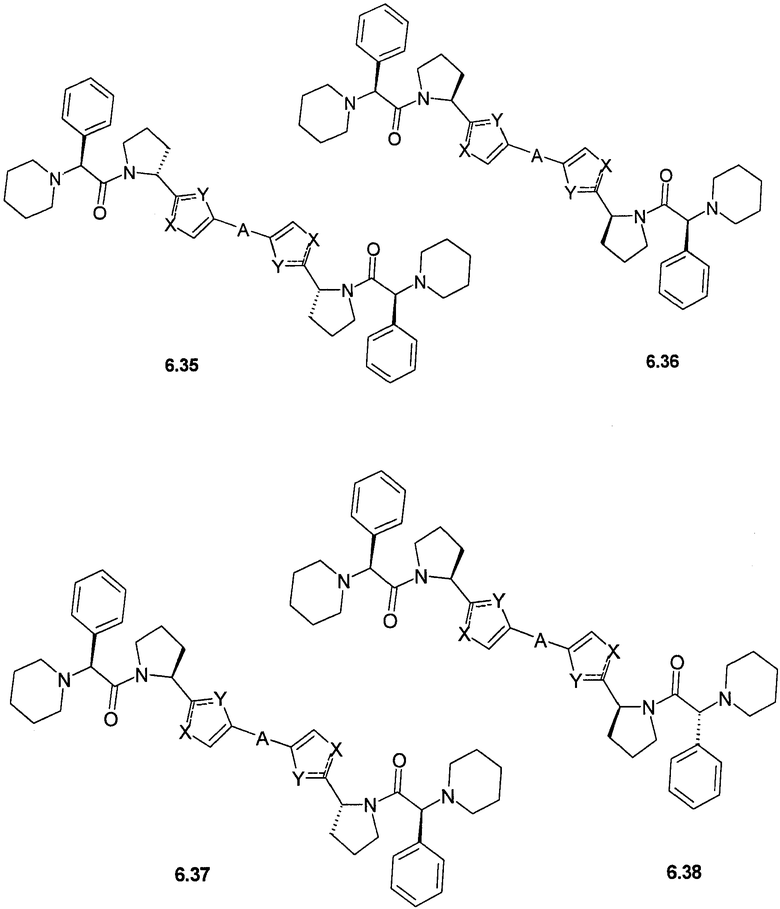
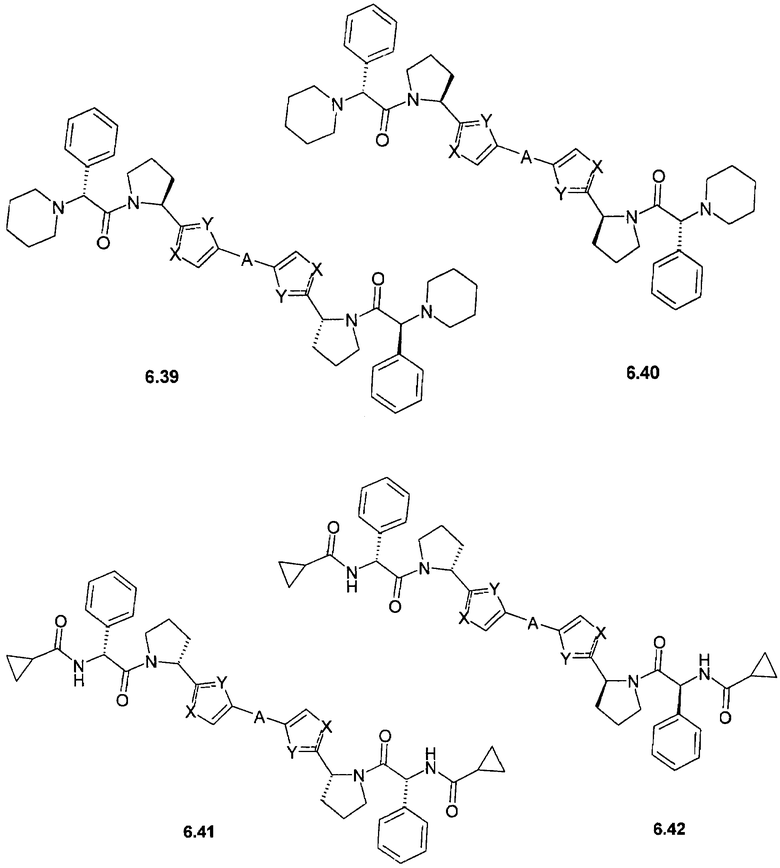
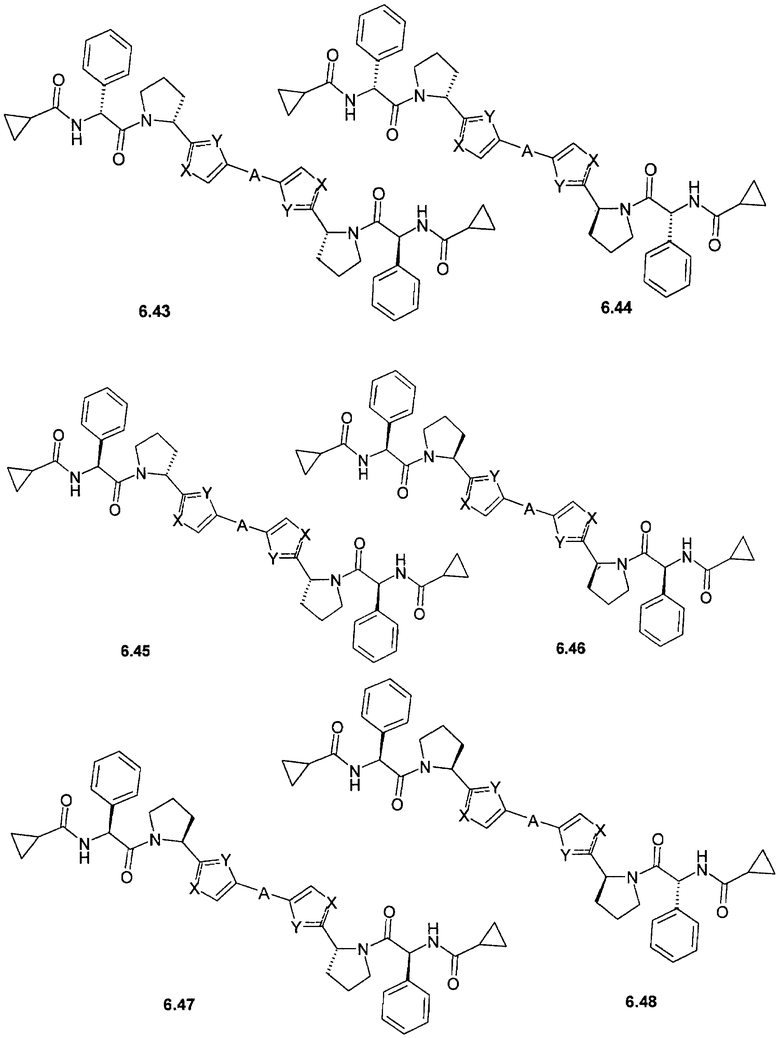
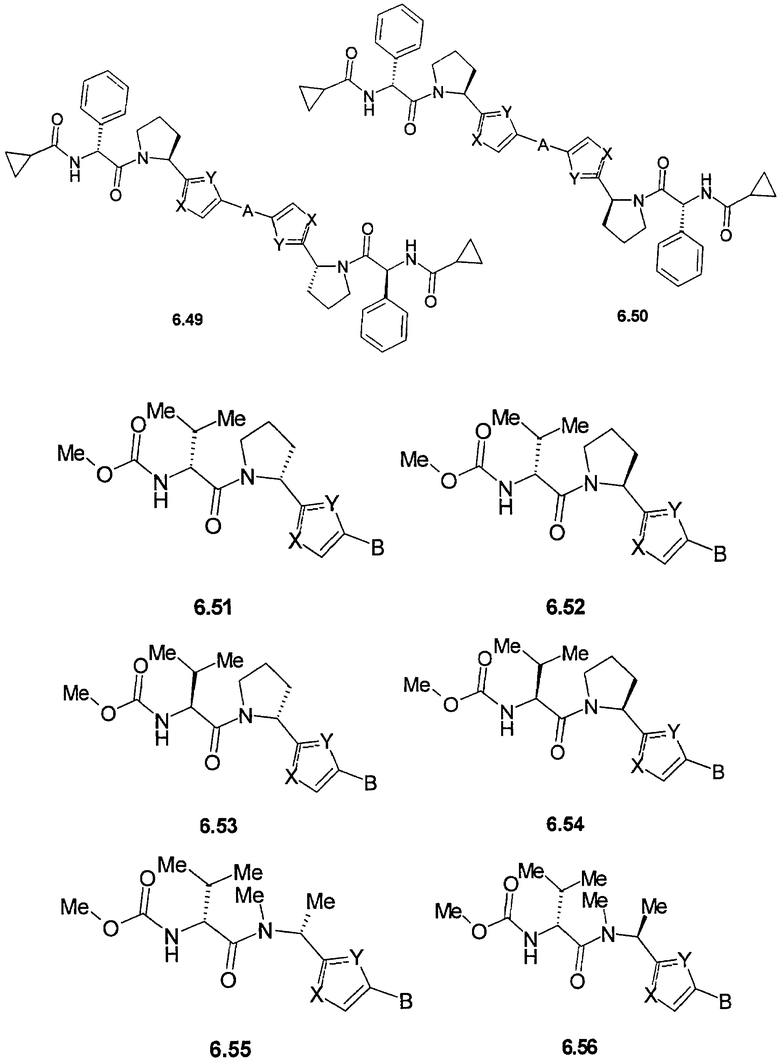
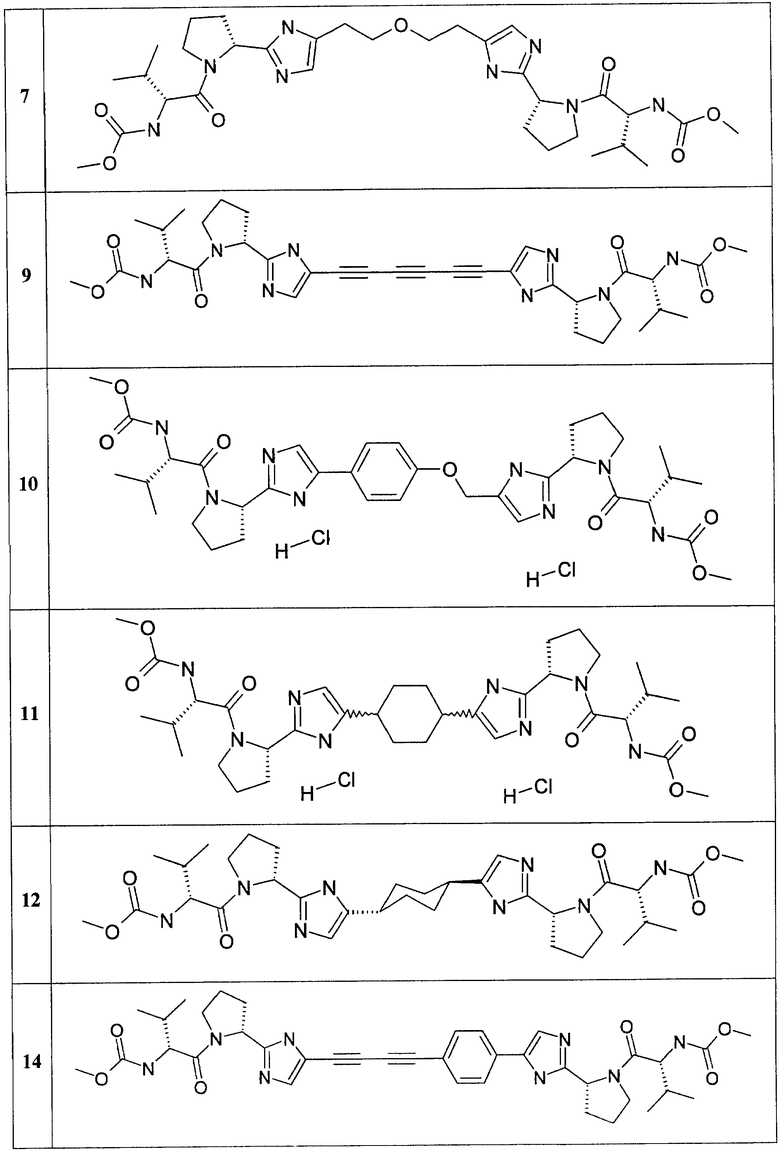
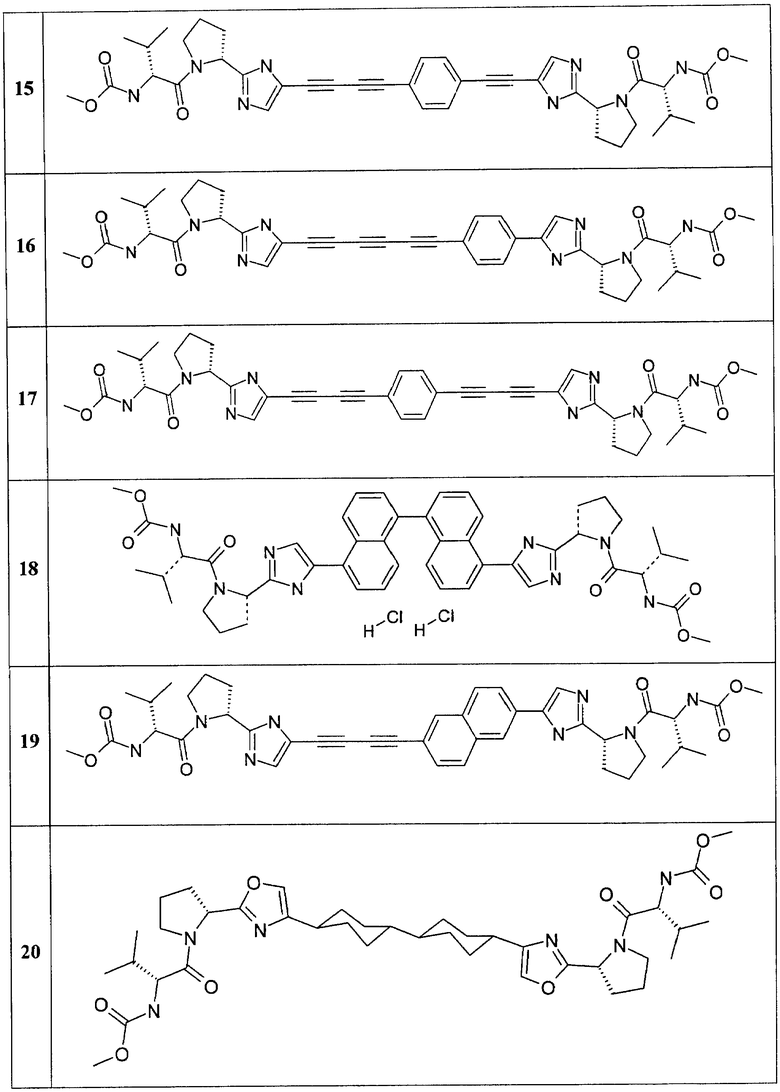
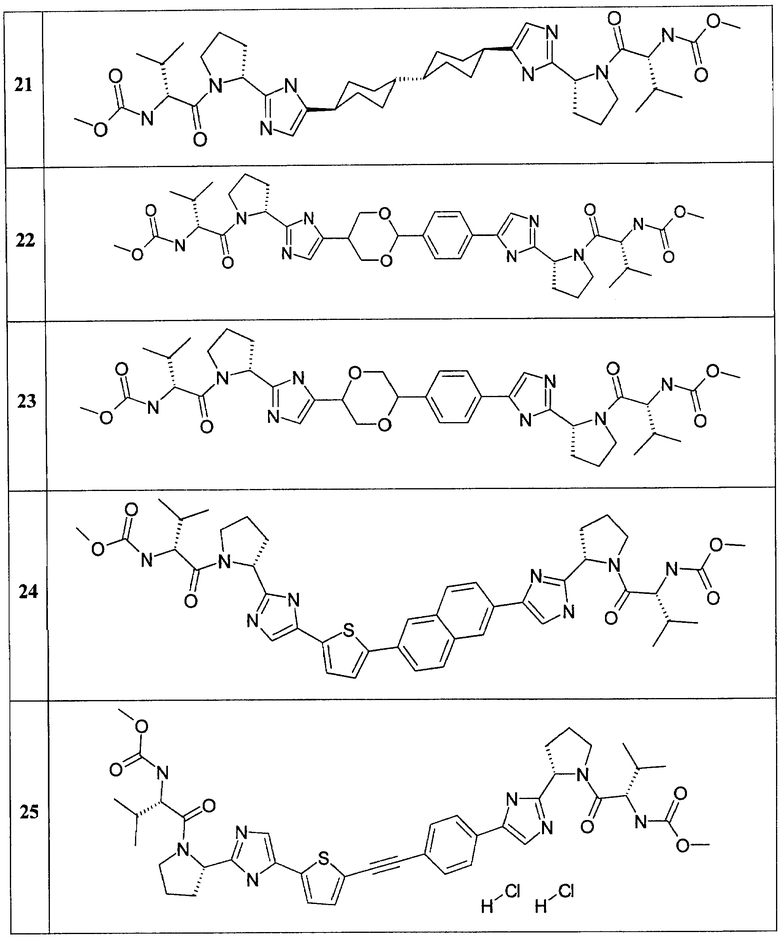
Более предпочтительными замещенными азолами являются соединения общей формулы 6.1-6.70, в которых А, X, Y и сплошные линии с сопровождающими их пунктирными линиями 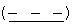 имеют вышеуказанное значение.
имеют вышеуказанное значение.
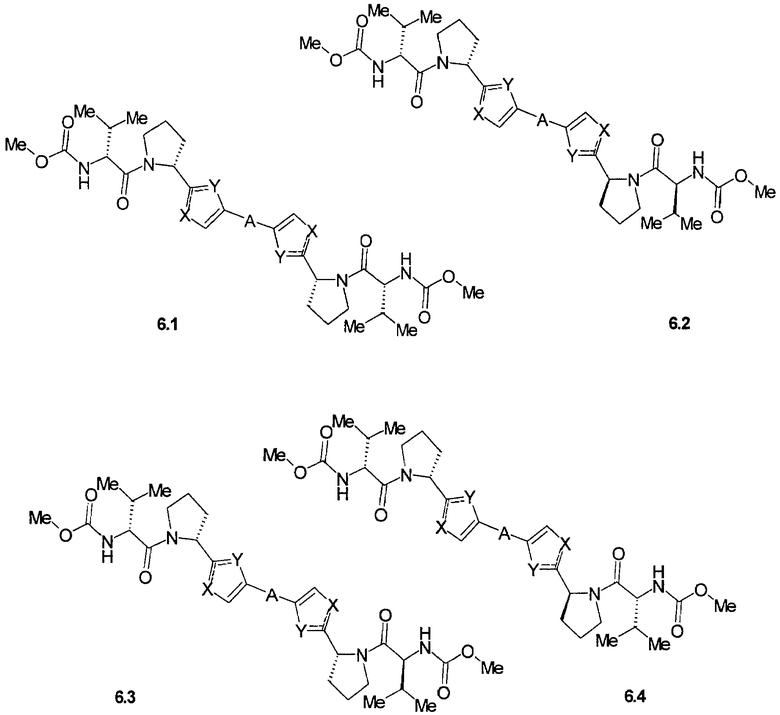
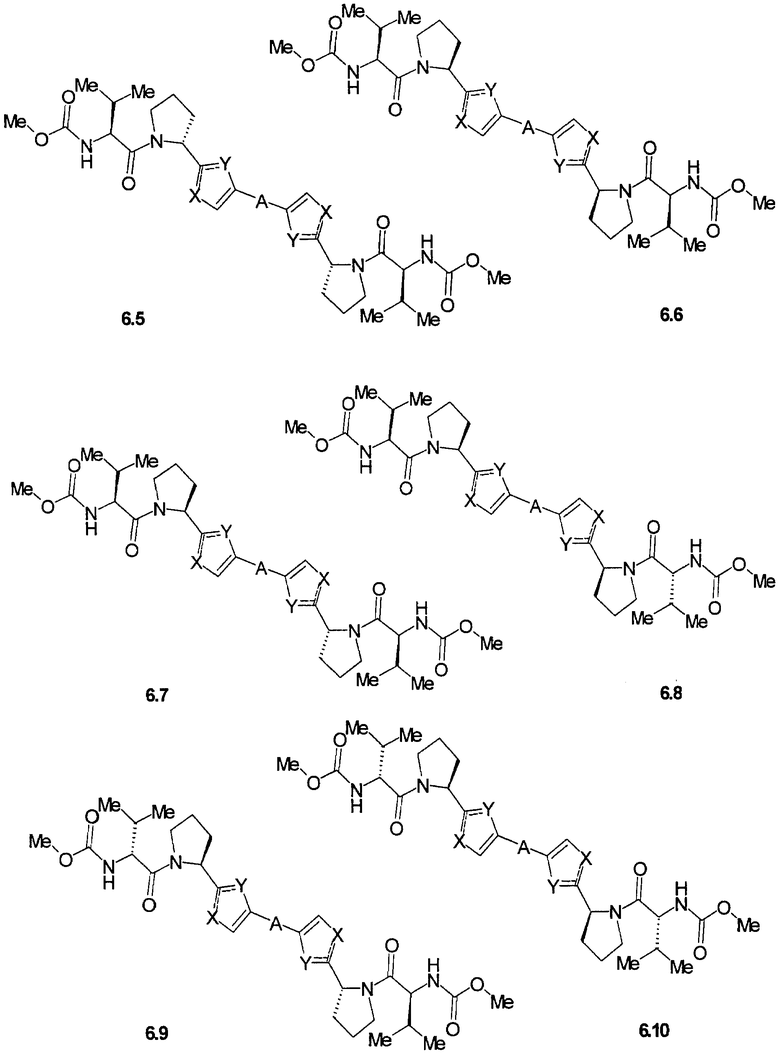



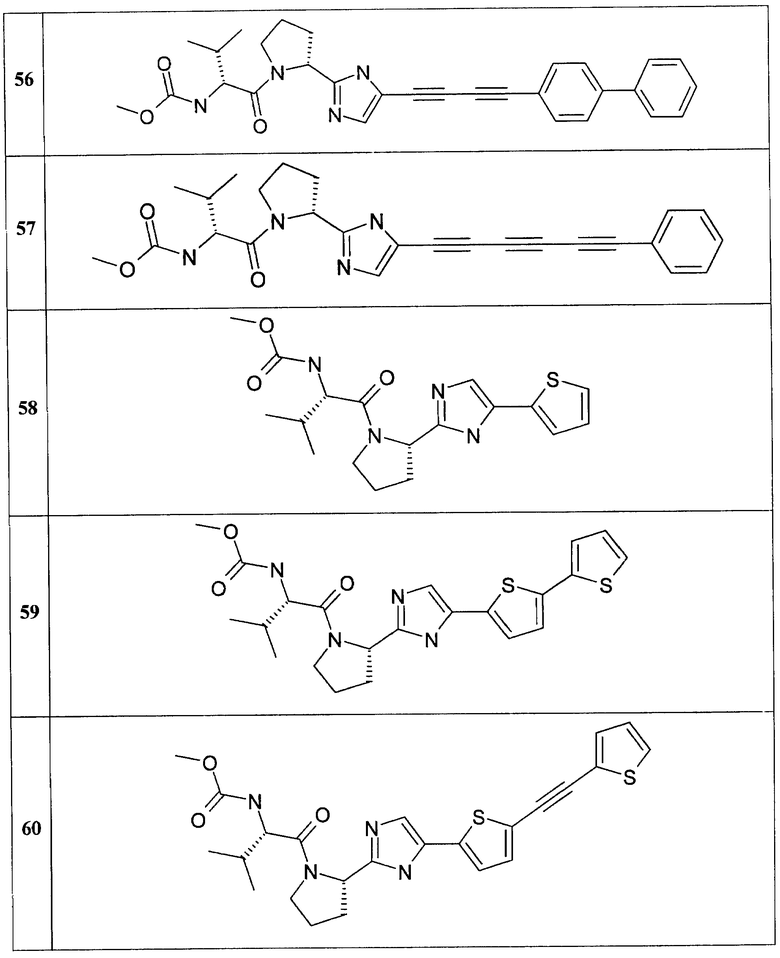
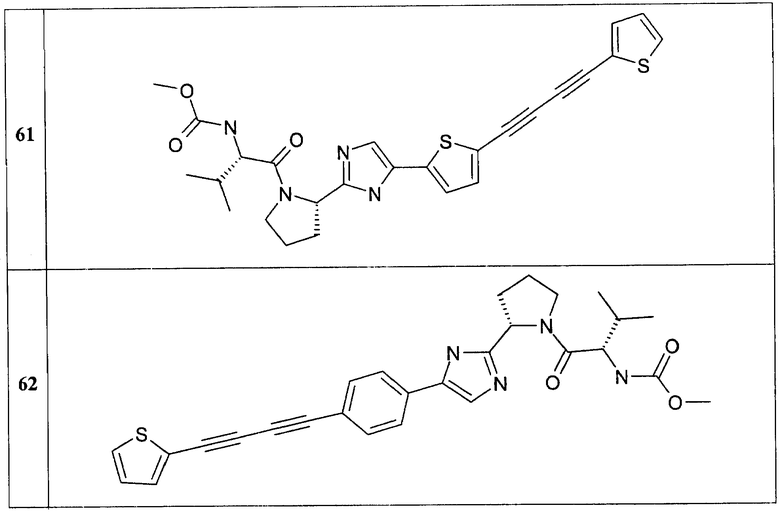
Замещенные азолы общей формулы 1А и 1В по данному изобретению были получены с использованием известных химических реакций и коммерческих реагентов. Строение полученных соединений подтверждено данными LCMS и ЯМР спектроскопии. Соединения названы с использованием Chem Draw (Chembridge Soft Inc.) программы.
В схемах использованы следующие сокращения: DIPEA - диизопропилэтиламин, EDAC - N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид, HOBt - 1-гидроксибензотриазол, N-Boc-L-Pro-OH - N-(трет-бутоксикарбонил)-L-пролин, N-Moc-L-Val-OH = N-(метоксикарбонил)-L-валин, RP HPLC - Обращенно-фазная Высокоэффективная жидкостная хроматография, ВЭЖХ - Высокоэффективная жидкостная хроматография, ДСМ=DCM - дихлорметан, DMF - N,N-диметилформамид, PdCl2dppf - [1,1'-Бис(дифенилфосфино)ферроцен]дихлорпалладий(II), TBTU - O-(Бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний тетрафторборат, DBU - 1,8-Диазабицикло[5.4.0]ундец-7-ен, ВГС - вирус гепатита С, ДМЕМ (DMEM) - Dulbecco's Modified Eagle Medium - Питательная среда ДМЕМ.
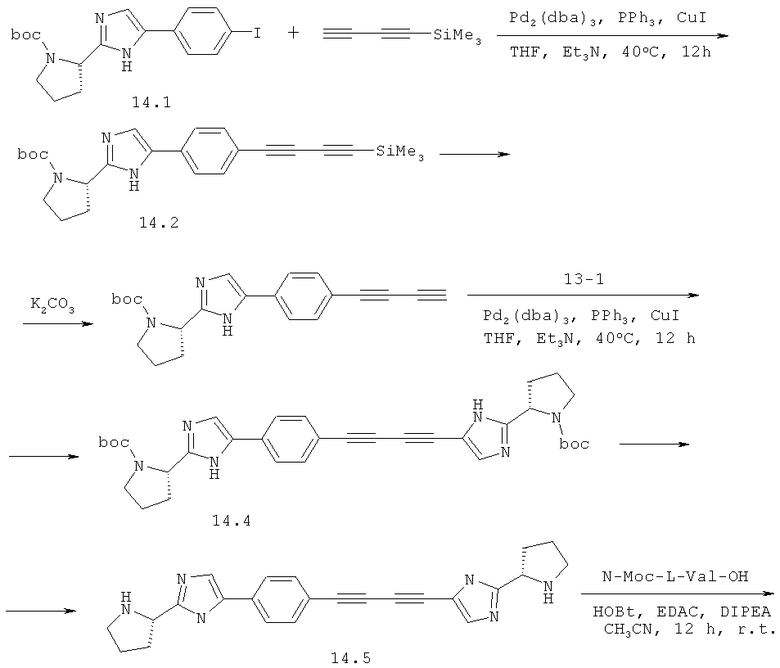
Так, метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты 14 получают по нижеследующей схеме:
 v
v
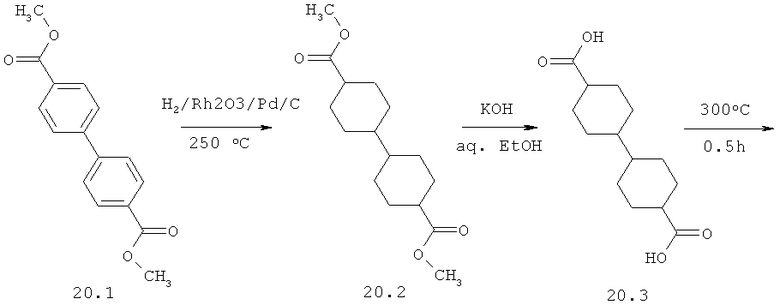
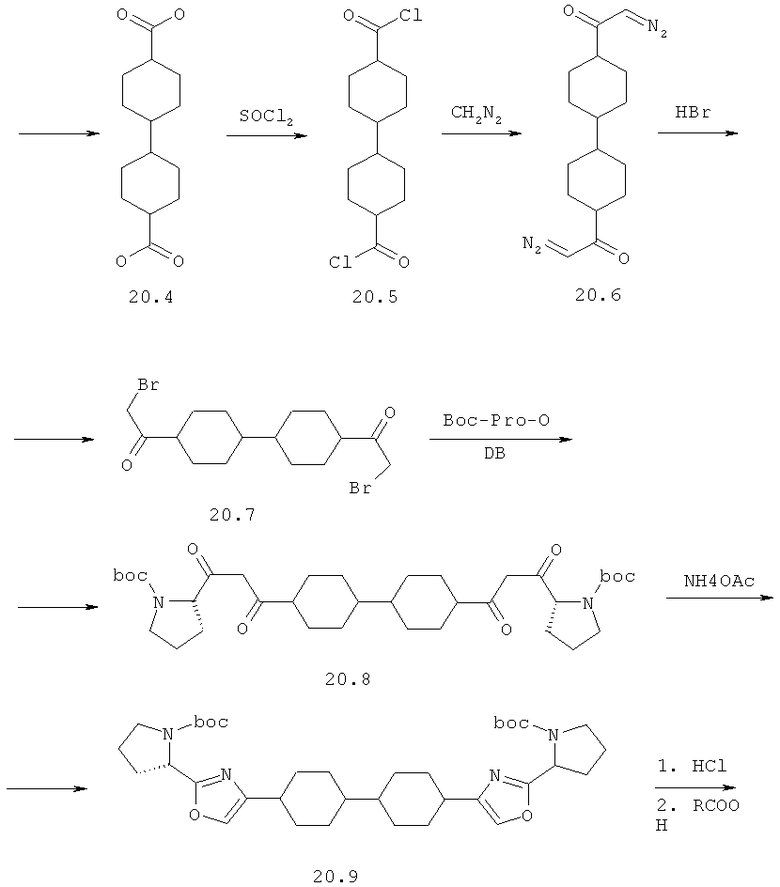
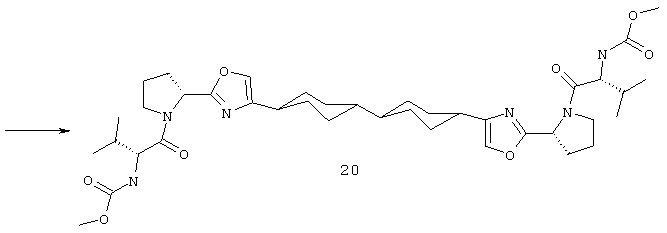
Диметиловый эфир [[1,1'-транс,транс-бициклогексил]-4,4'-диилбис[4,2-оксазолдиил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты 20 получают исходя из диметилового эфира дифенил-4,4'-дикарбоновой кислоты 20.1 по представленной ниже схеме.
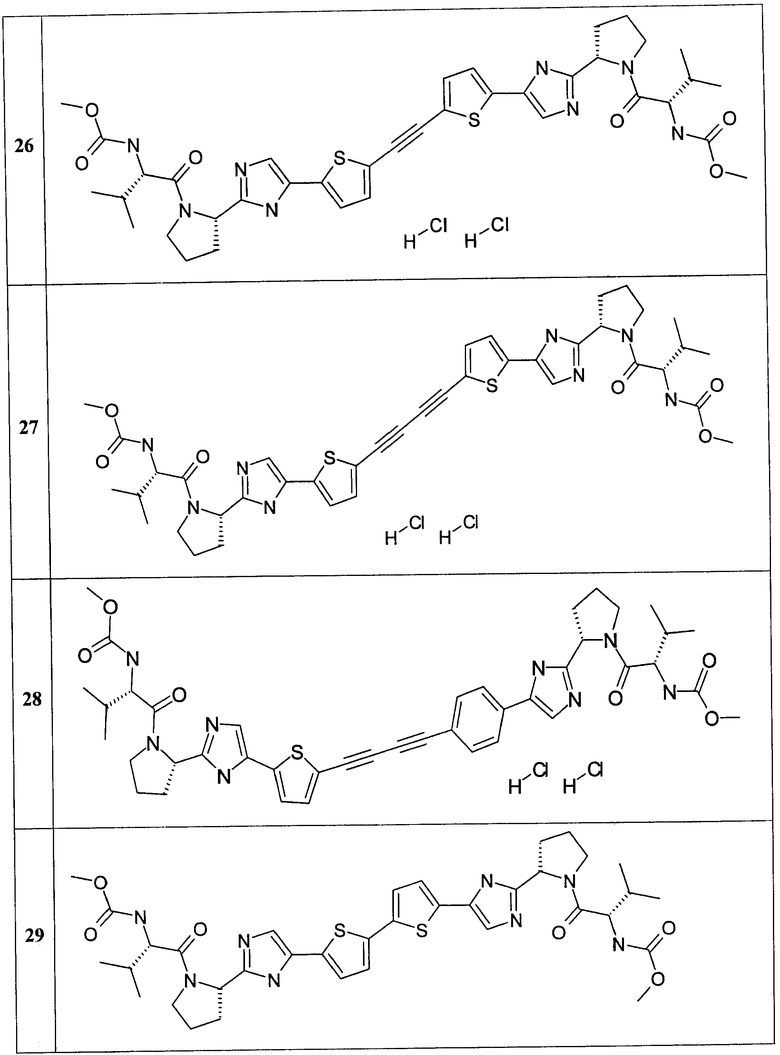
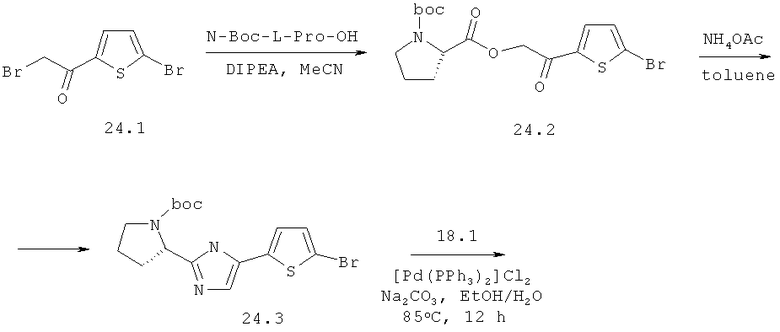
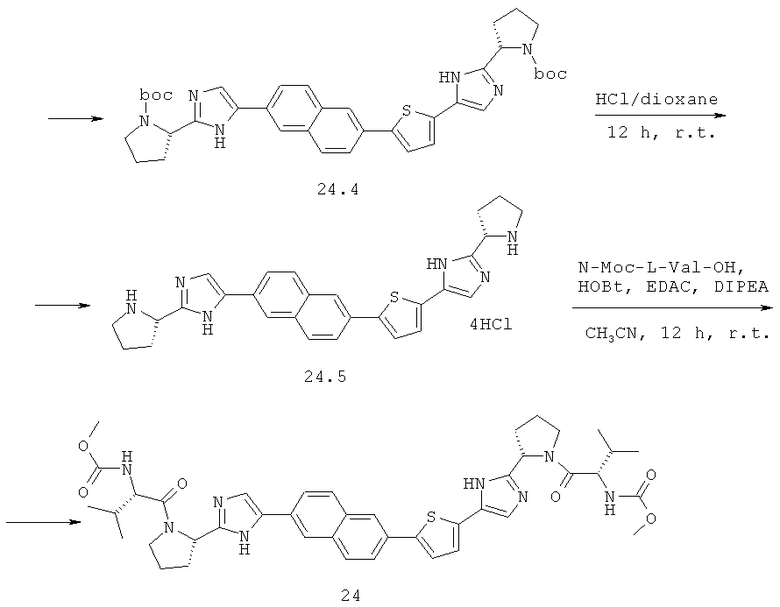
Метиловый эфир [(S)-1-((S)-2-{5-[5-(6-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-2-ил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 24 получен по нижеследующей схеме.
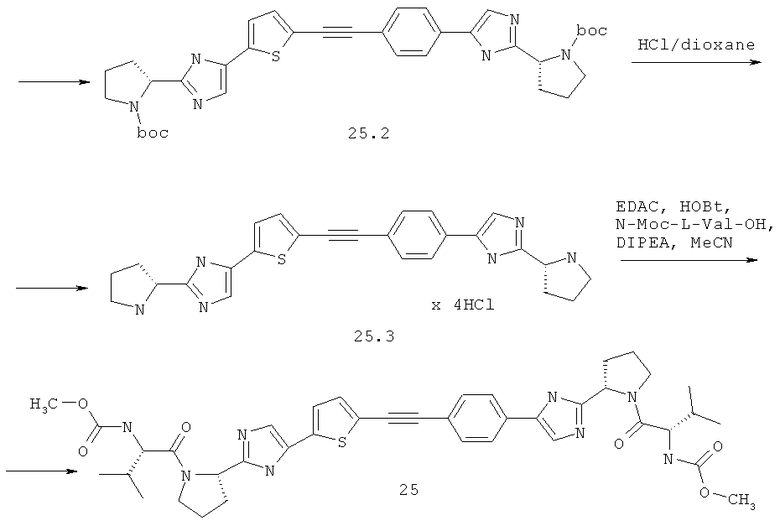
Метиловый эфир [(S)-1-((S)-2-{5-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирол)-пирролидин-2-ил]-3Н-имидазол-4-ил}-фенилэтинил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 25 получен по нижеследующей схеме.

Метиловый эфир ((S)-1-{(S)-2-[5-(5'-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-[2,2']битиофенил-5-ил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовой кислоты 30 получен по нижеследующей схеме.
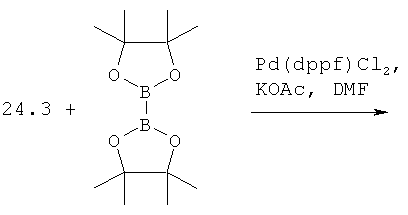

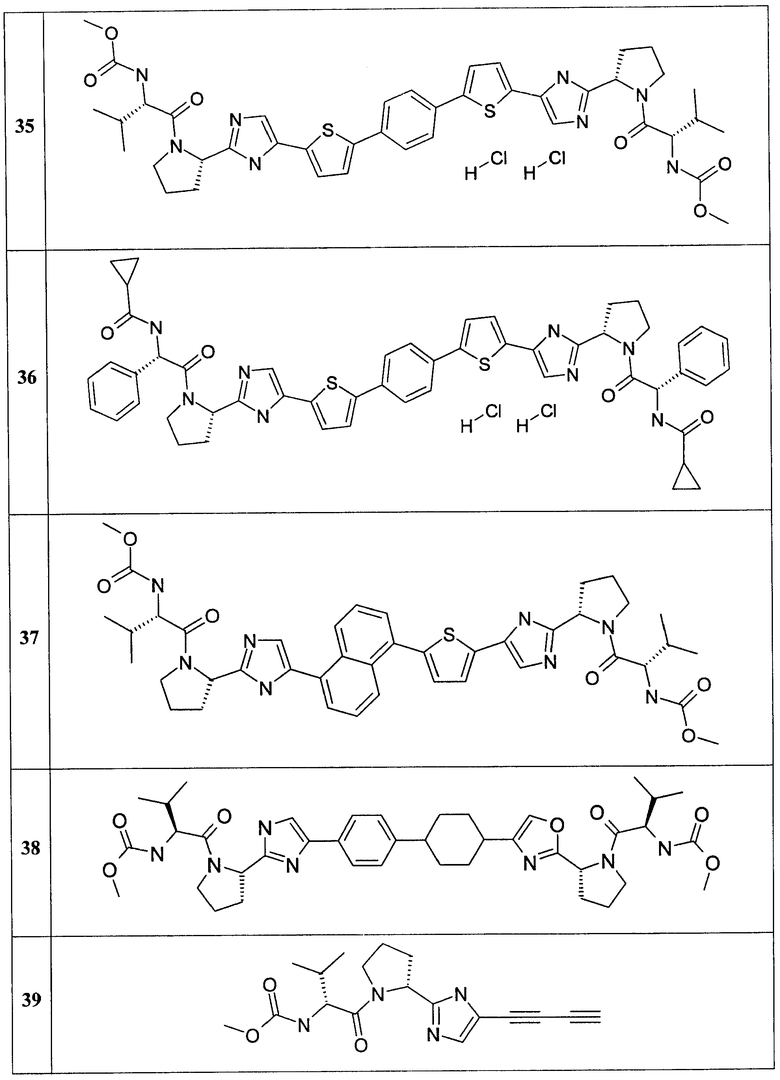
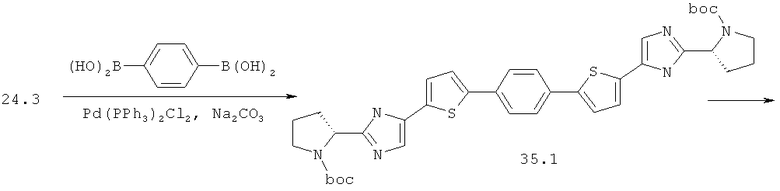
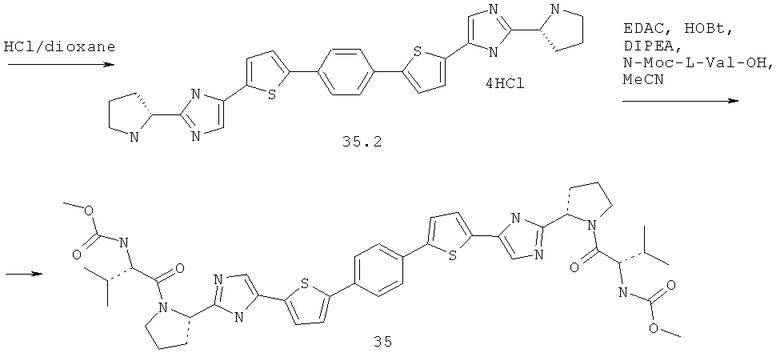
Метиловый эфир {(S)-1-[(S)-2-(5-{5-[4-(5-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-тиофен-2-ил)-фенил]-тиофен-2-ил}-1Н-имидазол-2-ил)-пирролидин-1-карбонил]-2-метил-пропил}-карбаминовой кислоты 35 получен по нижеследующей схеме.
1,4-Бис-{5-[5-{(R)-1-[(R)-2-(циклопропанкарбонил-амино)-2-фенил-ацетил]-пирролидин-2-ил}-3Н-имидазол-4-ил]-тиофен-2-ил}-бензол 36 получен по нижеследующей схеме.

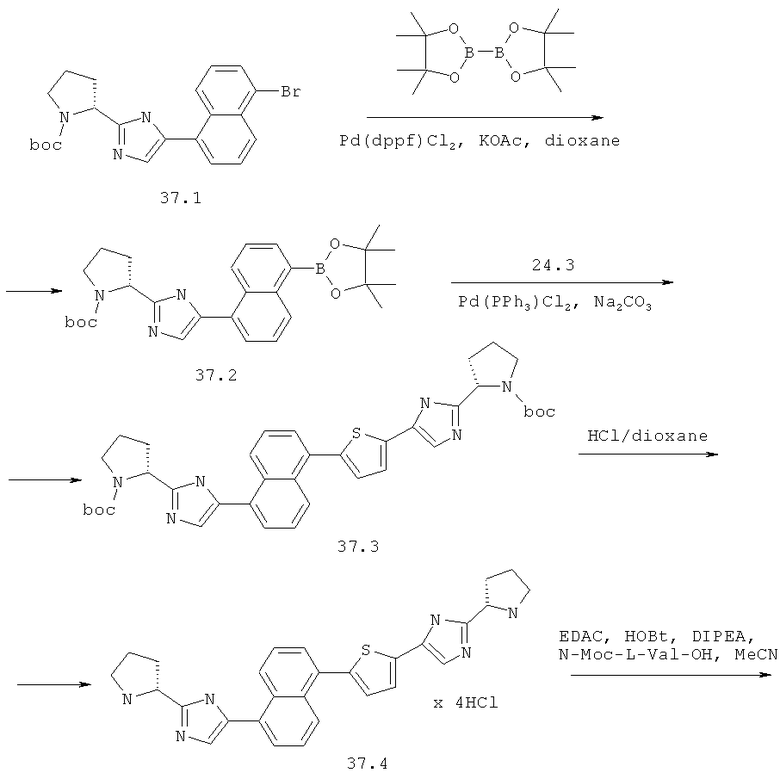
Метиловый эфир [(S)-1-((S)-2-{5-[5-(5-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-1-ил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 37 получен по нижеследующей схеме.

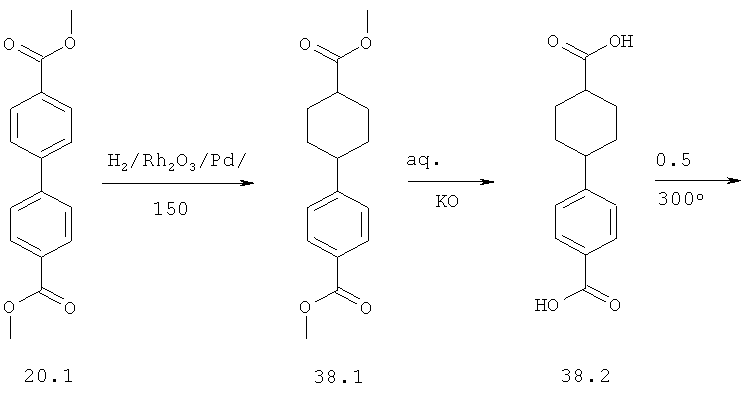
Метиловый эфир [(S)-1-((R)-2-{4-[4-(4-{2-[(S)-1-((R)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-оксазол-4-ил}-транс-циклогексил)-фенил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 38 получен исходя из диметилового эфира дифенил-4,4'-дикарбоновой кислоты 20.1 по схеме, представленной ниже.

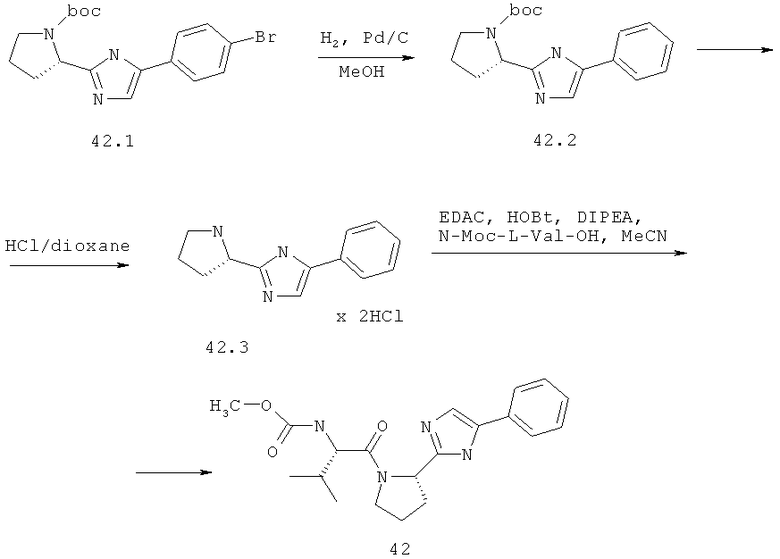
Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-фенил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 42 получают по схеме, представленной ниже.
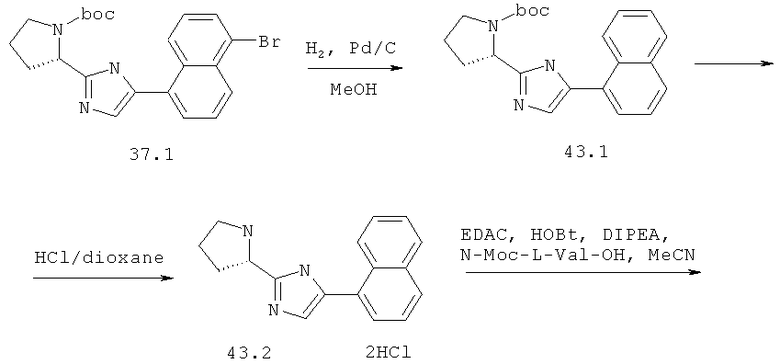
Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-нафталин-1-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 43 получают по схеме, представленной ниже.
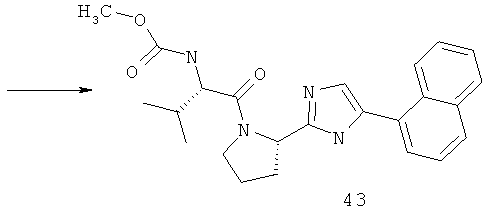
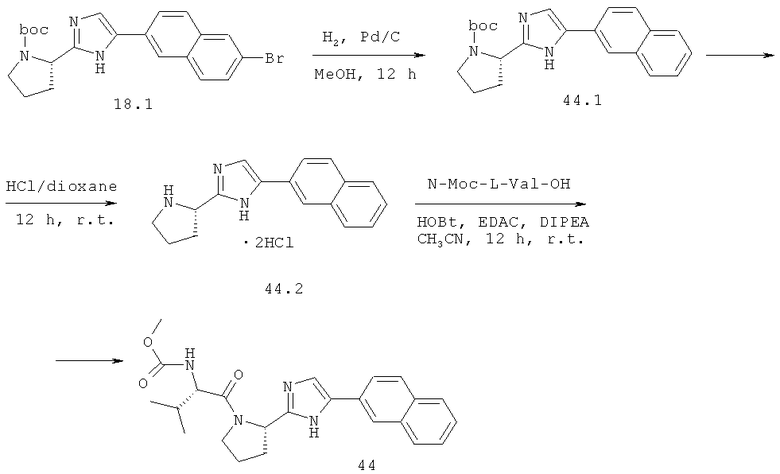
Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-нафталин-2-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 44 получают по схеме, представленной ниже.
Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-тиофен-2-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 58 и метиловый эфир {(S)-2-метил-1-[(S)-2-[5-(2,2'-дитиофен-5-ил)-1Н-имидазол-2-ил]-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 59 получают по схеме, представленной ниже.

Биологическая активность азолов общей формулы 1А и 1В.
Противовирусную активность замещенных азолов общей формулы 1А и 1В определяли в клеточной линии гепатомы человека Huh7, содержащей субгеномный РНК-репликон ВГС (генотип 1b, клон Con1). В качестве экспериментальной методики был использован вариант иммунного теста ИФА на вирусный белок NS5A в 96-луночном формате. Цитотоксичность соединений оценивали в параллельном режиме.
Клетки Huh7 высевались в 96-луночные планшеты (7.5×103 клеток на лунку в 100 мкл питательной среды). Растворы тестируемых соединений в среде ДМЕМ {(DMEM) 1X; Источник: Cellgro; Каталог: 10-013-CV} готовились непосредственно перед использованием. Всего готовилось одиннадцать серийных трехкратных разведений с концентрацией от 20 нМ до 0,2 пМ. Через 4 часа после высевания клеток серийные разведения препаратов добавлялись к клеткам (100 мкл на лунку). Конечная концентрация тестируемых соединений составляла от 10 нМ до 0,1 пМ, а ДМСО - 0.5%. При необходимости исследовались более высокие концентрации заявляемых азолов. Каждое разведение препарата тестировалось на двух идентичных лунках. Далее клетки инкубировали в течение трех дней при 37°С/5% CO2. Клетки фиксировали добавлением 250 мкл/лунку смеси ацетон/метанол (1:1). Через 1 минуту клетки трижды промывали раствором PBS (Phosphate Buffered Saline). После этого клетки блокировали добавлением 150 мкл/лунку 10% фетальной телячьей сыворотки в растворе PBS на 1 час при комнатной температуре. Далее клетки инкубировали с мышиными моноклональными антителами к кор-антигену ВГС, клон С7-50 (Источник: Affinity BioReagents; Каталог: МА1-080) (100 мкл/лунку, рабочее разведение - 1:500 в 10% фетальной телячьей сыворотке в растворе PBS) в течение двух часов при 37°С. Клетки промывали 6 раз раствором PBS/0.05% Твин 20, после чего инкубировали в течение 1 часа с антителами козы к иммуноглобулинам мыши (конъюгированными с пероксидазой хрена, 100 мкл/лунку, рабочее разведение - 1:2500 в 10% фетальной телячьей сыворотке в растворе PBS). Клетки промывали 6 раз раствором PBS/0.05% Твин 20, один раз раствором PBS, после чего добавляли 100 мкл/лунку субстрата (1 таблетка ОПД+12 мл цитрат/фосфатного буфера+5 мкл 30% H2O2). Планшеты выдерживали 30 мин в темноте при комнатной температуре. Реакцию останавливали добавлением 100 мкл/лунку 2н. H2SO2 и измеряли оптическую плотность (длина волны 490 нм) при помощи многоканального спектрофотометра Victor3 V 1420 (Perkin Elmer). Значения ИК50 (концентрация азола, понижающая уровень вирусного РНК-репликона на 50%) для каждого тестируемого азола рассчитывали при помощи программы XLfit 4.
Цитотоксичность тестируемых азолов изучалась в опытах на культуре линии клеток гепатомы человека Huh7. Количество живых клеток определяли при помощи набора ATPLite (Perkin Elmer, Бостон, США) в соответствии с инструкциями производителя. Цитотоксическое действие оценивали, высеивая клетки в черной микроплате с прозрачным дном (96 ячеек, 104 клеток на лунку). Для каждого бис-азола использовали три независимых повтора. Тестируемые бис-азолы добавляли через 18 часов, после чего клетки инкубировали с веществами в течение 96 часов. Промывали дважды каждую лунку фосфатно-солевым буфером (0,2 мл/лунку) и затем лизировали клетки добавлением клеточного буфера (50 мкл/лунку) (все указанные реактивы входят в комплект набора ATPLite). Микроплату инкубировали в течение 5 минут на вращающейся платформе при 600 об/мин, после чего добавляли в каждую лунку 50 мкл раствора субстрата (часть набора ATPLite). Инкубировали еще 5 минут на вращающейся платформе при 600 об/мин, выдерживали 10 минут в темноте и затем измеряли люминесценцию на приборе TopCount NXT (Packard, Perkin Elmer).
В качестве количественного параметра для оценки цитотоксичности использовали величину ЦК50, которая соответствует концентрации бис-азола, при которой погибает 50% клеток.
Расчет параметра ЦК50: для расчета эффективности ингибирования (% Инг) использовали формулу: % Инг=[(Лпоз-Лэкс)/(Лпоз-Лотр)]·100%, где Лпоз - положительный контроль, люминесценция в ячейках с клетками без вещества; Лотр - отрицательный контроль, люминесценция в ячейках со средой без клеток; Лэкс - люминесценция в ячейках с веществом в определенной концентрации. Значения ЦК50 затем расчитывали при помощи программы XLfit 4. Результаты испытаний новых азолов общей формулы 1А и 1В свидетельствуют об их высокой (наномолярной) или очень высокой (пикомолярной) активности. Ингибирующая активность по отношению к генотипу gT1b, gT1a и gT2a HCV новых азолов общей формулы 1А и 1В представлена в представленной ниже таблице и обозначена как: *>1000 нМ, ** от 999 нМ до 10 нМ, *** от 9.9 нМ до 1 нМ и ****<1 нМ.
Предметом настоящего изобретения являются новые лиганды, спектр, биологической активности которых включает вирусный белок NS5A, представляющие собой азолы общей формулы 1А и 1В и их фармацевтически приемлемые соли.
Предметом данного изобретения является активный компонент для фармацевтических композиций и лекарственных средств, предназначенный для лечения и предупреждения флававирусных (genus Flaviviridae) заболеваний, таких как заболевания, обусловленные вирусом гепатита С и вирусом гепатита GBV-C, представляющий собой азолы общей формулы 1А и 1В и их фармацевтически приемлемые соли.
Предметом данного изобретения является фармацевтическая композиция, содержащая в качестве активного компонента фармацевтически эффективное количество лиганда общей формулы 1А и 1В и их фармацевтически приемлемые соли.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с активным компонентом общей формулы 1А и 1В по настоящему изобретению может включать и другие активные ингредиенты, при условии что они не вызывают нежелательных эффектов, например аллергических реакций.
При необходимости использования фармацевтических композиций по настоящему изобретению в клинической практике они могут смешиваться для изготовления различных форм, при этом они могут включать в свой состав традиционные фармацевтические носители: например пероральные формы (такие, как таблетки, желатиновые капсулы, пилюли, растворы или суспензии); формы для инъекций (такие, как растворы или суспензии для инъекций или сухой порошок для инъекций, который требует лишь добавления воды для инъекций перед использованием); местные формы (такие, как мази или растворы).
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом настоящего изобретения является также способ получения фармацевтической композиции, который заключается в смешении, по крайней мере, одного активного компонента общей формулы 1А и 1В или его фармацевтически приемлемой соли с инертным наполнителем и/или растворителем.
Предметом данного изобретения является также фармацевтическая композиция в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для лечения и предупреждения флававирусных (genus Flaviviridae) заболеваний, обусловленных вирусом гепатита С и вирусом гепатита GBV-C, содержащая в качестве активного компонента фармацевтически эффективное количество лиганда общей формулы 1А и 1В и их фармацевтически приемлемые соли.
Предметом настоящего изобретения также является способ лечения флававирусных болезней путем введения фармакологически эффективного количества замещенного азола общей формулы 1А и 1В, или его фармацевтически приемлемой соли, или фармацевтической композиции, содержащей указанный выше азол.
Клиническая дозировка фармацевтической композиции, содержащей в качестве активного компонента азол общей формулы 1А и 1В, у пациентов может корректироваться в зависимости от: терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг. Поэтому во время приготовления фармацевтических композиций по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг азола общей формулы 1А и 1В. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно от одного до шести раз).
Предметом настоящего изобретения является также терапевтический коктейль для профилактики и лечения флававирусных заболеваний, в том числе заболеваний, обусловленных вирусами гепатита С, включающий в качестве одного из компонентов замещенный азол общей формулы 1А и 1В, или его фармацевтически приемлемую соль, или фармацевтическую композицию, содержащую указанный выше азол.
Терапевтические коктейли для профилактики и лечения указанных выше флававирусных заболеваний, в том числе гепатита С, наряду с лекарственными средствами по данному изобретению могут включать: ингибиторы инозин-5-монофосфат дегидрогеназы, например Рибавирин (разрешен) и Рибамидин; ингибиторы NS3 протеазы гепатита С, например Телапревир и boceprevir; ингибиторы РНК-полимеразы NS5B, например VX222, R7128, PF-868554, ANA598; ингибиторы альфа-глюкозидазы, например аминоуглевод Селгозивир; а также агонисты TLR-рецепторов, гепатопротекторы, циклоспорины, различные белки (например, интерфероны), антитела, вакцины и т.д.
Для комбинированной терапии любые классы агентов, которые могут оказаться полезными, будучи объединены с замещенными азолами настоящего изобретения, могут подразумевать, например, нуклеозидные и не-нуклеозидные ингибиторы HCV полимеразы, ингибиторы протеазы, ингибиторы геликазы, NS4B ингибиторы и медицинские агенты, которые функционально ингибируют внутренний рибосомный сайт вхождения (IRES) и другие медикаменты, которые ингибируют прикрепление или вхождение вируса в клетки, транскрибирование HCV RNA, репликацию, созревание или ослабление вируса. Специфические соединения в этих классах и полезные в этом изобретении включают, но не ограничивают макроциклические, гетероциклические и линейные ингибиторы протеазы HCV, такие как telaprevir (VX-950), boceprevir (SCH-503034), narlaprevir (SCH-900518), ITMN-191 (R-7227), TMC-435350 (a.k.a. TMC-435), MK-7009, BI-201335, BI-2061 (ciluprevir), BMS-650032, ACH-1625, ACH-1095 (HCV NS4A ингибитор сопутствующего фактора протеазы) VX-500, VX-813, PHX-1766, PHX2054, IDX-136, IDX-316, ABT-450 EP-013420 (и родственные) и VBY-376; ингибиторы нуклеозидной HCV полимеразы (репликазы), полезные в данном изобретении, включают, но не ограничены следующим: R7128, PSI-7851, IDX-184, IDX-102, R1479, UNX-08189, PSI-6130, PSI-938 и PSI-879 и различные другие нуклеозиды и нуклеотидные аналоги и HCV ингибиторы, включающие (но не ограничивающие) происходящие от 2'-С-метил модифицированные нуклеозиды и нуклеотиды; и 7'-деаза модифицированные нуклеозиды и нуклеотиды. Ингибиторы не-нуклеозидной HCV полимеразы (репликазы), полезные в данном изобретении, включают, но не ограничены: HCV-796, HCV-371, VCH-759, VCH-916, VCH-222, ANA-598, МК-3281, АВТ-333, АВТ-072, PF-00868554, BI-207127, GS-9190, A-837093, JKT-109, GL-59728 и GL-60667.
Кроме того, ингибиторы NS5A настоящего изобретения могут быть использованы в комбинации с антагонистами циклофиллина и иммунофиллина (например, без ограничений DEBIO соединения, NM-811, а также циклоспорин и его производные), ингибиторами киназ, ингибиторами протеинов теплового шока (напр., HSP90, HSP70), другими иммуномодуляторными агентами, которые могут включать без ограничения интерфероны (альфа-, бета-, омега-, гамма-, лямбда или синтетические), такие как Intron A™, Roferon-A™, Canferon-А300™, Advaferon™, Infergen™, Humoferon™, Sumiferon MP™, Alfaferon™, IFN-β™, Feron™ и подобные интерфероновые соединения, дериватизированные полиэтиленгликолем (pegylated), такие как: PEG interferon-α-2a (Pegasys™), PEG interferon-α-2b (PEGIntron™), pegylated IFN-α-con 1 и подобные; пролонгированные формулы и производные интерфероновых соединений, такие как альбумин-конденсированный интерферон, Albuferon™, Locteron™, и подобные; интерфероны с различными типами контролируемой доставки (напр., ITCA-638, омега-интерферон, доставляемый DUROS подкожной системой доставки); соединения, которые стимулируют синтез интерферона в клетках, такие как resiquimod и подобные; интерлейкины; соединения, которые улучшают развитие отклика клетки type 1 helper T, такие как SCV-07 и подобные; TOLL-подобные агонисты рецепторов, такие как: CpG-10101 (action), isotorabine, ANA773 и подобные; thymosin α-1, ANA-245 и ANA-246, гистамин дигидрохлорид, propagermanium; tetrachlorodecaoxide; ampligen; IMP-321; KRN-7000; антитела, такие как: civacir, XTL-6865 и подобные и профилактические и терапевтические вакцины, такие как: Inno Vac, HCV E1E2/MF59 и подобные. В добавление любой из вышеописанных методов, включающий введение NS5A ингибитора, агонист рецептора интерферона типа I (напр., IFN-α) и агонист рецептора интерферона типа II (напр., IFN-γ), может быть усилен введением эффективного количества TNF-α антагониста. Типичные неограничивающие TNF-α антагонисты, которые подходят для использования в такой комбинированной терапии, - ENBREL™ и HUMIRA™.
В дополнение NS5A ингибиторы настоящего изобретения могут быть использованы в комбинации с антипротозоанами, а другие антивирусы считаются эффективными при лечении HCV инфекции, такие как: пролекарство nitazoxanide. Nitazoxanide может быть использован как агент в комбинации с соединениями, раскрытыми в этом изобретении, а также в комбинации с другими агентами, полезными при лечении HCV инфекции, такими как: peginterferon alfa-2a и ribavarin (напр., Rossignol, JF и Keeffe, ЕВ, Future Microbiol. 3: 539-545, 2008).
NS5A ингибиторы настоящего изобретения могут быть также использованы с альтернативными формами интерферонов и пегилированных интерферонов, ribavirin или его аналогами (напр., Tarabavarin, levovirion), microRNA, маловредными RNA соединениями (напр., SIRPLEX-140-N и подобные), аналогами нуклеотидов или нуклеозидов, иммуноглобулинами, гепатопротекторами, противовоспалительными агентами и другими ингибиторами NS5A. Ингибиторы других мишеней в жизненном цикле HCV включают ингибиторы NS3 геликазы; ингибиторы NS4A ко-фактора, ингибиторы антисмысловых олигонуклеотидов, такие как: ISIS-14803, AVI-4065 и подобные; вектор-зашифрованную короткую «шпильку» RNA (shRNA); HCV специфические рибозимы, такие как: heptazyme, RPI, 139199 и подобные; ингибиторы вхождения, такие как: НереХ-С, HuMax-НерС и подобные; ингибиторы альфа-глюкозидазы, такие как: celgosivir, UT-231B и подобные; КРЕ-02003002 и BIVN 401 и IMPDH ингибиторы. Другие показательные соединения - ингибиторы HCV включают ингибиторы, раскрытые в известных научных и патентных публикациях.
Дополнительно комбинации, например, рибавирина и интерферона могут быть введены как комбинированная терапия с, по крайней мере, одним азолом настоящего изобретения. Настоящее изобретение не ограничивается вышеуказанными классами или соединениями и рассматривает известные и новые соединения и комбинации биологически активных агентов. Имеется в виду, что комбинированные терапии настоящего изобретения включают любые химически совместимые комбинации бис-азолов этой патентоспособной группы с другими соединениями патентоспособной группы или другими соединениями вне патентоспособной группы, а также комбинация не исключает антивирусную активность соединения этой патентоспособной группы или антивирусную активность самой фармацевтической композиции.
Комбинированная терапия может быть последовательной, т.е. лечение сначала одним агентом, а затем другим (например, когда каждый этап лечения подразумевает другое соединение настоящего изобретения или когда один этап лечения включает соединение настоящего изобретения, а другой подразумевает один или более биологически активных агентов) или может быть лечение с обоими агентами одновременно. Последовательная терапия может подразумевать существенное время после завершения первой стадии терапии до начала второй стадии. Лечение обоими агентами в одно и то же время может осуществляться в одной ежедневной дозе или в разных дозах. Комбинированная терапия не нуждается в ограничении двумя агентами и может включать три или более агентов. Дозы для одновременной и последовательной комбинированной терапии будут зависеть от всасывания, распределения, скоростей обмена веществ и выведения компонентов комбинированной терапии, а также других факторов, хорошо известных специалисту. Размер дозы будет также изменяться в зависимости от тяжести состояния, которое нужно облегчить. Для каждого особого пациента специфическая схема приема доз и расписание могут быть отрегулированы по времени в соответствии с потребностью индивидуума и профессиональным суждением лица, которое лечит или наблюдает за лечением методом комбинированной терапии.
Несмотря на то что вышеприведенное изобретение было описано в некоторых деталях с помощью иллюстраций и примеров с целью облегчить понимание, для специалиста в этой области совершенно очевидно, что с учетом этого изобретения возможны некоторые изменения и модификации, не отклоняясь от духа и объема изобретения, как определено в приложенной формуле изобретения.
Представленные ниже примеры иллюстрируют, но не ограничивают изобретение.
Пример 1. Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты 14.
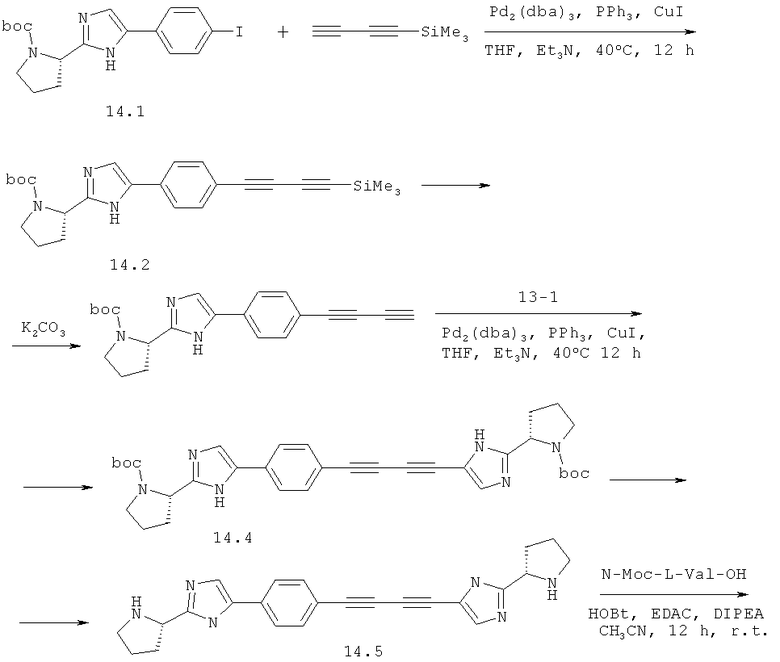
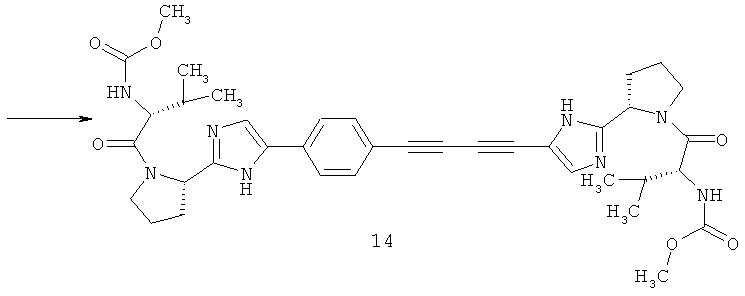
К раствору 8,15 г (42 ммоль) 1,4-бис-(триметилсилил)-1,3-бутадиина в 50 мл сухого эфира под аргоном добавляют 31 мл (46,5 ммоль) 1,5 М раствора MeLi×LiBr в эфире. Смесь перемешивают 6 ч при комнатной температуре. К смеси медленно добавляют 50 мл насыщенного раствора NH2Cl, экстрагируют пентаном, сушат над Na2SO4 и удаляют растворители в слабом вакууме. Жидкий остаток растворяют в 70 мл ТГФ, добавляют 20 мл триэтиламина, 8,8 г (20 ммоль) соединения 14.1, 458 мг (0,5 ммоль) Pd2(dba)3, 524 мг (2 ммоль) трифенилфосфина, 190 мг (1 ммоль) CuI и смесь перемешивают под аргоном 12 ч при 40°С. Смесь фильтруют через целит, наносят на силикагель и выделяют соединение 2 флэш-хроматографией (элюент CHCl3: EtOAc=10:1). Выход 7,56 г (87%). LCMS (M+H)+ 434.
К раствору 7,36 г (17 ммоль) соединения 14.2 в 120 мл ТГФ и 120 мл метанола добавляют 7,04 г (51 ммоль) поташа и смесь перемешивают 2 ч. Растворители удаляют в вакууме, остаток обрабатывают 150 мл ТГФ и фильтруют. К полученному раствору соединения 14.3 добавляют 5,56 г (15,3 ммоль) соединения 13-1 (5-иод-2-[(2S)-1-вос-пирролидин-2-ил]-1Н-имидазол), 366 мг (0,4 ммоль) Pd2(dba)3, 630 мг (2,4 ммоль) трифенилфосфина, 152 мг (0,8 ммоль) CuI и смесь перемешивают под аргоном 12 ч при 40°С. Смесь фильтруют через целит, наносят на силикагель и отделяют соединение 14.4 от основной части примесей флэш-хроматографией (элюент CHCl3: МеОН=80:1). После упаривания растворителя остаток обрабатывают 60 мл ацетонитрила, выдерживают в УЗИ-бане до начала кристаллизации и оставляют на 3 часа. Выпавший осадок отфильтровывают, промывают ацетонитрилом, эфиром и высушивают в вакууме. Выход 5,47 г (54%). LCMS (M+H)+ 597. К соединению 14.4 (0.695 г) добавляют 15 мл 3М раствора HCl в диоксане и перемешивают 12 ч. Смесь упаривают в вакууме, получают соединение 14.5 с выходом 55%. LCMS (ESI): LCMS (М+H)+ 397. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 2.02 (уш.с., 8Н), 2.99 (м, 4Н), 3.40 (уш.с., 2Н), 6.22 (м, 4Н), 6.75 (с, 1Н), 7.22 (с, 1Н), 7.77 (м, 2Н), 7.83 (д, 2Н). Смесь 50 мг (0.283 ммоль, 2.4 экв.) N-метоксикарбонил-L-валина, 40 мг (0.295 ммоль, 2.5 экв.) 1-гидроксибензотриазола и 53 мг (0.277 ммоль, 2.35 экв.) N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида в 1 мл ацетонитрила перемешивают 1 ч, добавляют 64 мг (0.118 ммоль, 1 экв.) соединения 14.5 и 82 мкл (61 мг, 0.472 ммоль, 4 экв.) диизопропилэтиламина. Реакционную массу перемешивают 12 ч при комнатной температуре. Полноту протекания реакции контролируют методом LCMS. После завершения реакции растворитель полностью отгоняют на роторном испарителе, остаток растворяют в дихлорметане. Экстракт промывают 10% раствором карбоната натрия, сушат над Na2SO4 и упаривают на роторном испарителе. Дальнейшую очистку проводят методом ВЭЖХ. Дигидрохлорид 14·2HCl получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 14 в CH2Cl2 и высаживанием эфиром. Получают 56 мг (67%) соединения 14·2HCl. LCMS (М+1)+ 711. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 0.87 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.99 (м, 4Н), 2.06 (м, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.02 (д, J=0.42, 2Н), 4.73 (м, 2Н), 6.86 (с, 1Н), 7.33 (с, 1Н), 7.76 (д, J=8.26, 2Н), 7.90 (м, 2Н), 8.80 (м, 4Н).
Пример 2. Диметиловый эфир [[1,1'-транс,транс-бициклогексил]-4,4'-диилбис[4,2-оксазолдиил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты 20.
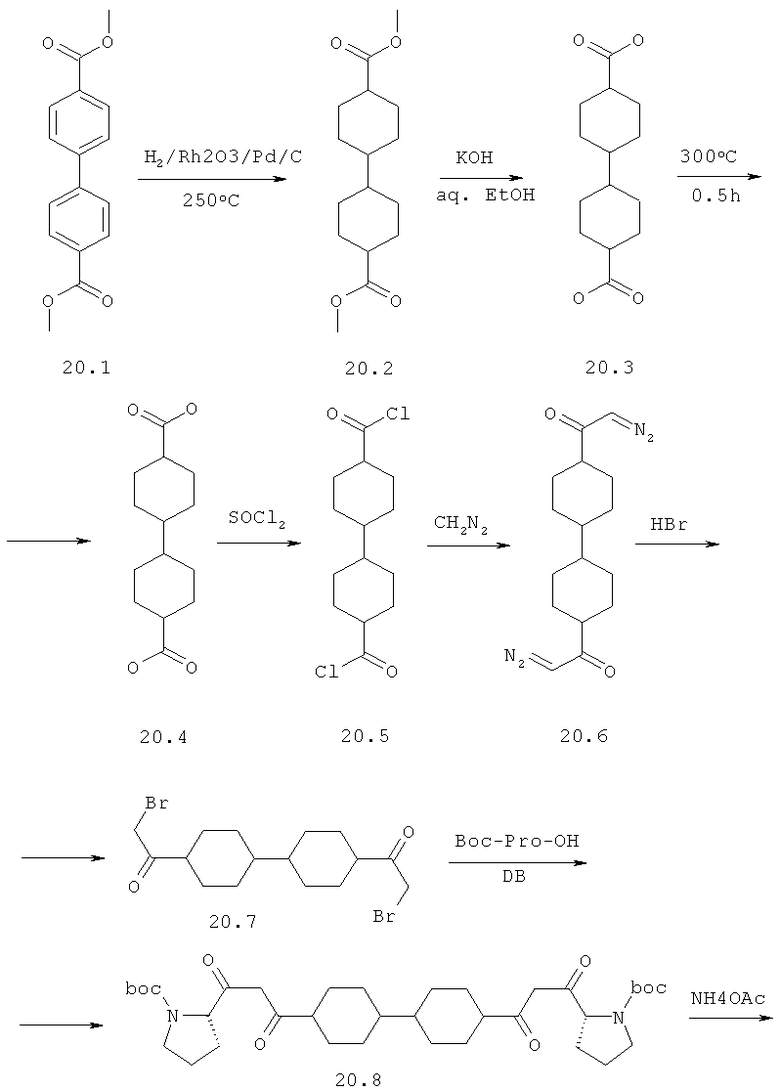
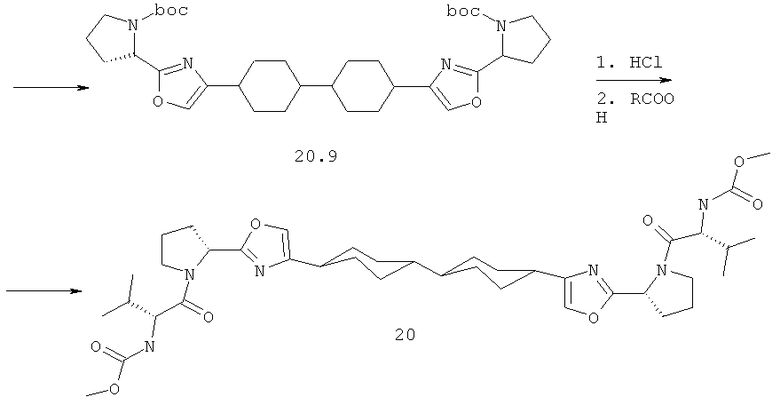
4,4'-Диметил дифенил-4,4'-дикарбоксилат 20.1 (9 г, 33 ммоль) гидрируют в СН3СООН (100 мл) в присутствии 10% Pd/C (3 г) и Rh2O3 (0.15 г) при 250°С в течение 16 часов и давлении 60-20 атм Н2. Смесь отфильтровывют, упаривают при пониженном давлении, к остатку добавляют избыток 10% раствора К2СО3 в воде и смесь экстрагируют CHCl3. Органический слой упаривют, что дает 9 г (96%) соединения 20.2. 1Н ЯМР (CDCl3): 3.67 (с); 3.65 (с) (total 6Н, 2Ме) 2.56 (1Н, уш.с) 2.20 (уш.т, 1Н) 2.0 (м, 4Н) 1.80 (уш.т, 2Н) 1.5-1.0 (м, 12Н). Соединение 20.2 (9 г, 31 ммоль) кипятят в EtOH (100 мл) и Н2О (20 мл) в присутствии 50% раствора КОН (9 г, 80 ммоль) в течение 30 минут. Раствор упаривают, остаток растворяют в H2O (0,5 л) и добавляют избыток HCl. Остаток отфильтровывают, что дает 7.2 г (91%) ди-кислоты 20.3. 1Н ЯМР (ДМСО-d6): 2.44 (1Н, уш.с) 2.05 (уш.т, 1Н) 1.88 (м, 4Н) 1.68 (м, 2Н) 1.43 (м, 4Н) 1.18 (м, 4Н) 0.98 (м, 4Н). Кислоту 20.3 7.2 г (28 ммоль) нагревают при 300°С в течение 0.5 часа при перемешивании в токе Ar. Сублимат и остаток растворяют в горячем 20% растворе КОН (50 мл) и перемешивают с 1 г активированного угля. Раствор отфильтровывают, разбавляют водой (0,5 л) и обрабатывают избытком HCl. Осадок отфильтровывают, что дает 5 г (69%) транс,транс-дикарбоновой кислоты 20.4. 1Н ЯМР 12.0 (уш.с, 2ОН) 2.50 (т, 2Н, 3J 1.8 Гц) 2.07 (т.т., 2Н, 3J 12 Гц, 3J 1.8 Гц) 1.95-1.85 (м, 4Н) 1.75-1.65 (м, 4Н) 1.30-1.20 (м, 4Н) 1.00-0.90 (м, 4Н). Транс,транс-дикарбоновую кислоту 20.4 (4.3 г, 17 ммоль) нагревают с SOCl2 (50 мл) в присутствии ДМФ (0.5 мл) в течение 2 часов. Раствор упаривают, что дает неочищенный твердый дихлорангидрид 20.5 (ЯМР LDA-2450), который используют в следующей стадии без дополнительной очистки. Раствор полученного соединения 20.5 в эфире медленно добавляют к раствору диазометана (136 ммол) в Et2O при температуре 0-10°С. Смесь перемешивают в течение 10 часов, выпавший осадок отфильтровывают и высушивают на воздухе. NMR LDA-2260, выход 5.4 г (42%) чистого транс,транс-соединения 20.6. 1H ЯМР LDA-2260 (CDCl3) 5.24 (уш.с, 2Н) 2.16 (уш.м. 2Н), 1.92-1.80 (м, 8Н) 1.40 (м, 4Н) 1.05 (м, 6Н). Бис-диазокетон 20.6 (1.3 g, 4.3 ммоль) растворяют в DCM (50 мл) и добавляют 40% раствор HBr в уксусной кислоте (1 мл). После прекращения выделения газа раствор дополнительно перемешивают 30 минут, затем добавляют толченый К2СО3 (10 г) и смесь перемешивают еще 30 минут; избыток К2СО3 отфильтровывают, фильтрат упаривают, остаток перекристаллизовывают из гептана. Выход соединения 20.7 составляет 1.5 г (85%). 1Н ЯМР (CDCl3) LDA-2459. 3.97 (с, 4Н, 2CH2 Br), 2.65 (т.т., 2Н, 3J 12 Гц 3J 3 Гц) 2.0-1.8 (м, 8Н) 1.3-1.4 (м, 4Н) 1.1-1.0 (м, 6Н). N-Вос-(S)-Пролин-ОН (765 мг, 3.6 ммоль) растворяют в MeCN (30 мл), добавляют при перемешивании DIPEA (460 мг, 3.6 ммоль) и через 5 минут добавляют соединение 20.7 (1.8 ммоль). Раствор кипятят в течение ночи, охлаждают, растворитель упаривают, остаток растворяют в DCM (50 мл) и промывают последовательно 0.1 н. раствором HCl (2×20 мл) и насыщенным раствором NaHCO3/NaCl (20 мл). Выход соединения 20.8 составляет 1.4 г (95%). Соединение 20.8 (1.7 ммоль) растворяют в толуоле (50 мл) и добавляют NH4OAc (10 г). Смесь кипятят при перемешивании в течение 24 часов, затем, органический слой упаривают, что дает 1.08 г (95%) соединения 20.9. LCMS М+1 639. Соединение 20.9 (1.6 ммоль) растворяют в 5 М растворе HCl в диоксане (50 мл) и перемешивают при 40°С в течение 1 часа. Затем раствор упаривают досуха, остаток экстрагируют CHCl3 (50 мл), экстракты промывают последовательно 10% раствором К2СО3 (50 мл), раствор сушат над К2СО3 и вновь упаривают досуха. Остаток растворяют в DCM (50 мл) и к нему добавляют последовательно DIPEA (1.02 г, 7.9 ммоль), N-метоксикарбонил-(S)-валин-ОН (1.04 г, 5.9 ммоль) и TBTU (1.92 г, 5.9 ммоль). Смесь перемешивают в течение 16 часов, затем промывают 0.1 н. раствором HCl (2×50 мл), 10% раствором К2СО3 (2×50 мл), органический слой упаривают и подвергают RP HPLC. Получают соединение 20. Дигидрохлорид 20·2HCl получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 20 в CH2Cl2 и высаживанием эфиром. LCMS (М+1) 753. 1Н ЯМР (CDCl3) 0.73 (д, 3Н, Me), 0.87 (д, 6Н, 2Ме), 1.06 (д, 3Н, Me), 1.4-2.7 (м, 32Н), 3.64 (м, 1Н), 3.69 (с, 3Н, ОМе), 3.75 (с, 3Н, ОМе), 3.80 (м, 3Н), 4.34 (м, 1Н), 5.24 (м, 1Н), 5.42 (м, 1Н), 7.12 (с, 1Н), 7.30 (с, 1Н).
Пример 3. Метиловый эфир [(S)-1-((S)-2-{5-[5-(6-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-2-ил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 24.
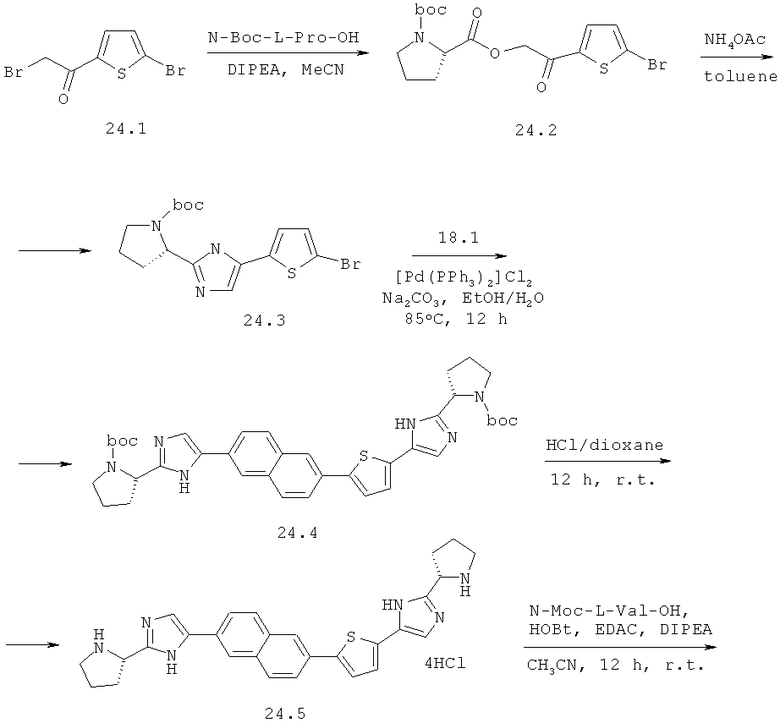
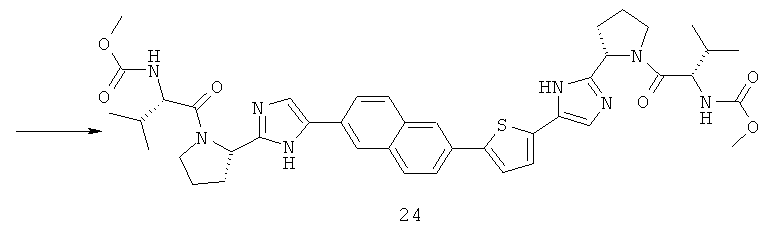
К смеси 6.87 г (24.2 ммоль) соединения 24.1 и 5.47 г (25.4 ммоль) N-Boc-L-пролина в 40 мл ацетонитрила добавляют 4.3 мл (24.8 ммоль) диизопропилэтиламина. Смесь перемешивают 3 ч при комнатной температуре, ацетонитрил отгоняют в вакууме, остаток разбавляют 100 мл толуола, промывают насыщенным солевым раствором, 5% раствором NaHCO3, сушат над Na2SO4 и упаривают в вакууме. Полученный эфир 24.2 растворяют в 75 мл толуола, добавляют 18.5 г (0.24 моль) ацетата аммония и перемешивают при 100°С в течение 18 ч. Смесь промывают водой, сушат над Na2SO4, наносят на SiO2 и выделяют продукт 24.3 колоночной хроматографией (элюент гексан-этилацетат=4:1). Выход соединения 24.3 4.76 г (49%). LCMS (ESI): m/z 398.1, 400.0 (М+Н)+. 1H ЯМР (CDCl3, 400 МГц) δ 10.80 (уш.с, 0.15Н), 10.52 (уш.с, 0.75Н), 7.09 (д, J=1.2 Гц, 1Н), 6.96 (м, 2Н), 4.93 (м, 1Н), 3.40 (уш.м, 2Н), 3.00 (уш.м, 1Н), 2.13 (м, 2H), 1.96 (м, 1Н), 1.50 (с, 9Н). Смесь 0.613 ммоль (1.1 экв.) боронового эфира 18.1 и 1.40 ммоль (2.5 экв.) карбоната натрия в 6 мл этанола и 1.4 мл воды продувают аргоном, добавляют 203 мг (0.56 ммоль, 1 экв.) соединения 24.3 и 20 мг (0.028 ммоль, 0.05 экв.) Pd(PPh3)2Cl2 и перемешивают 12 ч при 85°С в атмосфере аргона. Полноту протекания реакции контролируют методом LCMS. После завершения реакции реакционную массу фильтруют через целит и упаривают на роторном испарителе. Остаток растворяют в дихлорметане, промывают водой, сушат над Na2SO4 и упаривают на роторном испарителе. Соединение 24.4 выделяют методом колоночной хроматографии (элюэнт - толуол:этилацетат=2:1) с чистотой 85%. Дальнейшую очистку проводят методом ВЭЖХ. Получают 174 мг (41%) соединения 24.4 LCMS (ESI): m/z 681.4 (М+Н)+, которое дебокируют 3М раствором HCl в диоксане. Получают соединение 24.5 в виде тетрагидрохлорида с выходом 68%. LCMS (ESI): m/z 481.4 (М+Н)+. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 10.40 (уш.с, 1Н), 10.30 (уш.с, 1Н), 9.96 (уш.с, 0.8Н), 9.49 (уш.с, 0.8Н), 8.53 (c, 1H), 8.23 (д, J=13.6 Гц, 2Н), 8.07 (м, 2Н), 7.95 (м, 2Н), 7.83 (с, 1Н), 7.69 (с, 1Н), 7.56 (с, 1Н), 5.07 (уш.м, 1Н), 4.86 (уш.м, 1Н), 3.76 (уш.м, 1Н), 3.48 (уш.м, 1Н), 3.38 (уш.м, 2Н), 2.41 (уш.м, 2Н), 2.34 (уш.м, 2Н), 2.21 (уш.м, 2Н), 2.02 (уш.м, 2Н). Полученный продукт 24.5 превращают с выходом 53% в продукт 24 по аналогии с синтезом соединения 14 из соединения 14.5. Дигидрохлорид 24·2HCl получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 24 в CH2Cl2 и высаживанием эфиром. LCMS (ESI): m/z 795.8 (М+Н)+. 1H ЯМР (ДМСО-d6, 400 МГц) δ 15.29 (уш.с, 1Н), 14.76 (уш.с, 1.5Н), 8.49 (с, 1Н), 8.21 (д, J=16.0 Гц, 2Н), 8.10 (д, J=8.8 Гц, 1Н), 7.99 (м, 2Н), 7.93 (д, J=8.8 Гц, 1Н), 7.88 (уш.с, 1Н), 7.74 (с, 1Н), 7.71 (уш.с, 1Н), 5.22 (т, J=6.4 Гц, 1Н), 5.13 (т, J=6.4 Гц, 1Н), 4.13 (м, 2Н), 3.97 (м, 2Н), 3.84 (уш.м, 2Н), 3.54 (с, 6Н), 2.36 (м, 2Н), 2.19 (м, 4Н), 2.06 (м, 4Н), 0.92 (м, 1.6Н), 0.86 (д, J=6.8 Гц, 5.2Н), 0.79 (д, J=6.8 Гц, 5.2Н).
Пример 4. Метиловый эфир [(S)-1-((S)-2-{5-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирол)-пирролидин-2-ил]-3Н-имидазол-4-ил}-фенилэтинил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 25.
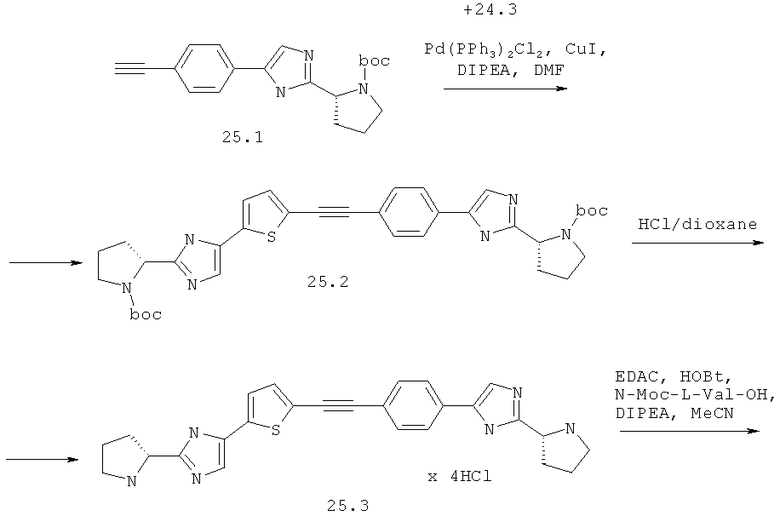
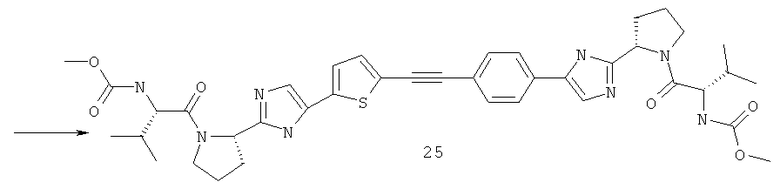
К смеси 348 мг (1 ммоль) соединения 24.3, 295 мг (0.87 ммоль) соединения 25.1 и 17 мг (0.09 ммоль) CuI в 3 мл ДМФА добавляют 0.15 мл (0.87 ммоль) диизопропилэтиламина и 31 мг (0.09 ммоль) Рd(PPh3)Cl2 под аргоном и смесь перемешивают при 80°С в течение 12 ч. По окончании реакции смесь разбавляют хлороформом, промывают водой, сушат над Na2SO4 и упаривают в вакууме. Выделяют продукт 25.2 методом ВЭЖХ. Выход 173 мг (30%). LCMS (ESI): m/z 655.3 (М+Н)+. Продукт 25.2 дебокируют 3М раствором HCl в диоксане с количественным выходом с получением соединения 25.3 (LC-MS (ESI): m/z 455.6 (М+Н)+), которое превращают в соединение 25 с выходом 41% по аналогии с превращением соединения 14.5 в соединение 14. LCMS (ESI): m/z 769.7 (М+Н)+. Дигидрохлорид 25 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 25 в CH2Cl2 и высаживанием эфиром. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 15.11 (уш.с, 0.95Н), 14.69 (уш.с, 1.25Н), 8.15 (с, 1Н), 7.93 (д, J=8.0 Гц, 2Н), 7.87 (уш.с, 1Н), 7.71 (д, J=8.0 Гц, 2Н), 7.58 (уш.с, 1Н), 7.45 (д, J=2.8 Гц, 1Н), 7.27 (м, 2Н), 5.16 (т, J=6.8 Гц, 1Н), 5.10 (т, J=6.6 Гц, 1Н), 4.11 (м, 2Н), 3.92 (м, 2Н), 3.83 (м, 2Н), 3.56 (с, 0.1Н), 3.54 (с, 5.9Н), 2.34 (м, 2Н), 2.16 (м, 4Н), 2.03 (м, 4Н), 0.90 (м, 1.2Н), 0.84 (т, J=7.2 Гц, 5.4Н), 0.77 (т, J=7.2 Гц, 5.4Н).
Пример 5. Метиловый эфир ((S)-1-{(S)-2-[5-(5'-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-[2,2']битиофенил-5-ил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовой кислоты 30.
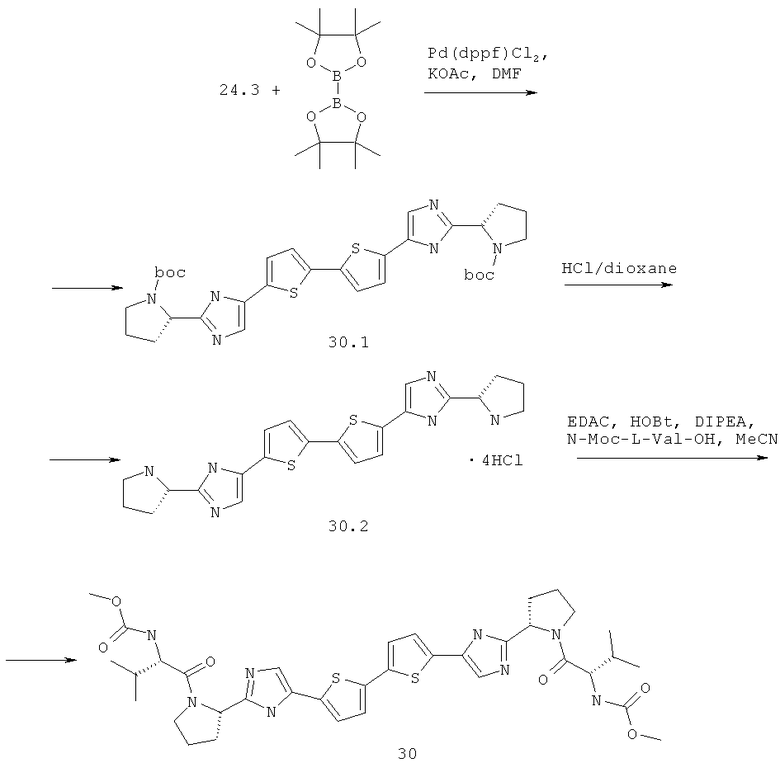
К смеси 1.194 г (3 ммоль) соединения 24.3, 840 мг (3.3 ммоль) бис(пинаколато)дибора и 882 мг (9 ммоль) КОАс в 9 мл ДМФА добавляют 75 мг (0.09 ммоль) Pd(dppf)Cl2·CH2Cl2 под аргоном и смесь перемешивают при 90°С в течение 12 ч. По окончании реакции смесь разбавляют хлороформом, промывают водой, сушат над Na2SO4, наносят на SiO2 и выделяют продукт 29.1 колоночной хроматографией (элюент гексан-этилацетат = 1:2). Выход 324 мг (34%). LCMS (ESI): m/z 637.5 (М+Н)+. Полученный продукт 30.1 дебокируют 3М раствором HCl в диоксане с количественным выходом с получением соединения 30.2. LCMS (ESI): m/z 437.3 (М+Н)+. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 10.31 (уш.с, 2Н), 9.50 (уш.с, 2Н), 7.81 (с, 2Н), 7.47 (д, J=3.2 Гц, 2Н), 7.31 (д.д, J1=4.0 Гц, J2=0.8 Гц, 2Н), 4.85 (уш.м, 2Н), 3.35 (м, 4Н), 2.41 (м, 2Н), 2.33 (м, 2Н), 2.15, (м, 2Н), 2.00 (м, 2Н). Последнее превращают в соединение 30 по аналогии с превращением соединения 14.5 в соединение 14. Соединение 30 получают с выходом 77%. LCMS (ESI): m/z 751.8 (М+Н)+. Дигидрохлорид 30 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 30 в CH2Cl2 и высаживанием эфиром. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 14.42 (уш.с, 0.8Н), 7.91 (с, 2Н), 7.91 (с, 2Н), 7.63 (с, 2Н), 7.41 (д, J=3.6 Гц, 2Н), 7.27 (д, J=8.4 Гц, 2Н), 5.10 (т, J=7.0 Гц, 2Н), 4.10 (т, J=7.8 Гц, 2Н), 3.92 (м, 2Н), 3.83 (м, 2Н), 3.53 (с, 6Н), 2.34 (м, 2Н), 2.15 (м, 4Н), 2.02 (м, 4Н), 0.89 (м, 1.2H), 0.83 (д, J=6.8 Гц, 5.4Н), 0.77 (д, J=6.8 Гц, 5.4Н).
Пример 6. Метиловый эфир {(S)-1-[(S)-2-(5-{5-[4-(5-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-тиофен-2-ил)-фенил]-тиофен-2-ил}-1Н-имидазол-2-ил)-пирролидин-1-карбонил]-2-метил-пропил}-карбаминовой кислоты 35.
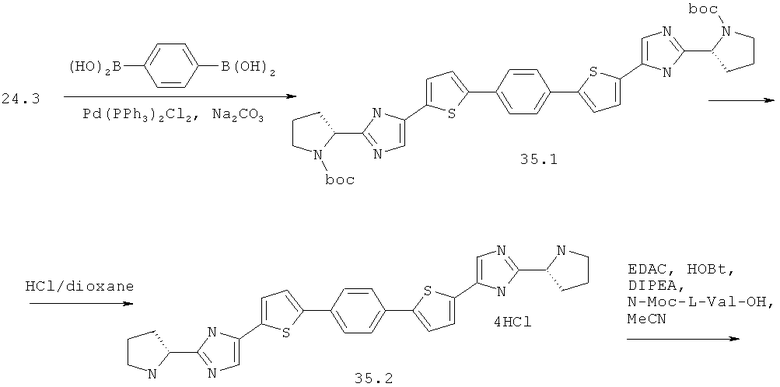
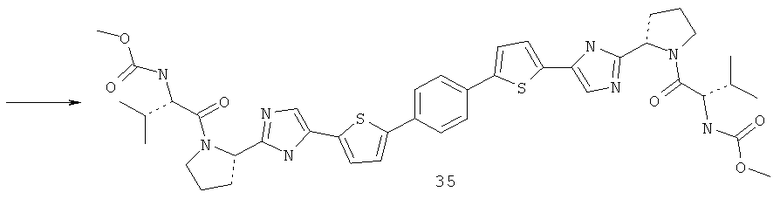
Смесь 598 мг (1.5 ммоль) соединения 24.3, 124 мг (0.75 ммоль) бензол-1,4-дибороновой кислоты и 320 мг (3 ммоль) Na2CO3 в 4 мл спирта и 0.35 мл воды продувают аргоном. Добавляют 105 мг (0.15 ммоль) Pd(PPh3)2Cl2 и смесь перемешивают под аргоном в закрытой пробирке при 80°С в течение 12 ч. По окончании реакции смесь разбавляют хлороформом, промывают водой, сушат над Na2SO4, наносят на SiO2 и выделяют продукт 35.1 колоночной хроматографией (элюент гексан-этилацетат=1:2). Выход 318 мг (59%). LC-MS (ESI): m/z 713.7 (M+H)+. К 310 мг соединения 35.1 добавляют 3 мл 3М раствора HCl в диоксане и перемешивают 12 ч. Смесь упаривают в вакууме, получают соединение 35.2. Выход количественный. LC-MS (ESI): m/z 513.5 (М+Н)+. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 10.32 (уш.с, 2Н), 9.56 (уш.с, 2Н), 7.83 (с, 2Н), 7.72 (с, 4Н), 7.58 (уш.м, 2Н), 7.55 (уш.м, 2Н), 4.88 (уш.м, 2Н), 3.37 (м, 4Н), 2.40 (м, 4Н), 2.17 (м, 2Н), 2.01 (м, 2Н). Смесь 46 мг (0.26 ммоль) N-(метоксикарбонил)-L-валина, 37 мг (0.27 ммоль) 1-гидроксибензотриазола и 49 мг (0.26 ммоль) N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорида в 1 мл ацетонитрила перемешивают 1 ч, добавляют 70 мг (0.11 ммоль) соединения 35.2 и 76 мкл (0.44 ммоль) диизопропилэтиламина. Смесь перемешивают 12 ч при комнатной температуре, упаривают досуха в вакууме и выделяют соединение 35 методом ВЭЖХ. Выход 59 мг (67%). LC-MS (ESI): m/z 827.8 (М+Н)+. Дигидрохлорид 35 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 6 в CH2Cl2 и высаживанием эфиром. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 14.40 (уш.с, 0.6Н), 7.75 (с, 4Н), 7.65 (уш.м, 4Н), 7.28 (д, J=8.0 Гц, 2Н), 5.11 (т, J=6.8 Гц, 2Н), 4.11 (т, J=7.8 Гц, 2Н), 3.92 (м, 2Н), 3.83 (уш.м, 2Н), 3.54 (с, 6Н), 2.34 (м, 2Н), 2.15 (м, 4Н), 2.03 (м, 4Н), 0.90 (м, 1.1Н), 0.84 (д, J=6.4 Гц, 5.45Н), 0.78 (д, J=6.4 Гц, 5.45Н).
Пример 7. 1,4-Бис-{5-[5-{(S)-1-[(S)-2-(циклопропанкарбонил-амино)-2-фенил-ацетил]-пирролидин-2-ил}-3Н-имидазол-4-ил]-тиофен-2-ил}-бензол 36.
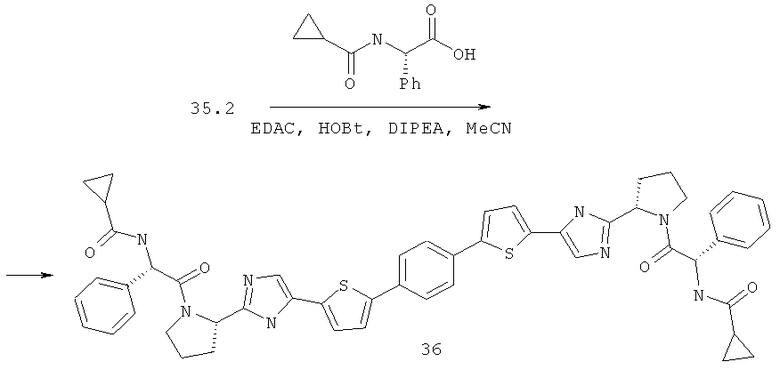
Соединение 36 получают по аналогии с превращением соединения 14.5 в соединение 14, но в качестве кислоты используют N-циклопропионил-L-фенилглицин. LCMS (ESI): m/z 915.7 (М+Н)+. Дигидрохлорид 36 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 36 в CH2Cl2 и высаживанием эфиром.
Пример 8. Метиловый эфир [(S)-1-((S)-2-{5-[5-(5-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-1-ил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовой кислоты 37.
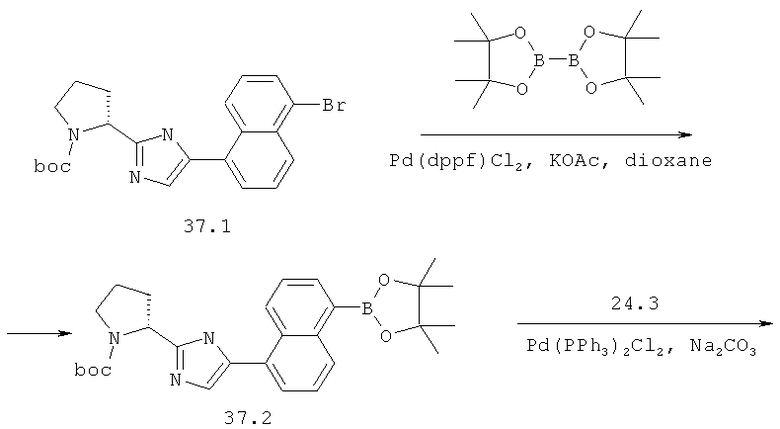
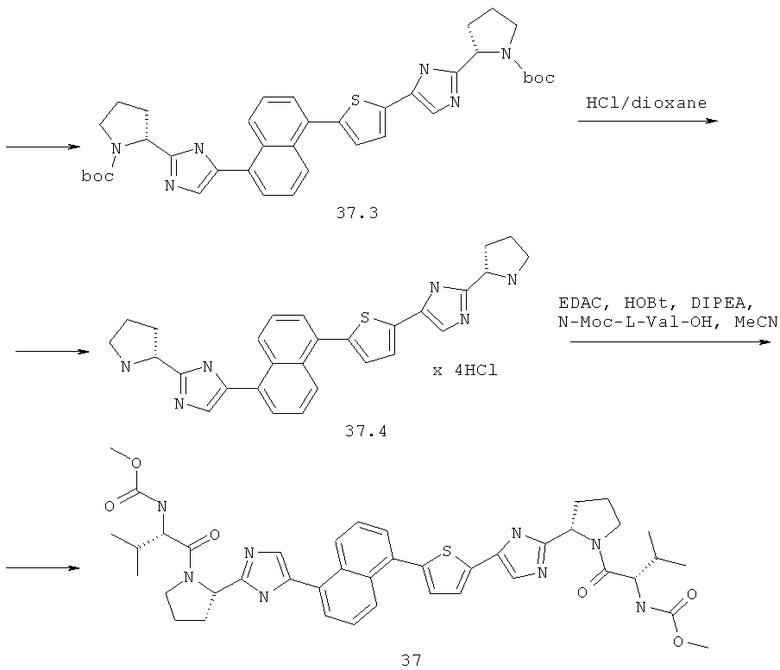
Смесь 442 мг (1 ммоль) соединения 37.1, 279 мг (1.1 ммоль) бис(пинаколато)диборана и 294 мг (3 ммоль) ацетата калия в 4 мл диоксана продувают аргоном, добавляют 24 мг (0.03 ммоль) Pd(dppf)Cl2·CH2Cl2 и смесь перемешивают под аргоном при 85°С в течение 24 ч. По окончании реакции смесь разбавляют хлороформом, промывают водой, сушат над Na2SO4 и упаривают в вакууме. Выделяют продукт 37.2 методом ВЭЖХ. Выход 250 мг (51%). LC-MS (ESI): m/z 490.8. (М+Н)+. Смесь 225 мг (0.46 ммоль) соединения 37.2, 182 мг (0.46 ммоль) соединения 24.3 и 98 мг (0.92 ммоль) Na2CO3 в 4 мл спирта и 0.35 мл воды продувают аргоном. Добавляют 32 мг (0.05 ммоль) Pd(PPh3)2Cl2 и смесь перемешивают под аргоном в закрытой пробирке при 80°С в течение 12 ч. По окончании реакции смесь разбавляют хлороформом, промывают водой, сушат над Na2SO4, наносят на SiO2 и выделяют продукт 37.3 колоночной хроматографией (элюент гексан-этилацетат-Et3N=1:1:0.05). Выход продукта 37.3 257 мг (82%, LC-MS (ESI): m/z 681.5 (M+H)+), который дебокируют 3М раствором HCl в диоксане с количественным выходом с получением соединения 37.4 (LC-MS (ESI): m/z 481.3 (М+Н)+), которое превращают в соединение 37 (LC-MS (ESI): m/z 795.7 (М+Н)+) по аналогии с превращением соединения 14.5 в соединение 14. Дигидрохлорид 37 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 37 в CH2Cl2 и высаживанием эфиром.
Пример 9. Синтез метилового эфира [(1S)-1-[[(2S)-2-[4-[4-[4-[2-[(2S)-1-[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]фенил]циклогексил]-2-оксазолил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты 38.
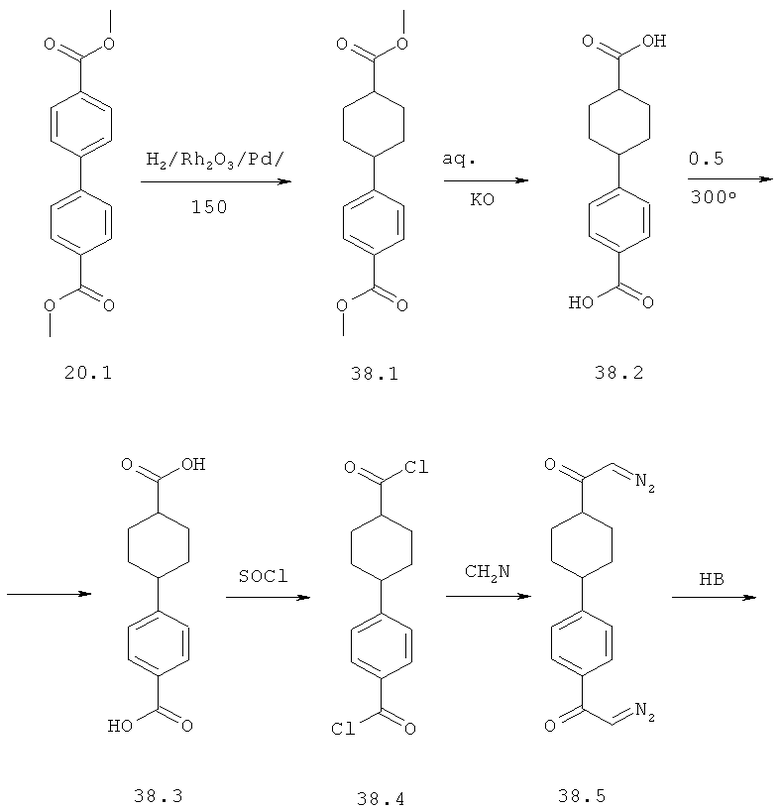

4,4'-Диметил дифенил-4,4'-дикарбоксилат 20.1 (9 г, 33 ммоль) гидрируют в СН3СООН (70 мл) в присутствии 10% Pd/C (3 г) и Rh2O3 (0.05 г) при 150°С в течение 16 ч при давлении 60-20 атм Н2. Смесь отфильтровывают, упаривают при пониженном давлении, к остатку добавляют избыток 10% водного раствора К2СО3 и смесь экстрагируют CHCl3. Органические экстракты упаривают и подвергают колоночной хроматографии, элюэнт 10% EtOAc-гексан. Выход соединения 38.1 составляет 6 г (65%). Соединение 27 (6 г, 22 ммоль) кипятят в EtOH (100 мл) и H2O (20 мл) в присутствии 50% раствора КОН (9 г, 80 ммоль) в течение 30 минут. Раствор упаривают, остаток растворяют в воде (0.5 л) и добавляют избыток HCl. Осадок отфильтровывают, что дает 5 г (92%) смеси цис+транс-дикарбоновых кислот 38.2. Смесь дикарбоновых кислот 38.2 5 г (20 ммоль) нагревают при 300°С при перемешивании в токе Ar в течение 30 мин (при этой температуре соединение расплавляется). Сублимат и остаток растворяют в горячем 20% растворе КОН (50 мл) и перемешивают с 1 г активированного угля. Раствор профильтровывают, разбавляют водой (0,5 л) и обрабатывают избытком HCl. Осадок отфильтровывают, что дает 3 г (60%) дикарбоновой кислоты 38.3 (транс-изомер 90%, цис-изомер 10%). 1Н ЯМР (ДМСО-d6) 12.5 (уш.с., 2Н) 7.88 (д, 2Н, J 8 Гц) 7.34 (д, 2Н, J 8 Гц) 2.56 (уш.м, 1Н) 2.26 (уш.м, 1Н) 2.0 (м, 2Н) 1.82 (м, 2Н) 1.50-1.40 (м, 4Н). Соединение 38.5 получают аналогично получению соединения 20.6, выход 50%. 1Н ЯМР LDA-2488 (CDCl3) 7.70 (д, 2Н) 7.28 (д, 2Н) 5.88 (с, 1Н) 5.31 (уш.с, 1Н) 2.60 (т.т., 1Н, 3J 12 Гц, 3J 2 Гц) 2.33 (уш.м, 1Н) 2.05-2.00 (м, 4Н) 1.65-1.45 (м, 4Н). Соединение 38.6 получают аналогично получению соединения 20.7, дибромид очищают колоночной хроматографией, выход 42%. 1H ЯМР (CDCl3): 7.94 (д, 2Н) 7.33 (д, 2Н) 4.44 (с, 2Н, ArCOCH2Br) 4.00 (с, 2Н, CyCOCH2Br) 2.84 (м, 1Н) 2.63 (м, 1Н) 2.15-2.05 (м, 4Н) 1.60 (м, 4Н). Соединение 38.7 получают аналогично получению соединения 20.8, выход 100%. Соединение 38.8 получают аналогично получению соединения 20.9, выход 100%, LCMS 632 (М+1). Соединение 38 (свободное основание, LCMS 746 (М+1)) получают аналогично получению соединения 20. Дигидрохлорид 38·2HCl получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 38 в CH2Cl2 и высаживанием эфиром. 1H ЯМР (CDCl3) 0.87 (д, 6Н, 2Ме), 0.93 (д, 3Н, Me), 1.03 (д, 3Н, Me), 1.5-2.5 (м, 22Н), 3.59 (м, 1Н), 3.68 (с, 3Н, ОМе), 3.71 (с, 3Н, ОМе), 3.80 (м, 3Н), 4.34 (м, 1Н), 5.24 (м, 1Н), 5.42 (м, 1Н), 7.16 (с, 1Н), 7.24 (с, 1Н), 7.22 (уш.д., 2Н), 7.68 (уш.м., 2Н).
Аналогичным образом, используя соответствующие исходные соединения и подходящие хиральные билдинг-блоки, были получены следующие соединения:








Диметиловый эфир [1,4-диоксан-2,5-диилбис[1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (М+1) 649.
Метиловый эфир [(1S)-1-[[[(1S)-1-[5-[2-[4-[2-[(1S)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]циклогексил]-1,3-диоксан-5-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 729.
Метиловый эфир [(1S)-1-[[[(1S)-1-[5-[5-[4-[2-[(1S)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]циклогексил]-1,3-диоксан-2-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 729.
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[5-[4-[2-[(1R-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]циклогексил]-1,4-диоксан-2-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 729.
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[5-[4-[2-[(1R)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]циклогексил]-1,4-диоксан-2-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 731.
Диметиловый эфир [1,4-циклогександиилбис[1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, дигидрохлорид, соединение 11, LCMS (М+1) 669, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.87 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 6Н), 1.86 (м, 6Н), 1.97 (м, 4H), 2.10 (м, 2Н), 2.51 (м, 2Н), 3.56 (м, 2Н), 3.61 (д, J=9.40, 6Н), 3.63 (м, 2Н), 4.02 (м, 2Н), 4.75 (д, J=0.42, 2Н), 6.42 (с, 2Н), 9.06 (м, 4Н).
Диметиловый эфир [[1,1'-транс-бициклогексил]-4,4'-диилбис[1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, соединение 21, LCMS (М+1) 751, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.46 (м, 8Н), 1.56 (м, 8Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 2.15 (м, 2Н), 2.42 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 6.37 (с, 2Н), 9.06 (м, 4Н).
Диметиловый эфир [бицикло[2.2.2]октан-1,4-диилбис[1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (М+1) 695.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]бицикло[2.2.2]окт-1-ил]-транс-циклогексил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 778.
Метиловый эфир [(1R)-1-[[(2R)-2-[5-[2-[2-[5-[(1R)-2-[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]циклопентил]-1H-имидазол-2-ил]этокси]этил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты (соединение 7). LCMS (М+1) 659. 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.45, J2=0.93, 6Н), 0.97 (т, J1=6.45, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97, (м, 4Н), 2.10 (м, 2Н), 2.46 (т, J1=14.76, J2=8.00, 4Н), 3.31 (т, J1=9.55, J2=0.81, 4Н), 3.56 (м, 2Н), 3.61 (м, 8Н), 3.96 (д, J=0.42, 2Н), 4.76 (м, 2Н), 6.95 (с, 2Н), 8.91 (м, 4Н).
Диметиловый эфир [тиобис[2,1-этандиил-1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1R)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (М+1) 651.
Метиловый эфир [(1R)-1-[[[(1S)-1-[5-[2-[[(E)-2-[2-[(1S)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]этенил]окси]этил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 633.
Диметиловый эфир [1,2-этандиилбис[окси-2,1-этандиил-1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1R)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, дигидрохлорид, LCMS (M+1) 679.
Диметиловый эфир [оксибис[(1Е)-1-пропен-3,1-диил-1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1R)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (М+1) 659.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[3-[2-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]этокси]-1-пропинил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 645.
Диметиловый эфир [оксибис[1-пропин-3,1-диил-1H-имидазол-5,2-диил(1R)этилиден(метилимино)[(1R)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (М+1) 645.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[3-[[(2E)-3-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5ил]-2-пропенил]окси]-1-припинил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 657.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[3-[2-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5ил]этокси]-1-пропинил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 645.
2,2'-[1,4-Нафталиндиилбис(1H-имидазол-5,2-диил)]бис[1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-,(2S,2'S)-пирролидин, LCMS (М+1) 802.
2,2'-[1,5-Нафталиндиилбис(1H-имидазол-5,2-диил)]бис[1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-,(2S,2'S)-пирролидин, LCMS (М+1) 802.
2,2'-[2,5-Тиендиилбис(1H-имидазол-5,2-диил)]бис[1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-,(2S',2'S)-пирролидин, LCMS (М+1) 758.
Диметиловый эфир [[2,2'-дитиофен]-5,5'-диилбис[1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1R)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, соединение 29, LCMS (М+1) 727, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.87 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.40 (т, J1=7.12, J2=6.78, 6Н), 1.95 (д, J=8.50, 2Н), 3.02 (т, J1=14.23, J2=1.50, 6Н), 3.61 (д, J=9.40, 6Н), (м, 2Н), 4.03 (д, J=8.50, 2Н), 4.89 (м, 2Н), 6.51 (д, J=4.00, 2Н), 6.86 (д, J=0.25, 2Н), 7.24 (д, J=0.25, 2Н), 8.79 (м, 4Н).
N,N'-[[2,2'-дитиофен]-5,5'-диилбис[1H-имидазол-5,2-диил(1S)этилиден]]бис[N'-метил-α-фенил-, (αR)-1-пиперидинацетамид, соединение 32, LCMS (М+1) 816, 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.39 (т, J1=7.12, J2=6.97, 6Н), 1.54 (м, 2Н), 1.67 (м, 6Н), 1.75 (м, 4Н), 2.63 (м, 4Н), 2.71 (м, 4Н), 2.97 (т, J1=14.23, J2=1.50, 6Н), 3.94 (м, 2Н), 5.37 (д, J=0.30, 2Н), 6.52 (д, J=4.00, 2Н), 6.87 (д, J=0.25, 2Н), 7.22 (м, 6Н), 7.39 (м, 4Н), 7.46 (т, J1=7.32, J2=2.10, 2Н), 11.18 (м, 2Н).
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[5'-[2-[(2S)-1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]-1Н-имидазол-2-ил]-, (2R)-пирролидин, соединение 33, LCMS (М+1) 840, 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.51 (м, 2Н), 1.70 (м, 10Н), 1.84 (м, 2Н), 1.99 (м, 2Н), 2.10 (м, 2Н), 2.65 (м, 4Н), 2.72 (м, 4Н), 3.45 (м, 2Н), 3.53 (м, 2Н), 3.96 (д, J=0.42, 2Н), 4.58 (м, 2Н), 4.64 (м, 2Н), 6.51 (д, J=4,00, 2Н), 6.92 (д, J=0.25, 2Н), 7.25 (уш.д., 6Н), 7.38 (м, 4Н), 7.44 (т, J1=7.32, J2=2.10, 2H), 11.18 (м, 2Н).
N,N'-[[2,2'-дитиофен]-5,5'-диилбис[1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-2-оксо-1-фенил-2,1-этандиил]]]бис-циклопропанкарбоксамид дигидрохлорид, соединение 34, LCMS (М+1) 840, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.83 (м, 4Н), 0.91 (м, 4Н), 1.64 (м, 2Н), 1.76 (м, 2Н), 1.84 (м, 2Н), 1.99 (м, 2Н), 2.10 (м, 2Н), 3.43 (д, J=4.78, 2Н), 3.50 (м, 2Н), 4.60 (м, 2Н), 5.17 (д, J=0.42, 2Н), 6.51 (д, J=4.00, 2Н), 6.92 (д, J=0.25, 2Н), 7.19 (м, 4Н), 7.27 (м, 8Н), 9.72 (м, 4Н).
1-[(2S)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[5-[4'-[2-[(2S)-1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил][1,1'-дифенил]-4-ил]-2-тиенил]-1H-имидазол-2-ил]-, (2S)-пирролидин, LCMS (М+1) 910.
2,2'-[2,5-Тиендиилбис(4,1-фенилен-1H-имидазол-5,2-диил)]бис[1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-, (2S,2'S)-пирролидин, LCMS (М+1) 910.
1-[(2S)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[4-[5'-[2-[(2R)-1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]фенил]-1H-имидазол-2-ил]-, (2R)-пирролидин, LCMS (М+1) 916.
2,2'-[2,6-Нафталиндиилбис(5,2-тиендиил-1H-имидазол-5,2-диил)]бис[1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-,(2R,2'R)-пирролидин, LCMS (М+1) 966.
1-[(2S)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[4-[5-[6-[2-[(2R)-1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-2-нафталенил]-2-тиенил]фенил]-1H-имидазол-2-ил]-, (2R,2'R)-пирролидин, LCMS (М+1) 966.
1-[(2S)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[[4-[4-[2-[(2R)-1-[(2S)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-транс-циклогексил]этинил]-1H-имидазол-2-ил]-, (2R)-пирролидин, LCMS (М+1) 830.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[4-[4-[2-[(2S)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-транс-циклогексил]-1H-имидазол-2-ил]-, (2S)-пирролидин, LCMS (М+1) 806.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[4-[4-[2-[(2S)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]циклогексил]-1H-имидазол-2-ил]-, (2S)-пирролидин, дигидрохлорид, LCMS (М+1) 806.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[6-[4-[2-[(2S)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]циклогексил]-1,3,5-гексатриинил]-1H-имидазол-2-ил]-, (2S)-пирролидин, LCMS (М+1) 830.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[[4-[4-[2-[(2S)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]циклогексил]этинил]-1H-имидазол-2-ил]-, (2S)-пирролидин, LCMS (М+1) 830.
2,2'-[1,4-Циклогександиилбис(1,3-бутадиин-4,1-диил-1H-имидазол-5,2-диил)]бис[1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-, (2R,2'R)-пирролидин, LCMS (М+1) 854.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[4-[4-[2-[(2R)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]бицикло[2.2.2]окт-1-ил]-1,3-бутадиинил]-1H-имидазол-2-ил]-, (2R)-пирролидин, LCMS (М+1) 832.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[6-[4-[2-[(2R)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]бицикло[2.2.2]окт-1-ил]-1,3,5-гексатриинил]-1H-имидазол-2-ил]-, (2R)-пирролидин, LCMS (М+1) 856.
1-[(2R)-2-Фенил-2-(1-пиперидинил)ацетил]-2-[5-[[4-[4-[2-[(2R)-1-[(2R)-2-фенил-2-(1-пиперидинил)ацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]бицикло[2.2.2]окт-1-ил]этинил]-1H-имидазол-2-ил]-, (2R)-пирролидин, LCMS (М+1) 856.
N-[(1S)-2-[(2S)-2-[5-[[5-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-диоксан-2-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 785.
N-[(1S)-2-[(2S)-2-[5-[[2-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-диоксан-5-ил]этинил]-1Н-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 785.
N-[(1S)-2-[(2S)-2-[5-[2-[4-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,3-диоксан-5-ил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 809.
N-[(1S)-2-[(2S)-2-[5-[5-[4-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,3-диоксан-2-ил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 809.
N-[(1S)-2-[(2S)-2-[5-[6-[5-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-диоксан-2-ил]-1,3,5-гексатриинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 833.
N-[(1S)-2-[(2S)-2-[5-[[5-[4-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,3-диоксан-2-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 833.
N-[(1S)-2-[(2S)-2-[5-[[2-[4-[2-[(2S)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,3-диоксан-5-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 833.
N-[(1S)-2-[(2R)-2-[5-[[5-[4-[2-[(2R)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,3-диоксан-2-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 833.
N-[(1S)-2-[(2R)-2-[5-[[5-[2-[(2R)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,4-диоксан-2-ил]этинил]-1Н-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 785.
N-[(1S)-2-[(2R)-2-[5-[5-[4-[2-[(2R)-1-[(2S)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,4-диоксан-2-ил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 809.
N,N'-[1,4-Диоксан-2,5-диилбис[2,1-этиндиил-1H-имидазол-5,2-диил(2R)-2,1-пирролидиндиил[(1S)-2-оксо-1-фенил-2,1-этандиил]]]бис-циклопропанкарбоксамид, LCMS (M+1) 809.
N-[(1R)-2-[(2S)-2-[5-[[5-[4-[2-[(2S)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1,4-диоксан-2-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 833.
N-[(1R)-2-[(2S)-2-[5-[6-[5-[2-[(2S)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,4-диоксан-2-ил]-1,3,5-гексатриинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 833.
N-[(1R)-2-[(2S)-2-[5-[6-[5-[[2-[(2S)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]этинил]-1,4-диоксан-2-ил]-1,3,5-гексатриинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (M+1) 857.
N,N-[1,4-Диоксан-2,5-диилбис[1,3-бутадиин-4,1-диил-1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1R)-2-оксо-1-фенил-2,1-этандиил]]]бис-циклопропанкарбоксамид, LCMS (M+1) 857.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[6-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3,5-гексатриинил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 16, LCMS (M+1) 735 40 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 6.86 (с, 1Н), 7.28 (с, 1Н), 7.72 (д, J=8.26, 2Н), 7.90 (д, J=1.95, 2Н), 8.80 (м, 4Н).
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]фенил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 15, LCMS (M+1) 735 40 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 6.82 (д, J=0.93, 1Н), 7.33 (с, 1Н), 7.88 (т, J1=2.02, J2=0.71, 2Н), 7.93 (м, 2Н), 8.80 (м, 4Н).
Диметиловый эфир [1,4-фениленбис[1,3-бутадиин-4,1-диил-1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, соединение 17, LCMS (М+1) 759 40 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2H), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 7.33 (с, 2Н), 7.81 (с, 4Н), 8.80 (м, 4Н).
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[6-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-нафталенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 19, LCMS (М+1) 761 40 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 6.94 (с, 1Н), 7.33 (с, 1Н), 7.65 (д, J=8.56, 1H), 7.85 (м, 1H), 7.91 (м, 1Н), 8.05 (уш.д, 2Н), 8.61 (т, J1=1.65, J2=0.33, 1H), 8.79 (м, 4H).
N-[(1R)-2-[(2R)-2-[5-[5-[6-[2-[(2R)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3,5-гексатриинил]-1-нафталенил]-1H-имидазол-2-ил]-1-пиррилидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 874.
N-[(1R)-2-[(2R)-2-[5-[[4-[4-[2-[(2R)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1-нафталениел]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 874.
N-[(1R)-2-[(2R)-2-[5-[[5-[4-[2-[(2R)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-1-нафталенил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 874.
N-[(1R)-2-[(2R)-2-[5-[5-[2-[2-[(2R)-1-[(2R)-2-[(Циклопропилкарбонил)амино]-2-фенилацетил]-2-пирролидинил]-1H-имидазол-5-ил]этил]-2-тиенил]-1H-имидазол-2-ил]-1-пирролидинил]-2-оксо-1-фенилэтил]-циклопропанкарбоксамид, LCMS (М+1) 785.
N,N'-[2,5-Тиендиилбис[2,1-этандиил-1H-имидазол-5,2-диил(1S)этилиден]]бис[N'-метил-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 790.
N-Метил-N-[(1S)-1-[5-[(E)-2-[5-[2-[(1S)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-2-тиенил]этенил]-1H-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 760.
N-Метил-N-[(1S)-1-[5-[(E)-2-[5-[2-[2-[(1S)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]этил]-2-тиенил]этенил]-1H-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (M+1) 788.
N,N'-[2,5-Тиендиилбис[(E)-2,1-этендиил-1H-имидазол-5,2-диил(1S)этилиден]]бис[N'-метил-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 786.
N-Метил-N-[(1R)-1-[5-[[5-[2-[2-[(1R)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]этил]-2-тиенил]этинил]-1Н-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 786.
N-Метил-N-[(1R)-1-[5-[(E)-2-[5-[[2-[(1R)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]этинил]-2-тиенил]этенил]-1H-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 784.
N-Метил-N-[(1R)-1-[5-[[5-[2-[(1R)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-2-тиенил]этинил]-1H-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 758.
N-Метил-N-[(1R)-1-[5-[4-[5-[2-[(1R)-1-[метил[(2S)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-2-тиенил]-1,3-бутадиинил]-1H-имидазол-2-ил]этил]-α-фенил-, (αS)-1-пиперидинацетамид, LCMS (М+1) 782.
N-Метил-N-[(1S)-1-[5-[5-[6-[2-[(1S)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-1,3,5-гексатриинил]-2-тиенил]-1Н-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 806.
N-Метил-N-[(1S)-1-[5-[[5-[4-[2-[(1S)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-тиенил]этинил]-1H-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 806.
N,N'-[2,5-Тиендиилбис[1,3-бутадиин-4,1-диил-1H-имидазол-5,2-диил(1S)этилиден]]бис[N'-метил-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 830.
N-Метил-N-[(1S)-1-[5-[[5-[4-[2-[(1S)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-тиенил]метил]-1H-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 796.
N-Метил-N-[(1R)-1-[5-[2-[5-[4-[2-[(1R)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-тиенил]этил]-1H-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 810.
N-Метил-N-[(1R)-1-[5-[(E)-2-[5-[4-[2-[(1R)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-тиенил]этенил]-1H-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (M+1) 808.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]фенил]этинил]-2-тиенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 769.
Диметиловый эфир [1,2-этиндиил[5,2-тиендиил-1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, дигидрохлорид, соединение 26, LCMS (M+1) 775, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 4Н), 2.10 (м, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.03 (м, 2Н), 4.74 (м, 2Н), 6.61 (д, J=3.50, 2Н), 7.00 (д, J=0.25, 2Н), 7.17 (д, J=3.50, 2Н), 8.79 (м, 4Н).
Диметиловый эфир [1,3-бутадиин-1,4-диилбис[5,2-тиендиил-1H-имидазол-5,2-диил(2S)-2,1-пирролидиндиил[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, дигидрохлорид, соединение 27, LCMS (M+1) 799, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 4Н), 2.10 (м, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.03 (м, 2Н), 4.74 (м, 2Н), 6.54 (д, J=3.50, 2Н), 7.00 (д, J=0.25, 2Н), 7.67 (д, J=3.50, 2Н), 8.79 (м, 4Н).
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]фенил]-1,3-бутадиинил]-2-тиенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, дигидрохлорид, соединение 28, LCMS (M+1) 793, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 4Н), 2.10 (м, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.03 (м, 2Н), 4.74 (м, 2Н), 6.54 (д, J=3.50, 1Н), 6.86 (с, 1Н), 7.00 (д, J=0.25, 1Н), 7.67 (с, 1Н), 7.76 (м, 2Н), 7.91 (д, J=8.26, 2Н), 8.79 (м, 4Н).
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[[5'-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]этинил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 775.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[5'-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]-1,3-бутадиинил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 799.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[4-[[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]этинил]фенил]-2-тиенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 769.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[4-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]фенил]-2-тиенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 793.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[5-[[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]этинил]-2-тиенил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 769.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[5-[4-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-бутадиинил]-2-тиенил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 793.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]метокси]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, гидрохлорид, соединение 10, LCMS (М+1) 693; 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 4Н), 2.10 (м, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 4.01 (д, J=0.42, 2Н), 4.75 (м, 2Н), 5.12 (с, 2Н), 6.71 (д, J=0.93, 1Н), 6.87 (с, 1Н), 7.07 (д, J=0,7.89, 2Н), 7.89 (д, J=0.7.89, 2Н), 8.98 (м, 4Н).
N-Метил-N-[(1R)-1-[5-[2-[4-[2-[(1R)-1-[метил[(2R)-2-фенил-2-(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]фенокси]этил]-1H-имидазол-2-ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 772.
N-Метил-N-[(1R)-1-[5-[3-[4-[2-[(1R)-1-[метил[(2R)-2-фенил-2(1-пиперидинил)ацетил]амино]этил]-1H-имидазол-5-ил]фенокси]пропил]-1H-имидазол-2-}ил]этил]-α-фенил-, (αR)-1-пиперидинацетамид, LCMS (М+1) 786.
Метиловый эфир [(1S)-1-[[[(1S)-1-[5-[(1E)-3-[4-[2-[(1S)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1Н-имидазол-5-ил]фенокси]-1-пропенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 695.
Метиловый эфир [(1S)-1-[[[(1S)-1-[5-[3-[4-[2-[(1S)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]фенокси]-1-пропинил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 693.
Диметиловый эфир [1,4-фениленбис[окси-2,1-этандиил-1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (M+1) 727.
Диметиловый эфир [1,4-фениленбис[окси-1-пропин-3,1-диил-1H-имидазол-5,2-диил(1S)этилиден(метилимино)[(1S)-1-(1-метилэтил)-2-оксо-2,1-этандиил]]]бис-карбаминовой кислоты, LCMS (M+1) 747.
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[5-[4-[2-[(1R)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1Н-имидазол-5-ил]циклогексил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 747.
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[5-[4-[2-[(1R)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-транс-циклогексил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 747.
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[5-[4-[2-[(1R)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]бицикло[2.2.2]окт-1-ил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 753.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[5-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,3-диоксан-2-ил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 22, LCMS (M+1) 749, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6H), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.22 (м, 1Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 3.84 (м, 2Н), 4.01 (д, J=0.42, 2Н), 4.08 (м, 2Н), 4.75 (м, 2Н), 5.48 (м, 1Н), 6.75 (с, 1Н), 6.86 (с, 1Н), 7.68 (д, J=8.06, 2Н), 7.92 (д, J=1.99, 2Н), 8.92 (м, 4Н).
Метиловый эфир [(1S)-1-[[[(1R)-1-[5-[4-[2-[2-[(1R)-1-[[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,3-диоксан-5-ил]фенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 725.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[4-[5-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил]-1,4-диоксан-2-ил]фенил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 23, LCMS (М+1) 749, 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 6Н), 0.97 (т, J1=6.50, J2=0.93, 6Н), 1.64 (м, 2Н), 1.84 (м, 2Н), 1.97 (м, 2Н), 2.10 (м, 2Н), 3.45 (д, J=14.76, 2Н), 3.56 (м, 2Н), 3.63 (м, 8Н), 3.73 (м, 2Н), 3.90 (м, 2Н), 4.03 (м, 2Н), 4.47 (м, 1Н), 4.64 (м, 1Н), 4.75 (м, 2Н), 6.82 (с, 1Н), 6.86 (с, 1Н), 7.68 (д, J=8.06, 2Н), 7.92 (м, 2Н), 8.92 (м, 4Н).
Метиловый эфир [(1R)-1-[[[(1S)-1-[5-[6-[5-[2-[(1S)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,3-диоксан-2-ил]-2-нафталенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 775.
Метиловый эфир [(1R)-1-[[[(1S)-1-[5-[6-[2-[2-[(1S)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,3-диоксан-5-ил]-2-нафталенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 775.
Метиловый эфир [(1R)-1-[[[(1S)-1-[5-[6-[5-[2-[(1S)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,4-диоксан-2-ил]-2-нафталенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 775.
Метиловый эфир [(1R)-1-[[[(1S)-1-[5-[2-[4'-[2-[(1S)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил][1,1'-дифенил]-4-ил]-1,3-диоксан-5-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 801.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[5-[4'-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил][1,1'-дифенил]-4-ил]-1,3-диоксан-2-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 801.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[5-[4'-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил][1,1-дифенил]-4-ил]-1,4-диоксан-2-ил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 801.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[5-[5-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,3-диоксан-2-ил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 731.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[5-[2-[2-[(1R)-1-[[(2R)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,3-диоксан-5-ил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 731.
Метиловый эфир [(1R)-1-[[[(1R)-1-[5-[5-[5-[2-[(1R)-1-[[(2H)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]метиламино]этил]-1H-имидазол-5-ил]-1,4-диоксан-2-ил]-2-тиенил]-1H-имидазол-2-ил]этил]метиламино]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 731.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[2-[5'-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]-1,3-диоксан-5-ил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 838.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[5'-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]-1,3-диоксан-2-ил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 838.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-[5-[5'-[2-[(2S)-1-[(2S)-2-[(метоксикарбонил)амино]-3-метил-1-оксобутил]-2-пирролидинил]-1H-имидазол-5-ил][2,2'-дитиофен]-5-ил]-1,4-диоксан-2-ил]-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 838.
Пример 10. Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-фенил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 42.
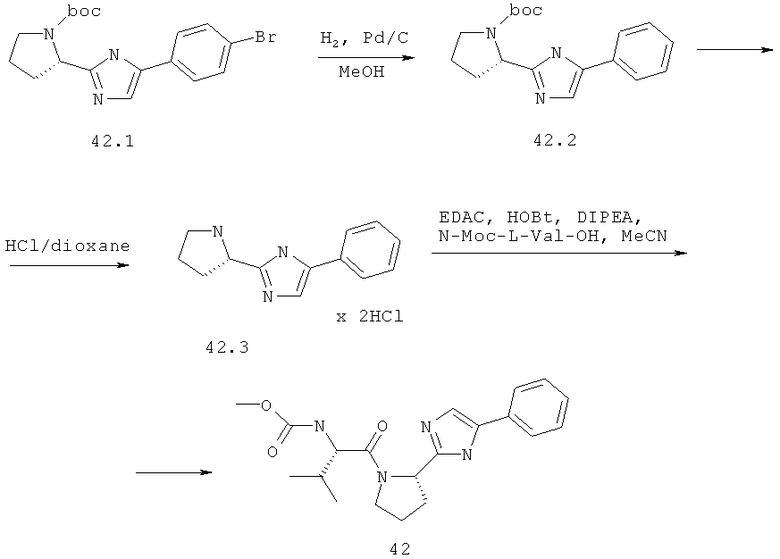
К раствору 196 мг (0.5 ммоль) соединения 42.1 в 10 мл метанола добавляют 10 мг 10% Pd/C и смесь перемешивают в токе водорода в течение 12 ч. Смесь фильтруют через целит и упаривают в вакууме. Выход соединения 42.2 153 мг (98%). LC-MS (ESI): m/z 314 (M+H)+. Соединение 42.2 дебокируют 3М раствором HCl в диоксане с количественным выходом с получением соединения 42.3 (LCMS (ESI): m/z 214 (M+H)+), которое превращают в соединение 42 (LCMS (ESI): m/z 371 (M+H)+) по аналогии с превращением соединения 18.5 в соединение 18. Дигидрохлорид 42 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 42 в CH2Cl2 и высаживанием эфиром. 1Н ЯМР (ДМСО-d6, 400 МГц) δ 14.85 (уш.м, 2Н), 8.05 (с, 1Н), 7.86 (м, 2Н), 7.50 (м, 2Н), 7.41 (м, 1Н), 7.27 (д, J=8.8 Гц, 1Н), 5.17 (т, J=6.8 Гц, 1Н), 4.11 (т, J=7.8 Гц, 1Н), 4.00 (м, 1H), 3.83 (уш.м, 1Н), 3.56 (с, 0.25Н), 3.53 (с, 2.75H), 2.36 (м, 1Н), 2.16 (м, 2Н), 2.06 (м, 1H), 2.00 (м, 1H), 0.90 (м, 0.5Н), 0.84 (д, J=6.4 Гц, 2.75Н), 0.77 (д, J=6.4 Гц, 2.75Н).
Пример 11. Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-нафталин-1-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 43.
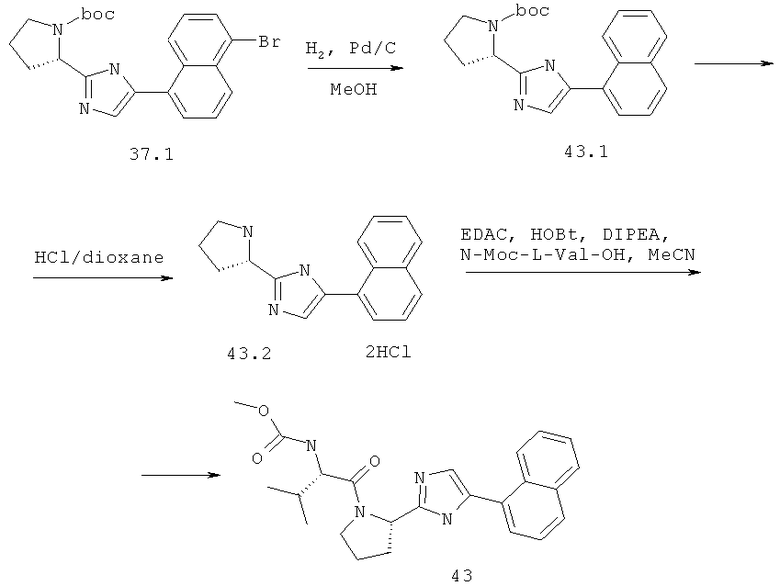
Соединение 43.1 получают по методике, приведенной для соединения 42.2. Выход 92%. LCMS (ESI): m/z 364 (М+Н)+. Соединение 43.1 дебокируют 3М раствором HCl в диоксане с количественным выходом с получением соединения 43.2 (LCMS (ESI): m/z 264 (M+H)+), которое превращают в соединение 43 (LCMS (ESI): m/z 421 (М+Н)+) по аналогии с превращением соединения 14.5 в соединение 14. Дигидрохлорид 43 получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 42 в CH2Cl2 и высаживанием эфиром.
Пример 12. Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-нафталин-2-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 44.
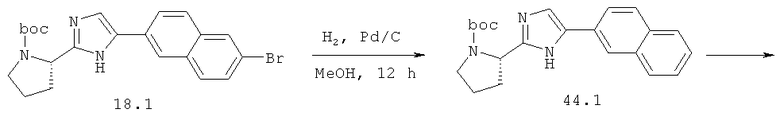
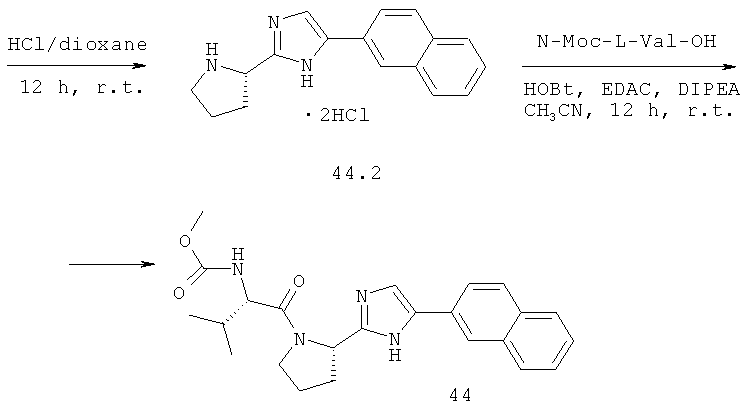
Синтез лиганда 44 осуществляют по аналогии с синтезом лиганда 43. Соединение 44.1 получено с выходом 97%. LCMS (ESI): m/z 364,4 (М+Н)+. ЯМР (ДМСО-d6, 400 МГц) δ 14.6 (уш.с, 1,5Н), 8.36 (с, 1Н), 8.22 (д, J=21.6 Гц, 1Н), 8.09 (д, J=18.8 Гц, 1Н), 7.97 (м, 2Н), 7.91 (д, J=8.8 Гц, 1Н), 7.60 (м, 2Н), 5.07 (м, 1Н), 7.20 (м, 1Н), 3.44 (м, 1Н), 2.43, (уш.м, 1Н), 2.08 (м, 1Н), 1.98 (м, 2Н), 1.41 (с, 3.5Н), 1.18 (с, 5.5Н). Соединение 44.2 получено с выходом 94%. LCMS (ESI): m/z 264,3 (М+Н)+. ЯМР (ДМСО-d6, 400 МГц) δ 10.09 (уш.с, 1Н), 9.58 (уш.с, 0.6Н), 8.43 (с, 1Н), 8.11 (с, 1Н), 8.00 (уш.с, 2Н), 7.93 (уш.м, 2Н), 7.54 (м, 2Н), 4.97 (уш.м, 1Н), 3.40 (уш.м, 1Н), 2.42 (м, 1Н), 2.20 (уш.м, 1Н), 2.03 (м, 2Н). Лиганд 44 получен с выходом 33%. Дигидрохлорид 44·2HCl получают добавлением избытка 3М раствора HCl в диоксане к раствору основания 1144 в CH2Cl2 и высаживанием эфиром. LCMS (ESI): m/z 421,2 (М+Н)+. ЯМР (ДМСО-d6, 400 МГц) δ 15.02 (уш.с, 1Н), 14.67 (уш.с, 1Н), 8.43 (с, 1Н), 8.18 (с, 1Н), 8.06 (д, J=8.8 Гц, 1Н), 7.94 (м, 3Н), 7.59 (м, 2Н), 7.29 (д, J=8,4 Гц, 1Н), 5.19 (т, J=6.6 Гц, 1Н), 4.13 (т, J=7.6 Гц, 1Н), 3.96 (уш.м, 1Н), 3.86, (уш.м, 1Н), 3.56 (с, 0.8Н), 3.54 (с, 2.2Н), 2.40 (м, 1Н), 2.18 (уш.м, 2Н), 2.05 (м, 2Н), 0.91 (м, 0.6Н), 0.81 (д.д, J1=27.2 Гц, J2=6.4 Гц, 5.4Н).
Пример 13. Метиловый эфир {(S)-2-метил-1-[(S)-2-(5-тиофен-2-ил-1Н-имидазол-2-ил)-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 58 и метиловый эфир {(S)-2-Метил-1-[(S)-2-[5-(2,2'-дитиофен-5-ил)-1Н-имидазол-2-ил]-пирролидин-1-карболин]-пропил}-карбаминовой кислоты 59.
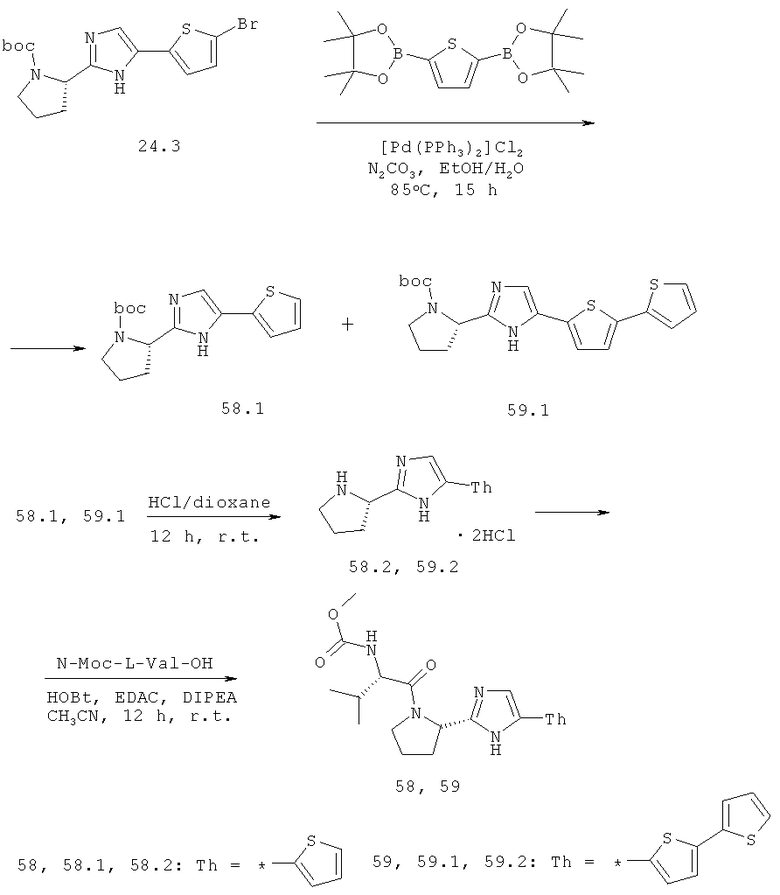
Суспендируют 256 мг (0,762 ммоль, 1 экв.) боронового эфира и 404 мг (3,81 ммоль, 5 экв.) карбоната натрия в смеси 7,5 мл этанола и 1,8 мл воды. Через смесь барботируют аргон в течение 40 минут при 90°С. Затем смесь охлаждают до 80°С, добавляют в нее 667 мг (1,68 ммоль, 2,2 экв.) соединения 24.3 и барботируют аргон в течение еще 10 минут. Далее добавляют 53 мг (0,0762 ммоль, 0,1 экв.) [Рd(РРh3)2]Cl2 и барботируют аргон 5 минут. В конце к реакционной смеси добавляют 2,9 мг (0,0762 ммоль, 0,1 экв.) боргидрида натрия. Реакционную массу перемешивают 15 ч при 85°С в атмосфере аргона. Полноту протекания реакции контролируют методом LCMS. После завершения реакции реакционную массу фильтруют через слой Celite, фильтрат упаривают на роторном испарителе. Остаток растворяют в дихлорметане, экстракт промывают водой, сушат безводным сульфатом натрия, упаривают на роторном испарителе. Соединение 7 очищают методом колоночной хроматографии (элюэнт - градиент гексан:ТГФ: триэтиламин= от 12:1:0,1 до 8:1:0,1). Соединение 6 очищают методом HPLC. Получают соединение 58.1 - 71 мг, выход 29%, соединение 59.1 - 120 мг, выход 39%.
Соединение 58.1 - LCMS (ESI): m/z 320.0 (М+Н)+. ЯМР (CDCl3-d3, 400 МГц) δ 10.5 (уш.с, 1.4Н), 7.21 (уш.м, 1Н), 7.17 (д, J=4.0 Гц, 1Н), 7.12 (с, 1Н), 7.02 (т, J=4.0 Гц, 1Н), 4.96 (м, 1Н), 3.50 (уш.м, 1Н), 3.41 (уш.м, 1Н), 3.00 (уш.м, 1Н), 2.15 (уш.м, 2Н), 1.96 (м, 1Н), 1.50 (с, 9Н). Соединение 59.1 - LCMS (ESI): m/z 402,1 (М+Н)+. Синтез лигандов 58 и 59 осуществляют по аналогии с синтезом соединения 14 из 14.5. Дигидрохлориды 58 и 59 получают добавлением избытка 3М раствора HCl в диоксане к растворам оснований 58 и 59 в CH2Cl2 и высаживанием эфиром. Соединение 58.2: LCMS (ESI): m/z 220,1 (М+Н)+. Лиганд 58: LCMS (ESI): m/z 377,2 (M+H)+. Соединение 59.2: LCMS (ESI): m/z 302,3 (M+H)+. ЯМР (ДМСО-d6, 400 МГц) δ 10.3 (уш.с, 1H), 9.48 (уш.с, 1Н), 7.80 (с, 1Н), 7.52 (д, J=4.8 Гц, 1H), 7.44 (д, J=3.2 Гц, 1H), 7,32 (д, J=4.8 Гц, 1H), 7.29, (т, J=3.6 Гц, 1H), 7.10 (дд, J1=4.8 Гц, J2=4.0 Гц, 1H), 4,84 (уш.м, 1H), 3.34 (уш.м, 2Н), 2.41 (м, 1H), 2.33 (м, 1H), 2.15 (м, 1H), 1.99 (м, 1H). Лиганд 59: LC-MS (ESI): m/z 459,5 (М+Н)+. ЯМР (ДМСО-d6, 400 МГц) δ 14.45 (уш.с, 1H), 7.90 (с, 1H), 7.58 (m, 2Н), 7.37 (с, 2Н), 7.28 (д, J=8.4 Гц, 1H), 7.13 (м, 1H), 5.09 (т, J=6.4 Гц, 1H), 4.10 (т, J=7.2 Гц, 1H), 3.90 (уш.м, 1H), 3.84 (уш.м, 1H), 3.56 (с, 0.5Н), 3.54 (с, 2.5Н), 2.35 (м, 1H), 2.15 (уш.м, 2Н), 2.02 (м, 2Н), 0.88 (м, 0.7Н), 0.80 (д.д, J1=23.0 Гц, J2=6.6 Гц, 5.3Н).
Метиловый эфир [(1S)-1-[[(2R)-2-(5-этинил-1H-имидазол-2-ил)-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 319.
Метиловый эфир [(1S)-2-метил-1-[[(2R)-2-[5-(2-пропинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]пропил]-карбаминовой кислоты, LCMS (M+1) 333.
Метиловый эфир [(1S)-1-[[(2R)-2-[5-(3-бутинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 347.
Метиловый эфир [(1S)-1-[[(2R)-2-[5-(2-бутинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 347.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-(1,3-бутадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, соединение 39, LCMS (M+1) 343. 1Н ЯМР (DMSO-D6, 400 МГц) δ 0.88 (т, J1=6.50, J2=0.93, 3Н), 0.95 (т, J1=6.75, J2=0.93, 3Н), 1.64 (м, 1H), 1.85 (м, 1H), 1.92 (с, 1H), 1.99 (м, 2Н), 2.10 (м, 1H), 3.56 (м, 1Н), 3.61 (д, J=9.40, 3Н), 3.68 (м, 1Н), 4.03 (д, J=0.42, 1H), 4.73 (м, 1Н), 7.25 (с, 1Н), 8.80 (м, 2Н).
Метиловый эфир [(1S)-2-метил-1-[[(2S)-2-[5-(2,4-пентадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]пропил]-карбаминовой кислоты, LCMS (М+1) 357.
Метиловый эфир [(1S)-2-метил-1-[[(2S)-2-[5-(1,3-пентадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]пропил]-карбаминовой кислоты, LCMS (M+1) 357.
Метиловый эфир [(1R)-2-метил-1-[[(2R)-2-[5-(1,4-пентадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]пропил]-карбаминовой кислоты, LCMS (M+1) 357.
Метиловый эфир [(1R)-1-[[(2R)-2-[5-(3,5-гексадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 371.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-(1,3-гексадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 371.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-(1,5-гексадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (M+1) 371.













Метиловый эфир [(1S)-1-[[(2S)-2-[5-(4-циклогексил-1,3-бутадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 425.
Метиловый эфир [(1S)-1-[[(2S)-2-[5-(4-бицикло[2.2.2]окт-1-ил-1,3-бутадиинил)-1H-имидазол-2-ил]-1-пирролидинил]карбонил]-2-метилпропил]-карбаминовой кислоты, LCMS (М+1) 451.
Пример 14. Получение фармацевтической композиции в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг бис-азола 14. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Пример 15. Получение фармацевтической композиции в форме капсул. Тщательно смешивают бис-азол 14 с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Пример 16. Получение фармацевтической композиции в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг бис-азола 14 с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛКИЛ [2-(2-{5-[4-(4-{2-[1-(2-МЕТОКСИКАРБОНИЛАМИНО-АЦЕТИЛ)-ПИРРОЛИДИН-2-ИЛ]-3Н-ИМИДАЗОЛ-4-ИЛ}-ФЕНИЛ)-БУТА-1,3-ДИИНИЛ]-1Н-ИМИДАЗОЛ-2-ИЛ}-ПИРРОЛИДИН-1-ИЛ)-2-ОКСО-ЭТИЛ]-КАРБАМАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2518369C1 |
| Пан-геномные ингибиторы белка NS5A вируса гепатита С, фармацевтические композиции, промежуточные продукты для синтеза ингибиторов и способы их получения и применения | 2016 |
|
RU2669919C1 |
| НУКЛЕОЗИДНЫЕ ИНГИБИТОРЫ РНК-ПОЛИМЕРАЗЫ HCV NS5B, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2014 |
|
RU2567854C1 |
| ПАРА-АМИНОБЕНЗИЛЬНЫЕ ЛИНКЕРЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КОНЪЮГАТАХ | 2021 |
|
RU2839675C1 |
| N-(1-(1-БЕНЗИЛ-4-ФЕНИЛ-1Н-ИМИДАЗОЛ-2-ИЛ)-2,2-ДИМЕТИЛПРОПИЛ)БЕНЗАМИДНЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНЕЗИНОВОГО БЕЛКА ВЕРЕТЕНА (KSP) ДЛЯ ЛЕЧЕНИЯ РАКА | 2005 |
|
RU2427572C2 |
| Пангенотипичный ингибитор белка NS5A вируса гепатита С, фармацевтическая композиция и способы их получения и применения | 2019 |
|
RU2723482C1 |
| ПРОИЗВОДНЫЕ 1-(4-ИЗОКСАЗОЛ-5-ИЛ)-1Н-ПИРАЗОЛ-1-ИЛ)-2-МЕТИЛПРОПАН-2-ОЛА И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИРОРОВ ИЛ-17 И ИФН-ГАММА ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ И ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ | 2018 |
|
RU2785342C2 |
| СОЕДИНЕНИЯ ТИЕНОПИРИМИДИНА | 2013 |
|
RU2637925C2 |
| ЦИТОТОКСИЧЕСКИЕ ПЕПТИДЫ И ИХ КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2012 |
|
RU2586885C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2726622C2 |
Настоящее изобретение относится к новым азолам общих формул 1А и 1В и их фармацевтически приемлемым солям, обладающим активностью в отношении вируса гепатита С и гепатита GBV-C. Указанные соединения обладают свойствами лигандов вирусного белка NS5A и могут быть использованы в качестве активных компонентов для фармацевтической композиции и лекарственного средства для лечения болезней обусловленных указанными вирусами. В общей формуле 1А и 1В


сплошные линии с сопровождающими их пунктирными линиями  представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь; Х и Y необязательно принимают разные значения и представляют собой атом азота, кислорода, серы или группу NH; R1 и R2 представляют собой необязательно одинаковые радикалы 2.1-2.20, в которых звездочкой (*) указано место присоединения к азольным фрагментам. Указанные фрагменты и значения А и В приведены в формуле изобретения. 6 н. и 4 з.п. ф-лы, 1 табл., 16 пр.
представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь; Х и Y необязательно принимают разные значения и представляют собой атом азота, кислорода, серы или группу NH; R1 и R2 представляют собой необязательно одинаковые радикалы 2.1-2.20, в которых звездочкой (*) указано место присоединения к азольным фрагментам. Указанные фрагменты и значения А и В приведены в формуле изобретения. 6 н. и 4 з.п. ф-лы, 1 табл., 16 пр.
1. Замещенные азолы общей формулы 1А и 1В и их фармацевтически приемлемые соли

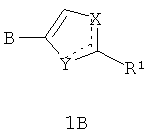
где сплошные линии с сопровождающими их пунктирными линиями  представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь;
представляют собой одинарную или двойную связь, причем если одна из них одинарная связь, то другая двойная связь;
Х и Y необязательно принимают разные значения и представляют собой атом азота, кислорода, серы или группу NH;
R1 и R2 представляют собой необязательно одинаковые радикалы 2.1-2.20, в которых звездочкой (*) указано место присоединения к азольным фрагментам;
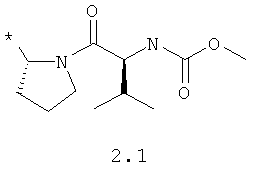
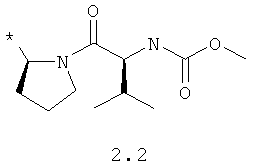
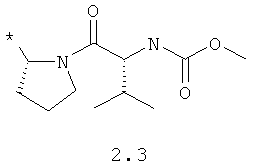

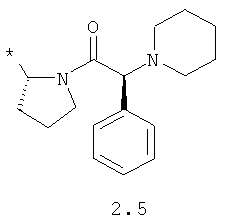
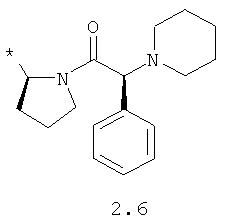
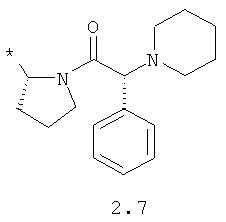
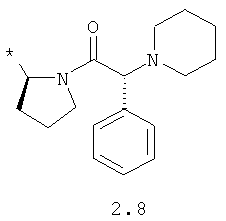
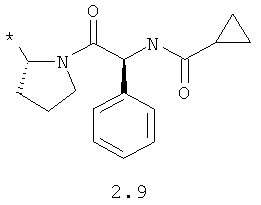
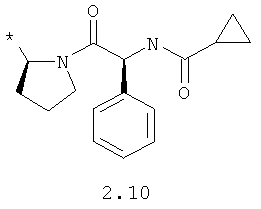
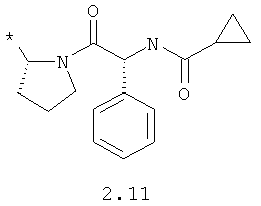
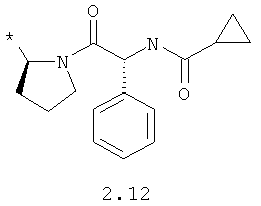
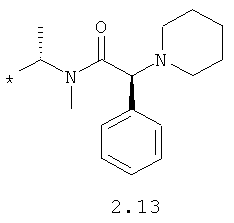
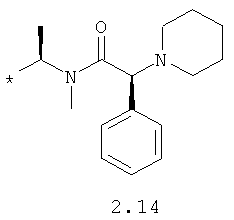
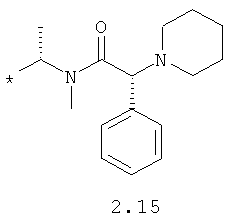
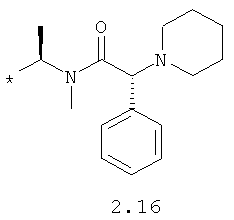
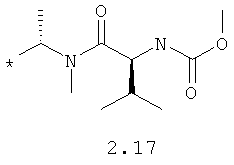
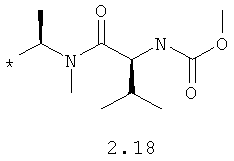
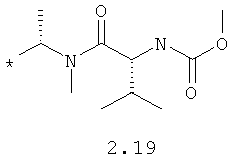

А представляет собой:
- алифатический C2-C8 бирадикал, выбранный из бирадикалов формул 3.1-3.36, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
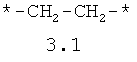
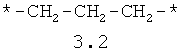
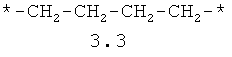
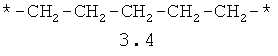
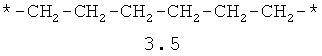
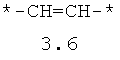
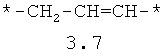
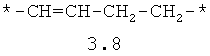
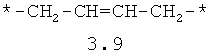
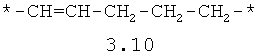
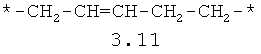
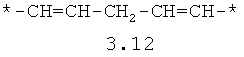
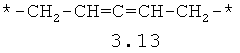
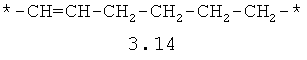

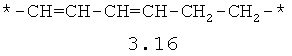


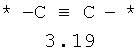
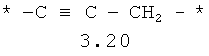
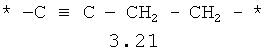

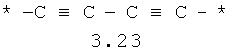
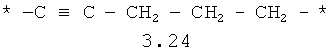
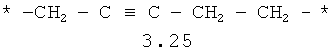
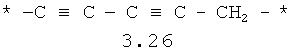

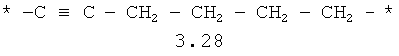
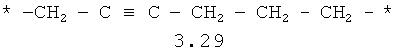
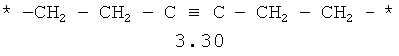
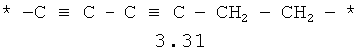

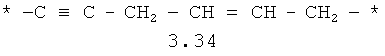
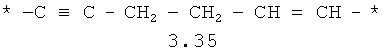
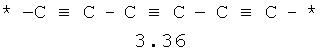
- диоксановый, цикло- и бициклоалифатический бирадикал, выбранный из бирадикалов формул 3.37-3.47, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
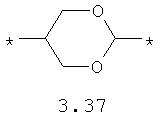
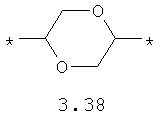
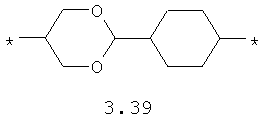
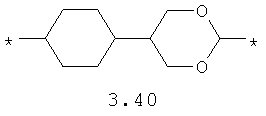

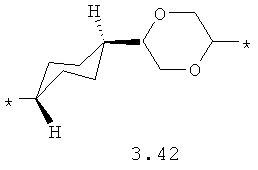
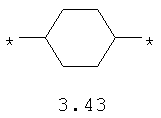
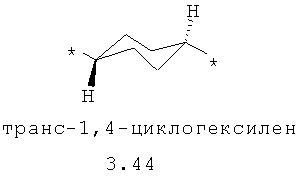
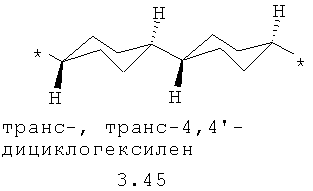
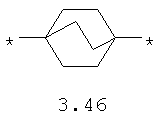
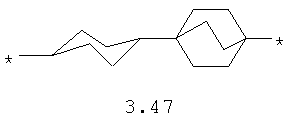
- алкилоксиалкильный, алкенилоксиалкильный, алкинилоксиалкильный бирадикал и их тиоаналог, выбранный из бирадикалов формул 3.48-3.56, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
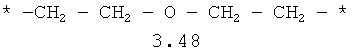
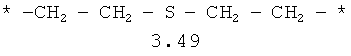
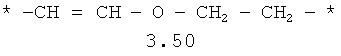

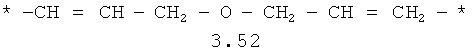
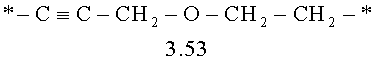
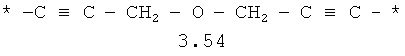
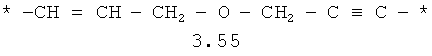
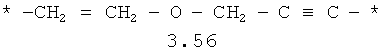
- арильный и тиофеновый бирадикал, выбранные из бирадикалов формул 3.57-3.71, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
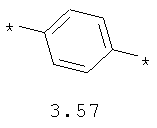
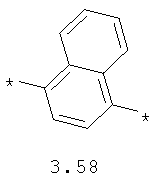
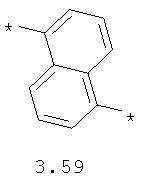
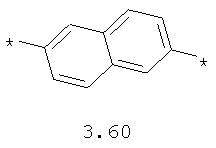
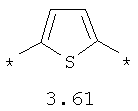
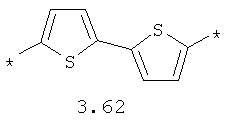
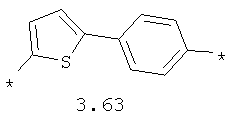
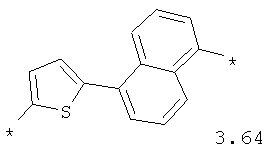
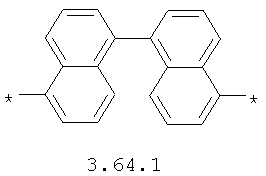
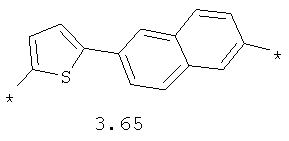
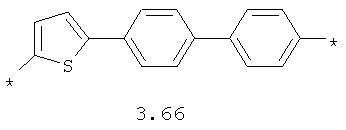
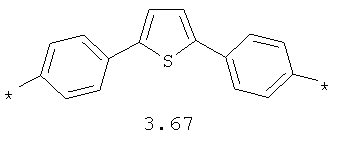
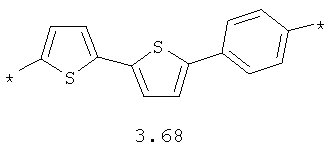
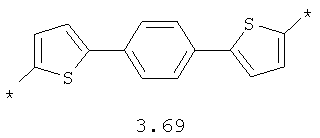


- алкинилциклоалкильный, алкинилдиоксановый, алкиниларильный, алкилтиофеновый, алкенилтиофеновый и алкинилтиофеновый бирадикал, выбранный из бирадикалов формул 3.72-3.129, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
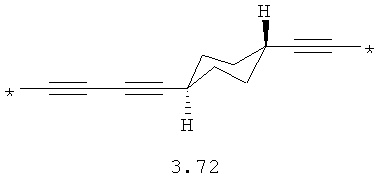
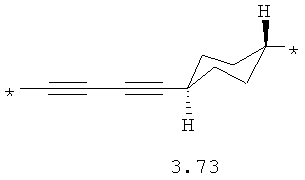
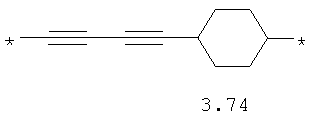
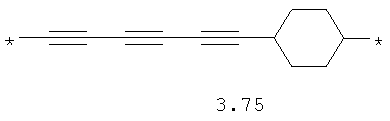
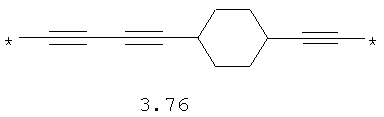


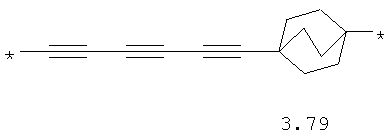
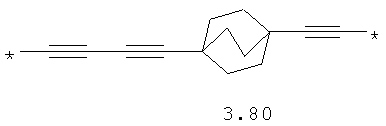
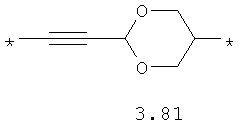
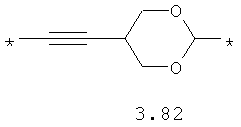
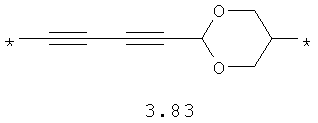
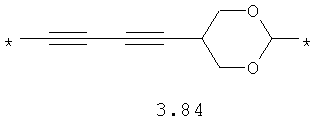
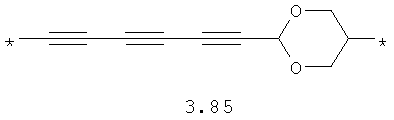
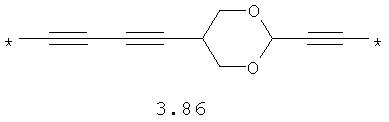
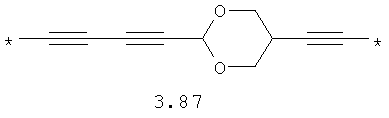
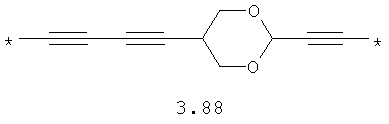
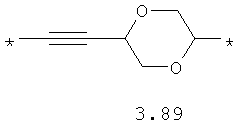
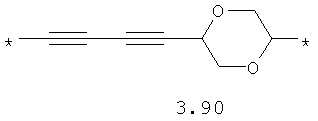
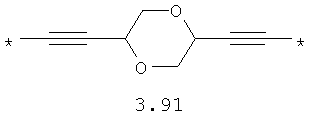
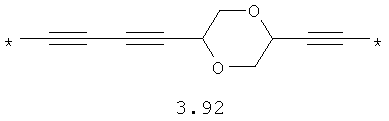
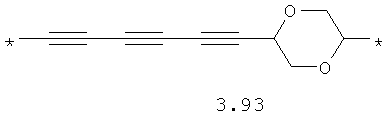


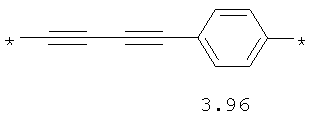
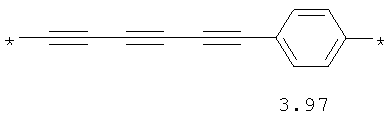

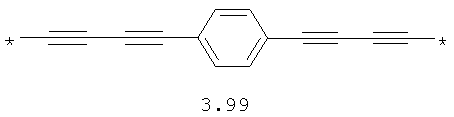
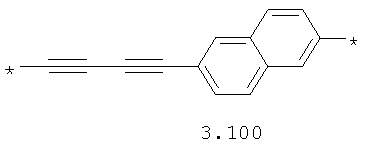
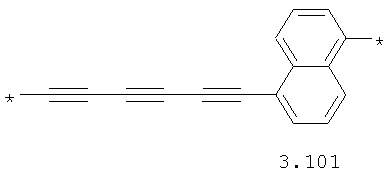
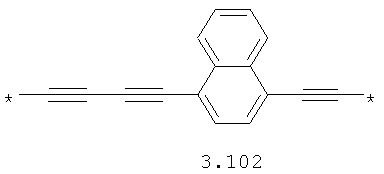
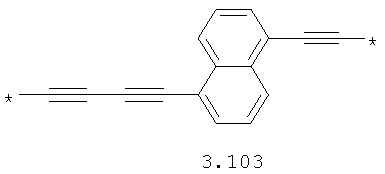
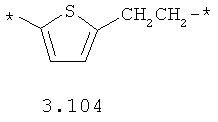
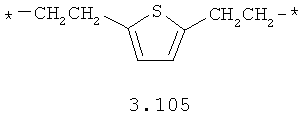
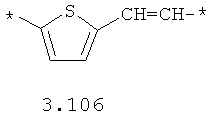
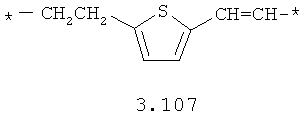
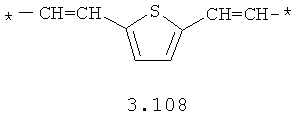

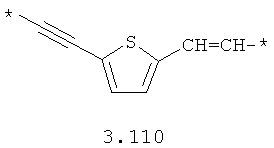
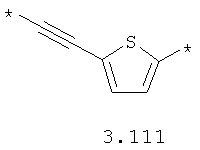
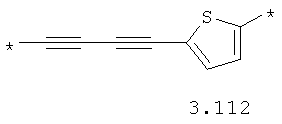
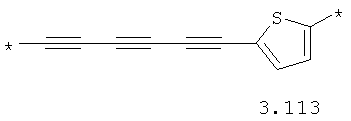
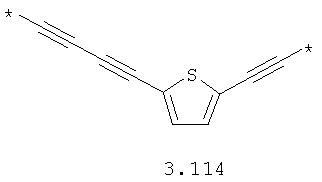
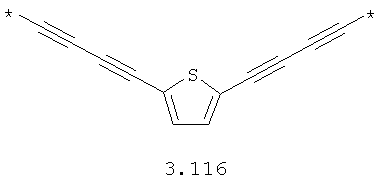
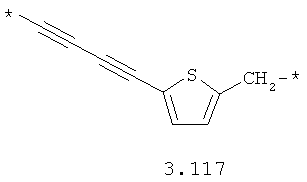
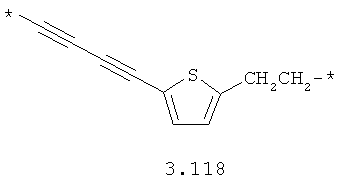
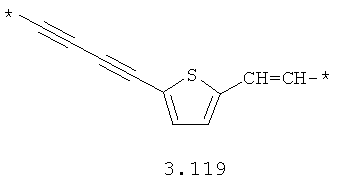
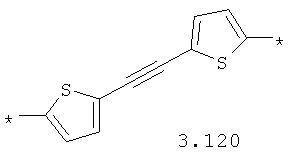
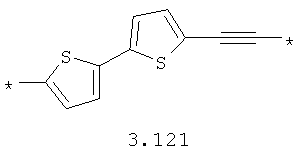
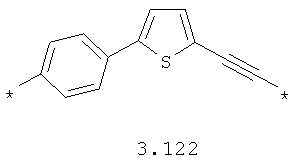
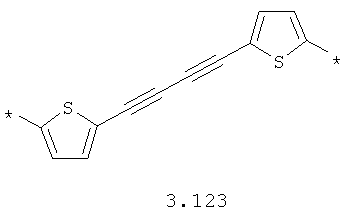
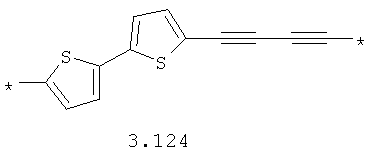
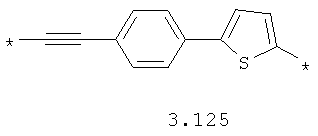
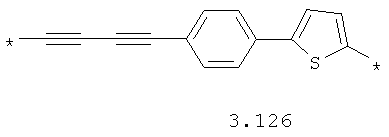
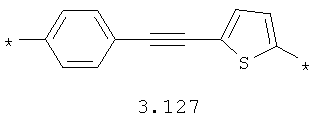
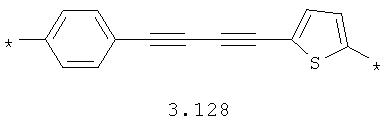
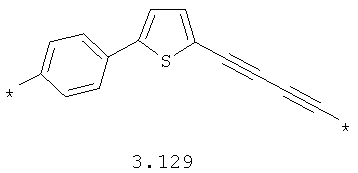
- алкилоксиарильный, алкенилоксиарильный, алкинилоксиарильный бирадикал, выбранный из бирадикалов формул 3.130 - 3.136, в которых звездочкой (*) указаны места присоединения азольных фрагментов;
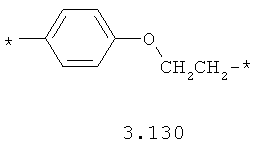
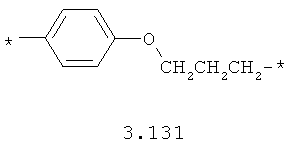
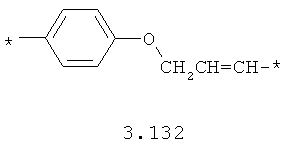
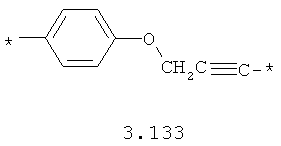
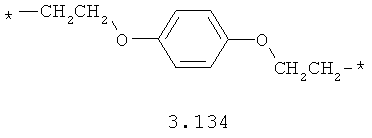
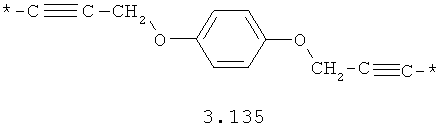
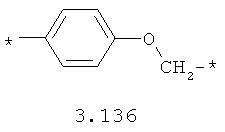
- циклоалкилтиофеновый, арилдиоксановый и тиофендиоксановый бирадикал, выбранный из бирадикалов формул 3.137-3.154, в которых звездочкой (*) указаны места присоединения азольных фрагментов,
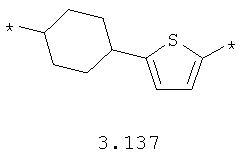
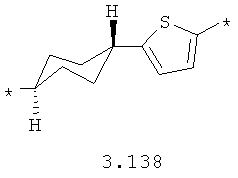
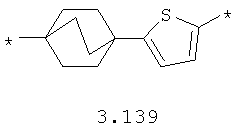
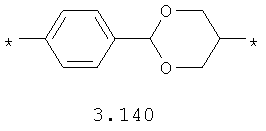
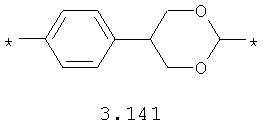
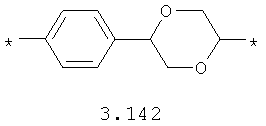
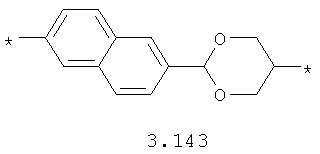
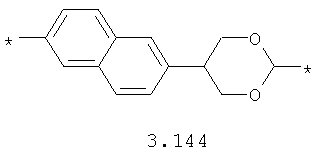


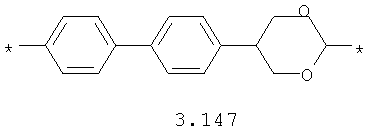
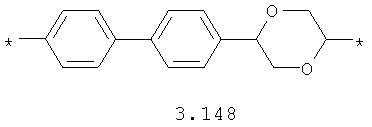
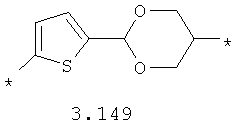
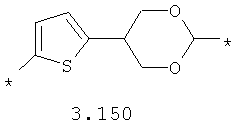
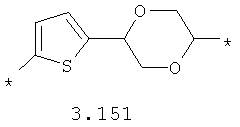
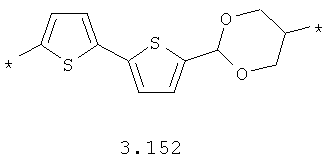
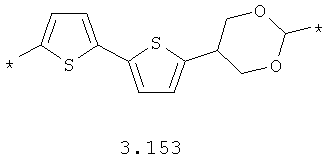
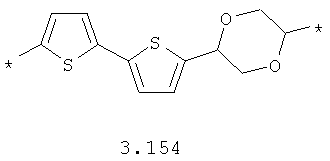
а также
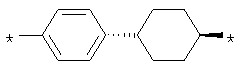
при условии, что в одном из азольных колец Y=NH, а в другом Y=О, R1=R2=2.3;
В представляет собой:
- алифатический С2-С8 радикал, выбранный из радикалов формул 4.1-4.12, в которых звездочкой (*) указано место присоединения азольного фрагмента;
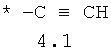
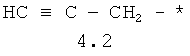


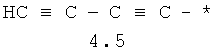
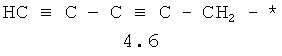
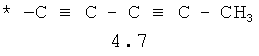
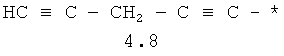
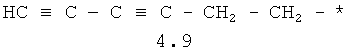
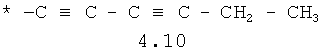

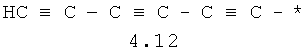
- арильный и тиофенильный радикал, выбранный из радикалов формул 4.13-4.30, в которых звездочкой (*) указано место присоединения азольного фрагмента;
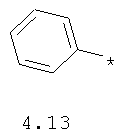
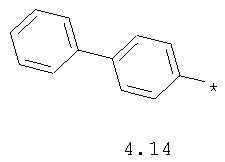

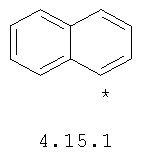
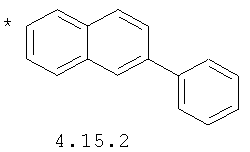
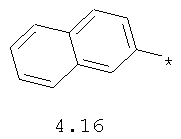
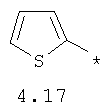
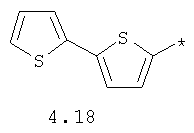
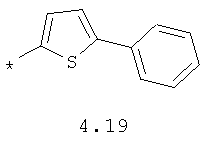
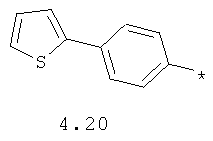
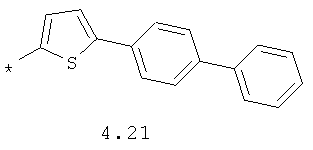
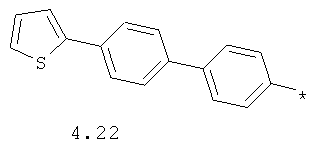

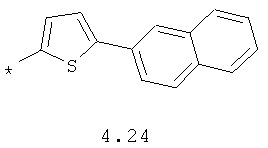
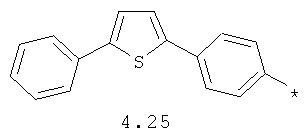
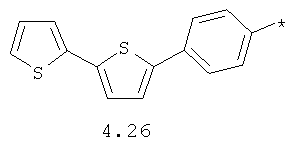
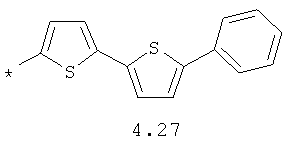
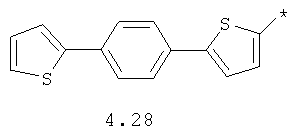
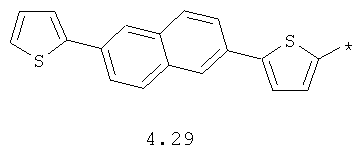
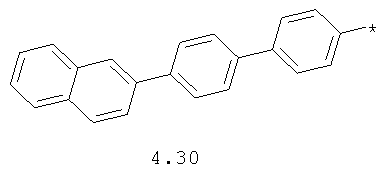
- алкинилциклоалкильный, алкиниларильный, алкилтиофеновый и алкинилтиофеновый радикал, выбранный из формул 4.31-4.47, в которых звездочкой (*) указано место присоединения азольного фрагмента;
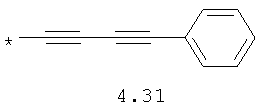
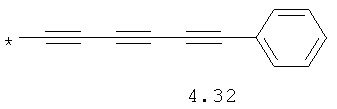

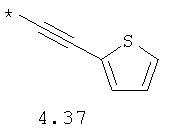
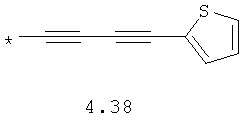
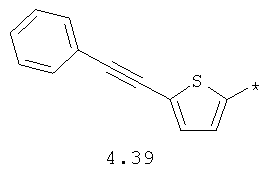
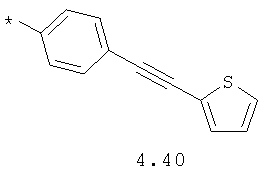
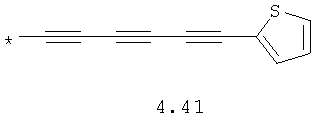
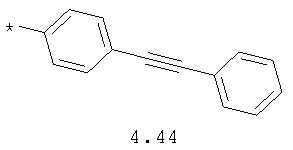
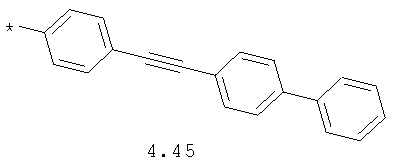
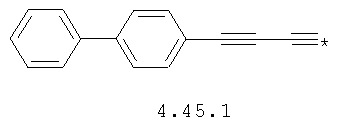
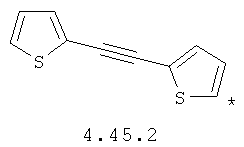
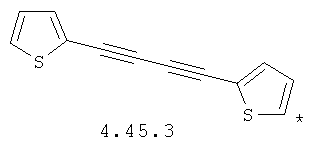

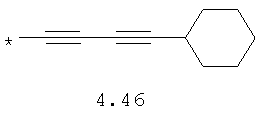
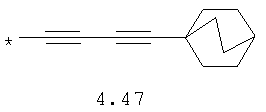
- циклоалкилбензольный, 4-циклоалкилбифенильный, (бициклооктан)бензольный, 4-(бициклооктан)бифениловый, арилдиоксановый и тиофендиоксановый радикал, выбранный из радикалов 4.48-4.72, в которых звездочкой (*) указано место присоединения азольных фрагментов;
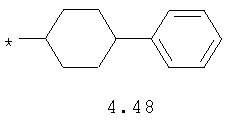
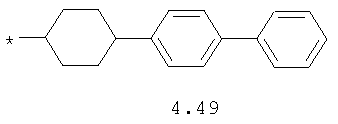
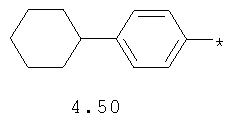
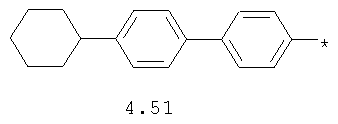
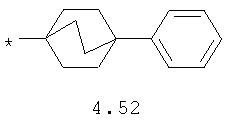
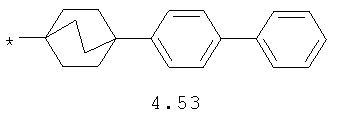
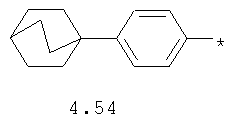
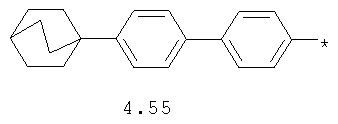
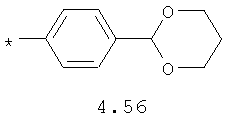
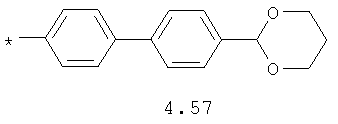
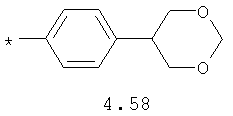
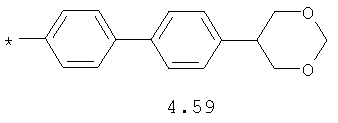
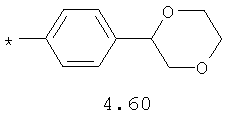
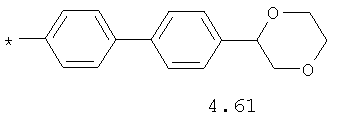
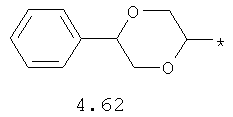

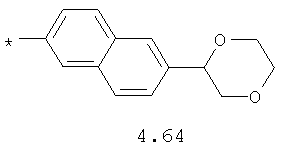
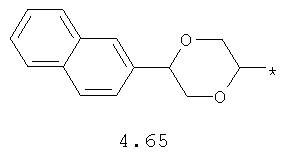
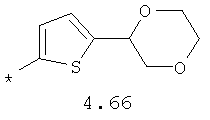
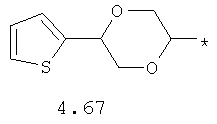
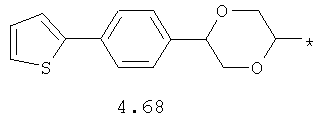
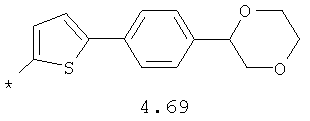
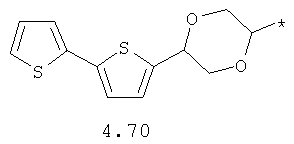
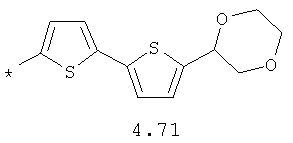
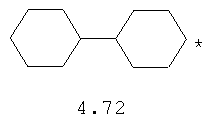
исключая
((R)-1-{(R)-2-[5-(4-{2-[(R)-1-((R)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3H-имидазол-4-ил}-бута-1,3-диинил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовая кислота метиловый эфир;
((S)-1-{(S)-2-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3H-имидазол-4-ил}-фенил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовая кислота метиловый эфир дигидрохлорид;
((S)-1-{(S)-2-[5-(6-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3Н-имидазол-4-ил}-нафталин-2-ил)-1Н-имидазол-2-ил]-пирролидин-1-карбонил}-2-метил-пропил)-карбаминовая кислота метиловый эфир дигидрохлорид;
[(S)-1-((S)-2-{5-[5-(4-{2-[(S)-1-((S)-2-метоксикарбониламино-3-метил-бутирил)-пирролидин-2-ил]-3H-имидазол-4-ил}-фенил)-тиофен-2-ил]-1Н-имидазол-2-ил}-пирролидин-1-карбонил)-2-метил-пропил]-карбаминовая кислота метиловый эфир;
диметил (2S,2'S)-1,1'-((2R,2'R)-2,2'-(5,5'-(4,4'-(тиофен-2,5-диил)бис(4,1-фенилен))бис(1 Н-имидазол-5,2-диил))бис(пирролидин-2,1-диил))бис(3-метил-1-оксобутан-2,1-диил)дикарбамат.
2. Соединения по п.1, представляющие собой замещенные азолы общей формулы 5.1-5.70, в которых X, Y, R1, R2 и сплошные линии с сопровождающими их пунктирными линиями  имеют вышеуказанное значение
имеют вышеуказанное значение
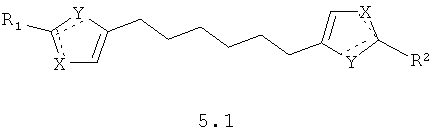
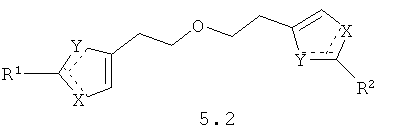
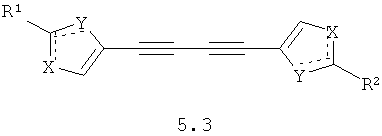
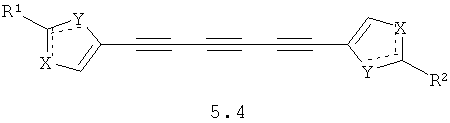

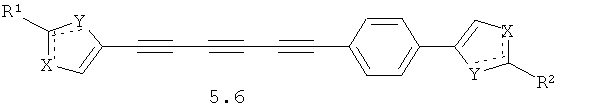
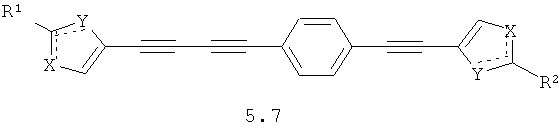

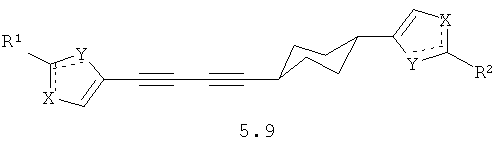
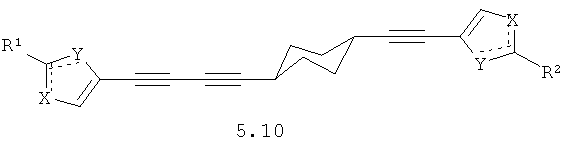
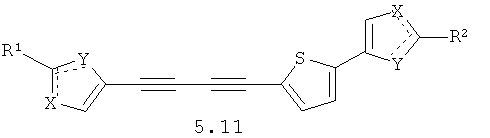

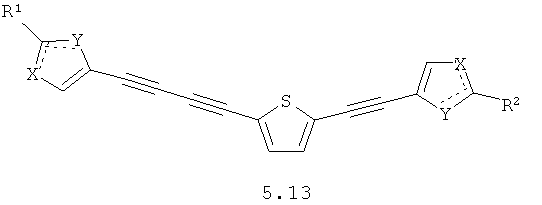
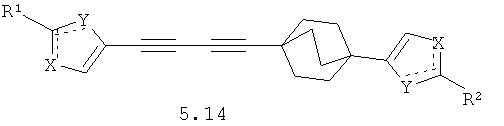
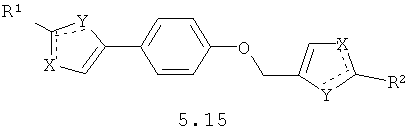
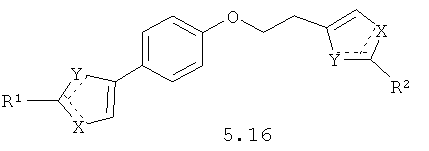
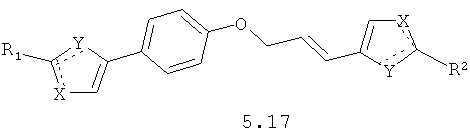
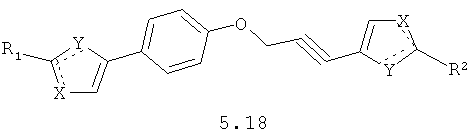

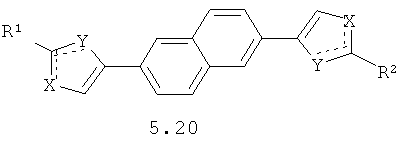
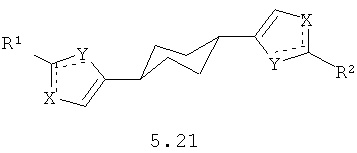
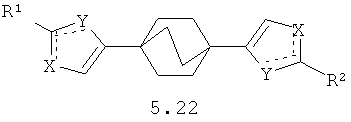
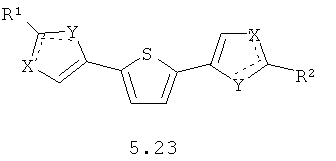
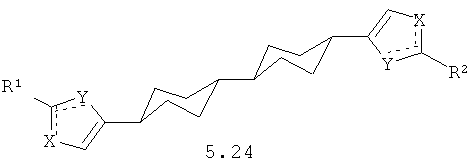

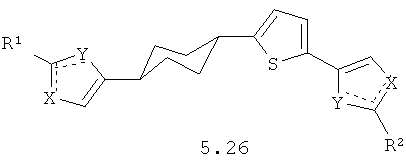
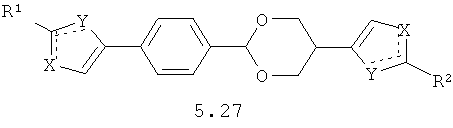
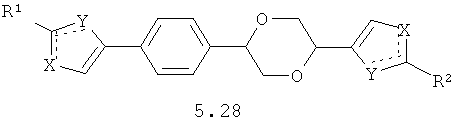
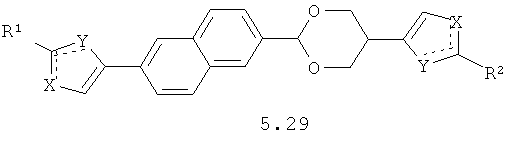
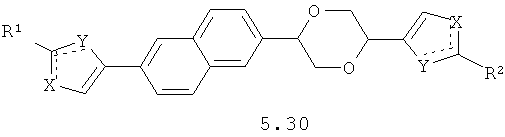
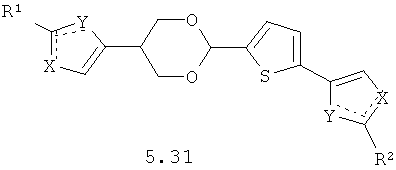
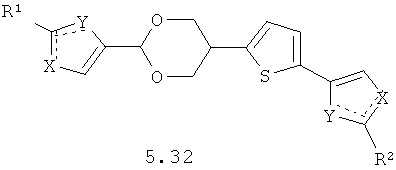
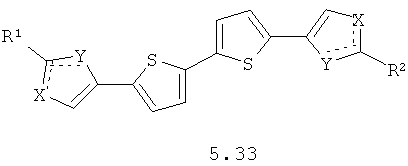
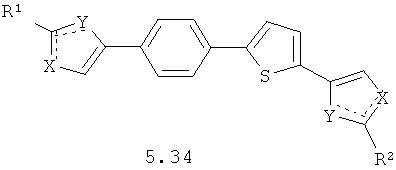
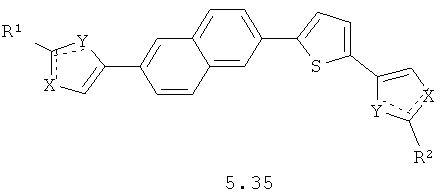

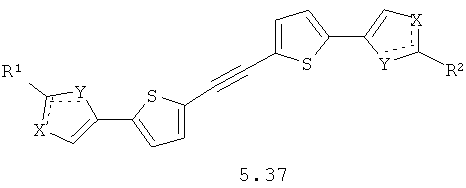
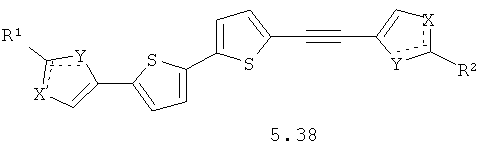
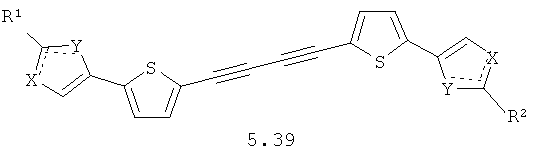
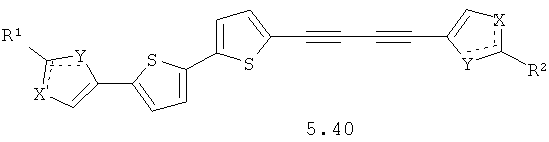
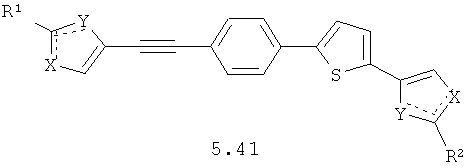
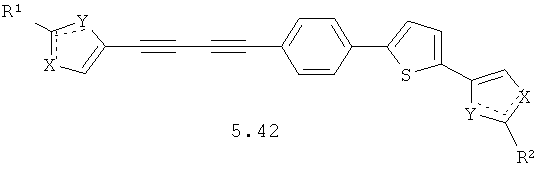
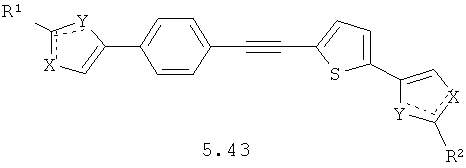
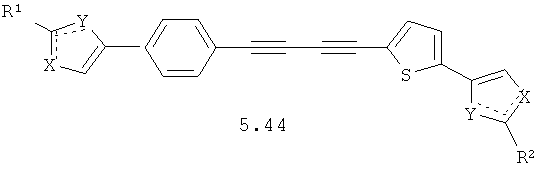
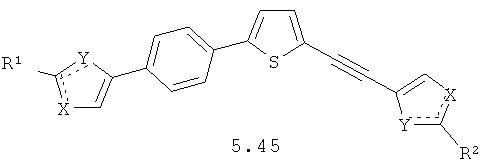
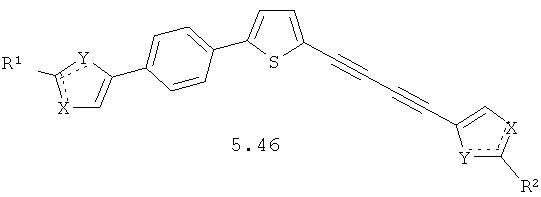
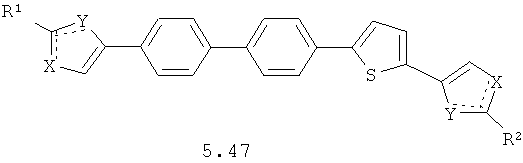
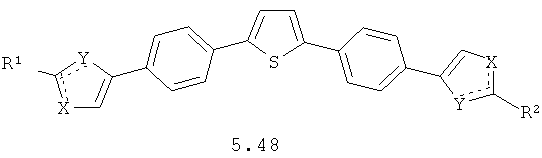

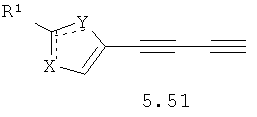
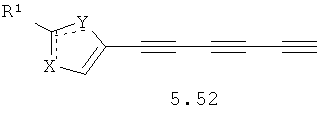
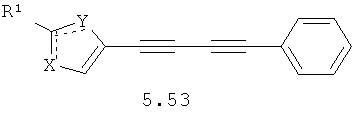
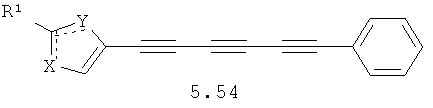
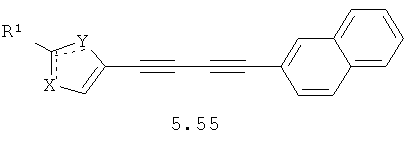
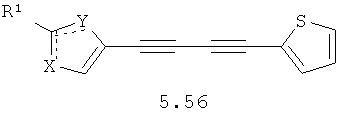
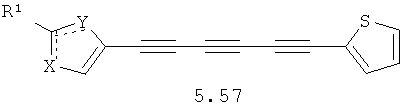

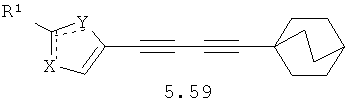
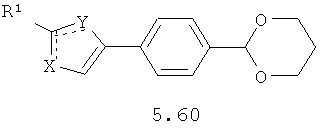
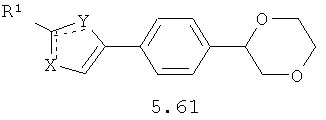
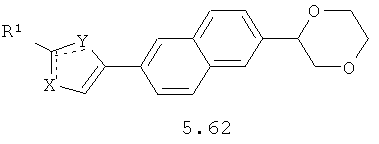
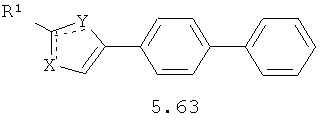
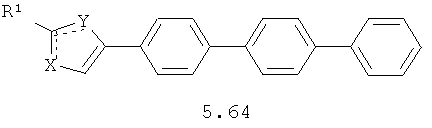
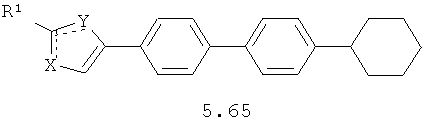
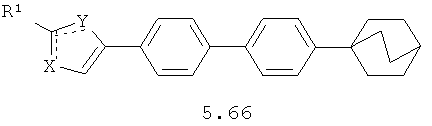
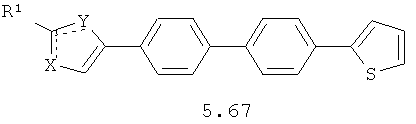
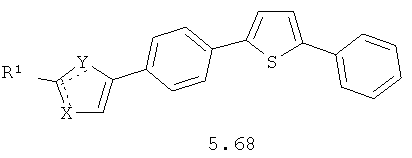
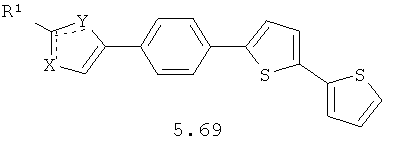
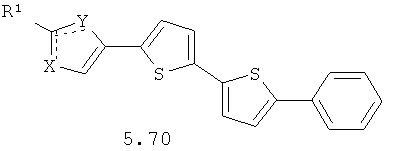
3. Соединения по п.1, представляющие собой замещенные азолы общей формулы 6.1-6.70, в которых А, X, Y и сплошные линии с сопровождающими их пунктирными линиями 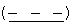 имеют вышеуказанное значение
имеют вышеуказанное значение
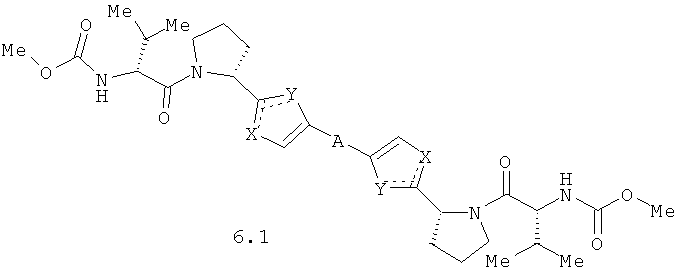
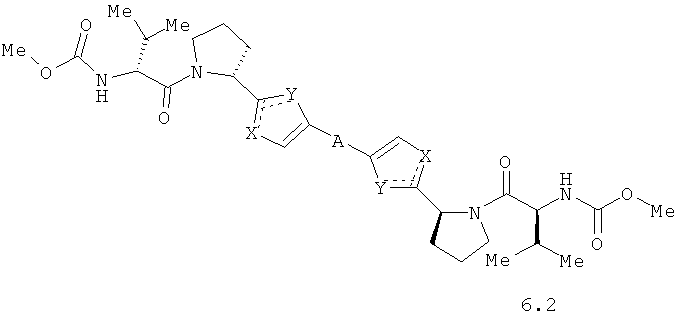
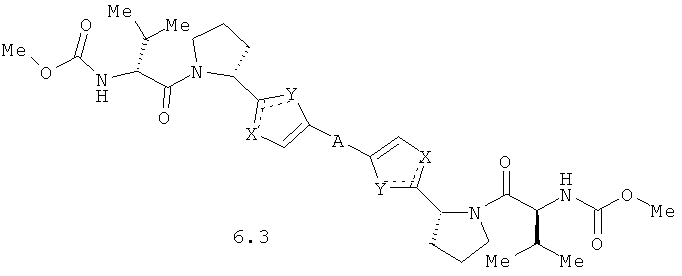
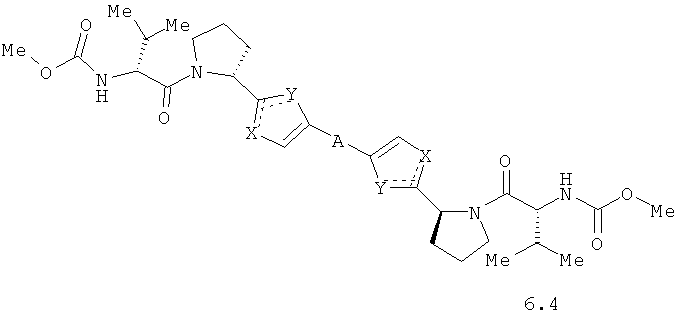
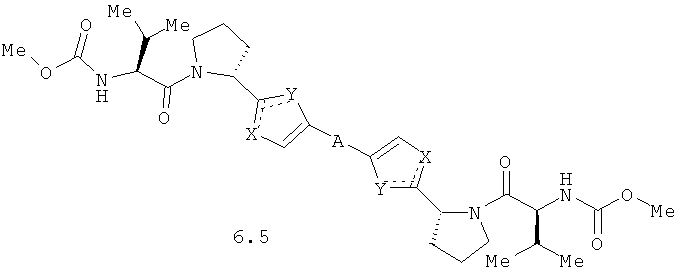
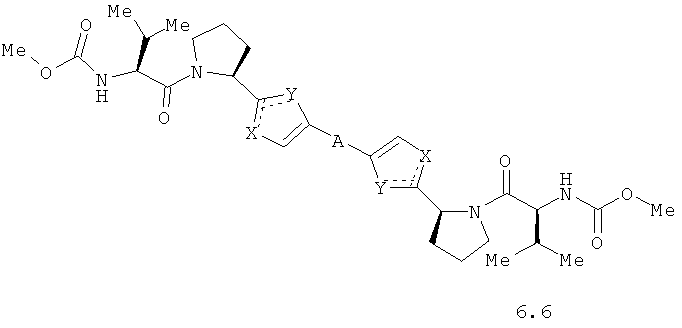
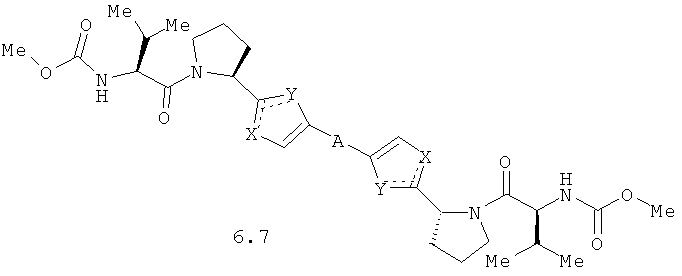
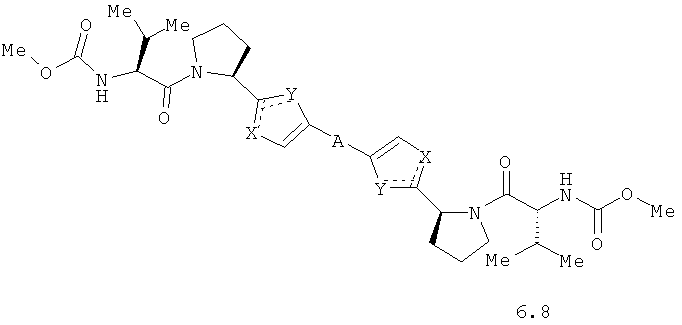
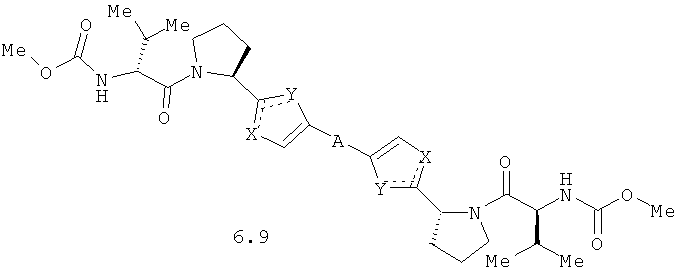
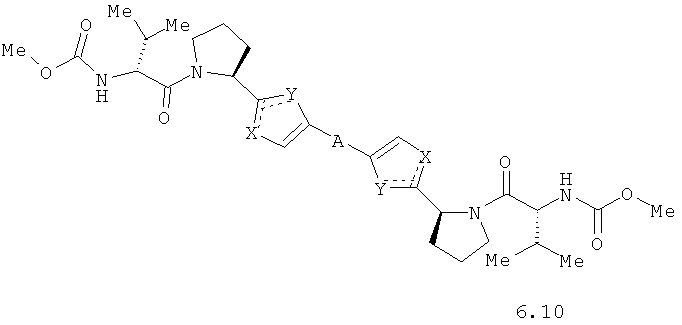
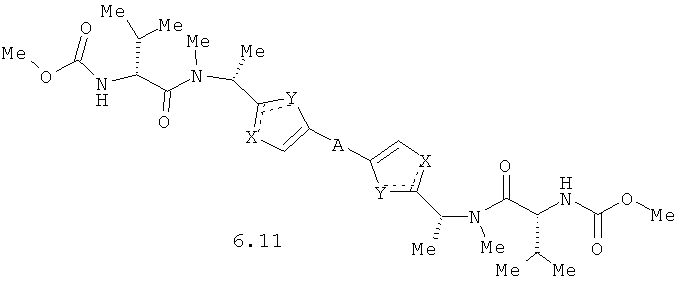
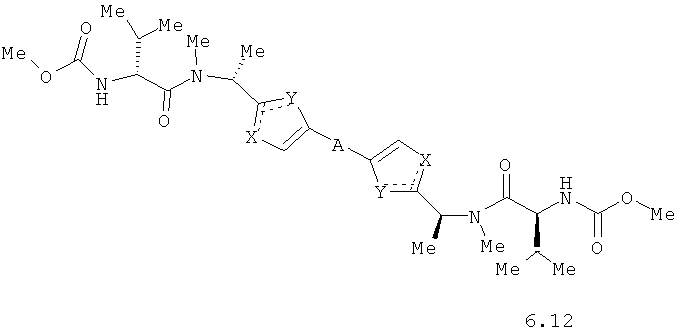

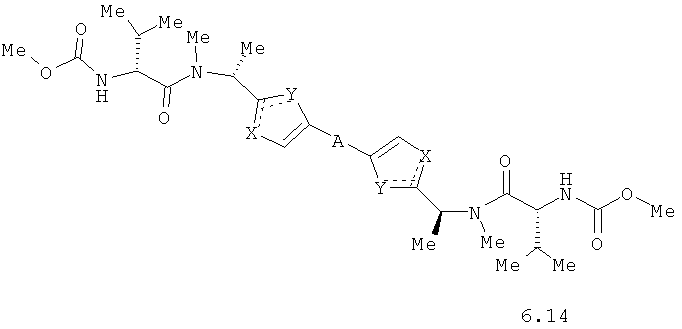
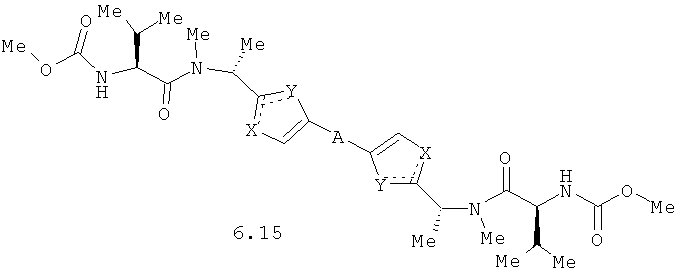

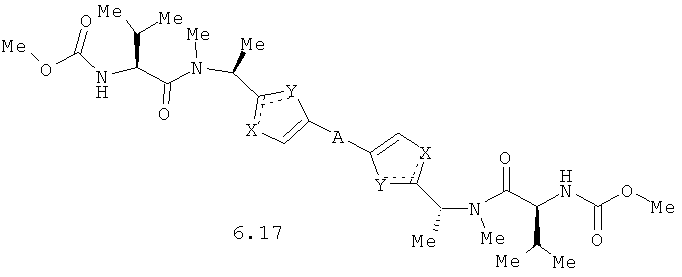
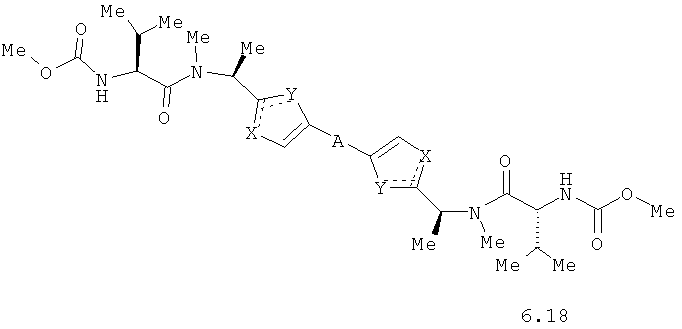
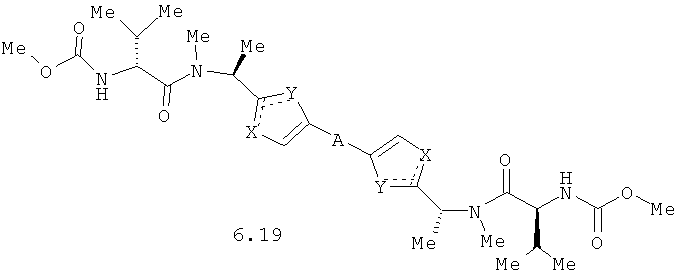
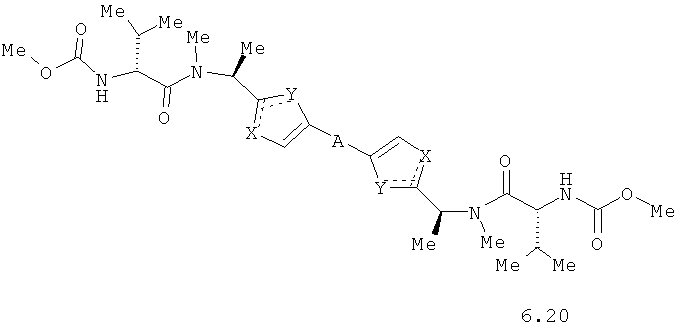
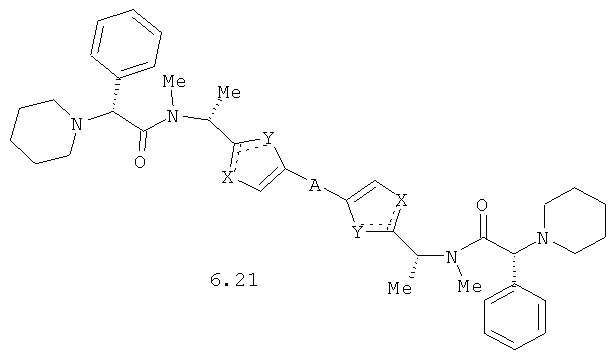

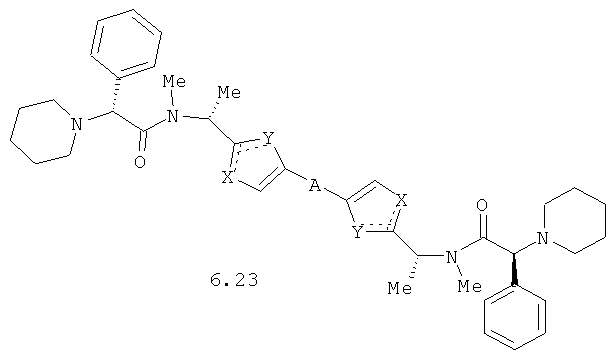
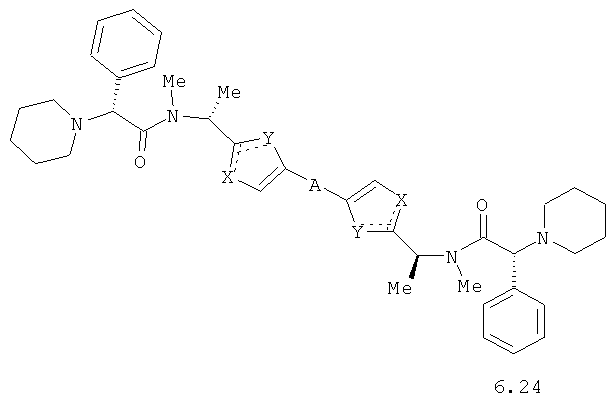
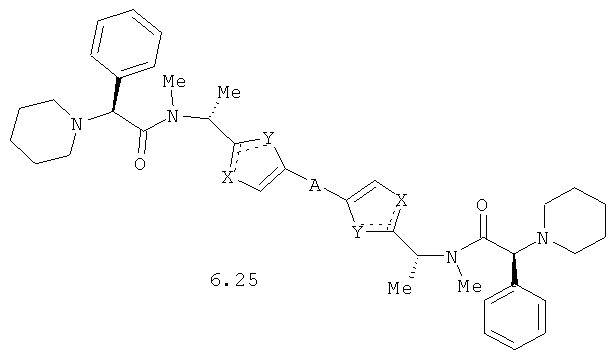
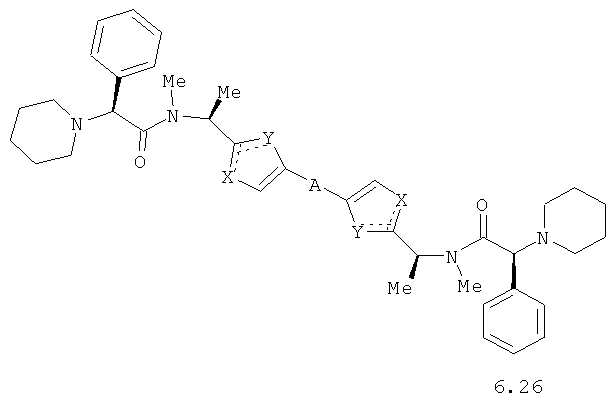
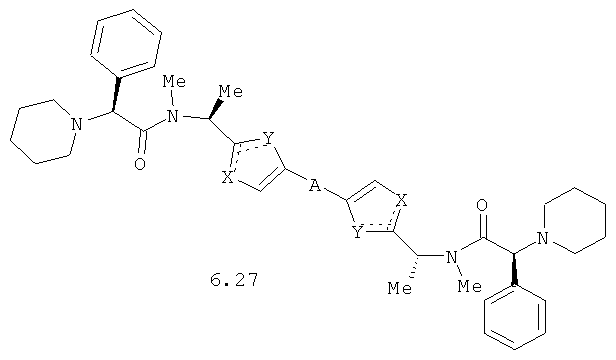
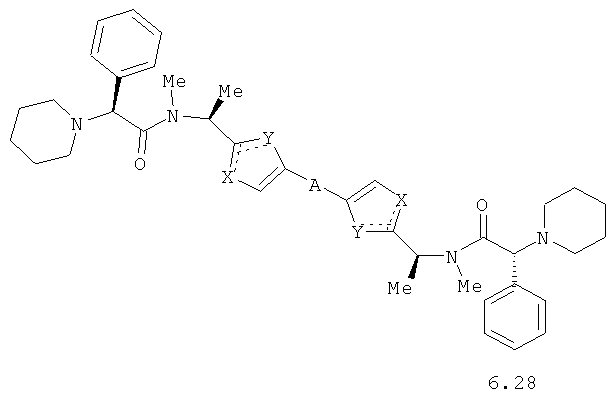
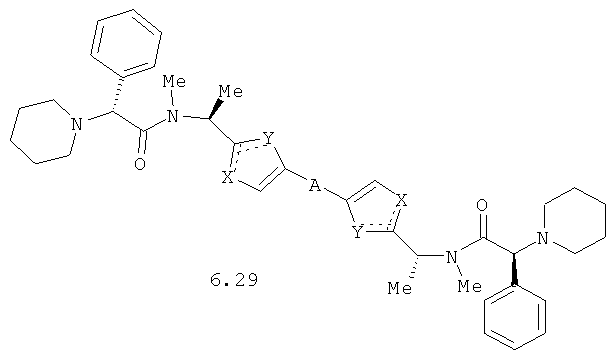
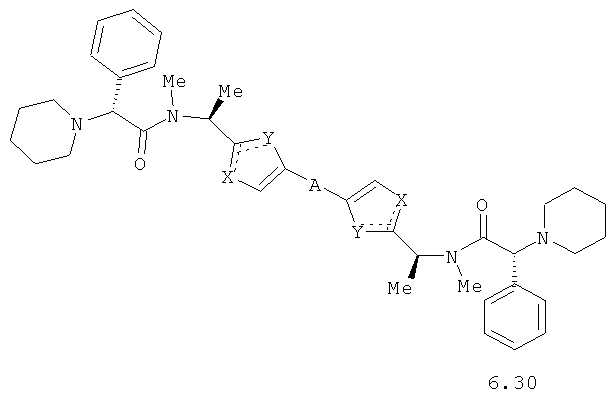
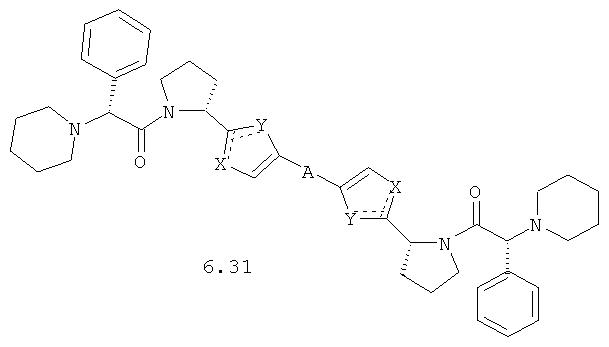
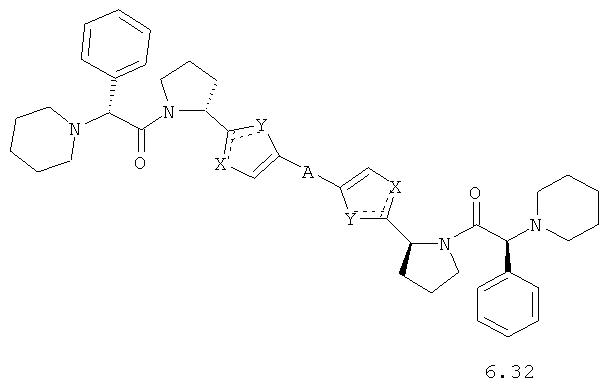
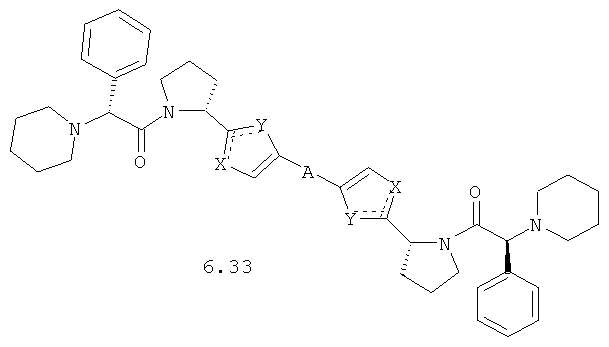
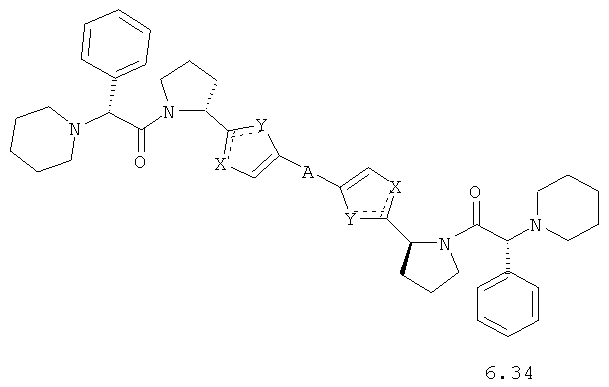
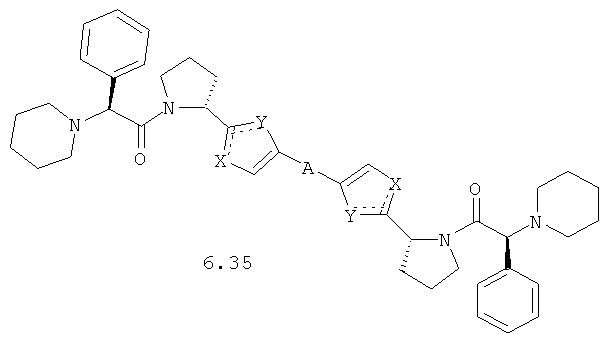

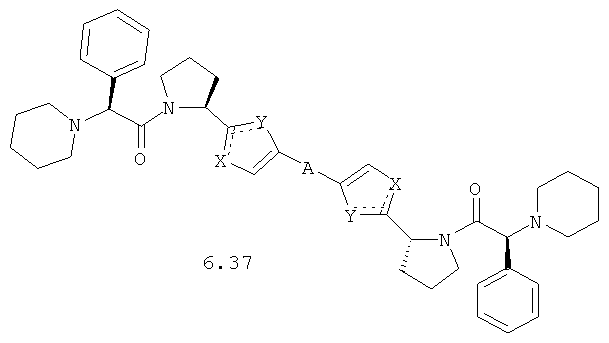
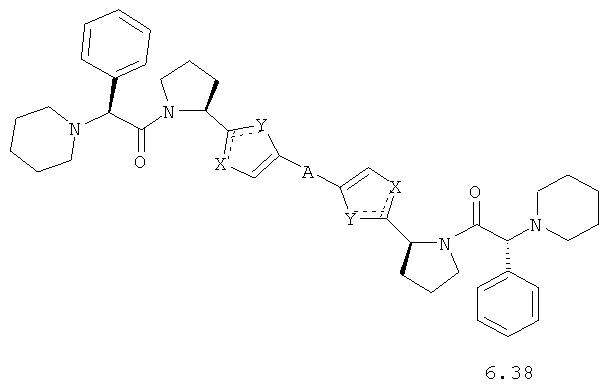
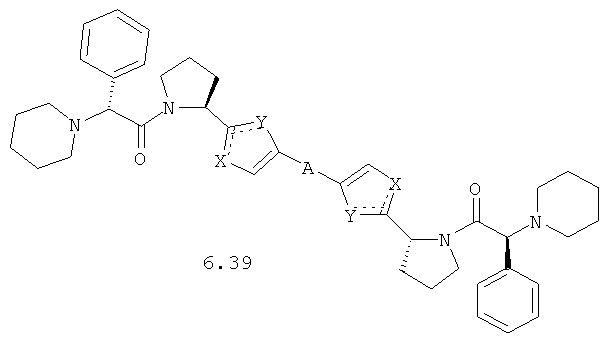
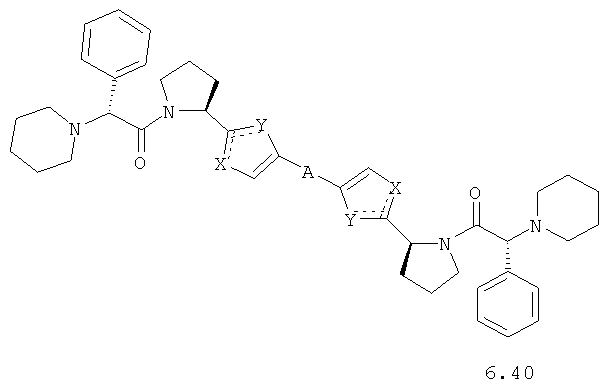
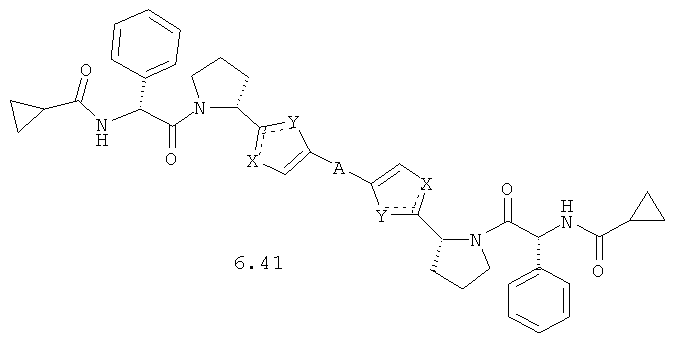
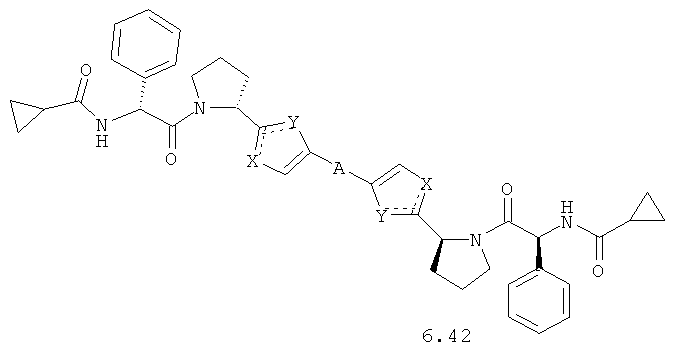
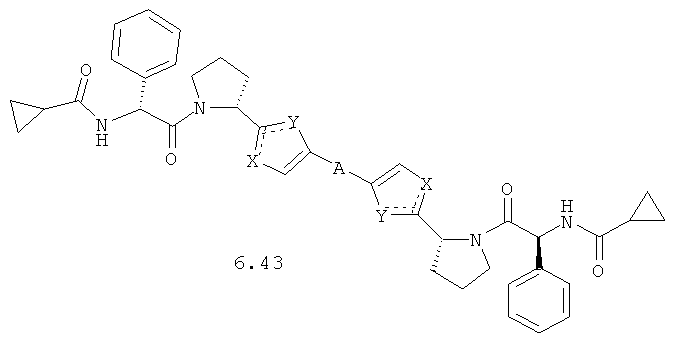
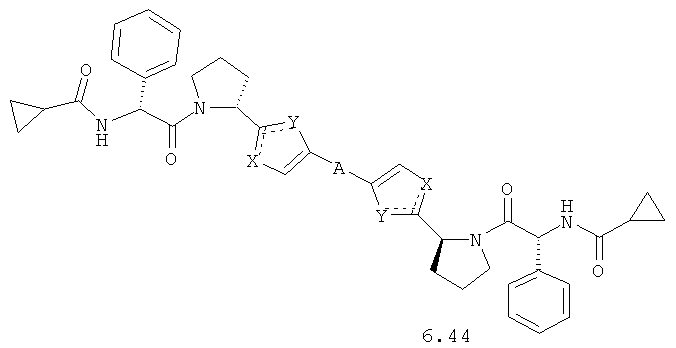
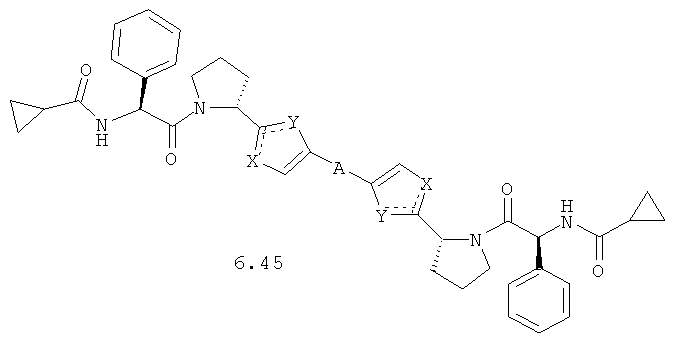
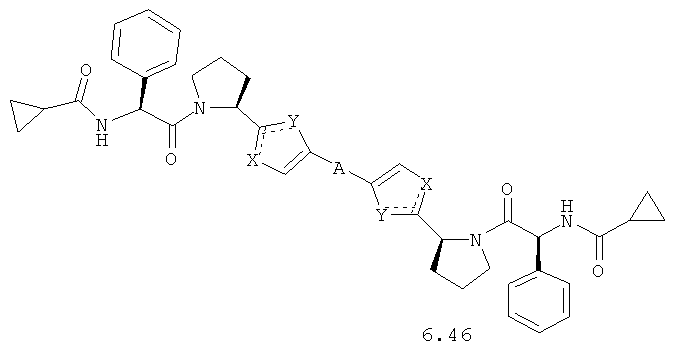
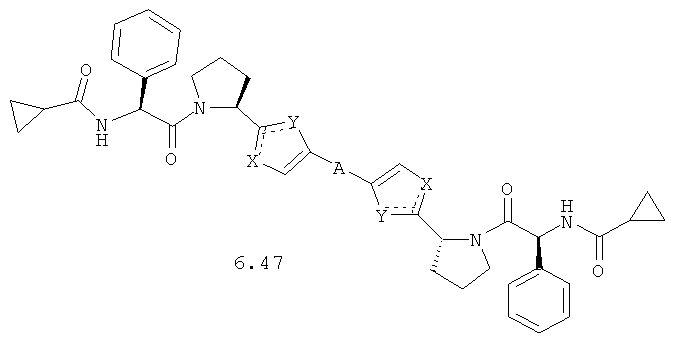
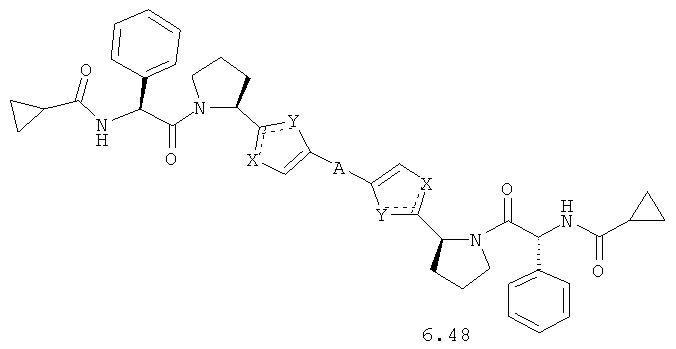
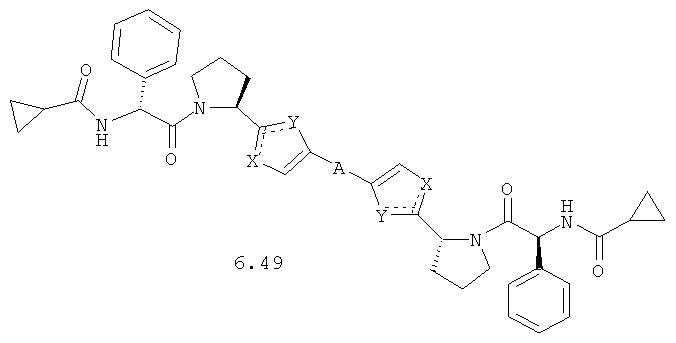
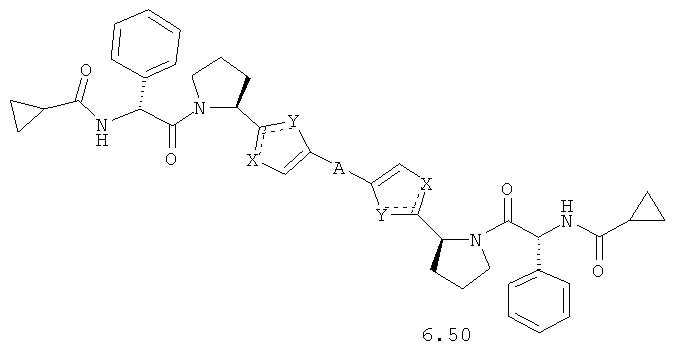
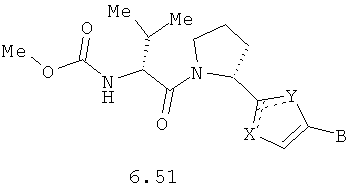
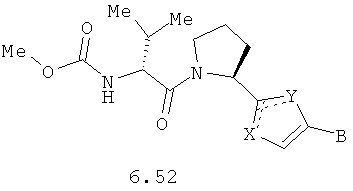
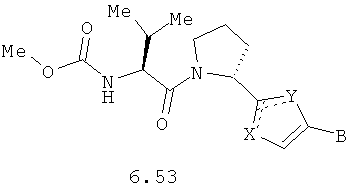
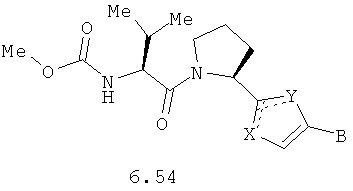
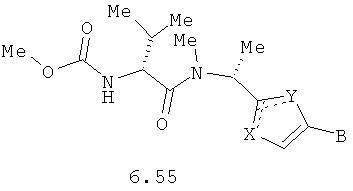
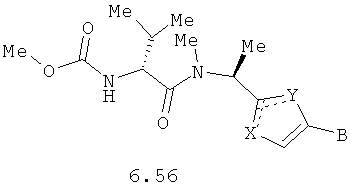
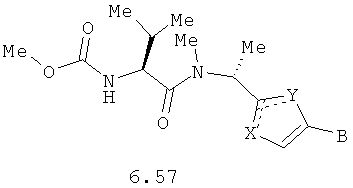
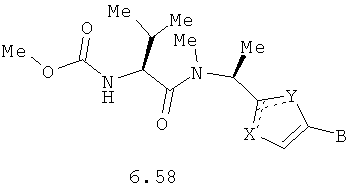
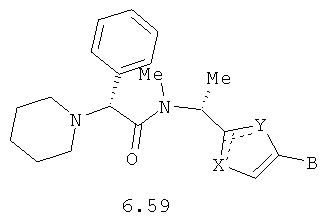
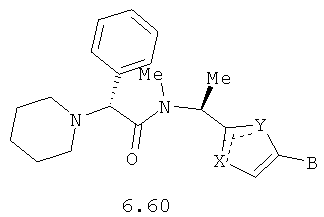
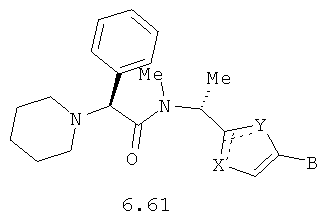
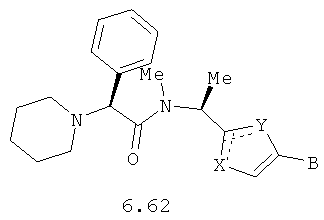
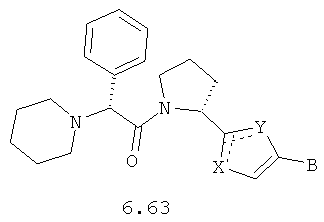
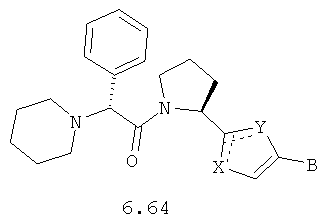
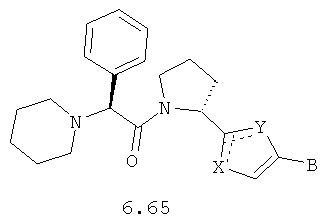
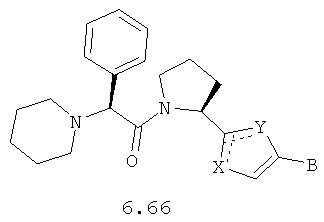
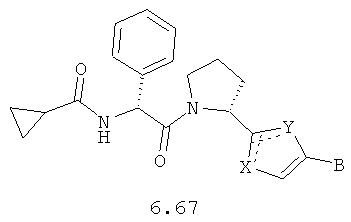
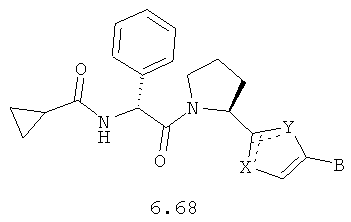
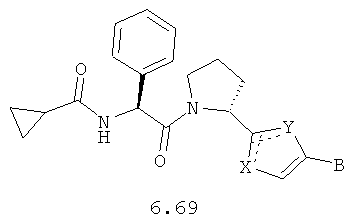
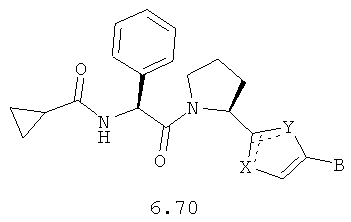
4. Соединения по пп.1-3, представляющие собой замещенные азолы формулы 6, 7, 9-12, 14-17, 19-30, 32-49, 51, 54, 56-62
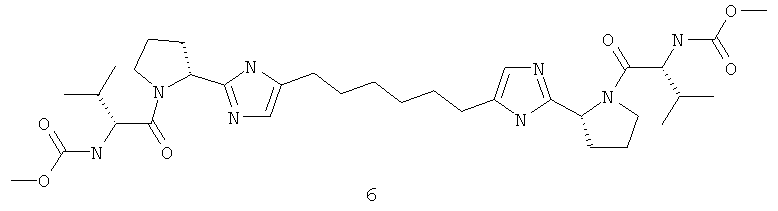
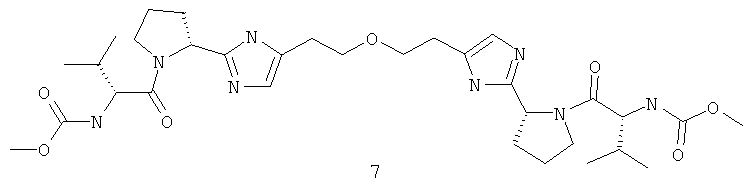
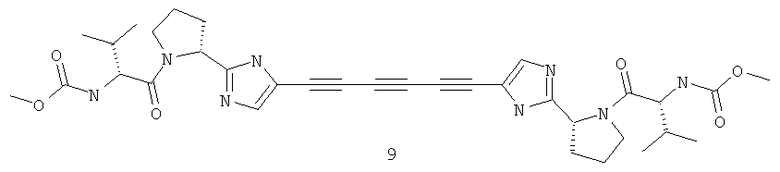

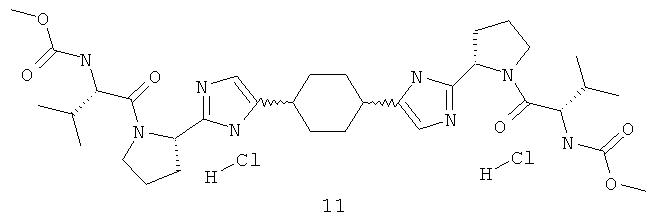
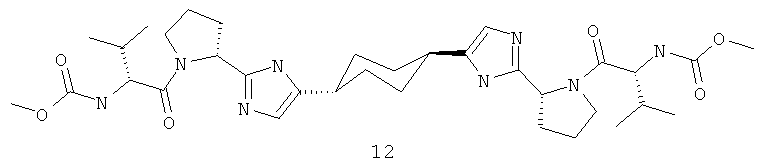
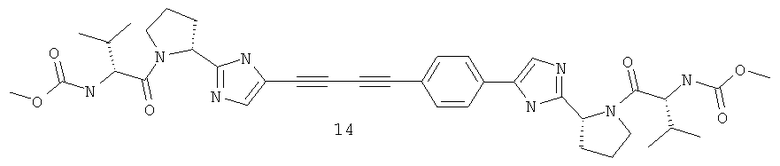
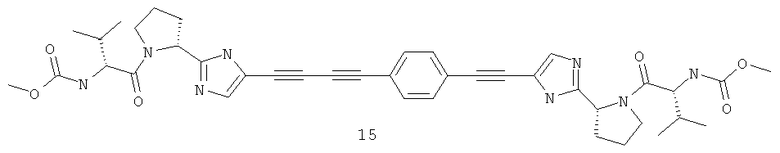
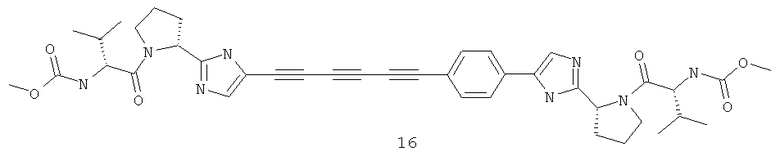
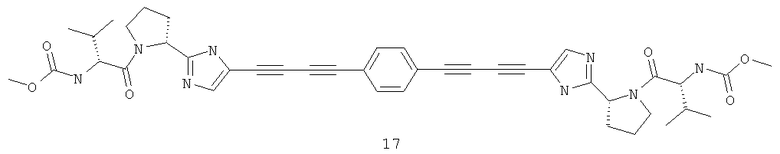
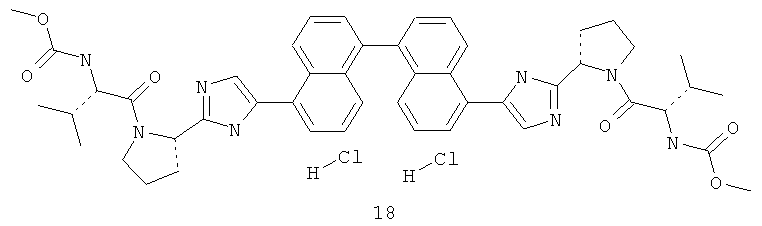
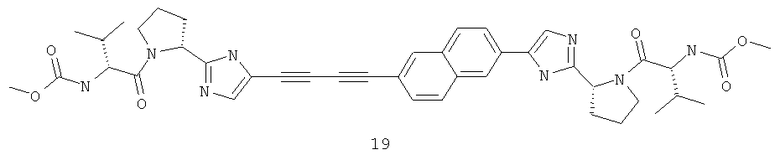
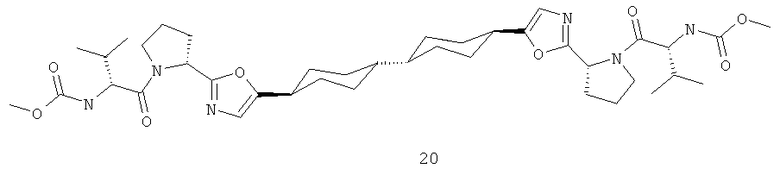
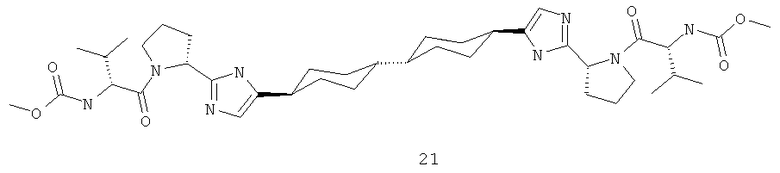
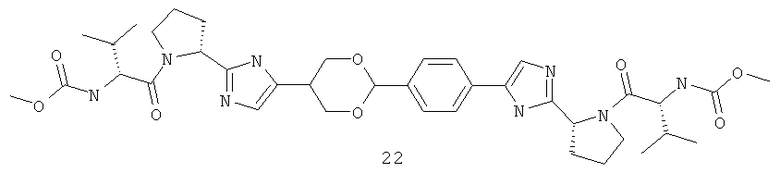
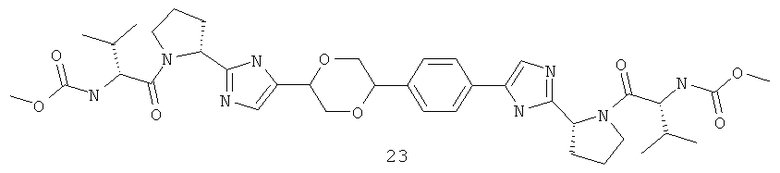

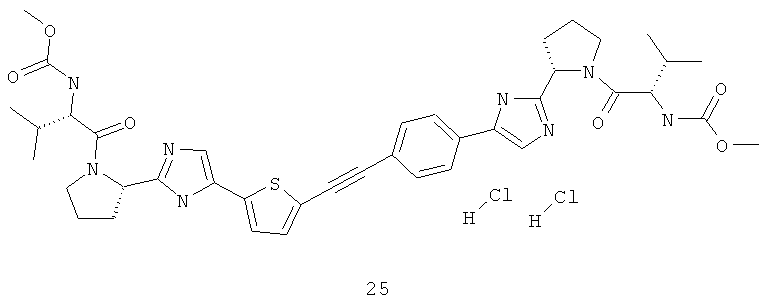
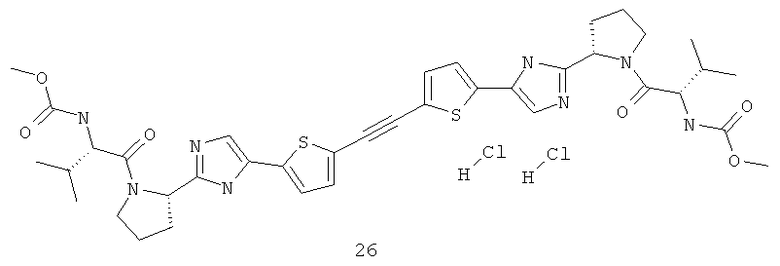
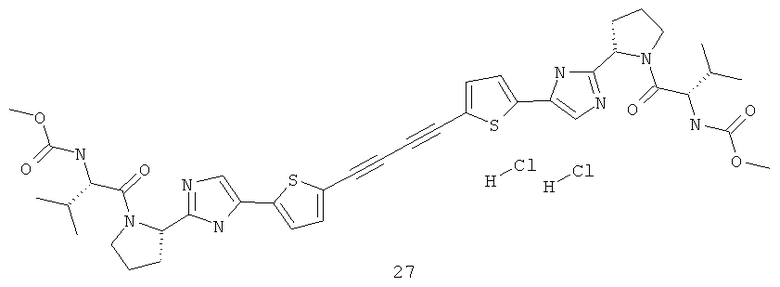
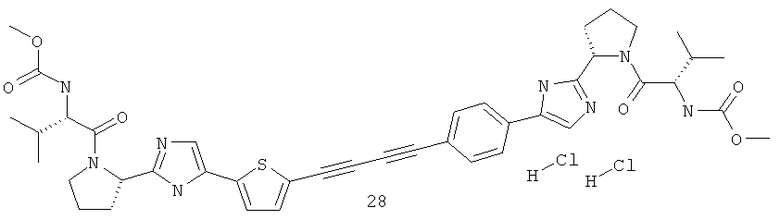

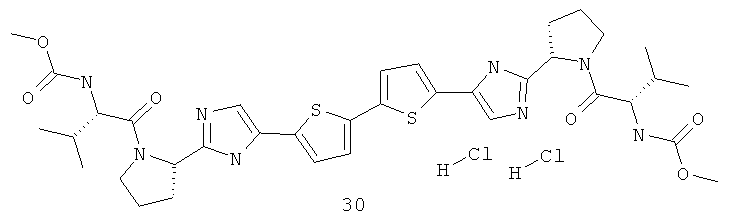
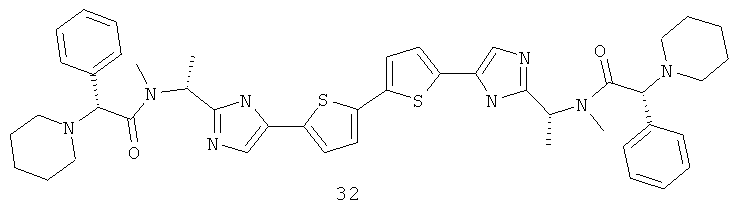
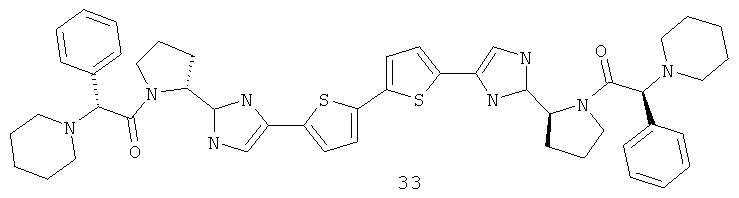
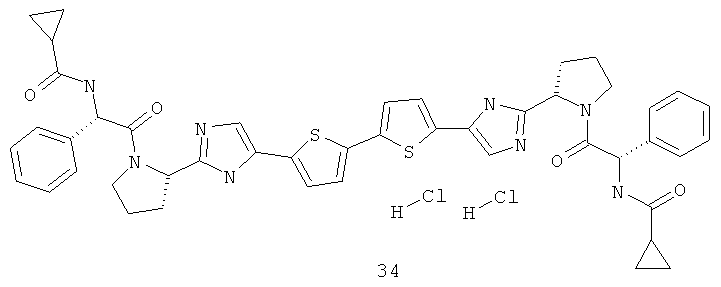
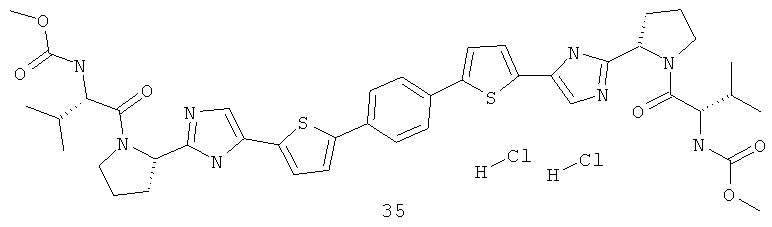
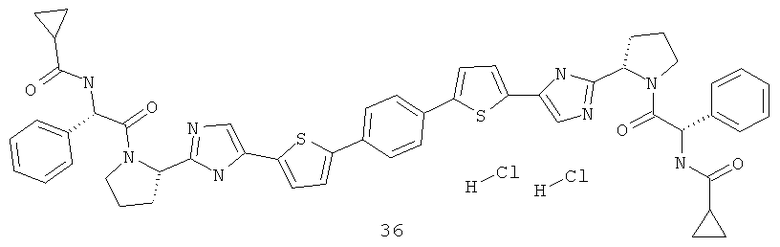
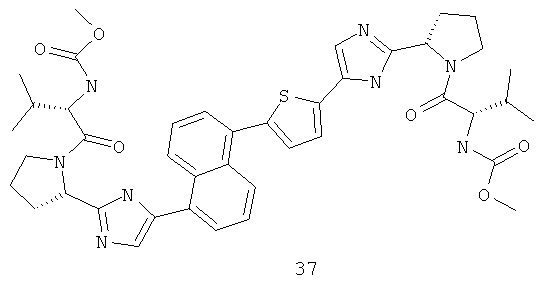
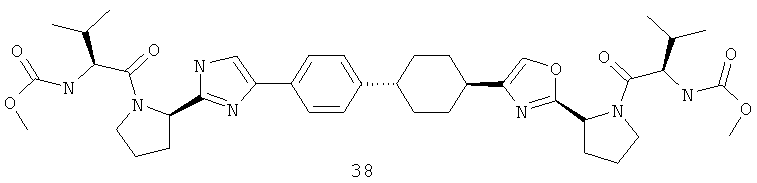
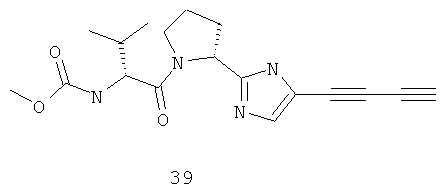
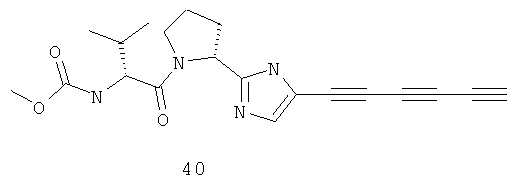
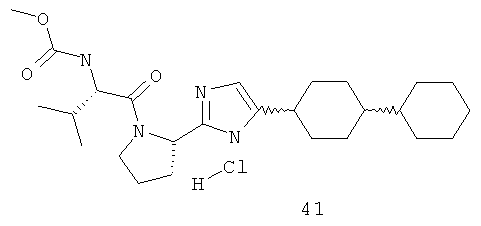
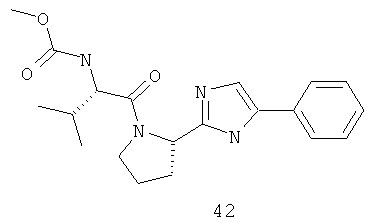
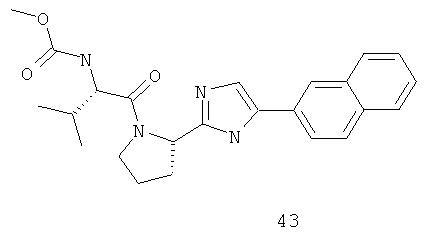

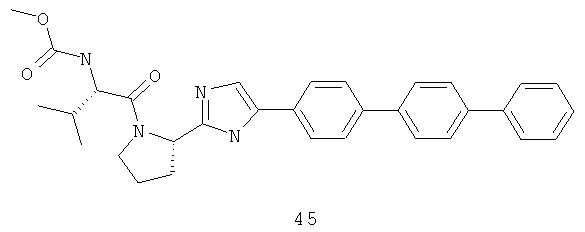


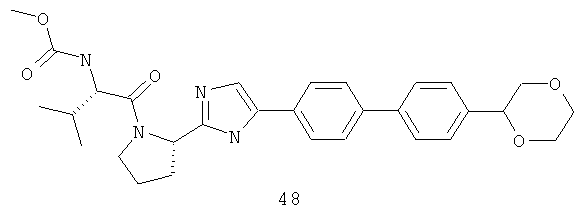
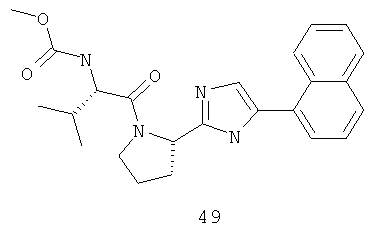
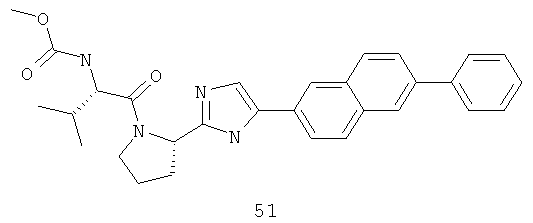
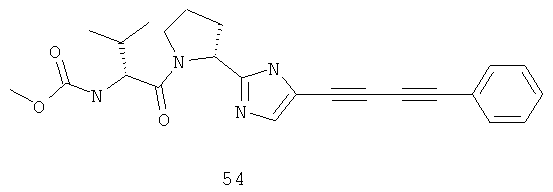
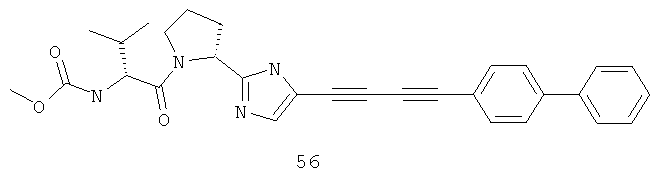
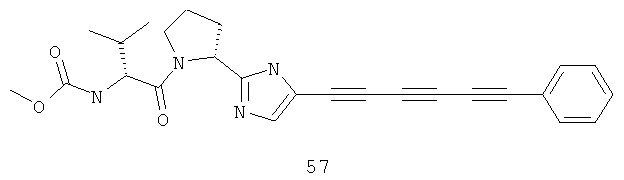
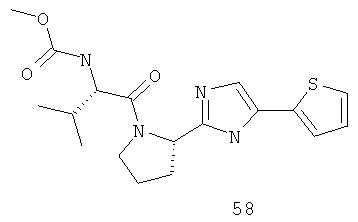
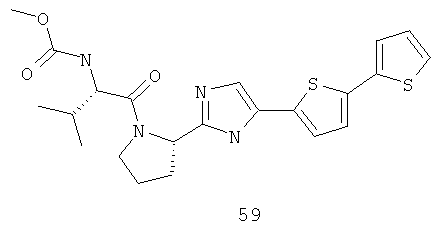
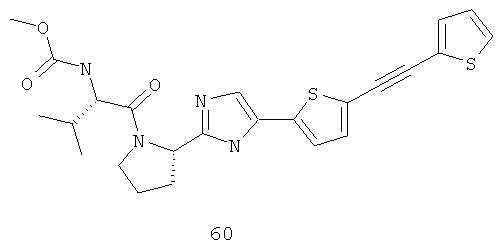

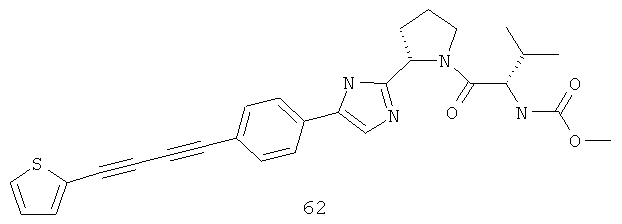
5. Лиганды, спектр биологической активности которых включает вирусный белок NS5A, представляющие собой замещенные азолы общей формулы 1А и 1В по любому из пп.1-4, и их фармацевтически приемлемые соли.
6. Активный компонент для фармацевтических композиций и лекарственных средств, предназначенных для лечения и предупреждения заболеваний, обусловленных вирусом гепатита С и гепатита GBV-C, представляющий собой замещенные азолы общей формулы 1А и 1В по любому из пп.1-4 и их фармацевтически приемлемые соли.
7. Фармацевтическая композиция для лечения и предупреждения заболеваний, обусловленных вирусом гепатита С и вирусом гепатита GBV-C, содержащая активный компонент по п.6 в фармацевтически эффективном количестве.
8. Фармацевтическая композиция по п.7 в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку.
9. Способ получения фармацевтической композиции смешиванием, по крайней мере, одного активного компонента общей формулы 1А и 1В или его фармацевтически приемлемой соли с инертным наполнителем и/или растворителем.
10. Способ лечения болезней, обусловленных вирусом гепатита С и вирусом гепатита GBV-C, путем введения фармакологически эффективного количества активного компонента по п.6 или фармацевтической композиции по п.7 или 8.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ЕА 201000196 А1, 30.06.2010 | |||
| ЕА 200900298, 30.10.2009 | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2012-06-10—Публикация
2010-11-30—Подача