Изобретение относится к получению нового штамма вируса гриппа А субтипа H1N1 для изучения эффективности лечебных и профилактических препаратов против пандемического гриппа А(H1N1/2009) и может быть использовано в медицинской вирусологии и микробиологии.
С помощью реассортации, биохимических и молекулярно-биологических методов получены известные штаммы-аналоги вируса гриппа субтипа H1N1 (А/17/Новая Каледония/99/145; А/17/Пекин/95/25; А/47/Пекин/95/35; А/47/Иоганнесбург/96/7/7; А/17/Перт/95/29; А/17/Техас/91/1/3; А/Техас/36/91) и генетические конструкции, которые используются для создания вакцинных препаратов с целью профилактики гриппа (в том числе гриппа свиней) среди людей различных возрастных групп [Патент РФ 2144955, МПК C12N 7/00, опубл. 27.01.00; Патент РФ 215981, МПК C12N 7/00, опубл. 25.05.99; Патент РФ 2183672, МПК C12N 7/00, опубл. 20.06.02; Патент РФ 2159810, МПК C12N 7/00, опубл. 27.11.00; Патент РФ 2151185, МПК C12N 7/00, опубл. 20.06.00; Патент РФ 2084524, МПК C12N 7/00, 20.07.97; Патент РФ 2077581, МПК C12N 7/00, опубл. 20.04.07; Заявка на патент США 2008031115, 18.12.08; Заявка на патент США 20080299151, 04.12.08; Заявка на патент США 20030099670, 29.05.03; Патент США 6485729, 26.11.02; Патент США 5162112, 10.11.92]. Однако все эти штаммы предназначены и использовались для производства профилактических препаратов, а не для оценки эффективности действия существующих и разрабатываемых лечебно-профилактических препаратов против гриппа.
Известен штамм A/duck/Novosibirsk/56/05 субтип H5N1 вируса гриппа птиц (аналог), выделенный на территории Западной Сибири, который используется для моделирования вирусной инфекции в научных экспериментах при изучении эффективности противовирусных препаратов на культурах клеток [Патент РФ 2309983, МПК C12N 7/00, опубл. 27.05.07].
Однако указанный штамм обладает следующими недостатками:
- предназначен для производства профилактических и диагностических препаратов и исходя из представленных данных о патогенности для культур клеток и отсутствия данных о вирулентности для животных, в т.ч. мышей, может быть использован для оценки противовирусной активности различных соединений только на культуре клеток;
- не может быть использован (учитывая его принадлежность к субтипу H5N1 вируса гриппа) для оценки эффективности разрабатываемых и существующих лечебно-профилактических препаратов против пандемического гриппа A(H1N1/2009).
В качестве еще одного аналога выступает штамм А/Бак/Россия/05 (субтип H5N1) вируса гриппа птиц [Патент РФ 2300564, МПК C12N 7/00, опубл. 10.06.07]. Однако указанный штамм может быть использован только для получения антигена и создания вакцинных и диагностических препаратов. Данных о вирулентных свойствах данного штамма для лабораторных животных, в т.ч. мышей, нет. Кроме того, учитывая его принадлежность к субтипу H5N1, штамм не может быть использован для оценки эффективности разрабатываемых и существующих лечебно-профилактических препаратов против пандемического гриппа A(H1N1/2009).
Также известен аналог - штамм вируса гриппа A/Swine/1976/31(H1N1), адаптированный к мышам, выделенный от свиней [Грипп A/H1N1 как типичная эмерджентная инфекция (вирусологические, клинико-эпидемиологические особенности, вопросы терапии и профилактика): Пособие для врачей / Под ред. Киселева О.И., Ершова Ф.И., Малого В.П., Сологуб Т.В., Романцова М.Г. - С.Пб. - Харьк. - Ужгород. - 2009. - С.30-32].
Однако указанный штамм генетически и по антигенным свойствам значительно отличается от штаммов вируса гриппа А(H1N1/2009).
Кроме того, известен штамм A/California/04/2009 субтип H1N1 вируса гриппа (аналог), выделенный в США от ребенка с легким течением заболевания, который используется для моделирования вирусной инфекции в научных экспериментах при изучении эффективности противовирусных препаратов в культуре клеток и на животных [Itoh Y., Shinya К., Kiso M. et al. In vitro and in vivo characterization of new swine-origin H1N1 influenza viruses. // Nature. 2009, 460:1021-5].
Однако указанный штамм A/California/04/2009 (H1N1) выделен не на территории России от больного с легким течением заболевания в самом начале пандемии, когда еще не было летальных случаев, вследствие чего не может вызывать весь спектр симптомов заболевания, в том числе приводящих к летальному исходу. Перечисленные характеристики штамма A/California/04/2009 (H1N1) не позволяют наиболее полно оценивать эффективность противовирусных препаратов особенно в отношении штаммов, способных вызвать летальный исход.
Наиболее близким штаммом (прототипом) является штамм вируса гриппа птиц A/Chicken/Kurgan/05/2005 субтипа H5N1 [Патент РФ 2361917, МПК C12N 7/00, опубл. 20.02.08].
Однако этот штамм (учитывая его принадлежность к вирусу гриппа птиц субтипа H5N1) не может быть использован для оценки эффективности разрабатываемых и существующих лечебно-профилактических препаратов против пандемического гриппа, вызванного вирусом гриппа А(H1N1/2009).
Поскольку штаммы пандемического вируса гриппа A(H1N1/2009) широко распространены во всем мире и будут продолжать циркулировать наряду с вирусами сезонного гриппа, они оказывают влияние при проведении эпидемиологических и клинических научно-практических исследований. В связи с этим для проверки эффективности противогриппозных препаратов необходимо использовать референс-штаммы пандемического вируса гриппа 2009 г. субтипа H1N1, проявляющие высокую инфекционность в модельных системах in vivo и in vitro.
Техническим результатом предлагаемого изобретения является получение более продуктивного штамма вируса гриппа А субтипа H1N1 для более достоверного моделирования инфекции пандемического гриппа А(H1N1/2009) на культуре клеток и беспородных мышах на территории РФ с целью изучения эффективности вакцин и противовирусных препаратов.
Указанный технический результат достигается тем, что получен новый штамм A/Salekhard/01/2009(H1N1)v пандемического вируса гриппа А субтипа H1N1, выделенного на территории РФ от умершего человека, для использования в экспериментах по изучению специфической активности противовирусных (противогриппозных) препаратов и эффективности вакцин в экспериментах in vivo на беспородных лабораторных мышах. В гене, кодирующем гемагглютинин штамма A/Salekhard/01/2009(H1N1)v, присутствует генетическая мутация G155E, которая по данным литературы приводит к повышению репродуктивных свойств вируса при культивировании в куриных эмбрионах и сохраняется при дальнейшем пассировании [Chen Z., Wang W., Zhou H. et al. Generation of live attenuated novel influenza virus A/California/7/09 (H1N1) vaccines with high yield in embryonated chicken eggs // J. Virol., 2010, 84 (I): 44-51]. Ген нейраминидазы штамма A/Salekhard/01/2009(H1N1)v не содержит мутаций E119G и H274Y, которые определяют устойчивость к действию препаратов озельтамивир и занамивира [Zürcher Т., Yates P.J., Daly J. et al. Mutations conferring zanamivir resistance in human influenza virus N2 neuraminidases compromise virus fitness and are not stably maintained in vitro //J. Antimicrobial Chemotherapy, 2006, 58(4):723-732], а также мутации Q136K, которая не влияет на чувствительность к озельтамивиру, однако приводит к повышению устойчивости мутантных изолятов к занамивиру и в меньшей степени к перамивиру [Hurt A.C., Holien J.K., Parker M. et al. Zanamivir-resistant influenza viruses with a novel neuraminidase mutation // J. Virol., 2009, 83 (20): 10366-73]. Как и все штаммы пандемического вируса гриппа А(H1N1/2009) штамм A/Salekhard/01/2009(H1N1)v устойчив к действию ремантадина. Других известных в литературе мутаций, влияющих на свойства вируса в геноме штамма A/Salekhard/01/2009(H1N1)v, не обнаружено.
Штамм высокопродуктивен: при культивировании в куриных эмбрионах (КЭ) биоконцентрация вируса достигает 8,5±0,6 lg ЭИД50/мл (десятичный логарифм 50% эмбриональных инфицирующих доз), при культивировании в клетках MDCK -7,3±0,4 lg ТЦД50/мл (десятичный логарифм 50% тканевых цитопатических доз), титр в РГА составляет 1:128. Штамм не вызывает заболевания с летальным исходом у мышей при аэрозольном, интраназальном, внутримозговом, внутримышечном заражении. Штамм эффективно размножается в носовой полости, трахее, бронхах и легких мышей и вызывает у мышей заболевание, которое по патоморфологической картине и перечню основных органов-мишеней, где происходит размножение данного патогена, наиболее адекватно моделирует гриппозную инфекцию у человека.
Характеристика заявляемого штамма. Штамм A/Salekhard/01/2009(H1N1)v относится к вирусу гриппа род Influenzavirus А семейство Orthomyxoviridae. Заявляемый штамм выделен от человека, умершего от гриппа в ноябре 2009 года. Штамм депонирован в коллекцию культур микроорганизмов Федерального государственного учреждения науки «Государственный научный центр вирусологии и биотехнологии «Вектор» (ФГУН ГНЦ ВБ «Вектор» Роспотребнадзора) под регистрационным номером №V-538 (дата регистрации - апрель 2011 г.).
Источник получения. Штамм выделен от жителя Салехарда, умершего от гриппа в ноябре 2009 г. Вирус был получен в высоких титрах при заражении гомогенатом легочной ткани (изолированный образец) 9-дневных КЭ после первого пассажа. Штамм агглютинировал эритроциты человека, цыпленка и морской свинки: показатели титров в РГА составляли 1:128-1:256. Инфекционная активность выделенного вируса составляла 7,3±0,4 lg ТЦД50/мл в культуре клеток MDCK и 8,5±0,6 lg ЭИД50/мл в КЭ.
Подлинность штамма. Вирусная РНК была выделена из аллантоисной жидкости РКЭ с помощью набора «РИБО-сорб» (ЦНИИЭ Роспотребнадзора, г. Москва) в соответствии с инструкцией производителя. ПЦР проводили с использованием набора реагентов «АмплиСенс Influenza virus A/H1-swine-FL» (Интерлабсервис, г. Москва). Определение нуклеотидной последовательности выделенных фрагментов проводили на приборе Beckman Coulter CEQ2000XL DNA Analysis System ("Beckman Coulter, Inc.") с использованием наборов "Beckman sequencing Kit". Полученные нуклеотидные последовательности и филогенетический анализ проводился с использованием прикладных программ VECTOR NTI 8.0 («InforMax») и Mega 2.1. Матрицу расстояний вычисляли по алгоритму Р-дистанции. Филогенетическое дерево строили с использованием метода «ближайшего соседа» (neighbor-joining). Достоверность проверялась методом «бутстреп» (bootstrap) с 500 репликациями. Достоверным считали «бутстреп» индекс >75. Для построения филогенетических деревьев использовали нуклеотидные последовательности генов вируса гриппа, депонированных в международной базе данных GenBank.
Все полученные первичные последовательности были депонированы в базу GenBank. Номера депонирования генов штамма вируса гриппа A/Salekhard/01/2009(H1N1)v представлены в таблице 1.
Филогенетический анализ нуклеотидной последовательности генов показал принадлежность штамма вируса гриппа A/Salekhard/01/2009(H1N1)v к субтипу H1N1. Штамм генетически близок к референс-штамму A/California/07/2009(H1N1) пандемического H1N1 (2009) вируса гриппа.
Культуральные свойства. Штамм A/Salekhard/01/2009(H1N1)v при культивировании при 36,0°С в аллантоисной жидкости КЭ достигает высоких концентраций 8,5±0,6 lg ЭИД50/мл через 2 суток после инфицирования в аллантоисную полость. Штамм A/Salekhard/01/2009(H1N1)v при культивировании в монослое клеток MDCK вызывает цитопатическое действие (ЦПД) через 2-4 суток после заражения (температура культивирования 37°С в атмосфере 5% СО2). Максимальную концентрацию вируса регистрировали через 4-6 суток после заражения монослоя клеток MDCK, и ее величина составляла 7,3±0,4 lg ТЦД50/мл.
Патогенность для человека. Штаммы пандемического вируса гриппа A(H1N1/2009) являются вирулентными для человека: летальность для людей составляет около 0,5% (от 0,02% до 4,6%).
Патогенность для свиней. Штаммы пандемического вируса гриппа A(H1N1/2009) являются высоковирулентными для свиней, вызывая, кроме респираторной симптоматики, нарушения функции воспроизводства у 10 - 30% заболевших животных.
Для длительного хранения. Штамм лиофилизируют с использованием в качестве защитной среды раствора желатина и сахарозы (САЖ). Лиофилизация с добавлением САЖ в соотношении 1:4 позволяет сохранить стабильную инфекционную активность вируса в течение 2 и более лет при температуре хранения минус 70°С.
Среды культивирования. Для размножения штамма используют следующие питательные среды: Игла МЭМ, Игла МЭМ×2АВК, среда 199, ДМЭМ, StemAlpha-MDCK, MegaVir-MDCK, содержащие 2 мкг/мл трипсина, 2 ммоль/л глютамина, 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина.
Пример 1. Изучение репродуктивных свойств штамма A/Salekhard/01/2009(H1N1)v
Выделенные на территории России штаммы пандемического вируса гриппа A(H1N1/2009) культивировали в куриных эмбрионах (КЭ) и в клетках MDCK.
Результаты изучения эффективности репродуцирования в указанных системах после пассирования в КЭ приведены в таблице 2.
Из данных таблицы 2 видно, что штамм A/Salekhard/01/2009(H1N1)v был получен в высоких титрах после 1-го пассажа на КЭ, тогда как для выделения других штаммов потребовалось не менее 2 пассажей в КЭ. При этом штамм A/Salekhard/01/2009(H1N1)v обладает высокими репродуктивными свойствами не только в КЭ, но и в культуре клеток MDCK, что является основанием для его использования при исследовании противовирусной эффективности лекарственных препаратов и иммуногенности вакцин.
Все исследуемые штаммы репродуцировались в культуре клеток MDCK и в КЭ. В то же время для проведения дальнейших исследований нами был выбран штамм вируса гриппа A/Salekhard/01/2009(H1N1)v. Это обусловлено тем, что данный штамм обладал более высокой репродуктивной активностью по сравнению с другими испытанными штаммами (поскольку в его геноме присутствует мутация G155E), которая способствует появлению более высоких репродуктивных свойств вируса при культивировании в куриных эмбрионах (КЭ) и сохраняется при дальнейшем пассировании.
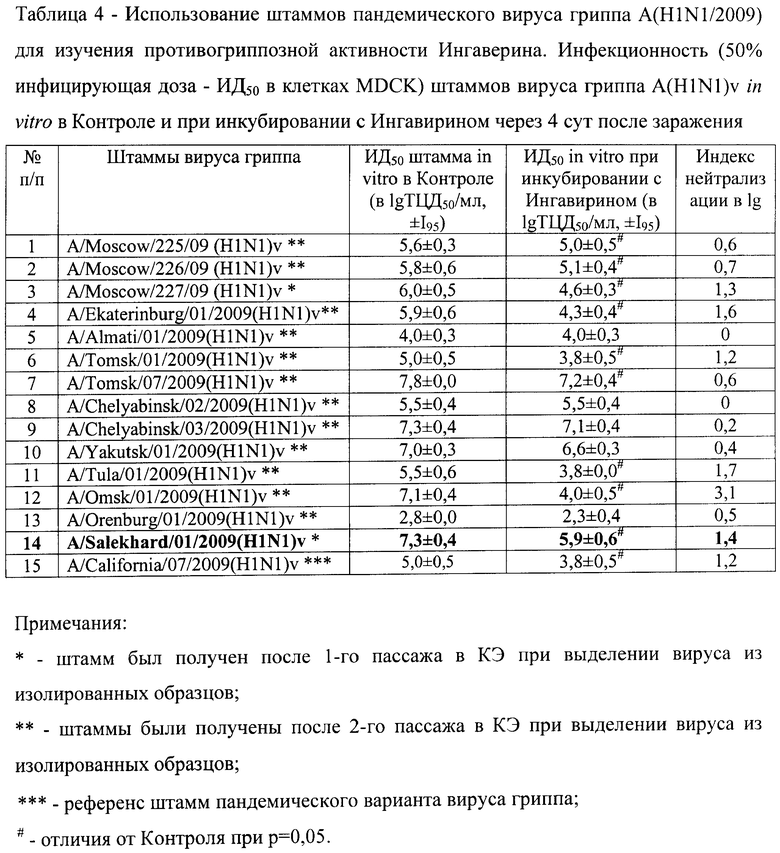
Пример 2. Использование штаммов пандемического вируса гриппа А(H1N1/2009) для проверки противовирусной активности препаратов in vitro
Далее было проведено исследование чувствительности полученных штаммов пандемического вируса гриппа А(H1N1/2009) к противогриппозным препаратам Тамифлю (табл.3), Ингавирин (табл.4), Реаферон (табл.5) и Ремантадин (табл.6) in vitro.
Как видно из таблиц 3, 4 и 5, штамм A/Salekhard/01/2009(H1N1)v, полученный после 1-го пассажа в КЭ, обладает чувствительностью к Тамифлю, Ингавирину и Реаферону, сопоставимой с чувствительностью референс-штамма A/California/07/2009(H1N1)v, полученного из CDC (США). Об этом свидетельствует достоверное уменьшение его инфекционности (ИД50 in vitro) при инкубировании с данными противовирусными препаратами в культуре клеток MDCK. При этом другие штаммы пандемического вируса гриппа А(H1N1/2009), которые нам удалось получить в относительно высоких титрах только после 2-го пассажа в КЭ, проявляли или пониженную, или повышенную чувствительность к исследованным препаратам. В связи с этим неясно, было ли это обстоятельство связано с пассированием вируса в КЭ или исходный изолят действительно был нечувствительным к данным противогриппозным препаратам. Показано также, что штамм A/Salekhard/01/2009(H1N1)v, также как и другие изученные штаммы вируса гриппа A(H1N1/2009), нечувствителен к Ремантадину (табл.6).
Полученные результаты показывают, что штамм A/Salekhard/01/2009(H1N1)v имеет ряд преимуществ при оценке эффективности противогриппозных препаратов. Это обусловлено тем, что он был выделен сразу после 1-го пассажа в КЭ и имеет мутацию G155E, способствующую появлению его более высоких репродуктивных свойств не только при культивировании в КЭ, но и в культуре клеток MDCK, и сохраняющуюся при дальнейшем пассировании в чувствительных системах [Chen Z., Wang W., Zhou H. et al. Generation of live attenuated novel influenza virus A/California/7/09 (H1N1) vaccines with high yield in embryonated chicken eggs // J. Virol., 2010, 84(1):44-51].
Пример 3. Изучение инфекционных свойств штамма A/Salekhard/01/2009(H1N1)v в экспериментах in vivo на разных линиях мышей
После 1-го или 2-го пассажа в КЭ были сформированы стоки штаммов пандемического вируса гриппа А(H1N1/2009), выделенных на территории России, и изучена их патогенность (инфекционность) для мышей разных линий (ICR, BALB/c, C57/black, CBA) при интраназальном заражении.
Результаты экспериментов приведены в таблице 7. Было отмечено, что более высокой инфекционной активностью по сравнению с референс-штаммом и другими российскими штаммами обладал штамм A/Salekhard/01/2009(H1N1)v. В течение всего срока наблюдения (12 суток) за животными указанных линий, инфицированными разведениями вируса 0, 10-1, 10-2, 10-3, 10-4, 10-5, 10-6, 10-7, 10-8, 10-9 гибели не наблюдалось. Через 4-7 суток после заражения в разведениях 0-10-5 у части животных всех линий регистрировали некоторые клинические признаки заболевания (взъерошенность, сниженная двигательная активность, конъюнктивит).
Каждый из штаммов вируса гриппа проявлял сходную инфекционную активность для всех исследованных линий мышей. В то же время инфекционность штамма вируса гриппа A/Salekhard/01/2009(H1N1)v была выше, чем у референс-штамма и других российских штаммов пандемического вируса гриппа А(H1N1/2009). В связи с этим для проведения дальнейших исследований нами был выбран штамм вируса гриппа A/Salekhard/01/2009(H1N1)v. Это было обусловлено следующими обстоятельствами:
- штамм был выделен из изолированного образца после 1-го пассажа в КЭ;
- наличием мутации, обеспечивающей более высокую продуктивность штамма в КЭ;
- его более высокой продуктивной активностью по сравнению с другими испытанными штаммами в КЭ и клетках MDCK;
- его более высокой инфекционностью: чувствительностью к нему лабораторных мышей (легких);
- более высокой актуальностью для населения нашей страны, поскольку был выделен на территории РФ.
С точки зрения последнего обстоятельства, наиболее адекватную для населения России оценку эффективности существующих и разрабатываемых лечебно-профилактических противовирусных препаратов может дать использование вирусных штаммов, выделенных прежде всего на территории России, по причине генетических различий между штаммами, изолированными в разных регионах мира. Использование российского штамма вируса гриппа A/Salekhard/01/2009(H1N1)v также позволит более корректно установить степень готовности учреждений Минздравсоцразвития к локализации и ликвидации в России вспышек заболеваний среди людей, вызванных пандемическим вирусом гриппа А(H1N1/2009), потенциально способным привести к летальному исходу.
Учитывая эти обстоятельства и отсутствие достоверных различий между всеми линиями мышей по инфекционной активности для данного российского штамма, а также существенно более низкую стоимость беспородных белых мышей (линия ICR), в дальнейшей работе были использованы следующие биоматериалы: штамм вируса гриппа A/Salekhard/01/2009(H1N1)v и беспородные белые мыши ICR.
Пример 4. Использование штамма A/Salekhard/01/2009(H1N1)v и беспородных лабораторных мышей для проверки противовирусной активности препаратов по индексу нейтрализации in vivo
Из литературных данных известно, что использование мышей в качестве модельного животного для проверки противовирусной активности препаратов при гриппозной инфекции широко распространено в научной практике [Droebner К., Ehrhardt С., Poetter A., Ludwig S. and Planz O. CYSTUS052, a polyphenol-rich plant extract, exerts anti-influenza virus activity in mice // Antiviral Research. 2007, 76 (I. LP): 1-10]. При этом исследователи использовали штаммы вируса гриппа, не имеющие отношение к субтипу H1N1. В этой связи, основываясь на ранее приведенных примерах (1 и 2), нами была подобрана адекватная биосистема [российский штамм вируса гриппа A/Salekhard/01/2009(H1N1)v и беспородные белые мыши], позволяющая моделировать течение инфекционного заболевания у человека, вызванного пандемическим вирусом гриппа A(H1N1/2009). Используя данную модельную систему, были проведены исследования по оценке противовирусной активности лекарственных препаратов, разрешенных к применению на территории России.
Для определения 50%-ной инфицирующей дозы (ИД50) штамма вируса гриппа A/Salekhard/01/2009(H1N1)v беспородных белых мышей массой 15-17 г инфицировали интраназально 5 разведениями ВАЖ: 10-3, 10-4, 10-5, 10-6 и 10-7 в объеме 40 мкл. Через 4 сут животных забивали, получали гомогенаты легких и определяли в них наличие или отсутствие вируса посредством инфицирования КЭ. При изучении лечебно-профилактического действия препараты Тамифлю, Ингавирин, Ремантадин, Реаферон-Липинт, Арбидол и Виразол вводили мышам перорально по 0,05 мг/г; 0,09 мг/г; 0,1 мг/г; 250 МЕ/г; 0,1 мг/г и 0,05 мг/г соответственно в дистиллированной воде по 0,2 мл ежедневно 1 раз в сутки (в день заражения через 1 час, а потом в течение 4 сут после заражения пандемическим вирусом гриппа). При расчете эквивалентных для мышей доз препаратов были использованы ранее опубликованные сведения [Kleiber M. The Fire of Life // New York - London, John Wiley and Sons. - 1961], где научно обосновано применение повышенных величин таких доз в пересчете на единицу массы мелких лабораторных животных. Контрольной группе мышей по аналогичной схеме вводили дистиллированную воду. Результаты исследований представлены в таблице 8.
 штаммов в lgЭИД50/гол.
штаммов в lgЭИД50/гол.
(М±I95) для белых мышей
Результаты представленных исследований свидетельствуют о наличии достоверного лечебно-профилактического эффекта у препаратов Тамифлю, Ингавирина, Арбидола, Реаферона-Липинта и Виразола при инфекции у мышей, вызванной пандемическим вирусом гриппа А(H1N1/2009). В то же время Ремантадин не проявлял лечебно-профилактического эффекта в экспериментах на животных.
Таким образом, предлагаемый штамм вируса гриппа A/Salekhard/01/2009(H1N1)v может быть успешно использован в экспериментах на беспородных белых мышах для изучения лечебно-профилактической активности препаратов против пандемического гриппа А(H1N1/2009) путем оценки индекса нейтрализации in vivo.
Пример 5. Использование штамма A/Salekhard/01/2009(H1N1)v и беспородных лабораторных мышей для проверки противовирусной активности препаратов по результатам накопления вируса в легких
Основываясь на ранее приведенных примерах (1 и 2), нами была подобрана адекватная биосистема [российский штамм вируса гриппа A/Salekhard/01/2009(H1N1)v и беспородные белые мыши], позволяющая моделировать течение инфекционного заболевания у человека, вызванного пандемическим вирусом гриппа A(H1N1/2009). В связи с успешной регистрацией лечебно-профилактического эффекта по ИН in vivo, используя данную модельную систему, были проведены исследования по оценке противовирусной активности тех же препаратов (Тамифлю, Ингавирин, Ремантадин, Реаферон-Липинт, Арбидол, Виразол) в экспериментах, связанных со сравнительным определением уровня накопления вируса в легких контрольных и опытных групп беспородных белых мышей.
Беспородных белых мышей массой 15-17 г инфицировали интраназально штаммом вируса гриппа A/Salekhard/01/2009(H1N1)v в дозе 10-30 ИД50/мышь. При изучении лечебно-профилактического действия препараты Тамифлю, Ингавирин, Ремантадин, Реаферон-Липинт, Арбидол и Виразол вводили мышам перорально по 0,05 мг/г; 0,09 мг/г; 0,1 мг/г; 250 МЕ/г; 0,1 мг/г и 0,05 мг/г соответственно в дистиллированной воде по 0,2 мл ежедневно 1 раз в сутки (в день заражения через 1 час, а потом в течение 4 дней после заражения вирусом гриппа). При расчете эквивалентных для мышей доз препаратов были использованы ранее опубликованные сведения [Schmid R.F. and Thews G. Физиология человека. // М.: Мир, 1986, С.19], где научно обосновано применение повышенных величин таких доз в пересчете на единицу массы мелких лабораторных животных. Контрольной группе мышей по аналогичной схеме вводили дистиллированную воду. Результаты исследований представлены в таблице 9.
Результаты представленных исследований свидетельствуют о наличии достоверного лечебно-профилактического эффекта у препаратов Тамифлю, Ингавирина, Реаферона-Липинта, Арбидола и Виразола при инфекции у мышей, вызванной пандемическим вирусом гриппа А(H1N1/2009). В то же время Ремантадин не проявлял какого-либо лечебно-профилактического эффекта в экспериментах на животных.
Таким образом, предлагаемый штамм вируса гриппа A/Salekhard/01/2009 (H1N1)v может быть успешно использован в экспериментах на беспородных белых мышах для изучения лечебно-профилактической эффективности препаратов против пандемического вируса гриппа А(H1N1/2009) путем сравнительной оценки уровня накопления вируса в легких в контрольной и опытных группах животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЗАЩИТЫ ОРГАНИЗМА ОТ ИНФЕКЦИИ, ВЫЗВАННОЙ ШТАММАМИ СУБТИПА H1N1 ВИРУСА ГРИППА А ПРЕПАРАТОМ НА ОСНОВЕ АЛЬФА-2 ИНТЕРФЕРОНА ЧЕЛОВЕКА | 2013 |
|
RU2523554C1 |
| ШТАММ ВИРУСА ГРИППА A/IIV-Anadyr/177-ma/2009 (H1N1) pdm09, АДАПТИРОВАННЫЙ К ТКАНЯМ ЛЕГКИХ ЛАБОРАТОРНЫХ МЫШЕЙ | 2012 |
|
RU2487936C1 |
| ШТАММ ВИРУСА ГРИППА А/Russia/01/2009-ma СУБТИПА H1N1 ДЛЯ ИССЛЕДОВАНИЯ ЛЕЧЕБНОЙ И ПРОФИЛАКТИЧЕСКОЙ АКТИВНОСТИ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ in vitro И in vivo | 2010 |
|
RU2451072C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЯ, ВЫЗВАННОГО ВИРУСОМ ГРИППА ПТИЦ А/Н5N1 | 2008 |
|
RU2395295C2 |
| ШТАММ ВИРУСА ГРИППА А/IIV-Moscow/01/2009 (H1N1)swl ДЛЯ РАЗРАБОТКИ СРЕДСТВ И МЕТОДОВ БИОЛОГИЧЕСКОЙ ЗАЩИТЫ | 2009 |
|
RU2412244C1 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ГРИППА А НА ОСНОВЕ ЭКСТРАКТА БАЗИДИАЛЬНОГО ГРИБА Laetiporus sulphureus | 2011 |
|
RU2475530C2 |
| ШТАММ ВИРУСА ГРИППА ПТИЦ A/CHICKEN/KURGAN/05/2005 СУБТИП H5N1 ДЛЯ ИЗУЧЕНИЯ АКТИВНОСТИ ЛЕЧЕБНЫХ И ПРОФИЛАКТИЧЕСКИХ ПРЕПАРАТОВ ПРОТИВ ВИРУСА ГРИППА | 2008 |
|
RU2361917C1 |
| ШТАММ ВИРУСА ГРИППА СВИНЕЙ A/SWINE/SIBERIA/1SW/2016 H1N1-СУБТИПА ДЛЯ ИСПОЛЬЗОВАНИЯ В ДИАГНОСТИКЕ ВИРУСА ГРИППА МЕТОДАМИ РТГА И ПЦР И ИССЛЕДОВАНИЯ ЭФФЕКТИВНОСТИ ВАКЦИН И ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ IN VITRO И IN VIVO | 2016 |
|
RU2631938C1 |
| СПОСОБ ЛЕЧЕНИЯ ГРИППА ПТИЦ | 2012 |
|
RU2502512C2 |
| Композиция на основе пептида, подавляющего репликацию вируса гриппа А | 2018 |
|
RU2695336C1 |
Изобретение относится к области вирусологии. Получен новый штамм вируса гриппа А субтипа H1N1 A/Salekhard/01/2009(H1N1)v, депонированный в Коллекции культур микроорганизмов ФГУН ГНЦ ВБ "Вектор" Роспотребнадзора под регистрационным номером V-538. Изобретение может быть использовано для изучения эффективности лечебных и профилактических препаратов против пандемического гриппа в медицинской вирусологии и микробиологии. 9 табл., 5 пр.
Штамм A/Salekhard/01/2009(H1N1)v вируса гриппа А субтипа H1N1 для исследования лечебной и профилактической эффективности препаратов против вируса гриппа, депонированный в Коллекции культур микроорганизмов ФГУН ГНЦ ВБ «Вектор» Роспотребнадзора под регистрационным номером №V-538.
| INFLUENZA RESEARCH DATABASE | |||
| ПРИБОР ДЛЯ КОНТРОЛЯ СМЕЩЕНИЯ ИСХОДНОГО КОНТУРА | 0 |
|
SU367334A1 |
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| ШТАММ ВИРУСА ГРИППА А/IIV-Moscow/01/2009 (H1N1)swl ДЛЯ РАЗРАБОТКИ СРЕДСТВ И МЕТОДОВ БИОЛОГИЧЕСКОЙ ЗАЩИТЫ | 2009 |
|
RU2412244C1 |
Авторы
Даты
2012-07-27—Публикация
2011-06-16—Подача