Область техники, к которой относится изобретение
Настоящее изобретение относится к способу измерения концентрации субстрата и к устройству (биосенсору) для его осуществления.
Предшествующий уровень техники
Биосенсор представляет собой сенсор для измерений субстрата с помощью биокаталитической реакции, а именно посредством предоставления возможности биокатализатору вступать в реакцию с соединением, его субстратом, причем сенсор имеет в качестве передатчика устройство, способное детектировать продукт, полученный в результате биокаталитической реакции, уменьшение количества субстрата или химического соединения, генерируемое посредством реакции с продуктом. Или же он представляет собой сенсор для измерения субстрата, также имеющий в качестве передатчика устройство, способное детектировать физические сигналы, такие как изменение света и/или цвета, или флюоресценции, полученной в результате биокаталитической реакции. Примеры биокатализатора включают в себя ферменты, органеллы, клетки и микроорганизмы.
Таким образом, можно сказать, что биосенсор представляет собой сенсор, который преобразует биокаталитическую реакцию в сигнал, который может детектироваться электронным устройством посредством использования биокатализатора в качестве элемента молекулярного распознавания и посредством объединения его сигнала с передатчиком, таким как электрохимическое устройство, оптическое устройство или устройство детектирования тепла, и тем самым способное анализировать субстрат, распознаваемый биокатализатором. Один из репрезентативных биосенсоров представляет собой ферментативный сенсор, использующий фермент в качестве биокатализатора. Например, для целей измерения глюкозы (виноградного сахара) разработан глюкозный сенсор на основе концепции, в которой фермент, окисляющий глюкозу, иммобилизуется на поверхности электрода, такого как кислородный электрод и электрод на основе перекиси водорода, и количество кислорода, потребляемое окислительной реакцией глюкозы, и количество перекиси водорода, генерируемое в это же время, измеряются электрохимически.
Среди ферментативных сенсоров, широко используемых в настоящее время, в основном используется сенсор, использующий оксидоредуктазу. Его главный принцип основывается на способе измерения с помощью амперметра, электронов, генерируемых когда восстановленное вещество, генерируемое с помощью ферментативной реакции на аноде, повторно окисляется под действием электрического потенциала, прикладываемого извне; или на способе измерения по различию электрических потенциалов, генерируемых между анодом и катодом, когда генерируемые электроны восстанавливаются на катоде.
Также в качестве способа, используемого в простом диагностическом устройстве для измерения сахара в крови или чего-либо подобного, используют способ, включающий в себя окрашивание восстановленного вещества, генерируемого с помощью ферментативной реакции, такого как перекись водорода или восстановленный искусственный акцептор электронов, в соответствии с обычным способом, и определение цвета с помощью оптического сенсора.
В дополнение к этому, в качестве примера конкретного фермента сообщалось о ферментативном сенсоре, использующем люциферазу в качестве фермента, она представляет собой фермент, получаемый из организма, испускающего свет, такого как светлячок, этот ферментативный сенсор отличается детектированием света, генерируемого с помощью ферментативной реакции, где реагирует субстрат для люциферазы. Кроме того, поскольку для этого способа применения ограничиваются случаями, когда может использоваться люцифераза, такими как случаи, где цель ограничивается детектированием вещества, которое является субстратом для люциферазы, таким как АТФ, или случаями, где может использоваться тот принцип, что когда детектируется реакция антитела, она может опосредованно детектироваться через оптический сигнал посредством мечения антитела люциферазой.
Непатентная литература 1: Katz et al., J. Am. Chem. Soc. 2001, 123, 10752-10753.
Раскрытие изобретения
Проблемы, которые должны решаться с помощью изобретения
В обычном биосенсоре, описанном выше, измерительное устройство, использующее биосенсор, такой как ферментативный сенсор (далее упоминаемый как система ферментативных сенсоров), состоит из измерительной части с помощью биосенсора, и отслеживающей части, в которой измеренный сигнал принимается и обрабатывается. В главных типах эти части объединяются или, как видно в диагностическом устройстве для самостоятельного измерения сахара в крови, часть, соответствующая измерительной части, может отсоединяться для замены. Также измерительная часть для детектирования концентрации субстрата и отслеживающая часть для детектирования сигнала от биосенсора должны находиться в прямом контакте или соединяться с помощью проводов с областью, где имеет место биокаталитическая реакция, или нуждаются в схеме для приведения в действие специального передатчика и для него должен предусматриваться, следовательно, источник питания - все это является проблематичным.
В то же время не так давно сообщалось о ферментативном сенсоре, использующем в качестве показателя электродвижущую силу ферментативного топливного элемента. Кроме того, поскольку электродвижущая сила этого топливного элемента сама по себе меньше чем 1 В, то с помощью электродвижущей силы топливного элемента топливный элемент сам по себе не способен питать сенсорное устройство. В случае измерения концентрации субстрата с использованием электродвижущей силы ферментативного сенсора типа топливного элемента в качестве показателя требуется, чтобы электродвижущая сила непосредственно соединялась с вольтметром для измерения электрического потенциала, измеряя тем самым концентрацию субстрата. Или требуется, чтобы электродвижущая сила непосредственно соединялась с вольтметром для измерения электродвижущей силы, и чтобы величина отклика вольтметра передавалась на внешний приемник с помощью беспроводного устройства, приводимого в действие с помощью внешнего источника питания (См. "A Novel Wireless Glucose Sensor Employing Direct Electron Transfer Principle Based Enzyme Fuel Cell", Noriko Kakehi, Tomohiko Yamazaki, Wakako Tsugawa и Koji Sode «Biosensors & Bioelectronics» Epub, 2006, Dec. 11).
Таким образом, хотя ферментативный сенсор типа топливного элемента является компактным и имеет возможность измерений с высокими рабочими характеристиками, в случаях когда он вводится внутрь или устанавливается на живом организме и его сигнал пытаются детектировать без проводов, данные ферментативного сенсора типа топливного элемента не могут считываться без создания дополнительного источника питания. По этой причине, для увеличения электродвижущей силы ферментативного топливного элемента считается, что посредством последовательного соединения ферментативных топливных элементов, электродвижущая сила может увеличиваться в зависимости от количества топливных элементов. Однако в случаях, когда целью является генерирование энергии в живом организме или мониторинг в живом организме, замена ферментативных топливных элементов, соединенных последовательно в живом организме, усложняет устройство и требует больших электродов, что является проблематичным и практически невозможным.
Средства решения проблем
По этой причине, в настоящем изобретении предлагается, чтобы измерение осуществлялось посредством аккумулирования энергии, получаемой в результате биокаталитической реакции, например фермента, и использования в качестве показателя скорости аккумулирования или частоты, с которой энергия высвобождается после аккумулирования. Таким образом, в настоящем изобретении, в случаях когда определенное количество энергии производится посредством биокаталитической реакции, в зависимости от концентрации субстрата, учитывая, что скорость ее производства зависит от концентрации субстрата, используется тот факт, что если энергия, которая должна аккумулироваться, устанавливается на определенном уровне, и энергия высвобождается, когда энергия аккумулируется на определенном уровне, частота высвобождения зависит от концентрации субстрата для биокатализатора. Настоящее изобретение предлагает, чтобы концентрацию субстрата для биокатализатора измеряли посредством измерения частоты высвобождения.
В частности, можно предусмотреть способ измерения концентрации субстрата и устройство для этого посредством объединения биокатализатора, такого как фермент, и устройства, имеющего схему, в которой посредством аккумулирования электрической энергии в конденсаторе до определенного уровня как энергии, получаемой в результате биокаталитической реакции, и высвобождения энергии, сигнал генерируется в зависимости от количества высвобождаемого электричества.
Также посредством объединения схемы, которая генерирует свет, звуковые волны, электромагнитные волны или что-либо подобное из электрической энергии аккумулируемой в конденсаторе, сигнал, генерируемый сенсором, можно легко принимать с помощью детектора сигналов в бесконтактной отслеживающей части. По этой причине измерительная часть и отслеживающая часть могут быть разделены. Таким образом разделение измерительной части и отслеживающей части позволяет сделать измерительную часть гораздо меньше. Такая миниатюризация является преимущественной у портативного сенсора или у сенсора, помещенного или вставленного внутрь организма.
Кроме того, в другом аспекте настоящего изобретения предусматривается схема нового беспроводного ферментативного сенсора, способного аккумулировать электрическую энергию, генерируемую с помощью ферментативной реакции, в конденсаторе, приводить в действие беспроводное устройство посредством электродвижущей силы и передавать сигнал на внешний приемник. Таким образом предусматривается автономный беспроводной ферментативный сенсор, способный передавать сигнал сенсора без проводов, использующий электродвижущую силу ферментативного топливного элемента, без источника питания. Также в устройстве по настоящему изобретению, в отличие от обычного измерения электрического потенциала или чего-либо подобного, беспроводной сигнал может детектироваться принимающей стороной, когда электродвижущая сила превышает пороговое напряжение беспроводного передатчика. На этой основе предусматривается устройство для измерения концентрации субстрата с использованием частоты срабатывания беспроводного передатчика в качестве показателя.
Структура настоящего изобретения является следующей:
(1) Способ измерения концентрации субстрата, включающий в себя:
аккумулирование энергии, получаемой в результате реакции между биокатализатором и субстратом, распознаваемым биокатализатором, на определенном уровне; и
измерение концентрации субстрата посредством использования в качестве показателя того, что скорость аккумулирования энергии зависит от концентрации субстрата.
(2) Способ в соответствии с указанным выше пунктом 1, в котором указанный показатель измеряют на основе частоты высвобождения энергии за заданный период времени, где указанная энергия высвобождается при достижении или превышении указанного определенного уровня.
(3) Способ в соответствии с указанными выше пунктами 1 или 2, где биокатализатор представляет собой фермент, органеллу, микроорганизм или клетку.
(4) Способ в соответствии с любым из указанных выше пунктов 1-3, в котором реакция, катализируемая биокатализатором, представляет собой реакцию окисления.
(5) Способ в соответствии с указанным выше пунктом 3, в котором биокатализатор представляет собой фермент.
(6) Способ в соответствии с указанным выше пунктом 5, в котором фермент представляет собой оксидоредуктазу.
(7) Способ в соответствии с любым из указанных выше пунктов 1-6, в котором энергия, которая должна аккумулироваться, аккумулируется в конденсаторе как электрический заряд.
(8) Устройство для измерения концентрации субстрата, содержащее:
топливный элемент, имеющий анод, на котором располагается субстрат для биокатализатора, и катод, на котором располагается внешний акцептор электронов;
конденсатор, соединенный последовательно с топливным элементом; и
измерительное устройство для измерения концентрации субстрата посредством использования скорости зарядки конденсатора в качестве показателя;
при этом электродвижущая сила, генерируемая посредством переноса электронов, генерируемых посредством реакции между субстратом и биокатализатором, во внешний акцептор электронов на катоде, заряжает конденсатор, и скорость его зарядки измеряют измерительным устройством.
(9) Устройство в соответствии с указанным выше пунктом 8, в котором измерительное устройство измеряет частоту разрядки, посредством указанного конденсатора, разряжающего аккумулируемый электрический потенциал, когда электрический потенциал, заряжающий конденсатор, достигает определенного уровня или превышает его.
(10) Устройство в соответствии с указанным выше пунктом 8 или 9, дополнительно содержащее генератор подкачки заряда для зарядки конденсатора, причем указанный генератор подкачки заряда усиливает электродвижущую силу на основе биокаталитической реакции, когда конденсатор заряжается.
(11) Устройство в соответствии с указанным выше пунктом 9 или 10, в котором измерительное устройство имеет схему генерирования сигнала, генерирующую сигнал посредством разрядки конденсатора, и измеряет частоту сигнала.
(12) Устройство в соответствии с указанным выше пунктом 11, в котором схема генерирования сигнала представляет собой беспроводной передатчик.
(13) Устройство в соответствии с указанным выше пунктом 11 или 12, в котором измерительное устройство измеряет физический сигнал и/или химический сигнал, генерируемый когда схема генерирования сигнала приводится в действие.
(14) Устройство в соответствии с указанным выше пунктом 13, в котором физический сигнал и/или химический сигнал представляют собой звуковую волну, свет или электромагнитную волну.
(15) Устройство в соответствии с любым из указанных выше пунктов 11-14, в котором измерительное устройство дополнительно содержит приемник для приема сигнала, генерируемого посредством разрядки конденсатора, когда конденсатор превышает пороговое напряжение беспроводного передатчика посредством зарядки.
(16) Устройство в соответствии с любым из указанных выше пунктов 8-15, в котором биокатализатор, располагающийся на аноде, представляет собой фермент.
(17) Устройство в соответствии с указанным выше пунктом 16, в котором фермент представляет собой оксидоредуктазу.
(18) Устройство в соответствии с указанным выше пунктом 16, в котором фермент катализирует окисление глюкозы.
В качестве биокатализатора, используемого в настоящем изобретении, могут использоваться ферменты, органеллы, клетки, микроорганизмы и тому подобное. Также в качестве реакции, катализируемой биокатализатором, предпочтительной является окислительно-восстановительная реакция объекта, который должен измеряться. В качестве фермента могут использоваться различные оксидоредуктазы. Примеры их включают в себя оксидазы для спирта, глюкозы, холестерина, фруктозиламина, глицерина и мочевой кислоты, причем оксидазы используют FAD в качестве кофермента; дегидрогеназы для спирта, глюкозы и глицерина, причем эти дегидрогеназы требуют FAD в качестве кофермента; и дегидрогеназы для спирта, глюкозы и глицерина, причем эти дегидрогеназы используют PQQ в качестве кофермента. В частности, в случаях когда должна измеряться глюкоза, предпочтительными являются глюкозаоксидаза и/или глюкозадегидрогеназа, использующие FAD или PQQ в качестве кофермента. Она может представлять собой фермент, выделенный и очищенный из микроорганизма или клеток, которые производят фермент. Или она может представлять собой рекомбинантный фермент, продуцируемый в E. coli или чем-либо подобным.
В дополнение к этому, биокатализатор, используемый в настоящем изобретении, может представлять собой не только фермент, но может представлять собой мембрану, содержащую фермент, органеллу, содержащую фермент, или клетку, содержащую фермент, при условии, что она способна окислять субстрат на аноде и переносить этот электрон в соответствующий акцептор электрона или непосредственно в электрод, и может использоваться при условии, что реакция окисления рассмотренного выше субстрата достигается как результат этих ферментативных реакций и множества ферментативных реакций, связанных с ними.
В качестве способа генерирования электрической энергии с использованием ферментов в соответствии с настоящим изобретением может использоваться ферментативный топливный элемент. То есть он представляет собой ферментативный топливный элемент, отличающийся тем, что оксидаза или дегидрогеназа иммобилизована на аноде.
В этом случае, в качестве катода может использоваться электрод, в котором используется фермент, восстанавливающий кислород, такой как билирубиноксидаза, или электрод, в котором объединяются соответствующие акцепторы электронов. Или может использоваться катализатор, имеющий способность к восстановлению кислорода, такой как платина, или неорганический катализатор, содержащий платину.
Также полагается, что структура, содержащая акцептор электронов, а также фермент, могут использоваться в качестве анода. То есть могут использоваться структуры, переносящие электроны, полученные с помощью ферментативной реакции, в искусственный акцептор электронов и окисляющие электрон на электроде. Или дегидрогеназы, способные непосредственно переносить электроны на электрод, такие как фермент, имеющий цитохром в субъединице переноса электрона, и тому подобное, могут составлять анод без добавления какого-либо искусственного акцептора электронов. В качестве материалов электродов для анода и катода могут использоваться электроды, заполненные или покрытые частицами углерода, угольные электроды, золотые электроды, платиновые электроды или что-либо подобное.
Искусственный акцептор электронов анода или катода не является конкретно ограниченным, и могут использоваться комплекс осмия, комплекс рутения, феназинметосульфат и его производное, хиноновое соединение или что-либо подобное.
Фермент для катода не является конкретно ограниченным и может наноситься билирубиноксидаза или лакказа. Искусственный акцептор электронов катода не ограничивается и могут использоваться феррицианид калия, ABTS или что-либо подобное.
В качестве фермента для анода могут использоваться различные оксидазы или дегидрогеназа. В частности, в случаях когда должна измеряться глюкоза, могут использоваться глюкозаоксидаза или глюкозадегидрогеназа, использующие PQQ или FAD в качестве кофермента.
В настоящем изобретении, в качестве способа размещения фермента на электроде может использоваться смесь фермента самого по себе и материала электрода, такого как углеродная паста. Или после получения с помощью общего способа иммобилизации фермента иммобилизованный фермент может размещаться на электроде. Примеры включают в себя способы, в которых обработка для поперечной сшивки с помощью бинарного реагента для поперечной сшивки, такого как глютаральдегид, осуществляется после смешивания их обоих; и способы инклюзивной иммобилизации в синтетическом полимере, таком как полимер, подвергающийся поперечной сшивке под действием света, электропроводящий полимер или окислительно-восстановительный полимер, или природная полимерная матрица. Полученный таким образом смешанный белок смешивают с частицами углерода или смешивают с угольной пастой, которая состоит из частиц углерода и находится в состоянии, когда она легко объединяется с ферментом. После этого полученную смесь дополнительно подвергают обработке для поперечной сшивки, а затем размещают на электроде, состоящем из углерода, золота или платины. В качестве углеродной частицы может использоваться частица, имеющая удельную площадь поверхности в пределах примерно от 10 м2/г до не менее чем 500 м2/г, более предпочтительно до не менее чем 800 м2/г. Примеры первых включают в себя VULCAN (торговая марка: Cabot Corporation) как коммерчески доступный продукт, а примеры вторых включают в себя сажу Ketchen (торговая марка: Akzo Nobel Chemicals Inc.).
Кроме того, когда фермент размещают на электроде таким способом, искусственный акцептор электронов может иммобилизоваться в то же самое время. Как правило, смешивают глюкозадегидрогеназу, использующую FAD в качестве кофермента, FADGDH и метоксифеназинметосульфат (mPMS). Смесь дополнительно смешивают с угольной пастой, а затем сушат вымораживанием. Ее размещают на угольном электроде и полученный продукт погружают в водный раствор глютаральдегида для поперечной сшивки белка, изготавливая при этом ферментативный электрод.
В ферментативном топливном элементе оксидаза или дегидрогеназа, использующая объект измерения в качестве субстрата, иммобилизуется на анодном электроде. Кислородредуктаза иммобилизуется на катоде. Полученные таким образом электроды используют в качестве электродов для анода и катода. На аноде, например, m-PMS может использоваться в качестве искусственного акцептора электронов, а также на катоде, например, ABTS может использоваться в качестве искусственного акцептора электронов.
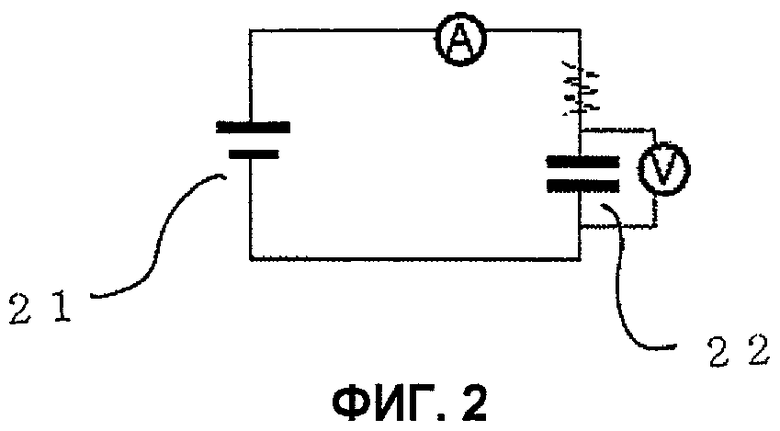
Посредством присоединения полученной таким образом части, где электрическая энергия генерируется с помощью ферментативной реакции, к конденсатору может сохраняться электрическая энергия. То есть на основе электродвижущей силы, получаемой посредством ферментативной реакции, конденсатор, соединенный со схемой, показанной на фиг.2, заряжается, пока емкость конденсатора не зарядится полностью. По этой причине, в случаях когда ферментативная реакция осуществляется в растворе с такой же концентрацией субстрата, когда используют конденсатор с большей емкостью, он требует более продолжительного периода времени для полной зарядки. В противоположность этому, когда используют конденсатор меньшей емкости, время до полной зарядки короче. Или в случаях когда используют конденсатор одинаковой емкости, когда концентрация субстрата для фермента ниже, величина электрической энергии, генерируемая в единицу времени, меньше, и таким образом время до полной зарядки больше, при этом когда концентрация субстрата выше, время до полной зарядки в противоположность этому короче. Таким образом, при установке конденсатора на заданную величину емкости время, необходимое для зарядки, изменяется в зависимости от концентрации субстрата для фермента. По этой причине концентрация субстрата может измеряться посредством использования времени, необходимого для зарядки (скорости зарядки), в качестве показателя. То есть посредством регистрации заранее корреляции между наблюдаемым временем, необходимым для зарядки (скоростью зарядки), и концентрацией субстрата, и на этой основе построения калибровочной кривой концентрация субстрата для неизвестного образца может измеряться по наблюдаемому времени, необходимому для зарядки.
Также посредством присоединения соответствующей схемы к конденсатору, так что разрядка начинается когда завершается зарядка, концентрация субстрата может измеряться таким же образом посредством измерения частоты зарядки и разрядки в единицу времени. То есть посредством регистрации заранее корреляции между наблюдаемой частотой разрядки в единицу времени и концентрацией субстрата и построения на этой основе калибровочной кривой концентрация субстрата в неизвестном образце может измеряться по наблюдаемой частоте разрядки.
Кроме того, если посредством присоединения схемы генерируется свет, звуковая волна или электромагнитная волна, посредством наблюдения света, звуковой волны или электромагнитной волны и измерения частоты, с которой она наблюдается в единицу времени, или интервала между ее наблюдениями, может измеряться концентрация субстрата. То есть посредством регистрации заранее корреляции между наблюдаемым временем, необходимым для генерирования света, звуковой волны или электромагнитной волны, и концентрацией субстрата и построения на этой основе калибровочной кривой концентрация субстрата для неизвестного образца может измеряться по наблюдаемому времени, необходимому для генерирования света, звуковой волны или электромагнитной волны, или частоты в единицу времени.
В дополнение к этому, в зависимости от схемы, которая должна приводиться в действие, возможно, чтобы электрический потенциал конденсатора устанавливался соответствующим образом. То есть посредством объединения электродвижущей силы ферментативного топливного элемента, который генерирует электрическую энергию, генерируемую ферментативной реакцией, в качестве электродвижущей силы, со схемой усиления, электрический потенциал, заряжающий конденсатор, может быть увеличен. Для этого усиления может использоваться коммерчески доступный генератор подкачки заряда или ИС с ним. Электрический потенциал, сохраняемый в конденсаторе, может устанавливаться в зависимости от типа и количества объединяемых генераторов подкачки заряда. Электрический потенциал в конденсаторе может устанавливаться в зависимости от схемы генерирования сигнала, которая должна приводиться в действие.
Частота, с которой заряжается и разряжается конденсатор, зависит, как описано выше, от емкости конденсатора и от концентрации субстрата. То есть если концентрация субстрата является постоянной, то чем меньше емкость конденсатора, тем выше частота зарядки и разрядки. И чем больше емкость конденсатора, тем ниже частота зарядки и разрядки. Также если емкость конденсатора является постоянной, частота зарядки и разрядки изменяется в зависимости от концентрации субстрата. И чем ниже концентрация субстрата, тем ниже частота зарядки и разрядки. Чем выше концентрация субстрата, тем выше частота зарядки и разрядки.
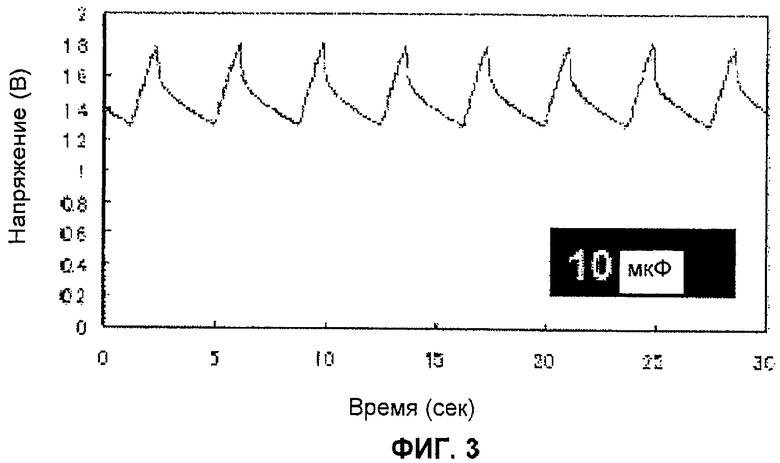
Например, то что наблюдается, когда вольтметр соединен с обоими концами конденсатора, показано на фиг.3. В этом режиме образец с постоянной концентрацией глюкозы используется в качестве субстрата; в качестве фермента используется фермент, катализирующий дегидрирование глюкозы; и электродвижущая сила, генерируемая ферментативным топливным элементом, усиливается от 0,3 В на ферментативном топливном элементе до 1,8 В посредством генератора подкачки заряда, заряжая при этом конденсатор. Как показано на фиг.3, можно наблюдать, что электрический потенциал конденсатора достигает 1,8 В через регулярные интервалы времени, и электрическая энергия, генерируемая ферментативной реакцией, сохраняется, а затем высвобождается. В этом случае когда емкость присоединенного конденсатора изменяется от 0,47 мкФ до 1 мкФ, наблюдаемый интервал зарядки и разрядки изменяется. То есть когда емкость конденсатора составляет 0,47 мкФ, интервал составляет 0,2 секунды (частота зарядки и разрядки 5 раз/секунда, 5 Гц), в то время как частота изменяется следующим образом: 2,4 Гц при 1 мкФ, 0,27 Гц при 10 мкФ и 0,028 Гц при 100 мкФ.
Кроме того, когда наблюдается состояние, когда конденсатор заряжается, посредством использования конденсатора 10 мкФ и изменения концентрации глюкозы, интервал зарядки и разрядки более продолжительный при более низкой концентрации глюкозы, и интервал зарядки и разрядки короче при более высокой концентрации глюкозы (см. фиг.4). В противоположность этому, когда это наблюдается как частота зарядки и разрядки, частота зарядки и разрядки ниже при более низкой концентрации глюкозы, и частота зарядки и разрядки выше при более высокой концентрации глюкозы.
Посредством соединения этой схемы со схемой, генерирующей сигнал в зависимости от зарядки и разрядки конденсатора, таким же образом и наблюдения света, звуковой волны или электромагнитной волны, генерируемой при этом, концентрация субстрата может измеряться таким же образом. Например, в случаях когда присоединяется светодиод, посредством наблюдения интервала испускания светодиода или частоты испускания может измеряться концентрация субстрата.
Как показано на фиг.5, интервал испускания дольше при более низкой концентрации глюкозы и интервал испускании короче при более высокой концентрации глюкозы. В противоположность этому, когда это наблюдается как частота испускания, частота испускания ниже при более низкой концентрации глюкозы и частота испускания выше при более высокой концентрации глюкозы.
Также в случаях когда резонансная схема, генерирующая электромагнитную волну, соединяется с этой схемой, посредством наблюдения интервала или частоты передачи электромагнитной волны может измеряться концентрация субстрата. В этом случае интервал передаваемой электромагнитной волны больше при более низкой концентрации глюкозы и интервал короче при более высокой концентрации глюкозы. Когда это наблюдается как частота передачи электромагнитной волны, частота передачи ниже при более низкой концентрации глюкозы и частота передачи выше при более высокой концентрации глюкозы.
Как можно видеть, из такого режима ясно, что когда присоединяется передатчик сигналов, приводимый в действие емкостью и электрическим потенциалом конденсатора, независимо от типа сигнала, передаваемого от него, то есть света, звуковой волны или электромагнитной волны, концентрация субстрата для ферментативной реакции может измеряться посредством наблюдения интервала и частоты. В дополнение к этому также ясно, что фермент не ограничивается дегидрогеназой, использующей глюкозу в качестве субстрата, как показано в настоящем документе, и могут использоваться различные оксидазы и дегидрогеназы. Примеры их включают в себя оксидазы для спирта, глюкозы, холестерина, фруктозиламина, глицерина и мочевой кислоты, эти оксидазы используют FAD в качестве кофермента; дегидрогеназы для спирта, глюкозы и глицерина, эти дегидрогеназы используют FAD в качестве кофермента; и дегидрогеназы для спирта, глюкозы и глицерина, эти дегидрогеназы используют PQQ в качестве кофермента. Даже если это и не один только фермент, при условии, что он способен окислять субстрат на аноде и переносить этот электрон в соответствующий акцептор электронов или непосредственно в электрод, он может представлять собой мембрану, органеллу, клетку или микроорганизм - все они содержат фермент. Если реакция окисления рассмотренного выше субстрата достигается в результате этих ферментативных реакций, он может использоваться, что понятно само по себе из изучения случаев биосенсоров, использующих биокатализаторы, катализирующие различные окислительно-восстановительные реакции.
Также в качестве другого режима схема передачи, используемая в беспроводной связи, может использоваться как схема передачи сигнала, соединенная с конденсатором. Эти схемы передачи требуют определенного уровня или более высокого электрического потенциала для приведения их в действие. Если электродвижущая сила ниже этого уровня, схема останавливается, как и передача. Также она не может приводиться в действие, когда электродвижущая сила не превышает определенного уровня. То есть когда схема беспроводной передачи, приводимая в действие при 1,5 В, соединяется с конденсатором и передаваемый сигнал наблюдается с помощью системы удаленного приема, передача от беспроводного передатчика наблюдается в соответствии с зарядкой и разрядкой конденсатора. То есть в зависимости от концентрации субстрата для ферментативной реакции схема беспроводной передачи приводится в действие и передается сигнал. Интервал дольше, когда концентрация субстрата для фермента ниже, и интервал короче, когда концентрация субстрата для фермента выше. Также частота передачи сигнала ниже, когда концентрация субстрата для фермента ниже, и частота передачи сигнала выше, когда концентрация субстрата для фермента выше. По этой причине концентрация субстрата для фермента может измеряться посредством наблюдения принимаемых передающихся данных.
В качестве такой схемы беспроводной передачи может использоваться резонансный контур. Также в качестве конденсатора в таком резонансном контуре может также использоваться конденсатор, у которого переменная емкость.
Краткое описание чертежей
Фиг.1 показывает схематический вид способа и устройства для измерения субстрата в соответствии с настоящим изобретением.
Фиг.2 показывает схему конденсатора, используемого в настоящем изобретении.
Фиг.3 показывает изменение электрического потенциала посредством повторяющейся зарядки и разрядки конденсатора в устройстве в соответствии с настоящим изобретением.
Фиг.4 показывает соотношение между частотой зарядки конденсатора и концентрацией глюкозы.
Фиг.5 показывает интервал (время) испускания светодиода для изменения концентрации глюкозы.
Фиг.6A показывает время, необходимое для зарядки конденсатора (сопротивление 100 кОм).
Фиг.6B показывает время, необходимое для зарядки конденсатора (сопротивление 500 кОм).
Фиг.6C показывает время, необходимое для зарядки конденсатора (сопротивление 500 кОм).
Фиг.7A показывает время, необходимое для зарядки конденсатора для изменения концентрации глюкозы (10 кОм).
Фиг.7B показывает время, необходимое для зарядки конденсатора для изменения концентрации глюкозы (500 кОм).
Фиг.8A показывает изменения электрического потенциала конденсатора посредством ферментативного топливного элемента в течение времени (0,47 мкФ).
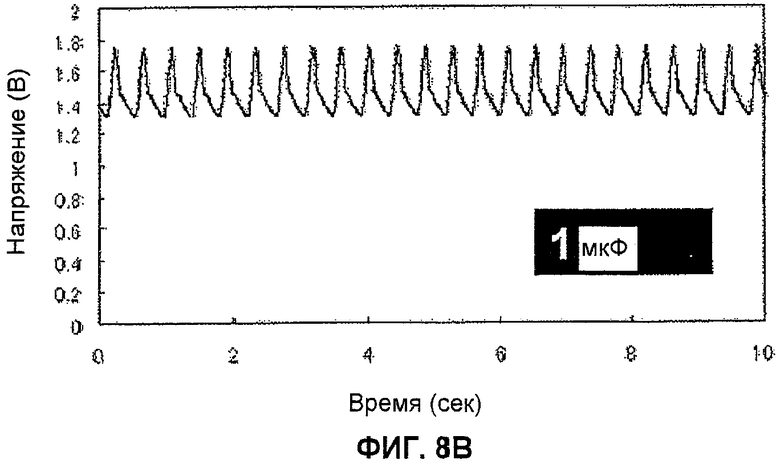
Фиг.8B показывает изменение электрического потенциала конденсатора посредством ферментативного топливного элемента в течение времени (1 мкФ).
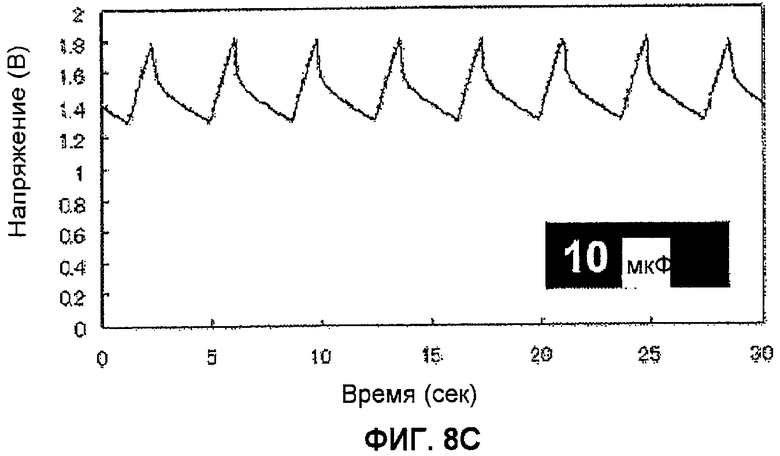
Фиг.8C показывает изменение электрического потенциала конденсатора посредством ферментативного топливного элемента в течение времени (10 мкФ).
Фиг.8D показывает изменение электрического потенциала конденсатора посредством ферментативного топливного элемента в течение времени (100 мкФ).
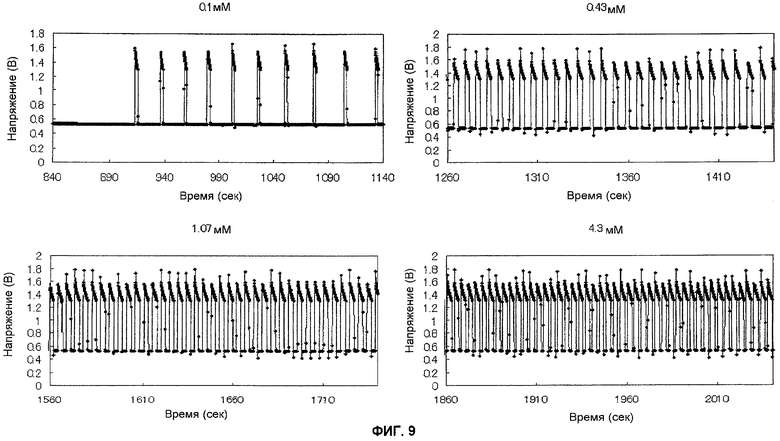
Фиг.9 показывает частоту сигнала в случае изменения концентрации глюкозы.
Фиг.10 показывает изменение времени, необходимого для конденсатора, чтобы достичь 1,8 В, для изменения концентрации глюкозы.
Фиг.11 Корреляция частоты, при которой конденсатор достигает 1,8 В, в единицу времени для изменения концентрации глюкозы.
Фиг.12 Корреляция между частотой наблюдаемого сигнала и концентрацией глюкозы в беспроводном сенсоре (1,8 В, усиление).
Фиг.13 Корреляция между частотой наблюдаемого сигнала и концентрацией глюкозы в беспроводном сенсоре (2,4 В, усиление).
Фиг.14 показывает пример в качестве схемы передачи сигнала, схемы измерения/передачи, использующей резонансный контур в качестве передатчика.
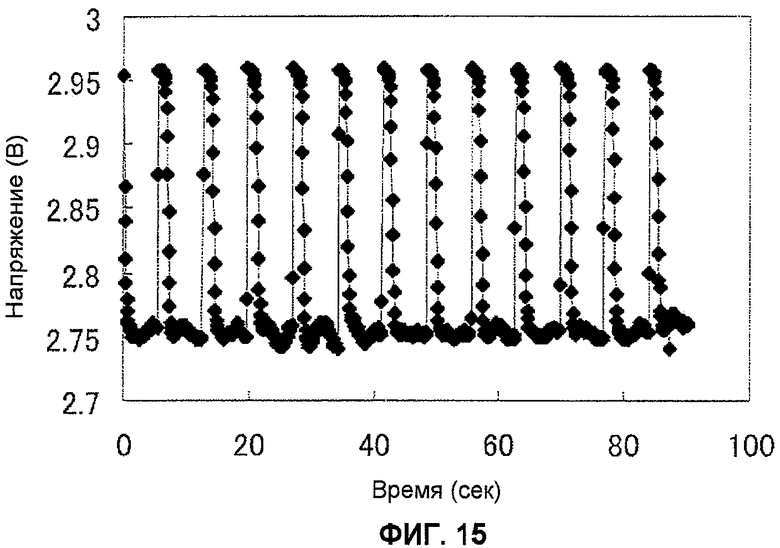
Фиг.15 показывает пример, в котором регистрируется электромагнитная волна, наблюдаемая посредством использования схемы передачи, показанной на фиг.14.
Фиг.16 показывает пример в качестве схемы передачи сигнала, схемы измерения/передачи, использующей в качестве передатчика резонансный контур с использованием варикапа.
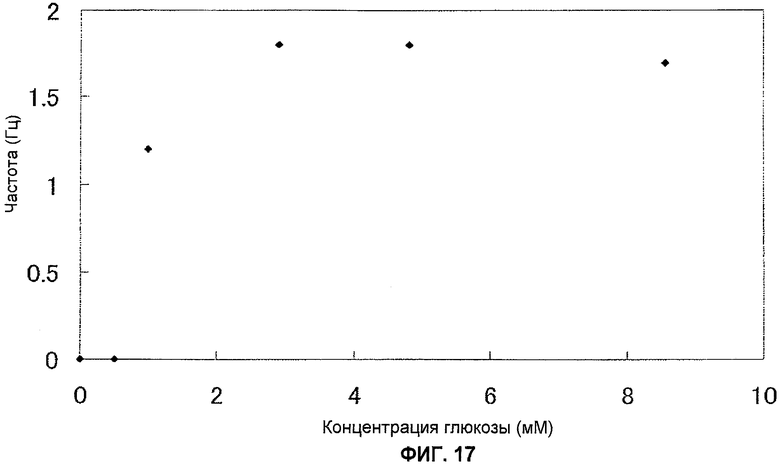
Фиг.17 показывает пример, в котором электромагнитную волну наблюдают посредством использования схемы передачи, показанной на фиг.16, и измеряют концентрацию глюкозы в образец.
Наилучший способ осуществления изобретения
Настоящее изобретение теперь будет описано более подробно ниже с помощью его примеров. Однако настоящее изобретение не ограничивается этими примерами.
Пример 1
Приготовление анода:
Черную краску Ketchen (10 мл), 100 мМ PPB (pH 7,0) (10 мл) и раствор комплекса FADGDH (40 мл) (1,2 Ед./мл) смешивают. 50 мл смеси равномерно наносят на 1 см2 углеродной ткани, а затем сушат на воздухе при 4°C в течение 3 часов. Посредством погружения полученного продукта в 1% раствор глютаральдегида (10 мл) при комнатной температуре в течение 30 минут осуществляют обработку для поперечной сшивки. Затем путем погружения этой углеродной ткани в 10 мМ Tris-HCl (10 мл) в течение 20 минут удаляют непрореагировавший глютаральдегид. Затем полученный продукт погружают в 100 мМ PPB (pH 7,0) (10 мл) в течение 1 часа для уравновешивания, при этом получают анод.
Приготовление катода:
Черную краску на платиновом носителе (10 мл) и 100 мМ PPB (pH 7,0) (50 мл) смешивают. 50 мл смеси наносят равномерно на углеродную ткань, и полученный продукт сушат на воздухе при 4°C в течение 3 часов. На полученный продукт капают 50 мл 3% (масс/объем) поли(диметилсилоксана) (PDMS), разбавленного этанолом, и сушат на воздухе в течение ночи с получением катода.
Конструкция электрической ячейки и схемы:
Используя полученные анод и катод, конструируют электрическую ячейку, используя 100 мМ PPB (pH 7,0), содержащего 20 мМ глюкозы в качестве реакционного раствора. Электрическую ячейку, переменное сопротивление, конденсатор и переключатель - все соединяют последовательно, получая при этом схему.
В полученной таким образом схеме исследуют время зарядки конденсатора.
Таким образом, используя два типа конденсаторов (0,1 мкФ и 1 мкФ), при условии, когда зарядку осуществляют при концентрации глюкозы 20 мМ, электрический потенциал, прикладываемый к конденсатору, и электрический ток, который протекает в схеме, когда переключатель соединяют с сопротивлением, измеряют для исследования времени зарядки конденсатора.
В этом случае результаты, когда используют конденсатор в 1 мкФ в качестве конденсатора и сопротивление равно 100 кОм, 500 кОм и 1000 кОм, показаны на фиг.6. Электрический ток протекает в то время, когда переключатель включен. Также электрический ток уменьшается со временем и электрический потенциал на конденсаторе увеличивается. Кроме того, когда значение сопротивления изменяется для уменьшения или увеличения значения электрического тока, время зарядки конденсатора увеличивается или уменьшается соответственно. При любом сопротивлении, когда величина заряда, заряжающего конденсатор, вычисляется из значения электрического тока, который протекает в схеме, она почти равна емкости конденсатора. В дополнение к этому, когда используют конденсатор 0,1 мкФ, получают сходные результаты. Кроме того, по сравнению с конденсатором 1 мкФ время зарядки короче. Показано, что даже в случаях, когда в качестве источника питания используют ферментативный топливный элемент, конденсатор способен функционировать адекватно.
Используя схему, приготовленную таким же образом, оценивают зависимость времени зарядки конденсатора от концентрации глюкозы. Используя конденсатор 1 мкФ, измеряют электрический потенциал на конденсаторе, когда сопротивление устанавливают на 10 кОм или 500 кОм. В этом случае посредством постепенного добавления образца глюкозы для увеличения концентрации глюкозы в реакционном растворе исследуют время зарядки при каждой концентрации глюкозы.
Результаты показаны на фиг.7. При сопротивлении либо 10 кОм, либо 500 кОм, когда концентрация глюкозы увеличивается, время зарядки уменьшается. При 500 кОм уменьшение времени зарядки едва наблюдается, примерно при 6 мМ, в то время как при 10 кОм увеличение электрического тока наблюдают вплоть до 11 мМ. Показано, что используя время для зарядки конденсатора в качестве показателя, можно измерять концентрацию субстрата для фермента.
Пример 2
Приготовление анода:
Черную краску Ketchen (10 мл), 100 мМ PPB (pH 7,0) (10 мл) и раствор комплекса FADGDH (40 мл) (4,2 Ед./мл) смешивают. 300 мл смеси наносят равномерно на 6 см2 углеродной ткани, а затем сушат на воздухе при 4°C в течение 3 часов. Посредством погружения полученного продукта в 1% раствор глютаральдегида (10 мл) при комнатной температуре в течение 30 минут осуществляют обработку для поперечной сшивки. Затем посредством погружения этой углеродной ткани в 10 мМ Tris-HCl (10 мл) в течение 20 минут удаляют непрореагировавший глютаральдегид. Затем полученный продукт погружают в 100 мМ PPB (pH 7,0) (10 мл) в течение 1 часа для уравновешивания, при этом получают анод.
Приготовление катода:
Черную краску на носителе из платины (60 мл) и 100 мМ PPB (pH 7,0) (300 мл) смешивают. 300 мл смеси равномерно наносят на углеродную ткань (6 см2), и полученный продукт сушат на воздухе при 4°C в течение 3 часов. На полученный продукт капают 300 мл 3% (масс/объем) поли(диметилсилоксана) (PDMS), разбавленного этанолом, и сушат на воздухе в течение ночи с получением катода.
Конструкция электрической ячейки и схемы:
Используя полученные анод и катод, электрическую ячейку конструируют, используя 100 мМ PPB (pH 7,0) в качестве реакционного раствора. Генератор подкачки заряда (усилительная ИС IC; S-882Z18 производится Seiko Instruments Inc.), способный усиливать от 0,3 В до 1,8 В, объединяют с этим топливным элементом, конструируя тем самым схему, показанную на фиг.1. В качестве схемы генерирования сигнала присоединяют оранжевый светодиод и дополнительно присоединяют различные конденсаторы от 0,47 до 100 мкФ. Посредством измерения электрического потенциала на конденсаторе и интервала времени испускания и частоты светодиода оценивают цикл зарядки и разрядки.
Конструкция схемы с использованием усилительной ИС и оценка частоты сигнала по емкости конденсатора
Приведение в действие настоящей схемы посредством ферментативного топливного элемента оценивают по миганию светодиода или по изменению со временем электрического потенциала конденсатора. Разницу в частоте сигнала, получаемую когда конденсатор заменяют конденсаторами от 0,47 до 100 мкФ, также оценивают. Концентрация глюкозы в реакционном растворе равна 20 мМ.
Изменение со временем электрического потенциала конденсатора в этом случае показано на фиг.8. Когда используют конденсатор 0,47 мкФ, наблюдают пикообразные сигналы при частоте пять раз в секунду (5/сек). Также в том же цикле наблюдают мигание диода. Когда емкость конденсатора изменяется, изменяется и частота сигнала. Цикл составляет 2,4/сек, 0,27/сек и 0,028/сек, когда используют конденсатор 1 мкФ, 10 мкФ и 100 мкФ соответственно. Показано, что частота сигнала может увеличиваться, если сделать емкость конденсатора меньше.
Зависимость цикла зарядки и разрядки конденсатора от концентрации глюкозы
Когда концентрация глюкозы, которая является субстратом для фермента, изменяется, частота сигнала, получаемая в это время, оценивается посредством мигания светодиода или изменения со временем электрического потенциала конденсатора. В качестве конденсатора используют конденсатор с емкостью 10 мкФ. Результаты показаны на фиг.9. Когда концентрация глюкозы увеличивается, время, необходимое для конденсатора, чтобы достигнуть максимального электрического потенциала, становится короче, и наблюдается увеличение частоты, с которой достигается пиковый электрический потенциал, в единицу времени. На основе этого результата определяют концентрацию глюкозы и мигание LED, т.е. время, необходимое для конденсатора, чтобы достичь 1,8 В (фиг.10), и количество миганий LED в единицу времени, т.е. частоту, при которой конденсатор достигает 1,8 В в единицу времени (фиг.11). Как показано на этих кривых, из полученной кривой продемонстрировано, что мигание LED, т.е. время, необходимое для конденсатора, чтобы достичь 1,8 В, и количество миганий LED в единицу времени, т.е. частота, с которой конденсатор достигает 1,8 В в единицу времени, зависят от концентрации глюкозы. Из этого показано, что концентрацию глюкозы можно измерять посредством использования частоты сигнала в качестве показателя, и конструируется новый биосенсор, который использует зарядку и разрядку конденсатора.
Приведение в действие беспроводной системы с помощью усиливаемого ферментативного топливного элемента
Используя полученный анод и катод, конструируют электрическую ячейку с использованием 100 мМ PPB (pH 7,0) в качестве реакционного раствора. Генератор подкачки заряда (усилительная ИС; S-882Z18, производится Seiko Instruments Inc.), способный усиливать от 0,3 В до 1,8 В, или генератор подкачки заряда (усилительная ИС; S-882Z24, производится Seiko Instruments Inc.), способный усиливать от 0,3 В до 2,4 В, объединяется с этим топливным элементом, составляя тем самым схему, показанную на фиг.1. В качестве схемы генерирования сигнала присоединяют передатчик беспроводной системы (инфракрасная передача). Т.е. часть с источником питания беспроводного передатчика соединяют со схемой генерирования сигнала, показанной на фиг.1, тем самым конструируется биосенсор, использующий в качестве показателя приведение в действие системы беспроводной передачи под действием электрического потенциала, разряжающегося когда заряжается конденсатор. Концентрация глюкозы в реакционном растворе составляет 0-25 мМ.
В результате в присутствии глюкозы передатчик беспроводной системы приводится в действие и сигнал передается приемнику через регулярные интервалы времени.
Фиг.12 показывает корреляцию между частотой сигнала, наблюдаемого при усилении до 1,8 В, и концентрацией глюкозы. Фиг.13 показывает корреляцию между частотой сигнала, наблюдаемого при усилении до 2,4 В, и концентрацией глюкозы. Как здесь показано, при любом усилении частота приема сигнала коррелирует с концентрацией глюкозы, и посредством мониторинга этой частоты может измеряться концентрация глюкозы. Измеряемая концентрация глюкозы, в любом случае, составляет от 0,5 мМ до 20 мМ, что перекрывает диапазон, достаточный для измерения количества сахара в крови при сахарном диабете. Таким образом показано, что это может хорошо применяться в устройстве для диагностики сахара в крови, включая устройство для диагностики сахара в крови непрерывного действия.
Из этого показано, что беспроводная система может приводиться в действие посредством использования электродвижущей силы, аккумулируемой в результате ферментативной реакции, и эта электродвижущая сила заряжает конденсатор. Следовательно, показано, что в настоящем новом биосенсоре беспроводной передатчик может применяться как схема передачи сигнала.
Конструкция схемы измерения/передачи с использованием резонансного контура в качестве передатчика
Топливный элемент конструируют таким же образом, как описано в примере 1, и конденсатор 10 мкФ и усилительная схема ИС с усилением от 0,3 до 1,8 В объединяются с ним, тем самым конструируется биоконденсатор. В качестве источника питания выходная мощность биоконденсатора соединяется с обоими концами, создавая тем самым колебательный контур Хартли. Используя этот передатчик, частота приема электромагнитной волны может измеряться с помощью приемной схемы. В результате в присутствии глюкозы, как описывается на фиг.15, наблюдается, что электромагнитная волна принимается через регулярные интервалы. Из приводимого описания полностью понятно, что эта частота приема электромагнитной волны зависит от концентрации глюкозы.
Конструкция схемы измерения/передачи с использованием в качестве передатчика резонансного контура, использующей варикап
Топливный элемент конструируют таким же образом, как описывается в примере 1, и конденсатор 0,47 мкФ и усилительная схема ИС с усилением от 0,3 до 1,8 В объединяются с ним, тем самым конструируется биоконденсатор. В качестве источника питания выходная мощность биоконденсатора соединяется с обоими концами варикапа (1sV149), образуя тем самым колебательный контур Хартли. Используя этот передатчик, частота приема электромагнитной волны может измеряться с помощью приемной схемы. Фиг.17 показывает пример, в которой наблюдается частота электромагнитной волны, когда используется эта схема передатчика и измеряется концентрация глюкозы в образцах. Как здесь показано, концентрация глюкозы может измеряться посредством использования настоящей схемы.















Изобретение относится к измерению концентрации субстрата посредством аккумулирования энергии, полученной из реакции между биокатализатором и субстратом, распознаваемым биокатализатором. Сущность изобретения: изобретение предусматривает способ, в котором измерение скорости аккумулирования осуществляют посредством измерения частоты энергии, высвобождаемой за определенную величину времени, когда энергия, аккумулируемая в конденсаторе, достигает определенного уровня, а затем высвобождается. Изобретение позволяет миниатюризировать и упростить схему измерения концентрации субстрата. 3 н. и 20 з.п. ф-лы, 17 ил., 2 пр.
1. Способ измерения концентрации субстрата, включающий в себя:
аккумулирование энергии, получаемой в результате реакции между биокатализатором и субстратом, распознаваемым указанным биокатализатором; и
измерение концентрации субстрата на основе скорости аккумулирования или частоты разрядки указанной энергии.
2. Способ по п.1, в котором указанную скорость аккумулирования измеряют с помощью аккумулирования указанной энергии до определенного уровня, используя в качестве показателя того, что скорость аккумулирования энергии зависит от концентрации субстрата.
3. Способ по п.2, в котором указанную концентрацию субстрата измеряют на основе времени, необходимого для зарядки указанной получаемой в результате энергии, с использованием калибровочной кривой, подготовленной на основе соотношения между скоростью аккумулирования и концентрацией субстрата.
4. Способ по п.1, в котором указанная частота разрядки, которая является частотой, при которой указанная энергия высвобождается при достижении или превышении указанного определенного уровня, зависит от указанной концентрации субстрата.
5. Способ по п.4, в котором указанную концентрацию субстрата измеряют на основе частоты разрядки указанной получаемой в результате энергии с использованием калибровочной кривой, подготовленной на основе соотношения между частотой разрядки и концентрацией субстрата.
6. Способ по п.1, в котором указанный биокатализатор представляет собой фермент, органеллу, микроорганизм или клетку.
7. Способ по п.1, в котором указанная реакция, катализируемая биокатализатором, представляет собой реакцию окисления.
8. Способ по п.7, в котором указанный биокатализатор представляет собой фермент.
9. Способ по п.8, в котором указанный фермент представляет собой оксидоредуктазу.
10. Способ по любому из пп.1-9, в котором указанная энергия, которая должна аккумулироваться, аккумулируется в конденсаторе как электрический заряд.
11. Устройство для измерения концентрации субстрата, содержащее:
топливный элемент, имеющий анод, на котором располагается биокатализатор, и катод, на котором располагается внешний акцептор электронов;
конденсатор, последовательно соединенный с топливным элементом; и
измерительное устройство для измерения концентрации субстрата посредством использования скорости зарядки конденсатора в качестве показателя;
при этом электродвижущая сила, генерируемая посредством переноса электронов, генерируемых посредством реакции между субстратом и биокатализатором, во внешний акцептор электронов на катоде, заряжает конденсатор, при этом скорость его зарядки измеряется указанным измерительным устройством.
12. Устройство по п.11, в котором указанное измерительное устройство измеряет частоту разрядки посредством указанного конденсатора, разряжающего аккумулируемый электрический потенциал, когда электрический потенциал, заряжающий конденсатор, достигает определенного уровня или превышает его.
13. Устройство по п.11, дополнительно содержащее генератор подкачки заряда для зарядки конденсатора, причем указанный генератор подкачки заряда усиливает электродвижущую силу на основе биокаталитической реакции, когда конденсатор заряжается.
14. Устройство по п.12, в котором указанное измерительное устройство имеет схему генерирования сигнала, генерирующую сигнал посредством разрядки конденсатора, и измеряет частоту указанного сигнала.
15. Устройство по п.14, в котором указанная схема генерирования сигнала представляет собой беспроводной передатчик.
16. Устройство по п.14, в котором указанное измерительное устройство измеряет физический сигнал и/или химический сигнал, генерируемый, когда приводится в действие указанная схема генерирования сигнала.
17. Устройство по п.16, в котором указанный физический сигнал и/или химический сигнал представляет собой звуковую волну, свет или электромагнитную волну.
18. Устройство по п.17, в котором указанный физический сигнал представляет собой электромагнитную волну и варикап используют для схемы передачи указанной электромагнитной волны.
19. Устройство по п.14, в котором указанное измерительное устройство дополнительно содержит приемник для приема указанного сигнала, генерируемого посредством указанной разрядки указанного конденсатора, когда указанный конденсатор превышает пороговое напряжение указанного беспроводного передатчика, посредством зарядки.
20. Устройство по любому из пп.11-19, в котором указанный биокатализатор, располагающийся на аноде, представляет собой фермент.
21. Устройство по п.20, в котором указанный фермент представляет собой оксидоредуктазу.
22. Устройство по п.20, в котором указанный фермент катализирует окисление глюкозы.
23. Беспроводная система, содержащая:
конденсатор, в котором аккумулируется энергия, получаемая в результате реакции между биокатализатором и субстратом, распознаваемым указанным биокатализатором;
беспроводной передатчик, который генерирует сигнал на основе разрядки указанной энергии из указанного конденсатора; и
приемник для приема указанного генерируемого сигнала.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ определения концентрации сульфидов в физических средах | 1989 |
|
SU1814065A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| WO 00/46393 A1, 10.08.2000 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| JP 2005013210 A, 20.01.2005. | |||
Авторы
Даты
2012-07-27—Публикация
2008-09-18—Подача