Область техники, к которой относится изобретение
Настоящее изобретение относится к профилактическому или терапевтическому средству для возрастной дегенерации желтого пятна, содержащему 2-фенил-1,2-бензизоселеназол-3(2Н)-он или его соль в качестве активного ингредиента.
Уровень техники
Возрастная дегенерация желтого пятна (AMD) является одной из основных причин практической слепоты в развитых странах в настоящее время и в основном поражает пожилых людей возраста 50 лет или старше. AMD является болезнью, вызванной возрастными изменениями в желтом пятне, и в общем ее классифицируют на экссудативную и атрофическую формы. Экссудативная AMD является заболеванием, при котором новые кровеносные сосуды из собственно сосудистой оболочки глаза врастают в желтое пятно у пожилых людей, и имеет место кровоизлияние или экссудативное повреждение ниже ретинального пигментного эпителия или сетчатки, и в конце концов образуется рубцовая ткань. Атрофическая AMD является заболеванием, связанным с атрофией области желтого пятна или аккумуляцией друзы. Кроме того, предшествующее повреждение, которое приводит к развитию экссудативной и атрофической AMD, в некоторых случаях, в частности, называют ранней AMD, и считается, что это повреждение является одним патологическим условием AMD.
Основным патологическим условием AMD (особенно экссудативной AMD) является хороидальное образование новых сосудов, причиной развития которых, как считается, являются возрастные изменения в макулярных ретинальных пигментных эпителиальных клетках, оболочке Бруха и хороидальных сосудах. Однако многое из патогенной причины и механизма хороидального образования новых сосудов еще не было объяснено, и ожидается дальнейшее развитие этого вопроса.
С другой стороны, 2-фенил-1,2-бензизоселеназол-3(2Н)-он (родовое название: эбселен, далее называемый "эбселеном") обладает антиокислительным действием и, как описано, и его применяют при церебральном артериосклерозе и хронической недостаточности церебрального кровообращения (непатентный документ 1 и патентный документ 1). Кроме того, описано, что эбселен применяют при кератоконъюнктивитных нарушениях, таких как "сухой" глаз или поверхностная точечная кератопатия (патентный документ 2).
В непатентном документе 2, в котором изучается фармакологическое действие эбселена на образование новых сосудов, описывается, что эбселен ингибировал индуцированное ишемией образование новых сосудов в тканях задних конечностей мышей, и в непатентном документе 3 описывается, что эбселен ингибировал индуцированное эндогенным пероксидом водорода ремоделирование сонной артерии и образование новых сосудов у трансгенных мышей p22phox.
Однако эти документы показывают действие эбселена на такие ткани, как кровеносные сосуды задних конечностей и сонные артерии. То есть эти сообщения (непатентные документы 2 и 3) предполагают действие эбселена только на ткани, другие чем глазные ткани, и не предполагают фармакологическое действие эбселена на образование новых сосудов собственно сосудистой оболочки глаза.
Кроме того, в непатентном документе 4 описывается фармакологическое действие эбселена на образование новых сосудов, однако в отличие от ранее описанных сообщений (непатентные документы 2 и 3) в данном документе описывается, что эбселен ослаблял прогрессирующее развитие микроангиопатии и частично подавлял (возвращал к норме) образование новых сосудов. В частности, в непатентном документе 4 указано, что проводили исследование с применением крыс ZDF (диабетическая модель) и что в этих моделях ингибировалась почечная васкулярная функция и уменьшалась плотность капилляров вокруг почечного канальца, однако посредством повторного введения эбселена ренальное образование новых сосудов возвращалось к норме. То есть в непатентном документе 4 описаны результаты, противоречащие ранее описанным сообщениям (непатентные документы 2 и 3) в отношении фармакологического действия на образование новых сосудов, хотя исследование проводили с применением других модельных животных и не описали или вообще не предполагали образования новых сосудов собственно сосудистой оболочки глаза.
Как описано выше, образование новых сосудов собственно сосудистой оболочки глаза привлекло внимание в качестве основного патологического условия AMD (особенно экссудативного AMD), однако, многое из механизма ее остается неизвестным. Кроме того, не имеется сообщения по исследованию фармакологического действия эбселена на образование новых сосудов собственно сосудистой оболочки глаза, в частности, не имеется сообщения по исследованию профилактического и улучшающего действия эбселена на ADM.
С другой стороны, известно также, что повреждение ретинальных пигментных эпителиальных клеток, вызванное окислительным стрессом или тому подобное, является одной из причин развития или прогрессирования AMD, и считается, что его вклад в раннюю и атрофическую AMD является огромным (непатентный документ 5). Согласно этому, считается, что защита ретинальных пигментных эпителиальных клеток от клеточного повреждения является эффективной в качестве одного из способов профилактики или терапии AMD (особенно ранней и атрофической AMD). Однако отсутствует сообщение по исследованию такого защитного действия эбселена в отношении повреждения клеток.
Патентный документ 1: JP-A-2001-261555.
Патентный документ 2: WO 2006/123676.
Непатентный документ 1: Proc. Natl. Acad. Sci. USA, 100(13), 7919-7924 (2003).
Непатентный документ 2: Circulation, 111, 2347-2355 (2005).
Непатентный документ 3: Circulation, 109, 520-525 (2004).
Непатентный документ 4: Kidney International, 66, 2337-2347 (2004).
Непатентный документ 5: Progress in Retinal and Eye Research 19(2), 205-221, 2000.
Описание изобретения Проблемы, которые должны быть разрешены изобретением
Интересным предметом являются поиски нового медицинского применения эбселена.
Способ разрешения проблем
Авторы настоящего изобретения выполнили интенсивные исследования для поиска нового медицинского применения эбселена и обнаружили, что эбселен или его соль обладает превосходным ингибирующим действием на образование новых сосудов собственно сосудистой оболочки глаза на моделях-крысах с индуцированным лазером образованием новых сосудов собственно сосудистой оболочки глаза, и таким образом настоящее изобретение было достигнуто. То есть эбселен оказывает профилактическое или улучшающее действие на AMD (особенно экссудативную AMD).
Кроме того, авторы настоящего изобретения обнаружили, что эбселен обладает защитным действием в отношении повреждения клеток в линии ретинальных пигментных эпителиальных клеток человека, индуцированного пероксидом водорода или 4-гидроксиноненалем (HNE). То есть эбселен оказывает профилактическое или улучшающее действие на AMD (особенно раннюю или атрофическую AMD). С другой стороны, не обнаружено, что кверцетин и эдаравон, в общем известные, как обладающие антиокислительной активностью, обладают таким защитным действием в отношении повреждения клеток и поэтому неожиданным открытием является тот факт, что эбселен обладает также таким действием.
То есть настоящее изобретение относится к профилактическому или терапевтическому средству для AMD, содержащему эбселен или его соль в качестве активного ингредиента. В частности, настоящее изобретение характеризуется тем, что это средство может быть профилактическим или терапевтическим средством для различных патологических состояний AMD, т.е. атрофической и экссудативной AMD и предшествующих ей повреждений (ранняя AMD).
Эбселен является конденсированным гетероциклическим соединением, представленным следующей химической структурной формулой [1]
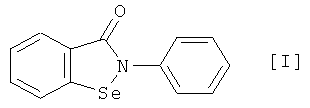
Кроме того, соль эбселена конкретно не ограничивают, пока она является фармацевтически приемлемой солью, и примеры ее включают в себя соль с неорганической кислотой, такой как хлористоводородная кислота, азотная кислота или серная кислота; и соль с органической кислотой, такой как уксусная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота или винная кислота. Эбселен может быть в форме сольвата.
В настоящем изобретении AMD включает в себя экссудативную AMD, атрофическую AMD и предшествующие им повреждения (ранняя AMD). Как описано выше, AMD является заболеванием, вызванным возрастными изменениями в желтом пятне и в основном ее классифицируют на экссудативную и атрофическую формы. Экссудативная AMD является заболеванием, при котором новые кровеносные сосуды из собственно сосудистой оболочки глаза врастают в желтое пятно у пожилых людей, и имеет место кровоизлияние или экссудативное повреждение ниже ретинального пигментного эпителия или сетчатки, и в конце концов образуется рубцовая ткань. Атрофическая AMD является заболеванием, связанным с атрофией области желтого пятна или аккумуляцией друзы.
Эбселен можно изготовить в виде отдельного препарата или комбинированного препарата добавлением фармацевтически приемлемой добавки, как необходимо, с применением широко применяемой методики.
Когда эбселен применяют для профилактики или лечения указанного выше заболевания глаз, его можно вводить пациенту перорально или парентерально. Примеры пути введения включают в себя пероральное введение, местное введение в глаза (такое как введение закапыванием, введение в конъюнктивальный мешочек, интравитреальное введение, субконъюнктивальное введение и введение ниже теноновой капсулы глазного яблока), внутривенное введение и чрескожное введение. Кроме того, его изготовляют в виде лекарственной формы, подходящей для введения вместе с фармацевтически приемлемой добавкой, если необходимо. Примеры лекарственной формы, подходящей для перорального введения, включают в себя таблетки, капсулы, гранулы и порошки, и примеры лекарственной формы, подходящей для парентерального введения, включают в себя инъекции, глазные капли, глазные мази, повязки, гели и вставки. Их можно получить с применением обычного способа, широко применяемого в данной области. Кроме того, данное соединение можно также ввести в составе препарата для внутриглазного имплантирования или препарата DDS (система для доставки лекарственного средства), такого как микросфера, другого, чем эти препараты.
Например, таблетку можно получить посредством правильного выбора и применения эксципиента, такого как лактоза, глюкоза, D-маннит, безводный гидрофосфат кальция, крахмал или сахароза; дезинтегрирующего вещества, такого как карбоксиметилцеллюлоза, кальциевая соль карбоксиметилцеллюлоза, натриевая соль кроскармеллозы, кросповидон, крахмал, частично предварительно желатинированный крахмал или слабозамещенная гидроксипропилцеллюлоза; связующее вещество, такое как гидроксипропилцеллюлоза, этилцеллюлоза, гуммиарабик, крахмал, частично предварительно желатинированный крахмал, поливинилпирролидон или поливиниловый спирт; смазывающее вещество, такое как стеарат магния, стеарат кальция, тальк, водный диоксид кремния или гидрогенизированное масло; средство для образования покрытия, такое как очищенная сахароза, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, метилцеллюлоза, этилцеллюлоза или поливинилпирролидон; корригент, такой как лимонная кислота, аспартам, аскорбиновая кислота или ментол, или тому подобное.
Инъекционный раствор можно получить посредством выбора и применения средства тоничности, такого как хлорид натрия; буфера, такого как фосфат натрия; поверхностно-активного вещества, такого как моноолеат полиоксиэтиленсорбитана; вязкого средства, такого как метилцеллюлоза; или тому подобное, когда необходимо.
Глазные капли можно получить посредством выбора и применения средства тоничности, такого как хлорид натрия или концентрированный глицерин; буфера, такого как фосфат натрия или ацетат натрия; поверхностно-активного вещества, такого как моноолеат полиоксиэтиленсорбитана, стеарат полиоксила-40 или полиоксиэтилированное гидрогенизированное касторовое масло; стабилизатора, такого как цитрат натрия или эдетат натрия; консерванта, такого как хлорид бензалкония или парабен; или тому подобное, когда необходимо. Разрешается значение pH глазных капель, если оно находится в диапазоне, который является приемлемым для офтальмического препарата, но обычно оно предпочтительно находится в диапазоне от 4 до 8. Кроме того, глазную мазь можно получить с применением широко используемого основания, такого как белый вазелин или жидкий парафин.
Имплантат можно получить пульверизацией и смешиванием биоразлагаемого полимера, такого как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксивиниловый полимер или полиакриловая кислота, вместе с настоящим соединением и прямым прессованием образовавшегося порошка. Если необходимо, можно применять эксципиент, связывающее вещество, стабилизатор или средство регуляции pH. Препарат для внутриглазной имплантации можно получить с применением биоразлагаемого полимера, такого как полимолочная кислота, полигликолевая кислота, сополимер молочной кислоты и гликолевой кислоты или гидроксипропилцеллюлоза.
Дозу эбселена можно должным образом изменять в зависимости от лекарственной формы, тяжести симптомов, возраста или массы тела пациента, нуждающегося в таком введении, медицинского заключения и тому подобное. В случае перорального введения ее обычно вводят взрослому человеку один раз или разделяют для введения несколько раз при дозе от 0,01 до 5000 мг, предпочтительно от 0,1 до 2500 мг, более предпочтительно от 0,5 до 1000 мг в день. В случае инъекции ее обычно вводят взрослому человеку один раз или разделяют для введения несколько раз при дозе от 0,0001 до 2000 мг в день. В случае глазных капель или вставки препарат, обычно содержащий активный ингредиент в количестве от 0,000001 до 10% (мас./об.), предпочтительно от 0,00001 до 1% (мас./об.), более предпочтительно, от 0,0001 до 0,1% (мас./об.), можно вводить один или несколько раз в день. Кроме того, в случае повязки, для взрослого человека можно применять повязку, содержащую активный ингредиент в количестве от 0,0001 до 2000 мг, и в случае препарата для внутриглазной имплантации в глаз взрослого человека можно имплантировать препарат для внутриглазного имплантата, содержащий активный ингредиент в количестве от 0,0001 до 2000 мг.
Благоприятные действия патента
Как будет описано ниже, когда были проведены нижеследующие фармакологические испытания, было показано, что эбселен обладает превосходным ингибирующим действием на образование новых сосудов собственно сосудистой оболочки глаза на крысиных моделях с индуцированным лазером образованием новых сосудов собственно сосудистой оболочки глаза. Кроме того, было показано, что эбселен обладает также защитным действием в отношении индуцированного пероксидом водорода повреждения клеток и индуцированного HNE повреждения клеток в линии ретинальных пигментных эпителиальных клеток человека. То есть эбселен является применимым в качестве профилактического или терапевтического средства для различных патологических состояний AMD.
Лучший способ осуществления изобретения
Ниже будут показаны результаты фармакологических испытаний и примеры препаратов. Однако эти примеры предназначены для правильного понимания настоящего изобретения, и не предполагается, что они ограничивают объем настоящего изобретения.
Фармакологическое испытание 1
Применимость эбселена оценивали с применением крысиной модели индуцированным лазером образования новых сосудов собственно сосудистой оболочки глаза.
Способ индуцированного криптоновым лазером образования новых сосудов собственно сосудистой оболочки глаза для крысиной модели
Крысе давали общую анестезию внутримышечным введением 1 мг/кг смешанного раствора 5% (мас./об.) раствора для инъекции гидрохлорида кетамина и 2% раствора для инъекции гидрохлорида ксилазина (7:1) и в глаза закапывали офтальмический раствор 0,5% (мас./об.) тропикамида и 0,5% (мас./об.) гидрохлорида фенилэфрина для индуцирования мидриаза и затем проводили фотокоагуляцию криптоновой лазерной аппаратурой для фотокоагуляции. Фотокоагуляцию проводили в задней части глазного дна у разбросанных по поверхности восьми пятнах на глаз фокусировкой на ретинальный, глубоко расположенный слой, избегая попадания на густую сеть ретинальных кровеносных сосудов (условия коагуляции: размер пятна: 100 мкм, мощность: 100 мВ, время коагуляции: 0,1 сек). После фотокоагуляции глазное дно фотографировали и подтверждали место, которое облучали лазером.
Способ введения лекарственного средства
Эбселен суспендировали в 1% (мас./об.) растворе метилцеллюлозы (полученном растворением метилцеллюлозы в очищенной воде) до получения конечной концентрации 1 мг/мл или 3 мг/мл и каждую из образовавшихся суспензий перорально вводили дважды в день при дозе 5 мг/кг или 15 мг/кг (10 мг/кг или 30 мг/кг в день), начиная за 5 дней до даты операции фотокоагуляции и в течение 12 дней, включая день операции.
Способ оценки
На 7 день после фотокоагуляции каждой крысе давали общую анестезию внутримышечным введением 1 мл/кг смешанного раствора 5% (мас./об.) раствора для инъекции гидрохлорида кетамина и 2% раствора для инъекции гидрохлорида ксилазина (7:1) и в глаза закапывали офтальмический раствор 0,5% (мас./об.) тропикамида и 0,5% (мас./об.) гидрохлорида фенилэфрина для индуцирования мидриаза и затем в хвостовую вену инъецировали 0,1 мл 10% раствора флуоресцеина и проводили фотографирование флуоресценции глазного дна. На фотографии флуоресценции глазного дна пятно, у которого не наблюдали флуоресценцию (отсутствие образования новых сосудов), оценивали как отрицательное и пятно, у которого наблюдали флуоресценцию, оценивали как положительное. Когда имелось два места фотокоагуляции, у которых наблюдали небольшую флуоресценцию, их оценивали как положительные (образование новых сосудов). Степень встречаемости (%) образования новых сосудов собственно сосудистой оболочки глаза вычисляли из числа положительных пятен относительно восьми пятен облучения лазером согласно уравнению 1 и степень ингибирования (%) оцениваемым лекарственным средством вычисляли согласно уравнению 2. Результаты оценки эбселена показаны в таблице 1. Число случаев (мышей) в каждой группе введения было 8.
Уравнение 1
Степень встречаемости (%) образования новых сосудов собственно сосудистой оболочки глаза (%) = (число положительных пятен/общее число мест фотокоагуляции) × 100
Уравнение 2
Степень ингибирования (%)=(АО-АХ)/АО×100.
АО: степень встречаемости образования новых сосудов собственно сосудистой оболочки глаза группы введения наполнителя.
АХ: степень встречаемости образования новых сосудов собственно сосудистой оболочки глаза группы введения лекарственного средства.
Обсуждение
Как видно из таблицы 1, было показано, что эбселен ингибирует образование новых сосудов собственно сосудистой оболочки глаза на крысиных моделях индуцированных лазером образования новых сосудов собственно сосудистой оболочки глаза. То есть было показано, что эбселен обладает превосходным ингибирующим действием на образование новых сосудов собственно сосудистой оболочки глаза и оказывает значительное профилактическое или улучшающее действие на AMD (особенно экссудативную AMD).
Фармакологическое испытание 2
Окислительный стресс вызывает ретинальную пигментную эпителиальную дисфункцию и, считается, что он является одной из причин развития или прогрессирования AMD (Proc. Natl. Acad. Sci. USA, 2006; 103: 11282-11287). Поэтому посредством применения клеток ARPE-19 (линии ретинальных пигментных эпителиальных клеток человека) оценивали защитное действие эбселена на индуцированное пероксидом водорода повреждение клеток. Кроме того, в то же время оценивали также действия кверцетина и эдаравона, которые являются соединениями, которые в общем известны как обладающие антиокислительной активностью, и проводили сравнительное изучение.
Экспериментальный способ
Клетки ARPE-19 засевали в 96-луночном планшет при плотности 5×10 клеток/лунку и культивировали в течение 24 часов при 37°С в атмосфере 5% CO2/95% воздуха. В качестве культуральной среды для ARPE-19 применяли DMEM/F12, содержащую 10% фетальной бычьей сыворотки, 2 мМ L-глутамин и 100 Е/мл пенициллина и 100 мкг/мл стрептомицина. Затем культуральную среду удаляли и заменяли ее культуральной средой, содержащей эбселен, кверцетин и эдаравон, или культуральной средой без добавок. В данном случае каждое соединение растворяли в ДМСО и разводили 1000-кратно культуральной средой для получения культуральной среды, содержащей каждое соединение в количестве 6,25 мкМ или 12,5 мкМ. Культуральную среду без добавок получали разведением ДМСО, не содержащего соединение, 1000-кратно культуральной средой. После культивирования клеток в течение 24 часов в условиях 37°C в атмосфере 5% CO2/95% воздуха культуральную среду удаляли и заменяли культуральной средой, содержащей пероксид водорода (250 мкМ). После дополнительного культивирования клеток в течение 24 часов в указанных выше условиях измеряли жизнеспособность клеток. При измерении применяли набор Cell Counting Kit-8 (Dojin Kagaku).
Способ оценки
Среднее значение ± стандартная ошибка (%) жизнеспособности клеток каждой группы, обработанной соединением, выражали с применением средней величины жизнеспособности необработанных клеток как 100%. Число опытов в каждой группе составляло 4.
Результаты
Защитное действие каждого соединения в отношении повреждения клеток, индуцированного пероксидом водорода, показано в таблице 2. Жизнеспособность клеток ARPE-19, обработанных пероксидом водорода, уменьшалась до 7,2% жизнеспособности клеток необработанного случая. Как видно из таблицы 2, эбселен эффективно защищал клетки от повреждения, вызванного пероксидом водорода, зависимым от концентрации способом и, в частности, при 12,5 мкМ эбселен повышал жизнеспособность клеток до 82,6%. С другой стороны, не было обнаружено, что кверцетин и эдаравон обладают защитным для клеток действием при любой концентрации.
Обсуждение
На основании приведенных выше результатов было обнаружено, что эбселен проявляет сильное защитное действие в отношении повреждения ретинальных пигментных эпителиальных клеток, вызванного пероксидом водорода. С другой стороны, ввиду того факта, что другие соединения, обладающие антиокислительной активностью, не проявляют такое действие, неожиданным открытием является тот факт, что эбселен обладает также защитным действием в отношении повреждения клеток. То есть было показано, что эбселен обладает профилактическим или улучшающим действием на AMD (особенно раннюю и атрофическую AMD).
Фармакологическое испытание 3
Известно, что реакционно-способные кислородные соединения промотируют перокисление мембранных липидов, приводящее к продуцированию HNE (Exp. Eye. Res., 2006; 83:165-175). HNE образует ковалентную связь с цистеиновой, лизиновой или гистидиновой боковой цепью белка и ингибирует нормальную функцию белка и поэтому обладает высокой цитотоксической активностью (Invest. Ophthalmol. Vis. Sci. 2007; 48:3469-3479). Описано, что HNE-модифицированный белок присутствует также в друзах ниже сетчатки и, как считается, является отложением, индуцирующим AMD, и считается, что оно является также одной из причин развития или прогресса заболевания, относящегося к ретинальному пигментному эпителиальному повреждению (Mol. Vis., 2005; 11:1122-1134, Invest. Ophthalmol. Vis. Sci, 2003; 44:3663-3668, FEBS Lett., 2002; 528:217-221). Поэтому посредством применения клеток ARPE-19 оценивали защитное действие эбселена на HNE-индуцированное повреждение клеток. Кроме того, в то же время оценивали также действия кверцетина и эдаравона, которые являются соединениями, которые в общем известны как обладающие антиокислительной активностью, и проводили сравнительное изучение.
Экспериментальный способ
Клетки ARPE-19 засевали в 96-луночном планшете при плотности 5×103 клеток/лунку и культивировали в течение 24 часов в условиях 37°C в атмосфере 5% CO2/95% воздуха. В качестве культуральной среды для ARPE-19 применяли DMEM/F12, содержащую 10% фетальной бычьей сыворотки, 2 мМ L-глутамин и 100 Е/мл пенициллина и 100 мкг/мл стрептомицина. Затем культуральную среду удаляли и заменяли культуральной средой, содержащей эбселен, кверцетин и эдаравон, или культуральной средой без добавок. В данном случае каждое соединение растворяли в ДМСО и разводили 1000-кратно культуральной средой для получения культуральной среды, содержащей каждое соединение в количестве 12,5 мкМ. Культуральную среду без добавок получали разведением ДМСО, не содержащего соединение, 1000-кратно культуральной средой. После культивирования клеток в течение 24 часов в условиях 37°C в атмосфере 5% CO2/95% воздуха культуральную среду удаляли и заменяли культуральной средой, содержащей HNE (100 мкМ). После дополнительного культивирования клеток в течение 24 часов в указанных выше условиях измеряли жизнеспособность клеток. При измерении применяли набор Cell Counting Kit-8 (Dojin Kagaku).
Способ оценки
Среднее значение ± стандартная ошибка (%) жизнеспособности клеток группы, обработанной каждым соединением, выражали посредством применения среднего значения жизнеспособности необработанных клеток как 100%. Число (опытов) случаев в каждой группе составляло 4.
Результаты
Защитное действие каждого соединения в отношении повреждения клеток, индуцированного HNE, показано в таблице 3. Жизнеспособность клеток ARPE-19, обработанных HNE, уменьшалась до 21,9% жизнеспособности клеток необработанного случая. Как видно из таблицы 3, эбселен эффективно защищал клетки от повреждения, вызванного HNE, и увеличивал жизнеспособность клеток до 92,9%. С другой стороны, не было обнаружено, что кверцетин и эдаравон обладают защитным для клеток действием.
Обсуждение
На основании приведенных выше результатов было обнаружено, что эбселен проявляет сильное защитное действие в отношении повреждения ретинальных пигментных эпителиальных клеток, вызванного HNE. С другой стороны, ввиду того факта, что другие соединения, обладающие антиокислительной активностью, не проявляют такое действие, неожиданным открытием является тот факт, что эбселен обладает также защитным действием в отношении повреждения клеток. То есть было показано, что эбселен обладает профилактическим или улучшающим действием на AMD (особенно раннюю и атрофическую AMD).
Фармакологическое испытание 4
Моделью светового повреждения является животная модель, у которой повреждение было индуцировано световым излучением в основном в фоторецепторных клетках и слое ретинальных пигментных эпителиальных клеток и которую широко применяют в основном в качестве животной модели ретинальной дегенерации (например, AMD, особенно атрофической AMD, или пигментной дегенерации сетчатки (Invest. Ophthalmol. Vis. Sci., 2005; 46:979-987)).
Способ индуцирования светового повреждения у крысиной модели
После закапывания офтальмического раствора 0,5% (мас./об.) тропикамида и 0,5% гидрохлорида фенилэфрина в глаза крысы для индуцирования мидриаза проводили обработку световыми лучами (например, освещение: 2000 лк, время освещения: 48 часов) аппаратурой для индуцирования светового повреждения, тем самым индуцируя световое повреждение.
Способ оценки
Эбселен растворяют в подходящем наполнителе, и раствор вводят в каждый глаз перед обработкой световыми лучами. После завершения световой обработки в темной комнате проводили 4-часовую адаптацию к темноте. Крысе дают общую анестезию внутримышечным введением 1 мл/кг смешанного раствора 5% (мас./об.) раствора для инъекции гидрохлорида кетамина и 2% раствора для инъекции гидрохлорида ксилазина (7:1) и в глаза для индуцирования мидриаза закапывали офтальмический раствор 0,5% (мас./об.) тропикамида и 0,5% гидрохлорида фенилэфрина. Затем снимают электроретинограмму (ERG) и а- и b-волновые амплитуды вычисляют из полученных форм волн. Вычислением степени ингибирования (%) эбселеном снижения в амплитудах а- и b-волн (повреждение фоторецепторных клеток), вызванного обработкой световыми лучами, можно оценить профилактическое или улучшающее действие эбселена на AMD (особенно атрофическую AMD). Кроме того, посредством применения глаза после измерения ERG патологически подсчитывали число ядер в наружном ядерном слое. Вычислением также степени ингибирования (%) эбселеном уменьшения числа ядер в наружном ядерном слое, вызванного обработкой световыми лучами, можно аналогично оценить профилактическое или улучшающее действие эбселена на AMD (особенно атрофическую AMD).
Примеры составов
Фармацевтические составы изобретения будут более конкретно описаны обращением к примерам составов, однако изобретение не ограничивается только этими составами.
Пример 1: глазные капли
в 100 мл
Эбселен и другие вышеуказанные ингредиенты добавляют к стерильной очищенной воде, и эти ингредиенты хорошо смешивают, тем самым получая глазные капли. Изменением добавляемого количества эбселена можно получить глазные капли, содержащие эбселен при концентрации 0,05% (мас./об.), 0,1% (мас./об.), 0,5 (мас./об.) или 1% (мас./об.).
Пример 2: глазная мазь
в 100 г
Эбселен добавляют к равномерно расплавленному белому вазелину и жидкому парафину, эти ингредиенты хорошо смешивают и образовавшуюся смесь постепенно охлаждают, тем самым получая глазную мазь. Изменением добавляемого количества эбселена можно получить глазную мазь, содержащую эбселен при концентрации 0,05% (мас./об.), 0,1% (мас./мас.), 0,5 (мас./мас.), 1% (мас./мас.) или 3% (мас./мас.).
Пример 3: таблетка
в 100 мг
Эбселен и лактозу смешивают в смесителе, к ним добавляют кальциевую соль карбоксиметилцеллюлозы и гидроксипропилцеллюлозы и образовавшуюся смесь гранулируют. Полученные гранулы сушат с последующей сортировкой по размеру гранул. Затем добавляют стеарат магния и смешивают с сортированными по размерам гранулами и образовавшуюся смесь таблетируют таблетирующей машиной. Изменением добавляемого количества эбселена можно получить таблетку, содержащую эбселен в количестве 0,1 мг, 10 мг или 50 мг в 100 мг таблетки.
Пример 4: инъекция
в 10 мл
Эбселен и хлорид натрия растворяют в стерильной очищенной воде, тем самым получая инъекцию. Изменением добавляемого количества эбселена можно получить инъекцию, содержащую эбселен в количестве 0,1 мг, 10 мг или 50 мг в 10 мл инъекции.
Промышленная применимость
Эбселен обладает превосходным ингибирующим действием на образование новых сосудов собственно сосудистой оболочки глаза, а также обладает защитным действием в отношении вызываемого пероксидом водорода повреждения клеток и вызываемого HNE повреждения клеток в линии ретинальных пигментных эпителиальных клеток человека. Согласно этому, эбселен является применимым в качестве профилактического или терапевтического средства для различных патологических состояний возрастной дегенерации желтого пятна.
Предложено: профилактическое или терапевтическое средство для применения при возрастной дегенерации желтого пятна, содержащее 2-фенил-1,2-бензизоселеназол-3(2Н)-он (эбселен) или его соль в качестве активного ингредиента, его применение для производства профилактического или терапевтического средства того же назначения, соответствующие способы профилактики или терапии возрастной дегенерации желтого пятна (варианты). Показано превосходное ингибирующее действие 2-фенил-1,2-бензизоселеназол-3(2Н)-она или его соли на образование новых сосудов в собственно сосудистой оболочке глаза, а также защитное действие в отношении повреждения ретинальных пигментных эпителиальных клеток. Поэтому соединение может применяться в качестве профилактического или терапевтического средства при возрастной дегенерации желтого пятна. 5 н. и 3 з.п. ф-лы, 3 табл., 4 пр.
1. Профилактическое или терапевтическое средство, применяемое при возрастной дегенерации желтого пятна, содержащее 2-фенил-1,2-бензизоселеназол-3(2Н)-он или его соль в качестве активного ингредиента.
2. Профилактическое или терапевтическое средство по п.1, путем введения которого является введение закапыванием, интравитреальное введение, субконъюнктивальное введение, введение в конъюнктивальный мешочек, введение ниже теноновой капсулы глазного яблока или пероральное введение.
3. Профилактическое или терапевтическое средство по п.1, лекарственной формой которого являются глазные капли, глазная мазь, имплантат, повязка, инъекция, таблетка, тонкоизмельченные гранулы или капсула.
4. Способ профилактики или терапии возрастной дегенерации желтого пятна, включающий введение фармакологически эффективного количества 2-фенил-1,2-бензизоселеназол-3(2Н)-она или его соли пациенту.
5. Способ профилактики или терапии возрастной дегенерации желтого пятна, включающий введение фармакологически эффективного количества 2-фенил-1,2-бензизоселеназол-3(2Н)-она или его соли пациенту посредством введения закапыванием, интравитреального введения, субконъюнктивального введения, введения в конъюнктивальный мешочек, введения ниже теноновой капсулы глазного яблока или перорального введения.
6. Способ профилактики или терапии возрастной дегенерации желтого пятна, включающий введение пациенту глазных капель, глазной мази, имплантата, наложение повязки, введение инъекции, таблетки тонкоизмельченных гранул или капсулы, содержащей фармакологически эффективное количество 2-фенил-1,2-бензизоселеназол-3(2Н)-она или его соли.
7. Применение 2-фенил-1,2-бензизоселеназол-3(2Н)-она или его соли для изготовления профилактического или терапевтического средства, применяемого при возрастной дегенерации желтого пятна.
8. Применение по п.7, где лекарственной формой профилактического или терапевтического средства являются глазные капли, глазная мазь, имплантат, повязка, инъекция, таблетка, тонкоизмельченные гранулы или капсула.
| NOWAK JZ | |||
| Age-related macular degeneration (AMD): pathogenesis and therapy | |||
| Pharmacol Rep | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ получения твердой лекарственной формы | 1988 |
|
SU1834657A3 |
| US 4784994 A, 15.11.1988 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| KHATRI JJ | |||
| et al | |||
| Vascular oxidant stress enhances progression and angiogenesis of | |||
Авторы
Даты
2012-09-10—Публикация
2008-05-23—Подача