Изобретение относится к медицине, в частности к хирургии, и может быть использовано для лечения абсцессов.
Абсцессы брюшной полости относятся к тяжелым гнойным осложнениям абдоминальной хирургии и сопровождаются летальностью от 10,5 до 26,1% (Тимошин А.Д., Шестаков А.Л., Юрасов А.В. Малоинвазивные вмешательства в абдоминальной хирургии. - М.: Триада - X, 2003 г., с.101-102).
Это обусловлено в первую очередь трудностями проведения качественной санации полости абсцесса и адекватной антибактериальной терапии. Полость абсцесса изнутри покрыта плотным слоем фибринозных наложений и гнойно-некротических масс, которые являются убежищем и питательным субстратом для бактерий, препятствуют действию лекарственных препаратов и снижают эффективность лечения. Также в полости длительно существующего абсцесса практически всегда определяются госпитальные штаммы бактерий, которые устойчивы к действию большинства антибактериальных средств и антисептиков. Все это удлиняет продолжительность лечения, снижает качество жизни, увеличивает вероятность возникновения таких осложнений, как сепсис и перитонит, и обуславливает необходимость в совершенствовании существующих и разработке новых способов лечения больных абсцессом брюшной полости.
Описан способ видеоэндоскопического пункционно-дренажного лечения абсцессов патент РФ 2246324. Проводят пункцию полости гнойника под контролем ультразвука, в полость абсцесса вводят лапароскоп, подсоединяемый к монитору для установки дренажей. Полость абсцесса заполняют на 2/3 объема озонированным раствором и барботируют озоново-кислородной смесью в течение 2-3 минут со сменой раствора до получения прозрачности. Стенки опорожненной полости обрабатывают 2-3 минуты ламинарным потоком воздуха, нагретого до температуры 38-40°C, под давлением 1-1,5 атм, с расстояния 3-4 см. После этого стенки полости облучают некогерентным красным светом по 2-3 минуты на каждый участок с расстояния 2-3 см. Недостатки: сложное многоэтапное лечение с использованием различных видов дополнительной аппаратуры, привлечение к лечебному процессу специалистов по эндоскопии и физиотерапии.
В патенте РФ №2195970 описан "Способ внутриполостного дренирования и санации патологического очага", заключающийся в лазерном облучении патологического очага низкоинтенсивным лазерным излучением в течение 4-10 суток ежедневно двукратно по 20-30 минут. Также проводят санацию патологического очага последовательно озонированным раствором Рингера и активированной электрохимическим методом водопроводной питьевой водой в виде анолита два раза в сутки в течение 7-14 дней. "Способ лечения гнойных заболеваний печени", патент РФ №2215562, предусматривает взятие из подключичной вены больного крови, лазерное облучение ее, пропускание крови через перфузионный контур, включающий гемосорбцию и малопоточную мембранную оксигенацию, и возвращение крови в портальную вену. Недостатками указанных выше способов являются необходимость наличия специальной аппаратуры, сложность выполнения, травматичность, возможность дополнительного инфицирования брюшной полости, длительность и недостаточная эффективность лечения.
В комплексном лечении гнойных хирургических инфекций в последнее время достаточно широко применяют фаготерапию. Способ лечения послеоперационных интраабдоминальных абсцессов, предусматривающий включение в послеоперационном периоде в комплекс терапии местное введение бактериофага, который используется для повышения эффективности лечения (Курбангалеев С.М. Гнойная инфекция в хирургии. - М.: Медицина, 1985 г., с.106-109). "Средство для лечения гнойно-воспалительных заболеваний", патент РФ №2105544, на основе очищенного концентрата пиобактериофага комбинированного, содержащего стафилококковый, стрептококковый, коли, протейный, псевдомонас аэругиноза монофаги, хинозол, альбумин, безводный ланолин и масло растительное, или же описанный в патенте РФ №2144368 "Препарат для лечения гнойно-воспалительных заболеваний", содержащий очищенный концентрат стафилококкового или стрептококкового, или протейного, или коли, или псевдомонас аэругиноза, или их смеси бактериофага и целевую добавку.
В патенте РФ 2243780, «Способ лечения послеоперационных абсцессов брюшной полости», проводят общепринятую медикаментозную терапию, при этом в первые один-два дня после операции в курс лечения дополнительно назначают химопсин, который вводят местно 2-3 раза в дневное время суток в концентрации 0,5-1,0 мг на 1 мл 10%-го раствора натрия хлорида с экспозицией 1,5-2 часа в количестве от 1/4 до 1/3 объема удаленного из полости абсцесса гноя, после чего в курс лечения включают бактериофаг, который при суточной дозе не более 200 мл вводят местно 2 раза в дневное время суток с экспозицией 1,5-2 часа в количестве от 1/10 до 1/5 объема удаленного из полости абсцесса гноя, вид бактериофага выбирают в соответствии с результатами бактериологического исследования содержимого полости абсцесса, курс лечения составляет 6-9 дней.
Однако, несмотря на некоторое повышение эффективности медикаментозной терапии, область применения указанных препаратов при лечении абсцессов ограничена, а лечение продолжительно, также применение бактериофага возможно лишь после определения вида возбудителя - минимальное время исследования 5-7 дней.
Наиболее близким по технической сущности и принятым в качестве прототипа является способ пункционно-дренажного лечения абсцессов под контролем УЗИ (А.Ф.Черноусов, А.Д.Тимошин, В.Ю.Мишин, Ю.И.Яшков. «Пункционно-дренажные методы лечения в абдоминальной хирургии», Анналы хирургии. №2, 1997, с.42-47), заключающийся в пункции и дренировании гнойной полости одним или несколькими дренажами, в зависимости от ее объема, с промыванием антибиотиками и антисептиками. Недостатки: данный метод не дает возможности качественной обработки стенок полости, из-за образования антибиотико-устойчивых форм бактерий приходиться менять препарат каждые 5 дней.
Проблема лечения абсцессов не перестает быть актуальной, несмотря на успехи клинической медицины и фармакологической науки, поскольку вопросы эффективного влияния на все фазы воспаления решаются не всегда успешно. Имеется множество антибактериальных и антисептических средств, однако существующие средства не способны стимулировать в достаточной степени процессы регенерации, поскольку в настоящее время изменилась структура возбудителей гнойных осложнений и обычно используемые препараты не обладают необходимой антимикробной активностью, также из-за образования полиантибиотикорезистентных штаммов бактерий приходиться постоянно менять препарат.
Наночастицы меди проявляют ярко выраженную биологическую активность, в том числе бактериостатическое и бактерицидное действия. Наночастицы меди обладают многосторонним действием на бактериальную клетку. В частности установлено, что после обработки клеток медью происходит утечка из них катионов К+. Ионы меди ингибируют трансмембранный транспорт Na+ и Са++, подавляют деятельность фермента, обеспечивающего кислородный обмен у простейших микроорганизмов болезнетворных бактерий, вирусов и грибков. Разобщают процессы окисления и окислительного фосфорилирования в микробных клетках, в результате чего клетка гибнет. Имеются данные, свидетельствующие об образовании комплексов нуклеиновых кислот с тяжелыми металлами, вследствие чего нарушается стабильность ДНК и, соответственно, жизнеспособность бактерий. Известно ранозаживляющее действие наночастиц меди, железа и цинка, полученных методом высокотемпературной конденсации (Н.Н.Глущенко и др., 2010). Наночастицы меди в отличие от антибиотиков не вызывают селекции резистентных штаммов, что позволяет в дальнейшем рекомендовать для использования при лечении гнойных заболеваний, вызванных полиантибиотикорезистентными штаммами.
Задачей изобретения является разработка способа санации абсцессов антисептическим средством, эффективно подавляющим рост патогенных микроорганизмов, к которому ни одна бактерия или вирус не образуют устойчивых форм, тем самым не вызывая селекции резистентных штаммов микроорганизмов.
Технический результат заключается в возможности обработки полости абсцессов суспензией наночастиц, повышение качества санации полости абсцесса.
Определение эффективной антибактериальной концентрации суспензии наночастиц меди проводили in vitro в отношении клинического штамма Staphylococcus aureus с лабораторным шифром №92. Из наночастиц меди, размер которых равен 40-80 нм, готовили суспензию в физиологическом растворе хлорида натрия, создавая концентрации 1000, 100, 10 и 1 мкг/мл. Микробная нагрузка составляла 3×104 микробных тел/мл (по стандарту мутности МакФарланда). Сразу и через 1, 2, 3 часа по мере культивирования делали мерный высев (по 0,1 мл) на чашки с мясо-пептонным агаром, которые инкубировали при 37°C в условиях постоянного перемешивания со скоростью 50 оборотов в минуту. Через 24 часа подсчитывали количество выросших колоний. При проведении статистической обработки руководствовались методикой определения среднего квадратичного отклонения найденных в опыте значений, предложенной И.П.Ашмариным и А.А.Воробьевым.
Как видно из данных табл.1, во всех опытных вариантах полученные количества колоний сразу после посева соответствовали ожидаемым значениям. При концентрации ультрадисперсного порошка меди 1000 и 100 мкг/мл по мере культивирования (1, 2 и 3 ч) отмечалось резкое снижение количества клеток опытного штамма, о чем свидетельствует отсутствие колоний на чашках при росте в виде газона в контрольном варианте. Подобные изменения отмечены и при концентрации меди 10 мкг/мл. Очевидно, что концентрация 1 мкг/мл не оказывала влияния на рост опытной культуры.
Создание абсцесса печени у лабораторных крыс осуществляли следующим образом: интрапаренхиматозно вводили через подключичный катетер 70% раствора этилового спирта. Через сутки в установленный в паренхиме печени катетер вводили 2 млн КОЕ в 1 мл стафилококкового гноя. К 7-10 суткам формировался абсцесс печени (патент РФ №2318248).
Способ осуществляется следующим образом.
Белой крысе с моделированным абсцессом ежедневно через установленный дренаж аспирируют содержимое, санацию полости осуществляют физиологическим раствором хлорида натрия до получения прозрачной жидкости, после чего полость заполняют суспензией наночастиц меди в физиологическом растворе хлорида натрия концентрацией 100 мкг/мл с экспозицией 30 мин и эвакуируют суспензию.
Оценка результатов лечения производили на 3, 5, 7, 10, 14, 30 сутки. Животных выводили из опыта введением летальных доз гексенала внутриплеврально. Выполняли гистологическое исследование кусочков ткани печени.
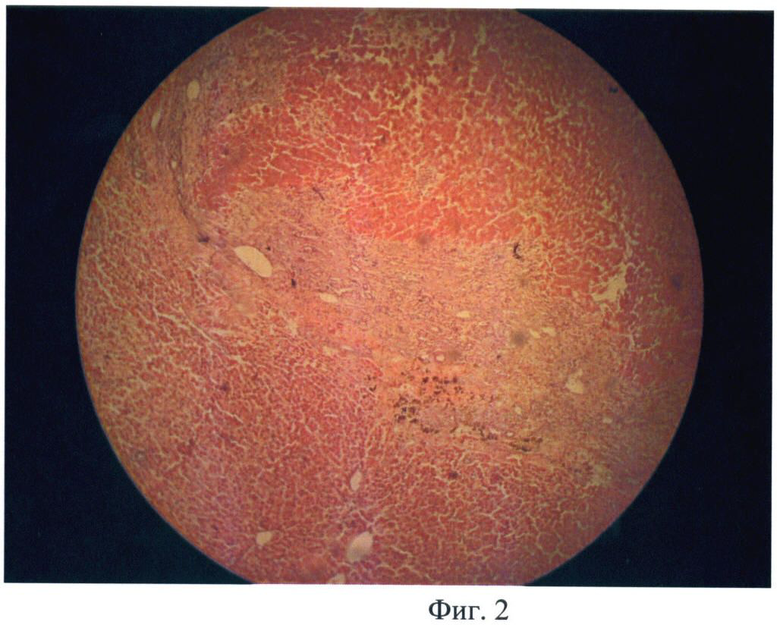
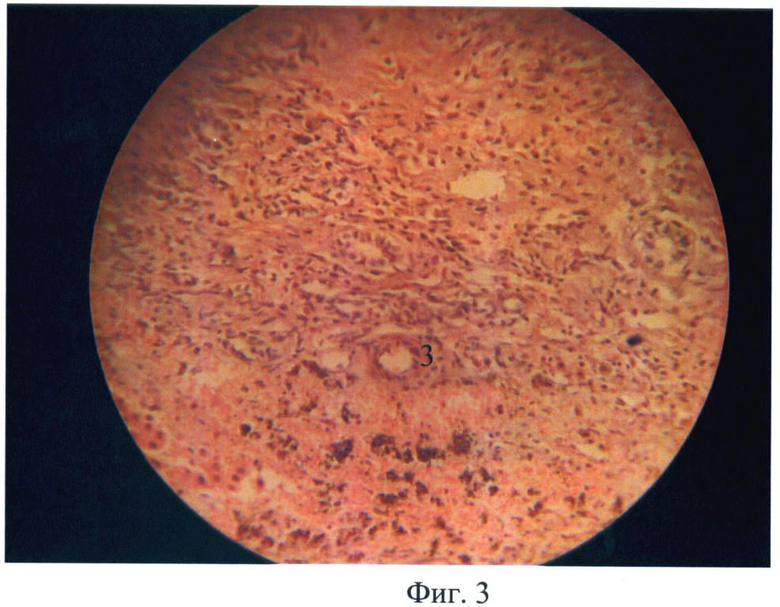
На Фиг.1 - микрофотография гистологического препарата (окраска гематоксилин-эозин, увеличение 200), где к третьим суткам вокруг полости формируется слабовыраженная соединительнотканная капсула 1, в прилежащей ткани печени определяется диффузная лейкоцитарная инфильтрация 2 с умеренным количеством дегенеративных форм гепатоцитов. К пятым суткам лечения формируется грануляционная ткань в зоне дефекта печени, инфильтрированная нейтрофилами и макрофагами. Отмечается пролиферация гепатоцитов за счет увеличения доли многоядерных гепатоцитов. На - Фиг.2 микрофото, где к седьмым суткам полость абсцесса не определяется, в данном месте имеются очаги лимфоцитарной и гистоцитарной инфильтрации с умеренным количеством фибробластов, отделяемого из дренажа для проведения микробиологического исследования не получено. На четырнадцатые сутки на месте абсцесса отмечается скопление беспорядочно расположенных гепатоцитов. На Фиг.3 - микрофото, где к тридцатым суткам очаги некрозов и лейкоцитарной инфильтрации отсутствуют, многоядерные гепатоциты формируют отдельные участки с дольками правильной структуры 3.
В результате применения суспензии наночастиц меди для лечения абсцесса отмечалось более раннее очищение полости абсцесса от возбудителя, о чем свидетельствует отсутствие роста колоний микроорганизма к седьмым суткам, к тридцатым суткам санации абсцессов печени в эксперименте в морфологической картине очаги некроза и лейкоцитарной инфильтрации отсутствуют, многоядерные гепатоциты, на отдельных участках регенерата печени гепатоциты формируют дольки правильной структуры.
В результате применения традиционных методик санации (5% раствором хлоргексидина биглюконата) абсцессов печени в эксперименте полость абсцесса очищается от возбудителя лишь к четырнадцатым суткам (при обработке наночастицами меди к седьмым суткам), в морфологической картине к тридцатым суткам дефект печени замещается соединительнотканным регенератом, в прилегающей паренхиме сохраняются очаги лейкоцитарной инфильтрации (Олимов С.С. «Низкоинтенсивное лазерное облучение и озон-ультразвуковая кавитация абсцессов печени и околопеченочных пространств», 2008).
Способ иллюстрируется следующим примером.
ПРИМЕР.
Лабораторной белой крысе с моделированным абсцессом ежедневно через катетер аспирировали содержимое абсцесса, санировали гнойную полость физиологическим раствором хлорида натрия до получения прозрачной жидкости, затем полость заполняли суспензией наночастиц меди в физиологическом растворе хлорида натрия концентрацией 100 мкг/мл с экспозицией 30 мин, после чего эвакуировали суспензию. На седьмые сутки эксперимента отделяемое по дренажу отсутствовало, последний удаляли. На тридцатые сутки животное выводили из эксперимента введением летальных доз гексенала внутриплеврально. Выполняли гистологическое исследование ткани печени. На месте абсцесса отсутствуют очаги некрозов и лейкоцитарной инфильтрации, многоядерные гепатоциты формируют отдельные участки с дольками правильной структуры.
Таким образом, в опытах с применением суспензии наночастиц меди для санации полости абсцесса отмечается более ранняя ликвидация возбудителя, более выраженная морфологическая картина регенерации печени, нормализация печеночной паренхимы в более короткие сроки, в то время как применение традиционной санации гнойников показали поздние сроки очищения полости от возбудителя, более длительное сохранение в печени воспалительно-дистрофических изменений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ АБСЦЕССОВ В ЭКСПЕРИМЕНТЕ | 2012 |
|
RU2475251C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ МЕСТНОГО ОТГРАНИЧЕННОГО ПЕРИТОНИТА В ЭКСПЕРИМЕНТЕ | 2023 |
|
RU2834555C1 |
| Способ комбинированного лечения местного отграниченного перитонита в эксперименте | 2023 |
|
RU2822708C1 |
| Способ комбинированного лечения гнойного мастита в эксперименте | 2021 |
|
RU2781245C1 |
| СПОСОБ ЛЕЧЕНИЯ АБСЦЕССОВ МЯГКИХ ТКАНЕЙ В ЭКСПЕРИМЕНТЕ | 2016 |
|
RU2639595C1 |
| Способ лечения инфекции, связанной с оказанием медицинской помощи, вызванной возбудителем или возбудителями с множественной лекарственной устойчивостью | 2017 |
|
RU2664681C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ АБСЦЕССОВ БРЮШНОЙ ПОЛОСТИ | 2004 |
|
RU2243780C1 |
| СПОСОБ ЛЕЧЕНИЯ ОТГРАНИЧЕННЫХ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ И ПЛЕВРЫ СТАФИЛОКОККОВОЙ ЭТИОЛОГИИ | 2000 |
|
RU2192880C2 |
| Способ моделирования отграниченного острого гнойного мастита в эксперименте | 2021 |
|
RU2772397C1 |
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ (ВАРИАНТЫ), ШТАММЫ БАКТЕРИОФАГОВ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ | 2015 |
|
RU2628312C2 |
Изобретение относится к области медицины. Способ включает ежедневную санацию полости абсцесса, эвакуацию санирующей жидкости. Затем полость абсцесса заполняют суспензией наночастиц меди в физиологическом растворе хлорида натрия концентрацией 100 мкг/мл, с экспозицией 30 мин, которую затем эвакуируют. Способ обеспечивает быстрое и эффективное подавление роста патогенных микроорганизмов в полости абсцесса, ускоряет регенерацию печени, нормализацию печеночной. 3 ил., 1 пр.
Способ лечения абсцессов в эксперименте, включающий ежедневную санацию полости абсцесса, отличающийся тем, что после эвакуации санирующей жидкости полость абсцесса заполняют суспензией наночастиц меди в физиологическом растворе хлорида натрия концентрацией 100 мкг/мл, с экспозицией 30 мин, которую затем эвакуируют.
| ЗАТОЛОКИН В.Д | |||
| и др | |||
| Водные дисперсии оксидных наноструктур металлов при местном лечении раневых процессов | |||
| - Ученые записки орловского государственного университета, научный журнал, Орел, 2008, №2, с.126-128 | |||
| БАБУШКИНА И.В | |||
| Наночастицы металлов в лечении экспериментальных гнойных ран | |||
| - Саратовский научно-медицинский журнал, 2011, т.7, |
Авторы
Даты
2012-09-10—Публикация
2011-07-28—Подача