Настоящее изобретение относится к новому материалу на основе кремниевого золя, используемому в качестве исходного материала для изготовления обладающих улучшенными свойствами биологически расщепляющихся и/или рассасывающихся силикагелевых материалов, а также к способу изготовления и применению подобных силикагелевых материалов. Кроме того, изобретение относится к биологически расщепляющимся и/или биологически рассасывающимся материалам из силикагелевых волокон.
Известны многочисленные попытки создания биологически расщепляющихся и/или биологически рассасывающихся материалов, предназначенных для использования в самых разных сферах медицины и медицинской техники. Вместе с тем постоянно растет уровень предъявляемых к указанным материалам требований, которые прежде всего касаются их биологической совместимости, биологической эффективности и токсикологических свойств.
Рассасывающиеся силикагели известны из уровня техники. Так, например, в немецкой заявке на патент DE 19609551 C1 описаны биологически расщепляющиеся и рассасывающиеся волокна. Подобные волокна могут быть изготовлены с помощью золь-гель технологии, в соответствии с которой из прядильной массы вытягивают нити, при необходимости подвергаемые последующей сушке. Прядильная масса содержит одно или несколько частично или полностью гидролитически конденсированных соединений кремния, образующихся в результате гидролитической конденсации мономеров общей формулы SiX4. Недостаток предлагаемых в цитируемой заявке волокон состоит в том, что их испытание на цитотоксичность при расщеплении, осуществляемом непосредственно по завершении процесса прядения, не приводит к оптимальным результатам, в связи с чем указанные волокна следует считать в определенной степени цитотоксичными. Подобная токсичность волокон, проявляющаяся при их применении в медицине или медицинской технике, например в сфере заживления ран, как правило, является нежелательной. Кроме того, предлагаемый в цитируемой заявке способ изготовления волокон страдает недостатком, состоящим в том, что смесь, образующаяся на стадии гидролитической конденсации после удаления растворителя, является многофазной, и для удаления твердого вещества приходится осуществлять ее фильтрование. Помимо этого, вследствие образования твердой фазы и необходимости фильтрования теряют значительную часть пригодного для прядения золя. В соответствии с предлагаемым в цитируемой заявке способом не удается также надежно предотвращать происходящее во время созревания образование довольно значительного количества твердой фазы, прежде всего гелеобразование. Подобное образование твердой фазы обусловливает дополнительное сокращение количества пригодной для прядения зольмассы.
Независимо от этого было обнаружено, что предлагаемые в настоящем изобретении волокна и нетканые материалы обладают улучшенной способностью заживлять раны. Кроме того, обнаружено, что предлагаемые в изобретении волокна и нетканые материалы особенно пригодны для применения в качестве опорных структур для клеток.
В основу настоящего изобретения была положена задача предоставить новый материал на основе кремниевого золя, используемый для изготовления биологически расщепляющихся и/или биологически рассасывающихся силикагелевых материалов. Другая задача настоящего изобретения состояла в том, чтобы предложить биологически расщепляющиеся и/или биологически рассасывающиеся силикагелевые материалы, которые отличаются улучшенной цитотоксичностью и/или способностью заживлять раны. Кроме того, задача настоящего изобретения состояла в том, чтобы предложить улучшенные опорные структуры для клеток, предназначенные, например, для изготовления имплантатов кожи, хрящей и костей in-vitro.
Указанные выше задачи решаются с помощью материала на основе кремниевого золя по пункту 1 формулы изобретения. Предлагаемый в изобретении материал на основе кремниевого золя может быть изготовлен следующим образом:
a) при необходимости в присутствии водорастворимого растворителя в течение по меньшей мере 16 часов при температуре от 0 до 80°C и начальном показателе pH от 0 до ≤7 осуществляют кислотно катализируемую реакцию гидролитической конденсации одного или нескольких соединений кремния формулы (I):
 ,
,
в которой остатки X, одинаковые или разные, означают гидрокси, водород, галоген, амино, алкокси, ацилокси, алкилкарбонил и/или алкоксикарбонил и являются производными алкильных остатков, представляющих собой при необходимости замещенные неразветвленные, разветвленные или циклические остатки с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода, которые могут быть прерваны атомами кислорода или серы или аминогруппами,
b) путем последующего упаривания формируют однофазный раствор, вязкость которого, измеренная при скорости сдвига 10 с-1 и температуре 4°C, составляет от 0,5 до 2 Па·с,
c) полученный раствор затем охлаждают и
d) подвергают кинетически контролируемому созреванию, в результате которого образуется гомогенный однофазный золь.
На стадии a) используют одно или несколько разных соединений кремния формулы (I):

в которой остатки X, одинаковые или разные, означают гидрокси, водород, галоген, амино, алкокси, ацилокси, алкилкарбонил и/или алкоксикарбонил и являются производными алкильных остатков, представляющих собой при необходимости замещенные неразветвленные, разветвленные или циклические остатки с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода, которые могут быть прерваны атомами кислорода или серы или аминогруппами.
В предпочтительной форме исполнения изобретения X в формуле (I) означает при необходимости замещенный неразветвленный, разветвленный и/или циклический алкоксильный остаток с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода. Остаток X в формуле (I) особенно предпочтительно означает при необходимости замещенный неразветвленный и/или разветвленный алкоксильный остаток с 1-5 атомами углерода. Кроме того, X в формуле (I) особенно предпочтительно означает замещенный, предпочтительно незамещенный, неразветвленный и/или разветвленный алкоксильный остаток с 2-3 атомами углерода, например, такой, как этокси, N-пропокси и/или изопропокси.
Согласно изобретению для осуществления предлагаемой в изобретении гидролитической конденсации в качестве соединения кремния еще более предпочтительно используют тетраэтоксисилан. В качестве водорастворимого растворителя предпочтительно можно использовать этанол или смесь этанола с водой. При этом отношение соединения кремния к этанолу может составлять ≥1:1.
В предпочтительной форме исполнения изобретения начальное значение показателя pH, которому соответствует диапазон от 0 до ≤7, предпочтительно от 2 до 5, устанавливают посредством азотнокислой воды. Однако для осуществления настоящего изобретения можно использовать также другие кислые смеси и/или растворы, пригодные для местного высвобождения монооксида азота (NO) или диоксида азота (NO2). Речь при этом идет, например, о кислых смесях и/или растворах, которые в содержащей молекулярный кислород физиологической среде ферментативно (посредством нитроксид-синтазы) генерируют монооксид азота, в свою очередь, быстро превращающийся в организме в диоксид азота, или об органических нитратах, соответственно нитроэфирах (так называемых донорах монооксида азота), например этилнитрате, выделяющих NO в присутствии органической нитратредуктазы. Для подобного ферментативного высвобождения монооксида азота требуется присутствие тиольных групп (цистеина).
Таким образом, согласно изобретению для установления необходимого показателя pH (в диапазоне от слабокислого до среднекислого) помимо разбавленной азотной кислоты можно использовать также в качестве субстрата для нитроксид-синтазы водный или спиртовый (особенно предпочтительно разбавленный этанолом водный) раствор физиологически совместимой кислоты (например, лимонной, янтарной, винной, уксусной или аскорбиновой кислоты) и по меньшей мере одной эссенциальной аминокислоты (например, особенно предпочтительно L-аргинина, а также L-валина, L-лейцина, L-изолейцина, L-фениланилина, L-тироксина, L-метионина, L-бетаина или L-триптофана) или неэссенциальной аминокислоты (например, L-гутамина, L-глутаминовой кислоты, L-аспарагина, L-аспарагиновой кислоты, L-цистеина, L-глицина, L-аланина, L-пролина, L-гистидина или L-тирозина).
В соответствии с предпочтительной формой исполнения изобретения реакцию гидролитической конденсации реализуют при молярном соотношении между соединением кремния и азотнокислой водой, составляющем от 1:1,7 до 1:1,9, особенно предпочтительно от 1:1,7 и 1:1,8. При этом азотнокислую воду можно использовать в виде 0,01 Н азотной кислоты.
Гидролитическую конденсацию осуществляют в течение промежутка времени, составляющего, по меньшей мере, 16 часов, предпочтительно, по меньшей мере, 18 часов, при температуре от 0 до 80°C, предпочтительно от 0 до 78°C, особенно предпочтительно от 20 до 60°C, еще более предпочтительно в примерном интервале от 20 до 50°C, и, например, в случае использования предлагаемых в изобретении материалов для лечения ран, при комнатной температуре (то есть примерно от 20 до 25°C) или при температуре около 37°C.
В предпочтительной форме исполнения изобретения гидролиз можно осуществлять в течение промежутка времени, составляющего, по меньшей мере, 16 часов, предпочтительно, по меньшей мере, от 18 часов до 4 недель. Длительность гидролиза предпочтительно составляет от 24 часов до 18 дней, особенно предпочтительно от 3 до 8 дней. Неожиданно было обнаружено, что в случае длительности гидролитической конденсации, увеличенной по сравнению с обычной длительностью протекания этой реакции при комнатной температуре, которая не превышает нескольких часов, в результате реализуемого на стадии b) удаления растворителя может быть сформирован гомогенный однофазный раствор, который не требует фильтрования перед реализуемым на стадии d) созреванием.
Первичную реакцию гидролитической конденсации предпочтительно осуществляют в периодическом режиме в снабженной мешалкой емкости, соответственно круглодонной колбе. В указанные резервуары предпочтительно загружают соединение кремния формулы (I) (например, тетраэтоксисилан) и растворитель (например, этанол). Затем осуществляют медленную подачу кислоты предпочтительно в виде 0,01 Н азотной кислоты (например, из расчета 0,01 моль HNO3 на моль тетраэтоксисилана). В связи с повышенной концентрацией кислоты в реакционной смеси реакция гидролитической конденсации протекает с высокой скоростью, и содержимое резервуара разогревается до температуры около 40°C, пока в ходе реакции (то есть на стадии (a)) температура не станет снижаться вследствие естественного охлаждения до температуры окружающей среды, соответственно теплоносителя.
В предпочтительной форме исполнения изобретения удаление водорастворимого растворителя (например, этанола, воды) на стадии (b) осуществляют в закрытом аппарате с возможностью перемешивания (предпочтительно в ротационном испарителе и/или в емкости с мешалкой) при одновременном удалении растворителя (воды, этанола), реализуемом путем его испарения при давлении от 1 до 1013 мбар, предпочтительно менее 600 мбар, при необходимости с непрерывной подачей от 1 до 8 м3/ч (предпочтительно от 2,5 до 4,5 м3/ч) химически инертного газа-носителя, осуществляемой с целью снижения парциального давления испаряющихся компонентов, при реакционной температуре от 30 до 90°C, предпочтительно от 60 до 75°C, более предпочтительно от 60 до 70°C, и предпочтительно при осторожном перемешивании реакционной системы мешалкой, вращающейся со скоростью до 80 об/мин (предпочтительно от 20 до 60 об/мин), пока вязкость смеси не окажется в интервале от 0,5 до 30 Па·с, предпочтительно в интервале от 0,5 до 2 Па·с, особенно предпочтительно около 1 Па·с (вязкость измеряют при 4°C и скорости сдвига 10 с-1).
Согласно изобретению термин «поток газа-носителя» используют для обозначения газового потока, который поступает в газовый объем над жидкой фазой реакционной системы. При этом для поддержания постоянного давления в реакционном сосуде из него следует выводить газообразный объемный поток, который состоит как из газа-носителя, так и из подлежащего(их) испарению компонента(ов). Происходящее вследствие этого снижение парциального давления подлежащего(их) испарению компонента(ов), то есть уменьшение его (их) концентрации в газовом объеме реактора, обусловливает увеличение движущей силы, способствующей испарению растворителя на поверхности жидкости.
В соответствии с особенно предпочтительной формой исполнения изобретения поток газа-носителя распределяют посредством надлежащего устройства для распределения газа, которое устанавливают в газовом объеме реактора таким образом, чтобы можно было обеспечить достаточно полную замену газа-носителя вблизи поверхности жидкости без непосредственного конвекционного обтекания последней газом-носителем. Конвекционное обтекание поверхности жидкости газом-носителем в наихудшем случае может приводить к нежелательному гелеобразованию. Устройства для распределения газа, которые можно использовать для реализации данной формы исполнения изобретения, известны специалистам.
По мере сопровождаемого повышением вязкости протекания реакции/полимеризации происходит смещение фазового равновесия с одновременным постепенным снижением соответствующего равновесного давления растворителя в паровой фазе. При снижении равновесного давления до величины, соответствующей общему давлению в газовой фазе, испарение растворителя прекращается.
В соответствии с этим с целью дальнейшего испарения растворителя в оптимальном варианте необходимо снижать давление, надлежащим образом изменять расход газа-носителя и/или повышать температуру.
В предпочтительной форме исполнения изобретения варьируют во времени, по меньшей мере, один из следующих технологических параметров: давление, расход газа-носителя и/или температуру.
В предпочтительной форме исполнения изобретения упаривание на стадии b) осуществляют при постоянной температуре и варьируемом во времени давлении.
В предпочтительной форме исполнения изобретения для снижения парциального давления растворителя в качестве химически инертного газа-носителя используют азот и/или воздух.
В предпочтительной форме исполнения изобретения водорастворимый растворитель удаляют благодаря комбинированному использованию вакуума и газа-носителя. В соответствии с предпочтительной формой исполнения изобретения общее давление и расход газа-носителя можно поддерживать постоянными или независимо друг от друга варьировать во времени. В предпочтительной форме исполнения изобретения в идеальном случае варьируют во времени, по меньшей мере, один из следующих технологических параметров: давление, расход газа-носителя и/или температуру. Тем самым, например, может быть обеспечено протекание реакции в течение определенного общего промежутка времени при необходимой степени упаривания, и/или скорость упаривания может быть приведена в соответствие с кинетикой реакции.
В соответствии с предпочтительной формой исполнения изобретения упаривание на стадии b) выполняют при постоянной температуре и варьируемом во времени давлении, причем вплоть до завершения вторичной реакции гидролитической конденсации давление снижают от нормального или слегка пониженного значения до величины, составляющей менее 600 мбар, предпочтительно менее 500 мбар, особенно предпочтительно менее 100 мбар.
В случае использования комбинированного технологического режима (совместного использования вакуума и газа-носителя) предпочтительным является постоянное или варьируемое разрежение, составляющее менее 600 мбар.
Температура выше 60°C является особенно предпочтительной, чтобы в случае значительного повышения концентрации азотной кислоты в остаточном растворителе способствовать восстановлению HNO3 до монооксида азота. Монооскид азота, который является чрезвычайно легколетучим газом (температура его кипения при нормальном давлении составляет около -150°C), после улетучивания из жидкой фазы при контакте с воздухом окисляется до легкокипящего диоксида азота (температура кипения около 21°C), который удаляют из системы вместе с отходящим воздухом или соответственно отходящим газовым потоком. Подобным образом ограничивают, соответственно снижают, концентрацию кислоты в предлагаемом в изобретении материале. В другом варианте концентрацию кислоты можно снижать также на одной из последующих стадий, например, путем проветривания твердого материала, например нетканого материала.
В случае использования вместо азотной кислоты системы органическая кислота/аргинин повышение показателя pH, соответственно снижение концентрации кислоты, выполняют при необходимости, например, посредством трис-растворов (если удаление кислоты, например, уксусной кислоты, не представляется возможным), осуществляя промывку материала незадолго до его применения в водном трис-растворе.
Неожиданно было обнаружено, что благодаря реализуемому в соответствии с настоящим изобретением осторожному перемешиванию реакционной системы (скорости вращения мешалки соответствует интервал от 20 до 80 об/мин) в противоположность немецкой заявке на патент DE 19609551 C1 можно предотвратить формирование концентрационных градиентов по высоте композиции, находящейся в реакционном сосуде на стадии реакционного упаривания (стадии b). Помимо увеличения продолжительности реакции гидролитической конденсации, по меньшей мере, до 16 часов подобное осторожное перемешивание способствует тому, что в соответствии с предлагаемым в изобретении способом прядению может быть подвергнуто, по меньшей мере, 70%, предпочтительно, по меньшей мере, 80% и еще более предпочтительно, по меньшей мере, 90% совокупной реакционной смеси.
Стадию (b) предпочтительно реализуют до тех пор, пока не образуется однофазный раствор, вязкость которого, измеренная при скорости сдвига 10 с-1 и температуре 4°C, составляет от 0,5 до 2 Па·с.
В соответствии с предпочтительной формой исполнения изобретения протекание реакции на стадии b) контролируют по изменению вязкости реакционной системы.
Гомогенный однофазный раствор, образующийся в результате гидролитической конденсации на стадии b), может быть охлажден и в предпочтительном варианте подвергнут кинетически контролируемому количественному созреванию, реализуемому при необходимости без предшествующего фильтрования.
Согласно изобретению созревание на стадии с) можно осуществлять при температуре от -20 до 10°C, предпочтительно от 2 до 4°C (например, в холодильнике). Созревание особенно предпочтительно осуществляют при температуре 4°C. Низкая температура созревания благоприятствует кинетически контролируемому протеканию дополнительной конденсации соединений кремния указанной выше формулы (I) в процессе созревания. В соответствующей смеси может происходить образование олигомеров и/или полимеров силоксанов и/или силанолов. Олигомеры и/или полимеры могут также соединяться посредством водородных мостиковых связей. Согласно изобретению в результате созревания может быть сформирована структурно-вязкая гомогенная однофазная прядильная зольмасса. Преимуществом настоящего изобретения является возможность максимального подавления конкурирующего образования пространственной полимерной сетчатой структуры (гелеобразования). В связи с этим согласно изобретению можно получать гомогенную прядильную зольмассу, которая преимущественно не содержит дополнительной твердой фаза, прежде всего геля.
Длительность реализуемого на стадии d) созревания согласно изобретению может составлять от 3 до 4 недель, предпочтительно, по меньшей мере, 10 дней, более предпочтительно, от 14 до 40 дней, например, от 14 до 28 дней, еще более предпочтительно по меньшей мере 25 дней и, в частности, в случае использования предлагаемых в изобретении материалов для заживления ран, от 25 до 40 дней. Согласно изобретению вязкость образующегося на стадии d) золя предпочтительно составляет от 30 до 100 Па·с (вязкость измеряют при температуре 4°C и скорости сдвига 10 с-1) при коэффициенте потерь (4°C, 10 с-1, деформация 1%), составляющим от 2 до 5, предпочтительно от 2,5 до 3,5 (коэффициент потерь представляет собой отношение вязкой составляющей динамической вязкости к ее упругой составляющей). Указанные условия созревания являются особенно предпочтительными в случае, если образовавшийся на стадии d) кремниевый золь подлежит прядению в волокна.
В случае использования предлагаемых в изобретении волокон/нетканого материала для лечения ран вязкость образующегося на стадии d) кремниевого золя, измеренная при температуре 4°C и скорости сдвига 10 с-1, предпочтительно составляет от 35 до 75 Па·с и еще более предпочтительно от 35 до 45 Па·с при коэффициенте потерь, измеренном при температуре 4°C, скорости сдвига 10 с-1 и деформации 1%, который предпочтительно находится в интервале от 2,5 до 3,5.
Слишком высокий коэффициент потерь означает слишком высокую эластичность материала, которая препятствует, например, формированию при прядении стабильных нитей из-за их желирования или обрыва. В случае слишком низкого коэффициента потерь материал характеризуется текучестью (образованием капель), что не позволяет формировать из него стабильные нити.
В случае если предлагаемый в изобретении кремниевый золь предназначен для последующей переработки в порошок, а не в прядильные волокна, условия созревания можно варьировать. В подобном случае динамическая вязкость, измеренная при температуре 4°C и скорости сдвига 10 с-1 по завершении стадии (d), предпочтительно составляет около 60 Па·с.
В случае переработки кремниевого золя в монолит динамическая вязкость, измеренная при температуре 4°C и скорости сдвига 10 с-1 по завершении стадии (d), предпочтительно больше или равна 70 Па·с. В случае если кремниевый золь подлежит использованию для нанесения на твердые тела или поверхности, динамическая вязкость в зависимости от требуемой толщины покрытия меньше или равна 10 Па·с (скорость сдвига 10 с-1, температура 4°C).
Полученную зольмассу, по меньшей мере, почти количественно предпочтительно можно использовать для реализации дополнительной технологической стадии и/или технологического процесса изготовления биологически расщепляющихся и/или рассасывающихся силикагелевых материалов. Полученный на стадии d) золь предпочтительно пригоден для прядения. Согласно изобретению может быть предусмотрена дополнительная стадия е), на которой осуществляют процесс прядения.
Подобная технологическая стадия может быть реализована при использовании обычных условий прядения, приведенных, например, в немецких заявках на патент DE 19609551 C1 и DE 102004063599 A1.
При этом золь пропускают через пластину с фильерами, например, посредством резервуара со сжатым газом (давление газа составляет от 1 до 100 бар, предпочтительно от 20 до 30 бар).
Длина прядильной шахты обычно составляет от 1 до 5 м, предпочтительно 2 м. В прядильной шахте осуществляют регулирование температурно-влажностного режима. Температура в прядильной шахте предпочтительно составляет от 20 до 30°C, точка росы находится в интервале от -5 до 10°C, что соответствует относительной влажности, составляющей от 20 до 40%, предпочтительно от 20 до 25% и особенно предпочтительно около 20%.
Волокна, образующиеся в результате пропускания зольмассы через прядильную шахту, обладают стабильной формой и их раскладывают на шанжировочном столе. Размер ячеек формируемого на шанжировочном столе волокнистого материала регулируют, в частности, путем варьирования скорости шанжирования. Последняя составляет несколько см/с. Вследствие двухосного движения шанжировочного стола происходит формирование мелкоячеистого волокнистого материала (нетканого материала) с остаточным содержанием этоксигрупп, составляющим, как правило, от 25 до 33% в пересчете на тетраэтоксисилан в качестве исходного кремнийсодержащего соединения.
В случае использования предлагаемых в изобретении материалов для заживления ран масса единицы поверхности волокнистого материала предпочтительно составляет, по меньшей мере, 90 г/м2, особенно предпочтительно по меньшей мере 150 г/м2. Толщина раневой накладки из получаемого прядением волокон нетканого материала предпочтительно составляет по меньшей мере 0,8 мм, особенно предпочтительно по меньшей мере 1,5 мм. Диаметр волокон предпочтительно составляет по меньшей мере около 45 мкм.
Силикагелевые волокнистые материалы и изделия, изготавливаемые из получаемого предлагаемым в изобретении способом силикагелевого материала, например, такие, как нити, волокна, нетканые материалы и/или ткани, обладают отличной способностью к биологической деструкции и биологическому рассасыванию.
Другое преимущество силикагелевых волокнистых материалов, изготавливаемых из предлагаемых в изобретении волокон, по сравнению с материалами из волокон, которые могут быть получены описанным в немецкой заявке на патент DE 19609551 C1 способом, состоит в том, что при испытании предлагаемых в настоящем изобретении материалов в присутствии фибропластов мышей L929 они характеризуются гораздо более благоприятными показателями цитотоксичности (смотри пример 1 и сравнительный пример). В связи с этим изделия, изготавливаемые из предлагаемого в изобретении материала на основе кремниевого золя, отличаются особенно высокой биологической совместимостью. Таким образом, предлагаемые в изобретении нити, волокна или нетканые материалы предпочтительно можно использовать в медицине или медицинской технике в качестве биологически расщепляющихся и/или биологически рассасывающихся материалов и изделий.
Независимо от этого экспериментально установлено, что предлагаемые в изобретении волокна и нетканые материалы обладают улучшенной способностью заживлять раны. В связи с этим предлагаемые в изобретении материалы прежде всего можно использовать предпочтительно в сфере лечения и заживления ран. Так, например, нити можно использовать в качестве хирургического материала для наложения швов или в качестве армирующих волокон. Предлагаемые в изобретении нетканые материалы особенно предпочтительно можно использовать для лечения поверхностных ран.
Предлагаемые в изобретении биологически расщепляющиеся и биологически рассасывающиеся волокна и нетканые материалы могут быть изготовлены благодаря реализации контролируемой гидролитической конденсации указанных выше соединений кремния и азотнокислой воды, включающей следующие стадии:
a) при необходимости в присутствии водорастворимого растворителя в течение, по меньшей мере, 16 часов, предпочтительно, по меньшей мере, 18 часов, при температуре от 0 до 80°C, предпочтительно от 20 до 60°C, особенно предпочтительно от 20 до 50°C, например, при комнатной температуре (примерно от 20 до 25°C) или при температуре около 37°С, при начальном показателе pH от 0 до ≤7 осуществляют кислотно катализируемую реакцию гидролитической конденсации одного или нескольких соединений кремния формулы (I):
 ,
,
в которой остатки X, одинаковые или разные, означают гидрокси, водород, галоген, амино, алкокси, ацилокси, алкилкарбонил и/или алкоксикарбонил и являются производными алкильных остатков, представляющих собой при необходимости замещенные неразветвленные, разветвленные или циклические остатки с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода, которые могут быть прерваны атомами кислорода или серы или аминогруппами,
b) путем последующего упаривания формируют однофазный раствор, вязкость которого, измеренная при скорости сдвига 10 с-1 и температуре 4°C, составляет от 0,5 до 2 Па·с,
c) полученный раствор затем охлаждают и
d) подвергают кинетически контролируемому созреванию, в результате которого образуется гомогенный однофазный золь, и
e) осуществляют прядение полученного по пункту d) золя.
В случае если для реализуемой на стадии а) гидролитической конденсации в качестве соединения кремния используют, например, тетраэтоксисилан, причем гидролиз выполняют в течение достаточно длительного времени, в результате реализуемого на стадии b) упаривания образуется гомогенный раствор. В процессе последующего созревания, реализуемого при пониженной температуре на стадии c), может протекать кинетически контролируемая реакция. В подобном случае смесь может находиться на стадии d) в виде гомогенной растворенной однофазной массы, то есть в виде пригодной для прядения зольмассы.
Изготавливаемые в соответствии с изобретением волокна или нетканые материалы предпочтительно можно использовать в качестве биологически рассасывающихся и/или биологически активных материалов в медицине, медицинской технике, технологии фильтрования, биотехнологии или промышленности изоляционных материалов. Изготавливаемые в соответствии с изобретением материалы предпочтительно можно использовать прежде всего для лечения и заживления ран. Волокна можно использовать, например, в качестве шовного хирургического материала или в качестве армирующих волокон. Нетканые материалы особенно предпочтительно можно использовать для лечения поверхностных ран, например, для фильтрования содержащихся в организме жидкостей, в частности крови, или в биотехнологии в качестве вспомогательных средств для выращивания микроорганизмов.
Другой формой исполнения изобретения может являться система доставки лекарственного средства к зоне его действия и/или лекарственный препарат в виде микропорошка и/или нанопорошка.
Соответствующие порошковые формы могут быть изготовлены путем совмещения предлагаемого в изобретении кремниевого золя с необходимым действующим веществом, например с одним или несколькими лекарственными средствами (благодаря реализации дополнительной реакции гидролитической конденсации действующее вещество при необходимости может быть также соединено с кремниевым золем ковалентными связями), и формирования соответствующей гомогенной смеси. Смесь кремниевого золя с действующим(и) веществом(ами) подвергают реализуемой в мягких условиях сушке, например, распылительной или сублимационной сушке, что прежде всего относится к смесям, содержащим чувствительные к температуре действующие вещества. В случае если действующее вещество не обладает повышенной термочувствительностью или смесь не содержит чувствительных к температуре действующих веществ, указанную сушку можно выполнять также при повышенных (существенным образом) температурах. При этом вокруг действующего вещества предпочтительно образуется биологически рассасывающаяся и/или биологически активная матрица из силикагеля. Подобная матрица прежде всего пригодна для капсулирования и контролируемого высвобождения жидких действующих веществ при одновременном сохрании их долговременной стабильности. Капсулирование способствует механической и химической стабилизации действующих веществ, предоставляет возможность более удобного обращения с жидкими действующими веществами и лекарственными средствами и позволяет избежать неконтролируемого улетучивания действующих веществ. В готовой композиции (порошке) в зависимости от ее назначения, очевидно, могут присутствовать также другие добавки и/или вспомогательные вещества. Размер частиц (средний диаметр) предлагаемого в изобретении микропорошка предпочтительно составляет от 0,01 до 100 мкм, прежде всего от 0,1 до 20 мкм. Размер (средний диаметр) частиц нанопорошка, как правило, составляет ≤100 нм.
Согласно другой форме исполнения изобретения смесь, по меньшей мере, одного действующего вещества с предлагаемым в изобретении кремниевым золем можно выливать в форму. В результате сушки подобной смеси может быть получен монолит. Подобные монолиты, например, в виде сплошных подкожных имплантатов можно использовать в качестве систем доставки действующих веществ к зоне их действия. Их можно использовать, например, в качестве депо для контрацептивов, высвобождающего действующее вещество в течение длительного периода времни. Подобные предлагаемые в изобретении имплантаты характеризуются отличной биологической совместимостью. Монолиты могут обладать диаметром, предпочтительно составляющим ≥0,5 мм. В другом варианте монолиты можно подвергать также измельчению в порошок и размалыванию.
В другой форме исполнения изобретения кремниевый золь можно использовать для нанесения покрытий, которые выполняют обычными методами, например окунанием подлежащего облицовке тела в кремниевый золь, его поливу кремниевым золем, а также центробежным методом или распылением кремниевого золя. Кремниевый золь предпочтительно можно использовать в качестве покрытия драже или капсулы. С этой целью спрессованные порошкообразные смеси лекарственных средств снабжают биологически рассасывающимся и/или биологически активным покрытием из предлагаемого в изобретении кремниевого золя. Это позволяет контролировать и/или регулировать (например, путем варьирования толщины покрытия и/или последовательности слоев) высвобождение (других) действующих веществ композиции. Указанное покрытие можно наносить также на внедряемые в тело имплантаты, что позволяет повысить (биологическую) совместимость подобных имплантатов, например ослабить или предотвратить реакции их отторжения.
Согласно другой форме исполнения изобретения предлагаемым в изобретении силикагелем можно дополнять или заменять высоковязкие золи, прежде всего гидрогели. Высоковязкие золи и гидрогели используют в медицине и в косметике в качестве действующих веществ или соответственно основ лекарственных средств. Гидрогели в общем случае часто используют для лечения и заживления ран большой площади. В предпочтительном варианте добавление к ним кремниевого золя способствует повышению биологической совместимости, а следовательно, более быстрому заживлению ран. Таким образом, предлагаемые в изобретении гидрогели предпочтительно можно использовать в качестве биологически рассасывающихся и/или биологически активных изделий, используемых прежде всего в медицине или медицинской технике.
Кроме того, настоящее изобретение относится к способу размножения клеток in-vitro, в соответствии с которым матрица, состоящая из предлагаемых в изобретении волокон, выполняет функцию опорной структуры для выращивания клеток и/или направляющей структуры для формирующейся из клеток внеклеточной матрицы, соответственно предоставляет клеткам возможность находить пространственное положение, которое позволяет им размножаться и/или достигать генетически обусловленной дифференцировки. Преимущества предлагаемого в изобретении способа находят соответствующее экспериментальное подтверждение (смотри пример 3).
В качестве клеток можно использовать, например, недифференцированные плюрипотентные стволовые клетки или генетически измененные или нативные дифференцированные клетки с варьируемыми характером и степенью дифференцировки.
Клетки, наносимые на волокнистую матрицу, прилипают к ней или размножаются на ней главным образом двухмерно, совместно образуя внеклеточную матрицу, соответственно медиаторы (гормоны). Волокнистая матрица предпочтительно обладает формой плоскостного элемента, прежде всего нетканого материала или ткани из предлагаемых в изобретении волокон. Подобная волокнистая матрица предпочтительно обладает пористой структурой, в связи с чем нанесенные на нее клетки проникают внутрь, распределяясь в ее объеме, и в соответствии с их генетически обусловленной дифференцировкой или индуцированной факторами дифференцировки дополнительной дифференцировкой могут инициировать пространственный рост тканей и органов, соответственно высвобождать медиаторы. В другой форме исполнения изобретения матрицу формируют в виде непроницаемой для нанесенных на нее клеток плотной сетки волокон с возможностью двухмерного распределения клеток и одновременной возможностью трехмерного роста тканей и органов наподобие сложного трансплантата.
Предлагаемый в изобретении способ размножения in-vitro предпочтительно предназначен для формирования клеточных комбинаций, тканей и/или органов in-vitro.
Предпочтительным объектом настоящего изобретения является клеточный комплекс, ткань и/или орган, которые могут быть изготовлены указанным выше способом. Подобный клеточной комплекс, ткань и/или орган (подобные клеточные комплексы, ткани и/или органы) пригоден(ы) для использования, например, в качестве модели протекающих in vitro взаимодействий в системе «медикамент-ткани-орган». Известно множество методов изготовления тканей вне человеческого организма, объединяемых общим названием «тканевая инженерия». В соответствии с подобными методами из состоящего из клеток того или иного типа тканевого комплекса выделяют клетки и осуществляют их размножение. Для этого клетки наносят на плоскостные материалы различной консистенции или вводят в пористые, соответственно желеобразные материалы, тем самым индуцируя и при необходимости стимулируя посредством факторов дифференцировки созревание ткани. Созревание ткани может происходить вне или внутри организма. При этом преимущество предлагаемой в изобретении волокнистой матрицы состоит в том, что она способна к биологическому расщеплению и/или биологическому рассасыванию, однако несмотря на это при размножении in-vitro в течение определенного периода времени она, как показано в примере 3, почти полностью сохраняет свою двухмерную или соответственно трехмерную форму. В соответствии с этим настоящее изобретение предпочтительно относится к клеточному комплексу, ткани и/или органу с волокнистой матрицей из поликремниевой кислоты, предпочтительно изготовленной из предлагаемых в изобретении волокон, причем форма биологически расщепляющейся и/или биологически рассасывающейся волокнистой матрицы по истечении четырех недель с момента первичного заселения клетками in-vitro, по меньшей мере, на 60%, предпочтительно, по меньшей мере, на 70% и особенно предпочтительно, по меньшей мере, на 80% идентична ее первоначальной двухмерной или соответственно трехмерной форме. Так, например, в соответствии с подобной формой исполнения изобретения предлагаемая в изобретении волокнистая матрица расщепляется и/или рассасывается предпочтительно лишь после нанесения клеточного комплекса, ткани и/или органа на тело животного или человека, или соответственно после внедрения клеточного комплекса, ткани и/или органа в тело животного или человека.
Клетки в зависимости от их типа подлежат растворению вследствие предварительного ферментативного усвоения или механического выделения из соответствующего матричного комплекса, или следует стимулировать их рост в физиологических условиях путем нанесения на питательную среду, соответственно введения в питательную среду. При этом указанная выше волокнистая матрица выполняет функцию направляющей структуры для роста клеток или функцию направляющей структуры для аккумулирования компонентов внеклеточной матрицы и ткани. Согласно изобретению возможны различные варианты упорядочения волокнистого материала. Специалист выбирает надлежащий вариант упорядочения волокнистого материала в зависимости от типа подлежащей изготовлению (клеточной) ткани. Возможны следующие варианты упорядочения волокнистого материала.
1) Волокнистый материал в виде плоскостного элемента, то есть плотной сетки из волокон, которая предоставляет нанесенным клеткам зависящую от их размера возможность ограниченного проникания (то есть средний размер отверстий/волокон, соответственно промежутков сетки, ни в коем случае не превышает средний размер подлежащих культивированию клеток, а предпочтительно даже меньше его, благодаря чему клетки могут «врастать» в волокна, однако при этом они оптимальным образом адгезируют к соответствующей подложке), с преимущественно единственной возможностью, по меньшей мере, первоочередного двухмерного распределения клеток, а также плоскостного роста клеток, тканей и органов.
2) Волокнистый материал в виде трехмерного элемента, то есть в виде допускающей возможность проникания клеток пористой сетки из волокон (при этом средний размер отверстий/волокон, соответственно промежутков сетки, ни в коем случае не меньше среднего размера подлежащих культивированию клеток, а предпочтительно даже превышает его) с возможностью пространственного распределения клеток, а также пространственного роста клеток, тканей и органов; 3) в качестве сочетания вариантов 1) и 2) в смысле «сложного трансплантата» или органа, реализуемое комбинированием клеток, тканей, соответственно органов, с поверхностной оболочечной тканью (например, капсулой органа).
3) Данный вариант волокнистого материала подходит для структур тканей, состоящих из клеток нескольких разных типов. Так, например, кровеносные сосуды состоят из эндотелия и соединительной ткани, причем обладающий плоской структурой эндотелий служит для выстилки кровеносных сосудов, в то время как соединительная ткань выполняет функцию соответствующего опорного материала и образует пространственную полую структуру. Для восстановления кровеносного сосуда можно использовать комбинацию волокнистого материала 1) в виде плоскостного элемента, предназначенного для роста эндотелия, с волокнистым материалом 2) в виде трехмерного пространственного элемента, предназначенного для роста соединительной ткани.
Ниже приведены некоторые типы тканей, соответственно клеток, которые особенно пригодны для размножения/изготовления с помощью волокнистого материала одного из указанных выше типов и поэтому согласно изобретению являются предпочтительными.
Волокнистые материалы 1) пригодны для предпочтительного применения на следующих тканях: эпителии, эндотелии, уротелии, слизистой оболочке, твердой мозговой оболочке и соединительных тканях, а также предпочтительно на следующих клетках: плюрипотентных стволовых клетках, хондроцитах (хрящевых клетках) [для размножения хондроцитов требуется двухмерная среда, тогда как для дифференцировки хондроцитов и формирования хрящевой матрицы нужна трехмерная среда; в данном случае под хондроцитами подразумевают только дедифференцированные и размножившиеся клетки; для дифференцировки используют волокнистый материал 2), остеоцитах (костных клетках), в данном случае необходима как двухмерная, так и трехмерная среда, поэтому речь идет о волокнистых материалах, аналогичных применяемым для хондроцитов], нервных клетках (нервах), волосковых клетках (внутреннее ухо - орган слуха) или на соответствующих предварительных клетках любой стадии дифференцировки (например, плюрипотентных стволовых клетках).
Волокнистые материалы 2) пригодны для применения на следующих клетках: пригодных для применения волокнистого материала 1) клетках указанного выше типа после их плоскостного размножения, специфичных для соответствующих органов клетках (например, на гепатоцитах, нефроцитах, кардиомиоцитах или панкреоцитах), клетках центральной нервной системы с эндокринной функцией или без эндокринной функции, например на клетках сетчатки, нейроцитах, клетках шишковидной железы, дофаминергических клетках или сосудобразующих клетках (например, ангиоцитах), клетках с эндокринной или экзокринной функцией (например, на островковых клетках, клетках надпочечников, клетках слюнных желез, тельцах эпителия или тироцитах), клетках имунной системы (например, на макрофагах, В-клетках, Т-клетках или соответствующих предварительных клетках любой стадии дифференцировки, таких как плюрипотентные стволовые клетки). Клетки имунной системы культивируют трехмерно, поскольку после проникания в ткань через существующий между кровью и тканью барьер они наталкиваются на зависящий от типа ткани пространственный каркас и проявляют присущее им действие в трехмерном объеме.
Волокнистые материалы 3) пригодны для применения на следующих клетках/тканях/органах: трахее, бронхах, сосудах, лимфоидной ткани, мочеиспускательном канале, мочеточнике, почках, мочевом пузыре, надпочечниках, печени, селезенке, сердце, щитовидной железе, миндалинах, слюнных железах, головном мозге, мышцах (гладких и поперечно-полосатых), межпозвоночных дисках, суставных менисках, легких, желчном пузыре, пищеводе, кишечнике и глазах.
Сферы возможного использования волокон, известных из немецкой заявки на патент DE 19609551 С1 В, указаны в примерах 1-3 европейской заявки на патент EP 1262542. Другой сферой возможного использования предлагаемого в настоящем изобретении материала является его заселение клетками с эндокринной, соответственно экзокринной функцией, высвобождающими действующие вещества (например, гормоны, интерлейкины, медиаторы воспаления и энзимы), которые проявляют присущее им действие внутри или вне организма. Это значит, что используемый согласно настоящему изобретению материал при его заселении обладающими эндокринной или экзокринной функцией клетками может служить также для производства указанных выше действующих веществ вне организма, причем соответствующие действующие вещества посредством известных методов затем предоставляются в распоряжение организма в качестве лекарственных средств. Проявляемое вне организма действие может служить для того, чтобы высвобождающееся вещество оказывало воздействие на ткани или клетки.
Другой сферой применения волокнистой матрицы является биологически рассасывающийся биоимплантат в виде направляющей шины, используемой для аутогенного заживления ран при операциях на органах и тканях, осуществляемых ниже уровня кожи или слизистой оболочки, соответственно на уровне кожи или слизистой оболочки, а также внутри тела. С этой целью, например, во время операции хирург по возможности внедряет в рану или орган/ткань материал в виде плоскостного или трехмерного пространственного элемента непосредственно или совместно со способствующими заживлению ран веществами или медикаментами. Свойства применяемого в соответствии с изобретением биологически рассасывающегося неорганического материала в виде волокон обуславливают лишь незначительное изменение тканевой среды подлежащих выращиванию клеток, прежде всего отсутствие возникновения кислой среды, благодаря чему предотвращается негативное влияние дифференцировки тканей и органов. Кроме того, полная диссимиляция материала происходит независимо от показателя pH ткани. В случае ненамеренного попадания возбудителей заболеваний (инфекции) благодаря одновременно происходящему формированию ткани, соответственно органа, постоянно сохраняется возможность проникновения противоинфекционных медикаментов через витальную ткань. Кроме того, волокнистую матрицу можно совмещать с действующими веществами из самых разных групп с возможностью положительного воздействия на дифференцировку тканей и органов, реализуемой благодаря проявлению активного и пассивного действия в месте применения, и также в удаленных зонах. К подобным веществам прежде всего относятся, во-первых, противоинфекционные действующие вещества, а во-вторых, действующие вещества, поддерживающие и модулирующие заживление ран, противовоспалительные реакции, а также дифференцировку тканей, например, такие, как факторы роста (IGF, TGF, FGF и другие), с одной стороны, и гликокортикоиды и интерлейкины, с другой стороны, а также химиотерапевтические и подавляющие иммунитет средства.
Используемые согласно изобретению биологически рассасывающиеся неорганические волокна способны адгезировать подлежащие использованию клетки с возможностью их размножения вдоль волокон, а также с возможностью формирования матрицы ткани, соответственно органа. Одновременно с размножением клеток, или соответственно формированием ткани, или соответственно матрицы органа происходит диссимиляция волокнистой структуры. В идеальном случае варьирование конденсации волокон позволяет обеспечить корреляцию формирования тканей, органов, соответственно клеток, со скоростью диссимиляции волокнистого материала. При этом чем менее глубок процесс поликонденсации (то есть чем меньше количество отщепляемой воды), тем эффективнее деструкция соответствующего волокнистого материала. Максимального содержания OH-групп, а следовательно, наиболее высокой скорости деструкции волокон достигают для свежеизготовленных прядением волокон с последующим погружением в этанол. На процесс конденсации оказывают влияние также параметры прядения, а именно скорость приема волокон, внешняя среда, температура и тому подобное. Изготавливаемые волокна являются биологически расщепляющимися и биологически рассасывающимися материалами, которые деструктируют в течение управляемого периода, составляющего предпочтительно от двух до десяти недель, причем скорость диссимиляции коррелирует с содержанием силанольных групп в волокнах. Другим аспектом настоящего изобретения является применение предлагаемых в изобретении клеток, органов и тканей после их совмещения с медикаментами и/или действующими веществами в качестве модели взаимодействий in vitro в системах «медикамент-ткани-орган». Благодаря подобной модели можно свести к минимуму объем выполняемых на животных экспериментальных исследований или избежать их вовсе.
Другим особенно предпочтительным объектом настоящего изобретения является способ изготовления кожного имплантата, в соответствии с которым клетки кожи наносят на поверхность питательного раствора и оставляют расти, причем на питательный раствор укладывают плоскостный элемент из предлагаемых в изобретении волокон.
Кроме того, предпочтительным объектом настоящего изобретения является кожный имплантат, состоящий из клеток кожи и плоскостного элемента из предлагаемых в изобретении волокон. Плоскостный (предпочтительно планарный) элемент обеспечивает возможность плоскостного, а следовательно, быстрого роста клеток кожи при необходимости с одновременным использованием инфильтрирующих медикаментов.
Приведенные ниже примеры служат для более подробного пояснения настоящего изобретения и не ограничивают его объема.
Все указанные в примерах значения вязкости получены измерением с помощью вискозиметров типа MCR300 и MCR301 фирмы Physica, осуществляемом при температуре 4°C и скорости сдвига 10 с-1.
Примеры
Пример 1. Кремниевый золь и биологически рассасывающийся и биологически расщепляющийся силикагелевый материал
В реакционный сосуд в качестве эдуктов для гидролитической конденсации загружали и перемешивали друг с другом 4 моля тетраэтоксисилана (тетраэтоксисилоксана) в этаноле и 7 молей воды в виде 0,01 Н раствора HNO3. Перемешивание эдуктов продолжали при комнатной температуре в течение восьми дней. Раствор, полученный в результате протекания реакции гидролитической конденсации, путем осуществляемого в химическом стакане упаривания и конденсации при 70°C переводили в почти не содержащий воду и этанол раствор. Последний представлял собой не содержащий твердых веществ однофазный раствор, вязкость которого, измеренная при температуре 4°C и скорости сдвига 10 с-1, составляла 1 Па·с. Раствор охлаждали до 4°C и при этой температуре подвергали созреванию. По завершении 18-дневного созревания получали гомогенную однофазную прядильную зольмассу, вязкость которой, измеренная при температуре 4°C и скорости сдвига 10 с-1, составляла 43 Па·с. Прядильная зольмасса не содержала заметного количества твердой фазы. Гомогенная прядильная зольмасса была пригодна для прядения волокон (ниже ее называют также прядильной зольмассой).
Изготовление волокон осуществляли на обычном прядильном устройстве. С этой целью прядильную массу загружали в охлажденный до -15°C напорный цилиндр, в который нагнетали воздух под давлением 20 бар. Под действием давления происходило выдавливание золя через фильеры и формирование нитей. В зависимости от диаметра фильер нити обладали диаметром от 5 до 100 мкм.
Нити из обладающего медообразной консистенцией текучего материала под действием собственного веса опускались в расположенную ниже напорного цилиндра прядильную шахту, в которой они реагировали с образованием преимущественно твердых нитей стабильной формы. Поверхность нитей продолжала сохранять реакционную способность, в связи с чем при попадании нитей на при необходимости используемый шанжировочный стол могло происходить склеивание нитей друг с другом по соответствующим поверхностям контакта. Благодаря регулируемой цикличности движений шанжировочного стола происходило формирование дополнительных узлов сетки между волокнами слоя волокнистой массы.
Формируемые согласно изобретению нити преимущественно были более сухими по сравнению с волокнами, формируемыми в сравнимых условиях прядения способом, предложенным в немецкой заявке на патент DE 19609551 C1. Благодаря этому согласно изобретению при последующем изготовлении нетканых материалов получали менее сшитые, а следовательно, более гибкие изделия.
Изготовленный согласно изобретению нетканый материал подвергали цитотоксикологическому испытанию согласно ISO 10993-5 (1999) и европейскому стандарту EN 30993-5 (1994). Экстракт, полученный в результате экстракции нетканого материала модифицированной по способу Дульбекко средой Игла, фильтровали в стерильных условиях и смешивали с фетальной телячьей сывороткой (концентрация последней в экстракте составляла 10%). Смешанный с фетальной телячьей сывороткой экстракт наносили в стерильных условиях на фибропластовые клетки мышей L929 и в течение 48 часов выдерживали при 37°C и парциальном давлении диоксида углерода 5%.
В качестве токсичного контрольного вещества использовали Triton X 100, в качестве нетоксичного контрольного вещества использовали среду для клеточной культуры. Для определения количества клеток их фиксировали и окрашивали метиленовым голубым. После кислотной экстракции метиленового голубого осуществляли фотометрическое измерение содержания красителя и для определения количества клеток на основании полученных данных сравнивали измеренную экстинкцию со стандартной кривой. Измерения количества клеток в сравнении с контрольными опытами показали, что предлагаемый в изобретении силикагелевый материал не обладает цитотоксическим действием. Результаты измерения содержания протеина (щелочным растворением и определением протеина по методу Брэдфорда) и высвобождения лактат-дегидрогеназы (фотометрическим методом) согласуются с этим выводом.
Сравнительный пример
В аналогичных экспериментальных условиях выполняли измерения токсичности, используя нетканый материал, изготовленный в соответствии с приведенным в немецкой заявке на патент DE 19609551 C1 примером при длительности гидролитической конденсации 1,5 часа. При этом прядению удавалось подвергнуть лишь 50% совокупной реакционной смеси. Изготовленный из полученных волокон материал согласно результатам соответствующего испытания характеризуется цитотоксичностью.
Пример 2
В другой серии опытов осуществляли сравнительное исследование заживления ран, используя пять разных предлагаемых в изобретении нетканых материалов (KG211, KG226, AEH06KGF553, AEH06KGF563 и AEHKGF565) и контрольный ранозаживляющий рассасывающийся материал Promogran®, причем испытания проводили в течение трех месяцев на морских свинках.
Различия исследуемых образцов предлагаемого в изобретении нетканого материала обусловлены варьированием используемых для их изготовления параметров, которые приведены в таблице 1.
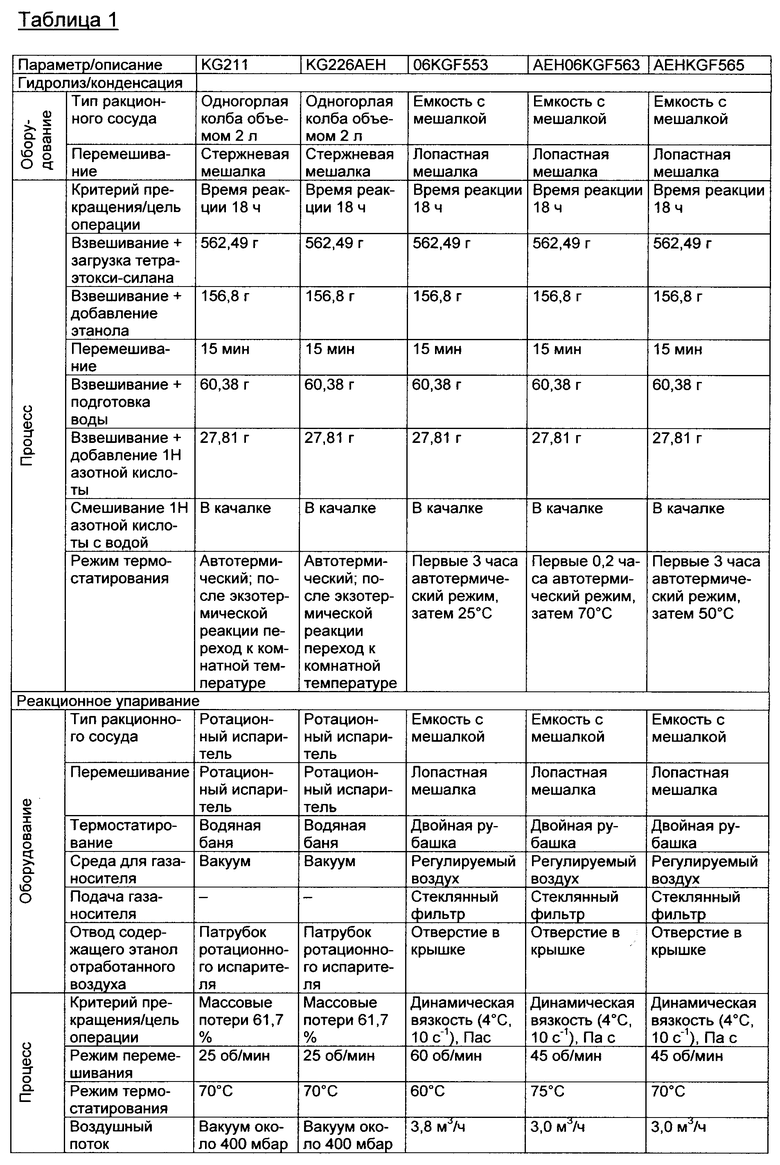


Хирургическим методом у 36 морских свинок были выполнены используемые в последующих исследованиях дермоэпидермальные раны. При этом с обеих сторон от позвоночника каждого животного удаляли участок дермы и эпидермиса площадью около 6,25 см2 (2,5×2,5 см). Удаление ткани выполняли скальпелем. При этом Panniculus carnosus оставался неповрежденным. На соответствующие раны накладывали предлагаемые в изобретении раневые накладки и материал Promogran®. Указанные материалы закрывали неадгезионной повязкой для ран URGOTUL® и полупроницаемой адгезионной полиуретановой пленкой TEGADERM® или OPSITE®. Поверх накладывали защитную когезионную повязку (Gaze и ELASTOPLAST®). Каждый из образцов нетканого материала, соответственно контрольного материала, испытывали на пяти животных, соответственно на десяти ранах (n=10). Через разные промежутки времени оценивали заживление ран методами макроскопического, морфометрического и гистологического исследования.
Ни для одной из исследуемых раневых накладок не было обнаружено местной интолерантности. Морфометрические исследования показали, что 50-процентное закрытие обработанных посредством материала Promogran® ран наступало несколько быстрее по сравнению с ранами, обработанными неткаными материалами. Однако в случае использования материала Promogran® полное (100%), соответственно почти полное (75%, 95%) закрытие ран было несколько более продолжительным по сравнению с большинством образцов нетканого материала. 100-процентного заживления ран в случае использования материалов KG211 и KG226 достигали в среднем примерно через 23 дня, материалов AEH06KGF553, AEH06KGF563 и AEH06KGF565 в среднем примерно через 24 дня и материала Promogran® в среднем лишь по истечении 26 дней.
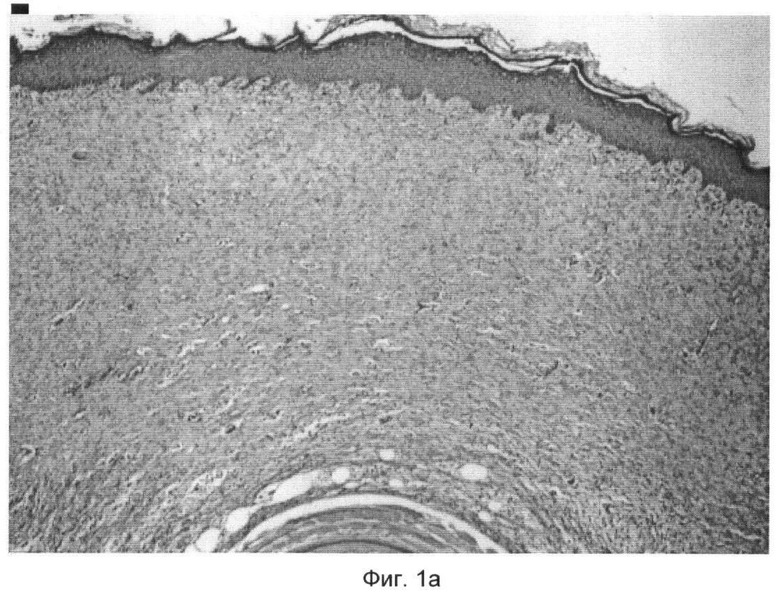
В результате гистологических исследований, выполненных через 28 дней после генерирования ран, в случае использования нетканого материала KG211 было обнаружено чрезвычайно хорошее ранозаживление (смотри фиг.1а). Исключение составляло отсутствие полной стабилизации местной реакции ткани, поскольку в отдельных случаях наблюдали наличие макрофагов. Независимо от этого грануляционная ткань была незаметной, обладала нормальной толщиной и была покрыта сплошным слоем вновь образовавшегося эпителия.
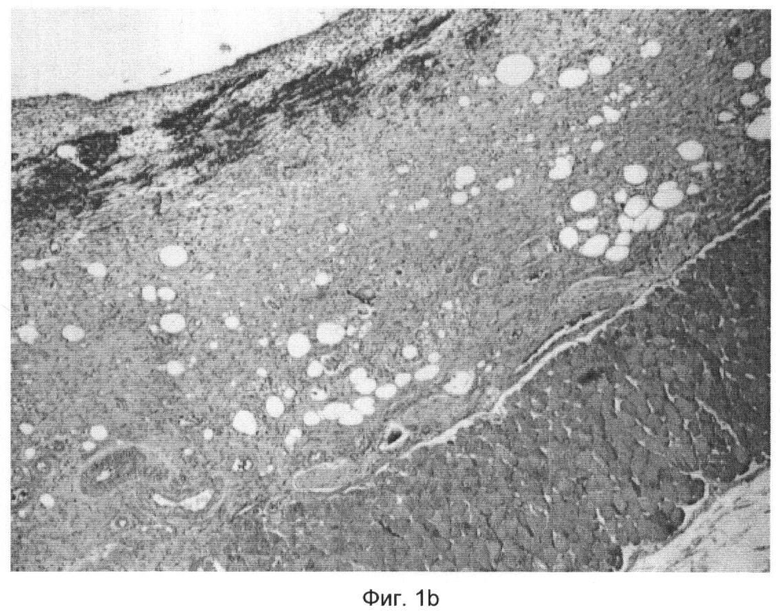
В случае использования материала Promogran® в результате выполненных по истечении 28 дней после генерирования ран гистологических исследований была обнаружена сильно вакуолизированная и пронизанная полиморфноядерными клетками грануляционная ткань (смотри фиг.1b). При этом в отличие от KG211 грануляционная ткань не была закрыта слоем эпителия.
Таким образом, предлагаемые в изобретении раневые накладки позволяют сократить длительность заживления ран по сравнению с материалом Promogran® при одновременном формировании улучшенного грануляционного слоя и сведении к минимуму воспалительных процессов в течение четырех первых недель ранозаживления.
Пример 3
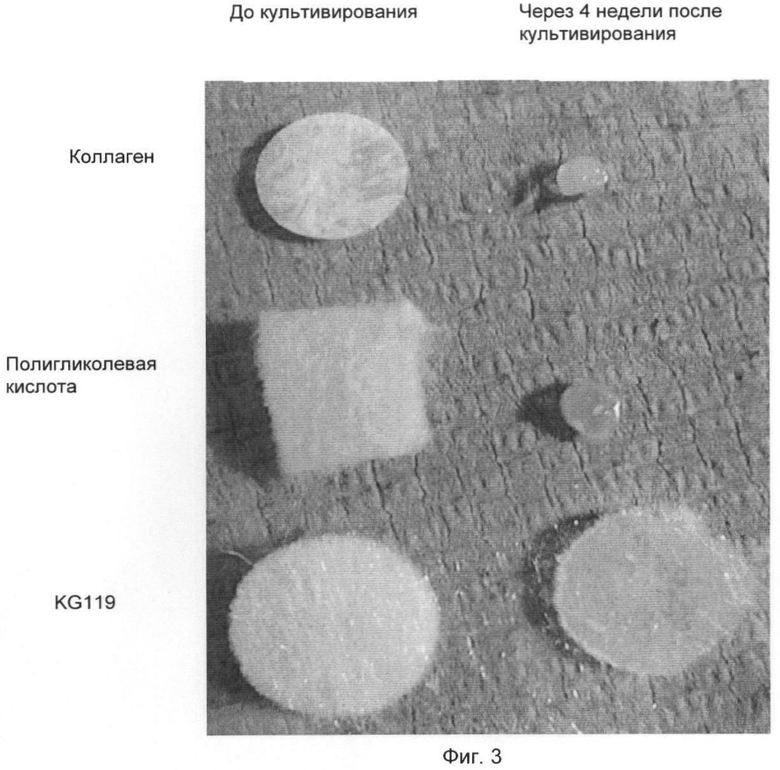
Предлагаемую в изобретении волокнистую матрицу KG119, состоящую из биологически расщепляющихся и/или биологически рассасывающихся волокон, в качестве опорного материала для выращивания клеток, а также коллаген и полигликолевую кислоту стерилизовали гамма-лучами и в цельной среде на один час помещали в инкубатор. Волокнистую матрицу KG119 использовали в виде плоскостного элемента из нетканого материала. Технологические параметры изготовления соответствующего нетканого материала приведены в таблице 2. Для вырубки плоскостных элементов из нетканого материала использовали круглый штамп (смотри фиг.3).
Перед заселением клетками среду обновляли. Затем добавляли дермальные фибробластовые клетки человека. Клеточную культуру выращивали в пластиковом планшете Falcon 351147 с 24 лунками. Выполняли ежедневную замену среды. В качестве среды для выращивания клеток использовали модифицированную по способу Дульбекко среду Игла 42430-250 с добавлением 10% фетальной телячьей сыворотки и пенициллина (100 единиц/мл), 0,25 мкг/мл амфотерицина В и 0,1 мг/мл используемого в качестве антибиотика стрептомицина. Во время роста клеток после первоначальной замены среды к ней добавляли 50 мкг/мл аскорбиновой кислоты. Кроме того, по мере увеличения количества клеток в среду необходимо было добавлять буферный раствор карбоната натрия (7,5% Sigma). Клеточный стандартный образец (контрольные клетки без соответствующего опорного материала) культивировали в обычных чашках Петри для тканевых культур и на стеклянных пластинах Иваки.
Контроль методом Alamar Blue осуществляли с использованием реагентов фирмы Serotec. Указанные реагенты разбавляли до концентрации 10% не содержащим фенола сбалансированным солевым раствором Хенкса, повышали температуру до 37°C и фильтровали в стерильных условиях. Опорный материал с клетками промывали фосфатно-солевым буфером, удаляли с первоначальных пластин и помещали в чашки Петри и на стеклянные пластины Иваки.
Измеренная методом Alamar Blue метаболическая активность является функцией количества клеток и метаболической активности отдельных клеток. На фиг.2 показана активность (в виде результатов измерения флюоресценции) дермальных фибробластов на различных матрицах (коллагене, полигликолевой кислоте и предлагаемой в изобретении волокнистой матрице KG119), а также клеток без опорного каркаса (контрольная культура, Ctrl)) при длительности культивирования, составляющей одну неделю (Wk 1), две недели (Wk 2) и четыре недели (Wk 4).
Клетки обладают сильной адгезией к материалу KG119, сравнимой с их адгезией к коллагену. Адгезия клеток к материалу KG119 и коллагену превосходит их адгезию к полигликолевой кислоте (соответствующие данные на фиг.2 не показаны). Чем дольше клетки растут на матрицах, тем более явно обнаруживается преимущество волокнистой матрицы KG119. Как показано на фиг.2, волокнистый материал KG119 превосходит опорные структуры других типов в отношении метаболической активности клеток.
Высокая метаболическая активность в случае использования материала KG119 сохраняется в течение всего периода выполнения измерений (четырех недель). В отличие от этого коллаген, полигликолевая кислота и клетки без соответствующих опорных структур не способны обеспечить метаболическую активность в течение указанного промежутка времени. Высокой адгезией и пролиферацией клеток при сохранении метаболической активности в течение всего указанного периода характеризуется лишь волокнистая матрица KG119.
На фиг.3 показаны клеточные опорные каркасы на основе коллагена, полигликолевой кислоты и KG119 перед культивированием дермальных фибробластовых клеток человека и по истечении четырех недель культивирования. Каркасы из коллагена и полигликолевой кислоты стягиваются и деструктируют, образуя плотный тканевый шар. Первоначальную форму сохраняет лишь волокнистый материал KG119. Внутри него формируется плотная масса дермальной ткани, с которой прочно соединены волокна материала KG119.

Изобретение относится к материалу на основе кремниевого золя, а также его применению для изготовления биологически рассасывающихся и биологически расщепляющихся силикагелевых материалов с улучшенными свойствами. Указанные силикагелевые материалы, такие как волокна, нетканый материал, порошок, монолит и/или покрытие, используют, например, в медицинской технике и/или медицине, прежде всего для лечения ран. Материал получен способом, включающим кислотно катализируемую реакцию гидролитической конденсации соединений кремния вида SiX4, например тетраэтоксисилана, в присутствии водорастворимого растворителя в течение не менее 16 часов (предпочтительно от 3 до 8 дней), последующего упаривания с получением однофазного раствора, охлаждения до 4°C и кинетически контролируемого созревания. Готовый однофазный раствор пригоден для прядения волокон. Технический результат изобретения - получение нетоксичного биологически разлагаемого однофазного материала, полностью пригодного для получения волокон. 5 н. и 8 з.п. ф-лы, 2 табл., 3 пр., 4 ил.
1. Материал на основе кремниевого золя, который может быть изготовлен тем, что:
a) при необходимости в присутствии водорастворимого растворителя в течение, по меньшей мере, 16 ч при температуре от 0 до 80°C и начальном показателе pH от 0 до ≤7 осуществляют кислотно катализируемую реакцию гидролитической конденсации одного или нескольких соединений кремния формулы (I):

в которой остатки Х одинаковые или разные, означают гидрокси, водород, галоген, амино, алкокси, ацилокси, алкилкарбонил и/или алкоксикарбонил и являются производными алкильных остатков, представляющих собой, при необходимости, замещенные неразветвленные, разветвленные или циклические остатки с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода, которые могут быть прерваны атомами кислорода или серы или аминогруппами,
b) путем последующего упаривания формируют однофазный раствор, вязкость которого, измеренная при скорости сдвига 10 с-1 и температуре 4°C, составляет от 0,5 до 2 Па·с,
c) полученный раствор затем охлаждают и
d) подвергают кинетически контролируемому созреванию, в результате которого образуется гомогенный однофазный золь.
2. Материал на основе кремниевого золя по п.1, отличающийся тем, что для кислотного катализа используют азотнокислую воду в молярном отношении от 1:1,7 до 1:1,9, предпочтительно от 1:1,7 до 1:1,8, причем гидролитическую конденсацию осуществляют, по меньшей мере, в течение 16 ч, предпочтительно в течение 18 ч, при температуре от 20 до 60°C, особенно предпочтительно при комнатной температуре (от 20 до 25°C).
3. Материал на основе кремниевого золя по п.1, отличающийся тем, что гидролитическую конденсацию на стадии а) осуществляют при температуре от 20 до 60°C, предпочтительно при температуре от 20 до 50°C и особенно предпочтительно при комнатной температуре (от 20 до 25°C), в течение промежутка времени, по меньшей мере, от 16 ч до 4 недель, предпочтительно от 18 ч до 4 недель, особенно предпочтительно от 24 ч до 18 дней и еще более предпочтительно от 3 до 8 дней.
4. Материал на основе кремниевого золя по п.1, отличающийся тем, что стадию b) реализуют в закрытой аппаратуре при реакционной температуре примерно от 30 до 90°C.
5. Материал на основе кремниевого золя по п.1, отличающийся тем, что раствор на стадии с) охлаждают до температуры от 2 до 4°C, предпочтительно до 4°C.
6. Материал на основе кремниевого золя по п.1, отличающийся тем, что созревание на стадии d) осуществляют при температуре от 2 до 4°C, предпочтительно при 4°C.
7. Материал на основе кремниевого золя по п.1, отличающийся тем, что созревание на стадии d) осуществляют до тех пор, пока вязкость золя при скорости сдвига 10 с-1 и температуре 4°C не составит от 30 до 100 Па·с, а коэффициент потерь при температуре 4°C, скорости сдвига 10 c-1 и деформации 1% не составит от 2 до 5.
8. Материал на основе кремниевого золя по одному из пп.1-7, отличающийся тем, что используемым на стадии а) соединением кремния является тетраэтоксисилан.
9. Применение материала на основе кремниевого золя по одному из пп.1-8 для изготовления биологически расщепляющихся и/или биологически рассасывающихся силикагелевых материалов.
10. Способ изготовления материала на основе кремниевого золя, по меньшей мере, 70% которого в пересчете на совокупную реакционную смесь пригодно для прядения, путем
a) по меньшей мере 16-часовой гидролитической конденсации одного или нескольких соединений кремния формулы (I):

в которой остатки Х одинаковые или разные, означают гидрокси, водород, галоген, амино, алкокси, ацилокси, алкилкарбонил и/или алкоксикарбонил и являются производными алкильных остатков, представляющих собой при необходимости замещенные неразветвленные, разветвленные или циклические остатки с 1-20 атомами углерода, предпочтительно с 1-10 атомами углерода, которые могут быть прерваны атомами кислорода или серы или аминогруппами,
b) упаривания с целью формирования однофазного раствора, которое предпочтительно реализуют при одновременном осторожном перемешивании реакционной системы,
c) охлаждения однофазного раствора и
d) кинетически контролируемого созревания с целью формирования материала на основе кремниевого золя.
11. Способ размножения клеток in-vitro, причем волокнистая матрица из волокон, полученных путем прядения материала на основе кремниевого золя по пп.1-8, выполняет функцию опорного материала для клеток и/или направляющей структуры для образуемой клетками внеклеточной матрицы.
12. Способ по п.11, причем волокна представляют собой филаментные нити, нетканые материалы или ткани.
13. Клеточный комплекс, ткань и/или орган, которые могут быть изготовлены способом по п.11 или 12.
| WO 00/50349 A2, 31.08.2000 | |||
| DE 19609551 C1, 17.07.1997 | |||
| СРЕДСТВО ДЛЯ ДОСТАВКИ, ОБЕСПЕЧИВАЮЩЕЕ НЕПРЕРЫВНОЕ И/ИЛИ РЕГУЛИРУЕМОЕ ВЫСВОБОЖДЕНИЕ БИОЛОГИЧЕСКИ АКТИВНЫХ АГЕНТОВ | 1997 |
|
RU2208582C2 |
| US 6624237 B2, 23.09.2003 | |||
| Устройство для порометрических измерений | 1978 |
|
SU775669A1 |
Авторы
Даты
2012-09-10—Публикация
2008-01-10—Подача