Изобретение относится к области медицины, конкретно к комбинации Клопидогреля и производного 3-гидроксипиридина, обладающей антиагрегантной и липидрегулируещей активностями, фармацевтической композиции на основе этой комбинации. В качестве производного 3-гидроксипиридина предлагается Этилметил-гидроксипиридина малат или Этилметилгидроксипиридина сукцинат (Мексидол).
В настоящее время профилактика и лечение нарушений процессов тромбообразования занимает одно из ведущих мест в терапии ишемической болезни сердца, инсультах, патологиях, связанных с усиленным тромбообразованием. За счет агрегации тромбоцитов антиагреганты более эффективно, чем антикоагулянты, предотвращают образование тромбов в артериальных сосудах. Эффективность антиагрегантов при венозных тромбозах существенно ниже.
Наиболее широкое распространение на практике получили ацетилсалициловая кислота и производные тиенопиридина - клопидогрель и тиклопидин (М.Д.Машковский. Лекарственные средства. М.: ООО "Новая волна", 2002, т.I, стр.466-468). Эти препараты имеют различный механизм проявления антиагрегантной активности.
Свойство тромбоцитов агрегировать друг с другом с образование ядра, вокруг которого формируется тромб, во многих случаях является причиной сужения сосудов и даже закупорки неповрежденных сосудов, если их эндотелий по каким-либо причинам нарушается. В норме скорость агрегации тромбоцитов определяется соотношением двух простагландинов - простациклина эндотелия и тромбоксана тромбоцитов. Простациклин, угнетающий адгезию тромбоцитов, не образуется в атеросклеротических бляшках, чем и объясняется ускоренное тромбообразование на их поверхности. В этой связи терапевтический эффект различных антиагрегантов при таких заболеваниях несомненен.
Антиагреганты применяют для профилактики послеоперационных тромбозов, в комплексном лечении тромбофлебитов, нарушениях мозгового кровообращения, для предупреждения тромбоэмболических осложнений при ишемической болезни сердца и инфаркте миокарда (Регистр лекарственных средств России РЛС-пациент, вып. №3, ООО РЛС-2002, с.626-629).
Одним из наиболее широко применяемых антиагрегантных препаратов является ацетилсалициловая кислота. Последняя в небольших дозах 50-125 мг препятствует образованию тромбоксана, но не простациклина. Поэтому ее применяют для профилактики инфаркта миокарда и сосудистых осложнений у пациентов, перенесших инфаркт миокарда.
Клопидогрель - новый (середина 1990-х гг.) антиагрегант, считающийся в настоящее время одним из лучших препаратов, применяемых для профилактики тромбообразования у больных ишемической болезнью сердца (после инфаркта миокарда), при атеросклерозе мозговых и периферических сосудов (М.Д.Машковский. Лекарственные средства. М.: ООО "Новая волна", 2002, т.I, стр.468).
Препарат необратимо изменяет АДФ рецептор тромбоцитов, нарушает связывание с ними АДФ, подавляя агрегацию тромбоцитов. Восстановление функции тромбоцитов происходит по мере их обновления в течение 7 суток. Клопидогрель быстро, но неполно всасывается из желудочно-кишечного тракта, интенсивно метаболизируется в печени. Время полувыведения основного циркулирующего метаболита - неактивного производного карболовой кислоты составляет 8 час. Около 50% выводится с мочой и столько же - с фекалиями в течение 5 суток после введения.
Применяют внутрь независимо от приема пищи по 75 мг 1 раз в сутки. Торможение агрегации тромбоцитов наблюдается через 2 часа после приема разовой дозы. Повторные дозы по 75 мг/кг приводят к значительному повышению АДФ-индуцированной агрегации (средний уровень подавления - 40-60%) с первого дня применения. Антиагрегационное действие стабилизируется через 3-7 дней от начала терапии и продолжается 7 дней после прекращения лечения (Энциклопедия лекарств. Регистр лекарственных средств России. Изд. 17, М.: «РЛС-2009», 2008 г., стр.438, 693-695).
Делалась попытка усилить эффективность препаратов для лечения патологии, вызванной агрегацией тромбоцитов, в которых действующие начала представляют собой Клопидогрель и Аспирин (патент РФ №2184547). Данный препарат предлагается для лечения устойчивой или неустойчивой стенокардии, расстройств сердечно-сосудистой и черепно-сосудистой систем или расстройств, которые возникают при использовании сосудистых протезов или аортокоронарных шунтирований. Недостатком данной комбинации является достаточное количество противопоказаний, обусловленных ограничением применения препаратов, входящих в состав данной комбинации (М.Д.Машковский. Лекарственные средства. М.: ООО "Новая волна", 2002, т.I, стр.466-468). Кроме того, эта комбинация не обладает липидрегулирующей активностью.
В терапии ишемической болезни сердца и инсультах немаловажное значение имеет также нормализация липидного обмена. Одним из способов воздействия на развившиеся нарушения липидного обмена является медикаментозная терапия.
За последние годы появилось несколько гиполипидемических препаратов с различными механизмами коррекции липидного гомеостаза. К последним могут быть отнесены никотиновая кислота, статины, пробукол и др. (М.Д.Машковский. Лекарственные средства. М.: ООО "Новая волна", 2002, т.I, стр.444-445, 448-453).
Сделана попытка объединить антитромботическую и липидрегулирующую активности. Так, предложена комбинация Клопидогреля и Симвастатина или Правастатина (патент РФ №2176504), применение которой рекомендуется для лечения стабильной или нестабильной стенокардии, рецидива стеноза после ангиопластики, эндартерэктомии или при установке металлических эндососудистых протезов. Недостатком данной комбинации является достаточное количество противопоказаний применения, обусловленных ограничением применения препаратов, входящих в состав данной комбинации (М.Д.Машковский. Лекарственные средства. М.: ООО "Новая волна", 2002, т.I, стр.444-445, 448-453), а также высокая стоимость препарата из-за использования импортных субстанций.
Поэтому весьма актуальным является поиск и разработка новых оригинальных препаратов, сочетающих в себе антиагрегантную и липидрегулирующую активности и обладающих менее выраженными побочными эффектами.
Поставленная цель достигается комбинацией Клопидогреля и производного 3-гидроксипиридина, являющегося синтетическим антиоксидантом. В качестве производного 3-гидроксипиридина предлагаются Этилметилгидроксипиридина малат или Этилметилгидроксипиридина сукцинат.
Получение комбинаций Клопидогреля и производного 3-гидроксипиридина осуществляют известным способом.
Пример 1. Получение комбинации Клопидогреля и Этилметилгидроксипиридина малата.
В подготовленном к работе смесителе первоначально смешивают 150,0 кг Этилметилгидроксипиридина малата, 24,0 кг крахмала картофельного, 42,0 кг сахара молочного. Порошки перемешивают в течение 10-12 минут, затем прибавляют 45,0 кг 10%-ного раствора пласдона К-90.
Смесь перемешивают до равномерного увлажнения. Увлажненную массу протирают на грануляторе через сито с диаметром отверстий 2 мм. Гранулы сушат при температуре 45-50°C до содержания влаги 1,5±0,5%. Высушенные гранулы протирают через сито с диаметром отверстий 1 мм и передают для опудривания. Получают 217,10 кг сухого гранулята, содержащего 147,69 кг Этилметилгидроксипиридина малата. Выход на стадии составляет 98,46%, считая на Этилметилгидроксипиридина малат.
Далее смешивают 146,82 кг Клопидогреля гидросульфата, 28,5 кг крахмала картофельного, 46,68 кг сахара молочного, затем прибавляют 60,0 кг 5%-ного раствора гидроксипропилцеллюлозы, смесь перемешивают до равномерного увлажнения. Увлажненную массу протирают через сито с диаметром отверстий 2 мм. Гранулы сушат при температуре 45-50°C до содержания влаги 1,5±0,5%. Высушенные гранулы протирают через сито с диаметром отверстий 1 мм и передают для опудривания. Получают 221,53 кг сухого гранулята, содержащего 144,56 кг Клопидогреля гидросульфата. Выход на стадии составляет 98,46%, считая на Клопидогрель гидросульфат.
Смесь гранулятов Этилметилгидроксипиридина малата и Клопидогреля опудривают смесью 1,484 кг кремния диоксида коллоидного и 2,969 кг стеарата магния до получения однородной массы. Получают 445,45 кг смеси порошков для капсулирования, содержащей 147,14 кг Этилметилгидроксипиридина малата и 144,02 кг Клопидогреля гидросульфата, которую передают на стадию капсулирования. Выход на стадии составляет 99,63%.
По ходу процесса капсулирования масса 20 капсул с содержимым должна быть 7,692 г +10%. С одной операции получают 431,91 кг порошка для капсулирования, содержащего 143,96 кг Этилметилгидроксипиридина малата и 140,93 кг Клопидогреля гидросульфата или 1439,7 тыс. штук наполненных капсул. Выход на стадии составляет 97,84%.
Общий выход готовой продукции составляет 94-95%.
Капсулы изготавливают массой 75 мг и 100 мг.
Пример 2. Получение комбинации Клопидогреля и Этилметилгидроксипиридина сукцината.
В подготовленном к работе смесителе первоначально смешивают 150,0 кг Этилметилгидроксипиридина сукцината, 26,0 кг крахмала картофельного; 38,0 кг сахара молочного. Порошки перемешивают в течение 10-12 минут, затем прибавляют 41,5 кг 10%-ного раствора пласдона К-90.
Смесь перемешивают до равномерного увлажнения. Увлажненную массу протирают на грануляторе через сито с диаметром отверстий 2 мм. Гранулы сушат при температуре 45-50°C до содержания влаги 1,5±0,5%. Высушенные гранулы протирают через сито с диаметром отверстий 1 мм и передают для опудривания. Получают 212,50 кг сухого гранулята, содержащего 146,3 кг Этилметилгидроксипиридина сукцината. Выход на стадии составляет 97,50%, считая на Этилметилгидроксипиридина сукцинат.
Далее смешивают 146,82 кг Клопидогреля гидросульфата, 25,7 кг крахмала картофельного, 51,34 кг сахара молочного, затем прибавляют 66,0 кг 5%-ного раствора гидроксипропилцеллюлозы, смесь перемешивают до равномерного увлажнения. Увлажненную массу протирают через сито с диаметром отверстий 2 мм. Гранулы сушат при температуре 45-50°С до содержания влаги 1,5±0,5%. Высушенные гранулы протирают через сито с диаметром отверстий 1 мм и передают для опудривания. Получают 223,1 кг сухого гранулята, содержащего 144,8 кг Клопидогреля гидросульфата. Выход на стадии составляет 98,62%, считая на Клопидогрель гидросульфат.
Смесь гранулятов Этилметилгидроксипиридина сукцината и Клопидогреля опудривают смесью 1,48 кг кремния диоксида коллоидного и 2,97 кг стеарата магния до получения однородной массы. Получают 445,3 кг смеси порошков для капсулирования, содержащей 146,97 кг Этилметилгидроксипиридина сукцината и 144,10 кг Клопидогреля гидросульфата, которую передают на стадию капсулирования. Выход на стадии составляет 99,68%.
По ходу процесса капсулирования масса 20 капсул с содержимым должна быть 7,692 г±10%. С одной операции получают 431,89 кг порошка для капсулирования, содержащего 143,91 кг Этилметилгидроксипиридина сукцината и 140,95 кг Клопидогреля гидросульфата или 1439,8 тыс. штук наполненных капсул. Выход на стадии составляет 97,87%.
Общий выход готовой продукции составляет 94-95%.
Капсулы изготавливают массой 75 мг и 100 мг.
Предметом настоящего исследования явилось сравнительное изучение антиагрегантной активности Клопидогреля, а также комбинации Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат в капсульной лекарственной форме, а также сравнительное изучение липидрегулирующей активности Этилметилгидроксипиридина малата или Этилметилгидроксипиридина сукцината и комбинации Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат в капсульной лекарственной форме.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В работе использовали капсулы препарата Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат. Состав на одну капсулу: Клопидогреля гидросульфата 0,0979 г (в пересчете на Клопидогрель 0,075 г), Этилметилгидроксипиридина малата или Этилметилгидроксипиридина сукцината 0,1 г, а также вспомогательные вещества - сахар молочный (лактоза), крахмал картофельный, пласдон К-90, гидроксипропилцеллюлоза (Клуцел LF), магния стеарат, аэросил (кремния диоксид коллоидный). Масса содержимого капсулы 0,3 г. Содержимое капсул представляет собой порошок или гранулы белого с желтоватым или кремоватым оттенком цвета. Капсулы кремового цвета №0.
В первой части исследования по изучению антиагрегантной активности опыты проводились на нелинейных белых крысах массой 250-300 г с использованием схемы эксперимента, изложенной в работе Yoichi Niitsu (Yoichi Niitsu, Atsuhiro Sugidachi, Taketoshi Ogawa, Josef A. Jakubowski, Masami Hashimoto, Takashi Isobe, Kenichi Otsuguro, Fumitoshi Asai. Repeat oral dosing of prasugel, a novel P2Y12 receptor ingibitor, results in cumulative and potent antiplatelet and antitrombotic activity in several animal species // European Journal of Pharmacology, v.579, 2008, p.276-282). Для акклиматизации животные содержались в виварии в течение 14 дней до начала эксперимента при 18-22°C и влажности 50-60% в стандартных клетках при 12-часовом режиме освещения день-ночь на стандартном пищевом рационе и воде в соответствии с нормами, утвержденными МЗ РФ.
Животных делили на 3 группы по 8 голов в каждой:
1. Интактный контроль (животным в течение 3 суток перорально вводили дистиллированную воду);
2. Клопидогрель (животным в течение 3 суток перорально вводили раствор Клопидогреля в дозе 10 мг/кг);
3. Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат (животным в течение 3 суток перорально вводили суспензию Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат в дозе 10 мг по Клопидогрелю/кг).
Суточная доза была близка к максимальной терапевтической суточной для человека (75 мг/60-70 кг веса) с учетом межвидового переноса доз для крыс, составляющего 1:7. Кроме того, выбранная доза для Клопидогреля соответствовала оптимальной для аналогичных исследований в ранее цитированной работе (Yoichi Niitsu, Atsuhiro Sugidachi, Taketoshi Ogawa, Josef A. Jakubowski, Masami Hashimoto, Takashi Isobe, Ken-ichi Otsuguro, Fumitoshi Asai. Repeat oral dosing of prasugel, a novel P2Y12 receptor ingibitor, results in cumulative and potent antiplatelet and antitrombotic activity in several animal species // European Journal of Pharmacology, v.579, 2008, p.276-282).
Вещества вводили внутрижелудочно в 2,0 мл 4%-ного крахмального геля в течение 3 дней. Число животных в каждой группе было одинаковым (8 крыс). Через 4 часа после последнего введения животных декапитировали, кровь собирали в тефлоновую посуду, содержащую 0,13 M цитрата натрия в соотношении 1:9, центрифугировали при 200 g за 7 мин и супернатант, представляющий собой богатую тромбоцитами плазму (БТП), использовали для изучения процесса АДФ-индуцированной агрегации тромбоцитов. Для получения обедненной тромбоцитами плазмы (ОТП) использовали повторное центрифугирование при 2000 g за 15 мин.
При проведении анализа использовали метод, основанный на анализе флуктуаций светопропускания образца суспензии, вызванных изменениями числа частиц в оптическом канале устройства в богатой тромбоцитами плазме после добавления индуктора агрегации - раствора АДФ - методу Борна/О'Браена (Габбасов З.А., Попов Е.Г., Гаврилов И.Ю., Позин Е.Я., Маркосян Р.А. Новый высокочувствительный метод анализа агрегации тромбоцитов. Лабораторное дело, 1989, №10, с.15-18. Габбасов З.А., Попов Е.Г., Гаврилов И.Ю., Позин Е.Я., Маркосян Р.А. Новый методический подход к исследованию агрегации тромбоцитов in vitro. Бюллетень экспериментальной биологии и медицины, 1989, №10, с.437-439).
Анализ проводили на разработанном в ГКНЦ компьютеризированном анализаторе агрегации тромбоцитов.
В опыте в термостатируемую при 37°C кювету, содержащую микромешалку, вводили 0,3 мл БТП, проводили калибровку с помощью ОТП. Далее к 0,3 мл БТП добавляли 10 мкл 155 мкМ раствора АДФ до конечной концентрации 5 мкМ и регистрировали изменение светопропускания, пропорциональное проценту агрегации, рассчитываемое в соответствии с разработанной программой.
Во второй части исследования по изучению липидрегулирующей активности исследования проводили на нелинейных белых крысах-самцах с исходной массой 220-250 г, полученных из питомника. Для акклиматизации животные содержались в виварии в течение 14 дней до начала эксперимента при 18-22°С и влажности 50-60% в стандартных клетках при 12-часовом режиме освещения день-ночь на стандартном пищевом рационе и воде в соответствии с нормами, утвержденными МЗ РФ. За 18 часов перед забоем крыс лишали корма, вода оставалась в достаточном количестве.
Животных делили на 4 группы по 8 голов в каждой:
1. Интактный контроль (животным в течение 3 суток перорально вводили дистиллированную воду);
2. Атерогенная диета;
3. Атерогенная диета+Этилметилгидроксипиридина малат или Этилметилгидроксипиридина сукцинат (Габбасов З.А., Попов Е.Г., Гаврилов И.Ю., Позин Е.Я., Маркосян Р.А. Новый методический подход к исследованию агрегации тромбоцитов in vitro. Бюллетень экспериментальной биологии и медицины, 1989, №10, с.437-439. Габбасов З.А., Попов Е.Г., Гаврилов И.Ю., Позин Е.Я., Маркосян Р.А. Новый методический подход к исследованию агрегации тромбоцитов in vitro. Бюллетень экспериментальной биологии и медицины, 1989, №10, с.437-439) (животным в течение 10 суток перорально давали атерогенную диету и вводили раствор Этилметилгидроксипиридина малата или Этилметилгидроксипиридина сукцината в дозе 10 мг/кг);
4. Атерогенная диета+(Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат) (животным в течение 10 суток перорально давали атерогенную диету и вводили суспензию Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат в дозе 10 мг по Этилметилгидроксипиридина малату или Этилметилгидроксипиридина сукцинату/кг).
Суточная доза была близка к терапевтической суточной для человека (100 мг/60-70 кг веса) с учетом межвидового переноса доз для крыс, составляющего 1:7.
Вещества вводили внутрижелудочно в 2,0 мл 4%-ного крахмального геля в течение 10 дней. Число животных в каждой группе было одинаковым (8 крыс).
Гиполипидемическую активность оценивали по степени торможения индуцированной гиперлипидемии (Парфентьева Е.П., Василенко Ю.К., Лисевицкая Л.И. и др. Влияние урсоловой кислоты на некоторые показатели липидного обмена при экспериментальном атеросклерозе. - Вопр. мед. химии. - 1980. - №2. - С.174-179), анализируя следующие биохимические показатели в сыворотке крови:
- общий холестерин (ХС-общий),
- холестерин ЛПВП (ХС-ЛПВП),
- холестерин ЛПНП (ХС-ЛПНП),
- холестерин ЛПОНП (ХС-ЛПОНП),
- триглицериды (ТГ).
Определение содержания общего холестерина
Содержание ХС в сыворотке крови определяли методом Илька (Родионова Л.П. Модификация метода определения содержания триглицеридов в сыворотке крови. - Лаб. дело. - 1980. - №5. - С.297-299) - зиматическим колориметрическим методом. Принцип метода заключается в том, что присутствующие в плазме или сыворотке крови эфиры холестерина гидролизуются холестеролэстеразой. При этом образуется свободный холестерин. Образовавшийся и имеющийся в плазме или сыворотке крови холестерин окисляется кислородом воздуха под действием холестеролоксидазы с образованием эквимолярного количества перекиси водорода. Под действием пероксидазы (POD) перекись водорода окисляет хромогенный субстрат с образованием окрашенного продукта. Интенсивность окраски пропорциональна концентрации холестерина в пробе.
Определение концентрации общего холестерина в сыворотке и плазме крови проводили с помощью набора реагентов CHOLESTEROL"E-D" фирмы «Витал Диагностикс СПб».
Состав набора:
№1. Буфер: фосфатный буфер - 100 ммоль/л; фенол - 20 ммоль/л.
№2. Лиофилизат холестеролэстераза - 400 U/л, холестеролоксидаза - 250 U/л, пероксидаза (POD) - 500 U/л.
№3. Стандартный раствор холестерина: 5,17 ммоль/л (200 мг/100 мл).
При проведении анализа смесь лиофилизированных ферментов растворяют в буферном растворе №1, раствор выдерживают при комнатной температуре 20-30 мин. В пробирку помещают 2 мл полученного реагента, добавляют 0,02 мл сыворотки или плазмы (опытная проба). Одновременно приготавливают калибровочную и контрольную пробы. Для этого к 2 мл реагента добавляют 0,02 мл калибровочного раствора холестерина (калибровочная проба) или 0,02 мл дистиллированной воды (контрольная проба). Реакционную смесь тщательно перемешивают и инкубируют не менее 5 минут при комнатной температуре (20-25°С) или при 37°C.
Далее измеряют оптическую плотность опытной и калибровочной проб против контрольной пробы в кюветах с толщиной поглощающего слоя 5 мм (1 см) при длине волны 500 нм.
Расчет концентрации холестерина проводят по формуле:
С=Ео/Ест·5,17 [ммоль/л] или С=Ео/Ест·200 [мг/100 мл],
где Ео и Ест - экстинкции образца и стандарта, измеренные относительно контрольной пробы.
Определение концентрации липопротеидов высокой плотности
ХС-ЛПВП оценивали в супернатанте после гепарин-марганцевой преципитации ЛПОНП+ЛПНП (Кейтс М. Техника липидологии. - М.: Мир, 1975. - С.74-76).
В принципе метода лежит то, что хиломикроны, липопротеиды очень низкой плотности (ХС-ЛПОНП) и липопротеиды низкой плотности осаждаются при добавлении к образцу фосфорновольфрамовой кислоты и солей Mg и удаляются центрифугированием. После центрифугирования в супернатанте остаются только липопротеиды высокой плотности (ХС-ЛПВП), концентрация которых определяется так же, как концентрация общего холестерина.
Определение концентрации липопротеидов высокой плотности в сыворотке и плазме крови проводили с помощью набора реагентов CHOLESTEROL"FL-E" фирмы «Витал Диагностикс СПб».
Состав набора:
№1. Осаждающий реагент - фосфорновольфрамовая кислота - 55 ммоль/л, магния хлорид - 25 ммоль/л.
Ход определения. В пробирку помещают 0,15 мл исследуемой плазмы или сыворотки, затем 0,3 мл осаждающего реагента, хорошо перемешивают и оставляют на 10 мин при комнатной температуре. Центрифугируют 10 мин при 4000 об/мин при температуре 4-6°C. Прозрачный супернатант используют для определения концентрации липопротеидов высокой плотности при помощи реактивов и методики для определения концентрации общего холестерина.
Определение содержания триглицеридов
Триглицериды или нейтральные жиры представляют собой сложные эфиры глицерина и трех остатков жирных кислот, чаще всего с 16 или 18 атомами углерода. Точный состав жирнокислотных остатков может колебаться в определенных пределах и зависит, главным образом, от характера питания. Поэтому говорят о триглицериде не как об индивидуальном химическом веществе, а как о группе родственных соединений. Это осложняет выражение результатов анализа в весовых единицах, т.е. в г/л или мг/100 мл, так как существующие аналитические методы позволяют определять количество молекул триглицеридов, но молекулярная масса в разных образцах может быть несколько отличной. Другая аналитическая сложность вызвана нестойкостью сложноэфирной связи, которая легко распадается в щелочной среде, а также под действием ферментов сыворотки или микроорганизмов.
Содержание в сыворотке крови ТГ определяли общепринятым методом (Родионова Л.П. Модификация метода определения содержания триглицеридов в сыворотке крови. - Лаб. дело. - 1980. - №5. - С.297-299). В работе применен метод определения концентрации триглицеридов в сыворотке и плазме крови с помощью набора реагентов TRIGLYCERIDES "E-D" фирмы «Витал Диагностикс СПб». Принцип метода состоит в том, что триглицериды под действием фермента липазы расщепляются на глицерин и жирные кислоты. Далее глицерин в присутствии АТФ и фермента глицерокиназы превращается в глицерид-3-фосфат, который под действием кислорода и фермента глицерофосфатоксидазы превращается в диоксиацетон фосфат, при этом образуется перекись водорода. Перекись водорода воздействует на 4-аминоантипирин и 4-хлорфенол в присутствии пероксидазы, при этом образуется хинонимин. Концентрация хинонимина, определяемая фотометрически, пропорциональна концентрации триглицеридов в пробе.
Состав набора:
№1. Буфер TRIS буфер - 50 ммоль/л, рН 7,5, 4-хлорфенол - 4 ммоль/л, Mg - 1 ммоль/л.
№2. Лиофилизат АТФ - 2 ммоль/л, Пероксидаза - 5000 U/л, Липаза - 150 U/л, Глицерокиназа - 1200 U/л, Глицерофосфатоксидаза - 4000 U/л, 4-аминоантипирин - 0,4 ммоль/л.
№3. Стандартный раствор 250 мг/100 мл.
При проведении анализа смесь лиофилизированных ферментов и реактивов (№2) растворяют в буферном растворе №1, раствор выдерживают при комнатной температуре 20-30 мин. В пробирку помещают 2 мл полученного реагента, добавляют 0,02 мл сыворотки или плазмы (опытная проба). Одновременно приготавливают калибровочную и контрольную пробы. Для этого к 2 мл реагента добавляют 0,02 мл калибровочного раствора триглицеридов (калибровочная проба) или 0,02 мл дистиллированной воды (контрольная проба). Реакционную смесь тщательно перемешивают и инкубируют не менее 5 минут при комнатной температуре (20-25°C).
Далее измеряют оптическую плотность опытной и калибровочной проб против контрольной пробы в кюветах с толщиной поглощающего слоя 5 мм (1 см) при длине волны 505 нм.
Расчет концентрации триглицеридов проводят по формуле:
С=(Ео/Ест·2,85) - 0,11 [ммоль/л] или С=(Ео/Ест·250) - 10 [мг/100 мл],
где Ео и Eст - экстинкции образца и стандарта, измеренные относительно контрольной пробы.
0,11 ммоль/л и 10 мг/100 мл поправка на содержание свободного глицерина в сыворотке (плазме) крови.
Определение содержания холестерина липопротеидов низкой плотности и холестерина липопротеидов очень низкой плотности
Определение ХС-ЛПНП проводили путем расчета по формуле (Грибанов Г.А., Сергеев С.А. Экспресс-микроанализ общих липидов сыворотки крови и их фракций. - Вопр. мед. химии. - 1975. - Т.21, №6. - С.652-655). Зная количество холестерина ЛПВП, можно, используя формулу, предложенную Rifkind, рассчитать содержание холестерина (ХС) в ЛПОНП и ЛПНП:

Содержание холестерина ЛПОНП рассчитывается по формуле:
ХЛ ЛПОНП=Триглицериды/5.
Расчет коэффициента атерогенности
Холестериновый коэффициент атерогенности (Кхс) рассчитывали по (Родионова Л.П. Модификация метода определения содержания триглицеридов в сыворотке крови. - Лаб. дело. - 1980. - №5. - С.297-299).
Для оценки влияния изученных препаратов на соотношение атерогенных и антиатерогенных липопротеидов крови вычисляли индекс атерогенности по формуле:
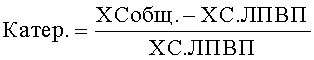 .
.
Постановка эксперимента
Гиперлипидемию индуцировали у беспородных крыс-самцов массой 220-250 г атерогенным рационом, содержавшим в масляной суспензии 10% холестерина и 1% холевой кислоты (из расчета 1,0 мл жировой нагрузки на 100 г массы тела) (Федеральное руководство по использованию лекарственных средств (формулярная система). Вып.4, под ред. А.Г.Гучалина, А.И.Вялкова, Ю.Б.Белоусова, В.В.Яснецова, М., 2003, с.106-112).
Экспериментальным животным вводили жировую суспензию (зондом, внутрижелудочно) в течение 10 дней и одновременно внутрижелудочно вводили исследованные препараты (в 2%-ном крахмальном геле) в дозе 10,0 мг Этилметилгидроксипиридина малата или Этилметилгидроксипиридина сукцината/кг и комбинацию Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат в той же дозе по Этилметилгидроксипиридина малату или Этилметилгидроксипиридина сукцинату.
Полученные данные обрабатывались общепринятым методом с использованием в качестве критерия различия средних двух выборок t критерия Стьюдента. Разница между результатами считалась достоверной при уровне значимости Р<0,05 (Плохинский П.А. Биометрия. - Новосибирск, 1961).
В таблицах приведены средние арифметические значения параметров агрегации для каждой группы животных и их стандартные ошибки.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Полученные данные по изучению антиагрегантной активности препаратов ин виво представлены в Таблице 1.
Как следует из результатов, приведенных в таблице, у животных контрольной группы степень максимальной АДФ-индуцированной агрегации тромбоцитов колеблется от 41 до 63%, составляя в среднем 47,9±2,4%.
При 3-кратном введении Клопидогреля через 4 часа после последнего введения интенсивность АДФ-индуцированной агрегации существенно снижалась и колебалась от 23 до 47%, составляя в среднем 34,1±2,9 с t-критерием Стьюдента 3,67 в сравнении с контрольной группой, что соответствует уровню вероятности различий более 95%.
Аналогично при введении комбинации Клопидогрель+Этилметилгидроксипиридина малат или Клопидогрель+Этилметилгидроксипиридина сукцинат наблюдается снижение интенсивности АДФ-индуцированной агрегации с колебаниями от 32 до 51%, в среднем до 37,3±3,3% с t-критерием Стьюдента 2,60 в сравнении с контрольной группой, что соответствует уровню вероятности различий.
Комбинация Клопидогрель+Этилметилгидроксипиридина сукцинат также обладала антиагрегантной активностью.
Величины снижения интенсивности агрегаций в опытных группах животных (22-27%) достоверно не различались между собой: статистически значимого различия между показателями при введении исследованных препаратов Клопидогрель+Этилметилгидроксипиридина малат и Клопидогрель+Этилметилгидроксипиридина сукцинат не выявлено.
Кроме того, Этилметилгидроксипиридина сукцинат и Этилметилгидроксипиридина малат обладают меньшей токсичностью и меньшим количеством побочных эффектов, чем известные антиагрегантные и липидрегулирующие препараты (патент РФ №2377237).
Полученные данные по изучению липидрегулирующей активности Этилметилгидроксипиридина малата, комбинации Клопидогрель+Этилметилгидроксипиридина малат, Этилметилгидроксипиридина сукцината, комбинации Клопидогрель+Этилметилгидроксипиридина сукцинат ин виво при 10-дневном введении с атерогенной диетой представлены в Таблице 2.
Как следует из результатов, приведенных в таблице, у животных контрольной группы при атерогенной диете гиперлипидемия приводит к достоверному повышению уровня ТГ и общего ХС в сыворотке крови крыс, причем наблюдаемая гиперхолестеринемия развилась за счет атерогенных фракций липопротеидов на фоне снижения уровня ХС-ЛПВП. Индекс атерогенности возрос до 2,028±0,200, превышая этот показатель группы интактных животных в 2 раза.
Введение экспериментальным животным Этилметилгидроксипиридина малата в виде субстанции в дозе 10 мг/кг в течение 10 дней замедлило развитие патологического процесса - снизился уровень общего холестерина в 1,27 раза, ТГ - в 1,56 раза и ХС в составе атерогенных фракций липопротеидов - в 1,38 раза. Величина коэффициента атерогенности снизилась в 1,5 раза.
Как следует из представленных в таблице 2 данных, как и в предыдущем случае, при введении комбинации Клопидогрель+Этилметилгидроксипиридина малата в дозе 10 мг (малата)/кг животным в течение 10 дней в такой же степени, как и введение при монотерапии Этилметилгидроксипиридина малата в виде субстанции в дозе 10 мг/кг также в течение 10 дней замедлило развитие патологического процесса - снизился уровень общего холестерина в 1,3 раза, ТГ - в 1,4 раза и ХС в составе атерогенных фракций липопротеидов - в 1,70 раза. Величина коэффициента атерогенности снизилась в 1,85 раза.
Аналогичным действием обладал и Этилметилгидроксипиридина сукцинат, а также комбинация Клопидогрель+Этилметилгидроксипиридина сукцинат в дозе 10 мг (сукцината)/кг.
Следует отметить, что при сравнении эффектов капсулированной формы Клопидогрель+Этилметилгидроксипиридина малат и Клопидогрель+Этилметилгидроксипиридина сукцинат достоверные отличия отсутствуют, причем для обоих препаратов характерна липидрегулирующая активность.
Таким образом, доказано, что комбинация Клопидогреля и производного 3-гидроксипиридина, в качестве которого предлагается Этилметилгидроксипиридина малат или Этилметилгидроксипиридина сукцинат, обладает антиагрегантной и липидрегулируещей активностями. Кроме того, в силу того, что Этилметилгидроксипиридина малат и Этилметилгидроксипиридина сукцинат обладают гораздо меньшей токсичностью (патент РФ №2377237), чем известные препараты с атерогентной и липидрегулирующей активностями, также менее токсичны заявляемые комбинации известных препаратов с вышеназванной активностью.
пиридина малат (субстанция)
пиридина малат)
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНАЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ, ЛИПИДРЕГУЛИРУЮЩЕЙ И ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2453314C1 |
| 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЙГИДРОКСИБУТАНДИОАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ, НЕЙРОТРОПНОЙ И ЛИПИДРЕГУЛИРУЕМОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2377237C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-L-ГЛУТАМИЛГИСТАМИНА, ПРИМЕНЕНИЕ ГАММА-L-ГЛУТАМИЛГИСТАМИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2141968C1 |
| СПОСОБ ПРОФИЛАКТИКИ НАРУШЕНИЙ ЛИПИДНОГО ОБМЕНА | 2009 |
|
RU2423123C1 |
| ПРОТИВОИШЕМИЧЕСКОЕ И АНТИАТЕРОСКЛЕРОТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1998 |
|
RU2144822C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2004 |
|
RU2268714C1 |
| ГАММА-ГИДРОКСИПРОПИЛАМИНИЙ-5-ГИДРОКСИНИКОТИНАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2245329C1 |
| Новое производное 3-гидроксипиридина, обладающее липидрегулирующей активностью | 2020 |
|
RU2743923C1 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2141483C1 |
| N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕВЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГИПОЛИПИДЕМИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2335495C2 |
Изобретение относится к медицине и фармацевтической промышленности, а именно к комбинации Клопидогреля и Этилметилгидроксипиридина. Композиция на основе этой комбинации представлена в виде твердой фармацевтической композиции, а именно в виде капсул. Композиция Клопидогреля и Этилметилгидроксипиридина перспективна для профилактики и лечения ожирения; патологических состояний сердечно-сосудистой системы; профилактики ишемических нарушений с выраженным атеросклерозом; перенесенного инфаркта, ишемического инсульта; заболевания периферических артерий. 2 н.п. ф-лы, 2 табл.
1. Фармацевтическая комбинация, обладающая антиагрегантной и липидрегулирующей активностями, характеризующаяся тем, что содержит Клопидогрель и Этилметилгидроксипиридина малат или сукцинат в терапевтически эффективных количествах.
2. Твердая дозированная фармацевтическая композиция, характеризующаяся тем, что содержит в качестве действующих веществ комбинацию по п.1.
| Беликов В.Г | |||
| Фармацевтическая химия, т.1 | |||
| - M.: Высшая школа, 1993, с.43-47 | |||
| ПРОТИВОТРОМБОЦИТНАЯ И АНТИАТЕРОГЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТИЕНПИРИДИНОВОЕ ПРОИЗВОДНОЕ И ИНГИБИТОР HMG-KОA-РЕДУКТАЗЫ | 1997 |
|
RU2176504C2 |
| 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЙГИДРОКСИБУТАНДИОАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ, НЕЙРОТРОПНОЙ И ЛИПИДРЕГУЛИРУЕМОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2377237C1 |
| «Мексидола», 14.07.2006 [Найдено 23.01.2012, найдено в Интернете: http://meksidola.lek-va.ru/]. | |||
Авторы
Даты
2012-09-20—Публикация
2010-12-09—Подача