ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретении относится к фармацевтической композиции для лечения фибромиалгии или аналогичных заболеваний.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0002]
Синдром фибромиалгии представляет собой заболевание, характеризующееся болями, причины заболевания неизвестны, и в Японии около двух миллионов человек страдают синдромом фибромиалгии. Наиболее характерной чертой указанного заболевания является отсутствие аномальных симптомов при проведении обычного обследования, за исключением субъективных симптомов, таких как боль. Ввиду этого существуют трудности с постановкой точного диагноза, что может привести к ситуации, при которой либо лечение является невозможным, либо симптомы не могут рассматриваться как заболевание.
[0003]
Диагностирование фибромиалгии проводится с использованием метода, в соответствии с которым ссылка дается на критерии классификации синдрома фибромиалгии, опубликованные в 1990 году Американской коллегией ревматологии (АКР) (непатентный документ 1). Ниже обобщены примеры характерных особенностей при диагностике заболевания: 1) наличие постоянной боли в течение 3 месяцев и более; 2) отсутствие аномальных симптомов при проведении обычного обследования и 3) ощущение боли в 11 точках или более из 18 предварительно определенных точек чувствительности при надавливании с усилием в 4 кг или менее. Кроме того, оценку состояний заболевания также проводили с использованием показателя, называемого опросником воздействия при фибромиалгии (FIQ).
[0004]
Примеры симптомов синдрома фибромиалгии включают болевой симптом, физический симптом, неврологический симптом и психологический симптом. Специфические особенности болевых симптомов включают ощущение скованности, боли в суставах и мышцах, боли позади глазных яблок, боли в ротовой полости и головные боли. Кроме того, примеры физических симптомов включают бессонницу, чувство истощения, чувство усталости, сухой кератоконъюнктивит (синдром сухого глаза), ксеростомию (сухость слизистой оболочки рта), частое мочеиспускание, диарею, констипацию, энтерит, интерстициальный цистит, дисменорею и нарушение менструального цикла. Примеры неврологических симптомов включают снижение уровня болевого порога конечностей, онемение, головокружение, шум в ушах и желудочно-кишечные расстройства. Примеры физиологических симптомов включают чувство беспокойства, раздражительности, депрессию, нарушение сна и нарушение сосредоточенности и внимания. Как указывалось выше, синдром фибромиалгии проявляется кроме боли в виде различных симптомов.
[0005]
Примеры терапевтических средств для лечения фибромиалгии включают антидепрессанты, транквилизаторы, противовоспалительные средства (болеутоляющие средства). Тем не менее, существуют возможности для усовершенствования указанных терапевтических средств в плане повышения терапевтического эффекта.
Документы, отражающие известный уровень техники
Непатентные документы
[0006]
Непатентный документ 1: Wolfe F. et al., Arthritis Rheum., Feb. 1990, vol. 33(2), pp.160-172.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ С ПОМОЩЬЮ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0007]
При указанных выше обстоятельствах существует необходимость разработки нового терапевтического средства для лечения фибромиалгии.
СПОСОБЫ РЕШЕНИЯ ЗАДАЧИ ИЗОБРЕТЕНИЯ
[0008]
В результате проведения интенсивных исследований с целью решения вышеуказанных проблем настоящее изобретение разработано на основе открытия того факта, что фармацевтическая композиция, включающая пилокарпин или его фармакологически приемлемую соль, является эффективной при лечении фибромиалгии или аналогичных заболеваний.
[0009]
Таким образом, настоящее изобретение предусматривает создание нижеприведенной фармацевтической композиции для лечения фибромиалгии или аналогичных заболеваний.
(1) Фармацевтическая композиция для лечения фибромиалгии, включающая пилокарпин или его фармакологически приемлемую соль.
(2) Композиция по пункту (1) выше, в которой фармакологически приемлемая соль представляет собой гидрохлорид пилокарпина.
(3) Композиция по пункту (1) или пункту (2) выше, дополнительно включающая, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
(4) Применение пилокарпина или его фармакологически приемлемой соли для производства фармацевтической композиции для лечения фибромиалгии.
(5) Фармацевтическая композиция для лечения фибромиалгии, включающая комбинацию, как минимум, одного компонента, выбранного из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли и пилокарпин или его фармакологически приемлемую соль.
(6) Фармацевтическая композиция для лечения фибромиалгии, включающая пилокарпин или его фармакологически приемлемые соли в качестве активного ингредиента, предназначенного для лечения пациента, принимающего композицию, включающую, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
(7) Набор лекарственных средств для лечения фибромиалгии, включающий композицию, содержащую пилокарпин или его фармакологически приемлемые соли, в качестве активного ингредиента и композицию, включающую, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
(8) Способ для лечения фибромиалгии, включающий введение пилокарпина или его фармакологически приемлемых солей.
(9) Способ по пункту (8) выше, в котором фармакологически приемлемая соль является гидрохлоридом пилокарпина.
(10) Способ по пункту (8) или пункту (9) выше, дополнительно включающий введение, как минимум, одного компонента, выбранного из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
[0010]
В соответствии с настоящим изобретением предусматривается создание фармацевтической композиции для лечения фибромиалгии или аналогичных заболеваний. Композиция или аналогичная композиция настоящего изобретения является эффективной для лечения фибромиалгии или аналогичных заболеваний.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
[0011]
ФИГ.1 - опросник в отношении симптомов сухости слизистой оболочки рта (Пример 2).
ФИГ.2 - опросник в отношении симптомов сухого глаза, сухости слизистой оболочки носа, сухости кожи и сухости влагалища (Пример 2).
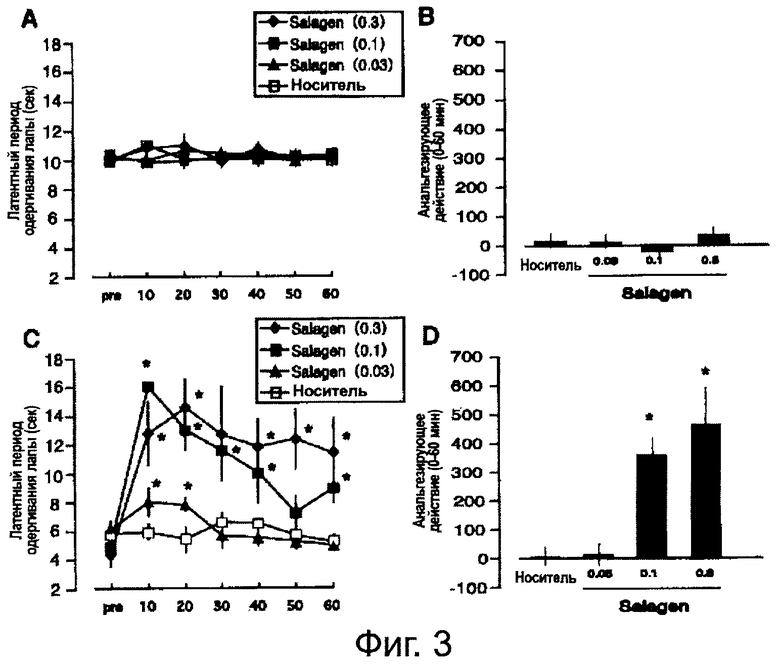
ФИГ.3 - диаграмма, иллюстрирующая анальгезирующее действие гидрохлорида пилокарпина (Пример 3). Данные выражены в виде среднего ±S.E.M (стандартная погрешность среднего) (n=4-9). * р<0,05 (сравнение с контрольной группой, получающей носитель). А: Диаграмма, иллюстрирующая изменения анальгезирующего действия гидрохлорида пилокарпина (Salagen (торговое название)) (0,3, 0,1, 0,01 мг/кг, при пероральном введении) во времени в контрольной группе (в условиях отсутствия стресса). В: Диаграмма, иллюстрирующая анальгезирующее действие в зависимости от дозы гидрохлорида пилокарпина (Salagen (торговое название)) (0,3, 0,1, 0,01 мг/кг, при пероральном введении) в контрольной группе (данные выражены в виде площади под фармакокинетической кривой (AUC)). С: Диаграмма, иллюстрирующая изменения анальгезирующего действия гидрохлорида пилокарпина (Salagen (торговое название)) (0,3, 0,1, 0,01 мг/кг, при пероральном введении) во времени в модельной группе, подвергшейся интермиттирующему стрессу от холода (ICS) (при стрессовом состоянии). D: Диаграмма, иллюстрирующая анальгезирующее действие в зависимости от дозы гидрохлорида пилокарпина (Salagen (торговое название)) (0,3, 0,1, 0,01 мг/кг, при пероральном введении) в модельной группе, подвергшейся интермиттирующему стрессу от холода (данные выражены в виде площади под фармакокинетической кривой).
ПРЕДПОЧТИТЕЛЬНЫЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0012]
Ниже приведено подробное описание настоящего изобретения.
Все публикации, приведенные в настоящем описании, например документы, содержащие информацию об известном уровне техники, выложенные патентные заявки, публикации патента и иные патентные документы, инкорпорированы в настоящее описание по ссылке. Кроме того, настоящее описание включает содержание, раскрытое в формуле изобретения, в описании изобретения и в реферате заявки на патент Японии №2008-130140, на основе которой заявляется приоритет.
[0013]
1. Краткое описание настоящего изобретения
Фармацевтическая композиция для лечения фибромиалгии настоящего изобретения включает пилокарпин или его фармакологически приемлемые соли. Предпочтительно, чтобы фармакологически приемлемая соль являлась гидрохлоридом пилокарпина. Известно, что гидрохлорид пилокарпина обладает действием, стимулирующим мускариновый рецептор и устраняющим симптомы сухости слизистой оболочки рта, связанные с радиотерпапией головы или шеи, либо симптомы сухости слизистой оболочки рта у пациентов с синдромом Шегрена. Когда авторы настоящего изобретения ввели гидрохлорид пилокарпина пациентам с фибромиалгией, как минимум, один симптом, включающий боли, сухость слизистой оболочки рта, сухой кератоконъюнктивит, интерстициальный цистит, раздражающий кишечный синдром или аналогичные симптомы, был устранен. На основе этого наблюдения было обнаружено, что композиция, включающая пилокарпин или его фармакологически приемлемые соли, является эффективной для лечения фибромиалгии. Композиция в соответствии с настоящим изобретением предпочтительно включает кроме пилокарпина или его фармакологически приемлемой соли, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
[0014]
2. Синдром фибромиалгии
Остается неизвестным не только механизм, инициирующий синдром фибромиалгии, но и не был разработан способ его лечения. Это обусловлено тем фактом, что синдром фибромиалгии кроме боли проявляется в виде различных симптомов (таких как физические симптомы, неврологические симптомы и психологические симптомы). Другими словами, синдром фибромиалгии является характеризующимся болями заболевания, причины которого неизвестны и которое проявляется в виде болевых симптомов, физических симптомов, неврологических симптомов и психологических симптомов. Специфические примеры болевых симптомов включают ощущение скованности, боли в суставах и мышцах, боли позади глазных яблок, боли в ротовой полости и головные боли. Кроме того, примеры физических симптомов включают бессонницу, чувство истощения, чувство усталости, сухой кератоконъюнктивит (синдром сухого глаза), ксеростомию (сухость слизистой оболочки рта), частое мочеиспускание, диарею, констипацию, энтерит, интерстициальный цистит, дисменорею и нарушение менструального цикла. Примеры неврологических симптомов включают снижение уровня болевого порога конечностей, онемение, головокружение, шум в ушах и желудочно-кишечные расстройства. Примеры физиологических симптомов включают чувство беспокойства, раздражительности, депрессию, нарушение сна и нарушение сосредоточенности и внимания. Как указывалось выше, синдром фибромиалгии проявляется кроме боли в виде различных симптомов.
[0015]
Диагностирование синдрома фибромиалгии проводится, например, с использованием метода, в соответствии с которым ссылка дается на критерии классификации синдрома фибромиалгии, опубликованные в 1990 году Американской коллегией ревматологии (АКР) (Wolfe F. et al., Arthritis Rheum., Feb. 1990, vol. 33(2), pp.160-172). В частности, примеры характерных особенностей при диагностике заболевания включают: 1) наличие постоянной боли в течение 3 месяцев и более; 2) отсутствие аномальных симптомов при проведении обычного обследования и 3) ощущение боли в 11 точках или более из 18 предварительно определенных точек чувствительности при надавливании с усилием в 4 кг или менее.
[0016]
3. Пилокарпин или его фармакологически приемлемые соли
Химическое название пилокарпина - (3S,4R)-3-этил-4-(1-метил-1Н-имидазол-5-илметил)-4,5-дигидрофуран-2(3Н)-он. Фармакологически приемлемая соль пилокарпина включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты) и соли органических кислот (такие как ацетаты или метансульфонат). Фармакологически приемлемая соль пилокарпина предпочтительно является солью неорганической кислоты (такие как гидрохлориды или нитраты) и более предпочтительно является гидрохлоридом.
[0017]
Пилокарпин может быть изготовлен с использованием стандартного способа. Описание способа изготовления пилокарпина приведено, например, в "An improved synthesis of pilocarpine" (J.I.Degraw, Tetrahydron Vol.28, Issue 4, 1972).
[0018]
Пилокарпин, а также его фармакологически приемлемая соль могут быть изготовлены с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке продукты. Примеры имеющихся на рынке продуктов пилокарпина включают гидрохлорид пилокарпина и нитраты пилокарпина, производимые Sigma-Aldrich, Inc.
[0019]
Пилокарпин или его фармакологически приемлемую соль, полученную таким образом, используют в качестве активного ингредиента в фармацевтической композиции для лечения фибромиалгии в соответствии с настоящим изобретением, как описано ниже.
[0020]
4. Фармацевтическая композиция
Фармацевтическая композиция для лечения фибромиалгии в соответствии с настоящим изобретением включает пилокарпин или его фармакологически приемлемые соли. Кроме того, настоящее изобретение также предусматривает применение пилокарпина или его фармакологически приемлемых солей для изготовления фармацевтической композиции для лечения фибромиалгии. Путем введения фармацевтической композиции в соответствии с предпочтительным примером осуществления настоящего изобретения пациентам с синдромом фибромиалгии может быть устранен, как минимум, один симптом, выбранный из группы, состоящей из болевых симптомов (таких как ощущение скованности, боли в суставах и мышцах, боли позади глазных яблок, боли в ротовой полости и головные боли), физических симптомов (таких как бессонница, чувство истощения, чувство усталости, сухой кератоконъюнктивит (синдром сухого глаза), ксеростомия (сухость слизистой оболочки рта), частое мочеиспускание, диарея, констипация, энтерит, интерстициальный цистит, дисменорея и нарушение менструального цикла), неврологических симптомов (таких как снижение уровня болевого порога конечностей, онемение, головокружение, шум в ушах и желудочно-кишечные расстройства) и физиологических симптомов (таких как чувство беспокойства, раздражительности, депрессия, нарушение сна и нарушение сосредоточенности и внимания). Более предпочтительно фармацевтическая композиция в соответствии с предпочтительным примером осуществления настоящего изобретения позволяет устранить, как минимум, один симптом, включающий боли, ксеростомию, сухой кератоконъюнктивит, интерстициальный цистит, раздражающий кишечный синдром или аналогичные симптомы.
[0021]
Несмотря на то, что лекарственная форма фармацевтической композиции настоящего изобретения может быть предназначена либо для перорального введения, либо парентерального введения, предпочтительным является пероральное введение.
[0022]
Указанные лекарственные формы могут быть составлены с использованием стандартного способа и также могут включать фармацевтически приемлемые носитель или добавку. Примеры таких носителей и добавок включают воду, фармацевтически приемлемый органический растворитель, коллаген, поливиниловый спирт, поливинилпирролидон, карбоксивиниловый полимер, карбоксиметилцеллюлозу натрия, полиакрилат натрия, алгинат натрия, водорастворимый декстран, карбоксиметиловый крахмал натрия, пектин, метилцеллюлозу, этилцеллюлозу, ксантановую камедь, арабскую камедь, казеин, агар, полиэтиленгликоль, диглицерол, глицерол, пропиленгликоль, вазелин, парафин, стеариловый спирт, стеариновую кислоту, альбумин сыворотки человека, маннитол, сорбитол, лактозу и поверхностно активные вещества, являющиеся приемлемыми в качестве медицинской добавки.
[0023]
Вышеуказанную добавку выбирают либо по отдельности, либо в соответствующем сочетании из указанных выше примеров в зависимости от лекарственной формы фармацевтической композиции настоящего изобретения. В случае перорального введения лекарственная форма может представлять собой таблетки, капсулы, небольшие гранулы, порошки, гранулы, жидкие лекарственные препараты, сиропы или аналогичные лекарственные формы либо может быть введен соответствующий состав. При парентеральном введении примеры лекарственной формы включают инъекции. В случае инъекции, например, лекарственное средство может быть введено системно или местно путем введения внутривенных инъекций, таких как внутривенное вливание.
[0024]
Также могут быть использованы имеющиеся на рынке составы в качестве композиции, включающей пилокарпин или его фармацевтически приемлемую соль. Примеры имеющихся на рынке составов включают таблетки Salagen (торговое название) (активный ингредиент: гидрохлорид пилокарпина, изготавливаемый компанией Kissei Pharmaceutical Co., Ltd.).
[0025]
Доза пилокарпина или его фармакологически приемлемой соли изменяется в зависимости от возраста, пола и симптомов пациента, а также способа введения, частоты введения и лекарственной формы. Например, при введении лекарственного средства взрослому человеку (60 кг) ежедневная доза может составлять от 0,1 мг до 1000 мг, от 1 мг до 100 мг или от 2,5 мг до 60 мг (например, 2,5 мг, 5 мг, 10 мг, 15 мг, 20 мг, 25 мг, 30 мг, 35 мг, 40 мг, 45 мг, 50 мг, 55 мг или 60 мг). Способ введения соответственно выбирают в зависимости от возраста и симптомов пациента. Лекарственное средство может быть введено, например, один раз в день либо может быть разделено на две - четыре дозы в день.
[0026]
Кроме того, фармацевтическая композиция настоящего изобретения также может включать дополнительно к пилокарпину или его фармакологически приемлемой соли, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли. В данном случае выражение «включает» означает, что, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, а также пилокарпин или его фармакологически приемлемые соли включены в состав одного и того же препарата.
[0027]
В другом случае фармацевтическая композиция настоящего изобретения может представлять собой фармацевтическую композицию, включающую сочетание, как минимум, одного компонента, выбранного из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, а также пилокарпин или его фармакологически приемлемые соли. В данном случае выражение «включает сочетание» означает, что, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, а также пилокарпин или его фармакологически приемлемые соли включены состав отдельных препаратов. В тех случаях, когда, как минимум, два компонента выбраны из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, компоненты могут быть включены в состав одного и того же препарата либо могут быть включены в состав отдельных препаратов, однако предпочтительным является их включение в состав отдельных препаратов.
[0028]
В ином случае фармацевтическая композиция настоящего изобретения может представлять собой фармацевтическую композицию, включающую пилокарпин или его фармакологически приемлемые соли в качестве активного ингредиента, предназначенного для пациента, принимающего композицию, включающую, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
[0029]
Химическое название габапентина - (1-аминометилциклогексил) уксусная кислота. Фармакологически приемлемая соль габапентина включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты). Габапентин, а также его фармакологически приемлемая соль могут быть изготовлены с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке их продукты. Примеры имеющихся на рынке продуктов габапентина, а также его фармакологически приемлемой соли включают таблетки Gabapen (торговое название) (активный ингредиент: габапентин, изготавливаемый компанией Pfizer Japan Inc.).
[0030]
Химическое название прегабалина - (S)-3-(аминометил)-5-метилгексановая кислота. Фармакологически приемлемая соль прегабалина включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты). Прегабалин, а также его фармакологически приемлемая соль могут быть изготовлены с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке их продукты. Примеры имеющихся на рынке продуктов прегабалина и его фармакологически приемлемой соли включают Lyrica (торговое название) (активный ингредиент: прегабалин, изготавливаемый компанией Pfizer Japan Inc.).
[0031]
Экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, может быть изготовлен с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Примеры имеющихся на рынке его продуктов включают таблетки Neurotropin (торговое название) (активный ингредиент: экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, изготавливаемый компанией Nippon Zoki Pharmaceutical Co., Ltd.).
[0032]
Клоназепам, а также его фармакологически приемлемая соль могут быть изготовлены с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Фармакологически приемлемая соль клоназепама, в частности, включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты). Примеры имеющихся на рынке продуктов клоназепама и его фармакологически приемлемой соли включают Rivotril (торговое название) (активный ингредиент: клоназепам, изготавливаемый компанией Chugai Pharmaceutical Co., Ltd.).
[0033].
Милнаципран может быть изготовлен с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Фармакологически приемлемая соль милнаципрана, в частности, включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты), и, в частности, примеры включают гидрохлорид милнаципрана. Примеры имеющихся на рынке продуктов милнаципрана включают Toledomin (торговое название) (активный ингредиент: гидрохлорид милнаципрана, изготавливаемый компанией Asahi Kasei Pharma Corporation).
[0034]
Пароксетин может быть изготовлен с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Фармакологически приемлемая соль пароксетина, в частности, включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты), и, в частности, примеры включают гидрохлорид пароксетина. Примеры имеющихся на рынке продуктов пароксетина включают Paxil (торговое название) (активный ингредиент: гидрохлорид пароксетина, изготавливаемый компанией GlaxoSmithKline plc.).
[0035]
Амитриптилин может быть изготовлен с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Фармакологически приемлемая соль амитриптилина, в частности, включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты), и, в частности, примеры включают гидрохлорид амитриптилина. Примеры имеющихся на рынке продуктов амитриптилина включают Tryptanol (торговое название) (активный ингредиент: гидрохлорид амитриптилина, изготавливаемый компанией Banyu Pharmaceutical Co., Ltd.).
[0036]
Миансерин может быть изготовлен с использованием стандартного способа либо могут быть приобретены имеющиеся на рынке его продукты. Фармакологически приемлемая соль миансерина, в частности, включает без ограничения, например, соли неорганических кислот (такие как гидрохлориды или нитраты), соли неорганических оснований (такие как соли натрия, соли калия или соли кальция) и соли органических кислот (такие как ацетаты, бензоаты, малеаты, тартраты, фумараты или мезилаты), и, в частности, примеры включают гидрохлорид миансерина. Примеры имеющихся на рынке продуктов миансерина включают Tetramide (торговое название) (активный ингредиент: гидрохлорид миансерина, изготавливаемый компанией Organon-Japan).
[0037]
В указанных случаях, когда габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли используют в сочетании, дозы указанных веществ изменяются в зависимости от возраста, пола и симптомов пациента, способа введения, частоты введения и лекарственной формы. Доза габапентина или его фармакологически приемлемых солей, вводимая взрослому человеку (60 кг) в день, может, например, составлять от 1 мг до 360 г, от 10 мг до 36 г или от 50 мг до 7200 мг. Доза прегабалина или его фармакологически приемлемых солей, вводимая взрослому человеку (60 кг) в день, может, например, составлять от 0,2 мг до 60 г, от 2 мг до 6 г или от 10 мг до 1200 мг. При приеме таблеток Neurotropin (торговое название) взрослым человеком (60 кг), например, доза экстракта из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, в день может составлять от 0,1 единицы нейротропина до 3200 единиц нейротропина, от 1 единицы нейротропина до 320 единиц нейротропина или от 4 единиц нейротропина до 64 единиц нейротропина. При лечении взрослого пациента (60 кг), например, доза клоназепама или его фармакологически приемлемой соли в день может составлять от 0,005 мг до 600 мг, от 0,05 мг до 60 мг или от 0,25 мг до 12 мг. При лечении взрослого пациента (60 кг), например, доза милнаципрана или его фармакологически приемлемой соли в день может составлять от 0,3 мг до 10 г, от 3 мг до 1 г или от 15 мг до 200 мг. При лечении взрослого пациента (60 кг), например, доза пароксетина или его фармакологически приемлемой соли в день может составлять от 0,1 мг до 4 г, от 1 мг до 400 мг или от 5 мг до 80 мг. При лечении взрослого пациента (60 кг), например, доза амитриптилина или его фармакологически приемлемой соли в день может составлять от 0,1 мг до 30 г, от 1 мг до 3 г или от 5 мг до 600 мг. При лечении взрослого пациента (60 кг), например, доза миансерина или его фармакологически приемлемой соли в день может составлять от 0,3 мг до 6 г, от 3 мг до 600 мг или от 15 мг до 120 мг. Способ введения лекарственного средства выбирают соответствующим образом в зависимости от возраста и симптомов пациента. Например, лекарство может вводиться один раз в день или может быть разделено на две - четыре дозы в день.
[0038]
Несмотря на то, что доза, как минимум, одного компонента, выбранного из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, в частности, не ограничена и отличается в зависимости от отдельных сочетаний с пилокарпином или его фармакологически приемлемыми солями, например, доза превышает от приблизительно 0,001 до 10000 раз (из расчета весового отношения) или от приблизительно 0,003 до 5000 раз (из расчета весового отношения) дозу пилокарпина или его фармакологически приемлемой соли.
[0039]
В указанных случаях, когда, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли, и пилокарпин или его фармакологически приемлемые соли включены в состав отдельных препаратов, указанные препараты могут быть введены одновременно либо любой один из них может быть введен первым, после чего могут быть введены другие препараты.
[0040]
Примеры других лекарственных средств, которые могут быть использованы в сочетании с фармацевтической композицией настоящего изобретения, включают лекарственное средство, которое может быть изготовлено в виде состава для лечения синдрома фибромиалгии. Конкретные примеры таких лекарственных средств включают таблетки Myslee (торговое название) (активный ингредиент: золпидема тартрат, изготавливаемый компанией Astellas Pharma Inc.), таблетки Gaster (торговое название) (активный ингредиент: фамотидин, изготавливаемый компанией Astellas Pharma Inc.) и таблетки Depas (торговое название) (активный ингредиент: этизолам, изготавливаемый компанией Mitsubishi Tanabe Pharma Corporation).
[0041]
5. Набор лекарственных средств
Набор лекарственных средств для лечения фибромиалгии в соответствии с настоящим изобретением включает композицию, содержащую пилокарпин или его фармакологически приемлемые соли в качестве активного ингредиента, и композицию, включающую, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
Набор лекарственных средств настоящего изобретения может также включать упаковочный контейнер, инструкцию по медицинскому применению препарата, листок-вкладыш или аналогичный информационный листок дополнительно к вышеуказанным композициям. В упаковочном контейнере в инструкции по медицинскому применению препарата, листке-вкладыше или аналогичном информационном листке может быть приведена информация о дозировке и способах введения либо аналогичная информация для применения вышеуказанных композиций в различных сочетаниях. Описание дозировки и способов введения может быть приведено со ссылкой на пояснения в отношении вышеуказанных фармацевтических композиций.
[0042]
6. Способ лечения
Настоящее изобретение предусматривает создание способа для лечения фибромиалгии, включающего введение пилокарпина или его фармакологически приемлемой соли. В данном случае предпочтительно, чтобы фармакологически приемлемая соль являлась гидрохлоридом пилокарпина. Более того, дополнительно к пилокарпину или его фармакологически приемлемой соли предпочтительно вводить, как минимум, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли. В способе для лечения фибромиалгии в соответствии с настоящим изобретением отсутствуют конкретные ограничения по пути введения, и могут быть даны ссылки на способ введения пилокарпина или его фармакологически приемлемой соли и на описание вышеуказанных фармацевтических композиций.
[0043]
За счет применения способа лечения в соответствии с предпочтительной особенностью настоящего изобретения в отношении пациентов, страдающих синдромом фибромиалгии, может быть устранен, как минимум, один симптом, выбранный из группы, состоящей из болевых симптомов (таких как ощущение скованности, боли в суставах и мышцах, боли позади глазных яблок, боли в ротовой полости и головные боли), физических симптомов (таких как бессонница, чувство истощения, чувство усталости, сухой кератоконъюнктивит (синдром сухого глаза), ксеростомия (сухость слизистой оболочки рта), частое мочеиспускание, диарея, констипация, энтерит, интерстициальный цистит, дисменорея и нарушение менструального цикла), неврологических симптомов (таких как снижение уровня болевого порога конечностей, онемение, головокружение, шум в ушах и желудочно-кишечные расстройства) и физиологических симптомов (таких как чувство беспокойства, раздражительности, депрессия, нарушение сна и нарушение сосредоточенности и внимания). Более предпочтительно способ лечения в соответствии с предпочтительным примером осуществления настоящего изобретения позволяет устранить, как минимум, один симптом, включающий боли, ксеростомию, сухой кератоконъюнктивит, интерстициальный цистит, раздражающий кишечный синдром или аналогичные симптомы.
[0044]
Ниже, в частности, приведено описание настоящего изобретения со ссылками на примеры. Тем не менее, настоящее изобретение не ограничено указанными примерами.
ПРИМЕРЫ
[0045]
[Пример 1]
Таблетки Salagen 5 мг (торговое название) (активный ингредиент: гидрохлорид пилокарпина), изготавливаемые компанией Kissei Pharmaceutical Co., Ltd., принимали 22 пациента с синдромом фибромиалгии (двое мужчин и 20 женщин), которым был поставлен диагноз на основе диагностических критериев Американской коллегии ревматологии (Wolfe F. et al., Arthritis Rheum., Feb. 1990, vol. 33(2), pp.160-172), в течение предварительно определенного периода времени для подтверждения их эффективности. В частности, примеры, в которых изложено описание лечения 4-х из 22-х пациентов, принимавших лекарственное средство, приведены ниже.
[0046]
1. Пациент А с синдромом фибромиалгии (52 года, пол - женский)
До приема таблеток Salagen 5 мг (торговое название) у пациентки наблюдали каждый симптом сухого кератоконъюнктивита (синдром сухого глаза), ксеростомии, раздражающего кишечного синдрома и интерстициального цистита.
Пациентка принимала две таблетки Salagen 5 мг (торговое название) в день (т.е. 10 мг/день). Указанная пациентка также получала таблетки Toledomin 25 (торговое название), таблетки Gabapen 200 мг (торговое название) и таблетку Rivotril 1 мг (торговое название) дополнительно к таблеткам Salagen 5 мг. Соответствующие дозы в день приведены ниже.
Таблетки Toledomin 25 (торговое название): 3 таблетки в день (т.е. 75 мг/день).
Таблетки Gabapen 200 мг (торговое название): 5 таблеток в день (т.е. 1000 мг/день).
Таблетки Rivotril 1 мг (торговое название): 1 таблетка в день (т.е. 1 мг/день).
После обследования указанной пациентки спустя 14 дней после начала приема таблеток Salagen 5 мг (торговое название) наблюдалось облегчение симптомов ксеростомии и раздражающего кишечного синдрома. В частности, были облегчены симптомы ксеростомии, и были устранены затруднения, связанные с приемом пищи. Кроме того, были облегчены симптомы раздражающего кишечного синдрома при одновременном уменьшении диареи.
[0047]
2. Пациент В с синдромом фибромиалгии (52 года, пол - женский)
До приема таблеток Salagen 5 мг (торговое название) у пациентки наблюдали каждый симптом сухого кератоконъюнктивита (синдром сухого глаза), ксеростомии и ксеродермии.
Указанная пациентка принимала половину таблетки Salagen 5 мг (торговое название) в день (т.е. 2,5 мг/день). Указанная пациентка также получала таблетки Gabapen 200 мг (торговое название), таблетку Myslee 5 мг (торговое название) и таблетки Gaster 10 мг (торговое название) дополнительно к половине таблетки Salagen 5 мг (торговое название) (т.е. 2,5 мг). Соответствующие дозы в день приведены ниже.
Таблетка Gabapen 200 мг (торговое название): 3 таблетки в день (т.е. 600 мг/день).
Таблетка Myslee 5 мг (торговое название): 1 таблетка в день (т.е. 5 мг/день).
Таблетка Gaster 10 мг (торговое название): 2 таблетки в день (т.е. 20 мг/день).
После обследования указанной пациентки спустя 28 дней после начала приема таблеток Salagen (торговое название) наблюдалось облегчение симптомов сухого кератоконъюнктивита, ксеростомии и раздражающего кишечного синдрома. В частности, были облегчены симптомы сухого кератоконъюнктивита, и инстилляция была уменьшена до одного раза в день. Более того, были облегчены симптомы ксеростомии, и выделялась слюна, которая текла тонкой струйкой из уголка рта. Кроме того, были облегчены симптомы ксеродермии, кожа стала влажной, и, таким образом, отпала необходимость в нанесении крема Hirudoid (торговое название) на кожу.
[0048]
3. Пациент С с синдромом фибромиалгии (71 год, пол - женский)
До приема таблеток Salagen 5 мг (торговое название) у указанной пациентки наблюдались симптомы системных болей, сухого кератоконъюнктивита и ксеростомии.
Указанная пациентка принимала одну таблетку Salagen 5 мг (торговое название) в день (т.е. 5 мг/день).
При обследовании указанной пациентки спустя 28 дней после начала приема таблеток Salagen 5 мг (торговое название) наблюдалось облегчение симптомов сухого кератоконъюнктивита и ксеростомии. С другой стороны, не были облегчены симптомы системных болей.
[0049]
4. Пациент D с синдромом фибромиалгии (29 лет, пол - женский)
До приема таблеток Salagen 5 мг (торговое название) у указанной пациентки кроме симптомов боли наблюдались симптомы сухого кератоконъюнктивита, ксеростомии, раздражающего кишечного синдрома и интерстициального цистита.
Указанная пациентка принимала две таблетки Salagen 5 мг (торговое название) в день (т.е. 10 мг/день). Указанная пациентка также получала таблетки Toledomin 25 (торговое название), таблетки Gabapen 200 мг (торговое название) и таблетку Depas 0,5 мг (торговое название) дополнительно к таблетке Salagen 5 мг (торговое название). Соответствующие дозы в день приведены ниже.
Таблетка Toledomin 25 (торговое название): 2 таблетки в день (т.е. 50 мг/день).
Таблетка Gabapen 300 мг (торговое название): 4 таблетки в день (т.е. 1200 мг/день).
Таблетка Depas 0,5 мг (торговое название): 1 таблетка в день (т.е. 0,5 мг/день).
При обследовании пациентки спустя 14 дней после начала приема таблеток Salagen 5 мг (торговое название) наблюдалось облегчение симптомов сухого кератоконъюнктивита, ксеростомии, раздражающего кишечного синдрома и интерстициального цистита. В частности, были облегчены симптомы сухого кератоконъюнктивита и уменьшена частота инстилляции. Кроме того, были облегчены симптомы раздражающего кишечного синдрома при отсутствии абдоминальных болей. Дополнительно к указанному были облегчены симптомы интерстициального цистита, устранены боли во время мочеиспускания, а также была уменьшена частота мочеиспускания.
[0050]
Как указывалось выше, было обнаружено, что при приеме гидрохлорида пилокарпина пациентами с синдромом фибромиалгии может быть облегчен, как минимум, один симптом, включающий боли, ксеростомию, сухой кератоконъюнктивит и интерстициальный цистит или подобные симптомы.
[0051]
Ниже приведены сводные данные о примере с 22-мя пациентами (двое мужчин и 20 женщин), которые принимали таблетки Salagen 5 мг (торговое название).
Достоверные: 6 примеров (4 примера из указанных 6 примеров были приведены выше).
Недостоверные и прерванные: 7 примеров.
Прерванные ввиду проявления побочных эффектов: 2 примера (чрезмерные потоотделение: 1 пример, высыпание на коже: 1 пример).
На настоящий момент определены эффекты по 7-ми примерам.
[0052]
[Пример 2]
Нижеприведенные пациенты с синдромом фибромиалгии, которые были диагностированы на основе диагностических критериев Американской коллегии ревматологии (Wolfe F. et al., Arthritis Rheum., Feb. 1990, vol.33(2), pp.160-172), принимали таблетки Salagen 5 мг (торговое название) (активный ингредиент: гидрохлорид пилокарпина), изготавливаемые компанией Kissei Pharmaceutical Co., Ltd., в течение заданного периода времени для подтверждения их эффекта.
[0053]
Пациент Е с синдромом фибромиалгии (54 года, пол - женский)
До приема таблеток Salagen 5 мг (торговое название) указанная пациентка ответила на каждый из вопросов в «опроснике в отношении симптомов сухости слизистой оболочки рта», приведенном на ФИГ.1, и в «опроснике в отношении симптомов сухих глаз, сухой слизистой оболочки носа, сухой кожи и сухого влагалища», приведенном на ФИГ.2. В частности, пациентка ответила на каждый из вопросов, прочертив вертикальную линию на расстоянии, указывающем на текущее состояние на горизонтальной линии (длина: 95 мм), начинающейся от фразы «абсолютное отсутствие симптома» и заканчивающейся у фразы «резко выраженный симптом». После сбора опросников измеряли длину (мм) от точки «абсолютное отсутствие симптома» до вертикальной линии, начерченной в положении, указывающем на текущее состояние, по каждому ответу, и результаты измерений приведены в таблице 1 ниже. Как показано в таблице 1, до приема таблеток Salagen 5 мг дополнительно к симптомам боли у указанной пациентки наблюдались симптомы сухого кератоконъюнктивита, ксеростомии и ксеродермии.
Таким образом, пациентка принимала две таблетки Salagen 5 мг (торговое название) в день (т.е. 10 мг/день). Указанная пациентка также получала таблетки Depas (торговое название), Mobic (торговое название), Gabapen (торговое название) и Neurotropin (торговое название) дополнительно к таблеткам Salagen 5 мг (торговое название). Соответствующие дозы в день приведены ниже.
Таблетки Depas (торговое название): 1 таблетка в день (т.е. 0,5 мг/день).
Таблетки Mobic (торговое название): 1 таблетка в день (т.е. 10 мг/день).
Таблетки Gabapen (торговое название): 1 таблетка в день (т.е. 300 мг/день).
Таблетки Neurotropin (торговое название): 4 таблетки в день (т.е. 16 единиц/день).
Спустя 7 дней с начала приема таблеток Salagen 5 мг (торговое название) указанная пациентка еще раз ответила на каждый вопрос в «опроснике в отношении симптомов сухости слизистой оболочки рта», приведенном на ФИГ.1, и в «опроснике в отношении симптомов сухих глаз, сухой слизистой оболочки носа, сухой кожи и сухого влагалища», приведенном на ФИГ.2. Результаты ответов также приведены в таблице 1 ниже. Кроме того, в таблице 1 значение, определенное путем деления значения, полученного до приема, на значение, полученное после приема, также указано как степень облегчения симптомов. Как показано в таблице 1, при сравнении состояния пациента до и после приема таблеток Salagen 5 мг (торговое название) наблюдалось облегчение каждого из симптомов сухого кератоконъюнктивита, ксеростомии и ксеродермии.
[0054]
«Абсолютное отсутствие симптома» - «Резко выраженный симптом»: 0-95 Единица измерения: мм
[0055]
[Пример 3]
I. Способ
1. Экспериментальные животные и экспериментальная среда
Во всех экспериментах использовали самцов мышей C57BL/6J в возрасте от 6 до 14 недель. Мышей кормили в помещении с постоянной температурой (24±2°С) и с постоянной влажностью (55±5%) при 12-часовом (с 8:00 до 20:00) цикле дня и ночи со свободным доступом к кормовым гранулам (умеренная жировая диета, Oriental Yeast Co., Ltd., Tokyo) для проведения стандартного эксперимента и к питьевой воде.
В плане экспериментальной среды в лаборатории использовали помещение с постоянной температурой (24±2°С) и постоянной влажностью (55±5%). Мышей, использовавшихся в эксперименте, разместили в помещении за 24 часа до начала эксперимента и кормили до эксперимента при 12-часовом (с 8:00 до 20:00) цикле дня и ночи со свободным доступом к кормовым гранулам (умеренная жировая диета, Oriental Yeast Co., Ltd., Tokyo) для проведения стандартного эксперимента и к питьевой воде.
Далее эксперимент проводили в интервале с 10 часов утра до 5 часов вечера. Эксперимент по введению лекарственного средства проводили в период времени, в течение которого стабильно наблюдались симптомы болевой гиперчувствительности, обусловленные интермиттирующим стрессом от холода с 5 дня до 14 дня после прекращения стресса.
Все эксперименты проводили в соответствии как с рекомендациями для проведения экспериментов на животных в университет Нагасаки, так и в соответствии со способом, указанным Международным комитетом по проведению экспериментов по оценке боли (номер разрешения для проведения экспериментов на животных: 0706130596).
[0056]
2. Введение лекарственного средства
Использовали таблетки гидрохлорида пилокарпина (Salagen (торговое название)), изготавливаемые компанией Kissei Pharmaceutical Co., Ltd. Также использовали гидрохлорид пилокарпин, закупленный у компании Wako Pure Chemical Industries, Ltd. Соответствующие лекарственные средства, растворенные в стерильной дистиллированной воде, вводили перорально в виде одноразовой дозы. Было использовано три дозы (т.е. в концентрациях 0,03 мг/кг, 0,1 мг/кг и 0,3 мг/кг). Мышам контрольной группы перорально вводили стерильную дистиллированную воду.
При интраперитонеальном введении и при пероральном введении на каждые 10 г веса тела вводили 0,1 мл.
[0057]
3. Создание мышиной модели
Модель интермиттирующего стресса от холода
(Модель хронической боли, обусловленная повторяющимся раздражением холодом)
Была использована модель интермиттирующего стресса от холода в качестве экспериментальной модели на животных для фибромиалгии. В настоящей модели уже было выявлено, что пролонгированная форма гипералгезии развивается после стресса, что в значительной степени аналогично клиническим симптомам у человека.
В плане температуры кормления в отношении мышиной модели интермиттирующего стресса от холода в дневное время повторяли цикл комнатной температуры (т.е. 24°С) и пониженной температуры (т.е. 4°С) и регулировали до пониженной температуры в ночное время. В плане среды кормления, во избежание образования влаги другая клетка была установлена перевернутой на верхнюю часть экрана клетки, и между клеткой и экраном был создан зазор с помощью кусочка кормовой гранулы (умеренная жировая диета, Oriental Yeast Co., Ltd., Tokyo) для проведения стандартного эксперимента. Кроме того, стерильную дистиллированную воду желировали с помощью агара (изготавливаемого компанией Asahi & Co., Ltd.) (1 г агара на 100 мл воды), полученное желе разрезали на кусочки размером 1 кв. см и мышей кормили в условиях постоянной влажности (55±5%) при 12-часовом (с 8:00 до 20:00) цикле дня и ночи со свободным доступом к кусочкам агара в качестве кормовых гранул и к воде.
В 16:30 на день 0 мыши, использовавшиеся в эксперименте, были перемещены вовнутрь холодильника в условия пониженной температуры, и их кормление продолжалось в холодильнике до 10:00 следующего дня.
На следующий день (день 1) в 10:00 мыши были помещены в условия комнатной температуры, и далее их кормление проводилось до 16:30 попеременно при пониженной температуре в течение 30 минут и при комнатной температуре в течение 30 минут.
На 2-й день кормление мышей проводилось таким же образом, как и в 1-й день, и далее мышей поместили в условия комнатной температуры в 10:00 на 3-й день для завершения эксперимента.
Мышей из контрольной группы кормили при комнатной температуре в течение трех дней.
[0058]
4. Способ оценки поведения, связанного с болевыми ощущениями
Тест Харгрейвса (тест отдергивания лап на тепловой стимул): способ испытаний по оценке боли при тепловом раздражении
Используемую в эксперименте мышь помещали в пластиковую клетку, установленную на стеклянной пластине, и мышь находилась в указанной среде в течение 30 или более минут для акклиматизации. Тепловой раздражитель проецировали в центр подушечки стопы задних конечностей снизу стеклянной пластины, измеряли и проводили оценку латентного периода до тех пор, пока у мыши в задней конечности не проявлялась реакция избегания (т.е. латентный период одергивания лапы). В эксперименте раздражитель подавался таким образом, чтобы у нормальных животных обеспечивалось достижение латентного периода в размере 10-12 секунд, и время завершения теста устанавливали на 20 секунд с целью предотвращения повреждения ткани.
[0059]
5. Измерение порогового значения в мышиной модели интермиттирующего стресса от холода и эффекта лекарственного средства на болевую гиперчувствительность.
I) Оценка болевой гиперчувствительности во времени
Анализ по измерению порогового значения проводили с использованием теста Харгрейвса. День, на который приступили к созданию интермиттирующего стресса от холода, определяли как день 0, день на который завершали создание интермиттирующего стресса от холода, определяли как послестрессовый день 1 (Р1) и далее значения болевого порога измеряли вплоть до послестрессового дня Р15. Латентный период и интенсивность измеряли три раза или более и принимали среднее значение. Кроме того, устанавливали временной интервал в размере 10 минут до тех пор, пока не проводилось измерение следующего порогового значения. Причина установления такого временного интервала заключалась в предотвращении ранее измеренного воздействия от теплового раздражителя.
[0060]
II) Анальгезирующее действие гидрохлорида пилокарпина
Оценка была проведена путем измерения с использованием теста Харгрейвса. После определенного периода времени, необходимого для адаптации, раствор лекарственного средства, приготовленный путем растворения таблеток гидрохлорида, перорально вводили в виде одноразовой дозы и измеряли латентный период до тех пор, пока не проявлялась реакция избегания. Латентный период измеряли через каждые 10 минут после введения лекарства в течение 60 минут. Мышам из контрольной группы перорально вводили стерильную дистиллированную воду. Анальгезирующее действие гидрохлорида пилокарпина определяли путем расчета площади под фармакокинетической кривой от кривой зависимости во времени и путем вычитания площади под фармакокинетической кривой при проведении параллельной линии в направлении х-оси по отношению к пороговому значению до введения лекарственного средства.
[0061]
6. Статистическая обработка данных
Были проанализированы данные во времени и площади под фармакокинетической кривой анальгезирующего действия с использованием t-теста для двух независимых групп. В отношении площади под фармакокинетической кривой было проведено сравнение группы мышей, которым вводили лекарственное средство, и группы мышей, которым не вводили его в группе мышей интермиттирующего стресса от холода. В плане статистики уровень значимости был установлен на 5% (указанный значком *), и все результаты выражены в виде среднего ±S.E.M (стандартная погрешность среднего).
Был использован тест-F Шеффе для проведения статистического анализа данных во времени. Данный тест проводится для сравнения среди всех независимых мультигрупп, в которых сначала проводили однофакторный дисперсионный анализ, и, если результат показывал существенное различие между группами, далее проводили многократный тест для определения того, между какими группами существует различие. Указанный тест проводили в целях сравнения анальгезирующего действия, вызываемого дозировкой только таблеток гидрохлорида пилокарпина с анальгезирующим действием, наблюдаемым в группе, принимавшей плацебо. В плане статистики уровень значимости был установлен на 5% (указанный значком *), и все результаты выражены в виде среднего ± S.E.M (стандартная погрешность среднего).
[0062]
II. Результаты
1. Изменение значения пороговой боли, обусловленное приемом таблеток гидрохлорида пилокарпина (Salagen)
Оценку эффективности гидрохлорида пилокарпина как лекарственного средства проводили при трех концентрациях (т.е. 0,3 мг/кг, 0,1 мг/кг и 0,03 мг/кг) с помощью теплового теста на болевую чувствительность (ФИГ.3).
[0063]
До начала лечения отсутствовала существенная разница между всеми группами, и состояние чувствительности было на одном и том же уровне (т.е. контрольная группа: 5,6±0,9 с, группа, принимавшая таблетки гидрохлорида пилокарпина (0,3 мг/кг): 4,2±0,9 с, группа, принимавшая таблетки гидрохлорида пилокарпина (0,1 мг/кг): 4,7±0,4 с, и группа, принимавшая таблетки гидрохлорида пилокарпина (0,03 мг/кг): 5,9±0,7 с). Тем не менее, анальгезирующее действие, достигаемое путем введения лекарственного средства, было подтверждено благодаря существенному различию (ФИГ.3С). Существенное различие также наблюдалось на основе результатов площади под фармакокинетической кривой (т.е. контрольная группа: 8,0±33,9, группа, принимавшая таблетки гидрохлорида пилокарпина (0,3 мг/кг): 460,2±130,4, группа, принимавшая таблетки гидрохлорида пилокарпина (0,1 мг/кг): 356,2±59,2, и группа, принимавшая таблетки гидрохлорида пилокарпина (0,03 мг/кг): 14,9±38,3) (ФИГ.3D). На ФИГ.3А и 3В приведены результаты по группе, не подвергавшейся стрессу, при этом не наблюдался эффект, обусловленный введением лекарственного средства при любой дозировке.
[0064]
Кроме того, площади под фармакокинетической кривой по анальгезирующему действию увеличились в зависимости от дозы (ФИГ.3D). Анальгезирующее действие, продолжавшееся в течение 1 часа, вернулось к первоначальному значению спустя 3 часа после введения лекарственного средства (дата не указана).
[0065]
2. Анальгезирующее действие гидрохлорида пилокарпина у мыши, подвергшейся интермиттирующему стрессу от холода
Пациенты с синдромом фибромиалгии обычно имеют неуравновешенную вегетативную нервную систему, которая обусловлена гипертонической симпатической нервной системой или аналогичной системой. В результате этого у пациентов проявляются не только системные боли, но также симптомы, аналогичные симптомам у пациентов с синдром Шегрена, такие как сухость слизистой оболочки рта. Гидрохлорид пилокарпина, используемый в данном эксперименте, является неселективным агонистом мускаринового рецептора и используется для лечения пациентов с синдромом Шегрена ввиду его действия, способствующего слюновыделению. Результаты показали существенное различие, что указывает на улучшение в отношении болевой гиперчувствительности в группе, в которой перорально принимали таблетки 0,3 мг/кг и 0,1 мг/кг гидрохлорида пилокарпина при проведении теста Харгрейвса (ФИГ.3).
[0066]
Дополнительно к корректировке уравновешивания вегетативной нервной системы ввиду активации парасимпатического нерва, служащего в качестве сайта приложения действия препарата для лечения, также является возможным воздействие на ацетилхолиновые рецепторы в головном мозге и спинном мозге. При проведении экспериментов на животных было выявлено, что мускариновые агонисты или ингибиторы холинэстеразы, введенные в спинальное субарахноидальное пространство, проявляют анальгезирующее действие (Zhuo, М. And Gebhart, G.F., Tonoc cholinergic inhibition of spinal mechanical transmission, Pain Vol.46 (1991) pp.221-222; and Scatton, В., Dubois, A., Javoy-Agid, F. and Camus, A., Autoradiographic localication of musucarinc cholinergic receptors at various segmentral levels of the human spinal cord, neurosic. Lett. Vol.49 (1984) pp.239-245). Мускариновые рецепторы, которые рассматриваются как сайт приложения действия препарата, сконцентрированы во втором слое заднего рога спинного мозга (т.е. substantia gelatinosa) (Todd, A.J. и Sullican, А.С., Light microscope study of the coexistence of GABA-like and Glycine-like immunoreactications in the spinal cord of the rat, J. Соmр. Neurol., Vol.296 (1990) pp.496-505; Kumazawa, Т. и Perl, E. R., Excitation of marginal and substatia gelationsa neurons in the primate spinal cord: indications of their place in dorsal horn functional orignization, J. Comp. Neurol., Vol.177 (1978) pp.417-434; and Yoshimura, M. and Jessell, Т.М., Primary afferent-evoked synaptic responses and slow potential generation in rat substantia gelationsa neurons in vitro, J. Neurophysiol., Vol.62 (1989) pp.96-108), и ввиду того, что многочисленные клетки, содержащие ГАМК, присутствуют на этом сайте (The role of supraspinal muscrinic receptor and GABAnergic system in neuropathic pain, PAIN RESEARCH Vol.23 No. 2 (2008)), в частности, было предположено воздействие на мускариновые рецепторы в ГАМК-нейроне. Указанное предположение вытекает из того факта, что карбохолин, являющийся синтезированным холиновым эфиром, действует таким образом, чтобы ускорить выработку ГАМК. Кроме того, поскольку substantia gelatinosa рассматривается как сайт, ответственный за интегрирование ноцицептивной информации с периферии, ее передачу на таламические проекционные нейроны и контролирование выходного сигнала (Yoshimura, M. and Jessell, Т.M., Primary afferent-evoked synaptic responses and slow potential generation in rat substantia gelationsa neurons in vitro, J. Neurophysiol., Vol.62 (1989) pp.96-108); and Facilitation of GABA Release by Carbachol and Neostigmine in Substatia Gelatinosa of Rat Spinal Cord. Pine research Vol.12 (1997) pp.65-72), было выдвинуто предположение о его участии в передаче боли. На основе результатов указанных работ считается, что повышение уровня высвобождения ГАМК ввиду активации мускариновых рецепторов, присутствующих в ГАМК, и активации ГАМКА-рецептора связано с облегчением боли. Другими словами, возможно, что открытие Cl-канала ввиду активации ГАМКА с последующей гиперполяризацией мембранного потенциала и снижением мембранного сопротивления может обуславливать стабилизацию мембранного потенциала нейронов substantia gelatinosa и снижение уровня их возбудимости. Это также согласуется с сайтом приложения действия гидрохлорида пилокарпина, и считается, что анальгезирующее действие проявлялось в данном эксперименте ввиду указанных действий.
[0067]
Кроме того, ввиду существования вероятности того, что холинергическое средство, такое как гидрохлорид пилокарпина, может оказывать действие на центральную нервную систему дозозависимым образом (The role of supraspinal muscrinic receptor and GABAnergic system in neuropathic pain, PAIN RESEARCH Vol.23, No. 2, 2008), также существует возможность того, что он оказывает действие на головной мозг. В одном исследовании содержится информация о подавлении аллодинии, обусловленной механическим раздражением путем интрацеребровентрикулярного (i.c.v.) введения агониста мускаринового рецептора McN-A-343, в эксперименте с использованием модели нейропатической боли, и делается предположение относительно того, что ГАМКВ-рецептор ввиду активации мускаринового М1 рецептора в головном мозге выступает в качестве сайта приложения действия препарата. Вводимый перорально в данном эксперименте гидрохлорид пилокарпина может действовать как на спинной мозг, так и на головной мозг, и вследствие этого предполагается, что анальгезирующее действие возникает за счет активации ГАМК-нейронов.
[0068]
Интересное открытие в данном эксперименте заключается в том, что дозировка лекарственного средства, приведшая к улучшению состояния, соответствовала дозировке, фактически используемой в клинической практике (введение 5 мг в качестве одной дозы взрослому человеку), и, кроме того, указанная дозировка не приводила к анальгезирующему действию у нормальных мышей. Указанные результаты позволяют предположить, что гипералгезия, наблюдаемая при заболевании, может быть вызвана аномалиями в парасимпатических нервах, на которые воздействует пилокарпин.


Изобретение относится к области фармакологии и представляет собой лекарственное средство для лечения фибромиалгии, включающее пилокарпин или гидрохлорид пилокарпина и фармацевтически приемлемый носитель, в котором ежедневная доза пилокарпина или гидрохлорида пилокарпина составляет от 0,1 мг до 1000 мг. Изобретение обеспечивает эффективное лечение симптомов фибромиалгии. 4 н. и 1 з.п. ф-лы, 3 пр., 1 табл., 3 ил.
1. Лекарственное средство для лечения фибромиалгии, включающее пилокарпин или гидрохлорид пилокарпина и фармацевтически приемлемый носитель, в котором ежедневная доза пилокарпина или гидрохлорида пилокарпина составляет от 0,1 мг до 1000 мг.
2. Лекарственное средство по п.1, в котором средство вводится для лечения сухого кератоконъюктивита или ксеростомии, вызванных симптомами фибромиалгии.
3. Фармацевтическая комбинация для лечения фибромиалгии, включающая комбинацию, по меньшей мере, одного компонента, выбранного из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и пилокарпин или гидрохлорид пилокарпина.
4. Фармацевтическая комбинация для лечения фибромиалгии, включающая пилокарпин или гидрохлорид пилокарпина в качестве активного ингредиента, предназначенного для лечения пациента, принимающего комбинацию, включающую, по меньшей мере, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
5. Набор лекарственных средств для лечения фибромиалгии, включающий лекарственное средство, содержащее пилокарпин или его фармакологически приемлемую соль, которая представляет собой гидрохлорид пилокарпина, в качестве активного ингредиента, и комбинацию, включающую, по меньшей мере, один компонент, выбранный из группы, включающей габапентин, прегабалин, экстракт из воспаленной кожной ткани кроликов, которым был привит вирус осповакцины, клоназепам, милнаципран, пароксетин, амитриптилин, миансерин и их фармакологически приемлемые соли.
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| US 2003185884 A1, 02.10.2003 | |||
| JP 2006076945 A, 23.03.2006 | |||
| WO 2005039497 A2, 06.05.2005 | |||
| ТАБЛЕТКА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ, СОДЕРЖАЩАЯ РЕБОКСЕТИН | 2003 |
|
RU2292873C2 |
Авторы
Даты
2012-10-20—Публикация
2009-05-15—Подача