Предлагаемое изобретение относится к области органического синтеза, в частности к способу получения метилового эфира 2-бензо[b]фуранкарбоновой кислоты (1) (МЭБФК).
Алкиловые и ариловые эфиры 2-бензо[b]фуранкарбоновой кислоты являются синтонами для получения ингибиторов биосинтеза лейкотриенов и применяются для лечения астмы, кожных болезней, аллергии и сердечно-сосудистых заболеваний [1. Патент США 4663347 (1987); 2. Патент США 4745127 (1988)].
2-Бензо[b]фуранкарбоновая кислота используется для синтеза азипанона и метилазипанона, являющихся в свою очередь основой для ингибиторов катепсина К [3. D.Yamashita, R.Marquis, R.Xie, S.Nidamarthy, H.Oh, J.Jeong, K.Erhard, K.Ward, T.Roethke, B.Smith, H.Cheng, X.Geng, F.Lin, P.Offen, B.Wang, N.Nevins, M.Head, R.Haltiwanger, A.Sarjeant, L.Liable-Sands, B.Zhao, W.Smith, C.Janson, E.Gao, T.Tomaszek, M.McQueney, I.James, C.Gress, D.Zembryki, M.W.Lark, D.Veber // J. Med. Chem. 2006. 49 (5). 1597-1612].
2-Бензо[b]фуранкарбоновая кислота служит исходным сырьем для получения допамина - эндогенного лиганда для дофаминовых рецепторов [4. L.Bettinetti, K.Schlotter, H.Hubner, P.Gmeiner // J. Med. Chem. 2002. 45 (21). 4594-4597).
Производные 2-бензо[b]фуранкарбоновой кислоты находят применение для синтеза хромонов [5. K.D.Banerji, D.Poddar // J. Indian. Chem. Soc. 1976. LIII. 1119-1121].
Производное 2-бензо[b]фуранкарбоновой кислоты-6-метилбензо[b]тиофен-2-карбокси-(1-{(S)-1-бензил-4-[4-тетрагидропиран-4-илметил)пиперазин-1-ил]бутилкарбамоил}циклопентил)амид является антогонистом нейрокинина 2 (НК2) [6. D.Fattori, M.Porcelloni, P.D'Andreat, R.-M.Catalioto, A.Ettorret, S.Giuliani, E.Marastoni, S.Maurot, S.Meini, C.Rossi, M.Altamura, Maggi // J. Med. Chem. 2010, 53 (10). 4148].
3-Бензофурил-4-фенил(аллил)-5-меркапто-1,2,4-триазолы, синтезированные циклизацией замещенных тиосемикарбазидов бензо[b]фуран-2-карбоновой кислоты проявили противоопухолевую активность [7. М.А.Калдрикян, Л.А.Григорян, Р.Г.Мелик-Оганджанян, Ф.Г.Арсенян // Хим.-фарм.ж. 2009.43 (5). 11-13].
2-Бензо[b]фуранкарбоновую кислоту можно синтезировать в три стадии из кумарина [8. Organic Synthesis, Coll. Vol.3, p.209, 1955]. На первой стадии свободно-радикальным бромированием с помощью Вr2 из кумарина синтезируют дибромид кумарина (выход 70%). Затем к раствору КОН в абсолютном этаноле при охлаждении до 15°С добавляют дибромид кумарина в (порционно по 10-15 г) и выдерживают реакционную массу при 20°С в течение 30 мин. Далее реакционную массу кипятят 30 мин, затем при охлаждении добавляют воду и 6N НСl. Общий выход 2-бензо[b]фуранкарбоновой кислоты по данному методу составил 57-61%.
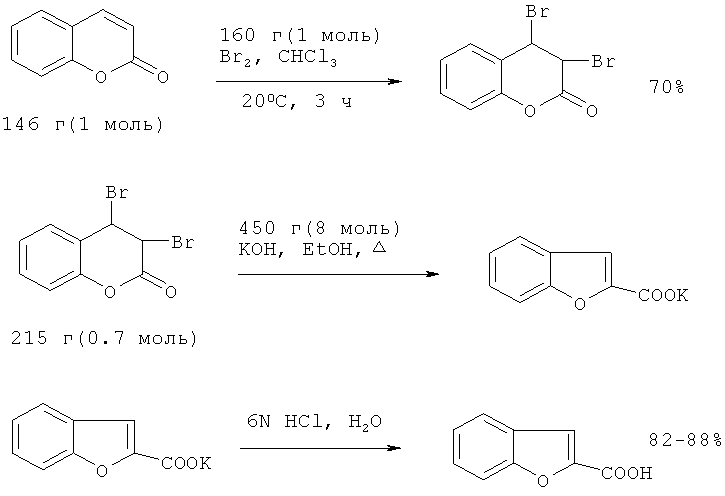
Недостатки метода:
1. Использование дорогостоящего исходного реагента - кумарина.
2. Применение ядовитого и легколетучего молекулярного брома.
3. Использование большого избытка КОН (8 моль).
4. Образование большого количества отходов, содержащих НСl, КСl и НСl.
5. Умеренный выход 2-бензо[b]фуранкарбоновой кислоты (57-61%). Этиловый эфир бензфуран-2-карбоновой кислоты был синтезирован из салицилового альдегида и этилового эфира хлоруксусной кислоты [9. S.Bednarz, M.Lukasiewitch, D.Bogdal // 9th Int. Electronic Conf. Synth. Org. Chem. ECSOC-9. 2005. 1-30 November. E 015]. Реакционная смесь была адсорбирована на K2СО3 в присутствии тетрабутиламмоний иодида и облучалась в течение 3 мин в микроволновом реакторе (Synth Wave 402, Prolabo, max power 300 W). В зависимости от длины волны микроволнового облучения возможно образование высокотермальных градиентов внутри реакционной смеси, что приводит к высокой конверсии исходных соединений только на локальных участках.
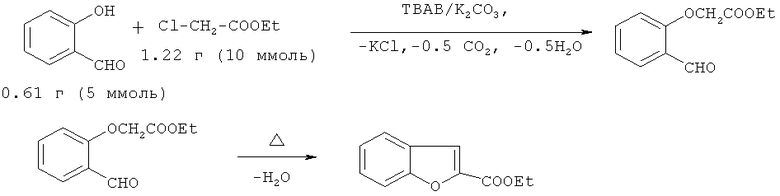
Недостатки метода:
1. Использование микроволнового реактора, который трудно масштабируется.
2. Высокая конверсия исходных соединений только на локальных участках.
2-Бензо[b]фуранкарбоновая кислота синтезирована из салицилового альдегида и этилового эфира броммалоновой кислоты в присутствии безводного K2СО3 в среде метилэтилкетона [10. S.Tanaka // J. Am. Chem. Soc. 1951. 73. 872]. После нейтрализации реакционной массы с помощью Н2SO4 и экстрагирования эфиром была выделена 2-бензо[b]фуранкарбоновая кислота, выход которой составил 76%.
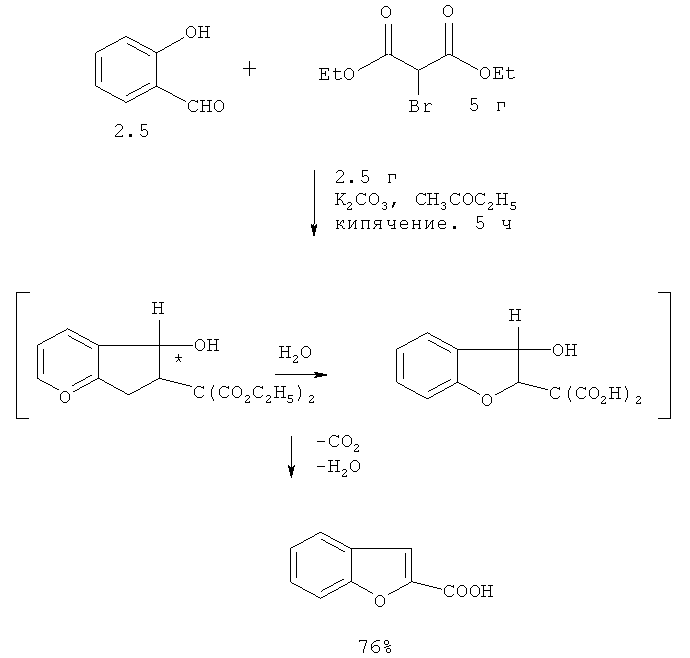
По аналогичной схеме из 5-иодсалицилового альдегида, этилового эфира броммалоновой кислоты в присутствии поташа и тетрабутиламмонийиодида синтезирован этиловый эфир 5-иодо-2-бензо[b]фуранкарбоновой кислоты (выход 62%) [11. A.Newman, P.Grundt, G.Cyriac, J.R.Deschamps, M.Taylor, R.Kumar, D.Ho, R.Luedtke // J. Med. Chem. 2009. 52. 2559-2570].

Недостатки методов:
1. Применение дорогостоящих исходных реагентов.
2. Значительная продолжительность реакции (36 ч).
Наиболее известный метод получения 2-бензо[b]фуранкарбоновой кислоты основан на реакции 2-бромбензо[b]фурана с BuLi при температуре -70°С. При этом образуется 2-литийбензо[b]фуран, который при последующей карбонизации превращается в 2-бензо[b]фуранкарбоновую кислоту с выходом 62% [12. R.Fuson, H.Jacson // J. Am. Chem. Soc. 1948. 70. 4. 1655-1657].
2-Бензо[b]фуранкарбоновая кислота была получена в качестве побочного продукта при реакции 3-бромбензо[b]фурана с BuLi и СO2. Выход кислоты составил от 13-23% [12. R.Fuson, H.Jacson // J. Am. Chem. Soc. 1948. 70. 4. 1655-1657].
2-Бензо[b]фуранкарбоновая кислота с выходом 70% получена карбонизацией 2-литийбензо[b]фурана [13. Organic Reactions (Hoboken, NJ, United States). 1979. V.26.]
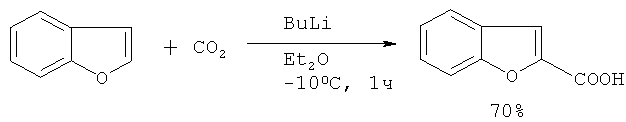
В работе [14. Costa A., Dean F., Jones M., Varma R. // J. Chem. Soc., Perkin Trans.1, 1985. 4. 799-808] 2-бензо[b]фуранкарбоновая кислота синтезирована в две стадии путем последовательного литирования и карбонизации бензо[b]фурана.
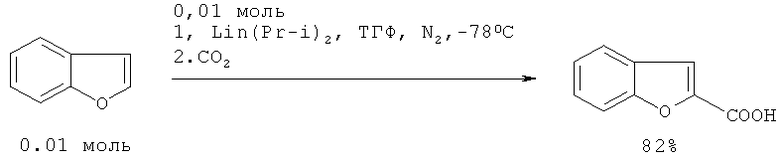
Недостатки методов:
1. Необходимость использования стехиометрических количеств высокореакционных, пожароопасных металлорганических реагентов - бутиллития и диизопропиламида лития.
2. Применение пониженных температур -10-(-78)°С.
2-Бензо[b]фуранкарбоновая кислота с выходом 85% была получена последовательным добавлением бензо[b]фурана и 1-хлороктана к суспензии натрия в толуоле, с последующей карбонизацией [15. A.Gissot, J.Becht, J.Desmurs; V.Pevere, A.Wagner, C.Mioskowski // Angew. Chem., Int. Ed., 2002, 41(2), 340-343; 16. Патент WO 2000064905 (2000 г)]
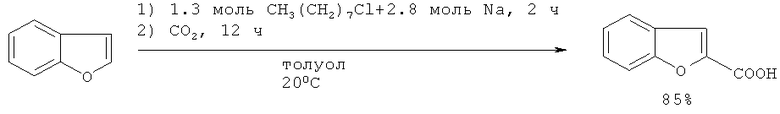
Недостатки метода:
1. Металлирование бензо[b]фурана с помощью пожароопасного металлического натрия.
Карбонилированием бензо[b]фурана при комнатной температуре в присутствии PdCl2, Hg(CF3CO2)2, Сu(ОАс)2 и LiBr в этаноле был получен этиловый эфир 2-бензо[b]фуранкарбоновой кислоты с выходом 5% [17. R.Jaouhari, P.H.Dixneuf, S.Lecolier // Tetrahedron Lett., 1986, 27(52), 6315-6318].
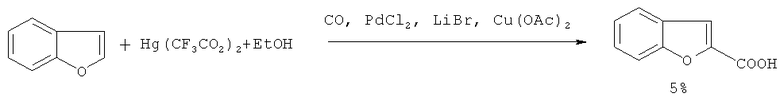
Недостатки метода:
1. Низкий выход целевого продукта - 5%.
2. Использование дорогостоящих реагентов.
В работе [18. Р.Babin, P.Bourgeois, J.Dunogues // Соmр. Rend., Serie С.1976, 283(4), 149-152] 2-бензо[b]фуранкарбоновая кислота получена взаимодействием EtMgBr и (Ме3Si)2NН с бензо[b]фураном, с последующей карбонизацией образующегося на I стадии 2-бензо [b] фурилмагнийбромида.
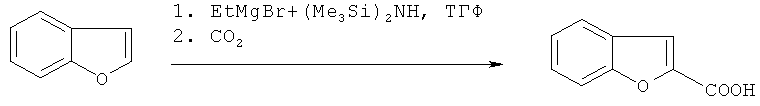
Авторами предлагается способ получения метилового эфира 2-бензо[b]фуранкарбоновой кислоты (1), не имеющий вышеперечисленных недостатков.
Сущность способа заключается во взаимодействии 2-бензо[b]фурана с четырехбромистым углеродом и метанолом в присутствии железосодержащих катализаторов, выбранных из ряда ферроцен, ацетилацетонат железа (III), бромид железа (II), при температуре 130-150°С в течение 4-5 ч при мольном соотношении [катализатор]:[бензо[b]фуранфуран]:[СВr4]:[метанол]=1:100:200:1000-1100, конверсия бензо[b]фурана составляет 100%, выход метилового эфира 2-бензо[b]фуранкарбоновой кислоты достигает 96-98%. Синтез проводят в атмосфере аргона. В отсутствие катализатора, СВr4 или метанола (любого из компонентов) реакция не идет.
Лучшим катализатором является ферроцен (выход целевого продукта 98%). В присутствии трис(2,4-пентанодионато)железа (Fе(асас)3), бромида железа (FeBr2) выходы метилового эфира 2-бензо[b]фуранкарбоновой кислоты несколько ниже и составляют 96%. Побочными продуктами реакции являются НВr и эфир СН3ОСН3.
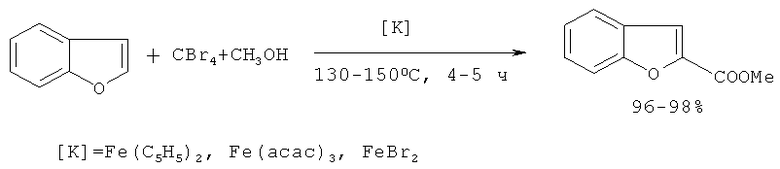
Существенные отличия предлагаемого способа от прототипа.
1. Для получения метилового эфира 2-бензо[b]фуранкарбоновой кислоты из бензо[b]фурана используют системы СВr4-СН3ОН-катализатор (катализатор: ферроцен Fe(C5H5)2, трис(2,4-пентанодионато)железа Fе(асас)3, бромид железа FеВr2).
2. Преимущества предлагаемого метода:
1. Высокий выход целевого продукта 96-98%.
2. Селективность процесса.
3. Отсутствие агрессивных окислителей.
4. Доступность и дешевизна исходных реагентов и катализаторов.
5. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат.
Предлагаемый способ поясняется примерами.
ПРИМЕР 1. Реакции проводили в стеклянной ампуле объемом 10-мл, помещенной в микроавтоклав из нержавеющей стали объемом 17 мл, при постоянном перемешивании и регулируемом нагреве. В ампулу в токе аргона загружали 1 ммоль Fe(C5H5)2, 100 ммоль бензо[b]фурана, 200 ммоль галогенметана и 1100 ммоль спирта. Запаянную ампулу помещали в автоклав, автоклав герметично закрывали и нагревали при 140°С в течение 4 ч при постоянном перемешивании. После окончания реакции автоклав охлаждали до комнатной температуры, ампулу вскрывали, реакционную массу фильтровали через слой силикагеля (2 г) (элюент - этилацетат). Растворитель отгоняли, остаток перекристаллизовывали из смеси метанол-вода (соединение (1)).
Строение полученных соединений доказано методами ЯМР, масс-спектрометрии, а также сравнением с известными образцами и справочными данными. Общий выход метилового эфира бензо[b]фуранкарбоновой кислоты (1) составляет 98%.
Метиловый эфир 2-бензо[b]фуранкарбоновой кислоты (1) Т.пл. 49.5-50°С (Т пл. 52°С [19. Feinstein A., Gore P.H., Reed G.L. J. Chem. Soc. (B). 1969. 3. 205.], 52-53°C [20. Suzuki Т., Horaguchi Т., Shimizu Т. Bull. Chem. Soc. Jpn. 1983. 56. 2762.]. Спектр ЯМР 13С (δ, м.д.): 52.35 (СН3), 112.32 (С7), 113.98 (С3), 122.83 (С4), 123.8 (С5), 126.9 (С3a), 127.66 (С6), 145.37 (С2), 155.69 (С7a), 159.95 (COO). Спектр ЯМР 1Н (СВСl3, δ, м.д.): 3.96 с (3Н, ОСН3), 7.30 т (1Н, J 8 Гц), 7.44 т (1Н, J 7.6 Гц), 7.52 (с, 1Н), 7.58 д (1Н, JS Гц), 7.67 д (1Н, J 10.4 Гц). Масс-спектр, m/z (Iотн. (%)): 176[M]+ (63), 145 (100), 118 (11), 89 (41), 63 (15), 44 (2). Найдено, %: С 68.20; Н 4.57; О 27.23. С10Н8О3. Вычислено, %: С 68.18; Н 4.55; О 27.27.
ПРИМЕР 2. Реакции проводили в стеклянной ампуле объемом 10 мл, помещенной в микроавтоклав из нержавеющей стали объемом 17 мл, при постоянном перемешивании и регулируемом нагреве.
В ампулу в токе аргона загружали 1 ммоль Fе(асас)3, 100 ммолей бензо[b]фурана, 200 ммолей галогенметана и 1100 ммоль спирта. Запаянную ампулу помещали в автоклав, автоклав герметично закрывали и нагревали при 140°С в течение 4 ч при постоянном перемешивании. После окончания реакции автоклав охлаждали до комнатной температуры, ампулу вскрывали, реакционную массу фильтровали через слой силикагеля (2 г) (элюент - этилацетат). Растворитель отгоняли, остаток перекристаллизовывали из смеси метанол-вода (соединение (1)). Общий выход метилового эфира бензо[b]фуранкарбоновой кислоты (1) составляет 96%.
ПРИМЕР 3. Реакции проводили в стеклянной ампуле объемом 10 мл, помещенной в микроавтоклав из нержавеющей стали объемом 17 мл, при постоянном перемешивании и регулируемом нагреве.
В ампулу в токе аргона загружали 1 ммоль FeBr2, 100 ммолей бензо[b]фурана, 200 ммолей галогенметана и 1100 ммолей спирта. Запаянную ампулу помещали в автоклав, автоклав герметично закрывали и нагревали при 140°С в течение 4 ч при постоянном перемешивании. После окончания реакции автоклав охлаждали до комнатной температуры, ампулу вскрывали, реакционную массу фильтровали через слой силикагеля (2 г) (элюент - этилацетат). Растворитель отгоняли, остаток перекристаллизовывали из смеси метанол-вода (соединение (1)). Общий выход метилового эфира бензо[b]фуранкарбоновой кислоты (1) составляет 96%. Другие примеры, подтверждающие способ приведены в таблице 1.
[kat]:[С8Н6О]:[СВr4]:[МеОН]
ность реакции, ч
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 2-БЕНЗО[b]ФУРАНКАРБОНОВОЙ КИСЛОТЫ | 2010 |
|
RU2455299C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 5-АЦЕТИЛФУРАН-2-КАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2404173C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 5-АЦЕТИЛПИРРОЛ-2-КАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2404162C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ДИХЛОРМЕТИЛИЗОХИНОЛИНА | 2008 |
|
RU2402535C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА 2,5-ТИОФЕНДИКАРБОНОВОЙ КИСЛОТЫ ИЗ 2-ТИОФЕНКАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2402541C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ ФЕНАНТРЕН-9-КАРБОНОВОЙ КИСЛОТЫ | 2014 |
|
RU2566086C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА 2,5-ТИОФЕНДИКАРБОНОВОЙ КИСЛОТЫ ИЗ ТИОФЕНА | 2008 |
|
RU2404176C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ФЕНИЛ-3-АЛКИЛХИНОЛИНОВ | 2014 |
|
RU2565787C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА | 2011 |
|
RU2486169C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЦЕТИЛИЗОХИНОЛИНА | 2009 |
|
RU2404166C1 |
Данное изобретение относится к способу получения метилового эфира 2-бензо[b]фуранкарбоновой кислоты, который используется в качестве исходного соединения при синтезе фармацевтических препаратов. Сущность способа заключается во взаимодействии бензо[b]фурана с четырехбромистым углеродом и метанолом в присутствии под действием железосодержащего катализатора, выбранного из ряда ферроцена (Fе(С5Н5)2), ацетилацетоната железа (III) или бромида железа (II) при температуре 130-150°С в течение 4-5 ч при мольном соотношении [катализатор]:[бензо[b]фуран]:[СВr4]:[метанол]=1:100:200:1000-1100, выход метилового эфира 2-бензо[b]фуранкарбоновой кислоты достигает 96-98%. Технический результат - высокий выход целевого продукта. 1 табл., 3 пр.
Способ получения метилового эфира 2-бензо[b]фуранкарбоновой кислоты формулы
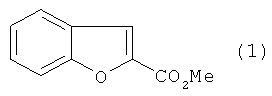
характеризующийся тем, что бензо[b]фуран подвергают взаимодействию с СВr4 и метанолом в присутствии железосодержащего катализатора-ферроцена (Fe(C5H5)2) или ацетилацетоната железа (III), или бромида железа (II) при мольном соотношении [катализатор]:[бензо[b]фуран]:[СВr4]:[метанол]=1:100:200:1000-1100, при температуре 130-150°С в течение 4-5 ч в атмосфере аргона.
| WO 200064905 А2, 01.11.2000 | |||
| A.Feinstein et al, J | |||
| Chem | |||
| Soc | |||
| В., 1969, p.205 | |||
| US 4663347 A, 05.05.1987 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ | 0 |
|
SU393827A1 |
| RU 2004106623 A, 20.07.2005. | |||
Авторы
Даты
2012-11-20—Публикация
2010-10-07—Подача