Предлагаемое изобретение относится к области органического синтеза, в частности к способу получения метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (1) (МЭАПК).
Пирролкарбоновая кислота и ацетилпирролкарбоновые кислоты служат исходными соединениями при синтезе порфиринов [1. Патент США 5179120, 1993; 2. JACS, 1960, 82(11); 2750-2755].
Пирролкарбоновые кислоты проявляют высокую биологическую активность. Так, производные 5-пирролкарбоновых кислот обладают противовирусным действием, в частности они активно подавляют вирусы классической чумы птиц (ВКЧП) [3. Собенина Л.Н., Михалева А.И., Бахарева Е.В. и др. // Хим.-фарм. журнал, 1992, №11-12, С.57-59], а натриевые соли 2-арил-5-пирролкарбоновых кислот проявляют противосудорожную активность [4. Собенина Л.Н., Михалева А.И., Бахарева Е.В. и др. // Хим.-фарм. журнал, 1992, №6, С.26-29].
2-Пирролкарбоновые кислоты можно получить при галоформном расщеплении соответствующих 2-трифторацетилпроизводных. Реакция протекает при кипячении спиртовых растворов трифторацетилпирролов в присутствии 4 н. NaOH при 80°С в течение 5 ч [5. Mackie R.K., Mhatre S, Tedder J.M. //J.Fluorine Chem., 1977, №10, P.437; 6. Собенина Л.Н., Сергеева М.П., Михалева А.И. и др.// ХГС, 1990, №5, С.612-616].
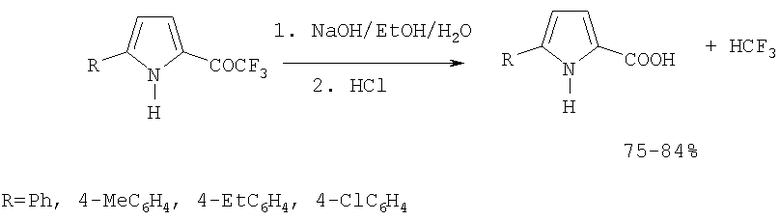
Исходный 2-фенил-5-трифторацетилпиррол получен реакцией 2-фенилпиррола (0.05 моль) с ангидридом трифторуксусной кислоты (0.05 моль) в 50 мл бензола в присутствии 0.06 моль пиридина при 20°С в течение 3 ч. Выход конечного продукта составляет 83% [7. Б.А.Трофимов и др. / ЖОрХ, 1979, т.15, С.2042]

Недостатки метода:
1. Использование агрессивных реагентов: NaOH и HCl.
2. Применение в качестве ацилирующего агента труднодоступного ангидрида трифторуксусной кислоты.
Метиловый эфир 4-ацетил- 2-пирролкарбоновой кислоты может быть синтезирован в несколько стадий из пиррола [8. Belanger P. // Tetrahedron Lett, 1979, 2505; 9. Harbuck J.W., Rapoport Н. J. Org. Chem., 37, 3618 (1972)].
К раствору 2-трихлорацетилпиррола (22 г, 0.1 моль) (его получают ацилированием пиррола хлорангидридом трихлоруксусной кислоты) в 100 мл хлороформа при 0°С прикапывали эквивалентное количество ацилирующего агента - хлористый ацетил CH3COCl в присутствии AlCl3, растворенного в хлористом метилене. В результате реакции с выходом 94% образуется 4-ацетил-2-трихлорацетилпиррол. Для превращения 4-ацетил-2-трихлорацетилпиррола в целевой метиловый эфир 4-ацетил-2-пирролкарбоновой кислоты его обрабатывали метилатом натрия. Выход метилового эфира 4-ацетил-2-пирролкарбоновой кислоты составляет 89%.

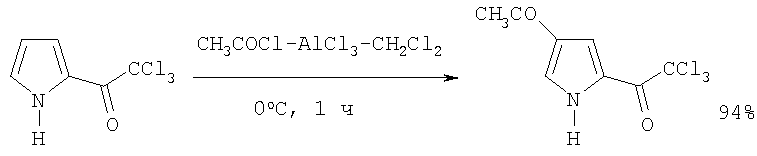

Недостатки метода:
1. Многостадийность процесса.
2. Использование низких температур (0°С).
3. Использование хлорангидридов уксусной кислоты и трихлоруксусной кислоты, которые легко гидролизуются при контакте с водой.
4. Необходимость использования металлического натрия (метилат натрия получают растворением Na в МеОН).
5. Образование большого количества отходов, содержащих NaCl, AlCl3, CH2Cl2 и метанол.
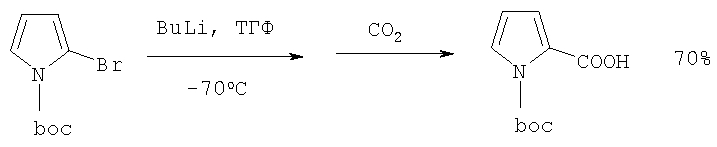
Известен метод получения 2-пирролкарбоновой кислоты исходя из 2-бромпиррола. Предварительно 2-бромпиррол реагирует с бутиллитием с замещением брома на литий, а полученное литийорганическое соединение при взаимодействии с диоксидом углерода превращается в 2-пирролкарбоновую кислоту [10. Chen W., Cava M.P. // Tetrahedron Lett., 28, 6025 (1987); 11. Chen W., Stephenson E.K., Cava M.P., Jackson Y.A. // Org. Synth., 70, 151 (1992); 12. Martina S. Enkelmann V., Wtgner G., Schuter A.-D. // Synthesis, 1991, 613].
Метод имеет ряд существенных недостатков:
1. Использование дорогостоящего металлоорганического реагента бутиллития.
2. Необходимость проведения реакции при пониженной температуре (-70°С).
3. Сложности выделения целевого продукта и образование трудноутилизуемых отходов и сточных вод, содержащих большое количество LiCl.
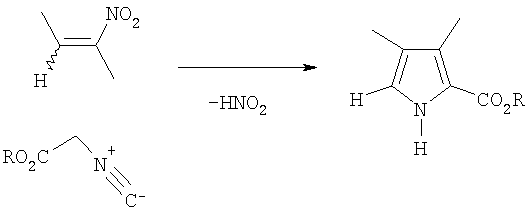
3,4,5-Замещенные 2-пирролкарбоновые кислоты получены конденсацией изоцианоацетатов с α, β-непредельными нитросоединениями с отщеплением азотистой кислоты [13. Дж.Джоуль, К.Миллс. Химия гетероциклических соединений, М.: Мир, 2004, С.728].
Синтез замещенных 2-пирролкарбоновых кислот осуществлен конденсацией 1,3-дикарбонильных соединений и эфиров глицина [14. Mataka S., Takahashi К., Tsuda Y, Tashiro M. // Synthesis, 1982, 157; 15. Walizei G.H., Breitmaier E. // ibid, 1989, 337; 16. Hombrecher H.K., Horter G. // ibid., 1990, 389].

2-Пирролкарбоновые кислоты можно получить синтезом Кеннера. Так, при взаимодействии α, β-ненасыщенных кетонов с тозиламинами образуется дигидропиррол, содержащий тозильную группу при атоме азота; элиминирование толуолсульфоната на заключительной стадии приводит к производным 2-пирролкарбоновой кислоты [17. Terry W.G., Jackson A.Y., Kenner G.W., Kornis G. // J. Chem. Soc., 1965, 4389; 18. Lash T.D, Hoehner M.C. // J. Heterocycl. Chem, 28, 1671 (1991)].
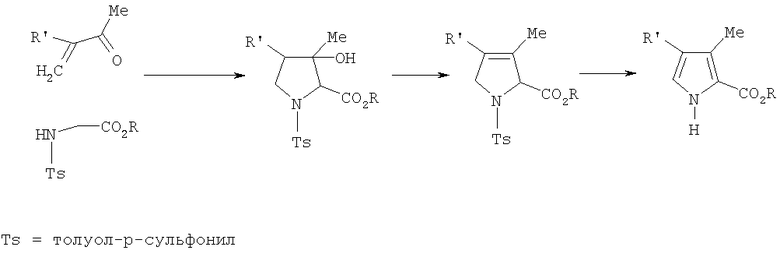
Недостатки методов:
1. Использование труднодоступных реагентов.
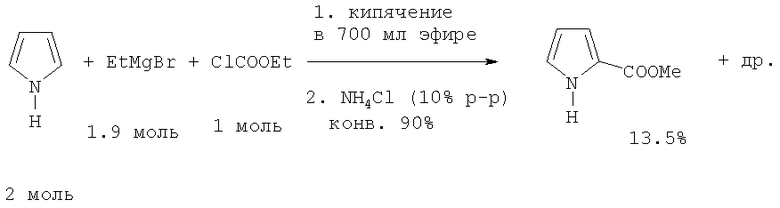
Метиловый эфир 5-ацетил-2-пирролкарбоновой кислоты с низким выходом (8%) был получен в качестве побочного продукта при синтезе метилового эфира 4-ацетил-2-карбоновой кислоты [19. H.J.Anderson, C.W.Huang // Canad. J. Chem., 1967, 45, №9, р.897-902 (РЖХим 23Ж334, 1967)].
Синтез проводили в две стадии. Сначала к раствору 1.9 моля EtMgBr в 600 мл эф. прибавляют по каплям при охлаждении 2 моля пиррола, кипятят 20 мин, охлаждают, вносят 100 мл эфира, прибавляют по каплям раствор ClCOOEt (1 моль) в 150 мл эфира, кипятят 30 мин, охлаждают, гидролизуют 10%-ным NH4Cl, водный слой экстрагируют эфиром, из объединенного органического слоя отгоняют растворитель, фракционируют в вакууме, остаток последовательно экстрагируют бензолом, спиртом и диоксаном, фракции хроматографируют на Al2O3. В реакционной массе обнаружены непрореагировавший пиррол (13 г), метиловый эфир 1-пирролкарбоновой кислоты (0.3 г), метиловый эфир 2-пирролкарбоновй кислоты (28 г), метиловый эфир 3-пирролкарбоновой кислоты (не выделен), метиловый эфир 1,2-пирролдикарбоновой кислоты (10,1 г), метиловый эфир 1,3-пирролдикарбоновой кислоты (8,53 г) и 2-пиррил-2'-пиррилкетон (0.58 г).
Для получения метиловых эфиров 4- и 5-ацетил-2-пирролкарбовых кислот метиловый эфир 2-пирролкарбоновой кислоты подвергают ацилированию с помощью уксусного ангидрида. К смеси 0.9 моль безв. AlCl3 и 250 мл сероуглерода CS2 прибавляют при охлаждении 0.284 моля метилового эфира 2-пирролкарбоновой кислоты в 150 мл CS2, прибавляют по каплям при 50°С 0.3 моля Ас2О, через 15 ч реакционную массу выливают в смесь льда и разб. HCl, отфильтровывают, осадок растворяют в CHCl3, хроматографируют на Al2O3, получают метиловые эфиры 4- и 5-ацетил-2-пирролкарбоновых кислот с выходами 73.4% и 7.6% соответственно.
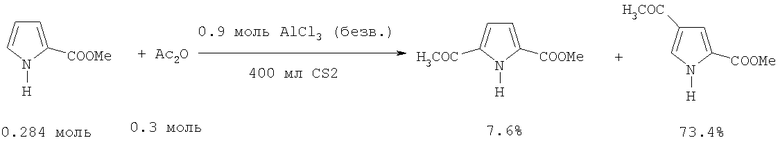
Недостатки метода:
1. Чрезвычайно низкий выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты - 7.6%.
2. Низкая селективность реакции.
3. Образование большого количества отходов, содержащих СН3СООН, Al(ОН)3 и ядовитый сероводород.
4. Использование большого количества катализатора хлорида алюминия (на 1 моль метилового эфира 2-пирролкарбоновой кислоты необходимо 3 моля AlCl3).
5. Следует отметить, что уксусный ангидрид является прекурсором наркотических препаратов, входит в список веществ, подлежащих строгому учету и контролю за его расходованием.
Авторами предлагается способ получения метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (МЭАПК), не имеющий вышеперечисленных недостатков.
Сущность способа заключается во взаимодействии 2-ацетилпиррола с четыреххлористым углеродом и метанолом в присутствии железосодержащих катализаторов - ферроцена (Fe(C5H5)2), трис(2,4-пентанодионато)железа (Fe(асас)3), бромида железа (FeBr2), ацетата железа (Fe(СН3СОО)2) при температуре 80-95°С в течение 3-6 ч при мольном соотношении [катализатор]:[2-ацетилпиррол]:[CCl4]:[метанол]=1:100:375÷1500:3250÷9750. Выход соединения (1) составляет 21-98%.
Следует отметить, что при оптимальных условиях ([катализатор]: [2-ацетилпиррол]:[CCl4]:[метанол]=1:100:750:6500, при 95°С, 5-6 ч выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты достигает 98% в зависимости от природы используемого катализатора. В отсутствие CCl4 или метанола реакция не идет.
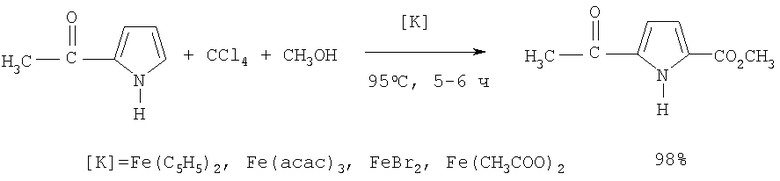
Существенные отличия предлагаемого способа от прототипа.
Для получения метилового эфира 5-ацетил-2-пирролкарбоновой кислоты из 2-ацетилпиррола используют реагент: CCl4-СН3ОН-катализатор (катализатор:ферроцен Fe(C5H5)2, трис(2,4-пентанодионато)железа Fe(асас)3, бромид железа FeBr2, ацетат железа Fe(СН3СОО)2)
Преимущества предлагаемого метода.
1. Высокий выход метилового эфира 5-ацетил-2-пирролкрбоновой кислоты.
2. Селективность процесса.
3. Отсутствие агрессивных реагентов.
4. Доступность и дешевизна исходных реагентов и катализаторов.
5. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат.
Предлагаемый способ поясняется примерами
ПРИМЕР 1. Реакции проводили в стеклянной ампуле (V=20 мл) или в микроавтоклаве из нержавеющей стали (V=17 мл).
В микроавтоклав (ампулу) под аргоном помещают 0.1 ммоль катализатора - ферроцена Fe(C5H5)2, 10 ммоль 2-ацетилпиррола, 75 ммоль CCl4 и 650 ммоль СН3ОН, автоклав герметично закрывают (ампулу запаивают) и нагревают при 95°С в течение 6 часов с постоянным перемешиванием. После окончания реакции автоклав (ампулу) охлаждают до 20°С, вскрывают, реакционную массу фильтруют через слой силикагеля (2 г) (элюент - гексан:эфир=1:1). Растворитель отгоняют, остаток перекристаллизовывают (бензол-гексан). Общий выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (1) составляет 98%.
Выделенный метиловый эфир 5-ацетил-2-пирролкарбоновой кислоты имеет т.пл. 112.5°С (лит. 109-110°С) ([19] H.J.Anderson, C.W.Huang // Canad. J. Chem. 1967, 45, №9, р.897-902 (РЖХим 23Ж334, 1967)]; 110-111.5 °С [20. C.E.Loader, M. Sc. Thesis, Memorial University of Newfounland, S. John's, Newfouland. 1965]
Спектр ЯМР 1H, δ, м.д.: 2.48 (с, 3Н, СН3СО), 3.90 (с, 3Н, ОСН3), 6.80-6.95 (м, 2Н, пиррол, =СН-СН=), 7.27(с, 1Н, N-H). ЯМР 13С, δ, м.д.: 25.85 (СОСН3), 52.04 (ОСН3), 115.58 (С4), 116.04 (С3), 134.18 (С2), 155.50(С5), 116.50 (СООСН3), 188.59 (СОСН3).
Масс-спектр, m/e (Iотн, %): 167 [M]+ (92), 43(22), 53(115), 64(18), 118(20), 120(100), 136(50), 152(85).
ПРИМЕР 2. Реакции проводили в стеклянной ампуле (V=20 мл) или в микроавтоклаве из нержавеющей стали (V=17 мл).
В микроавтоклав (ампулу) под аргоном помещают 0.1 ммоль катализатора - трис(2,4-пентанодионато)железа (Fe(асас)3), 10 ммоль 2-ацетилпиррола, 75 ммоль CCl4 и 650 ммоль СН3ОН, автоклав герметично закрывают (ампулу запаивают) и нагревают при 95°С в течение 6 часов с постоянным перемешиванием. После окончания реакции автоклав (ампулу) охлаждают до 20°С, вскрывают, реакционную массу фильтруют через слой силикагеля (2 г) (элюент-гексан:эфир=1:1). Растворитель отгоняют, остаток перекристаллизовывают (бензол-гексан). Общий выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (1) составляет 98%.
ПРИМЕР 3. Реакции проводили в стеклянной ампуле (V=20 мл) или в микроавтоклаве из нержавеющей стали (V=17 мл).
В микроавтоклав (ампулу) под аргоном помещают 0.1 ммоль катализатора - бромида железа (FeBr2), 10 ммоль 2-ацетилпиррола, 75 ммоль CCl4 и 650 ммоль СН3ОН, автоклав герметично закрывают (ампулу запаивают) и нагревают при 95°С в течение 6 часов с постоянным перемешиванием. После окончания реакции автоклав (ампулу) охлаждают до 20°С, вскрывают, реакционную массу фильтруют через слой силикагеля (2 г) (элюент-гексан:эфир=1:1). Растворитель отгоняют, остаток перекристаллизовывают (бензол-гексан). Общий выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (1) составляет 98%.
ПРИМЕР 4. Реакции проводили в стеклянной ампуле (V=20 мл) или в микроавтоклаве из нержавеющей стали (V=17 мл).
В микроавтоклав (ампулу) под аргоном помещают 0.1 ммоль катализатора - ацетата железа (Fe(СН3СОО)2), 10 ммоль 2-ацетилпиррола, 75 ммоль CCl4 и 650 ммоль СН3ОН, автоклав герметично закрывают (ампулу запаивают) и нагревают при 95°С в течение 5 часов с постоянным перемешиванием. После окончания реакции автоклав (ампулу) охлаждают до 20°С, вскрывают, реакционную массу фильтруют через слой силикагеля (2 г) (элюент-гексан:эфир=1:1). Растворитель отгоняют, остаток перекристаллизовывают (бензол-гексан). Общий выход метилового эфира 5-ацетил-2-пирролкарбоновой кислоты (1) составляет 98%.
Другие примеры, подтверждающие способ, приведены в таблице.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 5-АЦЕТИЛФУРАН-2-КАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2404173C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВЫХ ЭФИРОВ 2-ТИОФЕНКАРБОНОВОЙ КИСЛОТЫ И ЕЕ ПРОИЗВОДНЫХ | 2007 |
|
RU2359968C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА 2,5-ТИОФЕНДИКАРБОНОВОЙ КИСЛОТЫ ИЗ 2-ТИОФЕНКАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2402541C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА 2,5-ТИОФЕНДИКАРБОНОВОЙ КИСЛОТЫ ИЗ ТИОФЕНА | 2008 |
|
RU2404176C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 2-БЕНЗО[b]ФУРАНКАРБОНОВОЙ КИСЛОТЫ | 2010 |
|
RU2467004C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЦЕТИЛИЗОХИНОЛИНА | 2009 |
|
RU2404166C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 2-БЕНЗО[b]ФУРАНКАРБОНОВОЙ КИСЛОТЫ | 2010 |
|
RU2455299C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ДИХЛОРМЕТИЛИЗОХИНОЛИНА | 2008 |
|
RU2402535C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ДИХЛОРМЕТИЛПИРИДИНА | 2006 |
|
RU2316547C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОХЛОРЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ АДАМАНТАНА И ДИАМАНТАНА | 1996 |
|
RU2125552C1 |
Изобретение относится к способу получения метилового эфира 5-ацетил-2-пирролкарбоновой кислоты взаимодействием 2-ацетилпиррола с четыреххлористым углеродом и метанолом в автоклаве в присутствии железосодержащего катализатора, выбранного из группы, включающей ферроцен (Fe(С5Н5)2), трис(2,4-пентанодионато)железа (Fe(асас)3), бромид железа (FeBr2), ацетат железа (Fe(СН3СОО)2) при мольном соотношении [катализатор]:[2-ацетилпиррол]:[CCl4]:[метанол]=1:100:375÷1500:3250÷9750, при температуре 80-95°С в течение 3-6 ч. Способ обеспечивает получение целевого продукта с выходом 21-98%. 1 табл.
Способ получения метилового эфира 5-ацетилпиррол-2-карбоновой кислоты формулы

характеризующийся тем, что 2-ацетилпиррол подвергают взаимодействию с CCl4 и метанолом в автоклаве под аргоном в присутствии железосодержащего катализатора, выбранного из группы, включающей ферроцен (Fe(С5Н5)2), трис(2,4-пентанодионато)железа (Fe(асас)3), бромид железа (FeBr2), ацетат железа (Fe(СН3СОО)2 при мольном соотношении [катализатор]:[2-ацетилпиррол]:[CCl4]:[метанол]=1:100:375÷1500:3250÷9750, при температуре 80-95°С в течение 3-6 ч.
| J.Chem., v.45, n.9, 1967, p.897-902 | |||
| Chemical & Pharmaceutical Bulletin, v.44, n.8, 1631-33 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Нефтехимия, 48 (6), 2008, с.467-473. | |||
Авторы
Даты
2010-11-20—Публикация
2008-11-10—Подача