В настоящем изобретении предлагается способ профилактики или лечения заболеваний, связанных с ростом и/или пролиферацией опухолевых клеток и/или тканей и/или индукцией персистирующего ангиогенеза, у млекопитающих, прежде всего у человека, с использованием комбинации фармацевтических агентов, включающей:
(а) комплексен железа, и
(б) один или более фармацевтически активных агентов. В настоящем изобретении предлагается также комбинация фармацевтических агентов, включающая:
(а) комплексен железа, и
(б) один или более фармацевтически активных агентов. В одном варианте осуществления настоящего изобретения предлагается также применение комбинации фармацевтических агентов, включающей:
(а) комплексен железа, и
(б) один или более фармацевтически активных агентов, для получения лекарственного средства, предназначенного для лечения пролиферативного заболевания.
В настоящем изобретении предлагаются также фармацевтические композиции, включающие:
(а) комплексен железа,
(б) фармацевтически активный агент и
(в) фармацевтически приемлемый носитель. В настоящем изобретении предлагается также коммерческая упаковка или продукт, включающие:
(а) фармацевтический состав комплексона железа, и
(б) фармацевтический состав фармацевтически активного агента для одновременного, последовательного или раздельного применения.
Компоненты комбинации (а) и (б) можно вводить одновременно, один за другим или отдельно в виде одной комбинированной лекарственной формы или двух отдельных лекарственных форм. Лекарственной формой является также фиксированная комбинация.
Химиотерапия, предназначенная для лечения пролиферативных заболеваний, описана в литературе.
Неожиданно было установлено, что, при лечении пролиферативного заболевания, прежде всего, жидких опухолей, например, множественной миеломы, миелодисплазического синдрома или солидных опухолей, например, рака печени, такого как, например, гепатоцеллюлярная карцинома, которые, например, не поддаются лечению другими химиотерапевтическими агентами, известными как противоопухолевые агенты, противоопухолевый эффект комбинации противоопухолевого агента с комплексоном железа, например, с замещенным 3,5-дифенил-1,2,4-триазолом в отдельности, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислотой, является значительно выше по сравнению с лечением с использованием противоопухолевого агента или комплексона железа, например, замещенного 3,5-дифенил-1,2,4-триазола, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты, каждого в отдельности.
Перечень фигур чертежей.
На Фиг.2 показаны панели от А до Е, изображающие комбинации IC670 с 5-фторурацилом, митомицином С, цисплатином, тумодексом или лейковорином в человеческих клетках рака печени SK-HEP-1. В каждой панели показаны результаты двух исследований, представляющих изоболограммы, g-значение графиков и диаграммы поверхностных откликов (Surface Response Plots).
На Фиг.3 показаны панели от А до Е, изображающие комбинации IC670 с 5-фторурацилом, митомицином С, цисплатином, тумодексом или лейковорином в человеческих клетках рака печени НЕР3 В21-7. В каждой панели показаны результаты двух исследований, представляющих изоболограммы, g-значение графиков и диаграммы поверхностных откликов (Surface Response Plots).
Комбинации
Следует понимать, что ссылка на компоненты (а) и (б) означает также фармацевтически приемлемые соли любых активных веществ. Если активные вещества, включенные в состав компонентов (а) и/или (б), содержат, например, по крайней мере один основный центр, то они образуют кислотно-аддитивные соли. При необходимости получают также соответствующие кислотно-аддитивные соли, если они содержат дополнительный основный центр. Активные вещества, содержащие кислотную группу, например СООН, образуют соли оснований. Активные вещества, включенные в состав компонентов (а) и/или (б) или их фармацевтически приемлемых солей, можно использовать также в форме гидратов или сольватов, содержащих другие растворители, использованные при кристаллизации. Наиболее предпочтительным компонентом комбинации (а) являются замещенные 3,5-дифенил-1,2,4-триазолы.
В настоящем изобретении предлагается комбинация фармацевтических агентов, включающая:
(а) комплексен железа, такой как соединение формулы II
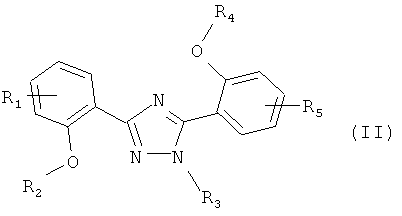
где R1 и R5 одновременно или независимо друг от друга означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси, галоген(низш.)алкокси, карбокси, карбамоил, N-(низш.)алкилкарбамоил, N,N-ди(низш.)алкилкарбамоил или нитрил, R2 и R4 одновременно или независимо друг от друга означают водород, незамещенный или замещенный (низш.)алканоил или ароил, или радикал, который можно удалить в физиологических условиях, R3 означает R6R7N-C(O)-(низш.)алкил, незамещенный или замещенный арил, арил(низш.)алкил, замещенный N-(низш.)алкиламино, N,N-ди(низш.)алкиламино или пирролидино, или незамещенный или замещенный гетероарил или гетероаралкил, при условии, что R3 не означает фенил или фенил, замещенный группами галоген, нитро, нитрил, гидрокси, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или (низш.)алкоксикарбонил, если R2 и R4 означают водород, a R1 и R5 означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или нитрил, R6 и R7 одновременно или независимо друг от друга означают водород, (низш.)алкил, гидрокси(низш.)алкил, алкокси(низш.)алкил, гидроксиалкокси(низш.)алкил, амино(низш.)алкил, N-(низш.)алкиламино(низш.)алкил, N,N-ди-(низш.)алкиламино(низш.)алкил, N-(гидрокси(низш.)алкил)амино(низш.)алкил, N,N-ди-(гидрокси(низш.)алкил)амино(низш.)алкил, или вместе с атомом азота, к которому они присоединены, образуют азаалициклическое кольцо или соли указанных соединений, и
(б) один или более других противоопухолевых агентов.
Термин «галоген» означает, например, хлор, бром или фтор, а также иод.
Термин «(низш.)» означает радикал, содержащий не более 7 и прежде всего не более 4 атомов углерода.
Алкил означает радикал с прямой или разветвленной цепью. Алкил сам по себе, например, (низш.)алкил, или в составе других групп, например, (низш.)алкокси, (низш.)алкиламин, (низш.)алканоил, (низш.)алкиламинокарбонил, является незамещенным или замещенным, например, группами галоген, гидрокси, (низш.)алкокси, трифторметил, цикло(низш.)алкил, азаалициклил или фенил, предпочтительно является незамещенным или замещенным группой гидрокси.
Термин «(низш.)алкил» означает, например, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, неопентил, н-гексил или н-гептил, предпочтительно метил, этил и н-пропил. Термин «галоген(низш.)алкил» означает (низш.)алкил, замещенный атомом галогена, предпочтительно хлора или фтора, предпочтительно не более 3 атомами хлора или фтора.
Термин «(низш.)алкокси» означает, например, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-амилокси, изоамилокси, предпочтительно метокси и этокси. Термин «галоген(низш.)алкокси» означает (низш.)алкокси, замещенный атомом галогена, предпочтительно хлора или фтора, предпочтительно вплоть до 3 атомов хлора или фтора.
Термин «карбамоил» означает радикал H2N-C(O)-, «N-(низш.)алкилкарбамоил» означает (низш.)алкил-HN-C(O)- и термин «N,N-ди(низш.)алкилкарбамоил» означает ди(низш.)алкил-N-C(O)-.
Термин «(низш.)аканоил» означает HC(O)- и (низш.)алкил-C(О)-, например ацетил, пропаноил, бутаноил или пивалоил.
Термин «(низш.)алкоксикарбонил» означает радикал (низш.)алкил-O-C(O)-, например, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, н-амилоксикарбонил, изоамилоксикарбонил, предпочтительно метоксикарбонил и этоксикарбонил.
Арил сам по себе, например, арил, или в составе других групп, например, арил(низш.)алкил или ароил, означает, например, фенил или нафтил, который является незамещенным или замещенным. Арил предпочтительно означает фенил, который является незамещенным или замещенным одним или более, прежде всего одним или двумя, заместителями, например, (низш.)алкил, (низш.)алкокси, гидрокси, нитро, амино, галоген, трифторметил, карбоксил, (низш.)алкоксикарбонил, N-(низш.)алкиламино, N,N-ди(низш.)алкиламино, аминокарбонил, (низш.)алкиламинокарбонил, ди(низш.)алкиламинокарбонил, гетероциклоалкил, гетероарил или циано. Прежде всего, арил означает незамещенный фенил или нафтил, или фенил, замещенный группами (низш.)алкил, (низш.)алкокси, гидрокси, галоген, карбокси, (низш.)алкоксикарбонил, N,N-ди(низш.)алкиламино или гетероциклоалкилкарбонил.
Термин «ароил» означает радикал арил-C(O)-, например, бензоил, толуоил, нафтоил или пара-метоксибензоил.
Термин «арил(низш.)алкил» означает, например, бензил, пара-хлорфенил, орто-фторбензил, фенилэтил, пара-толилметил, пара-диметиламинобензил, пара-диэтиламинобензил, пара-цианобензил, пара-пирролидинобензил.
Термин «гетероциклоалкил» означает циклоалкильный радикал, содержащий от 3 до 8, прежде всего от 5 до 7, атомов в кольце, по крайней мере один из которых является гетероатомом, предпочтительно атомом кислорода, азота и серы. Термин «азаалициклил» означает насыщенный циклоалкильный радикал, содержащий от 3 до 8, прежде всего от 5 до 7, атомов в кольце, по крайней мере один из которых является атомом азота. Азаалициклил может также содержать в составе кольца другие гетероатомы, например атомы кислорода, азота или серы, и означает, например, пиперидинил, пиперазинил, морфолинил или пирролидинил. Азаалициклические радикалы являются незамещенными или замещенными группами галоген или (низш.)алкил. Предпочтительными являются азаалициклические радикалы, которые присоединяются через атом азота в составе кольца, например пиперидино, пиперазино, морфолино, пирролидино и т.п.
Гетероарил сам по себе, например, гетероарил, или в качестве заместителей других групп, например, гетероарил(низш.)алкил, означает ароматический радикал, содержащий от 3 до 7, прежде всего от 5 до 7, атомов в составе кольца, по крайней мере один из которых является гетероатомом, например пирролил, имидазолил, триазолил, тетразолил, оксазолил, тиазолил, фуранил, тиофенил, пиридил, пиразинил, оксазинил, тиазинил, пиранил или пиримидинил. Гетероарил является незамещенным или замещенным. Предпочтительным является гетероарил, незамещенный или замещенный одним или более, прежде всего одним или двумя, заместителями, например (низш.)алкил, галоген, трифторметил, карбокси или (низш.)алкоксикарбонил.
Термин «гетероарил(низш.)алкил» означает (низш.)алкил, в котором, если алкильная цепь содержит 2 или более атомов углерода, по крайней мере один атом водорода, предпочтительно у концевого атома углерода, заменен на гетероарильную группу.
Термин «N-(низш.)алкиламино» означает, например, н-пропиламино, н-бутиламино, изопропиламино, изобутиламино, гидроксиэтиламино, предпочтительно метиламино и этиламино. Алкильные заместители в составе группы N,N-ди(низш.)алкиламино являются одинаковыми или различными. Термин «N,N-ди(низш.)алкиламино» означает, например, N,N-диметиламино, N,N-диэтиламино, N,N-метилэтиламино, N-метил-N-морфолиноэтиламино, N-метил-N-гидроксиэтиламино, N-метил-N-бензиламино.
Солями соединений формулы I являются, прежде всего, фармацевтически приемлемые соли, прежде всего соли оснований, такие как соли соответствующих щелочных металлов или щелочно-земельных металлов, например соли натрия, калия или магния, фармацевтически приемлемые соли переходных металлов, такие как соли цинка, или соли органических аминов, таких как циклические амины, такие как моно-, ди- или три(низш.)алкиламины, такие как гидрокси(низш.)алкиламины, например, моно-, ди- или тригидрокси(низш.)алкиламины, гидрокси(низш.)алкил(низш.)алкиламины или полигидрокси(низш.)алкиламины. Циклическими аминами являются, например, морфолин, тиоморфолин, пиперидин или пирролидин. Пригодными моно(низш.)алкиламинами являются, например, этил- и трет-бутиламин, ди(низш.)алкиламинами являются, например, диэтил- и диизопропиламин, и три(низш.)алкиламинами являются, например, триметил- и триэтиламин. Соответствующими гидрокси(низш.)алкиламинами являются, например, моно-, ди- и триэтаноламины, гидрокси(низш.)алкил(низш.)алкиламинами являются, например, N,N-диметиламино- и N,N-диэтиламиноэтанол, пригодным полигидрокси(низш.)алкиламином является, например, глюкозамин. В других случаях можно получать кислотно-аддитивные соли, например, сильных неорганических кислот, таких как минеральные кислоты, например, серная кислота, фосфорная кислота или галогенводородная кислота, сильных органических карбоновых кислот, таких как (низш.)алканкарбоновые кислоты, например, уксусной кислотый, таких как насыщенные или ненасыщенные дикарбоновые кислоты, например, малоновая, малеиновая или фумаровая кислота, или таких как гидроксикарбоновые кислоты, например лимонная или винная кислота, или сульфоновых кислот, таких как (низш.)алкан- или замещенные или незамещенные бензолсульфоновые кислоты, например метан- или пара-толуолсульфоновая кислота. Соединения формулы I, содержащие кислотную группу, например карбоксильную группу, и основную группу, например аминогруппу, могут существовать в форме внутренних солей, например в цвиттерионной форме, или часть молекулы может существовать в форме внутренней соли, а другая часть - в форме обычной соли.
Соединение формулы I, где R2 и R4 каждый независимо означает водород, R1 и R5 означает гидрокси, а R3 означает фенил, замещенный карбоксильной группой, то есть 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, выпускается под торговым названием EXJADE®.
Соединения формулы I и 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойная кислота и их фармацевтически приемлемые соли описаны в заявке WO 97/49395, опубликованной 31 декабря 1997 г, и в патенте US №6465504.
4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойная кислота в форме свободной кислоты, ее соли и кристаллогидраты описаны в заявке WO 97/49395, включенной в настоящее описание в качестве ссылки.
Термин «противоопухолевые агенты», использованный в данном контексте, включает, без ограничения перечисленным, ингибитор ароматазы,
1. антиэстроген, антиандроген или агонист гонадорелина,
2. ингибитор топоизомеразы I или ингибитор топоизомеразы II,
3. активный агент микротрубочек, алкилирующий агент, противоопухолевый метаболит или соединение платины,
4. соединение, связывающееся с протеин- или липидкиназой/снижающее их активность или связывающееся с протеин- или липидфосфатазой/снижающее их активность, другое противоопухолевое соединение или соединение, индуцирующее процессы дифференциации клеток,
5. моноклональные антитела,
6. ингибитор циклооксигеназы, бисфосфонат, ингибитор гепараназы, модификатор биологической ответной реакции,
7. ингибитор онкогенных изоформ Ras,
8. ингибитор теломеразы,
9. ингибитор протеазы, ингибитор матричной металлопротеиназы, ингибитор метионинаминопептидазы или ингибитор протеасомы,
10. агенты, используемые при лечении злокачественных заболеваний крови, или соединения, связывающиеся с Flt-3, снижающие или ингибирующие ее активность,
11. ингибитор HSP90,
12. антипролиферативные антитела,
13. ингибитор гистондеацетилазы (HDAC),
14. соединение, связывающееся с серин/треонинкиназой mTOR, снижающее или ингибирующее ее активность/функции,
15. антагонист рецептора соматостатина,
16. соединение, обладающее противолейкозным действием,
17. агенты, вызывающие повреждение опухолевых клеток,
18. агент, связывающий EDG,
19. ингибитор рибонуклеотидредуктазы,
20. ингибитор S-аденозилметиониндекарбоксилазы,
21. моноклональные антитела VEGF или VEGFR,
22. фотодинамические агенты,
23. ангиостатический стероид,
24. имплантат, содержащий кортикостероиды,
25. антагонист рецептора ATI и
26. ингибитор АКФ.
Термин «ингибиторы ароматазы», использованный в данном контексте, означает соединения, которые ингибируют продуцирование эстрогена, т.е. превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол соответственно. Данный термин включает, без ограничения перечисленным, стероиды, прежде всего атаместан, экземестан и форместан, и прежде всего нестероидные препараты, прежде всего аминоглутетимид, роглетимид, пиридоглутетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и предпочтительно летрозол. Экземестан можно вводить, например, в форме коммерческого препарата, например, под торговым названием AROMASIN™. Форместан можно вводить, например, в форме коммерческого препарата, например, под торговым названием LENTARON™. Фадрозол можно вводить, например, в форме коммерческого препарата, например, под торговым названием AFEMA™. Анастрозол можно вводить, например, в форме коммерческого препарата, например, под торговым названием ARIMIDEX™. Летрозол можно вводить, например, в форме коммерческого препарата, например, под торговым названием FEMARA™ or FEMAR™. Аминоглутетимид можно вводить, например, в форме коммерческого препарата, например, под торговым названием ORIMETEN™.
Термин «антиэстрогены», использованный в данном контексте, означает соединения, которые подавляют действие эстрогенов на уровне рецептора эстрогена. Данный термин включает, без ограничения перечисленным, тамоксифен, фулвестрант, ралоксифен и гидрохлорид ралоксифена. Тамоксифен можно вводить, например, в форме коммерческого препарата, например, под торговым названием NOLVADEX™. Гидрохлорид ралоксифена можно вводить, например, в форме коммерческого препарата, например, под торговым названием EVISTA™. Фулвестрант получают, как описано в патенте US №4659516 или его можно вводить в форме под торговым названием FASLODEX™. Комбинацию по настоящему изобретению, включающую противоопухолевый агент, который является антиэстрогеном, прежде всего можно использовать для лечения опухолей молочной железы, положительных в отношении гормональных рецепторов.
Термин «антиандрогены», использованный в данном контексте, означает вещество, способное ингибировать биологическое действие андрогенных гормонов и включает, без ограничения перечисленным, бикалутамид (CASODEX™), который получают, например, как описано в патенте US №4636505.
Термин «агонист гонадорелина», использованный в данном контексте, включает, без ограничения перечисленным, абареликс, госерелин и ацетат госерелина. Госерелин описан в патенте US №4100274 и его можно вводить, например, в форме коммерческого препарата, например, под торговым названием ZOLADEX™. Абареликс получают, например, как описано в патенте US №5843901.
Термин «ингибиторы топоизомеразы I», использованный в данном контексте, включает, без ограничения перечисленным, топотекан, гиматекан, иринотекан, камптотецин, например 9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148, т.е. соединение А1, как описано в заявке WO99/17804. Иринотекан можно вводить, например, в форме коммерческого препарата, например, под торговым названием CAMPTOSAR™. Топотекан можно вводить, например, в форме коммерческого препарата, например, под торговым названием HYCAMTIN™.
Термин «ингибиторы топоизомеразы II», использованный в данном контексте, включает, без ограничения перечисленным: антрациклины доксорубицин, включая липосомальные составы, например, продукт CAELYX™, даунорубицин, включая липосомальные составы, например, продукт DAUNOSOME™, эпирубицин, идарубицин, митомицин С, пирарубицин и неморубицин, антрахиноны митоксантрон и лозоксантрон, подофиллотоксины этопозод и тенипозид. Этопозид можно вводить, например, в форме коммерческого препарата, например, под торговым названием ETOPOPHOS™. Тенипозид можно вводить, например, в форме коммерческого препарата, например, под торговым названием VM 26-BRISTOL™. Доксорубицин можно вводить, например, в форме коммерческого препарата, например, под торговым названием ADRIBLASTIN™. Эпирубицин можно вводить в форме под торговым названием FARMORUBICIN™. Идарубицин можно вводить, например, в форме коммерческого препарата, например, под торговым названием ZAVEDOS™. Митоксантрон можно вводить, например, в форме коммерческого препарата, например, под торговым названием NOVANTRON™.
Термин «активный агент микротрубочек» означает агенты, стабилизирующие микротрубочки, агенты, дестабилизирующие микротрубочки и ингибиторы полимеризации микротрубочек и включает, без ограничения перечисленным, таксаны, например паклитаксел и доцетаксел, алкалоиды барвинка, например, винбластин, прежде всего сульфат винбластина, винкристин, прежде всего сульфат винкристина, и винорелбин и дискодермолид, колхицины и эпотилоны и их производные, например эпотилон В или его производные. Паклитаксел можно вводить, например, в форме коммерческого препарата, например, под торговым названием TAXOL™, доцетаксел - под торговым названием TAXOTERE™. Сульфат винбластина можно вводить, например, в форме коммерческого препарата, например, под торговым названием VINBLASTIN R.P.™. Сульфат винкристина можно вводить, например, в форме коммерческого препарата, например, под торговым названием FARMISTIN™. Данный термин включает также непатентованные и другие лекарственные формы паклитакселя. Непатентованные формы паклитакселя включают, без ограничения перечисленным, гидрохлорид бетаксолола. Различные лекарственные формы паклитакселя включают, без ограничения перечисленным, наночастицы паклитакселя на основе альбумина под торговыми названиями ABRAXANE™, ONXOL™, CYTOTAX™. Дискодермолид получают, например, как описано в патентах US №4939168 и 5618487 океанографического института Harbor Branch или химическим синтезом, как описано, например, в заявках GB 2280677, WO 98/24429 и патентах US №5789605 и 6031133, которые включены в настоящее описание в качестве ссылок. Данный термин означает также производные эпотилона, которые описаны в патенте US №6194181 и заявках WO 98/10121, WO 98/25929, WO 98/08849, WO 99/43653, WO 98/22461 и WO 00/31247. Наиболее предпочтительными являются эпотолин А и/или В.
Термин «алкилирующий агент», использованный в данном контексте, включает, без ограничения перечисленным, циклофосфамид, ифосфамид, мелфалан или нитрозомочевину (продукты BCNU или Gliadel), или темозоламид (продукт TEMODAR). Циклофосфамид можно вводить, например, в форме коммерческого препарата, например, под торговым названием CYCLOSTIN, а ифосфамид - под торговым названием HOLOXAN.
Термин «противоопухолевый антиметаболит» включает, без ограничения перечисленным, 5-фторурацил (5-FU), капецитабин, гемцитабин, агенты, деметилирующие ДНК, такие как 5-азацитидин и децитабин, метотрексат, эдатрексат, и антагонисты фолиевой кислоты, такие как, без ограничения перечисленным, пемретрексед и лейковорин, и ингибиторы тимидилатсинтазы, например ралтитрексед (продукт TOMUDEX). Капецитабин можно вводить, например, в форме коммерческого препарата, например, под торговым названием XELODA, а гемцитабин - под торговым названием GEMZAR.
Термин «соединение платины», использованный в данном контексте, означает карбоплатин, цисплатин, сатраплатин, оксалиплатин или агенты на основе платины, такие как продукт ZD0473. Предпочтитеным соединением платины является цисплатин.
Термин «карбоплатин», использованный в данном контексте, означает противоопухолевый агент цис-диамин (1,1-циклобутандикарбоксилато)платины (II), который описан, например, в патенте US №4140707 или в статье R.C. Harrison и др., Inorg. Chim. Acta, т.46, с. L15 (1980). Данное лекарственное средство можно вводить, например, в форме коммерческого препарата, например, под торговым названием CARBOPLAT™ или PARAPLATIN™.
Термин «оксалиплатин», использованный в данном контексте, означает противоопухолевый агент, известный также под названием оксалатоплатина, описанный, например, в патенте US №5716988. Данное лекарственное средство можно вводить, например, как описано в цитированном патенте US или в форме коммерческого препарата, например, под торговым названием ELOXANTINE™ или 1-ОНР™.
Термин «цисплатин», использованный в данном контексте, означает противоопухолевый агент, известный также под названием цисдиаминдихлорплатина, структура и использование которой в качестве противоопухолевого агента описаны, например, в патенте Германии DE 2318020.
Термин «соединения, связывающиеся с протеин- или липидкиназой/снижающие их активность или связывающиеся с протеин- или липидфосфатазой/снижающие их активность или другие антиангиогенные соединения», использованный в данном контексте, включает, без ограничения перечисленным, ингибиторы протеинтирозинкиназы и/или серин- и/или треонинкиназы или ингибиторы липидкиназы, например:
1. соединения, связывающиеся с рецепторами эндотелиального роста сосудов (VEGF), снижающие или ингибирующие их активность, такие как соединения, которые связываются с VEGF, снижают или ингибируют его активность, прежде всего соединения, ингибирующие активность рецептора VEGF, такие как, без ограничения перечисленным, производные 7Н-пирроло[2,3-d]пиримидина, например, производное 7Н-пирроло[2,3-d]пиримидина, {6-[4-(4-этилпиперазин-1-илметил)фенил]-7Н-пирроло[2,3-d]пиримидин-4-ил]-((R)-1-фенилэтил)амин, продукт BAY 43-9006, соединения изохолина, описанные в заявке WO 00/09495, такие как (4-трет-бутилфенил)-(4-пиридин-4-илметилизохинолин-1-ил)амин,
2. соединения, связывающиеся с рецептором тромбоцитарного фактора роста (PDGFR), снижающие или ингибирующие его активность, такие как соединения, которые связываются с PDGFR, снижают или ингибируют его активность, прежде всего соединения, которые ингибируют рецептор PDGF, например, производное N-фенил-2-пиримидинамина, например иматиниб, продукт SU101, SU6668 и GFB-111,
3. соединения, связывающиеся с рецептором фактора роста фибробластов (FGFR), снижающие или ингибирующие его активность,
4. соединения, связывающиеся с рецептором 1 инсулиноподобного фактора роста (IGF-1R), снижающие или ингибирующие его активность, такие как соединения, которые связываются с IGF-1R, снижают или ингибируют его активность, прежде всего соединения, которые ингибируют рецептор IGF-1R. Соединения включают, без ограничения перечисленным, соединения, описанные в заявке WO 02/092599 и их производные, а также производные 4-амино-5-фенил-7-циклобутилпирроло[2,3-d]пиримидина,
5. соединения, связывающиеся с семейством рецептора Trk тирозинкиназ, снижающие или ингибирующие его активность,
6. соединения, связывающиеся с семейством рецептора Ахl тирозинкиназ, снижающие или ингибирующие его активность,
7. соединения, связывающиеся с рецептором c-Met, снижающие или ингибирующие его активность,
8. соединения, связывающиеся с рецептором Ret тирозинкиназ, снижающие или ингибирующие его активность,
9. соединения, связывающиеся с рецептором Kit/SCFR тирозинкиназ, снижающие или ингибирующие его активность,
10. соединения, связывающиеся с рецептором тирозинкиназ (подсемейства PDGFR), снижающие или ингибирующие его активность, такие как соединения, которые связываются с рецептором c-Kit семейства тирозинкиназ, снижают или ингибируют его активность, прежде всего соединения, которые ингибируют рецептор c-Kit, например, иматиниб,
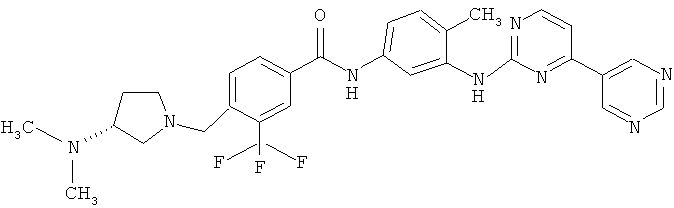
11. соединения, связывающиеся с членами семейства с-Abl и соответствующими гибридными белками, снижающие или ингибирующие их активность, например, киназы BCR-Abl, такие как соединения, которые связываются с членами семейства с-Abl и соответствующими гибридными белками, снижают или ингибируют их активность, например, производное N-фенил-2-пиримидинамина, например, иматиниб формулы (N-{5-[4-(4-метилпиперазинометил)бензоиламидо]-2-метилфенил}-4-(3-пиридил)-2-пиримидинамин, продукты PD180970, AG957, NSC 680410 или PD173955 фирмы ParkeDavis, нилотиниб или 4-метил-N-[3-(4-метилимидазол-1-ил)-5-(трифторметил)фенил]-3-[(4-пиридин-3-илпиримидин-2-ил)амино]бензамид, дазатиниб (продукт BMS3 54825) или моногидрат N-(2-хлор-6-метилфенил)-2-[[6-[4-(2-гидроксиэтил)-1-пиперазинил]-2-метил-4-пиримидинил]амино]-5-тиазолкарбоксамида, бозутиниб формулы
и продукт INNO-406 формулы
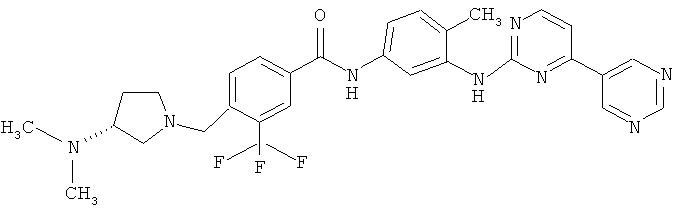
12. соединения, связывающиеся с членами семейства протеинкиназ С (РКС) и семейства серин/треонинкиназ Raf, членами семейств МЕK, SRC, JAK, FAK, PDK и Ras/MAPK или семейства киназ РI(3) или семейства киназ, родственных киназе РI(3) и/или членами циклин-зависимых киназ (CDK), снижающие или ингибирующие их активность, прежде всего производные стауроспорина, описанные в патенте US №5093330, например, мидостаурин, примеры других соединений влючают, например, UCN-01, сафингол, BAY 43-9006, бриостатин 1, перифозин, илмофозин, продукты RO 318220 и RO 320432, GO 6976, исис 3521, LY333531/LY379196, соединения изохинолина, такие как соединения, описанные в заявке WO 00/09495, продукты FTI, PD184352 или QAN697, а также ингибитор Р13K,
13. соединения, связывающиеся с протеинтирозинкиназой, снижающие или ингибирующие ее активность, тирфостин или пиримидиламинобензамид или их производные, например 4-метил-3-[[4-(3-пиридинил)-2-пиримидинил]амино]-N-[5-(4-метил-1Н-имидазол-1-ил)-3-(трифторметил)фенил]бензамид. Тирфостин предпочтительно является низкомолекулярным соединением (ММ<1500) или его фармацевтически приемлемой солью, прежде всего соединением, которое выбирают из бензилиденмалонитрилов или S-арилбензолмалонитрилов или бисубстратов хинолинов, более предпочтительно любым соединением, которое выбирают из группы, включающей тирфостин A23/RG-50810, AG 99, тирфостин AG 213, тирфостин AG 1748, тирфостин AG 490, тирфостин В44, тирфостин В44 (+) энантиомер, тирфостин AG 555, AG 494, тирфостин AG 556, AG957 и адафостин (адамантиловый эфир (4-{[(2,5-дигидроксифенил)метил]амино}бензойной кислоты, NSC 680410, адафостин),
14. соединения, связывающиеся с семейством рецепторных тирозинкиназ эпидермальных факторов роста (EGFR, ErbB2, ErbB3, ErbB4 в виде гомо- и гетеродимеров), снижающие или ингибирующие их активность семейства, такие как соединения, которые связываются с рецепторами семейства эпидермальных факторов роста, снижают или ингибируют их активность, прежде всего соединения, белки или антитела, которые ингибируют активность членов семейства рецепторов тирозинкиназ EGF, например рецептора EGF, ErbB2, ErbB3 и ErbB4, или связываются с EGF или EGF-подобными лигандами, и прежде всего соединения, белки или моноклональные антитела, описанные в заявке WO 97/02266, например соединение, описанное в примере 39, или в документах ЕР 0564409, WO 99/03854, ЕР 0520722, ЕР 0566226, ЕР 0787722, ЕР 0837063, US №5747498, WO 98/10767, WO 97/30034, WO 97/49688, WO 97/38983 и прежде всего в заявке WO 96/30347, например соединение СР 358774, в заявке WO 96/33980, например соединение ZD 1839, и в заявке WO 95/03283, например соединение ZM105180, например трастузумаб (продукт HERCEPTIN®), цетуксимаб, иресса, продукты OSI-774, CI-1033, ЕКВ-569, GW-2016, Е1.1, Е2.4, Е2.5, Е6.2, Е6.4, Е2.11, Е6.3 или Е7.6.3, и производные 7Н-пирроло[2,3-d]пиримидина, которые описаны в заявке WO 03/013541, эрлотиниб и гефитиниб. Эрлотиниб можно вводить в виде коммерческого продукта, например, продукта TARCEVA, а гефитиниб в виде продукта IRESSA, моноклональных антител человека против рецептора эпидермального фактора роста, включая ABX-EGFR,
15. соединения, связывающиеся с серин/треонинкиназами mTOR, снижающие или ингибирующие их активность/функцию, прежде всего соединения, белки или антитела, которые связываются с членами семейства киназ mTOR /ингибируют их активность, например, соединения RAD, RAD001, CCI-779, ABT578, SAR543, рапамицин и их производные/аналоги, продукты АР23573 и АР23841 фирмы Ariad, эверолимус (продукт CERTICAN), сиролимус, продукт CERTICAN (эверолимус, RAD), который является новым ингибитором передачи сигнала пролиферации, который предотвращает протиферацию Т-клеток и клеток гладкой мускулатуры сосудов.
Термин «антитела» включает интактные моноклональные антитела, нанотела, поликлональные антитела, мультиспецифичные антитела, полученные по крайней мере из 2 интактных антител, и фрагменты антител достаточной длины для проявления требуемой биологической активности.
Словосочетание «соединение, которое связывается с протеин- или липидфосфатазой, снижает или ингибирует их активность», использованное в данном контексте, означает, без ограничения перечисленным, ингибиторы фосфатазы 1, фосфатазы 2А, PTEN или CDC25, например, окадаевая кислота или ее производные.
Термин «другие антиангиогенные соединения», использованный в данном контексте, означает талидомид, например продукт THALOMID™, леналидомид, например продукты Revlimid®, TNP-470 и SU5416.
Словосочетание «соединения, которые индуцируют процессы дифференциации клеток», использованное в данном контексте, включает, без ограничения перечисленным, ретиноевую кислоту, токоферол или токотриенол.
Термин «моноклональные антитела», использованный в данном контексте, включает, без ограничения перечисленным, бевацизумаб, цетуксимаб, трастузумаб, ибритумомаб тиуксетан, тозитумомаб и иод I131. Бевацизумаб можно вводить в форме коммерческого продукта, например, в виде продукта AVASTIN, цетуксимаб - в виде продукта ERBITUX, трастузумаб в виде продукта HERCEPTIN, ритуксимаб - в виде продукта MABTHERA, ибритумомаб тиуксетан - в виде продукта ZEVULIN и тозитумомаб и иод I131 - в виде продукта BEXXAR.
Термин «ингибитор циклооксигеназы», использованный в данном контексте, включает, без ограничения перечисленным, например, ингибиторы Сох-2, 5-алкилзамещенную 2-ариламинофенилуксусную кислоту и ее производные, такие как целекоксиб (продукт CELEBREX), рофекоксиб (продукт VIOXX), эторикоксиб, валдекоксиб или 5-алкил-2-ариламинофенилуксусную кислоту, например, 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусную кислоту, лумиракоксиб.
Термин «бисфосфонаты», использованный в данном контексте, означает, без ограничения перечисленным, этридоновую кислоту, клодроновую кислоту, тилудроновую кислоту, памидроновую кислоту, алендроновую кислоту, ибандроновую кислоту, ризедроновую кислоту и золедроновую кислоту. Этридоновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием DIDRONEL™. Клодроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием BONEFOS™. Тилудроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием SKELID™. Памидроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием AREDIA™. Аледроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием FOSAMAX™. Ибадроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием BONDRANAT™. Ризедроновую кислоту можно вводить, например, в форме коммерческого препарата, например, под торговым названием ACTONEL™. Золедроновую кислоту можно вводить, например, в виде коммерческого препарата, например, под торговым названием ZOMETA™.
Термин «ингибитор гепараназы», использованный в данном контексте, означает соединения, которые связываются с сульфатом гепарина, снижают или ингибируют его деградацию. Данный термин включает, без ограничения перечисленным, продукт PI-88.
Термин «модификатор биологической ответной реакции», использованный в данном контексте, включает, без ограничения перечисленным, лимфокины или интерфероны, например интерферон γ.
Термин «ингибитор онкогенных изоформ Ras», использованный в данном контексте, включает, без ограничения перечисленным, H-Ras, K-Ras или N-Ras, и означает соединения, которые связываются с онкогенной Ras, снижают или ингибируют онкогенную активность Ras, например ингибитор фарнезилтрансферазы (FTI), например, продукты L-744832, DK8G557 или R115777 (ZARNESTRA).
Термин «ингибитор теломеразы», использованный в данном контексте, включает, без ограничения перечисленным, соединения, которые связываются с теломеразой, снижают или ингибируют ее активность. Соединениями, которые связываются с теломеразой, снижают или ингибируют ее активность, прежде всего являются соединения, которые ингибируют рецептор теломеразы, например теломестатин.
Термин «ингибитор матричной металлопротеиназы» или «ингибитор ММР», использованный в данном контексте, включают, без ограничения перечисленным, ингибиторы коллагеновых пептидомиметиков и непептидомиметиков, производные тетрациклина, например ингибитор-пептидомиметик гидроксамат батимастата, и его пероральные биодоступные аналоги маримастат (ВВ-2516), приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566, ТАА211, MMI270B или AAJ996.
Термин «ингибитор метионинаминопептидазы», использованный в данном контексте, включает, без ограничения перечисленным, соединения, которые связываются с метионинаминопептидазой, снижают или ингибируют ее активность. Соединениями, которые связываются с метионинаминопептидазой, снижают или ингибируют ее активность, являются, например, бенгамид или его производные.
Термин «ингибиторы протеасомы», использованный в данном контексте, включает соединения, которые связываются с протеосомой, снижают или ингибируют ее активность. Соединениями, которые связываются с протеосомой, снижают или ингибируют ее активность, являются, без ограничения перечисленным, продукты PS-341, MLN 341, бортезомиб или велкад.
Словосочетание «агент, используемый при лечении злокачественных заболеваний крови», использованный в данном контексте, включает, без ограничения перечисленным, ингибиторы тирозинкиназ типа FMS, например соединения, которые связываются с рецепторами тирозинкиназ типа FMS (Flt-3R), снижают или ингибируют их активность, интерферон, 1-b-D-арабинофуранзилцитозин (ara-c) и бисульфан, и ингибиторы ALK, например соединения, которые связываются с киназой анапластической лимфомы, снижают или ингибируют ее активность.
Словосочетание «соединения, которые связываются с Flt-3, снижают или ингибируют ее активность», использованный в данном контексте, включает, без ограничения перечисленным, соединения, белки или антитела, которые ингибируют Flt-3, например, N-бензоилстауроспорин, мидостаурин, производные стауроспорина, продукты SU11248 и MLN518.
Термин «ингибиторы HSP90», использованный в данном контексте, включает, без ограничения перечисленным, соединения, которые связываются с HSP90, снижают или ингибируют АТФ-азную активность HSP90, связываются с клиентными белками HSP90, расщепляют, снижают или ингибируют их активность через убихитиновый путь протеосомы. Соединениями, которые связываются с HSP90, снижают или ингибируют АТФ-азную активность HSP90, являются, прежде всего, соединения, белки или антитела, которые ингибируют АТФ-азную активность HSP90, например 17-аллиламино-,17-деметоксигелданамицин (17AAG), производные гелданамицина, другие соединения, родственные гелданамицину, радицикол и ингибиторы HDAC.
Термин «антипролиферативные антитела», использованный в данном контексте, включает, без ограничения перечисленным, трастузумаб (продукт HERCEPTIN), трастузумаб-DM1, эрлотиниб (продукт TARCEVA), бевацизумаб (продукт AVASTIN), ритуксимаб (продукт RITUXAN), продукт PRO64553 (анти-CD40) и антитела 2С4. Термин «антитела» означает, например, интактные моноклональные антитела, поликлональные антитела, мультиспецифичные антитела, полученные по крайней мере из 2 интактных антител, и фрагменты антител достаточной длины для проявления требуемой биологической активности.
Термин «ингибитор гистондеацетилазы (HDAC)», использованный в данном контексте, означает соединения, которые ингибируют гистондеацетилазу и проявляют антипролиферативную активность. Такие соединения включают, без ограничения перечисленным, соединения, описанные в заявке WO 02/22577, прежде всего N-гидрокси-3-[4-[[(2-гидроксиэтил)[2-(1Н-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид, N-гидрокси-3-[4-[[[2-(2-метил-1H-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид и их фармацевтически приемлемые соли. Такие соединения, кроме того, включают субероиланилид гидроксамовой кислоты (SAHA), продукты MS-275, FK228 (ранее известный под названием FR901228), пиридин-3-илметиловый эфир [4-(2-аминофенилкарбамоил)бензил]карбаминовой кислоты и их производные, бутановую кислоту, пироксамид, трихостатин А, оксамфлатин, апицидин, депзипептид, депудецин, трапоксин и соединения, описанные в заявке WO 02/22577, прежде всего N-гидрокси-3-[4-({(2-гидроксиэтил)-[2-(1Н-индол-3-ил)этил]амино}метилфенил]акриламид или его лактат.
Словосочетание «соединения, которые связываются с серин/треонинкиназами mTOR, снижают или ингибируют их активность/функцию», использованное в данном контексте, включает, без ограничения перечисленным, соединения, белки или антитела, которые связываются с членами семейства киназ mTOR/ингибируют их активность, например, продукты RAD, RAD001, CCI-779, ABT578, SAR543, рапамицин и их производные/аналоги, продукты АР23573 и АР23841 фирмы Ariad, эверолимус (продукт CERTICAN) и сиролимус (продукт RAPAMUNE), продукты CCI-779 и ABT578. Продукт CERTICAN (эверолимус, RAD) является новым ингибитором передачи сигнала пролиферации, который предотвращает пролиферацию Т-клеток и клеток гладкой мускулатуры сосудов.
Термин «антагонист рецептора соматостатина», использованный в данном контексте, включает, без ограничения перечисленным, агенты, которые связываются с рецептором соматостатина, снижают или ингибируют его активность, такие как октреотид, вапреотид, ланреотид и продукт SOM230.
Термин «противолейкозное соединение», использованный в данном контексте, включает, без ограничения перечисленным, продукт Ara-C, аналог пиримидина, который является 2'-α-гидроксирибозил (арабинозил) производным дезоксицитидина. Данный термин включает также пуриновый аналог гипоксантина, 6-меркаптопурин (6-МР) и фосфат флударабина.
Словосочетание «агенты, вызывающие повреждение опухолевых клеток», означает агенты, такие как ионизирующее излучение. Термин «ионизирующее излучение», использованный в данном контексте, означает ионизирующее излучение, т.е. поток электромагнитных лучей, таких как рентгеновские лучи или γ-лучи, или частиц, таких как α-, β- и γ-частиц. Ионизирующее излучение используют, без ограничения перечисленным, в лучевой терапии (см. статью Hellman, Cancer, 4-е изд, т.1, под ред. Devita и др., сс.248-275 (1993).
Термин «агент, связывающий EDG», использованный в данном контексте, включает, без ограничения перечисленным, класс иммунодепрессантов, которые модулируют рециркуляцию лимфоцитов, такие как продукт FTY720.
Термин «ингибитор рибонуклеотидредуктазы», использованный в данном контексте, включает, без ограничения перечисленным, аналоги нуклеозидов пиримидина или пурина, включающие, без ограничения перечисленным, флударабин и/или продукт Ara-C, 6-тиогуанин, 5-FU, кладрибин, 6-меркаптопурин, прежде всего в комбинации с продуктом Ara-C (для лечения острого лимфоцитарного лейкоза (ALL)), и/или пентостатин. Ингибиторами рибонуклеотидредуктазы прежде всего являются гидроксимочевина или производные 2-гидрокси-1H-изоиндол-1,3-диона, такие как продукты PL-1, PL-2, PL-3, PL-4, PL-5, PL-6, PL-7 или PL-8 (см. статью Nandy и др., Acta Oncologica, т.33, №8. с.953-961 (1994)).
Термин «ингибиторы S-аденозилметиониндекарбоксилазы», использованный в данном контексте, включает, без ограничения перечисленным, соединения, описанные в патенте US №5461076.
Термин «моноклональные антитела VEGF или VEGFR», использованный в данном контексте, включает, без ограничения перечисленным, соединения, описанные в заявке WO 98/35958, например, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин, или их фармацевтически приемлемые соли, например сукцинат, или в заявках WO 00/09495, WO 00/27820, WO 00/59509, WO 98/11223, WO 00/27819 и ЕР 0769947, описанные в статьях Prewett и др., Cancer Res, т.59, с.5209-5218 (1999), Yuan и др., Proc Nati Acad Sci USA, т.93, с.14765-14770 (1996), Zhu и др. Cancer Res, т.58, с.3209-3214 (1998) и Mordenti и др., Toxicol Pathol, т.27, №1, с.14-21 (1999), в заявках WO 00/37502 и WO 94/10202, продукт ANGIOSTATIN, описанный в статье O'Reilly и др., Cell, т.79, с. 315-328 (1994), продукт ENDOSTATIN, описанный в статье O'Reilly и др., Cell, т.88, с.277-285 (1997); амиды антраниловой кислоты, продукты ZD4190, ZD6474, SU5416, SU6668, бевацизумаб или антитела против VEGF или антитела против рецептора VEGF, например, продукты rhuMAb и RHUFab, аптамер VЕGF, например, макугон, ингибиторы FLT-4, ингибиторы FLT-3, антитела VEGFR-2 IgG1, ангиозим (RPI 4610) и авастан.
Термин «фотодинамическая терапия», использованный в данном контексте, означает терапию, при которой для лечения или профилактики рака используют определенные химические агенты, известные фотосенсибилизаторы. Примеры фотодинамической терапии включают, без ограничения перечисленным, лечение агентами, такими как, например, продукт VISUDYNE и натриевая соль порфимера.
Термин «ангиостатический стероид», использованный в данном контексте, включает, без ограничения перечисленным, агенты, блокирующие или ингибирующие ангиогенез, такие как, например, анекортав, триамцинолон, гидрокортизон, 11-α-эпигидрокортизол, кортексолон, 17α-идроксипрогестрон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон и дексаметазон.
Термин «имплантат, содержащий кортикостероиды», использованный в данном контексте, включает, без ограничения перечисленным, агенты, такие как, например, флуоцинолон и дексаметазон.
Термин «антагонист рецептора AT1», использованный в данном контексте, включает, без ограничения перечисленным, агенты, такие как продукт DIOVAN.
Термин «ингибитор АКФ», использованный в данном контексте, включает, без ограничения перечисленным, продукт CIBACEN, беназеприл, эназеприл (продукт LOTENSIN), каптоприл, эналаприл, фозиноприл, лизиноприл, моэксиприл, хинаприл, рамиприл, периндоприл и трандолаприл.
Другие фармацевтически активные агенты включают, без ограничения перечисленным, растительные алкалоиды, гормональные агенты и антагонисты, модификаторы биологической ответной реакции, предпочтительно лимфокины или интерфероны, антисмысловые олигонуклеотиды или производные олигонуклеотидов, или другие агенты или агенты, которые действуют по другому или неизвестному механизму.
Во всех случаях цитирования заявок на выдачу патентов или научных статей, прежде всего в отношении заявляемых в настоящем изобретении соединений и конечных продуктов, описанных в примерах, предмет конечных продуктов, фармацевтических составов и прилагаемых пунктов формулы изобретения включен в настоящее описание в качестве ссылок на указанные публикации. Указанные соединения включают также их соответствующие стереоизомеры, соответствующие кристаллические модификации, например, сольваты и полиморфные формы. Соединения, используемые в качестве активных ингредиентов в комбинациях, описанных в данном контексте, можно получать и вводить, как описано в цитированных документах, соответственно.
Структура активных агентов, их кодовые номера, общие или торговые названия приведены в текущем издании справочника «The Merck Index» или в базах данных, например, Patents International, например, IMS World Publications.
Соответствующее содержание указанных источников включно в настоящее описание в качестве ссылок.
В одном варианте настоящего изобретения предлагается комбинация (а) комплексона железа формулы II, где R1 и R5 одновременно или независимо друг от друга означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или галоген(низш.)алкокси, R2 и R4 одновременно или независимо друг от друга означают водород или радикал, который можно удалить в физиологических условиях, R3 означает R6R7N-C(O)-(низш.)алкил, замещенный арил, арил(низш.)алкил, замещенный N-(низш.)алкиламино, N,N-ди-(низш.)алкиламино или пирролидино, или незамещенный или замещенный гетероаралкил, при условии, что R3 не означает фенил, замещенный группами галоген, нитро, нитрил, гидрокси, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или (низш.)алкоксикарбонил, если R2 и R4 означают водород, а R1 и R5 означают водород, галоген, (низш.)алкил, галоген(низш.)алкил или (низш.)алкокси. R6 и R7 одновременно или независимо друг от друга означают водород, (низш.)алкил, гидрокси(низш.)алкил, алкокси(низш.)алкил, гидроксиалкокси(низш.)алкил, амино(низш.)алкил, N-(низш.)алкиламино(низш.)алкил, N,N-ди-(низш.)алкиламино(низш.)алкил, N-(гидрокси(низш.)алкил)амино(низш.)алкил, N,N-ди-(гидрокси(низш.)алкил)амино(низш.)алкил или вместе с атомом азота, к которому они присоединены, образуют азаалициклическое кольцо или соли указанных соединений, и
(б) один или более других противоопухолевых агентов.
В другом варианте настоящего изобретения предлагается комбинация
(а) соединения формулы II

где
R1 и R5 одновременно или независимо друг от друга означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси, галоген(низш.)алкокси, карбокси, карбамоил, N-(низш.)алкилкарбамоил, N,N-ди(низш.)алкилкарбамоил или нитрил, R2 и R4 одновременно или независимо друг от друга означают водород, незамещенный или замещенный (низш.)алканоил или ароил, или радикал, который можно удалить в физиологических условиях, R3 означает R6R7NC(O)-(низш.)алкил, незамещенный или замещенный арил, арил(низш.)алкил, замещенный N-(низш.)алкиламино, N,N-ди(низш.)алкиламино или пирролидино, или незамещенный или замещенный гетероарил или гетероаралкил, при условии, что R3 не означает фенил или фенил, замещенный группами галоген, нитро, нитрил, гидрокси, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или (низш.)алкоксикарбонил, если R2 и R4 означают водород, а R1 и R5 означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или нитрил, R6 и R7 одновременно или независимо друг от друга означают водород, (низш.)алкил, гидрокси(низш.)алкил, алкокси(низш.)алкил, гидроксиалкокси(низш.)алкил, амино(низш.)алкил, N-(низш.)алкиламино(низш.)алкил, N,N-ди-(низш.)алкиламино(низш.)алкил, N-(гидрокси(низш.)алкил)амино(низш.)алкил, N,N-ди-(гидрокси(низш.)алкил)амино(низш.)алкил, или вместе с атомом азота, к которому они присоединены, образуют азаалициклическое кольцо или соли указанных соединений,
(б) один или более фармацевтически активных агентов, которые выбирают из группы, включающей ингибитор ароматазы, антиэстроген, антиандроген, агонист гонадорелина, ингибитор топоизомеразы I, ингибитор топоизомеразы II, активный агент микротрубочек, алкилирующий агент, противоопухолевый антиметаболит, соединение платины, соединение, связывающееся с протеин- или липидфосфатазой или протеин- или липидкиназой/снижающее их активность, антиангиогенное соединение, соединение, индуцирующее процессы дифференциации клеток, моноклональные антитела, ингибитор циклооксигеназы, бисфосфонат, ингибитор гепараназы, модификатор биологической ответной реакции, ингибитор онкогенных изоформ Ras, ингибитор теломеразы, ингибитор протеазы, ингибитор матричной металлопротеиназы, ингибитор метионинаминопептидазы, ингибитор протеасомы, агенты, связывающиеся с Flt-3, снижающие или ингибирующие ее активность, ингибитор HSP90, антипролиферативные антитела, ингибитор HDAC, соединение, связывающееся с серин/треонинкиназой mTOR, снижающее или ингибирующее их активность/функции, антагонист рецептора соматостатина, соединение, обладающее противолейкозным действием, агенты, вызывающие повреждение опухолевых клеток, агент, связывающий EDG, ингибитор рибонуклеотидредуктазы, ингибитор S-аденозилметиониндекарбоксилазы, моноклональные антитела VEGF или VEGFR, фотодинамические агенты, ангиостатический стероид, имплантат, содержащий кортикостероиды, антагонист рецептора ATI и ингибитор АКФ.
В настоящем изобретении предлагается способ профилактики пролиферативных заболеваний или заболеваний, индуцированных персистирующим ангиогенезом у млекопитающих, предпочтительно у человека, который заключается во введении пацинту одновременно или последовательно фармацевтически эффективных количеств комбинации
(а) комплексона железа и
(б) фармацевтически эффективного агента.
В другом объекте настоящего изобретения предлагается фармацевтическая композиция, включающая комбинацию
(а) комплексона железа и
(б) фармацевтически эффективного агента.
В еще одном объекте настоящего изобретения предлагается фармацевтический препарат, включающий
(а) комплексен железа и
(б) один или более фармацевтически активных агентов в смеси с фармацевтически приемлемым носителем.
В предпочтительном варианте осуществления настоящего изобретения предлагается фармацевтический препарат, включающий
(а) соединение формулы II

где R1 и R5 одновременно или независимо друг от друга означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси, галоген(низш.)алкокси, карбокси, карбамоил, N-(низш.)алкилкарбамоил, N,N-ди(низш.)алкилкарбамоил или нитрил, R2 и R4 одновременно или независимо друг от друга означают водород, незамещенный или замещенный (низш.)алканоил или ароил, или радикал, который можно удалить в физиологических условиях, R3 означает R6R7N-C(O)-(низш.)алкил, незамещенный или замещенный арил, арил(низш.)алкил, замещенный N-(низш.)алкиламино, N,N-ди(низш.)алкиламино или пирролидино, или незамещенный или замещенный гетероарил или гетероаралкил, при условии, что R3 не означает фенил или фенил, замещенный группами галоген, нитро, нитрил, гидрокси, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или (низш.)алкоксикарбонил, если R2 и R4 означают водород, a R1 и R5 означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или нитрил, R6 и R7 одновременно или независимо друг от друга означают водород, (низш.)алкил, гидрокси(низш.)алкил, алкокси(низш.)алкил, гидроксиалкокси(низш.)алкил, амино(низш.)алкил, N-(низш.)алкиламино(низш.)алкил, N,N-ди-(низш.)алкиламино(низш.)алкил, N-(гидрокси(низш.)алкил)амино(низш.)алкил, N,N-ди-(гидрокси(низш.)алкил)амино(низш.)алкил, или вместе с атомом азота, к которому они присоединены, образуют азаалициклическое кольцо, и соли указанных соединений, и
(б) один или более фармацевтически активных агентов, которые выбирают из группы, включающей ингибитор ароматазы, антиэстроген, антиандроген, агонист гонадорелина, ингибитор топоизомеразы I, ингибитор топоизомеразы II, активный агент микротрубочек, алкилирующий агент, противоопухолевый антиметаболит, соединение платины, соединение, связывающееся с протеин- или липидфосфатазой или протеин- или липидкиназой/снижающее их активность, антиангиогенное соединение, соединение, индуцирующее процессы дифференциации клеток, моноклональные антитела, ингибитор циклооксигеназы, бисфосфонат, ингибитор гепараназы, модификатор биологической ответной реакции, ингибитор онкогенных изоформ Ras, ингибитор теломеразы, ингибитор протеазы, ингибитор матричной металлопротеиназы, ингибитор метионинаминопептидазы, ингибитор протеасомы, агенты, связывающиеся с Flt-3, снижающие или ингибирующие ее активность, ингибитор HSP90, антипролиферативные антитела, ингибитор HDAC, соединение, связывающееся с серин/треонинкиназой mTOR, снижающее или ингибирующее их активность/функции, антагонист рецептора соматостатина, соединение, обладающее противолейкозным действием, агенты, вызывающие повреждение опухолевых клеток, агент, связывающий EDG, ингибитор рибонуклеотидредуктазы, ингибитор S-аденозилметиониндекарбоксилазы, моноклональные антитела VEGF или VEGFR, фотодинамические агенты, ангиостатический стероид, имплантат, содержащий кортикостероиды, антагонист рецептора ATI и ингибитор АКФ.
В другом предпочтительном варианте осуществления настоящего изобретения предлагается фармацевтический состав, включающий
(а) соединение формулы II

где R1 и R5 одновременно или независимо друг от друга означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси, галоген(низш.)алкокси, карбокси, карбамоил, N-(низш.)алкилкарбамоил, N,N-ди(низш.)алкилкарбамоил или нитрил, R2 и R4 одновременно или независимо друг от друга означают водород, незамещенный или замещенный (низш.)алканоил или ароил, или радикал, который можно удалить в физиологических условиях, R3 означает R6R7N-C(O)-(низш.)алкил, незамещенный или замещенный арил, арил(низш.)алкил, замещенный N-(низш.)алкиламино, N,N-ди(низш.)алкиламино или пирролидино, или незамещенный или замещенный гетероарил или гетероаралкил, при условии, что R3 не означает фенил или фенил, замещенный группами галоген, нитро, нитрил, гидрокси, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или (низш.)алкоксикарбонил, если R2 и R4 означают водород, a R1 и R5 означают водород, галоген, (низш.)алкил, галоген(низш.)алкил, (низш.)алкокси или нитрил, R6 и R7 одновременно или независимо друг от друга означают водород, (низш.)алкил, гидрокси(низш.)алкил, алкокси(низш.)алкил, гидроксиалкокси(низш.)алкил, амино(низш.)алкил, N-(низш.)алкиламино(низш.)алкил, N,N-ди-(низш.)алкиламино(низш.)алкил, N-(гидрокси(низш.)алкил)амино(низш.)алкил, N,N-ди-(гидрокси(низш.)алкил)амино(низш.)алкил, или вместе с атомом азота, к которому они присоединены, образуют азаалициклическое кольцо, и соли указанных соединений,
(б) один или более фармацевтически активных агентов, которые выбирают из группы, включающей ингибитор топоизомеразы I, ингибитор топоизомеразы II, активный агент микротрубочек, алкилирующий агент, противоопухолевый антиметаболит, соединение платины, соединение, связывающееся с протеин- или липидкиназой или активность протеин- или липидфосфатазой/снижающее их активность, и антиангиогенное соединение.
Любая комбинация компонентов (а) и (б), способ лечения теплокровного животного, который заключается во введении указанных двух компонентов, фармацевтическая композиция, включающая указанные два компонента и предназначенная для одновременного, раздельного или последовательного применения, применение комбинации для замедления развития или лечения пролиферативного заболевания или для получения фармацевтического препарата указанного назначения, или коммерческий продукт, включающий указанную комбинацию компонентов (а) и (б), упомянутые или определенные выше, обозначены в данном контексте термином «комбинация по настоящему изобретению» (таким образом указанный термин означает каждый из указанных вариантов осуществления настоящего изобретения, которые таким образом можно при необходимости использовать вместо указанного термина).
Одновременное введение можно осуществлять, например, в форме одной фиксированной комбинации с двумя или более активными ингредиентами, или при одновременном введении двух или более активных ингредиентов, полученных независимым образом. Последовательное применение (введение) предпочтительно означает введение одного или более компонентов комбинации в одно и то же время, других компонентов - в другое время, т.е. поочередно, при этом предпочтительно комбинация проявляет большую эффективность по сравнению с независимым введением отдельных соединений (прежде всего наблюдается синергизм). Раздельное применение (введение) предпочтительно означает введение компонентов комбинации независимо друг от друга в различное время, что предпочтительно означает введение компонентов (а) и (б) таким образом, чтобы не наблюдалось перекрывание измеряемых уровней обоих компонентов в крови (в одно и то же время).
Можно использовать также комбинации двух или более последовательных, раздельных или одновременных введений, предпочтительно таким образом, чтобы комбинация компонент/лекарственные средства оказывала суммарный терапевтический эффект, превышающий эффект, который наблюдается при введении комбинации компонент/лекарственные средства независимо через такие значительные периоды времени, что не выявляется взаимное действие на их терапевтическую эффективность, наиболее предпочтительно, чтобы указанная комбинация проявляла синергетический эффект.
Термин «замедление развития», использованный в данном контексте, означает введение комбинации пациентам, у которых установлена предварительная стадия или начальная фаза, первое проявление или ремиссия заболевания, подлежащего лечению, при этом пациентам, например, поставлен диагноз предварительной стадии соответствующего заболевания или у пациентов, например, развивается состояние в процессе курса медикаментозного лечения или у них развивается состояние в результате несчастного случая, т.е. развивается соответствующее заболевание.
Термин «совместный терапевтический эффект» означает, что соединения, которые можно вводить раздельно (поочередно, прежде всего, в специфической последовательности) теплокровному животному, прежде всего человеку, нуждающемуся в таком лечении, через предпочтительные периоды времени, в которые наблюдается (предпочтительно синергетическое) взаимодействие (совместный терапевтический эффект). Такие случаи можно также определить по соответствующим уровням в крови, свидетельствующим о том, что оба компонента присутствуют в крови человека, нуждающегося в таком лечении, по крайней мере в течение определенных периодов времени.
Термин «фармацевтически эффективный» предпочтительно означает количество, которое проявляет терапевтическое или в более широком смысле профилактическое действие на развитие пролиферативного заболевания.
Термин «коммерческая упаковка» или «продукт», использованный в данном контексте, означает прежде всего «набор компонентов» в том смысле, что компоненты (а) и (б) можно вводить независимо друг от друга или при использовании различных фиксированных комбинаций с определенными количествами компонентов (а) и (б), т.е. одновременно или в различные моменты времени. Более того, указанные термины включают также коммерческую упаковку, включающую в качестве активных ингредиентов компоненты (а) и (б) вместе с инструкциями по их одновременному, последовательному (поочередно, предпочтительно в специфической последовательности) или (менее предпочтительно) раздельному применению для замедления развития или лечения пролиферативного заболевания. Компоненты набора можно вводить, например, одновременно или поочередно в различные моменты времени через равные или различные периоды времени для любого компонента набора. Наиболее предпочтительным является выбор таких периодов времени, чтобы эффект при комбинированном лечении заболевания с использованием компонентов превышал эффект при использовании только одного из компонентов комбинации (а) и (б) (эффект определяют по стандартным методикам). Соотношение количества компонента комбинации (а) и количества компонента комбинации (б), предназначенных для введения в форме комбинированного состава, можно изменять, например, в соответствии с требованиями для лечения популяции пациентов или отдельного пациента с учетом конкретного заболевания, возраста, пола, массы тела и т.п. Предпочтительным является наличие по крайней мере одного благоприятного эффекта, например, взаимное увеличение действия компонентов комбинации (а) и (б), прежде всего превышающего суммарный эффект, и, следовательно, который достигается при использовании меньших доз каждого из компонентов комбинации, т.е. доз, ниже переносимых доз при лечении лекарственными средствами в отдельности, а также обеспечивающего другие благоприятные эффекты, например, снижение побочных эффектов или совместный терапевтический эффект при использовании неэффективных доз одного или обоих компонентов комбинации (а) и (б). Наиболее предпочтительным является наличие значительного синергетического действия компонентов комбинации (а) и (б).
Как в случае применения комбинации компонентов (а) и (б), так и в случае применения коммерческой упаковки, можно использовать любые комбинации одновременного, последовательного или раздельного применения, т.е. компоненты (а) и (б) можно вводить в один момент времени одновременно с последующим введением только одного компонента с меньшей токсичностью для организма пациента, либо попеременно, например, более чем через 3-4 недели ежедневного введения, и затем другого компонента, либо введением комбинации обоих компонентов еще позднее (при соответствующем курсе лечения комбинацией лекарственных средств для обеспечения оптимального противоопухолевого лечения) и т.п.
Комбинацию по настоящему изобретению можно использовать также в комбинации с другими курсами лечения, например, хирургическим вмешательством, гипертермией и/или лучевой терапией.
Фармацевтические композиции по настоящему изобретению получают стандартными способами. Такими композициями являются композиции, пригодные для введения энтеральным способом, таким как пероральный или ректальный способы, и парентеральным способом млекопитающим, включая человека, и такие композиции включают терапевтически эффективное количество ингибитора VEGF и по крайней мере один фармацевтически активный агент в отдельности или в комбинации с одним или более фармацевтически приемлемыми носителями, прежде всего пригодными для энтерального или парентерального применения.
Фармацевтические композиции включают приблизительно от 0,00002 до приблизительно 100%, прежде всего, например, в случае растворов для вливания, готовых к применению, от 0,0001 до 0,02%, или например, в случае концентратов для инъекций или вливания или прежде всего парентеральных составов, приблизительно от 0,1% до приблизительно 95%, предпочтительно приблизительно от 1% до приблизительно 90%, более предпочтительно приблизительно от 20% до приблизительно 60% активного ингредиента (в каждом случае указаны мас.%). Фармацевтические композиции по настоящему изобретению можно использовать в виде стандартных лекарственных форм, таких как ампулы, флаконы, драже, таблетки, пакеты для вливания или капсулы.
Эффективная доза каждого компонента в составе комбинации по настоящему изобретению зависит от конкретного соединения или фармацевтических композиций, способа введения, состояния, предназначенного для лечения, и его степени тяжести. Лечащий врач или ветеринар может определить эффективное количество каждого активного ингредиента для профилактики, лечения или замедления развития состояния.
Термин «комбинированный препарат», использованный в данном контексте, означает прежде всего «набор компонентов» в том смысле, что компоненты комбинации (а) и (б), значение которых определено выше, можно использовать независимо друг от друга или в составе различных фиксированных комбинаций с определенными количествами компонентов комбинаций (а) и (б), т.е. одновременно или через различные периоды времени. Компоненты набора можно вводить, например, одновременно или поочередно, т.е. в различные моменты времени и через равные или различные периоды времени для любого компонента набора. Таким образом, в настоящем изобретении предлагается также коммерческая упаковка, включающая замещенные 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту или ее фармацевтически приемлемые соли в форме, пригодной для перорального введения, и инструкции по введению замещенных 3,5-дифенил-1,2,4-триазолов, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты или ее фармацевтически приемлемых солей, в ходе курса лечения пациента химиотерапией для лечения солидной опухоли.
В настоящем изобретении предлагается также применение комбинации по настоящему изобретению для лечения пролиферативного заболевания и для получения лекарственного препарата, предназначенного для лечения пролиферативного заболевания.
Комбинированная терапия по настоящему изобретению является прежде всего пригодной для лечения жидких опухолей. Термин «жидкая опухоль» означает, например, острый лимфоцитарный лейкоз (ALL), острый миелогенный лейкоз (AML), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), лимфому, множественную миелому и миелодисплазический синдром.
Комбинированная терапия по настоящему изобретению является прежде всего пригодной для лечения солидных опухолей. Термин «солидная опухоль» означает прежде всего рак печени, например, гепатоцеллюлярную карциному, рак почки, рак молочной железы, рак яичника, рак ободочной кишки, например, прогрессирующий колоректальный рак, и прежде всего, желудочного-кишечного тракта, например, рак желудка, рак шейки матки, рак легких, прежде всего мелкоклеточный и немелкоклеточный рак легких, рак головы и шеи, рак мочевого пузыря, рак предстательной железы, саркому Капоши, карциноидные опухоли и карциноидный синдром. Комбинации по настоящему изобретению подавляют рост солидных опухолей, а также являются пригодными для предотвращения роста метастаз указанных опухолей.
Термин «карциноидная опухоль», использованный в данном контексте, означает нейроэндокринную опухоль, возникающую в энтерохромаффинных клетках, которые в основном расположены в кишечнике и бронхах. Пептиды, которые синтезируются в карциноидных опухолях, включают 5-гидрокситриптамин и 5-гидрокситриптофан.
Термин «карциноидный синдром», использованный в данном контексте, означает заболевание, прежде всего проявление прогрессирующего заболевания, симптомы которого включают покраснение кожных покровов, диарею и пальпируемую абдоминальную массу или гепатомегалию. При указанном заболевании концентрация 5-гидроксииндолуксусной кислоты (5-HIAA) в моче обычно напрямую соответствует объему опухоли и коррелирует с вероятностью выживания пациента. Уровень 5-HIAA более 8 мг/24 ч является чувствительным индикатором карциноидного синдрома в 75% случаев. Другим индикатором указанного синдрома является повышенный уровень серотонина в плазме, прежде всего уровень серотонина в плазме более приблизительно 250, прежде всего 350 нг/мл.
Термин «рост метастаз», использованный в данном контексте, означает распространение метастаз опухоли и рост и развитие микрометастаз в других органах раковых пациентов.
Следует понимать, что термин «компоненты комбинации (а) и (б)» означает также фармацевтически приемлемые соли указанных соединений.
Комбинацией по настоящему изобретению в данном контексте называется комбинация, включающая (а) по крайней мере один противоопухолевый агент, известный в химиотерапии, и (б) замещенный 3,5-дифенил-1,2,4-триазол, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, активные ингредиенты в составе которой присутствуют в каждом случае в свободной форме или в форме фармацевтической приемлемой соли, и необязательно по крайней мере один фармацевтически приемлемый носитель.
Природа пролиферативных заболеваний зависит от многих факторов. При определенных обстоятельствах можно использовать лекарственные средства с различными механизмами действия. Однако простое комбинированное любых лекарственных средств с различными механизмами действия не всегда приводит к получению комбинаций с благоприятным действием.
Неожиданно при экспериментах in vivo было установлено, что введение комбинации по настоящему изобретению приводит не только к благоприятному эффекту, прежде всего к синергическому терапевтическому эффекту, например, в отношении замедления, приостановки или ремиссии новообразования или к увеличению продолжительности ответной реакции опухоли на лечение, но и к другим неожиданным благоприятным эффектам, например, к снижению побочных эффектов, улучшению качества жизни и снижению смертности и заболеваемости, по сравнению с монотерапией с использованием только одного фармацевтически активного ингредиента из состава комбинации по настоящему изобретению.
Эффективная доза каждого из компонентов комбинации в составе комбинации по настоящему изобретению зависит от конкретного соединения или фармацевтической композиции, способа введения, состояния, предназначенного для лечения, и степени его тяжести. Таким образом, дозы комбинации по настоящему изобретению выбирают в соответствии с рядом факторов, включающих способ введения и почечную и печеночную функции пациента. Врач или ветеринар может определить эффективное количество отдельных активных ингредиентов, требуемое для предотвращения, подавления или приостановки развития состояния. Определение оптимальной концентрации активных ингредиентов в интервале, обеспечивающем эффективность без токсичности, необходимо проводить с учетом кинетики доставки активных ингредиентов в требуемые участки организма.
Доза активного ингредиента зависит от различных факторов, таких как активность и продолжительность действия активного ингредиента, тяжесть заболевания, предназначенного для лечения, или его симптомов, способ введения, вид теплокровного животного, пол, возраст, масса и/или индивидуальное состояние теплокровного животного. Ежедневные дозы при введении пероральным способом составляют от 10 до приблизительно 120 мг/кг, прежде всего от 20 до приблизительно 80 мг/кг и для теплокровных животных с массой тела приблизительно 40 кг предпочтительно приблизительно от 400 мг до приблизительно 4800 мг, прежде всего приблизительно от 800 мг до 3200 мг, которую соответственно разделяют на 2-12 отдельных доз. Однако в настоящем изобретении предлагаются также другие курсы лечения, которые также являются эффективными.
В составе комбинации по настоящему изобретению замещенные 3,5-дифенил-1,2,4-триазоды, например 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту или ее фармацевтически приемлемые соли, можно вводить непрерывно, например ежедневно, в процессе или после химиотерапии. Суточная доза при введении пероральным способом составляет от 500 мг до 4000 мг, например, в интервале от 500 мг/сут до 2000 мг/сут, предпочтительно 1000, 1500 или 2000 мг/сут. Однако в настоящем изобретении предлагаются также другие курсы лечения. При введении замещенного 3,5-дифенил-1,2,4-триазола в форме соли указанные выше суточные дозы пересчитывают на эквивалентное количество вводимого свободного основания.
Если не указано иное, для обеспечения благоприятного эффекта, описанного в данном контексте при использовании компонентов комбинации по настоящему изобретению в форме отдельных коммерческих лекарственных средств, следует использовать дозы и способ введения, указанные на инструкциях, вложенных в упаковки.
Карбоплатин вводят человеку внутривенным способом в дозе приблизительно от 100 до 400, например, 200 мг/м2 поверхности тела приблизительно через каждые 4-6 недель.
Оксалиплатин вводят человеку внутривенным способом в дозе приблизительно от 25 до 135, например от 45 или 85 мг/м2 поверхности тела приблизительно через каждые 2-3 недели.
Цисплатин вводят человеку в дозе приблизительно от 25 до 100 мг/м2 приблизительно через каждые 3 недели.
Топотекан вводят человеку в дозе приблизительно от 1 до 5 мг/м2/сут.
Иринотекан вводят человеку в дозе приблизительно от 50 до 350 мг/м2/сут.
Фадрозол вводят человеку пероральным способом в дозе приблизительно от 0,5 до приблизительно 10 мг/сут, предпочтительно приблизительно от 1 до приблизительно 2,5 мг/сут.
Экземестан вводят человеку пероральным способом в дозе приблизительно от 5 до приблизительно 200 мг/сут, предпочтительно приблизительно от 10 до приблизительно 25 мг/сут, или парентеральным способом в дозе приблизительно от 50 до приблизительно 500 мг/сут, предпочтительно приблизительно от 100 до приблизительно 250 мг/сут. При необходимости введения лекарственного средства в форме отдельной фармацевтической композиции его следует вводить, как описано в патенте GB 2177700.
Форместан вводят человеку парентеральным способом в дозе приблизительно от 100 до приблизительно 500 мг/сут, предпочтительно приблизительно от 250 до приблизительно 300 мг/сут.
Анастрозол вводят человеку пероральным способом в дозе приблизительно от 0,25 до приблизительно 20 мг/сут, предпочтительно приблизительно от 0,5 до приблизительно 2,5 мг/сут.
Аминоглутемид вводят человеку в дозе приблизительно от 200 до 500 мг/сут.
Цитрат тамоксифена вводят человеку в дозе приблизительно от 10 до 400 мг/сут.
Винбластин вводят человеку в дозе приблизительно от 1,5 до 10 мг/м2/сут.
Винкристин вводят человеку парентеральным способом в дозе приблизительно от 0,025 до приблизительно 0,05 мг/кг массы тела в неделю.
Винорелбин вводят человеку в дозе приблизительно от 10 до 50 мг/м2/сут. Фосфат этопозида вводят человеку в дозе приблизительно от 25 до 115 мг/м2/сут, например 56,8 или 113, 6 мг/м2/сут.
Тенипозид вводят человеку в дозе приблизительно от 75 до 150 мг/сут приблизительно через каждые 2 недели.
Доксорубицин вводят человеку в дозе приблизительно от 10 до 100 мг/м2/сут, например 25 или 75 мг/м2/сут.
Эпирубицин вводят человеку в дозе приблизительно от 10 до 200 мг/м2/сут. Идарубицин вводят человеку в дозе приблизительно от 0,5 до 50 мг/м2/сут, например 8 мг/м2/сут в течение 3 сут.
Митоксантрон вводят человеку в дозе приблизительно от 2,5 до 25 мг/м2/сут. Паклитаксел вводят человеку в дозе приблизительно от 50 до 300 мг/м2/сут.
Алендроновую кислоту вводят человеку в дозе приблизительно от 5 до 10 мг/сут.
Клодроновую кислоту вводят человеку, например, в дозе приблизительно от 750 до 1500 мг/сут.
Этридоновую кислоту вводят человеку в дозе приблизительно от 200 до 400 мг/сут.
Ибандроновую кислоту вводят человеку в дозе приблизительно от 1 до 4 мг через каждые 3-4 недели.
Ризедроновую кислоту вводят человеку в дозе приблизительно от 20 до 30 мг/сут.
Памидроновую кислоту вводят человеку в дозе приблизительно от 15 до 90 мг через каждые 3-4 недели.
Тилудроновую кислоту вводят человеку в дозе приблизительно от 200 до 400 мг/сут.
Бикалутамид вводят человеку в дозе приблизительно от 25 до 50 мг/м2/сут.
Продукт ADRIAMYCIN вводят в дозе в интервале 100-1500 мг ежедневно, например 200-1000 мг/сут, например 200, 400, 500, 600, 800, 900 или 1000 мг/сут в виде одной или двух доз ежедневно.
Продукт 5-FU вводят в соответствующей дозе в интервале 100-1500 мг ежедневно, например 200-1000 мг/сут, например 200, 400, 500, 600, 800, 900 или 1000 мг/сут в виде одной или двух доз ежедневно.
Продукт CAMPTOTHECIN вводят в соответствующей дозе в интервале 100-1500 мг ежедневно, например 200-1000 мг/сут, например 200, 400, 500, 600, 800, 900 или 1000 мг/сут в виде одной или двух доз ежедневно.
Продукт 5-AZACYTIDINE вводят в соответствующей дозе в интервале 100-1500 мг ежедневно, например 200-1000 мг/сут, например 200, 400, 500, 600, 800, 900 или 1000 мг/сут в виде одной или двух доз ежедневно.
Продукт TOMUDEX (ралтитрексед, фирмы AstraZeneca Pharmaceuticals, Wilmington DE, США) вводят согласно инструкциям фирмы-изготовителя.
Продукт REVLIMID, известный под названиями леналидомид и СС-5013, выпускается фирмой Celgene и является производным талидомида, который выпускается с 2004 г. Изначально он был предназначен для лечения множественной миеломы, на которую талидомид оказывал значительное терапевтическое действие, но было установлено также, что он проявляет эффективность в отношении гематологических нарушений, таких как миелодиспластические синдромы.
Тирфостины, прежде всего адафостин, предпочтительно вводят теплокровному животному, прежде всего человеку, в дозе в интервале предпочтительно приблизительно от 1 до 6000 мг/сут, более предпочтительно от 25 до 5000 мг/сут, наиболее предпочтительно от 50 до 4000 мг/сут. Если не указано иное, то соединение предпочтительно вводят от 1 до 5, прежде всего от 1 до 4 раз в сут.
Фармацевтические составы, предназначенные для комбинированной терапии при введении энтеральным или парентеральным способом, включают, например, лекарственные формы, такие как таблетки с сахарным покрытием, капсулы или суппозитории и ампулы. Если не указано иное, то такие составы получают стандартными способами, например, с использованием стандартных способов перемешивания, грануляции, нанесения сахарного покрытия, растворения или лиофилизации. Предпочтительно каждая лекарственная форма должна содержать количество каждого компонента комбинации менее эффективного количества, т.к. требуемое эффективное количество обеспечивается при введении нескольких лекарственных форм. Специалист в данной области техники может определить соответствующие фармацевтически эффективные количества компонентов комбинации.
Предпочтительным является введение соединений или их фармацевтически приемлемых солей в форме перорального фармацевтического состава в виде таблетки, капсулы или сиропа, или при необходимости в виде парентеральных инъекций.
При получении композиций для введения пероральным способом используют любые фармацевтически приемлемые среды, такие как вода, гликоли, масла, спирты, ароматизаторы, консерванты, красители. Фармацевтически приемлемые носители включают крахмалы, сахара, микрокристаллическую целлюлозу, разбавители, гранулирующие агенты, замасливатели, связующие агенты, дезинтегрирующие агенты.
Растворы и суспензии активного ингредиента и прежде всего изотонические водные растворы или суспензии являются пригодными для введения активного ингредиента парентеральным способом. Например, в случае лиофилизированных композиций, включающих активный ингредиент в отдельности или в комбинации с фармацевтически приемлемым носителем, например маннитом, можно получать указанные растворы или суспензии непосредственно перед применением. Фармацевтические композиции можно стерилизовать или включать в их состав эксципиенты, например консерванты, стабилизаторы, смачивающие и/или эмульгирующие агенты, солюбилизаторы, соли для регуляции осмотического давления и/или буферные вещества, при этом их получают по стандартным методикам, например стандартными способами растворения или лиофилизации. Растворы или суспензии могут включать загустители, такие как натриевая соль карбоксиметилцеллюлозы, карбоксиметилцеллюлоза, декстран, поливинилпирролидон или желатин. Масляные суспензии включают в качестве масла растительные, синтетические или полусинтетические масла, используемые для инъекций.
Изотонический агент выбирают из любых стандартных изотонических агентов, например маннита, декстрозы, глюкозы и хлорида натрия. Составы для вливаний разбавляют водой. Количество воды, использованной в качестве разбавителя, выбирают в соответствии с требуемой концентрацией активного ингредиента в растворе для вливаний. Растворы для вливаний могут содержать другие стандартные эксципиенты, используемые в составах, предназначенных для введения внутривенным способом, такие как антиоксиданты.
В настоящем изобретении предлагается также «комбинированный препарат», использованный в данном контексте, который означает прежде всего «набор компонентов» в том смысле, что компоненты комбинации (а) и (б), как описано выше, вводят независимо друг от друга или в различных фиксированных комбинациях, содержащих определенные количества компонентов комбинации (а) и (б), т.е. одновременно или в различные моменты времени. Компоненты набора можно вводить, например, одновременно или поочередно, т.е. в различные моменты времени через равные или различные периоды для любых компонентов набора. Соотношение общих количеств компонентов комбинации (а) и (б), предназначенных для введения в составе комбинированного препарата, можно изменять, например, в зависимости от субпопуляции пациентов, нуждающихся в лечении, или от конкретного пациента с учетом степени тяжести любых побочных эффектов, наблюдаемых у пациентов.
В настоящем изобретении предлагается прежде всего комбинированный препарат, включающий:
(а) одну или более стандартных лекарственных форм, содержащих комплексен железа, и
(б) одну или более стандартных лекарственных форм, содержащих фармацевтически активный агент.
Целью настоящего изобретения является разработка фармацевтической композиции, включающей количество комбинации по настоящему изобретению, которое проявляет совместный терапевтический эффект в отношении пролиферативного заболевания. В указанной композиции компоненты (а) и (б) можно вводить одновременно, один за другим или в составе одной комбинированной стандартной лекарственной формы или в двух различных стандартных лекарственных формах. Лекарственной формой может являться также фиксированная комбинация.
Фармацевтические композиции, предназначенные для раздельного введения компонентов (а) и (б) и для введения в составе фиксированной комбинации, т.е. отдельной галеновой композиции, включающей по крайней мере 2 компонента (а) и (б), по настоящему изобретению, получают по стандартным методикам, являются пригодными для введения энтеральным способом, таким как пероральный или ректальный способ, и парентеральным способом млекопитающим (теплокровным животным), включая человека, и указанные композиции включают терапевтически эффективное количество по крайней мере одного фармацевтически активного компонента комбинации в отдельности или в комбинации с одним или более фармацевтически приемлемым носителем, прежде всего пригодным для введения энтеральным или парентеральным способом.
Новая фармацевтическая композиция содержит, например, приблизительно от 10% до приблизительно 100%, предпочтительно приблизительно от 20% до приблизительно 60% активных ингредиентов. Фармацевтическими препаратами, предназначенными для комбинированной терапии и введения энтеральным или парентеральным способом, являются, например, составы в виде стандартных лекарственных форм, таких как таблетки с сахарным покрытием, таблетки, капсулы или суппозитории и ампулы. Если не указано иное, то такие составы получают по стандартным методикам, например, с использованием стандартных способов смешивания, грануляции, нанесения сахарного покрытия, растворения или лиофилизации. Предпочтительно каждая лекарственная форма должна содержать неэффективное количество каждого компонента комбинации, т.к. требуемое эффективное количество обеспечивается при введении нескольких лекарственных форм.
Фармацевтические композиции, включающие замещенные 3,5-дифенил-1,2,4-триазолы или их фармацевтически приемлемые соли, описаны в заявке WO 97/49395, опубликованной 31 декабря 1997 г. и в патенте US №6465504. Диспергируемые таблетки, включающие 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, описаны в заявках WO 200/035026, опубликованной 29 апреля 2004 г., и WO 2005/097062, опубликованной 20 октября 2005.
В другом объекте настоящего изобретения предлагается применение улучшенных способов введения замещенных 3,5-дифенил-1,2,4-триазолов, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты, или их фармацевтически приемлемых солей, для лечения пациентов, страдающих от солидных опухолей, включающих, например, рак печени, прежде всего, гепатоцеллюлярную карциному.
Согласно одному способу введения замещенные 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, или их фармацевтически приемлемые соли, вводят 2 раза или более в сут, например, 2 или 3 раза в сут, в уменьшенных количествах по сравнению со стандартным способом введения 1 раз в сут. В другом варианте настоящего изобретения предлагается курс лечения, при котором замещенные 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, вводят 1 раз в сут в количестве от 50 мг/сут до 4200 мг/сут, прежде всего в количестве от 1200 мг/сут до 1300 мг/сут, прежде всего 1250 мг/сут.
Согласно одному объекту настоящего изобретения замещенные 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, вводят 1 раз в сут в отдельности или в процессе или после других курсов лечения, например химиотерапии. Фармацевтически эффективным количеством при пероральном введении 1 раз в сут является введение от 300 до 4000 мг, например, от 300 мг/сут до 2000 мг/сут или от 300 мг/сут до 1000 мг/сут, прежде всего 300, 500, 750, 1000, 1500 или 2000 мг/сут.
При введении замещенных 3,5-дифенил-1,2,4-триазолов, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты, в форме фармацевтически приемлемых солей их вводят в количестве, эквивалентом количеству свободного основания (т.е. 1 экв. свободной формы, как описано выше). В данном контексте ссылка на 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, означает также их фармацевтически приемлемые соли.
Различные объекты настоящего изобретения можно комбинировать друг с другом любым способом. Например, пациента, страдающего от рака почек или опухоли другого вида, можно лечить введением замещенных 3,5-дифенил-1,2,4-триазолов, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты, 1 раз в сут или 2 раза в сут. Улучшенный способ введения замещенных 3,5-дифенил-1,2,4-триазолов, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты, используют при лечении в режиме монотерапии или комбинированной терапии, иными словами, замещенные 3,5-дифенил-1,2,4-триазолы, например, 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту, вводят в отдельности или в комбинации с другими терапевтическими агентами. При комбинированной терапии их вводят 1 или 2 раза в сут, как описано в данном контексте, а любой другой терапевтический агент или агенты вводят согласно их стандартным способам введения.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение платины, которое выбирают из группы, включающей карбоплатин, цисплатин, оксалиплатин, сатраплатин и продукт ZD0473.
В другом варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение платины, которое выбирают из группы, включающей карбоплатин, цисплатин и оксалиплатин.
В еще одном варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) цисплатин.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибиторы топоизомеразы I, которые выбирают из группы, включающей топотекан, иринотекан, камптотецин, например 9-нитрокамптотецин, и макромолекулярный конъюгат камтотецина PNU-166148.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор ароматазы, который выбирают из группы, включающей атаместан, экземестан, форместан, аминоглутетимид, роглетимид, пиридоглутетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) антиэстроген, который выбирают из группы, включающей тамоксифен, фулвестрант, ралоксифен и гидрохлорид ралоксифена.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор топоизомеразы II, который выбирают из группы, включающей доксорубицин, включая липосомальные составы, например продукт CAELYX™, даунорубицин, включая липосомальные составы, например продукт DAUNOSOME™, эпирубицин, идарубицин, митомицин С, пирарубицин, неморубицин, митоксантрон, лозоксантрон, этопозид и тенипозид.
В одном варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) митомицин С.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) активный агент микротрубочек, который выбирают из группы, включающей паклитаксел и доцетаксел, винбластин, сульфат винбластина, винкристин, сульфат винкристина, винорелбин, дискодермолид, колхицин и эпотилон А, эпотилон В или их производные.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) антиангиогенное соединение, которое выбирают из группы, включающей талидомид, леналидомид, продукты TNP-470 и SU5416.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) антиангиогенное соединение, которое выбирают из группы, включающей талидомид, продукты TNP-470 и SU5416.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) агонист гонадорелина, который выбирают из группы, включающей абареликс, госерелин и ацетат госерелина.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) бикалутамид.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) бифосфонат, который выбирают из группы, включающей этридоновую кислоту, клодроновую кислоту, тилудроновую кислоту, памидроновую кислоту, алендроновую кислоту, ибандроновую кислоту, ризедроновую кислоту и золедроновую кислоту.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) алкилирующий агент, который выбирают из группы, включающей циклофосфамид, ифосфамид, мелфалан, нитрозомочевину (продукты BCNU или Gliadel) и темозоламид (продукт TEMODAR).
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) противоопухолевый антиметаболит, который выбирают из группы, включающей 5-фторурацил (5-FU), капецитабин, гемцитабин, 5-азацитидин, децитабин, метотрексат, эдатрексат, пеметрексед, лейковорин и ралтитрексед (продукт TOMUDEX), прежде всего из группы, включающей 5-FU, лейковорин и ралтитрексед.
В одном варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) 5-фторурацил (5-FU).
В другом варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) лейковорин.
В одном варианте настоящего изобретения предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ралтитрексед (продукт TOMUDEX).
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей фосфатазу 1, фосфатазу 2А, продукты PTEN и CDC25, например окадаевую кислоту или ее производные.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей талидомид, например, продукт THALOMID™, леналидомид, например продукты Revlimid®, TNP-470 и SU5416.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей талидомид, например продукты THALOMID™, TNP-470 и SU5416.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) антипролиферативные антитела, которые выбирают из группы, включающей трастузумаб (продукт HERCEPTIN), трастузумаб-DM1, эрлотиниб (продукт TARCEVA), бевацизумаб (продукт AVASTIN), ритуксимаб (продукт RITUXAN), продукт PRO64553 (анти-CD40) и антитела 2С4.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор гистондеацетилазы (HDAC), который выбирают из группы, включающей N-гидрокси-3-[4-[[(2-гидроксиэтил)[2-(1Н-индол-3-ил)этил]амино]метил]фенил]-2Е-2-пропенамид, N-гидрокси-3-[4-[[[2-(2-метил-1Н-индол-3-ил)этил]амино]метил]фенил]-2Е-2-пропенамид, субероиланилидгидроксамовую кислоту (SAHA), продукты MS-275, FK228 (ранее FR901228), пиридин-3-илметиловый эфир [4-(2-аминофенилкарбамоил)бензил]карбаминовой кислоты, бутановую кислоту, пироксамид, трихостатин А, оксамфлатин, апицидин, депсипептид, депудецин, трапоксин, N-гидрокси-3-[4-({(2-гидроксиэтил)[2-(1H-индол-3-ил)этил]амино}метилфенил]акриламид или фармацевтически приемлемые соли указанных соединений.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей ретиноевую кислоту, токоферол или токотриенол.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) продукт PI-88.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) FTY720.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое связывается с серин/треонинкиназой mTOR, снижает или ингибирует ее активность/функцию, и которое выбирают из группы, включающей продукты RAD, RAD001, CCI-779, АВТ578, SAR543, рапамицин, производные/аналоги рапамицина, продукты АР23573, АР23841, эверолимус (продукт CERTICAN), сиролимус (продукт RAPAMUNE), продукты CCI-779 и АВТ578.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор HSP90, который выбирают из группы, включающей 17-аллиламино,17-деметоксигелданамицин (17AAG), производные гелданамицина, соединения, родственные гелданамицину, и радицикол.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) противолейкозное соединение, которое выбирают из группы, включающей продукт Ara-С, 6-меркаптопурин (6-МР) и фосфат флударабина.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор циклооксигеназы, который выбирают из группы, включающей целекоксиб (продукт CELEBREX), рофекоксиб (продукт VIOXX), эторикоксиб, валдекоксиб, 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусную кислоту и лумиракоксиб.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей продукты L-744832, DK8G557 и R115777 (ZARNESTRA).
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор протеасомы, который выбирают из группы, включающей продукты PS-341, MLN 341, бортезомиб или продукт Velcade.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) продукт DIOVAN.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) теломестатин.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор АКФ, который выбирают из группы, включающей продукт CIBACEN, беназеприл, эназеприл (продукт LOTENSIN), каптоприл, эналаприл, фозиноприл, лизиноприл, моэксиприл, хинаприл, рамиприл, периндоприл и трандолаприл.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) ингибитор ММР, который выбирают из группы, включающей батимастат, маримастат (продукт ВВ-2516), приномастат (продукт AG3340), метастат (продукт NSC 683551), продукты BMS-279251, BAY 12-9566, TAA211, MMI270B и AAJ996.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) бенгамид и его производные.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) антагонист рецептора соматостатина, который выбирают из группы, включающей пазиреотид, ланреотид, октреотид и вапреотид.
В настоящем изобретении предлагается комбинация или комбинированный препарат, включающий (а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и (б) соединение, которое выбирают из группы, включающей (4-трет-бутилфенил)(4-пиридин-4-илметилизохинолин-1-ил)амин, продукты SU101, SU6668, GFB-111, PD 180970, AG957, NSC 680410, PD 173955, BMS3 54825, UCN-01, сафингол, продукт BAY 43-9006, бриостатин 1, перифозин, илмофозин, продукты RO 318220, RO 320432, GO 6976, Isis 3521, LY333531/LY379196, PD184352, QAN697, 4-метил-3-[[4-(3-пиридинил)-2-пиримидинил]амино]-N-[5-(4-метил-1H-имидазол-1-ил)-3-(трифторметил)фенил]бензамид, тирфостин A23/RG-50810, AG 99, тирфостин AG 213, тирфостин AG 1748, тирфостин AG 490, тирфостин В44, (+) энантиомер тирфостина В44, тирфостин AG 555, AG 494, тирфостин AG 556, AG957, адафостин, адамантиловый эфир (4-{[(2,5-дигидроксифенил)метил]амино}бензойной кислоты, NSC 680410, адафостин, продукты СР 358774, ZD 1839, ZM 105180, например трастузумаб (продукт HERCEPTIN®), цетуксимаб, продукты Iressa, OSI-774, CI-1033, EKB-569, GW-2016, E1.1, E2.4, E2.5, E6.2, E6.4, E2.11, E6.3 или Е7.6.3, эрлотиниб и гефитиниб.
В настоящем изобретении предлагается фармацевтическая композиция, включающая количество комбинации, как описано выше, которое проявляет совместную эффективность в отношении пролиферативного заболевания.
В настоящем изобретении предлагается применение комбинации, как описано выше, для получения лекарственного средства, предназначенного для лечения пролиферативного заболевания.
В настоящем изобретении предлагается коммерческая упаковка, включающая комбинацию, как описано выше, и инструкцию по ее применению.
Примеры
Пример 1
Определение синергетической антипролиферативной активности комбинации 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты (в данном контексте соединение I) и противоопухолевых агентов
Для соединения I оценивали синергетическую антипролиферативную активность в составе комбинации с 5-фторурацилом, митомицином С, цисплатином, тумодексом и лейковорином с использованием опухолевых клеток НЕР3В217 и SKHEP1 печени человека in vitro. Определяли синергетическую антипролиферативную активность соединения I и обоих компонентов комбинации с использованием серии стандартных химиотерапевтических агентов. Результаты, полученные для двух различных линий опухолевых клеток, значительно отличались. Для клеток НЕР3В217 при введении в концентрации менее 12,0 мкМ наблюдается синергетическая активность соединения I в комбинации со всеми исследованными химиотерапевтическими агентами. Однако уровень синергизма, рассчитанный по величине G, отличается для различных компонентов комбинации и наиболее высокий синергизм наблюдается для цисплатина. Синергетическая антипролиферативная активность соединения I значительно ниже для клеток SKHEP1, синергизм был установлен только для цисплатина и тумодекса. Однако для обоих соединений синергизм действия комбинации наблюдался при концентрациях менее 1,5 мкМ или более 3 мкМ. Отсутствие синергизма действия этих двух соединений наблюдалось при концентрациях тумодекса более 12,5 мкМ или цисплатина более 25,0 мкМ.
3. Материалы и методы
3.1. Материалы
Для анализа использовали клеточные линии НЕР3В217 и SKHEP1 из коллекции American Type Culture Collection (ATCC), Rockville, MD, США, клеточную культуральную среду RPMI 1640 и эмбриональную телячью сыворотку (ЭТС) фирмы Invitrogen (Mt. Waverley, VIC, Австралия), реагент CellTitreBlue фирмы Promega (Annandale, NSW, Австралия). Использовали материалы клеточных культур стандартного качества, производства различных фирм. Химические реагенты высокой степени чистоты были предоставлены местными поставщиками. Соединение I было предоставлено спонсором, подробное описание его выделения и свойств представлено в файле необработанных данных. 5-Фторурацил (фирмы Genentech, South San Francisco, CA, США), митомицин С, цисплатин, лейковорин (фирмы BristolMyers Squibb, New York, NY, США) и тумодекс (фирмы AstraZeneca Pharmaceuticals, Wilmington, DE, США) разбавляли клеточной культуральной средой.
3.2. Подготовка исследуемых соединений
Соединение I растворяли в ДМСО, при этом получали концентрированный раствор (1 мг/мл). Полученный концентрированный раствор интенсивно перемешивали на мешалке типа вортекс и разбавляли клеточной культуральной средой, при этом получали требуемые исходные концентрации для серийных разведений (1,3 мкМ) при добавлении в лунку (50:50, об./об.). 5-Фторурацил, митомицин С, цисплатин, лейковорин и тумодекс разбавляли клеточной культуральной средой до требуемых исходных концентраций для серийных разведений (см. табл.1).
ная
концентра-
ция, пкМ
ная
концентра-
ция, пкМ
3.3. Способ, порядок введения соединений, курс лечения
Клетки обоих линий культивировали в клеточной культуральной среде RPMI 1640, содержащей 10% ЭТС. Клеточная культуральная среда содержала пенициллин/стрептомицин (50 МЕд/мл, конечная концентрация 50 мкг/мл). Клетки обоих линий высеивали в количестве 800 клеток в лунке в 50 мкл среды в 96-луночные микротитрационные планшеты. Через 24 ч после высеивания в каждую лунку добавляли по 50 мкл клеточной культуральной среды, содержащей исследуемое соединение(я). Исследуемые соединения добавляли в отдельности или в соответствующем соотношении концентраций. Конечная концентрация ДМСО в смеси для инкубации составляла менее 0,05% (об./об.) для максимальной концентрации исследуемого соединения и, соответственно, снижалась для меньших концентраций исследуемых соединений. Пролиферацию клеток оценивали с использованием флуометрического анализа Alamar Blue (CellTiter Blue).
3.4. Сбор данных
Анализ Alamar Blue использовали для определения антипролиферативной активности исследуемых соединений. В качестве контроля роста использовали необработанные клетки. Данные оценивали в двойных повторах с использованием двух одинаковых разведений в 96-луночных микротитрационных планшетах. Каждый планшет анализировали в отдельности и для определения синергетической активности рассчитывали изоболограммы (фиг.2 и 3). Рассчитывали также величину g с использованием следующего уравнения: g=Ас/Ае+Вс/Ве, где А+В и А или В в отдельности означают равноэффективные концентрации (например, IC50), где Ас означает концентрацию компонента А в комбинации с компонентом В, Вс означает концентрацию компонента В в комбинации с компонентом А, Ае означает концентрацию компонента А в отдельности, a Be означает концентрацию компонента В в отдельности. Величина g отражает уровень взаимодействия двух компонентов комбинации. Величина g менее 1 означает синергизм, величина g более 1 означает антагонизм, и величина g, равная 1, означает аддитивные эффекты. Границы между этими категориями не определены и их следует использовать только для качественной оценки. Однако чем ниже величина g, тем выше синергетический эффект.
3.5. Анализ Alamar Blue
Результаты анализа Alamar Bluebased CellTiterBlue свидетельствуют о жизнеспособности клеток, которую оценивают по способности клеток в среде восстанавливать резазурин в резоруфин, при этом интенсивность сигнала флуоресценции прямо пропорционально зависит от числа живых клеток, что является косвенным индикатором пролиферации клеток.
На основании предварительных результатов культуры обоих клеточных линий высеивали в количестве 0,8×103 клеток/лунка в 96-луночные микротитрационные планшеты. Через 24 ч клетки инкубировали в течение 72 ч в присутствии индивидуального соединения или комбинации двух исследуемых соединений. После добавления реагента CellTiterBlue (20 мкл/лунка) и кратковременного перемешивания клетки инкубировали в течение еще 4 ч, затем измеряли флуоресценцию (λвозб/λисп 560/590 нм) с использованием ридера для микропланшетов Spectramax M2 (фирмы Molecular Devices, Surrey Hills, VIC, Австралия).
4. Результаты
Антипролиферативную активность соединения I исследовали в комбинации со стандартными химиотерапевтическими средствами, такими как 5-фторурацил, митомицин С, цисплатин, тумодекс и лейковорин. Соединение I исследовали при 9 концентрациях, начиная с 50 мкМ, и готовили девять 2-кратных серийных разбавлений. Все другие химиотерапевтические агенты исследовали с использованием исходных (максимальных) концентраций при 8 концентрациях, как показано в табл.1, и готовили семь 2-кратных серийных разведении. Для оценки синергетического действия соединения I в комбинации со стандартными химиотерапевтическими агентами, рассчитывали величину g (уравнение приведено в разделе Методы). При g менее 1 взаимодействие является синергетическим. При g, равном 1, эффекты являются аддитивными. При g более 1 взаимодействие лекарственных средств в комбинации является антагонистическим (табл.2 и 3, фиг.2 и 3)). Величины g наносили на изоболограммы (величины, расположенные ниже изоболической линии, означают синергетическое действие комбинации обоих лекарственных средств, величины, расположенные выше изоболической линии, означают антагонистическое действие комбинации обоих лекарственных средств). Однако указанные предельные величины не являются абсолютными и их следует интерпретировать в динамическом отношении. Для оценки оптимальной концентрации компонента комбинации использовали графики Surface Response Plot. Каждое исследование повторяли один раз.
Антипролиферативная эффективность в отношении клеток SKHEP1
Значительный синергизм антипролиферативной активности (g<1) наблюдали только для комбинаций соединения I с цисплатином или тумодексом (табл.2). Следует отметить, что оба компонента комбинации в двух интервалах концентраций для ICL670 проявляли синергизм антипролиферативного действия (в интервале от 25 мкМ до 3,25 мкМ и в интервале от 0,78 мкМ до 0,20 мкМ). Кроме того, незначительный синергизм антипролиферативной активности при концентрациях соединения I менее 3 мкМ наблюдали для комбинации соединения I с митомицином С (табл.2). Оценка графика Surface Response Plot свидетельствовала о том, что концентрация цисплатина или тумодекса в комбинации с соединением I играет незначительную роль в синергетическом действии, в то время как синергетическое действие наблюдается только при более низких концентрациях соединения I (фиг.2, ряды В и Е).
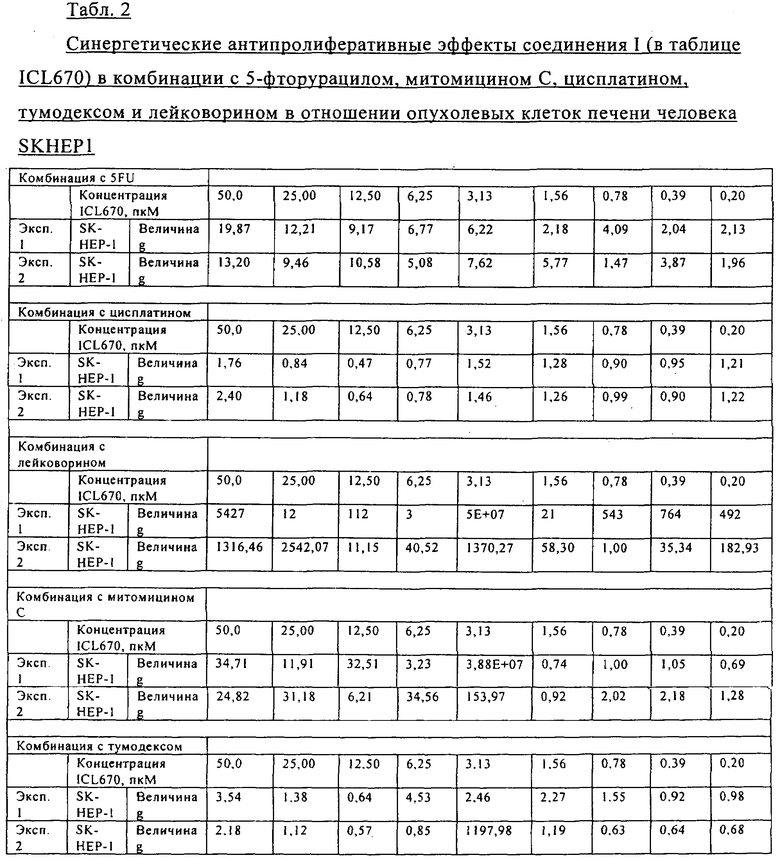
Антипролиферативная эффективность в отношении клеток НЕР3В217
По сравнению с действием на клетки SKHEP1, при введении соединения I в комбинации со всеми исследованными стандартными химиотерапевтическими агентами наблюдалась значительная синергетическая активность. Повторный эксперимент с использованием комбинации с лейковорином и митомицином С по неизвестной причине не подтверждает результаты первого эксперимента (табл.3, строки окрашены в серый цвет). Следовательно, вывод об эффективности комбинации соединения I с указанными двумя лекарственными средствами следует интерпретировать с осторожностью. Максимальный синергизм наблюдали при использовании комбинации соединения I с цисплатином. При концентрациях соединения I менее 12,5 мкМ в комбинации с цисплатином в широком интервале концентраций наблюдали синергетическое действие (табл.3 и фиг.2, график В: изоболограмма и зависимость от величины g). Кроме того, при введении меньших концентраций соединения I в комбинации с более высокими концентрациями цисплатина наблюдали более высокие синергетические эффекты по сравнению с использованием соединения I в комбинации с меньшими концентрациями цисплатина (фиг.3, график В: Surface Response). При введении комбинации соединения I с митомицином С при концентрациях в интервале от 6,25 мкМ до 0,781 мкМ (табл.3 и фиг.2, график D) также наблюдали синергетическое действие. Однако по сравнению с цисплатином концентрация митомицина С оказывает меньшее влияние на уровень синергетического взаимодействия. Так как величины g близки к 1, то при введении комбинации соединения I с 5-фторурацилом наблюдался незначительный синергизм. При введении тумодекса наблюдался значительный синергизм при меньших концентрациях соединения I (менее 1,56 мкМ) в первом эксперименте. К сожалению, полученный результат не подтверждается во втором эксперименте (табл.3).
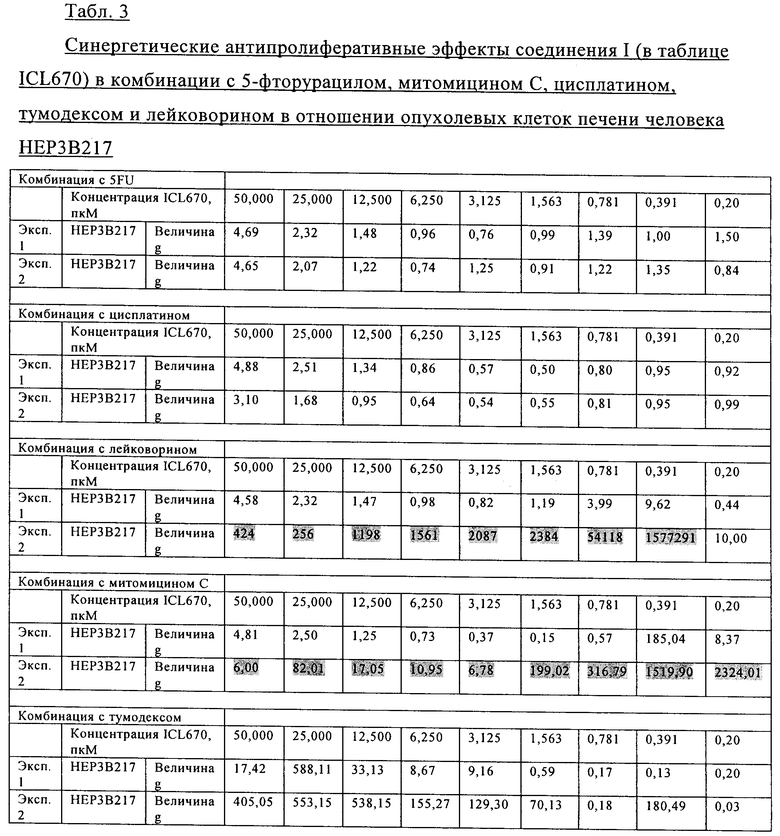
Синергизм антипролиферативной активности для соединения I в комбинации со стандартными лекарственными препаратами 5-фторурацилом, митомицином С, цисплатином, тумодексом и лейковорином оценивали in vitro с использованием опухолевых клеток печени человека SKHEP1 и НЕР3В217 с использованием оптимизированного анализа vivoPharm's в шахматном порядке. Для обоих клеточных линий цисплатин проявлял масимальный уровень синергизма, и меньший уровень наблюдали для тумодекса в клетках SKHEP1 и 5-фторурацила в клетках НЕРЗВ217. Соединение I ингибирует пролиферацию опухолевых клеток печени человека с проявлением синергизма. Наблюдаемый уровень синергизма значительно выше в отношении клеток НЕР3В217 по сравнению с клетками SKHEP1 и являлся максимальным для комбинации с цисплатином.
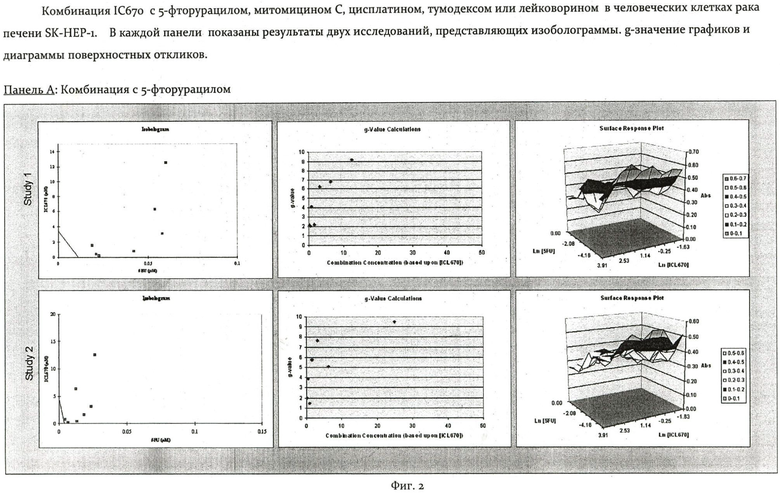
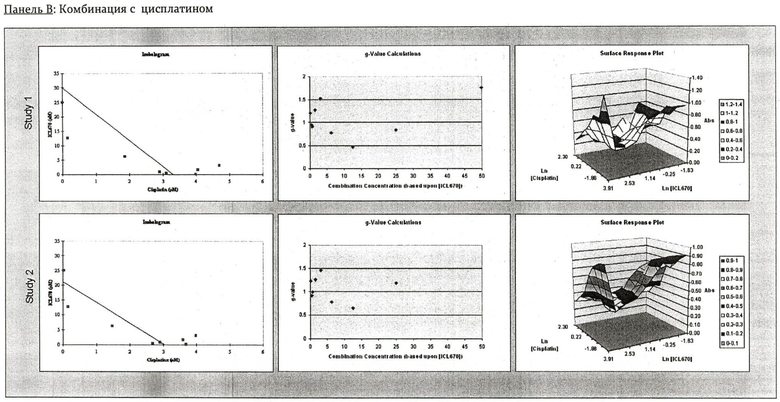
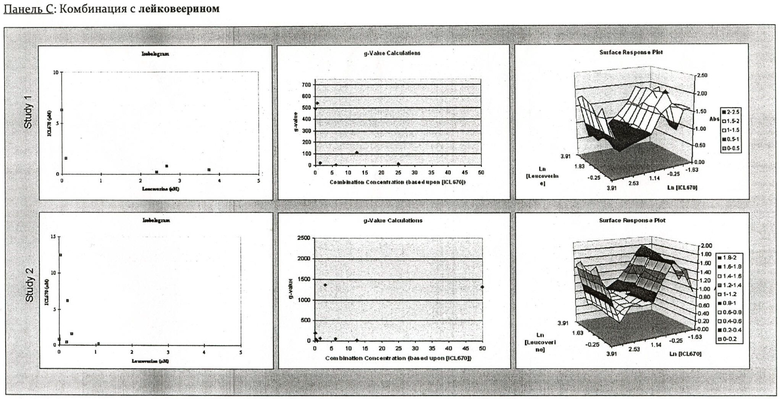
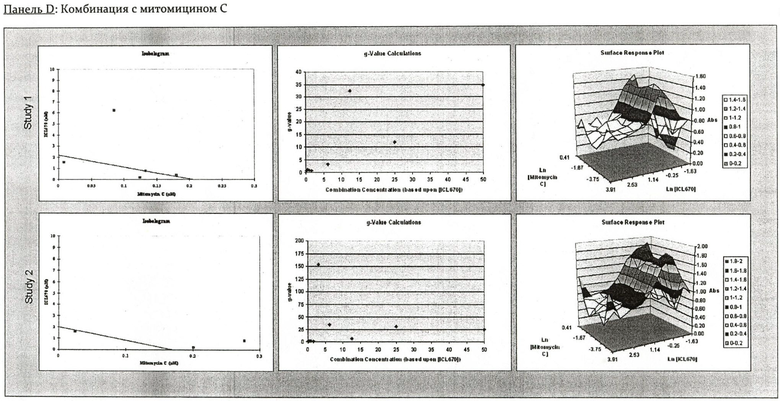
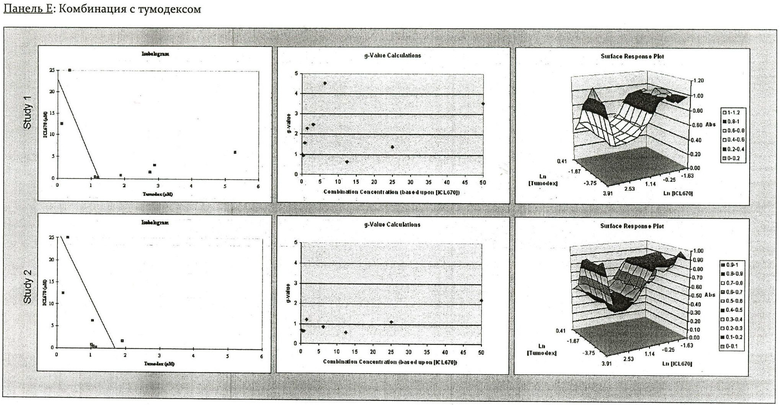
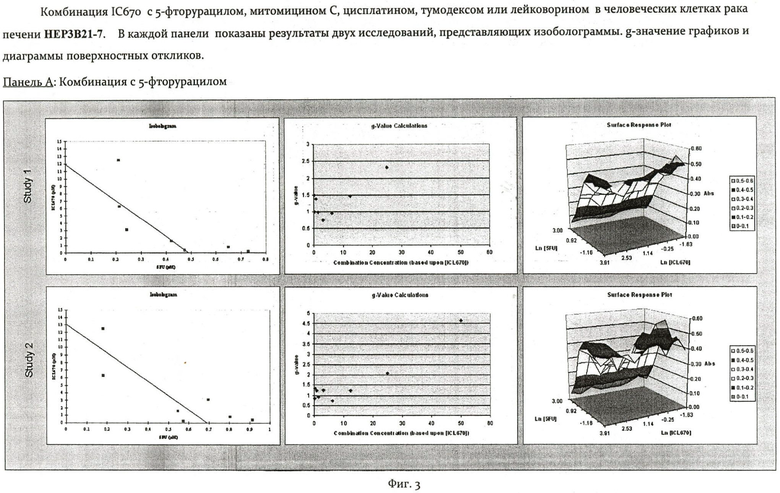
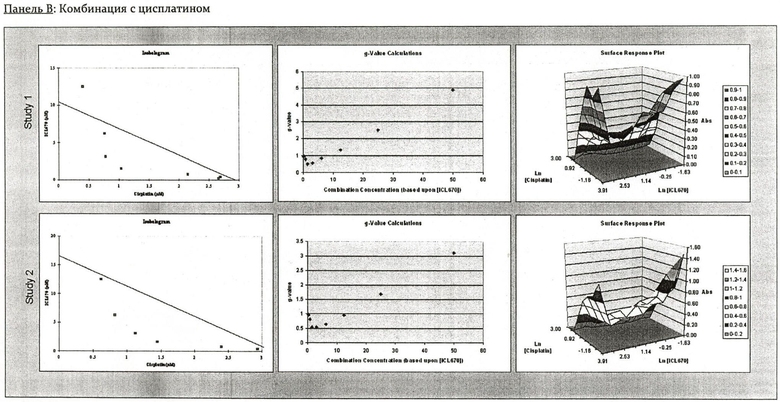
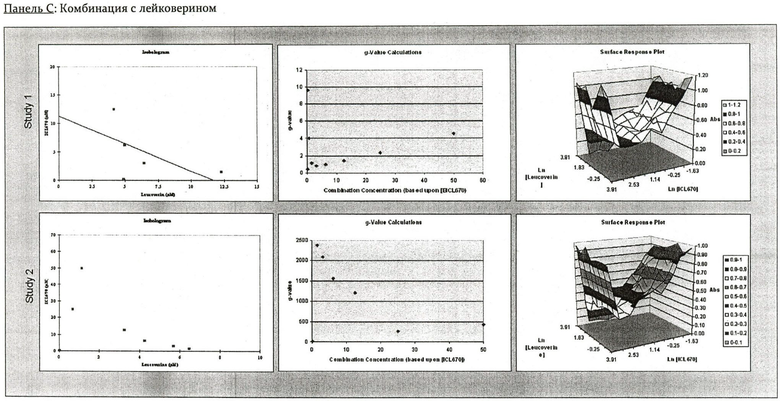
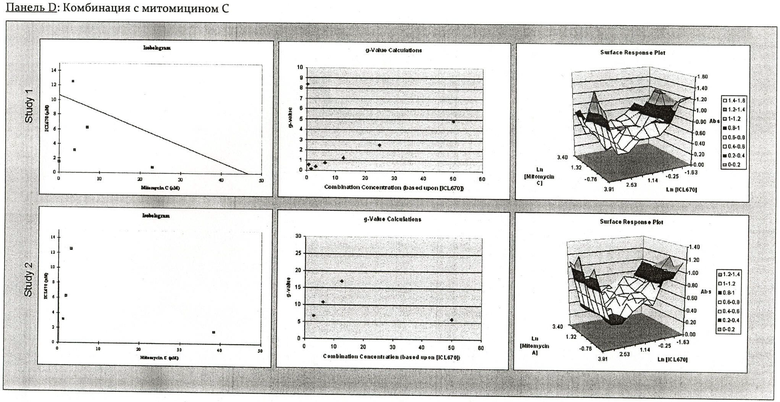
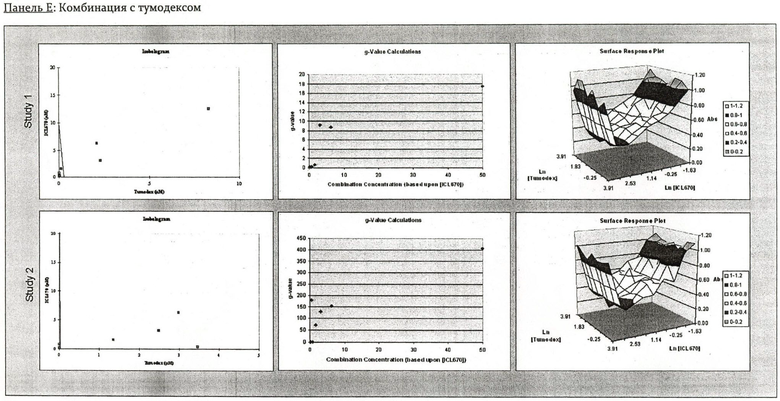
Изобретение относится к комбинации для лечения жидких и солидных опухолей, которая включает 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и цисплатин или их фармацевтические приемлемые соли. Изобретение также относится к применению указанной комбинации для получения лекарственного средства, предназначенного для лечения жидких и солидных опухолей, а также к набору, содержащему указанную комбинацию и инструкцию по применению. Заявленное изобретение обеспечивает синергетическое действие 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойной кислоты и цисплатина. 3 н. и 1 з.п. ф-лы, 3 табл., 10 ил., 1 пр.
1. Комбинация для лечения жидких и солидных опухолей, включающая
(а) 4-[3,5-бис(2-гидроксифенил)[1,2,4]триазол-1-ил]бензойную кислоту и
(б) цисплатин, в которой активные компоненты присутствуют в каждом случае в свободной форме или в форме фармацевтически приемлемой соли.
2. Комбинация по п.1, предназначенная для одновременного, раздельного или последовательного применения при лечении человека.
3. Применение комбинации по п.1 или 2 для получения лекарственного средства, предназначенного для лечения жидких и солидных опухолей.
4. Набор для лечения жидких и солидных опухолей, включающий комбинацию по п.1 или 2 и инструкцию по применению.
| WO 2004006859 А2, 22.01.2004 | |||
| US 6465504 B1, 15.10.2002 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2012-12-20—Публикация
2007-05-08—Подача