Настоящее изобретение относится к новым кристаллическим формам 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, к способам получения данных кристаллических форм, к композициям, содержащим данные кристаллические формы, и к применению данных кристаллических форм в методах диагностики или терапевтическом лечении теплокровных животных, особенно людей.
Предпосылки создания изобретения
4-[3,5-Бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, как лекарственное средство, представляет собой орально активный хелатор железа, используемый для лечения перенасыщения железом при анемиях, связанных с переливанием крови, в частности при большой талассемии, промежуточной талассемии и серповидно-клеточной анемии, для снижения связанной с уровнем железа заболеваемости и смертности. Также 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота может быть использована для лечения гемохроматоза. Получение 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, в основном, известно из уровня техники. Однако также известно, что различные кристаллические формы одного и того же лекарственного средства могут иметь существенные различия в определенных фармацевтически важных свойствах. Кроме того, все еще существует необходимость в новых твердых формах 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и в новых способах ее получения.
Краткое изложение изобретения
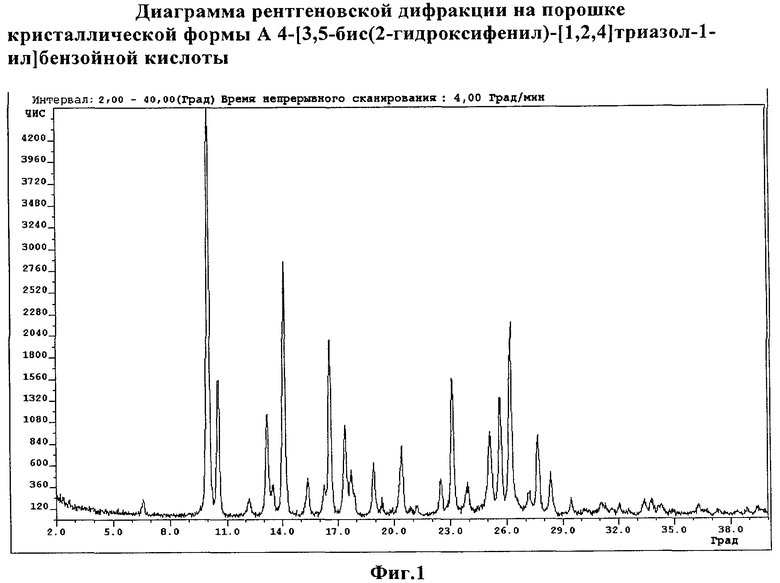
В соответствии с одним объектом изобретение относится к кристаллической форме А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции с пиком при угле преломления 2 тета (θ), составляющем 10,0°, 10,5°, 14,1°, 16,6°, 23,1°, 25,1°, 25,7°, 26,2°±0,2°, так как показано на фиг.1. Предпочтительно кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет спектр комбинационного рассеяния с характерными полосами при 3083, 1623, 1609, 1517, 1458, 1352, 991 см-1±0,3 см-1, так как показано на фиг.3.
В соответствии с еще одним объектом изобретение относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80 мас.% твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму А, имеющую картину рентгеновской дифракции с пиком при угле преломления 2 θ, составляющем 10,0°, 10,5°, 14,1°, 16,6°, 23,1°, 25,1°, 25,7°, 26,2°±0,2°, так как показано на фиг.1. Представлены различные воплощения и варианты осуществления изобретения.
В соответствии с еще одним объектом изобретение относится к фармацевтической композиции, содержащей кристаллическую форму А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель или разбавитель. Предпочтительно фармацевтической композицией является композиция для орального введения.
В соответствии с другим объектом изобретение относится к способу получения кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему:
(а) предоставление раствора 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, например, в аморфной форме, в протонном или апротонном растворителе,
(б) охлаждение раствора с образованием кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и
(в) выделение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Представлены различные воплощения и варианты осуществления изобретения.
В соответствии с еще одним объектом изобретение относится к кристаллической форме В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции с пиком при угле преломления 2 тета (θ), составляющем 6,5°, 7,4°, 10,8°, 13,4°, 14,8°, 19,2°, 21,7°, 26,1°±0,2°, так как показано на фиг.4.
В соответствии с еще одним объектом изобретение относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80 мас.% твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму В, имеющую картину рентгеновской дифракции с пиком при угле преломления 2 θ, составляющем 6,5°, 7,4°, 10,8°, 13,4°, 14,8°, 19,2°, 21,7°, 26,1°±0,2°, так как показано на фиг.4.
В соответствии с еще одним объектом изобретение относится к фармацевтической композиции, содержащей кристаллическую форму В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель или разбавитель. Предпочтительно фармацевтической композицией является композиция для орального введения.
Один из объектов изобретения относится к способу получения кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему:
(а) нагревание аморфного вещества при температуре стеклования, например при приблизительно 95°С, например при 95°С или вплоть до температуры, равной 105°С,
(б) начало кристаллизации при дальнейшем нагревании при температуре, составляющей, например, 150°С, и вплоть до температуры, равной приблизительно 190°С, например 190°С,
(в) выделение кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
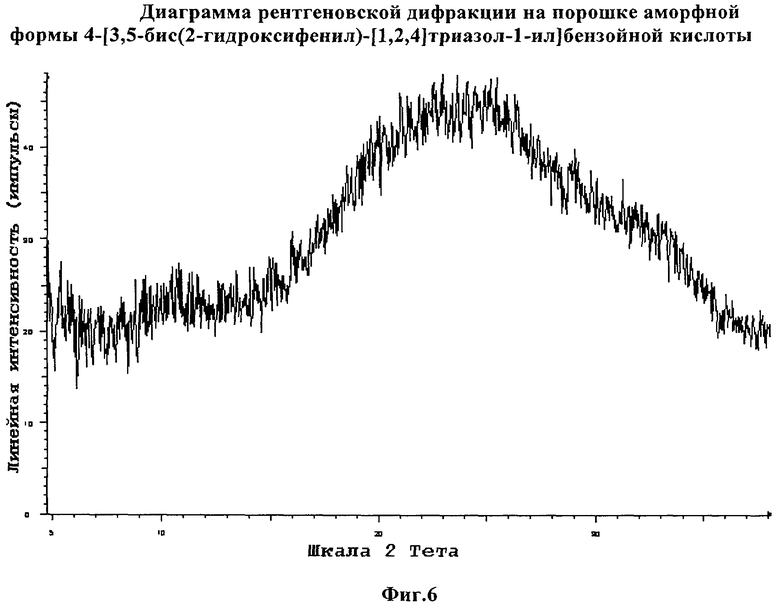
В еще одном воплощении изобретение относится к аморфной форме 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и к композициям, содержащим аморфную форму 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно аморфная форма 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты обладает спектром комбинационного рассеяния с характерными полосами при 3079, 1624, 1608, 1519, 1496, 1472, 1460, 1362, 1316, 997, 991 см-1±0,3 см-1, так как показано на фиг.7. Предпочтительно аморфная форма 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты демонстрирует характерные полосы спектра комбинационного рассеяния при 1496, 1472, 1362, 1316 см-1±0,3 см-1.
Изобретение также относится к способу получения аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему следующие стадии:
(а) нагревание, например, кристаллической формы модификации А или модификации В, например, при температуре плавления, составляющей для кристаллической формы модификации А, 261°С,
(б) быстрое охлаждение до температуры приблизительно 20-25°С или ниже, с получением аморфной формы.
Также изобретение относится к альтернативному способу получения аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему следующие стадии:
(а) растворение кристаллической формы модификации А или модификации В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в растворителе, например в водном растворителе, например в воде, или в смеси 50% органического растворителя/50% водной среды, например 50% воды/50% метилбутилового эфира, или 50% воды/50% диэтилового эфира, или в смеси органических растворителей, например 50% 3-пентанона/50% метилбутилового эфира, 50% 1-октанола/50% толуола, или 50% диоксана/50% толуола, или 50% толуола/50% диизопропилового эфира, или 50% н-гексана/50% ацетонитрила,
(б) быстрое выпаривание растворителя, например, в потоке азота,
(в) выделение аморфного твердого вещества.
Полезным свойством аморфной формы является ее очень высокая растворимость, например, по сравнению с кристаллической формой А или В.
Другой объект изобретения относится к кристаллической форме SA 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма SA 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции, как представленная на фиг.8.
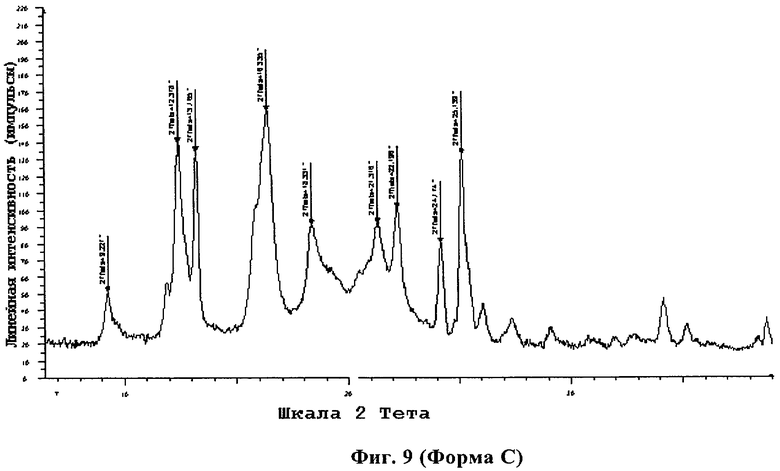
В соответствии с одним из объектов изобретение относится к кристаллической форме С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции с пиком при угле преломления 2 тета (θ), составляющем 9,2°, 12,4°, 13,2°, 16,3°, 18,3°, 21,3°, 22,2°, 24,2°, 25,1°±0,2°, так как показано на фиг.9.
В соответствии с еще одним объектом изобретение относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80 мас.% твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму С, имеющую картину рентгеновской дифракции с пиком при угле преломления 2 θ, составляющем 9,2°, 12,4°, 13,2°, 16,3°, 18,3°, 21,3°, 22,2°, 24,2°, 25,1°±0,2°, так как показано на фиг.9. Представлены различные воплощения и варианты осуществления изобретения.
В соответствии с еще одним объектом изобретение относится к фармацевтической композиции, содержащей кристаллическую форму С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель или разбавитель. Предпочтительно фармацевтической композицией является композиция для орального введения.
В соответствии с другим объектом изобретение относится к способу получения кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему:
(а) растворение 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в смеси ТГФ/вода/этанол, например, в соотношении (2:4:4),
(б) сушку раствора стадии (а), например, продувкой азотом при комнатной температуре,
(в) ресуспендирование сухого осадка стадии (б) в смеси (об./об.) растворителя 1, например, ацетонитрила, метанола или дихлорметана, и растворителя 2, например, н-гексана, толуола или циклогексана,
(г) перемешивание суспензии стадии (в) с использованием высокоскоростного вортекса, например, при температуре около 30°С, например при 30°С, например, около 2-х ч, например 2 ч,
(д) выпаривание раствора стадии (г), например, при комнатной температуре, например, в потоке азота,
(е) выделение модификации С.
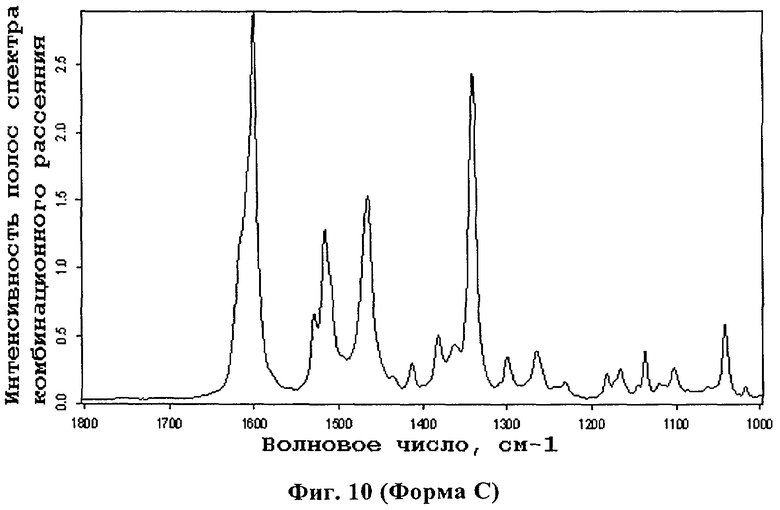
В другом воплощении изобретение относится к кристаллической форме С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и к композициям, содержащим кристаллическую форму С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты обладает спектром комбинационного рассеяния с характерными полосами при 3066 (w, ушир.), 2973 (w), 2940 (w), 1601 (st), 1530 (w), 1517 (m), 1467 (m), 1414 (w), 1341 (st), 1300 (w), 1264 (w), 1167 (w), 1042 (w), 986 (m), 837 (w), 781 (w), 659 (w), 413 (w) и 166 (w) см-1±3 см-1, так как показано на фиг.10. Предпочтительно кристаллическая форма С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты демонстрирует полосы спектра комбинационного рассеяния при 1601 и 1341 см-1±3 см-1.
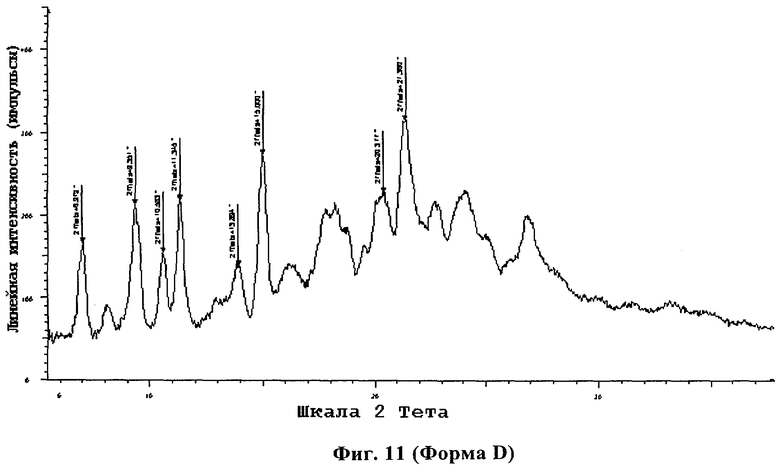
В соответствии с другим объектом изобретение относится к кристаллической форме D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции с пиком при угле преломления 2 тета (θ), составляющем 7,0°, 9,4°, 10,6°, 11,3°, 13,9°, 15,0°, 20,4°, 21,4°±0,2°, так как показано на фиг.11.
В соответствии с еще одним объектом изобретение относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80 мас.% твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму D, имеющую картину рентгеновской дифракции с пиком при угле преломления 2 θ, составляющем 7,0°, 9,4°, 10,6°, 11,3°, 13,9°, 15,0°, 20,4°, 21,4°±0,2°, так как показано на фиг.11.
В соответствии с еще одним объектом изобретение относится к фармацевтической композиции, содержащей кристаллическую форму D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель или разбавитель. Предпочтительно фармацевтической композицией является композиция для орального введения.
Один из объектов настоящего изобретения относится к способу получения кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, включающему:
(а) суспендирование модификации А в растворителе, например, смеси диэтиламин/циклогексан (1/1, об./об.),
(б) перемешивание суспензии стадии (а), например, при 30°С, например, в течение 2-х ч,
(в) фильтрование смеси стадии (б), например, на 0,2 мм фильтре, например, с однородной целлюлозной мембраной,
(г) выпаривание раствора стадии (в), например, в потоке N2,
(д) выделение кристаллов кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Еще один объект изобретения относится к кристаллической форме D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и к композициям, содержащим кристаллическую форму D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно форма D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет спектр комбинационного рассеяния с характерными полосами при 3071 (w, ушир.), 2973 (w, ушир.), 2940 (w, ушир.), 2887 (w, ушир.), 2852 (w, ушир.), 1604 (st), 1521 (m), 1483 (w, ушир.), 1462 (w, ушир.), 1385 (w, ушир.), 1346 (st), 1266 (w), 1158 (w), 1137 (w), 1034 (w), 984 (w), 660 (w), 414 (w) и 115 (w) см-1, так как показано на фиг.12. Предпочтительно кристаллическая форма D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты демонстрирует полосы спектра комбинационного рассеянии при 1521 и 1483 см-1±3 см-1.
Другой объект изобретения относится к кристаллической форме SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции, как представлена на фиг.13.
В соответствии с еще одним объектом изобретение относится к кристаллической форме SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Предпочтительно кристаллическая форма SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты демонстрирует картину рентгеновской дифракции с пиком при угле преломления 2 тета (θ), составляющем 9,4°, 10,0°, 11,3°, 12,8°, 15,0°, 16,1°, 22,1°, 24,3°±0,2°, так как показано на фиг.13.
В соответствии с еще одним объектом изобретение относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80 мас.% твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму SB, имеющую картину рентгеновской дифракции с пиком при угле преломления 2 θ, составляющем 9,4°, 10,0°, 11,3°, 12,8°, 15,0°, 16,1°, 22,1°, 24,3°±0,2°, так как показано на фиг.13.
В соответствии с еще одним объектом изобретение относится к фармацевтической композиции, содержащей кристаллическую форму SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель или разбавитель. Предпочтительно фармацевтическая композиция представляет собой композицию для орального введения.
Краткое описание чертежей
Фиг.1 демонстрирует диаграмму рентгеновской дифракции кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.2 демонстрирует кривую ДСК кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.3 демонстрирует спектр комбинационного рассеяния кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.4 демонстрирует диаграмму рентгеновской дифракции кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
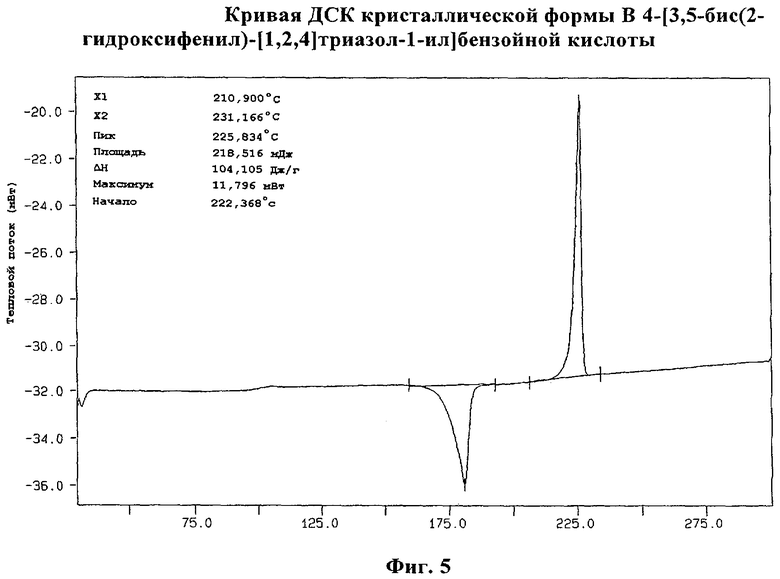
Фиг.5 демонстрирует кривую ДСК кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.6 демонстрирует диаграмму рентгеновской дифракции аморфной 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.7 демонстрирует спектр комбинационного рассеяния аморфной 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.8 демонстрирует диаграмму рентгеновской дифракции сольватной формы SA 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.9 демонстрирует диаграмму рентгеновской дифракции кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.10 демонстрирует спектр комбинационного рассеяния кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.11 демонстрирует диаграмму рентгеновской дифракции кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.12 демонстрирует спектр комбинационного рассеяния кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Фиг.13 демонстрирует диаграмму рентгеновской дифракции сольватной формы SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Подробное описание изобретения
Все технические и научные термины, используемые в настоящей заявке, имеют общепринятые значения, понятные специалисту в области, к которой относится данное изобретение, если не указано иное. Хотя любые способы и материалы, аналогичные или подобные описываемым в настоящей заявке, могут быть использованы при осуществлении настоящего изобретения, но предпочтительными способами и материалами являются описанные в настоящей заявке.
В рамках настоящего изобретения определяются следующие термины.
Кристаллическое соединение, обозначенное в настоящем описании как «кристаллическая форма А» и упоминаемое далее, как кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, является новым кристаллическим полиморфом 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, отличным от известных полиморфов. Данный полиморф охарактеризован рентгеновской дифракцией на порошке и ДСК, и раскрыт далее.
Кристаллическое соединение, обозначенное в настоящем описании как «кристаллическая форма В» и упоминаемое далее, как кристаллическая форма В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, является новым кристаллическим полиморфом 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, отличным от известных полиморфов. Данный полиморф охарактеризован рентгеновской дифракцией на порошке и ДСК, и раскрыт далее.
Также 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота может существовать в аморфной форме.
В рамках настоящего изобретения определяются следующие термины.
Кристаллическое соединение, обозначенное в настоящем описании как «кристаллическая форма С» и упоминаемое далее, как кристаллическая форма С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, является новым кристаллическим полиморфом 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, отличным от известных полиморфов.
Данный полиморф охарактеризован рентгеновской дифракцией на порошке, и раскрыт далее.
Кристаллическое соединение, обозначенное в настоящем описании как «кристаллическая форма D» и упоминаемое далее, как кристаллическая форма D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, является новым кристаллическим полиморфом 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, отличным от известных полиморфов. Данный полиморф охарактеризован рентгеновской дифракцией на порошке, и раскрыт далее.
Кристаллическое соединение, обозначенное в настоящем описании как «кристаллическая форма SB» и упоминаемое далее, как кристаллическая форма SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, является новым кристаллическим полиморфом 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, отличным от известных полиморфов. Данный полиморф охарактеризован рентгеновской дифракцией на порошке, и раскрыт далее.
«Фармацевтически приемлемый» означает пригодный для получения фармацевтической композиции, которая обычно не является токсичной и биологически нежелательной, и подразумевает возможность применения в ветеринарии и/или фармацевтических нуждах человека.
Термин «композиция» включает, но не ограничивается только этим, порошок, раствор, суспензию, гель, мазь, эмульсию и/или их смеси. Термин «композиция» включает продукт, содержащий определенные ингредиенты в определенном количестве, так же как и любой продукт, полученный непосредственно или косвенно, из комбинации определенных ингредиентов в определенных количествах. «Композиция» может содержать одно соединение или смесь соединений. «Соединение» представляет собой химическое вещество, включающее молекулы подобной химической структуры.
Термин «фармацевтическая композиция» следует понимать, как продукт, содержащий действущее(-ие) вещество(-а), фармацевтически приемлемые эксципиенты, составляющие носитель, также как и любой продукт, полученный, непосредственно или косвенно, из комбинации, комплекса или агрегата любых двух или более ингредиентов, или при диссоциации одного или более ингредиентов, или посредством иных типов реакций или взаимодействий одного или более ингредиентов. Таким образом, фармацевтические композиции настоящего изобретения охватывают любые композиции, полученные смешением действующего вещества, дополнительного(-х) действующего(-х) вещества(-в) и фармацевтически приемлемых эксципиентов.
Термин «эксципиент» означает компонент фармацевтического продукта, не являющийся активным ингредиентом, такой как наполнитель, разбавитель и носитель. Эксципиенты, пригодные для получения фармацевтической композиции, предпочтительно являются безопасными, нетоксичными и ни биологически, ни другим образом нежелательными, и приемлемы для ветеринарного применения, также как и для фармацевтических нужд человека. «Фармацевтически приемлемый эксципиент», так как используется в описании и формуле изобретения, включает как один, так и более чем один эксципиент.
«Терапевтически эффективное количество» означает количество соединения, которое при введении для лечения или предотвращения заболевания достаточно для оказания эффекта на такое лечение или предотвращение заболевания. «Терапевтически эффективное количество» будет меняться в зависимости от соединения, заболевания и его тяжести, возраста, массы и т.п., пациента, подвергающегося лечению.
В отношении химических реакций термины «обработка», «контактирование» и «взаимодействие» используются взаимозаменяемо в данном описании и относятся к добавлению или смешению двух или более реагентов в подходящих условиях, с получением указанного и/или требуемого продукта. Следует понимать, что реакция, в результате которой образуется указанный и/или требуемый продукт, может необязательно являться результатом комбинации двух реагентов, которые добавляют изначально, т.е. может существовать одно или более промежуточное соединение, образующееся в смеси, через которое в итоге получают указанный и/или требуемый продукт.
Термин «в основном свободный от», в отношении композиции, как используется в настоящем описании, означает, что форма вещества, от которого композиция свободна, не может быть определена способами, известными специалисту в данной области техники.
Термин «по существу чистый» в контексте настоящего изобретения следует в частности понимать, как, по меньшей мере, 90 мас.%, предпочтительно, по меньшей мере, 95 мас.% кристаллов кислотно-аддитивной соли формулы (I) находится в кристаллической форме настоящего изобретения.
В контексте данного описания следует понимать, что, для фразы «кристаллическая форма А, В, С или D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции по существу такую, как представлена на фиг.1, 4, 9 или 11, соответственно», термин «по существу» означает, что на диаграмме, представленной на фиг.1, 4, 9 или 11, соответственно, присутствуют, по меньшей мере, основные линии, т.е. линии, имеющие относительную интенсивность более чем 20%, особенно - более чем 30%, по сравнению с наиболее интенсивной линией на диаграмме.
В контексте данного описания следует понимать, что, для фразы «кристаллическая форма SA или SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет картину рентгеновской дифракции по существу такую, как представлена на фиг.8 или 13, соответственно», термин «по существу» означает, что на диаграмме, представленной на фиг.8 или 13, соответственно, присутствуют, по меньшей мере, основные линии, т.е. линии, имеющие относительную интенсивность более чем 20%, особенно - более чем 30%, по сравнению с наиболее интенсивной линией на диаграмме.
4-[3,5-Бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота имеет следующую химическую структуру:
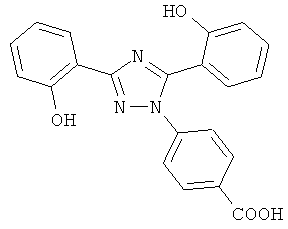
4-[3,5-Бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота описана в примере 5 выданного патента ЕР 09114118, способ ее получения также описан в ЕР 09114118.
Изобретение относится к кристаллической форме А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, к кристаллической форме В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, к кристаллической форме С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, к кристаллической форме D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, к сольватной форме SA 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, сольватной форме SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и к аморфной форме 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Различные твердые формы одного и того же лекарственного средства могут иметь различные свойства, включая характеристики, имеющие функциональные значения в зависимости от их применения в качестве лекарственного средства, и могут существенно различаться по фармацевтически важным параметрам, таким как скорость растворения и биодоступность. Подобным образом различные полиморфы могут обладать различными технологическими параметрами, такими как гидроскопичность, текучесть и т.п., которые могут влиять на их пригодность в качестве активных фармацевтических компонентов для промышленного производства.
Картины рентгеновской дифракции на порошке регистрируют Scintag X1, с источником излучения CuK-альфа, например, с использованием длины волны 0,15406 нм. Картина рентгеновской дифракции, представленная на фиг.1, обобщена в Таблице 1.
Следует иметь ввиду, что незначительные изменения, наблюдаемые для значений углов 2 θ или d-шага, основаны на специфике используемого дифрактометра, исследователя и методики приготовления образца. Наибольшее колебание наблюдается для относительной интенсивности пиков.
Идентификация требуемой кристаллической формы соединения будет основываться в первую очередь на наблюдаемых углах 2 θ, с наименьшей важностью описания при помощи относительной интенсивности пиков. Некоторый предел ошибки допускается для каждого значения угла 2 θ, представленного в настоящей таблице. Заданный предел ошибки, в предпочтительном варианте, для кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты составляет приблизительно ±0,2° для каждого значения пика.
Кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты также может быть охарактеризована дифференциальной сканирующей калометрией (ДСК). Кристаллическая форма А имеет характеристическую картину дифференциальной сканирующей калометрии (ДСК), как представлена на фиг.2. ДСК-анализ осуществляют с использованием Perkin Elmer DSC7 при скорости нагревания 10 К/мин. Кристаллическая форма А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет характеристический пик при приблизительно 261°С, например при 261°С. Некоторый предел ошибки существует для каждого представленного в настоящей таблице характеристического пика. Установленный предел ошибки составляет приблизительно +/-2 К, но может быть и больше, например меньше, в случае наличия примесей.
Одно или несколько физических свойств и/или спектроскопических свойств могут служить основой для характеристики кристалла полиморфных форм 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Изобретение также относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80% от общей массы твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму А. Предпочтительной формой данной композиции является измельченная твердая 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, пригодная для использования в качестве активного ингредиента при получении фармацевтических продуктов. Оставшаяся в композиции часть твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, т.е. 20% или менее от общей массы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, может представлять собой, например, другие кристаллические формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. В частном воплощении изобретения композиция содержит, по меньшей мере, 90% кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции. В другом частном воплощении изобретения композиция содержит, по меньшей мере, 95% кристаллической формы А формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции.
Также предложен способ получения кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Данный способ включает:
(а) предоставление раствора 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в протонном или апротонном растворителе, например, с использованием аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты,
(б) охлаждение раствора, с получением кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и
(в) выделение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Неограничивающими примерами протонных или апротонных растворителей являются следующие: ТГФ (тетрагидрофуран)/этанол, толуол/ТГФ, метанол/ТГФ, муравьиная кислота/этанол, вода, HXF.
В одном из воплощений изобретения 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту растворяют в смеси ТГФ/этанол и нагревают до соответствующей температуры, с получением кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Данный способ имеет высокую производительность, а полученный кристаллический продукт хорошо отфильтровывается.
Указанные выше условия селективного получения индивидуальных кристаллических форм не являются безусловными. В основном, например, возможно изменение параметров, таких как массовое соотношение соединения формулы (I) и растворителя или антирастворителя.
Картины рентгеновской дифракции на порошке регистрируют Scintag X1, с источником излучения CuK-альфа. Картина рентгеновской дифракции, представленная на фиг.4, обобщена в Таблице 2.
Следует иметь ввиду, что незначительные изменения, наблюдаемые для значений углов 2 θ или d-шага, основаны на специфике используемого дифрактометра, исследователя и методики приготовления образца. Наибольшее колебание наблюдается для относительной интенсивности пиков. Идентификация требуемой кристаллической формы соединения будет основываться в первую очередь на наблюдаемых углах 2 θ, с наименьшей важностью описания при помощи относительной интенсивности пиков.
Некоторый предел ошибки допускается для каждого значения угла 2 θ, представленного в настоящей таблице. Заданный предел ошибки, в предпочтительном варианте, для кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты составляет приблизительно ±0,2° для каждого значения пика.
Кристаллическая форма В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты также может быть охарактеризована дифференциальной сканирующей калометрией (ДСК). Кристаллическая форма В имеет характеристическую картину дифференциальной сканирующей калометрии (ДСК), как представлена на фиг.4. ДСК-анализ осуществляют с использованием Perkin Elmer DSC7. Кристаллическая форма В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты имеет характеристический пик при 266°С. Некоторый предел ошибки существует для каждого представленного в настоящей таблице характеристического пика. Установленный предел ошибки составляет приблизительно +/-2 К, но может быть и больше, например меньше, в случае наличия примесей.
Одно или несколько физических свойств и/или спектроскопических свойств могут служить основой для характеристики кристалла полиморфных форм 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Изобретение также относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80% от общей массы твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму В. Предпочтительной формой данной композиции является измельченная твердая 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, пригодная для использования в качестве активного ингредиента при получении фармацевтических продуктов. Оставшаяся в композиции часть твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, т.е. 20% или менее от общей массы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, может представлять собой, например, другие кристаллические формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. В частном воплощении изобретения композиция содержит, по меньшей мере, 90% кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции. В другом частном воплощении изобретения композиция содержит, по меньшей мере, 95% кристаллической формы В формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции.
Способ получения кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты включает следующие стадии:
(а) нагревание кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты до ее температуры плавления, составляющей около 261°С,
(б) охлаждение расплава 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты стадии (а) до приблизительно комнатной температуры, с получением аморфной формы,
(в) перекристаллизацию аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в кристаллическую форму В при нагревании до температуры выше 95°С, предпочтительно выше 190°С,
(г) выделение кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты посредством охлаждения до комнатной температуры.
Данный способ имеет высокую производительность, а полученный кристаллический продукт хорошо отфильтровывается.
Способ получения аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты включает следующие стадии:
(а) растворение кристаллической формы модификации А или модификации В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в растворителе, например в водном растворителе, например в воде или в смеси 50% органического растворителя/50% водной среды, например 50% воды/50% метилбутилового эфира, или 50% воды/50% диэтилового эфира, или в смеси органических растворителей, например 50% толуола/50% ацетонитрила, 50% н-гексана/50% толуола, или 50% н-гексана/50% ацетонитрила,
(б) быстрое выпаривание растворителя, например, в потоке азота,
(в) выделение аморфного твердого вещества.
Указанные выше условия селективного получения индивидуальных кристаллических форм и аморфной формы не являются безусловными. В основном, например, возможно изменение параметров, таких как массовое соотношение соединения формулы (I) и растворителя.
Предпочтительной формой композиции является измельченная твердая 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, пригодная для использования в качестве активного ингредиента при получении фармацевтических продуктов. Оставшаяся в композиции часть твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, т.е. 20% или менее от общей массы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, может представлять собой, например, кристаллические формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Также предложены фармацевтические композиции, содержащие кристаллическую форму А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель.
Также предложены фармацевтические композиции, содержащие кристаллическую форму В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель.
Изобретение также относится к композиции, содержащей твердую 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в кристаллической форме С, D или SB, или С и D, или С и/или D и SB.
Изобретение также относится к композиции, содержащей 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в твердой форме, в которой, по меньшей мере, 80% от общей массы твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму С или D. Предпочтительной формой данной композиции является измельченная твердая 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойная кислота, пригодная для использования в качестве активного ингредиента при получении фармацевтических продуктов. Оставшаяся в композиции часть твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, т.е. 20% или менее от общей массы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, может представлять собой, например, другие кристаллические формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. В частном воплощении изобретения композиция содержит, по меньшей мере, 90% кристаллической формы С или D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции. В другом частном воплощении изобретения композиция содержит, по меньшей мере, 95% кристаллической формы С или D формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты по отношению к общей массе твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в композиции.
Также предложен способ получения кристаллической формы С-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты. Данный способ включает:
(а) предоставление раствора 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты в смеси протонных и/или апротонных растворителей, например, в смеси ТГФ/вода/этанол (например, при соотношении 2:4:4), например, с использованием аморфной формы 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты,
(б) сушку раствора стадии (а),
(в) суспендирование осадка, полученного на стадии (б), например, в смеси растворителей, например в смеси, содержащей (об./об.) растворитель 1, например, ацетонитрил, метанол или дихлорметан, и растворитель 2, например, н-гексан, толуол или циклогексан, например, при перемешивании, например, с использованием высокоскоростного вортекса, например, при температуре, составляющей около 30°С, например при 30°С, около 2-х ч, например 2 ч,
(г) выделение кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, например, выпариванием раствора стадии (в), например, при комнатной температуре, например, в потоке азота.
В одном из воплощений изобретения 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту растворяют в смеси ТГФ/этанол, осаждают посредством добавления затравочных кристаллов кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и добавляют этанол, в качестве антирастворителя, и получают кристаллическую форму С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Картины рентгеновской дифракции на порошке регистрируют дифрактометром Bruker D8 Gadds, с источником излучения CuK-альфа, например, с использованием длины волны 0,15406 нм. Картина рентгеновской дифракции, представленная на фиг.9, обобщена в Таблице 3.
Картины рентгеновской дифракции на порошке регистрируют дифрактометром Bruker D8 Gadds, с источником излучения CuK-альфа, например, с использованием длины волны 0,15406 нм. Картина рентгеновской дифракции, представленная на фиг.11, обобщена в Таблице 4.
Картины рентгеновской дифракции на порошке регистрируют дифрактометром Bruker D8 Gadds, с источником излучения CuK-альфа, например, с использованием длины волны 0,15406 нм. Картина рентгеновской дифракции, представленная на фиг.13, обобщена в Таблице 5.
Следует иметь ввиду, что незначительные изменения, наблюдаемые для значений углов 2 θ или d-шага, основаны на специфике используемого дифрактометра, исследователя и методики приготовления образца. Наибольшее колебание наблюдается для относительной интенсивности пиков. Идентификация требуемой кристаллической формы соединения будет основываться в первую очередь на наблюдаемых углах 2 θ, с наименьшей важностью описания при помощи относительной интенсивности пиков.
Некоторый предел ошибки допускается для каждого значения угла 2 θ, представленного в настоящей таблице. Заданный предел ошибки, в предпочтительном варианте, для кристаллических форм С, D и SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты составляет приблизительно ±0,2° для каждого значения пика.
Одно или несколько физических свойств и/или спектроскопических свойств могут служить основой для характеристики кристалла полиморфных форм 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Способ получения кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты включает следующие стадии:
(а) суспендирование модификации А в растворителе, например, в смеси диэтиламин/циклогексан (1/1, об./об.),
(б) перемешивание суспензии стадии (а), например, при 30°С, например, в течение 2-х ч,
(в) фильтрование смеси стадии (б), например, на 0,2 мм фильтре, например, с однородной целлюлозной мембраной,
(г) выпаривание раствора стадии (в), например, в потоке N2,
(д) выделение кристаллов кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты.
Способ получения кристаллической формы SB 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты включает следующие стадии:
(а) суспендирование кристаллической формы модификации А в растворителе, например в ДМФА,
(б) обработку суспензии стадии (а) ультразвуком, например, около 15 мин, например 15 мин, и ее фильтрование, например, на 0,2 мм однородной целлюлозной мембране,
(в) добавление воды к раствору стадии (б),
(г) фильтрование и сушку осадка, полученного на стадии (в), например, в N2,
(д) выделение кристаллической формы SB.
Указанные выше условия селективного получения индивидуальных кристаллических форм и аморфной формы не являются безусловными. В основном, например, возможно изменение параметров, таких как массовое соотношение соединения формулы (I) и растворителя.
Также предложены фармацевтические композиции, содержащие кристаллическую форму С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель.
Также предложены фармацевтические композиции, содержащие кристаллическую форму D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты и фармацевтически приемлемый носитель.
В дополнение к активному ингредиенту фармацевтическая композиция содержит один или более фармацевтически приемлемых носителей, также известных как эксципиенты, которые обычно не имеют фармацевтической активности, но обладают различными полезными свойствами, которые, например, увеличивают стабильность, стерильность, биодоступность и облегчают получение фармацевтической композиции. Такие носители являются фармацевтически приемлемыми, что означает, что они не опасны для людей и животных при соответствующем применении и совместимы с другими ингредиентами данного состава. Носители могут быть твердыми, полутвердыми или жидкими, и могут быть составлены в смесь с другими соединениями в «балк», но, в конечном счете, в форме дозированного состава, т.е. физически дискретного при содержании определенного количества активного ингредиента, такого как таблетка или капсула. Фармацевтические композиции могут включать, в дополнение к соединению настоящего изобретения, одно или несколько активных фармацевтических соединений.
Фармацевтические композиции могут иметь форму суспензий, растворов, эликсиров, аэрозолей или твердых лекарственных форм.
Фармацевтические композиции, предусмотренные в различных составах, пригодны для различных типов введения, включающих, но не ограничивающихся только этим, ингаляционное, оральное, ректальное, парэнтеральное (включая подкожное, внутрикожное, внутримышечное и внутривенное), трансдермальное введение и имплантирование. Наиболее подходящий путь введения в данном случае зависит от длительности состояния, в котором находится субъект, продолжительности необходимого лечения, природы и тяжести состояния, подвергающегося лечению, и конкретного применяемого состава. Составы могут быть в форме «балка» или дозированной лекарственной формы, и могут быть получены способами, хорошо известными из уровня для данных составов.
Количество активного ингредиента, содержащегося в дозированной лекарственной форме, зависит от вида состава, в котором содержится активный ингредиент. Фармацевтическая композиция, как правило, содержит от около 0,1 мас.% до около 99 мас.% активного ингредиента, предпочтительно от около 1 мас.% до 50 мас.% для орального введения и от около 0,2 мас.% до около 20 мас.% для парентерального введения.
Составы, пригодные для орального введения, включают капсулы (жесткие и мягкие), крахмальные капсулы, пастилки, сиропы, суппозитории и таблетки, каждая из которых включает предварительно определенное количество активного соединения; в виде порошков или гранул, в виде раствора или суспензии в водной или безводной жидкости; или в виде эмульсии «масло-в-воде» или «вода-в-масле». Такие составы могут быть получены пригодным в фармакологии методом, включающим стадию объединения активного соединения и подходящего носителя или носителей.
Оральное введение является предпочтительным путем введения настоящего изобретения.
Другой объект изобретения относится к способам лечения с применением соединений и фармацевтических композиций настоящего изобретения.
Соединения и композиции настоящего изобретения могут быть введены субъекту в количестве, эффективном для применения для лечения избытка железа у людей или животных и/или расстройств, связанных с избытком железа у данных субъектов.
В частности настоящее изобретение относится к кристаллической форме А, кристаллической форме В, кристаллической форме С и кристаллической форме D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, раскрытым в настоящем описании, для лечения одного из упомянутых заболеваний или для получения фармакологического агента для лечения данных заболеваний. Различные заболевания теплокровных животных связаны с избытком металлов, в частности трехвалентных металлов, в тканях человека. Например, алюминия при диализной энцефалопатии и остеомаляции, также как и при болезни Альцгеймера. При других заболеваниях, особенно у мужчин, избыток железа наблюдается в различных тканях. Данное явление характеризуют как перенасыщение железом (прежде - гемосидероз). Оно встречается, например, после парентерального введения железа (особенно при повторяющихся переливаниях крови) или после увеличения поступления железа из желудочно-кишечного тракта. Повторяющиеся переливания крови необходимы при серьезных анемиях, особенно при большой талассемии, при тяжелой форме β-талассемии, но также и при других формах анемии. Повышение абсорбции железа из желудочно-кишечного тракта протекает первично, например, вследствие генетического дефекта (так называемый гемохроматоз), или вторично, в случае, когда после анемии переливания крови не нужны, например, при промежуточной талассемии, при легкой форме β-талассанемии. Уменьшение концентрации железа (II) также имеет значение при лечении заболеваний, вызванных зависимыми от железа (II) микроорганизмами и паразитами, что имеет ключевую роль не только в медицине человека, в частности, при малярии, но также и в ветеринарии. Образование комплексов иных металлов, в частности трехвалентных металлов, может быть также использовано для экскреции данных металлов из организма.
Также изобретение относится к способу лечения теплокровных животных, страдающих от упомянутых заболеваний, в котором количество кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, эффективное против данных заболеваний, вводят теплокровному животному, нуждающемуся в таком лечении.
Также изобретение относится к применению кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты для лечения избытка железа у человека или животного и/или связанных с избытком железа расстройств, или для получения фармацевтических композиций для применения для лечения человека или животного, в частности, для лечения расстройств, связанных с избытком железа.
Доза активного ингредиента может зависеть от различных факторов, таких как активность и продолжительность действия активного ингредиента, серьезность заболевания, подвергающегося лечению, или его симптомов, типа введения, вида теплокровного животного, пола, возраста, массы и/или индивидуального состояния теплокровного животного. Суточные дозы в случае орального введения составляют от 10 до приблизительно 120 мг/кг, в частности от 20 до 80 мг/кг, а для теплокровного животного с массой тела около 40 кг - предпочтительно от приблизительно 400 мг до приблизительно 4800 мг, в частности от приблизительно 800 мг до приблизительно 3200 мг, которые целесообразно вводить в виде 2-12 индивидуальных доз.
Изобретение также относится к фармацевтическим препаратам, содержащим эффективное количество, в частности эффективное количество для предотвращения или лечения одного из упомянутых заболеваний, особенно расстройств, связанных с избытком железа, кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы С 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, и/или кристаллической формы D 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, вместе с фармацевтически приемлемыми носителями, пригодными для топического, энтерального, например орального или ректального, или парентерального введения, которые могут быть неорганическими или органическими, твердыми или жидкими.
Фармацевтические составы для энтерального или парентерального введения представляют собой, например, дозированные лекарственные формы, такие как таблетки, покрытые сахарной оболочной, таблетки, диспергируемые таблетки, шипучие таблетки, капсулы, суспендированные порошки, суспензии или суппозитории, или ампулы. Данные составы получают с использованием методик, хорошо известных специалисту, например, посредством традиционных способов дражирования, смешения, гранулирования или лиофилизации. Фармацевтические составы для орального введения могут быть получены посредством объединения активного ингредиента с твердыми носителями, при необходимости, при гранулировании полученной смеси и обработке смеси или гранул, при желании или необходимости, после добавления подходящих адъювантов, с получением таблеток или покрытых сахарной оболочкой ядер таблеток.
Подходящими носителя являются, в частности, наполнители, такие как сахара, например лактоза, сахароза, маннит или сорбит, препараты на основе целлюлозы и/или фосфаты кальция, например трикальций фосфат или гидрофосфат кальция, кроме того, связующие вещества, такие как крахмальные пасты, например, на основе кукурузного, пшеничного, рисового или картофельного крахмала, желатин, трагакант, метилцеллюлоза и/или поливинилпирролидон, и, при желании, дезинтеграторы, такие как упомянутые выше крахмалы, а также карбоксиметиловый крахмал, сшитый поливинилпирролидон, агар, альгиновая кислота или ее соли, такие как альгинат натрия. Адъювантами в первую очередь являются агенты, регулирующие прохождение, и смазывающие агенты, такие как салициловая кислота, тальк, стеариновая кислота или ее соли, такие как стеарат магния или кальция, и/или полиэтиленгликоль. Ядра таблеток с сахарной оболочкой покрывают пригодными, при желании растворимыми в кишечнике, покрытиями, с использованием концентрированных сахарных растворов, которые, при желании, содержат гуммиарабик, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, растворы для покрытий в подходящих органических растворителях или смесях растворителей, или для получения покрытий, растворимых в кишечнике, растворы подходящих препаратов, на основе целлюлозы, таких как ацетилцеллюлозы фталат или гидроксипропилметилцеллюлозы фталат. Красители или пигменты, например, для идентификации или мечения различных доз активного ингредиента, могут быть добавлены в таблетки или покрытия для таблеток, с сахарной оболочкой.
Диспергируемые таблетки представляют собой таблетки, быстро разрушаемые в сравнительно небольшом количестве жидкости, например в воде, и которые, при необходимости, содержат отдушки или вещества, для маскировки вкуса активного ингредиента. Данные таблетки преимущественно используют для орального введения больших индивидуальных доз, в которых количество активного ингредиента, которое необходимо ввести, является таким большим, что при введении в виде таблетки, которую следует проглатывать целиком или без разжевывания, ее нельзя проглотить в течение долгого времени, не испытывая неудобства, в частности, детьми. Кроме того, фармацевтические составы для орального введения представляют собой твердые, а также мягкие желатиновые капсулы, закрытые капсулы из желатина и пластификатора, такие как глицерин и сорбит. Твердые желатиновые капсулы могут содержать активный ингредиент в форме гранул, например, в виде смеси с наполнителями, такими как лактоза, связующими веществами, такими как крахмалы, и/или веществами, способствующими скольжению, такими как тальк или стеарат магния, и, при необходимости, стабилизаторами. В мягких капсулах активный ингредиент предпочтительно растворен или суспендирован в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли, также возможно добавление стабилизаторов.
Кроме того, суспендированные порошки, например, которые описаны как «порошок в бутылке» - аббревиатура «PIB», или как готовые к применению суспензии, пригодны для формы орального введения. Для данной формы активный ингредиент смешивают, например с фармацевтически приемлемыми поверхностно-активными веществами, например с лаурилсульфатом натрия или полисорбатом, с суспендированными вспомогательными веществами, например с гидроксипропилцеллюлозой, гидроксипропилметилцеллюлозой или другими, хорошо известными из уровня техники и описанными, например, в «Handbook of Pharmaceutical Excipients», с регуляторами pH, такими как лимонная или винная кислоты, или их соли, или с USP буфером, и, при желании, с наполнителями, например, лактозой, и другими вспомогательными веществами, и помещают в подходящие сосуды, преимущественно в сосуды или ампулы с одноразовой дозой. Непосредственно перед применением добавляют определенное количество воды и посредством встряхивания получают суспензию. Как вариант, вода может быть добавлена и перед дозированием.
Фармацевтические препараты для ректального введения представляют собой, например, суппозитории, содержащие комбинацию активного ингредиента с основой для суппозиториев. Подходящей основой для суппозиториев являются, например, натуральные или синтетические триглицериды, парафиновые углеводороды, полиэтиленгликоли или высшие спирты. Также могут быть использованы ректальные желатиновые капсулы, содержащие комбинацию активного ингредиента с основным веществом. Возможные основные вещества представляют собой, например, жидкие триглицериды, полиэтиленгликоли или парафиновые углеводороды.
Для парентерального введения, прежде всего, пригодны водные растворы активного ингредиента в водорастворимой форме, например, в виде водорастворимой соли; кроме того, могут быть использованы суспензии активного ингредиента, такие как соответствующие масляные суспензии для инъекций, подходящие липофильные растворители или наполнители, такие как жирные масла, например кунжутное масло, или синтетические эфиры жирных кислот, например, этилолеат или триглицериды, а также водные суспензии для инъекций, содержащие вещества, увеличивающие вязкость, например натрий карбоксиметилцеллюлозу, сорбит и/или декстран, и, при необходимости, стабилизаторы.
Дополнительно изобретение определяется ссылкой на нижеследующие примеры, подробно описывающие получение соединений и композиций настоящего изобретения, а также их применение. Для специалиста очевидно, что различные модификации как материалов, так и методов могут быть осуществлены без отклонения от задач и целей настоящего изобретения. Нижеследующие примеры не следует рассматривать как ограничивающие объем настоящего изобретения как описанного ранее, так и заявленного далее в формуле изобретения.
ПРИМЕРЫ:
Пример 1. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием смеси ТГФ/этанол и HXF.
Пример 2. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием толуола и ТГФ.
Пример 3. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием смеси метанол/ТГФ.
Пример 4. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием муравьиной кислоты и этанола.
Пример 5. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием смеси метанол/ТГФ и воды.
Пример 6. Получение кристаллической формы А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты с использованием смеси метанол/ТГФ и HXF.
Пример 7. Получение кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты путем кристаллизации аморфной формы при температуре выше 100°С.
Пример 8. Получение кристаллической формы В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты путем кристаллизации аморфной формы при температуре выше 140°С.
Пример 9. Получение кристаллической формы С
4-[3,5-Бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту растворяют в смеси ТТФ/вода/этанол, например, при соотношении 2:4:4. Полученный раствор помещают в 96-ячеечный блок при общем количестве лекарственного вещества 2 мг на ячейку. Затем раствор высушивают посредством продувания азотом при комнатной температуре. Высушенный осадок ресуспендируют с использованием 125 мкл растворителя 1, например, ацетонитрила, метанола или дихлорметана, и 125 мкл растворителя 2, например, н-гексана, толуола или циклогексана. Полученную суспензию или раствор перемешивают с использованием высокоскоростного вортекса, например, при температуре около 130°С, например при 130°С, например, около 2-х ч, например 2 ч. Затем раствор выпаривают, например, при комнатной температуре, например, в потоке азота, и выделяют модификацию С.
Пример 10. Получение кристаллической формы D
Около 50 мг модификации А 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты суспендируют в 5 мл смеси диэтиламина и циклогексана (1/1, об./об.). Затем полученную суспензию перемешивают в течение 2-х ч при 30°С и фильтруют на 0,2 мм фильтре с однородной целлюлозной мембраной. После этого раствор выпаривают в потоке N2. Твердый осадок выделяют и анализируют посредством рентгеновской дифракции на порошке с использованием дифрактометра Bruker D8 Gadds.






Описывается новая кристаллическая форма В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты (деферасирокса) и две фармацевтические композиции для предотвращения или лечения расстройств, связанных с избытком железа, содержащие данную форму В. 3 н. и 5 з.п. ф-лы, 13 ил., 5 табл., 10 пр.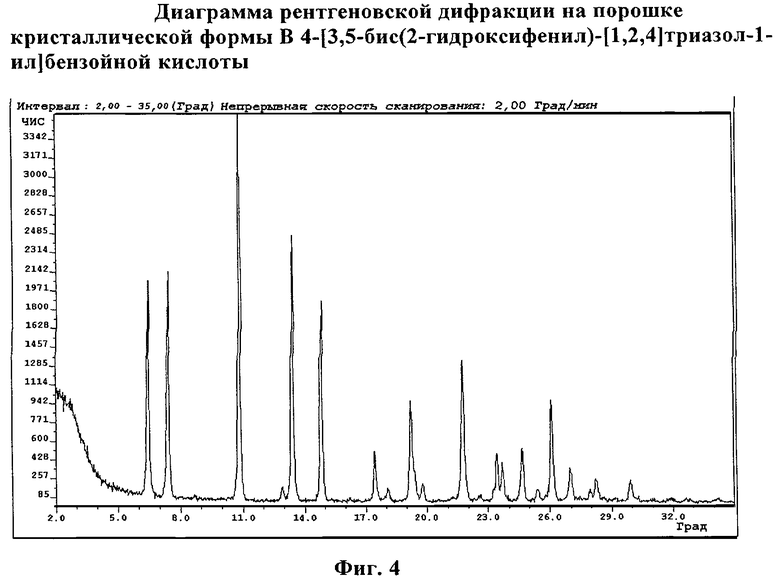
1. Соединение, представляющее собой кристаллическую форму В 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты, которая демонстрирует пик на картине рентгеновской дифракции при угле преломления 2θ, составляющем 6,5° и 7,4°±0,2°.
2. Соединение по п.1, имеющее картину рентгеновской дифракции, выраженную в значениях угла 2θ, дополнительно содержащую три или более пиков, выбранных из группы пиков при [[6,5°, 7,4°, 10,8°, 13,4°, 14,8°, 19,2°, 21,7°, 26,1°±0,2°]] 10,8°, 13,4°, 14,8°, 19,2°, 21,7° и 26,1°±0,2°.
3. Соединение по п.1, имеющее картину рентгеновской дифракции, по существу, такую, как представлена на фиг.4.
4. Фармацевтическая композиция для предотвращения или лечения расстройств, связанных с избытком железа, содержащая 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойную кислоту в виде твердого вещества, в которой, по меньшей мере, 80 мас.% упомянутой твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму В по п.1.
5. Фармацевтическая композиция по п.4, в которой, по меньшей мере, 90 мас.% упомянутой твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму В.
6. Фармацевтическая композиция по п.5, в которой, по меньшей мере, 95 мас.% упомянутой твердой 4-[3,5-бис(2-гидроксифенил)-[1,2,4]триазол-1-ил]бензойной кислоты представляет собой кристаллическую форму В.
7. Фармацевтическая композиция для предотвращения или лечения расстройств, связанных с избытком железа, содержащая:
(а) соединение по п.1 и
(б) фармацевтически приемлемый носитель или разбавитель.
8. Фармацевтическая композиция по п.7, представляющая собой лекарственную форму, пригодную для орального введения.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), ПРОИЗВОДНЫЕ 3,5-ДИФЕНИЛ-1,2,4-ТРИАЗОЛОВ, В НЕЕ ВХОДЯЩИЕ | 1997 |
|
RU2208010C2 |
| ЕР 0914118 А1, 12.05.1999 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| EUROPEAN JOURNAL OF CHEMISTRY, vol.21, 2004, p.4177-4192, Fig 2 и Tabl.4. | |||
Авторы
Даты
2012-11-27—Публикация
2007-11-27—Подача