Настоящее изобретение относится к химии и химической технологии, а именно к синтезу модифицированных силикагелей, содержащих ковалентно связанные с ним молекулы замещенных фталоцианинов, а также к применению этих силикагелей для фотообеззараживания воды от вирусного загрязнения.
Обеспечение населения доброкачественной питьевой водой является одной из важнейших проблем не только в России, но и во всем мире. Сброс в водоемы недостаточно очищенных и обеззараженных сточных вод привел к повсеместному увеличению химического и микробного загрязнения поверхностных и подземных водоисточников. Особую опасность представляет вирусное загрязнение воды в связи с тем, что используемые в настоящее время способы очистки воды недостаточно эффективны в отношении вирусов, а заражающие дозы вирусов чрезвычайно малы (единицы и десятки вирионов). В настоящее время известно более 150 патогенных для человека различных видов вирусов, циркулирующих в водоемах.
Из существующих на сегодняшний день методов обеззараживания воды по-прежнему наиболее широко используются соединения хлора (жидкий хлор, хлорная известь, гипохлорит кальция и др.). После обработки соединениями хлора вода по индикаторным бактериям является стандартной, но может содержать вирусы. Кроме того, в воде с высоким содержанием органических веществ природного и техногенного происхождения образуются токсичные для человека хлорорганические соединения - тригалометаны, обладающие канцерогенным и мутагенным эффектом. В то же время содержание в воде повышенных доз хлора и его производных приводит к нарушению биоценоза в водоемах.
В связи с вышеизложенным, поиск и внедрение новых эффективных и безопасных технологических решений для очистки и обеззараживания воды в отношении вирусного загрязнения является одной из важнейших проблем. В качестве одного из перспективных методов очистки воды является использование фотодинамического эффекта различных сенсибилизаторов.
Известны катионные фталоцианины, представляющие собой поли(триалкиламмониометил)замещенные фталоцианина цинка и алюминия, являющиеся сенсибилизаторами образования синглетного кислорода под действием видимого света, а также способ фотообеззараживания воды с использованием этих фталоцианинов [патент РФ №2281953, кл. С02F 1/30, 2006]. Положительный заряд катионных групп обеспечивает взаимодействие этих сенсибилизаторов с отрицательно заряженными внешними мембранами микроорганизмов, проникновение в них и эффективную фотодинамическую инактивацию. Несмотря на высокую эффективность, этот метод имеет существенный недостаток, который заключается в необходимости последующего удаления красителя из раствора. Эта операция осуществляется с помощью специально разработанных селективных фильтров, что существенно усложняет и удорожает процесс и, тем не менее, не гарантирует во всех случаях полного удаления сенсибилизатора и продуктов его фотодеградации из раствора.
Этого недостатка лишены гетерогенные (твердофазные) сенсибилизаторы образования синглетного кислорода. Твердофазные сенсибилизаторы могут быть легко отделены от воды после фотовоздействия простым фильтрованием.
Известны гетерогенные сенсибилизаторы для инактивации микроорганизмов, полученные адсорбцией красителей со светоустойчивостью от 4 до 8 баллов на инертный носитель [A.Yoshino, I.Iwami. US Patent N 4520072]. Однако адсорбированный краситель может десорбироваться и переходить в водный раствор, тем самым вызывая его химическое загрязнение.
Известны гетерогенные сенсибилизаторы для инактивации микроорганизмов, полученные химической пришивкой тетрафенилпорфиринов сурьмы и фосфора к гранулам силикагеля [Н.Yokoi, Т.Shiragami, J.Hirose, T.Kawauchi, K.Hinoue, Y.Fueda, K.Nobuhara, I.Akazaki, M.Yasuda. World J.Microbial. Biotechnol. 2003, 19, 559; Y.Fueda, Н.Suzuki, Y.Komiya, Y.Asakura, T.Shiragami, J.Matsumoto, Н.Yokoi, M.Yasuda. Bull. Chem. Soc. Jpn. 2006, 79, N9, 1420-1425]. Однако соединения сурьмы нежелательно вносить в окружающую среду из-за их потенциальной токсичности.
Задача изобретения - синтез гетерогенного сенсибилизатора, содержащего в качестве активной фазы ковалентно связанный с носителем замещенный фталоцианин, а также разработка способа фотообеззараживания воды от вирусного загрязнения с применением полученного сенсибилизатора.
Поставленная задача решается путем синтеза гетерогенного сенсибилизатора, который можно представить следующей формулой:
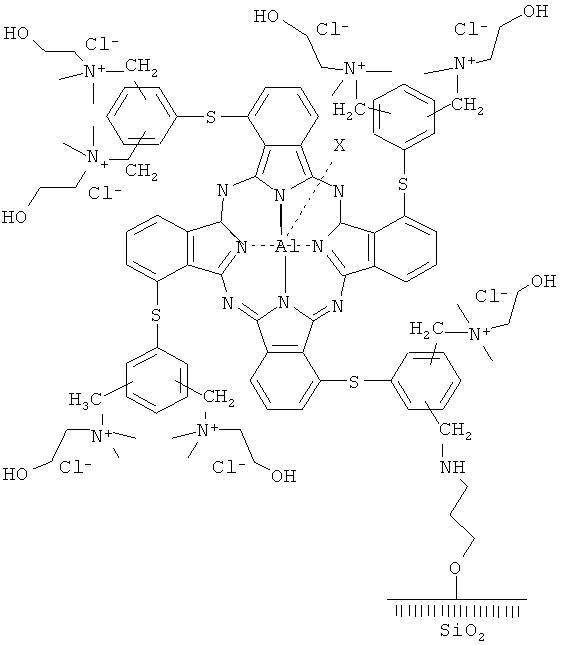
Где Х=Сl(ОН)
Получают этот сенсибилизатор химической прививкой тетракис [бис (хлорметил)фенилтио]фталоцианина алюминия к аминопропилированному силикагелю и последующей обработкой полученного продукта диметиламиноэтанолом:
…-Si-O(CH2)3NH2+Al(Cl)Pc(SPh)4(CH2Cl)8→
→…-Si-O(CH2)3NHCH2-[Al(Cl)Pc(SPh)4(CH2Cl)7]→
→…-Si-O(CH2)3NHCH2-{Al(X)Pc(SPh)4[CH2N+(СН3)2С2Н4OН]7}Cl7 -
где Х=Сl или ОН.
Гетерогенный сенсибилизатор, содержащий в качестве активной фазы тетракис[бис(холинил)фенилтио]фталоцианин алюминия, поглощает свет с длиной волны в областях от 300 до 450 нм и от 600 до 800 нм. Тиофенильные заместители в положении 3 находятся вне плоскости фталоцианинового макрокольца и препятствуют сближению молекул и образованию неактивных π-π димеров и агрегатов, что положительно сказывается на их антимикробной активности. Алюминиевые комплексы отличаются высокой фотостабильностью, что в отличие, например, от цинковых и титанильных комплексов позволяет их использовать в нескольких циклах фотодинамической обработки воды. Значительный положительный заряд молекулы фталоцианина обеспечивает хорошую адсорбцию отрицательно заряженных вирусов на силикагеле и их инактивацию под действием генерируемых при облучении активных форм кислорода.
На Фиг.1 представлен электронный спектр поглощения суспензии предлагаемого сенсибилизатора в глицерине.
Поставленная задача достигается также разработкой способа фотообеззараживания воды от вирусного загрязнения с применением вышеописанного гетерогенного сенсибилизатора и излучения видимого диапазона в присутствии кислорода.
Использованный для синтеза (тетракисфенилтио)фталоцианин алюминия получен, как описано в работе [Деркачева В.М., Лукьянец Е.А. // Журн. общ. Химии. 1980. Т.50. С.2313-2318]. Его хлорметилирование до тетракис[бис (хлорметил) фенилтио]фталоцианина алюминия проводили по известным методикам, приведенным, например, в патенте РФ №2405785 от 10.13.2010 г.
Предлагаемое изобретение иллюстрируется нижеприведенными примерами.
Пример 1
Синтез гетерогенного сенсибилизатора
Для химической прививки к аминопропилированному силикагелю взят тетракис [бис(хлорметил)фенилтио] фталоцианин алюминия Al(Cl)Pc(SPh)4(CH2Cl)8 (найдено %: Сl 20.02; вычислено %: Сl 20.59). Доказательством положения хлорметильных групп в фенильных кольцах служит сдвиг сигнала протонов в спектре 1Н ЯМР (5,0 м.д.), отличающийся от сдвига протонов СН2Сl групп, непосредственно связанных с фталоцианиновым кольцом (5,5-5,8 м.д.).
К 5·10-6 моль Al(Cl)Pc(SPh)4(CH2Cl)8 добавляют 20 мл диметилформамида и после растворения красителя 1 г промытого водой и высушенного при 100°С аминопропилированного силикагеля. Смесь перемешивают при нагревании и температуре 80-85°С в течение 1-2 часов до обесцвечивания раствора, затем добавляют 5·10-3 моля N,N-диметиламиноэтанола и нагревание продолжают еще в течение часа. Продукт отфильтровывают, промывают водой, затем сушат при температуре 100-105°С.
Электронный спектр поглощения суспензии гетерогенного сенсибилизатора в глицерине (4 г/л) указывает на преимущественно мономерное состояние активной фазы (хорошо разрешенный спектр с выраженной полосой поглощения Q при 715 нм и колебательным спутником при 650 нм, Фиг.1). Это должно обеспечить эффективную сенсибилизацию цитотоксических активных форм кислорода.
Пример 2
Определение активности гетерогенного сенсибилизатора, полученного по примеру 1, в фотоинактивации полиовируса в воде.
Экспериментальные исследования проводились в модельных водоемах, приготовленных с использованием фильтрованной автоклавированной водопроводной воды, в которую вносили гетерогенный сенсибилизатор в концентрации 4 г/л и полиовирус в концентрации n·104 ЦПД50/мл. После интенсивного перемешивания одна часть водоемов подвергалась освечиванию в течение 30, 60, 90 и 120 минут, а другая оставлялась в темноте в контакте с гетерогенным сенсибилизатором на это же время без освечивания и барботирования. Температура воды при освечивании проб составляла 20-24°С.
Исследовались следующие фракции.
1) Суспензия - 10 мл смеси надосадочной жидкости и гетерогенного сенсибилизатора.
2) Надосадочная жидкость в объеме 10 мл отбиралась после отстаивания в течение 5 минут для осаждения сенсибилизатора. Далее проба подвергалась антибактериальной обработке и использовалась для заражения клеточных культур.
3) Осадок. После отбора надосадочной жидкости и удаления ее остатков проводилась десорбция полиовируса с осадка при помощи 10 мл 3% раствора бифэкстракта с рН 9,1. Этот десорбент используется в вирусологических исследованиях для десорбции вирусов с различных адсорбентов в процессе концентрирования вирусов. Осадок с десорбентом тщательно встряхивали и отстаивали в течение 5 минут для осаждения сенсибилизатора. Затем надосадочную жидкость собирали и проводили корректировку рН до 7,0. Далее проба подвергалась антибактериальной обработке и использовалась для заражения клеточных культур.
Необходимость проведения десорбции была обусловлена следующим: во-первых, полиовирус, имея отрицательный заряд, должен сорбироваться на положительно заряженном гетерогенном сенсибилизаторе; во-вторых, использование непосредственно твердого осадка при титровании вируса на культуре клеток практически не представляется возможным.
Полученными пробами после антимикробной обработки заражали пробирки с монослоем клеток BGM. Наблюдение за появлением ЦПЭ проводилось в течение 2-х недель. Все отрицательные пробы исследовались во втором пассаже для подтверждения отсутствия вирусов, и затем проводился расчет титра вируса в пробе по методу Рида и Менка.
Данные об условиях и результатах фотообеззараживания полиовируса в пробе суспензии (10 мл смеси надосадочной жидкости и гетерогенного сенсибилизатора) приведены в таблице 1.
Данные таблицы 1 свидетельствуют о наличии высокого (4 порядка) снижения концентрации полиовируса при фотодинамической обработке воды с использованием предлагаемого гетерогенного сенсибилизатора.
Динамика изменения концентрации полиовируса в надосадочной жидкости и в осадке (десорбент с рН 9,1) в присутствии предлагаемого гетерогенного сенсибилизатора без освечивания представлена в таблице 2.
Как видно из таблицы 2, полиовирус через 30 мин контакта с частицами гетерогенного сенсибилизатора большей частью адсорбируется на нем, концентрация полиовируса в надосадочной жидкости на три порядка ниже. Далее установившееся равновесие мало зависит от времени контакта (30-90 минут).
В следующей серии исследований проводилось изучение фотообеззараживающего эффекта гетерогенного сенсибилизатора в отношении вирусов в тех же условиях при освечивании и барботировании. Результаты исследований представлены в таблице 3.
Как видно из табл.3, с увеличением времени освечивания концентрация полиовируса как в надосадочной жидкости, так и в осадке последовательно снижается, и через 120 мин облучения вирус не обнаруживается в обеих фракциях. Эти результаты свидетельствуют о том, что снижение концентрации вируса в воде в условиях облучения связано не только с адсорбцией на частицах гетерогенного сенсибилизатора, но и с его фотоинактивацией в фотодинамическом процессе.
Таким образом, можно отметить два фактора, за счет которых происходит снижение концентрации полиовируса в водоеме:
1) адсорбция полиовируса на частицах гетерогенного сенсибилизатора;
2) фотоинактивация полиовируса гетерогенным сенсибилизатором за счет генерации активных форм кислорода его активной фазой - химически привитым фталоцианином.
Пример 3
Определение активности гетерогенного сенсибилизатора, полученного по примеру 1, в фотоинактивации колифага в воде.
В экспериментах использовался колифаг MS2 (штамм ВКПМ РН 1505), который был получен из Всероссийской коллекции промышленных микроорганизмов ГУ НИИГенетика. Для выделения колифагов из исследуемых проб в качестве лизабельной культуры использовали штамм кишечной палочки ВКПМ В-3254, E.coli F+ К-12 KS 507, который был получен из Всероссийской коллекции промышленных микроорганизмов ГУ НИИ Генетика. Этот штамм позволяет выделять как дикие штаммы, циркулирующие в воде различных водоемов, так и модельный штамм MS-2. Колифаг на газоне суточной культуры E.coli через 24 часа образует литические пятна -бляшки (бляшкообразующие единицы). Концентрацию колифагов выражали в бляшкообразующих единицах (БОЕ). Исходная концентрация колифагов составляла n×104-n×105 БОЕ/мл. Время фотообеззараживания в экспериментах составляло 30, 60 и 90 минут. Исследование проб воды на наличие колифагов проводилось в соответствии с документом МУК 4.2.1018-01 «Санитарно-микробиологический анализ питьевой воды» с использованием двух методов: метода прямого посева и метода подращивания.
Проведенные исследования показали, что после совместного пребывания фотосенсибилизатора и колифагов в водной суспензии в темноте - в течение 30 минут концентрация колифагов оставалась на прежнем уровне. Эти данные свидетельствуют о том, что предлагаемый гетерогенный сенсибилизатор в концентрации 4 г/л токсического действия в отношении колифагов не оказывает. При облучении видимым светом уровень колифагов снижался.
Данные об условиях и результатах фотообеззараживания колифага в воде в присутствии гетерогенного фотосенсибилизатора приведены в таблице 4.
Как видно из материалов таблицы 4, при исходной концентрации колифагов на уровне 20000 БОЕ/мл, после фотообеззараживания воды в течение 30 минут колифаги выделялись из 1,0 мл пробы на уровне 28-80 БОЕ/мл. Таким образом, фотообеззараживание сопровождалось интенсивным снижением концентрации колифагов в надосадочной жидкости на 3 порядка, при этом процент инактивации колифага составлял 99,6-99,86%.
При изучении осадка установлено, что концентрация колифагов в нем была на порядок выше, чем в водной фазе, и составляла 600 БОЕ/мл. Таким образом, освечивание пробы в течение 30 минут не достаточно для инактивации колифагов, а снижение уровня его концентрации в водной фазе происходит не только за счет фотообеззараживающего эффекта, но и за счет сорбции на частицах фотосенсибилизатора.
При увеличении времени освечивания до 60 минут концентрация колифагов в водной фазе снижается еще на один порядок, достигая единичных бляшкообразующих единиц в 1 мл исследуемой воды (0-4 БОЕ/мл). Уровень инактивации при данных условиях эксперимента достигал 99,98-100%. При исследовании осадка было установлено, что концентрация колифагов в нем была на два порядка выше, чем в водной фазе пробы, и составляла 150-200 БОЕ/мл, уровень инактивации достигал 99,25-99%.
При освечивании пробы в течение 90 минут из водной фазы пробы колифаг не высевался и уровень инактивации достигал 100%. При исследовании осадка высевались единичные колифаги, уровень инактивации при этом составлял 99,99-99,995%.
Полученные данные свидетельствуют о двухстадийном механизме очистки воды от колифага при использовании предлагаемого гетерогенного сенсибилизатора - сорбция и фотодинамическое обеззараживание сорбированного колифага.
Таким образом, примеры 2 и 3 показывают, что гетерогенный сенсибилизатор, содержащий в качестве активной фазы тетракис[бис(холинил) фенилтио]фталоцианин алюминия, ковалентно пришитый к аминопропилированному силикагелю, является активным в фотоинактивации вирусного заражения водной среды. Полученные данные экспериментальных исследований показали, что очистка воды в отношении вирусов, заряженных отрицательно, при использовании предлагаемого гетерогенного сенсибилизатора связана с двухстадийным механизмом - сорбция и фотодинамическое обеззараживание сорбированного вируса. Это весьма перспективно по использованию его для очистки воды.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБЕЗЗАРАЖИВАНИЯ ВОДЫ И ОЦЕНКИ ЕГО ЭФФЕКТИВНОСТИ | 2012 |
|
RU2520857C2 |
| ГЕТЕРОГЕННЫЙ СЕНСИБИЛИЗАТОР И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2010 |
|
RU2447027C1 |
| ГЕТЕРОГЕННЫЙ СЕНСИБИЛИЗАТОР И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2013 |
|
RU2538261C2 |
| СЕНСИБИЛИЗАТОР И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2008 |
|
RU2375371C1 |
| СЕНСИБИЛИЗАТОР И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2010 |
|
RU2448135C1 |
| СПОСОБ ФОТОИНАКТИВАЦИИ ВИРУСА ГРИППА А ПТИЦ ПОДТИПА H5N1 | 2007 |
|
RU2357770C1 |
| СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2008 |
|
RU2358909C1 |
| КВАТЕРНИЗОВАННЫЕ ФТАЛОЦИАНИНЫ И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2005 |
|
RU2281953C1 |
| СПОСОБ КОНЦЕНТРАЦИИ ВИРУСОВ ИЗ ЖИДКИХ СРЕД | 2007 |
|
RU2349643C2 |
| ГЕТЕРОГЕННЫЕ СЕНСИБИЛИЗАТОРЫ И СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ АРОМАТИЧЕСКИХ АМИНОВ И ФЕНОЛОВ | 2011 |
|
RU2471715C2 |
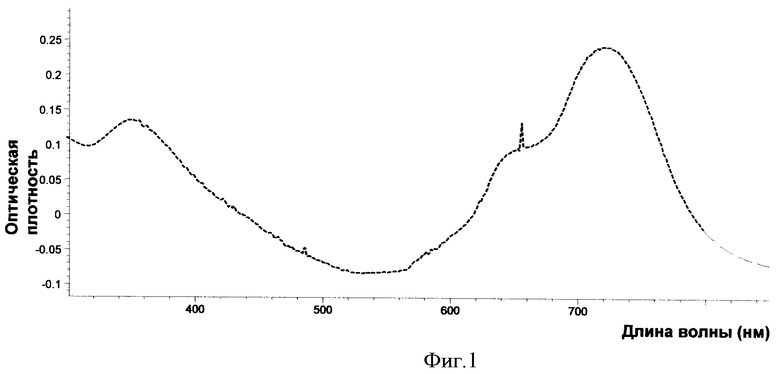
Изобретение относится к химии и химической технологии, а именно к новым гетерогенным сенсибилизаторам, представляющим собой модифированные силикагели, и их использованию для фотообеззараживанию воды от вирусного загрязнения. Предложен гетерогенный сенсибилизатор формулы:
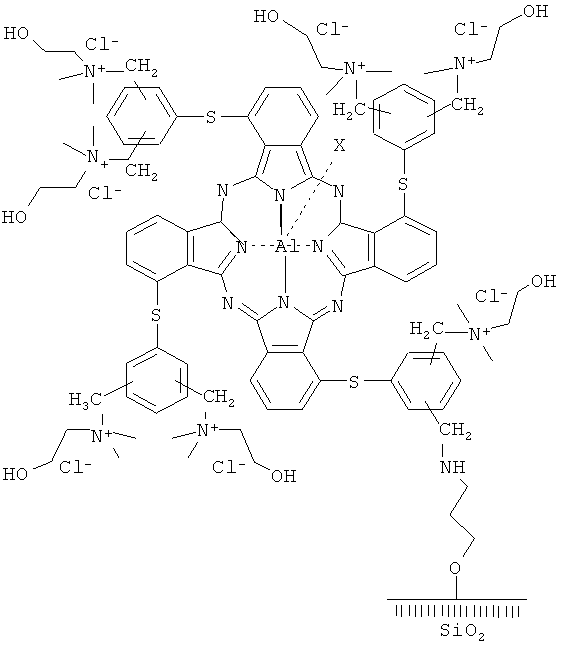 , где Х=Сl(ОН). Предложен также способ обработки воды с использованием этого гетерогенного сенсибилизатора. Предложенный способ обеспечивает эффективную очистку воды от вирусного загрязнения. 2 н.п. ф-лы, 1 ил., 4 табл., 3 пр.
, где Х=Сl(ОН). Предложен также способ обработки воды с использованием этого гетерогенного сенсибилизатора. Предложенный способ обеспечивает эффективную очистку воды от вирусного загрязнения. 2 н.п. ф-лы, 1 ил., 4 табл., 3 пр.
1. Гетерогенный сенсибилизатор формулы
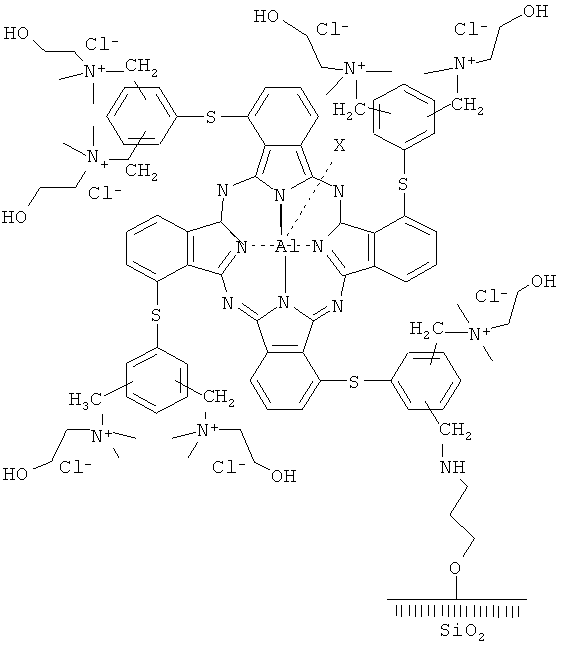
где Х - Сl(ОН).
2. Способ фотообеззараживания воды от вирусного загрязнения с использованием сенсибилизатора и излучения видимого диапазона в присутствии кислорода, отличающийся тем, что в качестве сенсибилизатора используют гетерогенный сенсибилизатор по п.1.
| СЕНСИБИЛИЗАТОР И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2008 |
|
RU2375371C1 |
| СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2002 |
|
RU2235688C2 |
| КВАТЕРНИЗОВАННЫЕ ФТАЛОЦИАНИНЫ И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2005 |
|
RU2281953C1 |
| ФОТОСЕНСИБИЛИЗАТОРЫ | 1994 |
|
RU2159612C2 |
| WO 9705203 A1, 13.02.1997. | |||
Авторы
Даты
2012-12-20—Публикация
2011-07-06—Подача