Изобретение относится к области медицины, а именно вирусологии и биотехнологии, и может быть использовано для концентрации вирусов из воды, водных растворов, биологических сред; для выявления вирусов в воде питьевой, сточной, воде открытых водоемов, которые используются как источники водоснабжения, водопроводной воде, воде подземных источников, питьевой воде бутылированной, воде морской и пресных водоемов, которые используются для рекреационных целей, воде плавательных бассейнов; для очистки вирусных суспензий, используемых для изготовления вирусных антигенов и вакцин, очистки вирусов, полученных из тканевых культур, от клеточного детрита.
Известен способ концентрации энтеровирусов из водопроводной и речной воды при помощи ионообменных смол АВ-17, АВ-17-8, АВ-17-2П, 1К (искусственные сорбенты, представленные анионитами, а именно аминосмолами, полученными из формальдегида с мочевиной, анилином, гуанидином). / Методические рекомендации по санитарно-вирусологическому контролю объектов окружающей среды. // Москва, 1982, 75 с., п.3.1.3.2, - с.14/. Концентрация вирусов при помощи ионообменных смол осуществляется следующим образом. Сухую ионообменную смолу замачивают в течение 3 суток в дистиллированной воде. Потом воду сливают и смолу обрабатывают смесью равных по объему, приготовленных непосредственно перед использованием растворов 2% HCl и 10% NaCl. Продолжительность обработки 24 часа. После этого смолу отмывают дистиллированной водой до нейтрального рН=7,0. Перед концентрацией рН исследуемой пробы воды (5 или 10 л) доводят до значений 5,5-6,0. Затем заполняют колонку диаметром 1,2-1,3 см подготовленным слоем сорбента толщиной 10-12 см. Колонку уравновешивают раствором суспензии смолы с рН=5,6-6,0. Пробу воды (5 л) пропускают через колонку со скоростью 10-12 мл/мин. Продолжительность концентрации - 12-16 ч. После завершения концентрации осуществляют десорбцию вирусов из смолы при помощи фосфатного буфера. Недостатками этого способа являются длительность подготовки сорбента, дополнительное использование колонки, продолжительность процесса концентрации - 12-16 ч, использование большого объема воды - 5 л.
Наиболее близким к заявляемому способу является способ концентрации вирусов из воды при помощи природных сорбентов, а именно 5% геля бентонита (Широбоков В.П., Гирин В.Н., Якименко А.И. и др. Применение бентонита для выявления энтеровирусов у человека и во внешней среде. // Методические рекомендации. Киев, 1986, 23 с.) Схема концентрации энтеровирусов из водной среды представлена в таблице 1. Способ осуществляется следующим образом. Сухой бентонит диспергируют в деионизированной воде. Для преобразования бентонита в натриевую форму к суспензии добавляют углекислый натрий. Смесь оставляют на сутки при комнатной температуре для набухания, после чего смесь кипятят в течение 1 часа. Охлажденную смесь центрифугируют 10 минут при 3000 об/мин, надосадочную жидкость сливают, а осадок ресуспендируют в 1 л дистиллированной воды и центрифугируют при 4000 об/мин в течение 20 минут. Надосадочную жидкость удаляют. Отбирают приблизительно 2/3 верхней части осадка, содержащей суспензию геля бентонита, остаток суспензии ресуспендируют в 1 л деионизированной воды и снова центрифугируют в течение 20 минут при 4000 об/мин. Отмытый осадок бентонита заливают 3 л воды и встряхивают в штудтельаппарате 3-4 часа. После этого суспензию центрифугируют в течение 5 минут при 1000 об/мин, 2/3 верхней части осадка отбирают, еще раз суспендируют в воде, надосадок декантируют. Отбирают 2/3 однородной части геля бентонита, которую суспендируют в 0,14 М раствора хлористого натрия и снова осаждают, как указано выше. Фракционирование повторяют трижды, увеличивая продолжительность центрифугирования и удаляя нижнюю часть осадка. После такой обработки бентонит представляет собой мелкодисперсную суспензию. Ее суспендируют в 95 объемах деионизированной воды, получая 5% суспензию геля бентонита. Полученный гель автоклавируют при 136°С в течение 20 минут. Срок хранения такого геля не ограничен. Полученный 5% гель бентонита используют для концентрации вирусов из воды, водных растворов, культуральной жидкости.
Схема концентрации вирусов из водной среды
2) вносят 0,5 мл 5% геля бентонита;
3) вносят 1 М HCl раствор до рН=4,5-5,0;
4) встряхивание 4-5 мин;
5) центрифугирование при 1000 об/мин 7-10 мин
2) встряхивание 4-5 мин;
3) центрифугирование при 3000 об/мин 7-10 мин;
2) встряхивание 4-5 мин;
3) центрифугирование при 3000 об/мин 7-10 мин;
4) отбирают элюат, деконтаминируют и исследуют на наличие в нем вирусов или вирусных антигенов.
Известный способ включает помещение сорбента в пробу жидкой среды, выдерживание временного интервала с последующим центрифугированием исследуемой пробы, удаление надосадочной жидкости, получение комплекса вирус + сорбент и последующую элюцию вирусов. Недостатками способа являются продолжительность и трудоемкость приготовления геля бентонита, нестандартизированностъ сорбента, которая зависит от места его добычи.
В основу изобретения поставлена задача усовершенствования способа концентрации вирусов из жидких сред, в котором применение гидрогеля метилкремниевой кислоты сокращает продолжительность и трудоемкость способа и повышает процент выявления вирусов при исследовании различных жидких сред.
Поставленная задача решается тем, что в способе концентрации вирусов из жидких сред, который включает помещение сорбента в пробу жидкой среды, выдерживание временного интервала с последующим центрифугированием исследуемой пробы, удаление надосадочной жидкости, получение комплекса вирус + сорбент и последующую элюцию вирусов, согласно изобретению в качестве сорбента используют гидрогель метилкремниевой кислоты (ГГМКК), который обладает адсорбционными свойствами по отношению к биологическим объектам вирусной природы, временной интервал выдерживают от 20 минут до 24 часов при температуре от +4°С до +22°С, а получение комплекса вирус + сорбент осуществляют без проведения этапа обессоливания.
Согласно изобретению ГГМКК, способный в концентрации не менее 30 мг/мл адсорбировать не менее 96% вирусных частиц из водных сред, помещают в пробу водной среды, при этом исследуемую пробу подкисляют раствором кислоты до рН=5,0.
Согласно изобретению ГГМКК, который способен в концентрации не менее 2 мг/мл адсорбировать не менее 90% вирусных частиц из биологических сред, помещают в пробу биологической среды.
Заявители изобретения являются изобретателями и заявителями способа получения сорбента на основе гидрогеля метилкремниевой кислоты (заявка № а 2006 10083), в котором, благодаря новому способу получения, указанный сорбент имеет объем пор не менее 0,8 см3/г и обладает высокой адсорбционной активностью в отношении веществ с большой молекулярной массой (5-900 кД) и различных биологических объектов, в том числе вирусной природы. Гидрогель метилкремниевой кислоты - это новый эффективный сорбент, который имеет глобулярную структуру пористой кремнийорганической матрицы. На ее поверхности присутствуют гидроксильные группы, благодаря чему поверхность глобул и пор активно сольватируется полярными молекулами воды, и метильные группы, обусловливающие гидрофобные свойства и сродство к тканям и биосубстратам организма. Сорбент ГГМКК безопасен, имеет высокую селективность, адсорбционная емкость по конго красному достигает 3,0-3,5 мг/г (или 4,5-5,0 мкмоль/г). Используется как сорбент в различных отраслях медицины и ветеринарии.
Цель изобретения состоит в повышении эффективности концентрации вирусов из проб жидких сред, уменьшении стадий в процедуре выполнения, сокращении времени концентрации, создании возможности концентрации вирусов из минимальных объемов жидких сред, использовании для концентрации готового вещества (сорбента), состав и качество которого гарантируется соответствующими ФС и ТУ.
Способ осуществляется следующим образом. ГГМКК, полученный способом, заявленным в № а 2006 10083, имеющий адсорбционные свойства относительно биологических объектов вирусной природы, помещают в пробу жидкой среды, выдерживают от 20 минут до 24 часов при температуре от +4°С до +22°С. ГГМКК, способный в концентрации 30 мг/мл адсорбировать не менее 96% вирусных частиц из водной среды, помещают в пробу водной среды, а также в пробу биологической среды, загрязненные вирусами. Проводят адсорбцию вирусов, после чего ГГМКК концентрируют центрифугированием и удаляют надосадочную жидкость. Затем осуществляют элюцию вирусов и отделяют ГГМКК от раствора центрифугированием. В надосадочной жидкости осуществляют индикацию и идентификацию вирусов.
Пример 1. Концентрация вирусов из проб сточной воды.
Способ осуществляется как описано в п.п.1.2, при этом пробу воды (500 мл предварительно осветленной сточной воды) подкисляют при помощи 1 М HCl до рН=5,0, в подкисленную пробу помещают сорбент ГГМКК в количестве 1 г и выдерживают 20 минут при температуре 20°С. После экспозиции пробу с сорбентом центрифугируют при 1000 об/мин. в течение 20 минут. Надосадочную жидкость удаляют и получают комплекс вирус + сорбент, процесс обессоливания отсутствует.
Пример 2. Концентрация вирусов из проб питьевой воды.
Способ осуществляется как описано в п.п.1.2, при этом пробу воды подкисляют при помощи 1 М HCl до рН=5,0, в подкисленную пробу (10 л питьевой воды) помещают сорбент ГГМКК в количестве 20 г и выдерживают до 20 часов при температуре 20°С, надосадок осторожно сливают через край, оставляя на дне стеклянного сосуда 200 мл неплотного белого осадка. Полученный осадок (осадок + небольшое количество надосадка) встряхивают и переносят в стаканы или флаконы для центрифугирования по 250 мл и центрифугируют при 1000 об/мин в течение 20 минут. Образовавшийся белый осадок также не плотный, поэтому надосадочную жидкость снова сливают через край, оставляя на дне флакона 20 мл. Этот осадок встряхивают, переносят в две пробирки для центрифугирования и повторно центрифугируют. После второго центрифугирования плотный осадок формируется на дне пробирок, надосадочную жидкость удаляют пастеровской пипеткой и получают комплекс вирус + сорбент, процесс обессоливания отсутствует.
Пример 3. Концентрация вирусов из проб воды открытых водоемов и подземных источников.
Способ осуществляется как описано в п.п.1.2, при этом пробу воды (2 л) подкисляют при помощи 1 М HCl до рН=5,0, в подкисленную пробу помещают сорбент ГГМКК в количестве 4 г и выдерживают до 20 минут при температуре 20°С. После экспозиции пробу с сорбентом центрифугируют при 1000 об/мин в течение 20 минут. Надосадочную жидкость удаляют и получают комплекс вирус + сорбент, процесс обессоливания отсутствует.
Пример 4.1. Концентрация вирусов из проб культуральной жидкости.
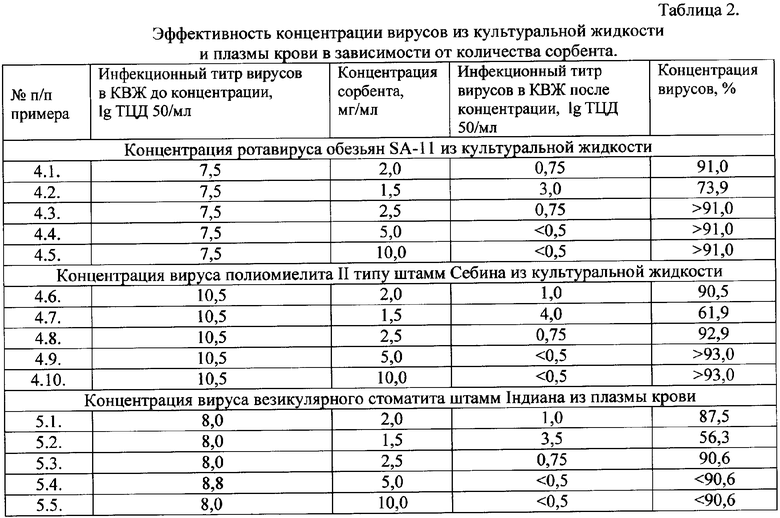
Способ осуществляется как описано в п.п.1.3, при этом в культуральную вирусосодержащую жидкость (КВЖ), содержащую ротавирус обезьян SA-11 с инфекционным титром 7,5 lg ТЦД50/мл, добавляют сорбент ГГМКК из расчета 2 мг на 1 мл жидкости. Формирование комплекса ротавирус + сорбент осуществляют при температуре 20°С в течение 10 часов, периодически перемешивая. Образовавшийся комплекс ротавирус + сорбент выделяют низкоскоростным центрифугированием. В надосадочной жидкости отсутствие вируса контролируют, определяя инфекционный титр ротавируса титрованием по ЦПД в чувствительной культуре клеток. Результаты осуществления способа представлены в таблице 2.
Пример 4.2.
Способ выполняют как в примере 4.1, но ГГМКК помещают в культуральную жидкость из расчета 1,5 мг/мл. Результаты выполнения способа представлены в таблице 2.
Пример 4.3.
Способ выполняют как в примере 4.1, но ГГМКК помещают в культуральную жидкость из расчета 2,5 мг/мл. Результаты выполнения способа представлены в таблице 2.
Пример 4.4.
Способ выполняют как в примере 4.1, но ГГМКК помещают в культуральную жидкость из расчета 5,0 мг/мл. Результаты выполнения способа представлены в таблице 2.
Пример 4.5.
Способ выполняют как в примере 4.1, но ГГМКК помещают в культуральную жидкость из расчета 10 мг/мл. Результаты выполнения способа представлены в таблице 2.
Примеры 4.6-4.10.
Способ выполняют как в примерах 4.1-4.5, но используют культуральную жидкость, которая содержит вирус полиомиелита II типа штамм Себина с инфекционным титром 10,5 lg ТЦД50/мл. Результаты выполнения способа представлены в таблице 2.
Примеры 5.1-5.5. Концентрация вирусов из проб плазмы крови человека.
Способ осуществляют как в п.3 и примерах 4.1.-4.5, но вместо вирусосодержащей жидкости используют плазму крови человека, которая содержит вирус везикулярного стоматита (ВВС), штамм Индиана. Результаты осуществления способа представлены в таблице 2.
Пример 6. Способ концентрации вирусов-колифагов из проб питьевой воды.
Способ осуществляется как описано в п.п.1.2 и в примере 2, только концентрируемые вирусы являются колифагами Т2 (бактериофаг эшерихии Т2), а ГГМКК вносят из расчета 50 мг/мл. После экспозиции пробу с сорбентом центрифугируют при 1000 об/мин в течение 20 минут, надосадочную жидкость удаляют и получают комплекс колифаг Т2 + сорбент, процесс обессоливания отсутствует.
Примеры осуществления способа с элюцией вирусов.
Пример 7.1.
Способ осуществляют как в примере 4.1., но удаленный низкоскоростным центрифугированием комплекс «ротавирус SA-11 + сорбент» помещают в раствор 0,14 М фосфатно-солевого буфера (ФСБ) с рН=8,5, объем которого в 10 раз меньше объема КВЖ, из которой был адсорбирован ротавирус. Полученную суспензию интенсивно встряхивают в течение 10 минут при температуре 20°С и оставляют в тех же условиях для десорбции еще на 20 минут. Сорбент удаляют низкоскоростным центрифугированием. Супернатантную жидкость, содержащую ротавирус, отбирают в стерильную пробирку, доводят ее рН до 7,2-7,4 1 М раствором HCl, и деконтаминируют. Инфекционный титр ротавируса в полученном супернатанте определяют по ЦПД титрованием микрометодом в культуре клеток НЕР-2. Одновременно, в этих же условиях титруют и образцы КВЖ, из которой адсорбируют ротавирус. Титрование повторяют в трех параллельных опытах. Титрование каждого образца проводят в 4 рядах лунок 96-лункового культурального планшета. Инфекционный титр ротавируса в культуральной жидкости и в образцах элюата рассчитывают по методу Кербера. Результаты выполнения способа представлены в таблице 3.
Пример 7.2.
Способ осуществляют как в примере 7.1, но элюцию проводят при рН=8,0. Результат выполнения способа представлен в таблице 3.
Пример 7.3.
Способ осуществляют как в примере 7.1, но элюцию проводять при рН=9,0. Результат виполнения способа представлен в таблице 3.
Пример 7.4.
Способ осуществляют как в примере 7.1, но элюцию проводят при рН=9,3. Результат выполнения способа представлен в таблице 3.
Пример 7.5.
Способ осуществляют как в примере 7.1, но элюцию проводят в 0,05 М трис-буферном растворе при рН=8,5. Результаты выполнения способа представлены в таблице 3.
Пример 7.6.
Способ осуществляют как в примере 7.5, но элюцию проводят при рН=8,0. Результаты выполнения способа представлены в таблице 3.
Пример 7.7.
Способ осуществляют как в примере 7.5, но элюцию проводят при рН=9,0. Результаты выполнения способа представлены в таблице 3.
Пример 7.8.
Способ осуществляют как в примере 4.6, но выделенный низкоскоростным центрифугированием комплекс «вирус полиомиелита II типа штамм Себина + сорбент» помещают в раствор 0,14 М фосфатно-солевого буфера с рН=8,5, объем которого в 10 раз меньше объема КВЖ, из которой был адсорбирован полиовирус. Полученную суспензию интенсивно встряхивают в течение 10 минут при температуре 20°С и оставляют в тех же условиях для десорбции еще на 20 минут. Сорбент удаляют низкоскоростным центрифугированием. Супернатантную жидкость, содержащую полиовирус, отбирают в стерильную пробирку, доводят ее рН до 7,2-7,4 1 М раствором HCl и деконтаминируют. Инфекционный титр полиовируса в полученном супернатанте определяют по ЦПД титрованием микрометодом в культуре клеток НЕР-2. Одновременно, в тех же условиях титруют и образцы КВЖ, из которой адсорбировали полиовирус. Титрование повторяют в трех параллельных опытах. Титрование каждого образца виполняют в 4 рядах лунок 96-лункового культурального планшета. Инфекционный титр полиовируса в культуральной жидкости рассчитывают по методу Кербера. Результаты выполнения способа представлены в таблице 3.
Пример 7.9.
Способ виполняют как в примере 7.8, но элюцию проводят в 0,05 М трис-буферном растворе при рН=8,5. Результаты виполнения способа представлены в таблице 3.
Пояснение. Элюцию вируса везикулярного стоматита из комплекса «вирус + сорбент» не проводили, поскольку цель состояла в максимальном очищении плазмы крови от вируса, а не в его концентрировании, в этом случае поиск условий десорбции ВВС не нужен.
Предлагаемый способ обеспечивает сокращение стадий в процессе выполнения, уменьшение времени концентрирования, возможность концентрации вирусов из минимальных объемов жидких сред, благодаря чему увеличивается точность и повышается процент выявления вирусов при исследовании различных жидких сред.
Эффективность элюции (десорбции) вирусов из комплексов «вирус + сорбент» в буферных растворах при различных значениях их ионной силы (рН).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ротавирусных антигенов | 1989 |
|
SU1700054A1 |
| СПОСОБ ВЫЯВЛЕНИЯ КИШЕЧНЫХ ВИРУСОВ В ВОДЕ | 2010 |
|
RU2444011C1 |
| Штамм ротавируса человека для получения иммунобиологических препаратов | 1989 |
|
SU1687613A1 |
| Способ хроматографической очистки экзосом и их разделения от вирионов вируса гриппа А на основе гидрофобного взаимодействия с сорбентом | 2022 |
|
RU2803848C1 |
| Способ выделения РНК и ДНК из сухих биологических образцов, хранившихся на бумажном носителе, и набор для его осуществления | 2016 |
|
RU2628695C1 |
| Способ инактивации культурального ротавируса человека | 2020 |
|
RU2743300C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2007 |
|
RU2359269C2 |
| КОМПЛЕКСНЫЙ АНТИГЕН ВИРУСА КОРИ, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ КОМПОНЕНТА ИММУНОФЕРМЕНТНОЙ ТЕСТ-СИСТЕМЫ ДЛЯ ДИАГНОСТИКИ АНТИТЕЛ К ВИРУСУ КОРИ | 2010 |
|
RU2441666C1 |
| СПОСОБ ПРОИЗВОДСТВА ПРЕПАРАТА НА ОСНОВЕ НЕРЕПЛИЦИРУЮЩЕГОСЯ ВИРУСНОГО ВЕКТОРА, ЭКСПРЕССИРУЮЩЕГО ГЕН ЧЕЛОВЕЧЕСКОГО TOLL-ПОДОБНОГО РЕЦЕПТОРА И ГЕН МОДИФИЦИРОВАННОГО БЕЛКА ФЛАГЕЛЛИНА | 2015 |
|
RU2590588C1 |
| Способ получения вакцин против лейкоза крупного рогатого скота | 1977 |
|
SU820015A1 |
Изобретение относится к области биотехнологии и касается способа концентрации вирусов из жидких сред. Способ включает адсорбцию вируса на гидрогеле метакриловой кислоты в концентрации не менее 2,0 мг/мл, сорбции при рН 5,0 от 20 минут до 24 часов при температуре от 4°С до 22°С и далее комплекс вирус-сорбент центрифугируют и вирус элюируют. Преимущество изобретения заключается в сокращении числа стадий и уменьшении времени концентрирования. 1 з.п. ф-лы, 3 табл.
| Широбоков В.П | |||
| и др | |||
| Применение бентонита для выявления энтеровирусов у человека во внешней среде | |||
| Методические рекомендации | |||
| - Киев, 1986 | |||
| Способ выделения из воды вирусов | 1989 |
|
SU1742333A1 |
| Способ концентрирования суспензии вируса Марбург | 1990 |
|
SU1747486A1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ ВИРУСОВ | 1989 |
|
SU1834289A1 |
| КРАСИЛЬНИКОВ И.В | |||
| и др., Выделение вирусов из воды с использованием пористых кремнеземов | |||
| - Вопр | |||
| Вирусол., 1985, 30 (2), с.608. | |||
Авторы
Даты
2009-03-20—Публикация
2007-01-22—Подача