По данной заявке испрашивается приоритет на основании предварительной заявки США с серийным № 60/938089, зарегистрированной 15 мая 2007 года, которая включена в данное описание в виде ссылки.
Область техники, к которой относится изобретение
Данное изобретение относится к способу применения антагонистов вазопрессина для снижения кардиальной токсичности и/или улучшения выживаемости пациентов, леченных антрациклиновыми химиотерапевтическими средствами, такими как доксорубицин (адриамицин®), включающему введение пациенту терапевтически эффективного количества композиции, содержащей в качестве активного ингредиента соединение-антагонист вазопрессина, одновременно или перед введением антрациклина, и к композициям, применимым для этого.
Уровень изобретения
Антрациклиновые средства являются противоопухолевыми и используются в химиотерапии для лечения человека, имеющего гематогенные или твердые злокачественные новообразования широкого спектра, включающие рак молочной железы и лейкоз. Однако применение антрациклинов, таких как доксорубицин (адриамицин®), ограничено кумулятивным и дозозависимым миокардиальным повреждением, которое может вести к застойной сердечной недостаточности (CHF).1,2 Было подсчитано, что у вплоть до 20% пациентов, леченных доксорубицином, может проявиться CHF.3
Кроме кумулятивной дозы, возраст, комбинированная терапия, гипертензия, заболевание печени, излучение от грудных стенок от предшествующего лечения рака и предшествующее сердечное заболевание представляют собой дополнительные факторы риска для CHF, вызываемой доксорубицином.4
Вопреки его известной кардиотоксичности доксорубицин является одним из самых широко используемых химиотерапевтических средств для продления жизни раковых пациентов благодаря его эффективности. Было подсчитано, более чем 50% из оставшихся на длительный срок живых от рака в детстве были пролечены доксорубицином или другим антрациклином.5 Однако многие из выживших, которые были пролечены доксорубицином, имеют долговременные проблемы, часто проявляемые как сердечные заболевания. Они часто присутствуют как изменения в ЭКГ и аритмии, или как кардиомиопатия, приводящая к CHF, а также к повышенному риску внезапной смерти и смерти от сердечных причин.6
Кардиотоксичность, вызываемая доксорубицином, связана с совокупной продолжительной дозой доксорубицина для пациента. CHF характеризуется сниженной способностью сердца прокачивать кровь, приводящей к удерживанию жидкости и вредной для здоровья нейрогормональной активации. Оставленные не пролеченными, пациенты с CHF имеют очень высокую степень смертности. Механизм, лежащий в основе данной кардиотоксичности, вызываемой доксорубицином, не ясен. Единственная эффективная стратегия снижения кардиотоксичности доксорубицина состоит в том, чтобы ограничивать воздействие доксорубицина. Но это также ограничивает эффективность доксорубицина для лечения рака.
Декстразоксан (цинекард®) в настоящее время представляет собой единственное разрешенное лекарственное средство лечения для снижения кардиотоксичности, вызываемой антрациклинами, с очень ограниченными преимуществами.6-8 Таким образом, существует срочная неудовлетворенная медицинская потребность в том, чтобы создать терапии, которые способны снижать кардиотоксичность, вызываемую доксорубицином. Снижение токсичности предоставит возможность безопасно вводить раковым пациентам более высокие дозы доксорубицина.
Вазопрессин (также известный как антидиуретический гормон (ADH)) представляет собой небольшой пептид из девяти аминокислот, синтезируемый в супраоптическом и паравентрикулярном ядрах гипоталамуса и сохраняемый в задней доли гипофиза. Его высвобождение регулируется осмолярностью плазмы и объемом/давлением крови.9 Вазопрессин вызывает вазоконстрикцию через V1 рецепторы в клетках гладких мышц сосудов и удерживание воды через V2 рецепторы в собирательных трубках почек.10
Уровни вазопрессина часто повышены у раковых пациентов.11-14 Гипонатремия, обусловленная аномально высокими уровнями вазопрессина, является также очень типичной для пациентов с раком.12,15 Кроме того, высокие уровни сывороточного вазопрессина, как показано, коррелируют с низкой степенью выживаемости пациентов с мелкоклеточным раком легкого,16 указывая на вредную роль вазопрессина у раковых пациентов.
Исследованиями показано, что доксорубицин может повышать уровень вазопрессина. У крыс, обработанных доксорубицином, экспрессия вазопрессина и аквапорина-2 водных каналов, которые транспортируют воду от собирательной трубки в почке в систему кровообращения, повышается.17 Кроме того, кролики, обработанные доксорубицином, имеют повышенную чувствительность к вазопрессину.18
Накопленные данные дают основание предполагать, что вазопрессин может играть важную роль в развитии и прогрессировании CHF: уровни вазопрессина и аквапорин-2 водных каналов повышены при CHF19-22 и V2 антагонисты показали преимущества в уменьшении застоя и улучшении симптомов в субъектах с CHF.23,24 Удерживание воды и системный отек представляют собой признаки CHF.
Ранее, в нескольких исследованиях исследовался потенциал антагонистов вазопрессина для снижения кардиального повреждения, вызываемого доксорубицином, и для стимулирования выживания экспериментальных животных. Было установлено, что антагонисты вазопрессина могут ослаблять симптомы CHF18, вызванные инъекцией доксорубицина. Однако в предшествующем исследовании ОРС-31260, антагонист V2 рецептора вазопрессина обладал слабым, но не значительным снижением степени смертности среди крыс, обработанных доксорубицином.25 Таким образом, хотя данные исследования показали общие полезные результаты антагонистов вазопрессина в лечении токсичности, вызываемой доксирубицином, эти эффекты были несущественными. В данных предыдущих исследованиях, антагонисты вазопрессина давались несколько недель после введения доксорубицина. Таким образом, перманентное миокардиальное повреждение возможно уже происходило перед началом терапии антагонистом вазопрессина. Важно, что модели в данных предыдущих исследованиях не могли точно воспроизводить окружающую среду с повышенным вазопрессином, которая часто находится у раковых пациентов, так как были использованы крысы только с нормальным здоровьем. Экспериментальная модель с повышенным вазопрессином может быть идеальной для оценки терапевтического потенциала V2 антагонистов.
Сущность изобретения
Авторы изобретения установили, что соединения-антагонисты вазопрессина являются эффективными для снижения кардиотоксичности и/или улучшения выживаемости субъектов, леченных антрациклинами, такими как доксорубицин, химиотерапевтическими обработками, если антагонисты вазопрессина вводят одновременно с или до введения антрациклина.
Таким образом, данное изобретение относится к способу снижения кардиотоксичности и/или улучшения выживаемости, включающему введение соединения-антагониста вазопрессина одновременно с или перед введением антрациклинового агента, такого как доксорубицин, пациенту, нуждающемуся в этом. Способы и композиции данного изобретения могут быть использованы для снижения побочных эффектов, связанных с химиотерапией, таких как кардиальное повреждение, особенно сердечная недостаточность. Способы и композиции данного изобретения могут быть также использованы для улучшения выживаемости при лечении доксорубицином.
Авторы изобретения также установили, что вазопрессин повышает уровень смертности субъектов, леченных антрациклинами, такими как доксорубицин. Таким образом, соединения-антагонисты вазопрессина могут быть особенно применимы и эффективны для пациентов, леченных доксорубицином, с повышенным вазопрессином.
Таким образом, данное изобретение включает следующие различные варианты осуществления.
В первом варианте осуществления данное изобретение относится к способу снижения кардиотоксичности и/или улучшения выживаемости после противоопухолевого лечения антрациклинами, включающему введение пациенту терапевтически эффективного количества композиции, содержащей соединение-антагонист вазопрессина или его фармацевтически приемлемую соль в качестве активного ингредиента, одновременно с или перед введением антрациклинового агента.
Во втором варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления для снижения кардиотоксичности.
В третьем варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления для улучшения выживаемости.
В четвертом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой соединение, изображаемое формулой (I), или его фармацевтически приемлемую соль.
В пятом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина выбран из группы, включающей, но без ограничения перечисленным, толваптан, мозаваптан, кониваптан, ликсиваптан, сатаваптан, RWJ-351647, RWJ-339489, SSR-149415, YM-222546, YM-471, YM-35471, YM-218, FR-218944, JNJ-17079166, JNJ-17308616, VMAX-367, VMAX-382, VMAX-372, ORG-52186, SRX-251 и их фармацевтически приемлемые соли.
В шестом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой V2 селективный вазопрессиновый антагонист или V1/V2 вазопрессиновый антагонист.
В седьмом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антрациклин включает даунорубицин, доксорубицин, эпирубицин и идарубицин совместно.
В восьмом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой толваптан.
В девятом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой гидрохлорид мозаваптана.
В десятом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой гидрохлорид кониваптана.
В одиннадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой ликсиваптан.
В двенадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой сатаваптан.
В тринадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой доксорубицин.
В четырнадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой даунорубицин.
В пятнадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой эпирубицин.
В шестнадцатом варианте осуществления данное изобретение относится к способу согласно первому варианту осуществления, в котором антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой идарубицин.
В семнадцатом варианте осуществления данное изобретение относится к фармацевтической композиции, содержащей соединение-антагонист вазопрессина или его фармацевтически приемлемую соль, для снижения кардиотоксичности и/или улучшенного выживания от антрациклиновой химиотерапии для введения одновременно или перед введением антрациклина.
В восемнадцатом варианте осуществления данное изобретение относится к фармацевтической композиции, содержащей терапевтически эффективное количество соединения-антагониста для вазопрессина или его фармацевтически приемлемой соли и терапевтически эффективное количество антрациклина.
В девятнадцатом варианте осуществления данное изобретение относится к применению соединения-антагониста вазопрессина или его фармацевтически приемлемой соли для приготовления лекарственного средства для снижения кардиотоксичности и/или улучшенного выживания от антрациклиновой химиотерапии для введения одновременно или перед введением антрациклина.
Краткое описание чертежей
На фигуре 1 представлены результаты анализа выживания по Каплан-Мейеру с помощью лог-ранк теста на крысах, обработанных толваптаном.
На фигуре 2 представлен график, показывающий результаты лечения толваптаном, начатого после завершения обработки доксорубицином.
На фигуре 3 показан протокол для DDAVP (вазопрессиновый агонист [деамино-Cys1,D-Arg8]-вазопрессин) изучения примера 2.
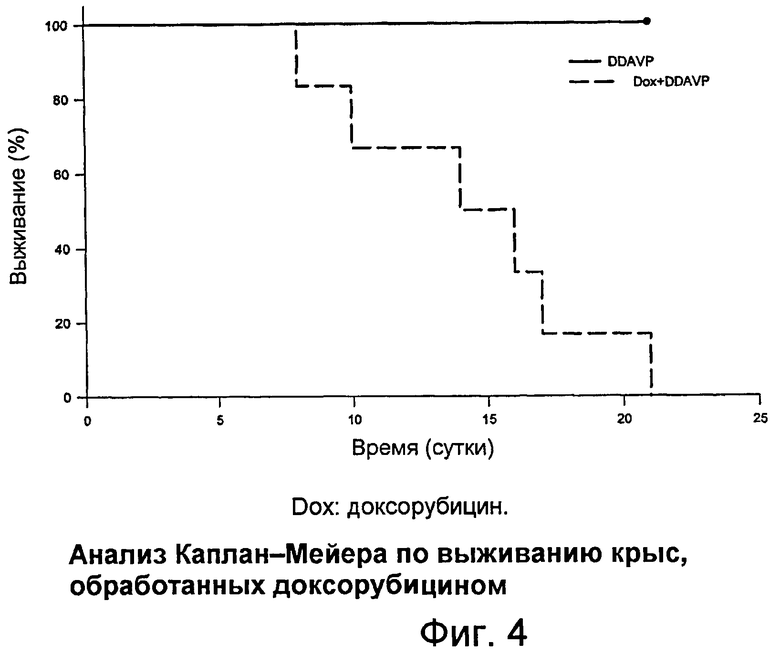
На фигуре 4 представлен анализ на выживание по Каплан-Мейеру с помощью лог-ранк теста на крысах, обработанных доксорубицином.
На фигуре 5 показан протокол обработки лекарственным средством и протокол отбора образцов крови для определения концентрации доксорубицина в примере 3.
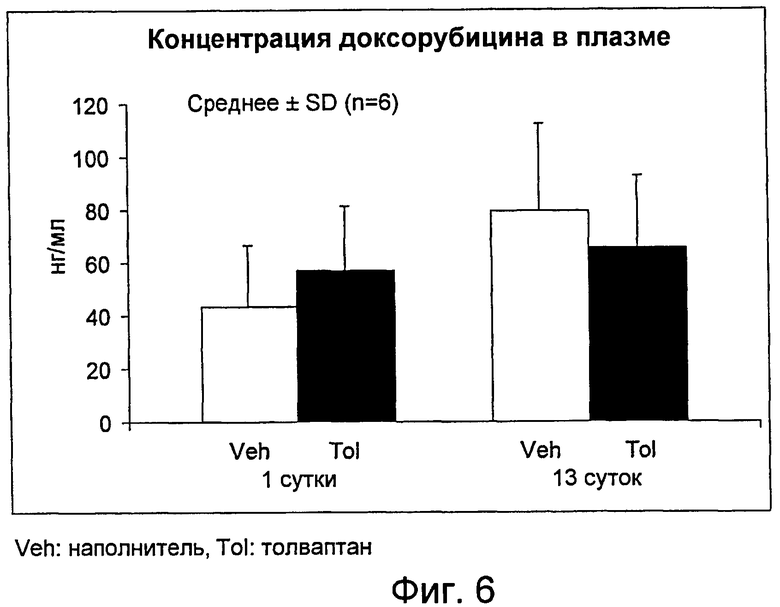
На фигуре 6 представлен график, показывающий результаты действия толваптана на концентрацию доксорубицина в плазме.
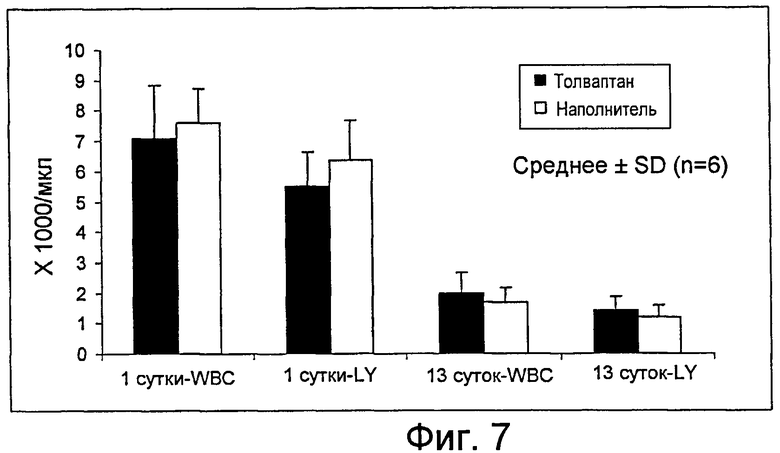
На фигуре 7 представлен график, иллюстрирующий действие толваптана на миелосупрессивный эффект доксорубицина.
На фигуре 8 представлен график, показывающий процент фракционного укорочения левого желудочка после обработки толваптаном в модели с внутривенной инъекцией.
На фигуре 9 представлен график, показывающий фракцию выброса левого желудочка после обработки толваптаном в модели с внутривенной инъекцией.
На фигуре 10 представлен график, показывающий объем/массу левого желудочка в конце диастолы, устанавливаемые в крысах, обработанных доксорубицином.
На фигуре 11 представлен график, показывающий диаметр/массу левого желудочка в конце диастолы, устанавливаемые в крысах, обработанных доксорубицином.
На фигуре 12 показано улучшение показателя сократительной способности у крыс, леченных толваптаном.
На фигуре 13 показан протокол исследования примера 5, чтобы выявить, ухудшает ли V2 агонист токсичность доксорубицина.
На фигуре 14 представлен анализ на выживание по Каплан-Мейеру для крыс, леченных толваптаном, с повышенным высвобождением вазопрессина.
Подробное описание изобретения
Антрациклиновые агенты представляют собой противоопухолевые средства, используемые в химиотерапии для лечения человека, имеющего гематогенные и твердые злокачественные новообразования широкого спектра, включающих рак молочной железы и лейкоз. Однако применение антрациклинов, таких как доксорубицин (адриамицин®), ограничено кумулятивным и дозозависимым миокардиальным повреждением.2 Токсичность, связанная с доксорубицином, часто присутствует как изменения в ЭКГ и аритмии, или как кардиомиопатия, приводящая к CHF, а также к повышенному риску внезапной смерти и смерти от сердечных причин.6
Способы данного изобретения подходят для лечения индивидуума, пораженного любой неоплазией/раком. Неопластические клетки, уничтожаемые способами данного изобретения, включают клетки новообразований, неоплазм, карцином, сарком, папиллом, лейкоза, лимфом, и тому подобные. Твердые новообразования представляют особый интерес.
Термин “рак”, как он используется в настоящем описании, охватывает любую клетку или клетки, механизмы контроля нормального роста которых нарушены, в результате чего создается потенциал для неконтролируемой пролиферации клеток. Термин “рак” включает как доброкачественные, так и злокачественные неопластические клетки/опухоли в обеих нервных системах и на периферии, где периферия предназначена для обозначения всех других частей организма, внешних к головному или спинному мозгу.
Термин “пациент”, как он используется в настоящем описании, включает пациента, который имеет рак, такой как лейкоз, лимфомы, рак молочной железы, рак матки, рак яичника или рак легкого, и которого лечат антрациклиновым средством.
Данное изобретение также относится к способу предупреждения и/или лечения поражения кардиальной ткани млекопитающего, такого как кардиотоксичность, вызванная антрациклиновыми противоопухолевыми средствами, такими как доксорубицин.
Термин “кардиотоксичность”, как он используется в настоящем описании, включает клиническую сердечную недостаточность, клиническую кардиотоксичность, такую как острая сердечная недостаточность и застойная сердечная недостаточность, и/или кардиальные аритмии и субклиническую кардиотоксичность, такую как кардиотоксичность, определяемую патологическими изменениями в кардиальной биопсии и/или химии крови или уменьшениями фракций выброса желудочков.
Способы данного изобретения могут быть также использованы для повышения выживаемости субъектов в течение или после противоракового лечения.
В первом варианте осуществления данного изобретения активный ингредиент в способе для снижения кардиотоксичности, связанной с лечением антрациклинами, по данному изобретению представляет собой соединение-антагонист вазопрессина. Соединения-антагонисты вазопрессина по данному изобретению включают, но без ограничения только ими, толваптан, мозаваптан, кониваптан, ликсиваптан, сатаваптан, RWJ-351647, RWJ-339489, SSR-149415, YM-222546, YM-471, YM-35471, YM-218, FR-218944, JNJ-17079166, JNJ-17308616, VMAX-367, VMAX-382, VMAX-372, ORG-52186, SRX-251, и/или их фармацевтически приемлемые соли и бензоазепиновое соединение или его соль, описанные в WO 2007/074915, и т.д.
Соединения-антагонисты вазопрессина по данному изобретению также включают бензоазепиновые соединения, обладающие активностью в качестве антагониста вазопрессина. Такие бензоазепиновые соединения имеют активность к аргинин-вазопрессиновым (AVP) рецепторам типа 1А (V1A) и типа 2 (V2) (т.е. V1/V2) или являются селективными для V2 рецептора. Бензоазепиновые соединения данного изобретения включают, но без ограничения только ими, соединения, изображаемые следующей формулой (I):
Формула (I)

в которой R1 представляет собой атом водорода или атом галогена, R2 представляет собой гидроксигруппу, или группу формулы: -NR5R6, в которой R5 и R6 одинаковые или различные и каждый представляет собой атом водорода или низшую алкильную группу, R3 представляет собой атом водорода, атом галогена, низшую алкильную группу, или низшую алкоксильную группу, R4 представляет собой атом галогена, низшую алкильную группу, или низшую алкоксильную группу, или их фармацевтически приемлемую соль.
В данном описании и в формуле изобретения группы в вышеприведенной формуле (I) обозначают следующие группы.
“Атом галогена” обозначает атом фтора, атом хлора, атом брома, или атом йода. “Низшая алкильная группа” обозначает алкильную группу с прямой цепью или с разветвленной цепью, содержащую от 1 до 6 атомов углерода, такую как метил, этил, пропил, изопропил, бутил, трет-бутил, пентил или гексил.
“Низшая алкоксигруппа” обозначает алкоксигруппу с прямой цепью или с разветвленной цепью, содержащую от 1 до 6 атомов углерода, такую как метокси, этокси, пропокси, изопропокси, бутокси, трет-бутокси, пентилокси, или гексилокси.
Бензоазепиновые соединения формулы (I) и способы приготовления этих соединений раскрыты в документах WO 91/05549, U.S. Pat. No. 5258510 и U.S. Pat. No. 5753677 и также в японском аналоге JP-A-6-80641, каждый из которых включен в настоящее описание ссылкой во всей полноте.
Бензоазепиновые соединения формулы (I) настоящего изобретения могут легко образовывать фармацевтически приемлемую кислотно-аддитивную соль с фармацевтически приемлемой кислотой. Фармацевтически приемлемые кислоты включают неорганические кислоты, такие как серная кислота, хлористоводородная кислота, фосфорная кислота, бромистоводородная кислота, и т.д., и органические кислоты, такие как уксусная кислота, п-толуолсульфоновая кислота, метансульфоновая кислота, щавелевая кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота, янтарная кислота, бензойная кислота, и т.д.
Среди бензоазепиновых соединений формулы (I), соединения, имеющие кислотную группу, могут легко образовывать соль с фармацевтически приемлемым основанием. Данные основания включают гидроксиды металлов, такие как гидроксид натрия, гидроксид калия, гидроксид лития, гидроксид кальция, и т.д.; карбонаты щелочных металлов или гидрокарбонаты, такие как карбонат калия, карбонат натрия, гидрокарбонат натрия, гидрокарбонат калия, и т.д.; и алкоголяты щелочных металлов, такие как метилат натрия, метилат калия, и т.д.
Соединения-антагонисты вазопрессина формулы (I) по данному изобретению используются в форме обычного фармацевтического препарата. Препарат готовят использованием обычных разбавителей или носителей, таких как наполнители, загустители, связующие вещества, смачиватели, диспергаторы, поверхностно-активные вещества, замасливатели и тому подобное. Фармацевтические препараты могут быть выбраны из различных форм в соответствии с желаемыми применениями, и репрезентативные формы представляют собой таблетки, пилюли, порошки, растворы, суспензии, эмульсии, гранулы, капсулы, суппозитории, инъекции (растворов, суспензий, и т.д.) и тому подобное.
Для формирования таблеток используются хорошо известные фармацевтические наполнители, такие как носители (например, лактоза, белый сахар, хлорид натрия, глюкоза, мочевина, крахмал, ксилит, маннит, эритрит, сорбит, карбонат кальция, каолин, кристаллическая целлюлоза, кремниевая кислота, и т.д), связующие вещества (например, вода, этанол, пропанол, простой сироп, раствор глюкозы, раствор крахмала, желатиновый раствор, карбоксиметилцеллюлоза, шеллак, метилцеллюлоза, фосфат калия, поливинилпирролидон, и т.д.), дезинтеграторы (например, сухой крахмал, альгинат натрия, агаровый порошок, порошок ламинарана, гидрокарбонат натрия, карбонат кальция, жирнокислотные сложные эфиры полиоксиэтиленсорбитана, лаурилсульфат натрия, стеариновый моноглицерид, крахмалы, лактоза, и т.д.), ингибиторы дезинтегрирования (например, белый сахар, стеарин, масло какао, гидрированные масла, и т.д.), стимуляторы абсорбции (например, четвертичное аммониевое основание, лаурилсульфат натрия, и т.д.), смачиватели (например, глицерин, крахмалы, и т.д.), адсорбенты (например, крахмалы, лактоза, каолин, бентонит, коллоидные силикаты, и т.д.), замасливатели (например, очищенный тальк, стеараты, порошок борной кислоты, полиэтиленгликоль, и т.д) и тому подобное. Кроме того, таблетки могут быть в форме обычной таблетки с покрытием, такой как таблетки с сахарным покрытием, таблетки с желатиновым покрытием, таблетки с энтеросолюбильным покрытием, таблетки с пленочным покрытием, или таблетки с двойными или многократными слоями. В приготовлении пилюль могут быть использованы обычные носители, которые включают, например, носители (например, глюкоза, лактоза, крахмалы, масло какао, гидрированные растительные масла, каолин, тальк, и т.д.), связующие вещества (например, порошок аравийской камеди, порошок трагаканта, желатин, этанол, и т.д.), диспергаторы (например, ламинаран, агар, и т.д.), и тому подобное. При приготовлении суппозиториев могут быть использованы обычные носители, и они включают, например, полиэтиленгликоль, масло какао, высший спирт, сложные эфиры высших спиртов, желатин, полусинтетические глицериды и тому подобное. Капсулы могут быть приготовлены помещением смеси соединения данного изобретения и вышеприведенных носителей в твердые желатиновые капсулы, мягкие капсулы или капсулы из гидроксиметилпропилцеллюлозы (НРМС капсулы) применяемым способом. При приготовлении инъекций растворы, эмульсии и суспензии стерилизуют и делают их предпочтительно изотоническими с кровью. При приготовлении данных растворов, эмульсий и суспензий используются обычные разбавители, такие как вода, этиловый спирт, макрогол, пропиленгликоль, этоксилированный изостеариловый спирт, полиоксилированный изостеариловый спирт, сложные жирнокислотные эфиры полиоксиэтиленсорбитана и тому подобное. В данном случае в фармацевтические препараты можно также включать хлорид натрия, глюкозу или глицерин в количестве достаточном, чтобы делать их изотоническими, и можно также включать обычные солюбилизаторы, буферы и анестетики. Кроме того, фармацевтические препараты необязательно могут включать красители, консерванты, отдушки, ароматизаторы, подсластители и другие лекарственные средства, если требуется.
Содержание соединений-антагонистов вазопрессина формулы (I), предназначенных для включения в фармацевтическую композицию данного изобретения, может быть выбрано из широкого интервала. Обычно данное количество предпочтительно в интервале от 1 до 70 мас.%, предпочтительнее от 5 до 50 мас.%, в расчете на массу композиции.
Подходящий способ для введения композиций данного изобретения может быть определен в соответствии с разными формами препаратов, возрастом, полом и другими состояниями пациентов, степенью тяжести заболеваний и тому подобного. Например, таблетки, пилюли, растворы, суспензии, эмульсии, гранулы и капсулы вводят перорально. Инъекции вводят внутривенно отдельно или вместе с обычной вспомогательной жидкостью (например, растворы глюкозы, аминокислоты), и, кроме того, необязательно вводят отдельно при внутримышечном, внутрикожном, подкожном или интраперитонеальном способах введения, если требуется. Суппозитории вводят интраректальным способом.
Дозировка соединений-антагонистов вазопрессина данного изобретения может быть выбрана в соответствии с применением, возрастом, полом и другими состояниями пациентов, степенью тяжести заболеваний, и тому подобного. Подходящая доза находится в интервале от 0,1 мг до 1000 мг/организм в сутки, предпочтительно от 0,5 мг до 500 мг/организм в сутки, предпочтительнее от 1 мг до 100 мг/организм в сутки.
Соединения-антагонисты вазопрессина данного изобретения включают, но без ограничения только ими, толваптан, мозаваптан, кониваптан, ликсиваптан и сатаваптан или его фармацевтически приемлемую соль. Кроме того, RWJ-351647 и 339489, SSR-149415, YM-222546, YM-471, YM-35471, YM-218, FR-218944, JNJ-17079166 и 17308616, VMAX-367, VMAX-382, VMAX-372, ORG-52186, SRX-251 и т.д. или их фармацевтически приемлемые соли также могут быть использованы в качестве вазопрессиновых антагонистов в данном изобретении.
В другом варианте осуществления данное изобретение относится к способу лечения рака, включающему введение пациенту терапевтически эффективного количества комбинации вазопрессинового соединения-антагониста и антрациклина. Антрациклины включают, но без ограничения только ими, даунорубицин (Cerubidine®), доксорубицин (Adriamycin®, Rubex®), эпирубицин (Ellence®, Pharmorubicin®) и идарубицин (Idamycin®). Комбинации изобретения могут включать фармацевтически приемлемый наполнитель, носитель или разбавитель.
Доза вазопрессинового соединения-антагониста и антрациклина составляет такую дозу, которая может приводить к ослаблению боли у пациента, что определяется снижением кардиотоксичности при лечении одним антрациклином и/или улучшением эффективности лечения рака. Как хорошо известно, дозировка каждого соединения зависит от нескольких факторов, таких как потенциал конкретного выбранного соединения, путь введения, возраст и масса пациента, тяжесть состояния, предназначенного для лечения, и тому подобное. Считают, что это находится в компетенции специалиста, и он может изучить существующую литературу относительно каждого компонента, чтобы определить оптимальное дозирование.
В данный момент предпочтительный вазопрессиновый антагонист, используемый согласно изобретению, представляет собой толваптан. Толваптан, также называемый 7-хлор-5-гидрокси-1-[2-метил-4-(2-метилбензоиламино)бензоил]-2,3,4,5-тетрагидро-1Н-бензоазепин, представляет собой селективный вазопрессиновый V2 антагонист. Толваптан изображается следующей структурой:

Толваптан вызывает повышенное, зависимое от дозы образование разбавленной мочи без изменения электролитного баланса сыворотки и без активации системы ренин-ангиотензин.
Другие вазопрессиновые антагонисты, которые могут быть использованы, включают, но без ограничения только ими, мозаваптан (описанный в патенте США № 5258510, который включен ссылкой в настоящее описание полностью), кониваптан (описанный в патенте США № 5723606, который включен ссылкой в настоящее описание полностью), ликсиваптан (описанный в EP 636625 и в патенте США № 5516774, каждый из которых включен ссылкой в настоящее описание полностью) и сатаваптан (описанный в WO 971556, который включен ссылкой в настоящее описание полностью). Кроме того, RWJ-351647 и 339489, SSR-149415, YM-222546, YM-471, YM-35471, YM-218, FR-218944, JNJ-17079166 и 17308616, VMAX-367, VMAX-382, VMAX-372, ORG-52186, SRX-251 и бензоазепиновое соединение или его соль, описанные в WO 2007/074915, и т.д., могут быть также использованы в качестве вазопрессиновых антагонистов в данном изобретении.
Для применения в медицине фармацевтически приемлемые соли могут быть применимы в препарате вазопрессиновых соединений-антагонистов согласно изобретению. Выражение ”фармацевтически приемлемые соли” включает как фармацевтически приемлемые кислотно-аддитивные соли, так и фармацевтически приемлемые катионные соли.
Термин “терапевтически эффективное количество”, как он используется в настоящем описании, относится к достаточному количеству соединения, чтобы снизить инфаркт, такой как, например, инфаркт миокарда, в допустимом соотношении польза/риск, подходящем для любого медицинского лечения.
Определенный терапевтически эффективный уровень доз для любого конкретного пациента будет зависеть от множества факторов, включающих тяжесть состояния; активность определенного используемого соединения; определенной используемой композиции и возраста пациента. Однако некоторые изменения в дозировке неизбежно будут происходить в зависимости от состояния субъекта, которого лечат. Лицо, ответственное за введение, будет, в любом случае, определять соответствующую дозу для конкретного субъекта.
Комбинация вазопрессиновых антагонистов и антрациклинов данного изобретения может быть введена стандартным образом, а именно: перорально, парентерально, трансмукозально (например, подъязычно или путем буккального введения), местно, трансдермально, ректально, путем ингаляции (например, назальная или глубокая легочная ингаляция). Парентеральное введение включает, но без ограничения только ими, внутривенное, внутриартериальное, внутрибрюшинное, подкожное, внутримышечное, внутриоболочечное и внутрисуставное, или методы высокого давления, подобные Powderject™.
Для буккального введения композиция может быть в форме таблеток или лепешек, формируемых обычным образом. Например, таблетки и капсулы для перорального введения могут содержать обычные эксципиенты, такие как связывающие вещества (например, сироп, аравийская камедь, желатин, сорбит, трагакант, слизь крахмала или поливинилпирролидон), наполнители (например, лактоза, сахар, микрокристаллическая целлюлоза, кукурузный крахмал, фосфат кальция или сорбит), замасливатели (например, стеарат магния, стеариновая кислота, тальк, полиэтиленгликоль или диоксид кремния), дезинтеграторы (например, картофельный крахмал или натрий-крахмалгликолат) или смачивающие вещества (например, лаурилсульфат натрия). Таблетки могут быть с покрытием в соответствии с методами, известными в данной области.
Кроме того, композиции данного изобретения могут быть изготовлены для парентерального введения инъекцией или непрерывной инфузией. Препараты для инъекций могут находиться в форме суспензий, растворов или эмульсий в масляных или водных носителях и могут содержать агенты для приготовления препаратов, такие как суспендирующие, стабилизирующие и/или дезинтегрирующие средства. В альтернативном случае активный ингредиент может быть в форме порошка для состава с подходящим носителем (например, стерильная, непирогенная вода) перед применением.
Для перорального введения фармацевтическая композиция может принимать форму растворов, суспензий, таблеток, пилюль, капсул, порошков и тому подобного. Таблетки, содержащие различные эксципиенты, такие как цитрат натрия, карбонат кальция и фосфат кальция, используются вместе с различными дезинтеграторами, такими как крахмал и предпочтительно картофельный крахмал или крахмал из тапиоки и определенные комплексные силикаты, вместе со связывающими веществами, такими как поливинилпирролидон, сахароза, желатин или аравийская камедь. Дополнительно для целей таблетирования очень часто применяются замасливатели, такие как стеарат магния, лаурилсульфат натрия и тальк. Твердые композиции подобного типа также используются как наполнители в мягких и твердых капсулах с желатиновым наполнением; предпочтительные продукты в этой связи также включают лактозу или молочный сахар, а также полиэтиленгликоли высокой молекулярной массы.
В альтернативном случае соединения данного изобретения могут быть включены в жидкие препараты для перорального введения, такие как, например, водные или масляные суспензии, растворы, эмульсии, сиропы или эликсиры. Кроме того, препараты, содержащие данные соединения, могут присутствовать в качестве сухого продукта для состава с водой или другим подходящим разбавителем перед применением. Такие жидкие препараты могут содержать обычные добавки, такие как суспендирующие средства, такие как сорбитный сироп, синтетические и природные камеди, такие как трагакант, аравийская камедь, альгинат, декстран, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин, глюкоза/сахарный сироп, желатин, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, гель из стеарата алюминия, эмульгаторы, такие как лецитин, сорбитанмоноолеат, или аравийская камедь; неводные носители (которые могут включать съедобные масла), такие как миндальное масло, фракционированное кокосовое масло, маслянистые сложные эфиры, пропиленгликоль и этиловый спирт; и консерванты, такие как метил или пропил-п-гидроксибензоат и сорбиновая кислота. Жидкие формы, в которые могут быть включены композиции данного изобретения для перорального введения или инъекцией, включают водные растворы, подходящим образом ароматизированные сиропы, водные или масляные суспензии и ароматизированные эмульсии со съедобными маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические носители.
Когда водные суспензии и/или эликсиры желательны для перорального введения, соединения данного изобретения могут быть объединены с различными подсластителями, ароматизаторами, красителями, эмульгаторами и/или суспендирующими средствами, а также с такими разбавителями как вода, этанол, пропиленгликоль, глицерин и их различные аналогичные комбинации. Подходящие диспергирующие или суспендирующие средства для водных суспензий включают синтетические и природные камеди, такие как трагакант, аравийская камедь, альгинат, декстран, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин.
Комбинация вазопрессиновых антагонистов и антрациклинов данного изобретения также может быть введена в препарат с контролируемым высвобождением активного ингредиента, такой как препарат с медленным высвобождением или препарат с быстрым высвобождением. Такие препараты с контролируемым высвобождением активного ингредиента из комбинаций данного изобретения могут быть приготовлены с применением методов, хорошо известных в данной области. Способ введения будет определяться обслуживающим врачом или другим специалистом в данной области после оценки состояния пациента и потребностей.
Фармацевтические композиции данного изобретения могут состоять из комбинации характеристик по немедленному высвобождению и по контролируемому высвобождению. Такие композиции могут принимать форму комбинаций активных ингредиентов, которые колеблются по размеру от наночастиц до микрочастиц или в форме множества шариков с разными скоростями высвобождения.
Комбинации данного изобретения могут быть введены также в парентеральной форме. Для парентерального введения могут быть использованы растворы в кунжутном или арахисовом масле или в водном пропиленгликоле, а также стерильные водные растворы соответствующих водорастворимых солей. Такие водные растворы подходящим образом могут быть обработаны буферами, если необходимо, и жидкий разбавитель сначала приведен в изотоническое состояние достаточным количеством физиологического раствора или глюкозы. Данные водные растворы особенно подходят для целей внутривенной, внутримышечной, подкожной и интраперитонеальной инъекции. В этой связи все стерильные водные используемые среды являются легко получаемыми по стандартным методикам, хорошо известным специалистам в данной области.
Способы приготовления различных фармацевтических композиций с определенным количеством активного ингредиента известны или будут очевидными в свете данного раскрытия для специалистов в данной области.
Фармацевтические композиции согласно изобретению могут содержать 0,1-95% терапевтических средств данного изобретения, предпочтительно 1-70%. В любом случае композиция или препарат, предназначенные для введения, будут содержать количество терапевтических(ого) средств(а) согласно изобретению на уровне, эффективном для лечения состояния или заболевания субъекта, которого лечат.
Два различных соединения данного изобретения, т.е. соединение-антагонист вазопрессина и антрациклин, могут быть введены совместно одновременно или вазопрессин первым, затем антрациклин.
Данное изобретение показано более подробно следующими примерами
ПРИМЕРЫ
Пример 1
Методы:
Известно, что повторяющиеся инъекции доксорубицина животным вызывают кардиальное повреждение и повышают смертность. Было предпринято изучение, чтобы исследовать эффект толваптана на вызванную доксорубицином кардиальную токсичность и смерть животных. Оценивали четыре группы крыс; все были с 6 инъекциями доксорубицина (2,5 мг/кг каждая) в течение двухнедельного периода. Чтобы тестировать способность толваптана предотвращать токсичность, толваптан (10 мг/кг перорально) ежедневно давали одной группе крыс (Tol+Dox). Другой группе крыс давали только наполнитель (Veh+Dox). Чтобы тестировать способность толваптана по обращению токсичности, толваптан (10 мг/кг перорально) ежедневно давали одной группе крыс, начиная с момента после завершения введения доксорубицина (Dox+Tol). Другой группе крыс давали только наполнитель (Dox+Veh). Таблица 1 суммирует данные по группам:
Обработанные группы для модели с интраперитонеальной инъекцией доксорубицина
Крыс наблюдали в течение 12 недель. Выживших анализировали, используя анализ выживания по Каплан-Мейеру с лог-ранк тестом.
На фигуре 1 показано, что показатель смертности был значительно снижен лечением с помощью толваптана (р<0,001).
Когда лечение толваптаном начинали после завершения 6 инъекций доксорубицина, защитный эффект толваптана значительно ослаблялся, как можно видеть на фигуре 2. Имелось только небольшое замедление смерти крыс под действием толваптана. В двух группах крыс, получавших доксорубицин и толваптан, и крыс, получавших доксорубицин и наполнитель только, в целом 24 крысы получали инъекции доксорубицина. Однако после завершения введения доксорубицина значительное число крыс оказалось больными, и считалось, что даже эффективная терапия не могла быть способной обратить повреждение у очень больных крыс. Только 10 из данных крыс отобрали для того, чтобы получить обработку толваптаном (5 крыс) или наполнителем (5 крыс).
Результаты, показанные на фигуре 2, наводят на мысль, что толваптан очень эффективен в предотвращении смертности, вызываемой доксорубицином, если толваптан вводится совместно с доксорубицином. Способность снижать смертность сильно утрачивается, если данное лечение начинают только после завершения 6 инъекций доксорубицина. Таким образом, новое открытие данного исследования состоит в том, что вазопрессиновым антагонистам требуется быть введенными прежде или совместно с химиотерапевтическими средствами, чтобы проявлять защитный эффект.
Пример 2
Авторы изобретения исследовали, может ли активация V2 рецепторов ускорять смертность, вызываемую доксорубицином. Непрерывную подкожную инфузию из 1 нг/ч DDAVP (деамино-Cys1, D-Arg-вазопрессин) на животное выполняли, применяя осмотический мининасос (скорость инфузии: 0,5 мкл/ч, ALZET модель 2002, DURECT Corporation, Cupertino, CA) в течение 14 суток. Протокол для данного изучения показан на фигуре 3. В 0 день осмотический мининасос имплантировали подкожно. Имитационные контрольные крысы имели аналогичную хирургическую процедуру, но только с физиологическим раствором в мининасосе. Затем крыс разделяли на две группы: одна с шестью интраперитонеальными инъекциями доксорубицина (2,5 мг/кг) в течение 13-суточного периода, и одна с инъекциями физиологического раствора. Крыс кормили жидким кормом на протяжении опыта. С непрерывной инфузией DDAVP кормление жидкой пищей увеличивает системную объемную перегрузку и отек, состояния, часто наблюдаемые в пациентах с CHF.
Поддерживая вредную роль вазопрессиновых V2 рецепторов в токсичности, вызываемой доксорубицином, DDAVP статистически и значительно повышал токсичность доксорубицина и значительно ускорял скорость смерти от доксорубицина по сравнению с таковой для крыс, обработанных одним доксорубицином (р<0,001, лог-ранк тест), как показано на фигуре 4. Таким образом, у пациентов, обработанных доксорубицином, повышенные уровни вазопрессина могут дополнительно усиливать токсичность.
Пример 3
Чтобы определить, влияет ли толваптан на концентрацию доксорубицина в плазме, образцы плазмы получали после первой (сутки 1) и шестой (сутки 13) инъекции доксорубицина с наполнителем или толваптаном, и измеряли концентрацию доксорубицина в плазме. Фигура 5 показывает протокол обработки лекарственным средством и протокол отбора образцов крови для данного изучения.
Как показано на фигуре 6, толваптан не влияет на концентрацию доксорубицина в плазме.
Известно, что антрациклины, включающие доксорубицин, вызывают миелосупрессию из-за их способности встраиваться в ДНК и ингибируют синтез новых белков и пролиферацию клеток в костном мозге (подобные механизмы включены в ингибирование пролиферации раковых клеток). Миелосупрессию использовали как показатель способности доксорубицина ингибировать пролиферацию клеток и как показатель противоракового эффекта. Толваптан не влиял на миелосупрессивный эффект доксорубицина, как показано на фигуре 7, который демонстрирует, что тринадцатидневная обработка доксорубицином значительно снижала общее число лейкоцитов (WBC) и лимфоцитов (LY). Образцы крови брали спустя 1 или 13 суток после обработки доксорубицином. Снижения в количестве клеток крови были аналогичными для крыс, обработанных наполнителем и обработанных толваптаном. Односуточная обработка доксорубицином не влияла на количества клеток крови.
Данные результаты дают основание предположить, что маловероятно, что толваптан влияет на противораковый эффект доксорубицина.
Пример 4
В клиническом учреждении доксорубицин вводят внутривенно раковым пациентам. Более того, основной побочный эффект, связанный с лечением доксорубицином, представляет собой кардиальную дисфункцию и развитие CHF. Поэтому оценивали эффект толваптана на CHF в модели на крысах с внутривенной инъекцией доксорубицина. Кардиальную функцию определяли, применяя ультразвуковую эхографию высокого разрешения.
Методы:
Крыс разделяли на 3 группы, как описано в таблице 2, и наблюдали в течение 10 недель.
Обработанные группы для модели с интраперитонеальной инъекцией доксорубицина
(Эхо изучение)
(Эхо изучение)
Контрольных крыс не обрабатывали. В группах 2 и 3 с обработкой доксорубицином крысам давали внутривенно три инъекции доксорубицина (3 мг/кг) каждый следующий день (общая доза 9 мг/кг). Выбирали более низкую дозу доксорубицина в данном опыте (по сравнению с дозой примера 1), чтобы предоставить возможность для развития CHF в течение 10-недельного периода. Крысам давали либо наполнитель, либо толваптан (10 мг/кг) ежедневно, начиная с первого дня инъекции доксорубина. В дни с совместным введением доксорубицина и толваптана, давали толваптан пероральным чреззондовым путем за 45 мин до внутривенной инъекции доксорубицина.
Кардиальную функцию оценивали, применяя эхокардиографию (Vevo 770, Visualsonics Inc, Торонто, Канада). Эхокардиограммы снимали раз в неделю в течение 10 последовательных недель. Крыс анестезировали изофлураном и регистрировали окологрудные длинные и короткие осевые эхоизображения. Проводили независимый анализ кардиальной функции (фракция выброса и фракционное укорочение) и анатомических данных сердца (диаметр и объем LV в конце диастолы). В конце 10-недельного периода измеряли кардиальную сократительную способность (LVdp/dtmax/ip) инвазивно.
Результаты:
Данные представлены как среднее+SD (стандартное отклонение). Обработка доксорубицином постепенно снижала как фракционное укорочение, так и фракцию выброса левого желудочка, указывающие на сердечную недостаточность, как показано на фигурах 8 и 9. Толваптан значительно улучшал кардиальную функцию и замедлял развитие сердечной недостаточности.
Кроме кардиальной дисфункции, признаки CHF также включают перестройку левого желудочка: полость становится больше и расширенной. Действительно, данные эхоизображения показали, что диастолический объем и диаметр левого желудочка постепенно повышались обработкой доксорубицином, как показано на фигурах 10 и 11. Толваптан замедлял процесс перестройки.
Инвазивные гемодинамические измерения проводили в конце 10-недельного периода. Показатель сократительной способности, определенный нормализацией LVdp/dtmax к мгновенному LV давлению в LVdp/dtmax, был выше у крыс, обработанных толваптаном, по сравнению с этим показателем у крыс, обработанных наполнителем, как показано на фигуре 12.
Пример 5
Авторы изобретения исследовали, может ли толваптан улучшать выживаемость при длительной активации состояния V2 рецептора (непрерывной инфузией V2 агониста DDAVP) у крыс, обработанных внутривенной инъекцией доксорубицина. Данное состояние может быть существенным для определенных раковых пациентов, которые повысили высвобождение вазопрессина и подвергаются химиотерапии, такой как с помощью доксорубицина.
Были изучены две группы крыс, и данный протокол описан на фигуре 13. Крысам внутривенно вводили инъекциями доксорубицин (3 мг/кг) 3 раза по одной в каждый следующий день для общей дозы в 9 мг/кг (то же самое, как описано в примере 4). Одной группе (Dox+DDAVP) давали наполнитель и другой группе (Dox+DDAVP+Tol) вводили толваптан (10 мг/кг) раз в сутки. Осмотический мининасос (скорость инфузии: 0,15 мкл/ч, ALZET модель 2006, ALZA Corporation) имплантировали в каждую крысу для непрерывной подкожной инфузии 1 нг/ч DDAVP (вазопрессиновый V2 агонист [деамино-Cys1, D-Arg8]-вазопрессин).
Анализ выживания по Каплан-Мейеру показан на фигуре 14. Хотя инфузия DDAVP делала доксорубицин очень токсичным и крысы погибали за 2 недели, толваптан значительно улучшал выживание. Эти данные дают основание предполагать, что токсичность доксорубицина усиливается при состоянии повышенного вазопрессина. Толваптан может быть особенно полезным для снижения токсичности доксорубицина у раковых пациентов с повышенным вазопрессином.
Все патенты, патентные заявки, научные и медицинские публикации, упоминаемые в настоящем описании, тем самым включены в него ссылкой во всей их полноте. Следует понимать, что вышеизложенное, конечно, относится только к предпочтительным вариантам осуществления данного изобретения и что разные модификации или изменения могут быть сделаны специалистами в данной области без отступления от сущности и объема изобретения, представленного в прилагаемой формуле изобретения.




| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ВЫЯВЛЕНИЯ СЕРДЕЧНЫХ НАРУШЕНИЙ | 2008 |
|
RU2498309C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С КАРДИОТОКСИЧНОСТЬЮ, ВЫЗВАННОЙ ХИМИОТЕРАПИЕЙ | 2017 |
|
RU2743433C2 |
| ЖИРНЫЕ КИСЛОТЫ И ГЛИЦЕРИДЫ СО СРЕДНЕЙ ДЛИНОЙ ЦЕПИ В КАЧЕСТВЕ НЕФРОПРОТЕКТИВНЫХ СРЕДСТВ | 2008 |
|
RU2519215C2 |
| ЛЕЧЕНИЕ РАКОВЫХ ЗАБОЛЕВАНИЙ ПРИ ПОМОЩИ КОМБИНАЦИИ ТАКСАНОВ И 13-ДЕЗОКСИАНТРАЦИКЛИНОВ | 2007 |
|
RU2421224C2 |
| ПРОИЗВОДНЫЕ 5-ИМИНО-13-ДЕЗОКСИ АНТРАЦИКЛИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ РАКА, АУТОИММУННЫХ ЗАБОЛЕВАНИЙ ИЛИ ИММУНОДЕФИЦИТНЫХ НАРУШЕНИЙ | 1999 |
|
RU2239640C2 |
| НАНОЧАСТИЦЫ, НЕСУЩИЕ ХИМИОТЕРАПЕВТИЧЕСКОЕ ПРОТИВОРАКОВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2012 |
|
RU2616494C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КУМУЛЯТИВНОЙ КАРДИОТОКСИЧНОСТИ ХИМИОТЕРАПЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2012 |
|
RU2510240C2 |
| ВОДОРАСТВОРИМОЕ СОЕДИНЕНИЕ БЕНЗОАЗЕПИНА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2418804C2 |
| Инозин как корректор антрациклиновой токсичности | 2018 |
|
RU2693825C1 |
| БИЦИКЛИЧЕСКИЕ ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ-АКТИВАТОРЫ АНТИОКСИДАНТНОЙ ПРОГРАММЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЦИТОПРОТЕКТОРОВ | 2014 |
|
RU2545758C1 |











Представлена группа изобретений, включающая способ и фармацевтическую композицию для снижения кардиотоксичности и/или улучшения выживаемости от антрациклиновой химиотерапии. Пациенту, нуждающемуся в этом, вводят терапевтически эффективное количество фармацевтической композиции, содержащей соединение, представляющее собой V2 селективный антагонист вазопрессина, или его фармацевтически приемлемую соль, в качестве активного ингредиента, одновременно с или перед введением антрациклина. Изобретения обеспечивают уменьшение кардиотоксичности антрациклинов при снижении побочных эффектов за счет снижения уровня сывороточного вазопрессина, аномальное содержание которого типично для больных, страдающих раком, и который, в свою очередь, играет важную роль в развитии застойной сердечной недостаточности. 2 н. и 13 з.п.ф., 14 ил., 2 табл., 5 пр.
1. Способ снижения кардиотоксичности и/или улучшения выживаемости от антрациклиновой химиотерапии, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества композиции, содержащей соединение, представляющее собой V2 селективный антагонист вазопрессина, или его фармацевтически приемлемую соль в качестве активного ингредиента, одновременно с или перед введением антрациклина.
2. Способ по п.1 для снижения кардиотоксичности.
3. Способ по п.1 для улучшения выживаемости.
4. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой соединение формулы (I):
Формула (I)

в которой R1 представляет собой атом водорода или атом галогена, R2 представляет собой гидроксигруппу или группу формулы: -NR5R6, в которой R5 и R6 одинаковые или различные и каждый представляет собой атом водорода или низшую алкильную группу, R3 представляет собой атом водорода, атом галогена, низшую алкильную группу, или низшую алкоксильную группу, R4 представляет собой атом галогена, низшую алкильную группу или низшую алкоксильную группу, или его фармацевтически приемлемую соль.
5. Способ по п.1, в котором V2 селективный антагонист вазопрессина выбран из группы, включающей толваптан, мозаваптан, ликсиваптан, сатаваптан, RWJ-351647 и их фармацевтически приемлемую соль.
6. Способ по п.1, в котором антрациклин выбран из группы, состоящей из даунорубицина, доксорубицина, эпирубицина и идарубицина.
7. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой толваптан.
8. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой гидрохлорид мозаваптана.
9. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой ликсиваптан.
10. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой сатаваптан.
11. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой даунорубицин.
12. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой доксорубицин.
13. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой эпирубицин.
14. Способ по п.1, в котором V2 селективный антагонист вазопрессина представляет собой толваптан и антрациклин представляет собой идарубицин.
15. Фармацевтическая композиция, содержащая соединение, представляющее собой V2 селективный антагонист вазопрессина или его фармацевтически приемлемую соль для снижения кардиотоксичности и/или улучшения выживания при антрациклиновой химиотерапии, предназначенная одновременно с или перед введением антрациклина.
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| RU 99101118 A, 10.01.2001 | |||
| ОРЛОВА Р.В | |||
| Пути снижения кардиотоксичности антрациклиновых антибиотиков при комбинированной химиотерапии диссеминированного рака молочной железы | |||
| - Актуальные вопросы онкологии, 1996, с.218-219 | |||
| WEXLERLH | |||
| Amelioration of chemotherapy induced cardiotoxicity | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Seminars in Oncology. | |||
Авторы
Даты
2012-12-27—Публикация
2008-05-12—Подача