Изобретение относится к медицине, а именно кардиологии и онкологии.
Некоторые лекарственные препараты, обладают значительным кардиодепрессивным действием. Нежелательный побочный эффект связывают с их способностью нарушать транспорт ионов Са2+ - важнейшим компонентом потенциала действия пейсмекеров. Значимую роль играют и ионы натрия Nа+, обеспечивая регуляция концентрации ионов кальция в сердечных клетках, обозначаемую как Nа+-Ca2+ обмен. Ингибирующее действие на эту транспортную систему оказывают некоторые антибиотики и цитостатики антрациклинового ряда - Хлорпромазин, Полимиксин, Доксорубицин.
Известно, что препарат Доксорубицин [регистр лекарственных средств https://www.rlsnet.ru/mnn_index_id_99.htm#xarakteristika--veshhestva-doksorubicin] является мощным противоопухолевым антибиотиком, используемым для лечения многих видов рака. Серьезным осложнением при лечении Доксорубицином является наличие у него кардиотоксического действия. Частота развития различных сердечных осложнений у пациентов, принимающих Доксорубицин, достигает 36%.
Точный механизм токсического действия Доксорубицина на сердце пока остается неизвестным. Имеются сведения об ингибирующем действии Доксорубицина на процесс Na+-Ca2+ обмена в изолированных фрагментах (везикулах) сарколеммы миокарда [Carafoli E. Calcium transport systems of heart sarcolemma vesicles. Naunyn - Schmiederberg's Arch / E. Carafoli. // Pharmacol. - 1982. - V. 321. - Р. 7.]
Известен эффект угнетения Доксорубицином процесса поглощения Са2+в изолированном сердце крысы во время Na+-Ca2+ обмена [Алабовский В.В., Винокуров А.А., Маслов О.В. Параметры селективности Nа-Са ионообменной системы к изменению внеклеточной концентрации ионов натрия при гипоксии и ишемии сердца, а также при воздействии некоторых кардиотропных лекарственных препаратов // Системный анализ и управление в биомедицинских системах. - 2010. - Т. 9, N 1. - С. 138-141.]
Существующие способы ослабления токсического влияния химиотерапии на сердце при лечении онкологических пациентов дороги и малоэффективны. Есть сведения о применении с этой целью препаратов N-ацетилцистеина, фенитиламины, коэнзим Q10, антагонисты вазопрессина [Патент A61P 9/04 Лю Юнгэ (US), Камбаяси Дзунити (US) (RU 2470643) и другие]. Стоимость этих препаратов высока, достичь существенного снижения кардиотоксичности Доксорубицина не удалось.
В этой связи имеет большое практическое значение поиск лекарственных средств, способных снижать токсическое действие Доксорубицина на Nа+-Ca2+ обмен в сердце.
Известен препарат Инозин [регистр лекарственных средств https://www.rlsnet.ru/mnn_index_id_644.htm] - нуклеозид, предшественник АТФ. Субстратно стимулирует синтез адениновых нуклеотидов, повышает активность некоторых ферментов цикла Кребса, обладает антиаритмическим, антигипоксическим, метаболическим эффектами. Согласно инструкции производителя применение вещества Инозин известно для следующего: ИБС (инфаркт миокарда, коронарная недостаточность, нарушения сердечного ритма), врожденные и приобретенные пороки сердца, ревматические пороки сердца, кардиомиопатии различного генеза, коронарный атеросклероз, дигиталисная интоксикация, миокардит, «легочное сердце», нагрузок, инфекционного и эндокринного генеза), заболевания печени (острый и хронический гепатит, цирроз печени, алкогольные и лекарственные повреждения печени, жировая дистрофия печени), язвенная болезнь желудка и двенадцатиперстной кишки, урокопропорфирия. Отравление ЛС, алкоголизм, лучевая лейкопения (профилактика), операции на изолированной почке (как средство фармакологической защиты при временном выключении кровообращения оперируемого органа).
В доступной литературе сведений об использовании Инозина для снижения антрациклиновой токсичности нет.
Технический результата - устранить токсичность антибиотиков антрациклинового ряда, представителем которого является Доксорубицин, уменьшить проявление его побочных эффектов и материальных затрат на лечение.
При выборе необходимого лекарственного средства для эффективной защиты сердца мы обратили внимание на экспериментальные данные, в которых было установлено значительное ослабление некоторыми нуклеотидами и нуклеозидами повреждений сердца в условиях возникновения, так называемого, «кальциевого парадокса».
Поэтому в качестве опытного образца, с предполагаемым защитным эффектом был взят лекарственный препарат Инозин.
Технический результат достигают добавлением Инозина в концентрации не менее 50 мкмоль/л во внеклеточную среду сердца в целях устранения токсического влияния Доксорубицина. Для оценки защитного влияния Инозина нами был исследован транспорт Са2+, сопряженный с изменением трансмембранного градиента Nа+, а также сократительная активность в изолированном сердце крысы. Такой методический подход позволял сохранить не только анатомическую целостность ткани миокарда, но и физиологические и биохимические процессы, сопряженные с работой Nа+-Ca2+ обмена [Пат. 2400825 Российская Федерация, МПК G09В 23/28 А61В 5/04. Способ одновременной регистрации Nа+ - зависимых потоков Са2+ и функционального состояния целого изолированного сердца в эксперименте / В.В. Алабовский, А.А. Винокуров, О.В. Маслов; заявитель и патентообладатель ВГМА им. Н.Н. Бурденко Росздрава. - №2009122349/14; опубл. 27.09.2010 // Бюл. - №27. - 3 с.]
Эксперименты проводили на лабораторных животных в строгом соответствии с современными требованиями правил лабораторной практики по экспериментальному (доклиническому) исследованию в РФ (ГОСТ 351000.3-96 и 51000.4-96)
Основным объектом исследования были белые крысы линии Wistar. Всего в работе было использовано 48 животных обоего пола массой 200-250 г. Каждая серия экспериментов проводилась на 7-10 крысах, в зависимости от воспроизводимости результатов исследований.
Под эфирным наркозом осуществляли декапитацию животного. Сердце быстро извлекали и помещали в охлажденный перфузионный раствор. При изучении Nа+-Ca2+ обмена перфузию сердца осуществляли с постоянной скоростью при помощи перистальтического насоса под контролем давления в аорте, которое колебалось в пределах 60-70 мм рт. ст. Скорость коронарного протока составляла от 8 до 10 мл/мин, в зависимости от массы желудочков сердца.
В аорту изолированного сердца, подавали раствор следующего состава: NаСl - 140 ммоль/л, NaHCO3 - 2 ммоль/л, KCl - 15 ммоль/л, трис-ОН - 5 ммоль/л, (рН 7,4), СаСl2 - 0,7 ммоль/л, глюкоза - 11 ммоль/л. Таким образом, суммарная концентрация ионов натрия [Nа+] в растворе составляла 142 ммоль/л.
В целях устранения влияния механической активности сердца на процесс аккумуляции и выхода Ca2+ во время Nа+-Ca2+ обмена сердечную деятельность останавливали с помощью высокой внеклеточной концентрации калия - 15 ммоль/л. Деполяризация кардиомиоцитов полностью блокировала их электрическую активность.
Опыты начинали после 15 минут адаптации сердца и стабилизации обменных процессов и сократительной функции сердца.
Инициацию натрий-зависимого поглощения ионов кальция (реверсное направление Nа+-Ca2+ обмена) изолированным сердцем крысы осуществляли путем снижения концентрации хлорида натрия в перфузионном растворе.
Гипонатриевый перфузионный раствор имел в своем составе: NаСl - 10 ммоль/л, NН4Сl - 130 ммоль/л, NaHCO3 - 2 ммоль/л, KCl - 15 ммоль/л, трис-ОН - 5 ммоль/л, (рН 7,4), СаСl2 - 0,7 ммоль/л, глюкоза -11 ммоль/л. Таким образом, данный раствор отличался от исходного низким количеством ионов натрия [Nа+] –12 ммоль/л.
Перфузию гипонатриевым раствором, в зависимости от цели эксперимента, осуществляли от 1 до 5 минут. Затем перфузию переводили на исходный раствор, содержащий физиологическую концентрацию натрия. При этом наблюдали выброс Са2+из сердца (прямое направление Nа+-Ca2+ обмена).
Концентрацию кальция в оттекающем от сердца перфузионном растворе непрерывно измеряли в течение всего периода опыта. С помощью перистальтического насоса перфузионный раствор смешивали с металлоиндикатором - арсеназо-III.
Арсеназо-III (2,7-бис-[(2-арсонофенил)азо]-1,8-диокси 3,6 нафталин-дисульфокислота) является реагентом для фотометического определения ионов кальция. Максимум поглощения света комплексом арсеназо-III-Са2+ регистрировали при длине волны 660 нм. Металлоиндикатор обладает высокой селективностью и чувствительностью к ионам кальция. В научных исследованиях его используют для измерения внутриклеточной концентрации Са2+, колебания, которой чрезвычайно малы и составляют от 10-6 до 10-8 моль/л.
Образовавшийся окрашенный продукт реакции между Са2+ перфузионного раствора и металлоиндикатором пропускали через проточную кварцевую кювету объемом 1 мл, помещенную в регистрационный блок спектрофотометра СФ-46 (ЗАО «ОКБ СПЕКТР», Россия). Показания спектрофотометра непрерывно регистрировали с помощью внешнего модуля аналого-цифрового преобразователя ZET 220 и программного обеспечения ZETLAB BASE (Предприятие "Электронные технологии и метрологические системы", Россия).
Калибровку системы осуществляли путем добавок хлорида кальция в перфузионные растворы, повышающие концентрацию кальция на 20 мкмоль/л. Сокращения сердца регистрировали в изоволюмическом режиме с помощью баллончика, вводимого в полость левого желудочка сердца. Развиваемое давление рассчитывали как разность систолического и диастолического давления.
При регистрации сокращений сердца перфузионные растворы с физиологической концентрацией NаСl (142 ммоль/л) и гипонатриевые растворы (12 ммоль/л) использовали в том же составе, отличающихся концентрацией КCl, которая составляла 5 ммоль/л и СаСl2 в количестве 2 ммоль/л.
Регистрацию сокращений осуществляли с помощью электроманометра фирмы "Bentley lab. Europe", сигналы от которого подавали к внешнему модулю аналого-цифрового преобразователя ZET 220, имеющему программное обеспечение ZETLAB BASE.
Концентрацию Доксорубицина в перфузионном растворе рассчитывали исходя из его количества вводимого в кровь во время лечения. При одноразовом введении 10 мг препарата в расчете на 5 литр крови создает его концентрацию приблизительно 4 мкмоль/л. В своих опытах мы добавляли препарат в перфузионные растворы до той же концентрации - 4 мкмоль/л.
Согласно инструкции по применению Инозина а, разовая доза препарата составляет не менее 200 мг/л крови (200 мкмоль/л). Однако нами использовалась минимальная концентрация Инозина (в четыре раза меньше) - 50 мкмоль/л перфузионного раствора.
Все полученные данные проверяли на распределение вероятностей, и в случае, когда выборка соответствовала нормальному распределению, осуществляли статистическую обработку данных с использованием t-критерия Стьюдента. При несоответствии критериям нормального распределения для сравнения выборок использовали непараметрический U-критерий Манна-Уитни-Уилкоксона. Все расчеты проводили с использованием пакетов статистического анализа.
Опыты показали, что различия Nа+-Са2+ обмена в контроле и опытах были связаны с разной скоростью аккумуляции Са2+ сердечной мышцей. Из представленной таблицы 1 видно, что Доксорубицин обладает свойством значительно снижать скорость поглощения Са2+ сердцем.
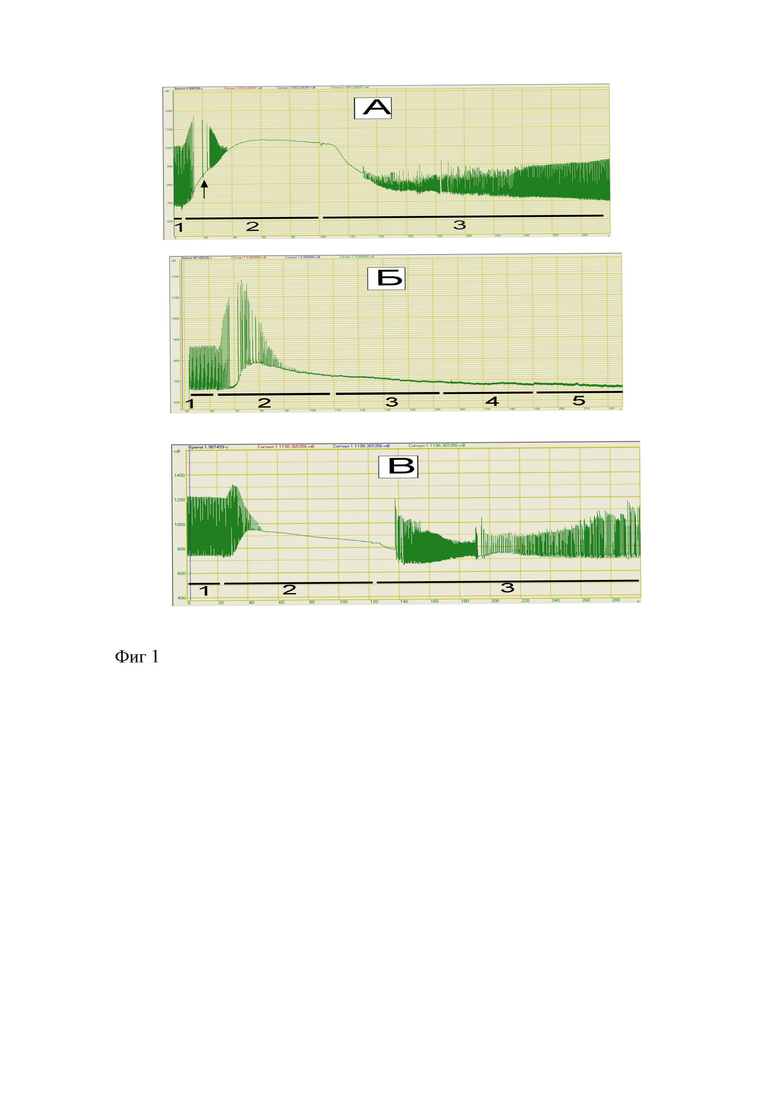
Результаты опыта показывают значительное снижение количества Са2+ поглощаемого в период его транспорта внутрь кардиомиоцитов и ослабление темпа нарастания диастолического напряжения миокарда, которое сразу, после небольшого подъема, монотонно снижается до исходного уровня контроля (фигура 1, А). Соответственно с этим, количество высвобождаемого Са2+ из сердца, в присутствии Доксорубицина было ниже чем в контрольных опытах.
Видно, что под влиянием Доксорубицина, реакция на повторные попытки активировать Nа+-Са2+ обмен в сердце в прямом и реверсном направлениях полностью отсутствовала. В отличие от контрольных опытов, переключение перфузии сердца на исходный раствор, с физиологическим уровнем NаСl, а также повторные попытки активировать Nа+-Са2+ обмен не вызывали никаких ответных реакций со стороны сократительного аппарата левого желудочка (фигура 1, Б). Это свидетельствует о значительных нарушениях Nа+-Са2+ обменного механизма.
Таким образом, полученные результаты указывают на то, что Доксорубицин, нарушая механизм транспорта Са2+ в сердце, ослабляет его поступление в кардиомиоциты в условиях реверсии Nа+-Са2+ обмена и его высвобождения из клеток при прямом направлении работы системы Nа+-Са2+ обмена. В результате наблюдается кардиодепрессивное действие Доксорубицина на сердце.
В другой серии опытов в перфузионные растворы добавляли одновременно Доксорубицин (4 мкмоль/л) и Инозин в концентрации 50 мкмоль/л. При этом ингибирующее влияние Доксорубицина на скорость поглощения Са2+, значительно ослабевало под влиянием Инозина (таблица 1). Таким образом, Инозин в сочетании с Доксорубицином восстанавливал способность Nа+-Са2+ обменной системы сердца накапливать Са2+ в условиях реверсии Nа+-Са2+ обмена.
Важно отметить, что Инозин не только устранял ингибирующее влияние Доксорубицина на процесс поглощения Са2+. Была отмечена его способность более активно высвобождать избыток Са2+ из сердечной мышцы по сравнению не только с опытами с Доксорубицином но и контрольными опытами (таблица 1).
Обозначения: n-количество животных в группах опытов;
р*<0,001 - сравнение дано с контролем;
р**<0,001- сравнение дано с Доксорубицином
Результаты исследования показывают, что способность максимально выводить Са2+миокардом под влиянием Инозина заметно увеличивалась.
Данное заключение отчетливо демонстрируют протоколы регистрации сократительной активности сердца (фигура 1, В). Во-первых, наблюдается восстановление сокращений в ответ на начало перфузии раствором с прежней, физиологической концентрации натрия. Во-вторых, при этом четко регистрируется ослабление диастолического напряжения, коррелирующее в этот момент с более активным выбросом ионов кальция посредством Nа+-Са2+ обмена.
Записи сокращений миокарда крысы при использовании различных комбинаций веществ свидетельствуют, что начало и продолжение перфузии раствором, содержащим сниженную концентрацию хлорида натрия (12 ммоль/л); в опытах серии “В” наблюдается ослабление диастолического напряжения. Совместное использование Доксорубицина с Инозином приводит с снижению диастолического напряжения за счет более активного выхода ионов кальция из кардиомиоцитов. Ослабление кальциевой нагрузки на миокард инициирует восстановление сокращений сердца.
Таким образом, нами предложено использование Инозина в качестве препарата, полностью ликвидирующего токсическое влияние Доксорубицина на сердечную мышцу. Доказано воздействие препарата на механизм сокращения миокарда (Nа+-Са2+ обмен). Инозин в концентрации не ниже 50 мкмоль/л устраняет кардиотоксичность антрациклиновых препаратов, например, Доксорубицина (4 мкмоль/л), заключающуюся в депрессии сократительной функции сердца и нарушении Na+ зависимых потоков Са2+(Nа+-Са2+ обмен) в интактном изолированном сердце.
Описание к фигурам.
Фигура. 1. Запись сокращений миокарда крысы в контроле (А) и при перфузии Доксорубицином (Б) и смесью Доксорубицина с Инозином (В)
1 - сокращения сердца в исходном состоянии;
2 - начало и продолжение перфузии раствором, содержащим сниженную концентрацию хлорида натрия (12 ммоль/л);
3 - переключение перфузии сердца на перфузионный раствор, содержащий исходную концентрацию хлорида натрия (142 ммоль/л).
4 - повторные включения гипонатриевого раствора
5 - повторые включения раствора с физиологическим содержанием хлорида натрия не вызывают ответные сократительные реакции сердца.Изобретение относится к медицине, а именно кардиологи и онкологии.
Некоторые лекарственные препараты, обладают значительным кардиодепрессивным действием. Нежелательный побочный эффект связывают с их способностью нарушать транспорт ионов Са2+ - важнейшим компонентом потенциала действия пейсмекеров. Значимую роль играют и ионы натрия Na+, обеспечивая регуляция концентрации ионов кальция в сердечных клетках, обозначаемую как Na+-Ca2+ обмен. Ингибирующее действие на эту транспортную систему оказывают некоторые антибиотики и цитостатики антрациклинового ряда - Хлорпромазин, Полимиксин, Доксорубицин.
Известно, что препарат Доксорубицин [регистр лекарственных средств https://www.rlsnet.ru/mnn_index_id_99. htm#xarakteristika-veshhestva-doksorubicin] является мощным противоопухолевым антибиотиком, используемым для лечения многих видов рака. Серьезным осложнением при лечении Доксорубицином является наличие у него кардиотоксического действия. Частота развития различных сердечных осложнений у пациентов, принимающих Доксорубицин, достигает 36%.
Точный механизм токсического действия Доксорубицина на сердце пока остается неизвестным. Имеются сведения об ингибирующем действии Доксорубицина на процесс Na+-Ca2+ обмена в изолированных фрагментах (везикулах) сарколеммы миокарда [Carafoli Е. Calcium transport systems of heart sarcolemma vesicles. Naunyn -Schmiederberg's Arch / E. Carafoli. // Pharmacol. - 1982. - V. 321. - P. 7.]
Известен эффект угнетения Доксорубицином процесса поглощения
Са2+ в изолированном сердце крысы во время Na+-Ca2+ обмена [Алабовский В.В., Винокуров А.А., Маслов О.В. Параметры селективности Na-Ca ионообменной системы к изменению внеклеточной концентрации ионов натрия при гипоксии и ишемии сердца, а также при воздействии некоторых кардиотропных лекарственных препаратов // Системный анализ и управление в биомедицинских системах. - 2 010. - Т. 9, N 1.- С.138-141.]
Существующие способы ослабления токсического влияния химиотерапии на сердце при лечении онкологических пациентов дороги и малоэффективны. Есть сведения о применении с этой целью препаратов N-ацетилцистеина, фенитиламины, коэнзим Q10, антагонисты вазопрессина [Патент А61Р 9/04 Лю Юнгэ (US), Камбаяси Дзунити (US) (RU 2470643) и другие].
Стоимость этих препаратов высока, достичь существенного снижения кардиотоксичности Доксорубицина не удалось.
В этой связи имеет большое практическое значение поиск лекарственных средств, способных снижать токсическое действие Доксорубицина на Na+-Ca2+ обмен в сердце.
Известен препарат Инозин [регистр лекарственных средств https://www.rlsnet.ru/mnnindexid644.htm] - нуклеозид, предшественник АТФ. Субстратно стимулирует синтез адениновых нуклеотидов, повышает активность некоторых ферментов цикла Кребса, обладает антиаритмическим, антигипоксическим, метаболическим эффектами. Согласно инструкции производителя применение вещества Инозин известно для следующего: ИБС (инфаркт миокарда, коронарная недостаточность, нарушения сердечного ритма), врожденные и приобретенные пороки сердца, ревматические пороки сердца, кардиомиопатии различного генеза, коронарный атеросклероз, дигиталисная интоксикация, миокардит, «легочное сердце»,
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОДНОВРЕМЕННОЙ РЕГИСТРАЦИИ Na-ЗАВИСИМЫХ ПОТОКОВ Ca И ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЦЕЛОГО ИЗОЛИРОВАННОГО СЕРДЦА В ЭКСПЕРИМЕНТЕ | 2009 |
|
RU2400825C1 |
| СПОСОБ ОЦЕНКИ КАРДИОПРОТЕКТИВНОЙ АКТИВНОСТИ ФАРМАКОЛОГИЧЕСКИХ СРЕДСТВ | 2017 |
|
RU2643104C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ СОКРАТИТЕЛЬНОЙ ФУНКЦИИ СЕРДЦА ПОСЛЕ КАРДИОПЛЕГИИ С АНТАГОНИСТАМИ КАЛЬЦИЯ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2133612C1 |
| СПОСОБ ИЗМЕРЕНИЯ НАБУХАНИЯ КАРДИОМИОЦИТОВ ЦЕЛОГО СЕРДЦА ПРИ УДАЛЕНИИ Са ИЗ ВНЕКЛЕТОЧНОЙ СРЕДЫ В ЭКСПЕРИМЕНТЕ | 2006 |
|
RU2368956C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ НЕКОРОНАРОГЕННЫХ НЕКРОЗОВ МИОКАРДА | 2005 |
|
RU2366004C2 |
| СПОСОБ ЗАЩИТЫ СЕРДЦА ОТ ИШЕМИИ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2144825C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ СОКРАЩЕНИЙ СЕРДЦА ПОСЛЕ ОСТАНОВКИ В ДИАСТОЛЕ В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2424582C1 |
| 3-(1Н-бензимидазол-2-ил)-1,2,2-триметилциклопентанкарбоновая кислота, обладающая кардиопротекторной активностью | 2017 |
|
RU2645356C1 |
| 5-ГИДРОКСИНИКОТИНАТ КАЛИЯ, ОБЛАДАЮЩИЙ КАРДИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2640580C1 |
| Способ моделирования фибрилляции желудочков сердца крысы | 1980 |
|
SU893205A1 |
Изобретение относится к медицине, а именно кардиологи и онкологии. Предложено применение инозина в концентрации не менее 50 мкмоль/л при перфузии сердца в качестве корректора антрациклиновой токсичности доксорубицина, путем снижения диастолического напряжения за счет более активного выхода Са2+ из кардиомиоцитов. Технический результат: инозин в заявленных условиях полностью ликвидирует токсическое влияние доксорубицина на сердечную мышцу, заключающееся в депрессии сократительной функции сердца и нарушении Na+ зависимых потоков Са2+ (Nа+-Са2+ обмен) в интактном изолированном сердце. 1 ил., 1 табл.
Применение Инозина в концентрации не менее 50 мкмоль/л при перфузии сердца в качестве корректора антрациклиновой токсичности Доксорубицина, путем снижения диастолического напряжения за счет более активного выхода Са2+ из кардиомиоцитов.
| TOCCHETTI CG et al | |||
| Ranolazine protects from doxorubicin-induced oxidative stress and cardiac dysfunction | |||
| Eur.J.Heart Fail | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| МЕМБРАНОСТАБИЛИЗИРУЮЩЕЕ И АНТИОКСИДАНТНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО "РИКАВИТ" | 1985 |
|
RU2006224C1 |
| SELIZAROVA N.O | |||
| et al | |||
| ;[Effect of purine nucleosides on the contractile function of the rat heart in ischemia and reperfusion] | |||
| Patol.Fiziol.Eksp.Ter | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| ГРЭХАМ-СМИТ Д.Г | |||
| и др | |||
| Оксфордский справочник по клинической фармакологии и фармакотерапии | |||
| М., Медицина 2000 с.606 | |||
| BRECHLER V | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J | |||
| Biol | |||
| Chem | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| М., Медицина 1993 12-е изд., т.2 с.167-168 статья Рибоксин | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2019-07-05—Публикация
2018-07-10—Подача