ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к способу содействия клиницисту при лечении пациентов, в частности пациентов, страдающих острыми функциональными заболеваниями.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Сепсис является тяжелым заболеванием, например, в форме поражения иммунной системы, вызванного инфекцией или другими травмами.
Если пациент, пораженный сепсисом, не лечится, или если терапия не оптимальна, то пациент может умереть.
Сепсис является осложненным заболеванием, вовлекающим реакции нескольких компонентов иммунной системы на инфекцию. Контролировать такие реакции сложно вследствие того, что они вовлекают многие типы клеток, обменивающихся между собой информацией посредством химических мессенджеров, которые повседневно не измеряют в клинике, а если бы даже измерялись, то соответствующие измерения трудно интерпретировать, поскольку динамика их откликов является очень сложной и сильно различается для разных пациентов. Сложность сепсиса можно понять с учетом того, что сепсис является десятой ведущей причиной смертности в США и ведущей причиной смертности в отделениях интенсивной терапии некардиологического профиля, несмотря на несколько десятилетий исследований.
Современная терапия сепсиса основана на опыте и квалификации клиницистов, однако, вследствие сложности сепсиса, даже опытные клиницисты могут быть лишены способности выполнять оптимальную терапию, или клиницист может выполнять даже такую терапию, которая приводит к ухудшению состояния пациента.
Некоторые из проблем, с которыми сталкиваются клиницисты, когда пораженный сепсисом пациент нуждается в лечении, обусловлены большим числом неизвестных биологических и физиологических факторов, влияющих на развитие заболевания, а также динамичным и часто быстрым изменением характера заболевания.
Соответственно, создание системы, способной содействовать клиницисту при выполнении подходящей терапии пациентов, пораженных такими заболеваниями, как сепсис, может представляться проблематичным.
Заявка США 2003/0097220 раскрывает систему поддержки принятия решений для рекомендации оптимального протокола лечения для конкретного человека. Система содержит, как правило, системную модель, множество протоколов лечения, модификатор системной модели, при этом упомянутая системная модель модифицируется модификатором системной модели на основе параметров, специфических для отдельного человека; и селектор для выбора оптимального протокола лечения из упомянутого множества протоколов лечения на основе модифицированной системной модели.
Способ, описанный в заявке США № 2003/0097220, связан с лечением рака и поэтому не может служить для лечения заболеваний с очень динамичным характером развития, который быстро изменяется через короткие временные промежутки (например, часы), и, следовательно, не пригоден для содействия клиницисту при лечении сепсиса.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соответственно, основной целью изобретения является ослабление, облегчение или устранение, по меньшей мере, одной из вышеупомянутых проблем поодиночке или в любой комбинации. В частности, целью настоящего изобретения можно считать предоставление способа и устройства, способных моделировать острые функциональные заболевания и прогнозировать будущие показатели пациентов для содействия клиницисту при организации лечения заболевания.
Упомянутая цель и различные другие цели достигаются в первом аспекте изобретения, предоставлением способа согласно независимому пункту формулы изобретения.
Изобретение, в частности, но не исключительно, полезно для прогнозирования показателей пациента в отношении пациента с острым функциональным заболеванием и выдачи информации по организации лечения заболевания, полученной из прогнозируемых показателей пациента, для содействия клиницисту при организации лечения заболевания.
Соответственно, в варианте осуществления первого аспекта изобретения, способ содержит этап адаптации математической модели к начальным показателям пациента. То есть множество показателей пациента, полученных из измерений биологических и/или физиологических параметров пациента, используют для адаптации или индивидуализации модели к пациенту или, точнее, к заболеванию пациента. Поскольку клиническое состояние пациента, вероятно, должно изменяться, например, вследствие развития заболевания, то, возможно, потребуется или будет полезно выполнить новую адаптацию модели к последним показателям пациента, чтобы модель лучше подходила для прогнозирования будущих показателей пациента. Таким образом, путем продолжения адаптации модели к динамике пациента с использованием последних показателей пациента и с использованием множества начальных показателей пациента, модель подстраивают к самому последнему состоянию здоровья пациента. Преимущество непрерывной адаптации модели может состоять в том, что модель способна прогнозировать будущие показатели пациента, даже когда острое функциональное заболевание характеризуется очень динамичными изменениями различных показателей пациента. Таким образом, посредством непрерывного определения прогнозируемых показателей пациента, информацию по организации лечения заболевания можно выдавать в блок вывода медицинского устройства для содействия клиницисту при организации лечения острого функционального заболевания. То есть информация по организации лечения заболевания может снабжать клинициста руководящими указаниями по выполнению конкретного вмешательства.
Преимущество первого аспекта изобретения может состоять в том, что модель сначала адаптируют к начальным показателям пациента, поскольку это может обеспечить возможность выдачи первого прогноза показателей пациента. Первый прогноз показателей пациента может быть выдан блоком вывода, что позволяет клиницисту сделать первую быструю оценку состояния здоровья пациента. Другое преимущество первого аспекта изобретения может состоять в том, что способ устойчив к потере показателей пациента, так как модель выполнена с возможностью использования множества показателей пациента, и, поэтому, способ будет продолжать обеспечивать допустимые прогнозы будущих показателей пациента, даже если некоторые показатели пациента, подаваемые в медицинское устройство, опаздывали.
Другое преимущество может состоять в том, что способ в соответствии с первым аспектом может объединять математическую модель динамики иммунной системы с последовательными измерениями ключевых химических мессенджеров и алгоритмами, способными подстраивать модель к отдельному пациенту и представлять клиницистам информационные дисплеи, которые показывают информацию по организации лечения заболевания, например текущее состояние пациента и/или его вероятное будущее направление развития.
В варианте осуществления изобретения в соответствии с зависимым пунктом 2 формулы изобретения информация по организации лечения заболевания содержит вмешательство. Пользователю или клиницисту может быть предоставлено, по меньшей мере, одно вмешательство в виде предложения режимов лекарственной терапии или вмешательств, например, в форме перечня возможных вмешательств или в виде графической иллюстрации возможных вмешательств. Предлагаемые вмешательства могут быть определены анализом прогнозируемых показателей пациента.
В варианте осуществления изобретения в соответствии с зависимым пунктом 3 формулы изобретения информация по организации лечения заболевания содержит временные данные для выполнения вмешательства, представляемые блоком вывода. Таким образом, выдача времени начала лекарственной терапии может оказаться полезной, так как это может усилить терапевтический эффект лекарственной терапии. Другое преимущество может быть в том, что клиницисту содействуют начать лекарственную терапию в оптимальное время. Временные данные могут быть определены анализом прогнозируемых показателей пациента.
В варианте осуществления изобретения в соответствии с зависимым пунктом 4 формулы изобретения информация по организации лечения заболевания содержит оценки степени достоверности прогнозируемых показателей пациента. Соответственно, обеспечение оценки степени достоверности прогнозов может оказаться полезным, поскольку это может позволить клиницисту судить о допустимых отклонениях оцененных показателей пациента, например, временной диаграммы наступления и пика гипервоспаления.
В варианте осуществления изобретения в соответствии с зависимым пунктом 5 формулы изобретения медицинское устройство выполнено с возможностью приема терапевтических показателей вмешательств. Терапевтические показатели могут обеспечиваться посредством блока ввода, или клиницист может вручную обеспечивать показатели для медицинского устройства с пользовательского интерфейса. При использовании терапевтических показателей прогнозируемые показатели пациента могут быть определены применением упомянутых терапевтических показателей в модели. Терапевтические показатели могут содержать показатели лекарственной терапии, например уровень антибиотика в сыворотке крови, противовоспалительный уровень или уровни других лекарственных препаратов в сыворотке крови. В качестве альтернативы или дополнительно, терапевтические показатели могут содержать показатели генератора режимов дозирования лекарственной терапии, например амплитуду дозы лекарственной терапии, период времени между лекарственными терапиями, рабочий цикл лекарственной терапии, т.е. время в процентах от периода, в течение которого применяют лекарственную терапию, время начала исполнения режима лекарственной терапии и/или время окончания исполнения режима лекарственной терапии. Использование терапевтических показателей в модели может оказаться полезным потому, что прогнозируемые будущие показатели пациента включают в себя терапевтический эффект лекарственной терапии, которая уже проведена. В качестве альтернативы или дополнительно, использование терапевтических показателей в модели может оказаться полезным, потому что позволяет обеспечить возможность проверки разных лекарственных терапий, чтобы клиницист мог выбрать конкретную лекарственную терапию с благоприятным результатом для пациента. Следовательно, предоставление клиницистам возможности изучать вероятное течение заболевания при различных лечебных стратегиях, разработанных самим клиницистом, может быть полезным, так как позволяет клиницистам применять знание об обстоятельствах, которые могут быть неизвестны системе (например, сочетанных заболеваниях).
В варианте осуществления изобретения в соответствии с зависимым пунктом 6 формулы изобретения применяют вычислительный блок для определения последующего времени отбора проб для снабжения медицинского устройства новыми показателями пациента, которые могут быть определены с использованием начальных и последних показателей пациента в связи с моделью. Полученное определением время для обеспечения новых показателей пациента может быть выдано в блоке вывода для содействия клиницисту, когда следует отбирать новые биологические и/или физиологические пробы от пациента, чтобы снабдить медицинское устройство последними показателями пациента через блок ввода или пользовательский блок ввода.
В варианте осуществления изобретения в соответствии с зависимым пунктом 7 формулы изобретения определяют время отбора проб из предшествующих показателей пациента, путем анализа динамики показателей пациента, например путем вычисления частотного спектра с использованием БПФ-анализатора (использующего алгоритм быстрого преобразования Фурье) или скорости изменения показателей пациента. Таким образом, если последние показатели пациента показывают стабильное состояние пациента, например, показывая низкочастотный спектр или низкую скорость изменений, то следующее время снабжения медицинского устройства новыми показателями пациента можно отсрочить, или новые показатели пациента, возможно, не потребуются совсем, пока клиницисты не начнут наблюдать изменение состояния пациента. Если последние показатели пациента показывают нестабильное состояние пациента, например, показывая высокочастотный спектр или высокую скорость изменений, то следующее время снабжения медицинского устройства новыми показателями пациента можно ускорить для повышения точности прогнозируемых показателей пациента.
В варианте осуществления изобретения в соответствии с зависимым пунктом 8 формулы изобретения время отбора проб является периодическим с фиксированной частотой. Частоту можно определять из динамики показателей пациента. Периодичность времени отбора проб может быть менее 10 часов, предпочтительно менее 5 часов, более предпочтительно менее 2 часов, например менее 1 часа.
В варианте осуществления изобретения в соответствии с зависимым пунктом 9 формулы изобретения определяют области состояния здоровья для распознавания результатов изменения состояния здоровья в пространстве модели посредством снабжения адаптированной модели данными пациента для прогнозирования результатов изменения состояния здоровья. Определение областей состояния здоровья может оказаться полезным, так как области состояния здоровья могут обеспечивать полезный способ анализа данных пациента и определения возможных вмешательств.
В варианте осуществления изобретения в соответствии с зависимым пунктом 10 формулы изобретения в пространстве модели определяют траектории различных результатов изменения состояния здоровья пациента. Определение траекторий пациента может оказаться полезным, так как траектории пациента могут снабдить клинициста легко понятным графическим представлением состояния здоровья пациента, результатами вмешательств и будущим развитием показателей пациента.
В варианте осуществления изобретения в соответствии с зависимым пунктом 11 формулы изобретения блок вывода выполнен с возможностью показа информации по организации лечения заболевания, например траекторий пациента, областей состояния здоровья и вмешательств, для содействия клиницисту.
Во втором аспекте настоящее изобретение относится к медицинскому устройству в соответствии с независимым пунктом 13 формулы изобретения.
В третьем аспекте настоящее изобретение относится к компьютерной программе, позволяющей процессору выполнять способ в соответствии с первым аспектом настоящего изобретения.
Каждый из первого, второго и третьего аспектов настоящего изобретения можно сочетать с любым из других аспектов. Упомянутые и другие аспекты изобретения станут очевидными и будут поясняться на примере нижеописанных вариантов осуществления.
В общих словах, настоящее изобретение относится к варианту осуществления медицинского устройства для содействия клиницистам, медсестрам и другим пользователям при выборе вмешательства для лечения пациента, страдающего острым функциональным заболеванием, например, пораженного сепсисом. Медицинское устройство основано на способе, в котором модель заболевания адаптируется или индивидуализируется соответственно пациенту. Чтобы обеспечить сохранение устройством способности к прогнозированию состояния здоровья пациента, устройство постоянно снабжают новыми показателями пациента, и модель непрерывно адаптируют соответственно к новым показателям пациента. Поскольку медицинское устройство выполнено с возможностью непрерывной адаптации соответственно к текущему состоянию здоровья, то устройство способно содействовать пользователю посредством генерации информации по организации лечения заболевания, например предложений по лекарственным терапиям, для блока вывода.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Ниже настоящее изобретение поясняется, но только для примера, со ссылкой на прилагаемые чертежи, на которых:
Фиг.1 показывает медицинское устройство 100 для содействия клиницисту при организации лечения острого функционального заболевания,
Фиг.2A-E показывает временные течения болезни, соответствующие пяти динамикам состояния здоровья пациента,
Фиг.3 показывает данные пациента в сравнении с прогнозируемой динамикой пациента,
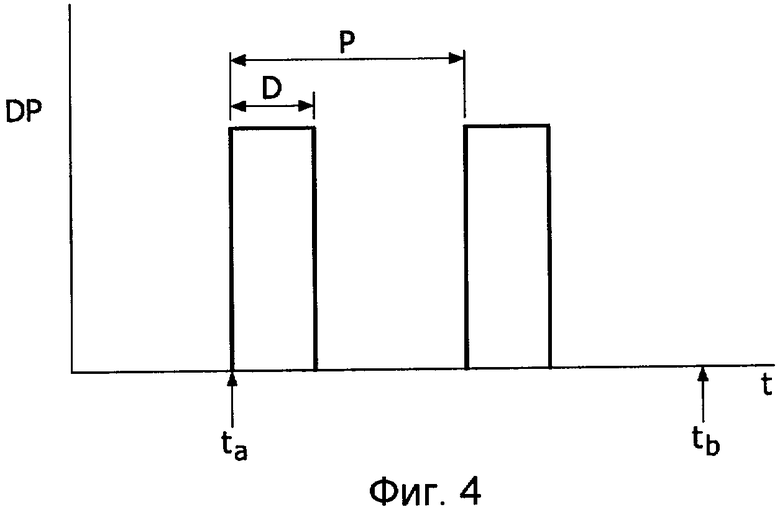
Фиг.4 показывает функцию r генератора режимов дозирования,
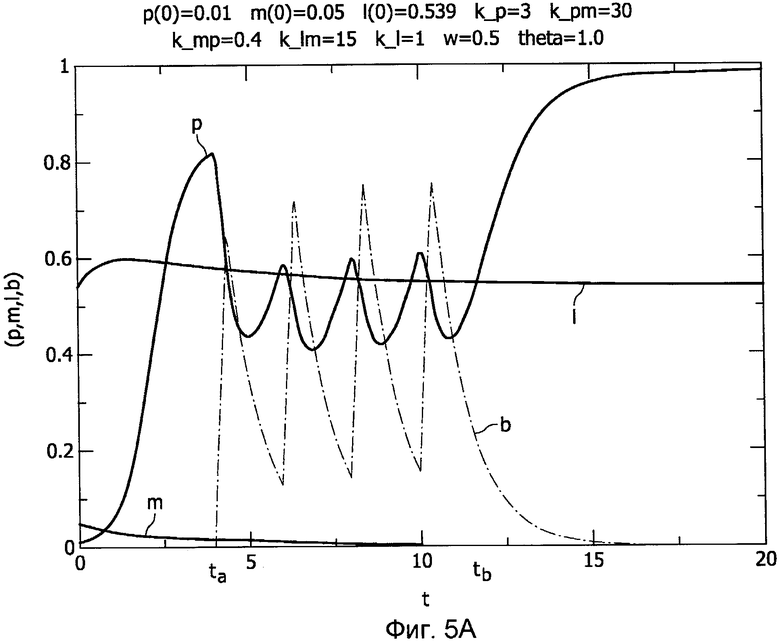
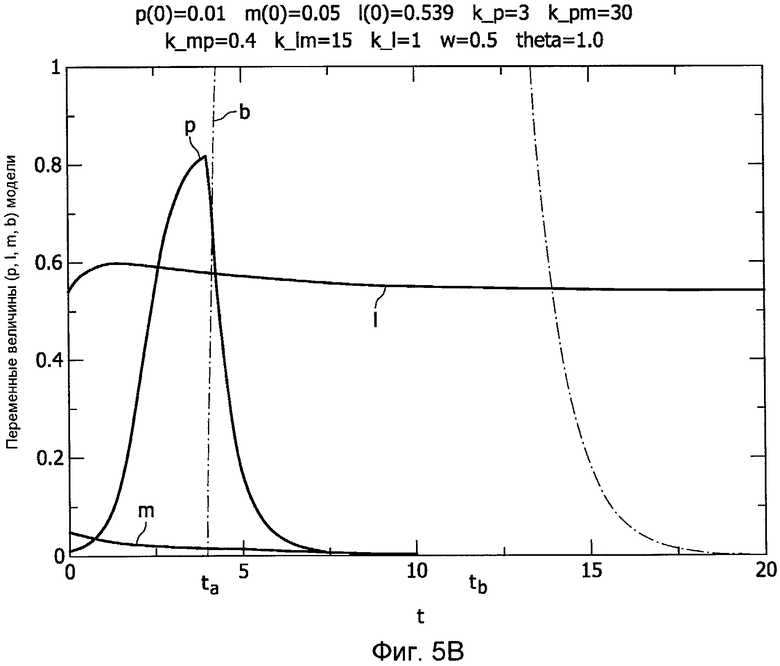
Фиг.5A-B показывает пример антибиотикотерапии, примененной при динамике тяжелого иммунодефицита,
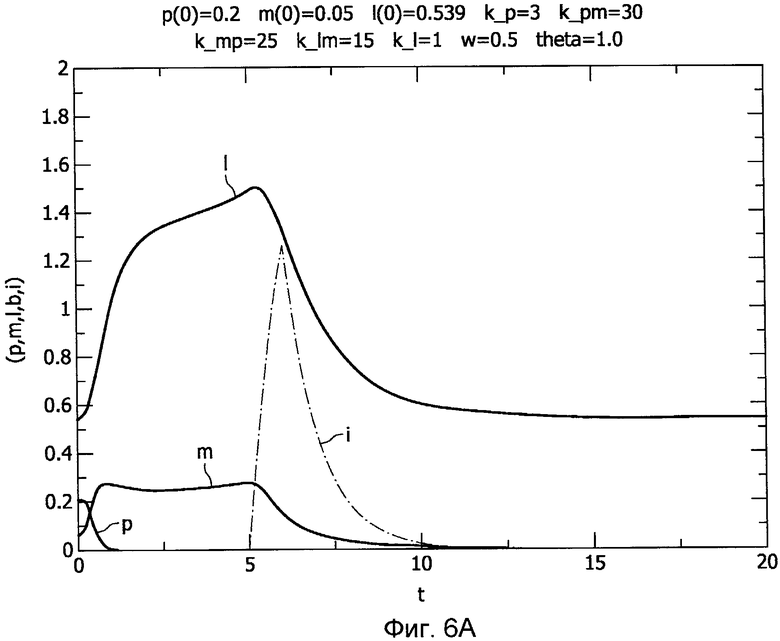
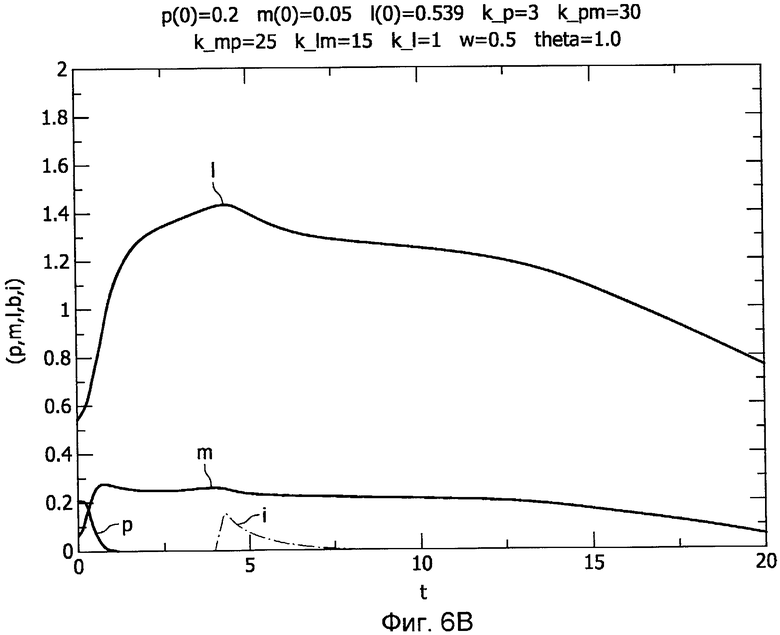
Фиг.6A-B показывает пример противовоспалительной терапии, примененной при динамике хронического неинфекционного воспалительного процесса,
Фиг.7 показывает пример пользовательского блока ввода и блока вывода,
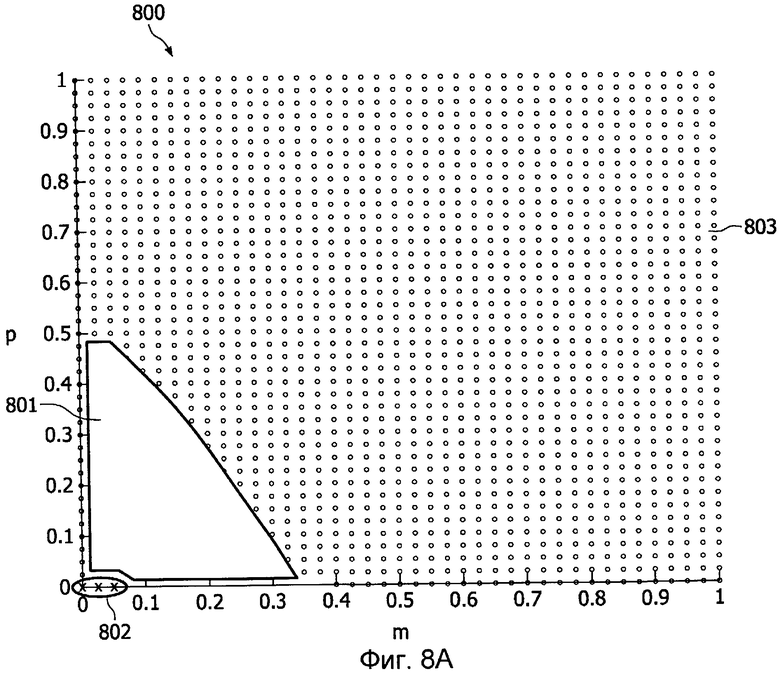
Фиг.8A показывает карту областей состояния здоровья для распознавания результатов изменения состояния здоровья в пространстве модели,
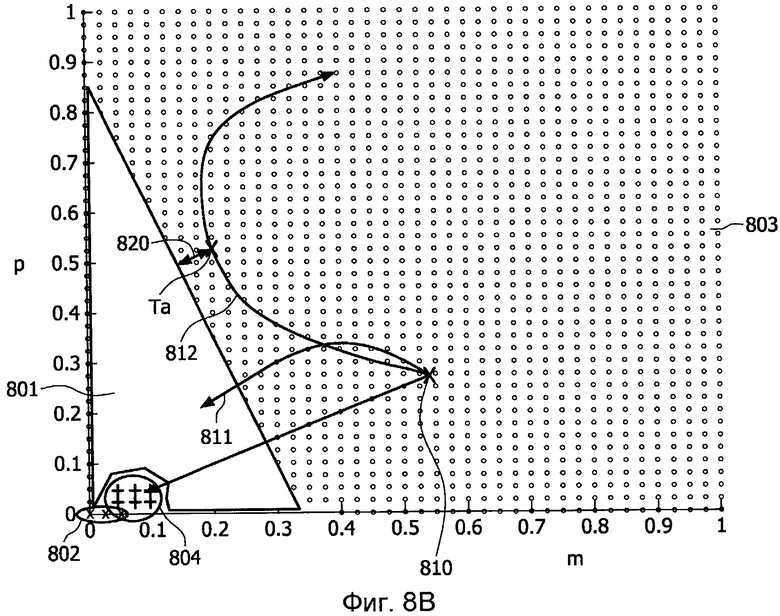
Фиг.8B показывает карту областей состояния здоровья с использованием такой же модели, как на Фиг.8A, но с увеличением k pm от 30 до 40,
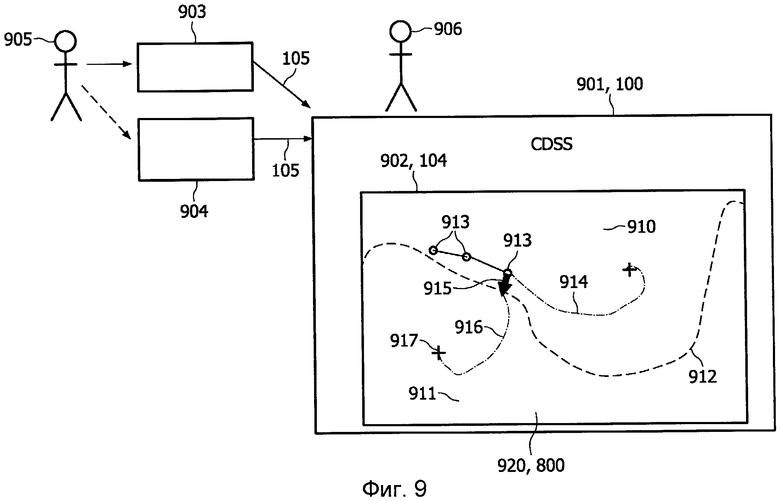
Фиг.9 показывает пример медицинского устройства, содержащего блок вывода,
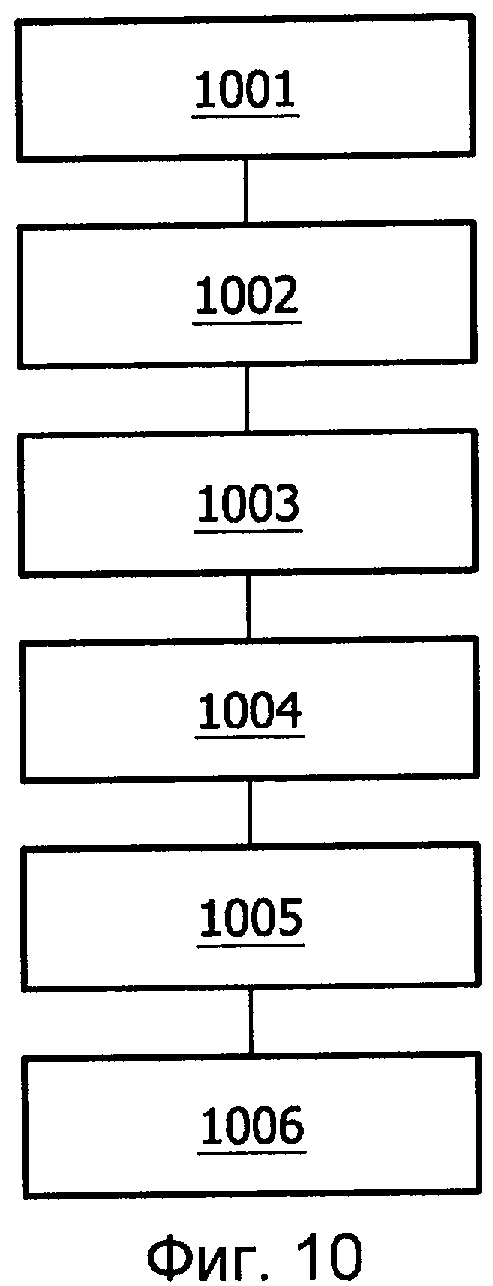
Фиг.10 показывает этапы способа в соответствии с вариантом осуществления изобретения,
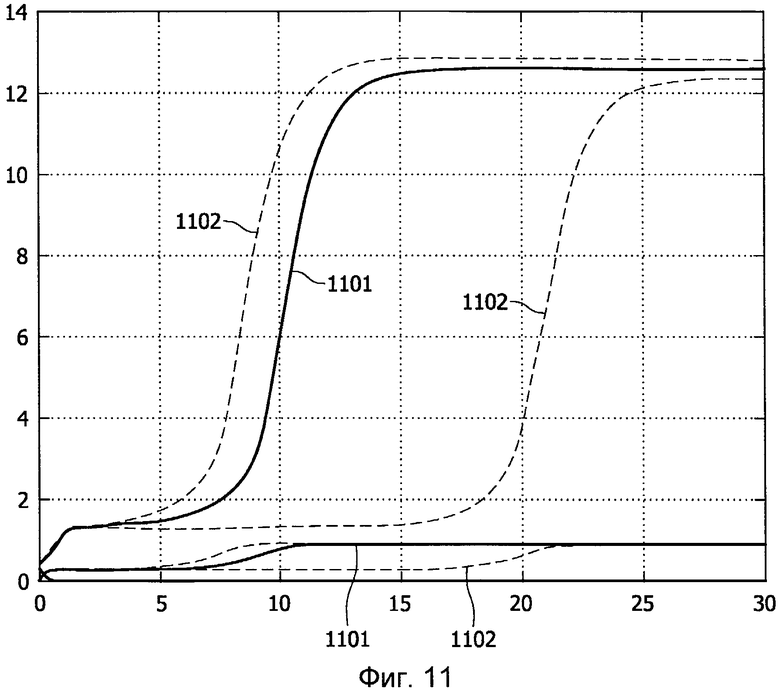
Фиг.11 показывает прогнозируемые показатели пациента в сочетании с доверительными огибающими.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
Вариант осуществления настоящего изобретения относится к заболеваниям, относимым к категории воспалительных заболеваний или функциональных заболеваний иммунной системы, например сепсису. Упомянутые тяжелые заболевания характеризуются очень динамичным характером, то есть упомянутые заболевания часто развиваются динамично, что предполагает сложность прогнозирования наступления и течения заболевания. Кроме того, упомянутые заболевания быстро развиваются за короткое время. Вмешательство приносит пользу в течение короткого временного интервала, иначе возможен очень неблагоприятный результат (например, смерть). Когда клиницист не может справиться с большим числом факторов, влияющих на заболевание, что может произойти в клинических условиях, клиницист может выбрать оптимальную терапию с использованием медицинского устройства, способного анализировать большое число показателей пациента, для содействия клиницисту при выборе терапии.
В контексте настоящего описания термин вмешательство следует понимать в смысле любого вида вмешательства, например лечебных вмешательств, диагностических вмешательств, административных вмешательств или паллиативных вмешательств.
В контексте настоящего описания термин клиницист следует понимать в смысле, эквивалентном терминам проводящее лечение лицо, медицинский работник, врач, медсестра, техник или администратор больницы.
Иммунная система является многократно избыточной системой управления, которая в результате развития стала очень стойкой. Сепсис является осложненным заболеванием, вовлекающим реакции нескольких компонентов иммунной системы на инфекцию. Упомянутые реакции сложно контролировать из-за того, что они вовлекают многие типы клеток, обменивающихся между собой информацией посредством химических мессенджеров, которые не измеряются в клинике в плановом порядке, и даже если бы измерялись, то соответствующие измерения трудно интерпретировать, так как динамика их откликов очень сложна и различается в широких пределах для разных пациентов. По описанной причине организация клинического лечения случаев сепсиса является сложной задачей, когда очевидно, что ни один терапевтический подход не является оптимальным для всех пациентов; недостаточный иммунный отклик может потребовать лечения антибиотиками, а острая реакция иммунной системы может потребовать противовоспалительной и/или антикоагулянтной терапии, и, как известно, время вмешательств является критичным, но с трудом допускающим его точную оценку.
Как упоминалось, вариант осуществления настоящего изобретения относится к сепсису. Однако изобретение не ограничено сепсисом, воспалительными заболеваниями или функциональными заболеваниями иммунной системы, так как варианты осуществления изобретения можно также применять к другим заболеваниям, например автоиммунным заболеваниям типа артрита, и воспалительной составляющей рака или заболеваний сердца. В общих вариантах осуществления изобретение можно применять к различным заболеваниям группы острых функциональных заболеваний, которые охватывают заболевания, упомянутые в настоящем описании, а также другие заболевания. Другими примерами острых функциональных заболеваний являются фибрилляция сердца, когда нарушается нормальная динамика стимуляции сердца, и эпилептические припадки, когда нарушается нормальная координация нервного возбуждения.
Вариант осуществления изобретения относится к группе заболеваний, называемых острыми функциональными заболеваниями. Острые функциональные заболевания содержат такие заболевания, при которых сущностью заболевания является дисфункция биологической динамики, когда ни один из биологических механизмов не поражен или не нарушен. Соответственно, некоторые острые функциональные заболевания можно рассматривать как нарушение биологической динамики иммунной системы. Лечение острых функциональных заболеваний можно рассматривать как восстановление биологической динамики или приведение биологической динамики к нормальному виду.
Когда в контексте применяют конкретный термин сепсис, такой контекст нельзя понимать как ограниченный сепсисом, а следует понимать, в широком смысле, как воспалительные заболевания, функциональные заболевания иммунной системы или острые функциональные заболевания в упомянутом контексте. Соответственно, ссылку на сепсис может использовать для удобства, когда фактический контекст равным образом применим к другим заболеваниям более обширной группы острых функциональных заболеваний или менее широкой группы воспалительных заболеваний или функциональных заболеваний иммунной системы.
В противоположность острым функциональным заболеваниям, например, рак является заболеванием, вызываемым поврежденными генами. Таким образом, течение ракового заболевания очень сильно отличается от течения острых функциональных заболеваний, так как рак развивается на протяжении намного большего времени (недель, месяцев или даже лет), рак отличается не динамичным, а более монотонным характером, и, поэтому, рак легче прогнозировать, по меньшей мере, на такой короткий срок, как несколько недель.
Следовательно, при раке опухолевые клетки являются поврежденными модификациями тех клеток, которые раньше были нормальными собственными клетками, и, поэтому, целью лечения является уничтожение опухолевых клеток. При остром функциональном заболевании необязательно имеет место какое-то нарушение каких-либо клеток иммунной системы, поэтому лечение не нацелено на уничтожение каких-либо упомянутых клеток. Разумеется, патогенные клетки (клетки возбудителя инфекции) должны уничтожаться, если сама иммунная система не способна сделать это. Заболевание состоит в том, что поведение множества таких клеток начинает отклоняться от здоровой реакции, которая обычно возвращает организм в гомеостаз (стабильное состояние организма). Поэтому цель лечения состоит в том, чтобы так или иначе модифицировать передачу сигналов между упомянутыми клетками, чтобы восстановить здоровую динамику управления. Упомянутая задача осложняется тем, что упомянутая система, в результате развития, стала очень стойкой; система является многократно избыточной, чем объясняются многочисленные неудачи при использовании предназначенных для этого монолекарств.
Острые функциональные заболевания обычно можно классифицировать по характеру динамики, вовлекающей быстрые изменения различных данных о состоянии здоровья или показателей пациента, например уровня патогенных факторов и различных типов лейкоцитов. Например, постоянные времени, описывающие динамику воспаления, явно отличаются от постоянных времени при раковом заболевании, так как динамика воспаления может развиваться за время от нескольких минут до нескольких часов, тогда как припадки и фибрилляции (особенно острые функциональные заболевания) развиваются даже за время от нескольких секунд до нескольких минут. Соответственно, данные о состоянии здоровья, связанные с острыми функциональными заболеваниями, могут значительно изменяться в течение нескольких часов, например в течение 4 часов, в течение 2 часов или даже в течение 1 часа. Однако данные о состоянии здоровья, связанные с конкретными воспалительными заболеваниями, могут изменяться еще быстрее, например в течение одного часа, в течение нескольких минут, например от 1 до 30 минут, или даже в течение нескольких секунд, например от 1 до 30 секунд.
Аналогично, острые функциональные заболевания могут развиться в фатальное состояние, приводящее к смерти в течение нескольких часов, например в течение 4 часов, в течение 2 часов или даже в течение 1 часа. Инфаркт, вызванный острым функциональным заболеванием, может оказаться фатальным через несколько минут, например от 1 до 5 минут.
Таким образом, быстрое развитие динамики острых функциональных заболеваний устанавливает конкретные требования к медицинским устройствам содействия в отношении способности отслеживать и прогнозировать течение упомянутых заболеваний, которые отличаются от аналогичных устройств для других заболеваний, например раковых заболеваний.
Фиг.1 показывает медицинское устройство 100 для содействия клиницисту при организации лечения острого функционального заболевания, например, посредством содействия клиницисту в выборе подходящей терапии. Медицинское устройство можно эквивалентно называть клинической системой содействия принятия решений. Медицинское устройство 100 содержит блок 101 ввода для приема показателей пациента, характеризующих биологические и/или физиологические показатели пациента, и для приема данных по терапии, характеризующих показатели методов лечения или лекарственных терапий.
Биологические показатели относятся, например, к данным измерений проб крови, в которых определяют присутствие или количество конкретных биологических веществ или биомолекул с использованием различных медицинских устройств, например, для анализа. Упомянутые биологические показатели содержат, например, цитокины, факторы свертывания крови и активные кислородные радикалы и патогенные факторы.
Физические показатели содержат значения, полученные из данных измерений, например температуры тела, артериального давления, частоты сердечных сокращений, частоты дыхания и, возможно, количества белых кровяных телец (лейкоцитов) разных типов.
Биологические и физические показатели могут быть предоставлены в блок 101 ввода через средство 105 связи с некоторыми внешними медицинскими устройствами или устройствами для анализа.
Медицинское устройство 100 может, в одном варианте осуществления, дополнительно содержать пользовательский блок 102 ввода, с которого пользователь медицинского устройства, например клиницист, может снабжать медицинское устройство 100 другими показателями пациента. Например, клиницист может вводить показатели пациента, которые не предоставляются через средство 105 связи. С помощью пользовательского блока 102 ввода клиницист может также вводить данные по терапии или показатели. Данные по терапии содержат данные или значения, например, лекарственных терапий или лекарств, которые давались или скоро будут даны. Кроме того, данные по терапии могут быть введены в виде данных испытаний для проверки терапевтического эффекта возможной терапии. Пользовательский блок 102 ввода может быть клавиатурой или сенсорным планшетом.
Данные по терапии могут быть типом, дозировкой и частотой дозировки, например, антибиотика.
Медицинское устройство 100 дополнительно содержит вычислительный блок 103, способный обрабатывать данные пациента и данные лечения, предоставляемые из блока 101 ввода и/или пользовательского блока 102 ввода. Вычислительный блок выполнен с возможностью обработки биологических и физических показателей, полученных через средство 105 связи, а также биологических, физических и терапевтических показателей, полученных с пользовательского блока 102 ввода. Обработка данных выполняется с использованием модели заболевания, чтобы можно было прогнозировать развитие болезни пациента.
Медицинское устройство 100 дополнительно содержит блок 104 вывода, например графический пользовательский интерфейс 104 для содействия клиницисту в понимании развития заболевания и для содействия клиницисту при выборе эффективного вмешательства. С этой целью различные данные из вычислительного блока предоставляются в блок 104 вывода, при этом блок вывода выполнен с возможностью представления данных в форме, которая полезна и легко воспринимается клиницистом.
Блок 101 ввода, пользовательский блок 102 ввода, вычислительный блок 103 и блок 104 вывода могут быть отдельными блоками, связанными между собой. В альтернативном варианте, по меньшей мере, один из упомянутых блоков (101-104) может быть комбинированным. Например, пользовательский блок 102 ввода и блок вывода могут быть объединены в одно устройство. Вычислительный блок 103 может быть компьютером, выполненным с возможностью выполнения программного кода, составляющего модель заболевания, и обработки входных показателей из блока 101 ввода и пользовательского блока 102 ввода, с использованием модели. Кроме того, вычислительный блок 103 может быть выполнен с возможностью адаптации модели к показателям пациента и определения некоторых рекомендуемых методов терапии. Блок 104 вывода и/или пользовательский блок 102 ввода могут входить в состав, например, компьютера и монитора.
Блок 101 ввода, пользовательский блок 102 ввода и блок 104 вывода могут быть электронным устройством, например печатной платой, соединяемой или объединенной с вычислительным блоком 103. Пользовательский блок 102 ввода и блок 104 вывода можно соединить с мониторами для обеспечения сигнала, представляющего показатели или данные в монитор для отображения упомянутых показателей или данных.
Как будет ясно из нижеследующего, условием способности медицинского устройства содействовать клиницисту во время лечения пораженного сепсисом пациента является способность медицинского устройства прогнозировать развитие сепсиса пациента. Чтобы обеспечивать точные прогнозы заболевания, возможно, важно снабжать медицинское устройство 100 всеми биологическими и физическими показателями, которые имеют отношение к модели на данной стадии заболевания, и обеспечивать показатели с достаточно высокой частотой. В то же время важно также не подвергать пациента слишком многочисленным процедурам отбора проб, например проб крови, поскольку пациент может находиться в критическом состоянии, и поскольку отбор проб крови может подвергнуть пациента дополнительному риску новой инфекции. Кроме того, возможно, было бы желательно сократить затраты на аналитическое оборудование, применяемое для взятия биологических замеров.
Как также будет ясно из нижеследующего, существенным может быть требование, чтобы конкретное медицинское вмешательство выполнялось в конкретное время или в течение конкретного периода времени. Соответственно, выбор определенного времени является важным вопросом как с точки зрения представления показателей пациента в медицинское устройство 100, так и с точки зрения определения временного периода для осуществления терапии.
Кроме того, поскольку сепсис может развиваться по-разному от пациента к пациенту, то важно, чтобы медицинское устройство было способно к адаптации или индивидуализации модели к пациенту, и, более того, поскольку развитие сепсиса может изменяться в течение нескольких часов или даже минут, то важным требованием может стать возможность повторной адаптации модели к текущему состоянию сепсиса с использованием последних данных пациента.
Как изложено выше, важно, чтобы модель была способна включать существенные динамические и временные характеристики иммунного отклика на инфекцию, чтобы точно моделировать заболевания типа сепсиса. Нижеописанная модель с 3 переменными, описанная в работе «R. Kumar, G. Clermont, Y. Vodovotz, C.C. Chow, The dynamics of acute inflammation, The Journal of Theoretical Biology, 2004.04.044, 145-155», включенная в настоящую заявку посредством ссылки, представляет, в зависимости от начальных состояний и значений параметров, множество динамик заболевания, которые наблюдались в клинике. Упомянутая относительно простая модель включает в себя только биологическую, биомолекулярную или клеточную динамику и не включает в себя физиологические данные пациента. Модель состоит из следующих трех обыкновенных дифференциальных уравнений:
dp/dt=k p p(1-p)-k pm mp (1) патогенный фактор (p)
dm/dt=(k mp p+l)m(1-m)-m (2) ранние противовоспалительные отклики (m)
dl/dt=k lm f(m)-k i l (3) поздние противовоспалительные отклики (l)
где 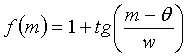 , и далее принято, что θ=1,0 и w=0,5.
, и далее принято, что θ=1,0 и w=0,5.
Переменными величинами состояния модели являются: p означает уровень численности патогенного фактора, ответственного за иммунный отклик и сепсис, m означает ранний противовоспалительный отклик (например, уровень цитокинов и макрофагов в сыворотке крови), и l означает поздний противовоспалительный отклик. Однако патогенный фактор (p) является возбудителем инфекции, содержащим, например, вирусы, бактерии, грибы или паразиты. Следовательно, измерения патогенных факторов могут обеспечивать информацию по развитию заболевания.
В дополнение к трем переменным величинам состояния существуют пять констант скорости, k. Упомянутые параметры являются константами скорости, где k ij означает скорость, с которой на скорость изменения переменной величины i влияет уровень переменной величины j; k i означает скорость, с которой на скорость изменения переменной величины i влияет его собственный уровень. Применяют также одну дополнительную модификацию модели: если переменная величина патогенного фактора снижается ниже порога (например, 0,0005), то вышеприведенные уравнения отбрасываются, и принимается, что патогенный фактор исключен. Без упомянутой модификации могут наблюдаться нереалистичные восстановления численности патогенных факторов, количества которых упали ниже уровня, который отражает менее чем одну клетку, и могут приводить, в результате, к ошибочным данным из вычислительного блока 103.
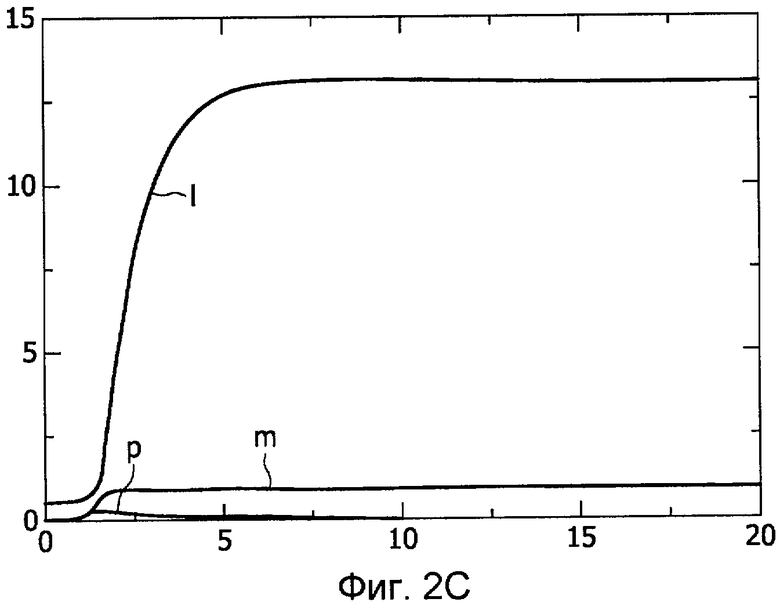
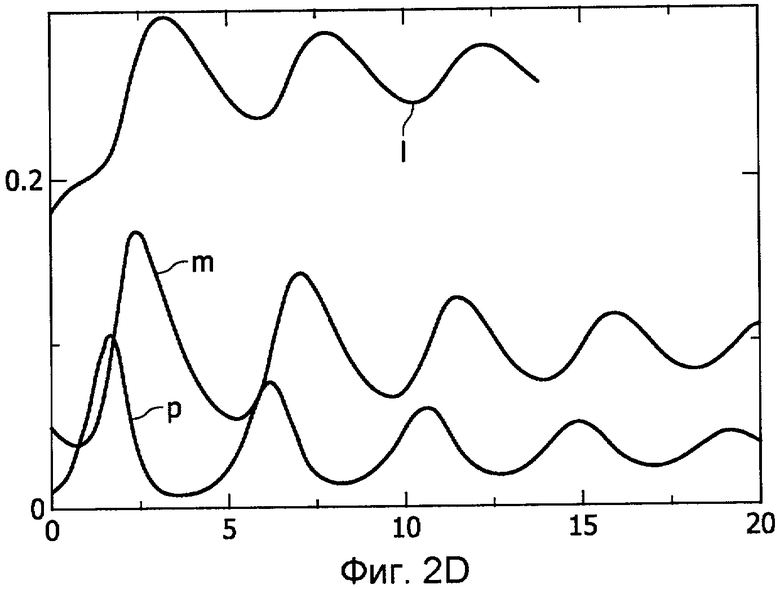
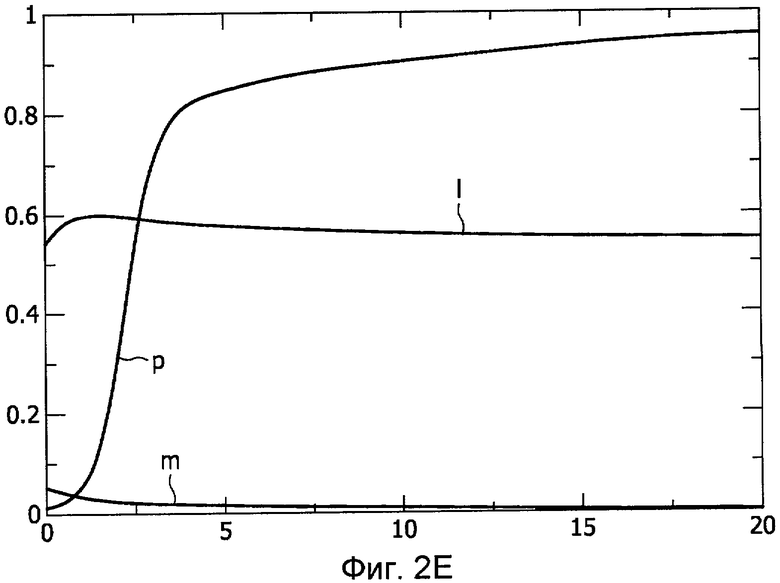
В нижеприведенной таблице показаны пять разных динамик, представляемых моделью. Все упомянутые динамики наблюдались в клинических условиях.
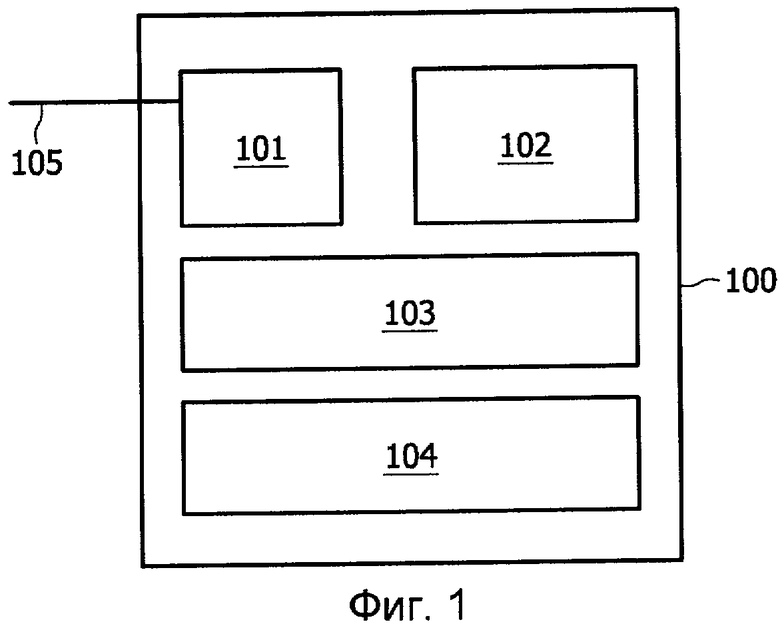
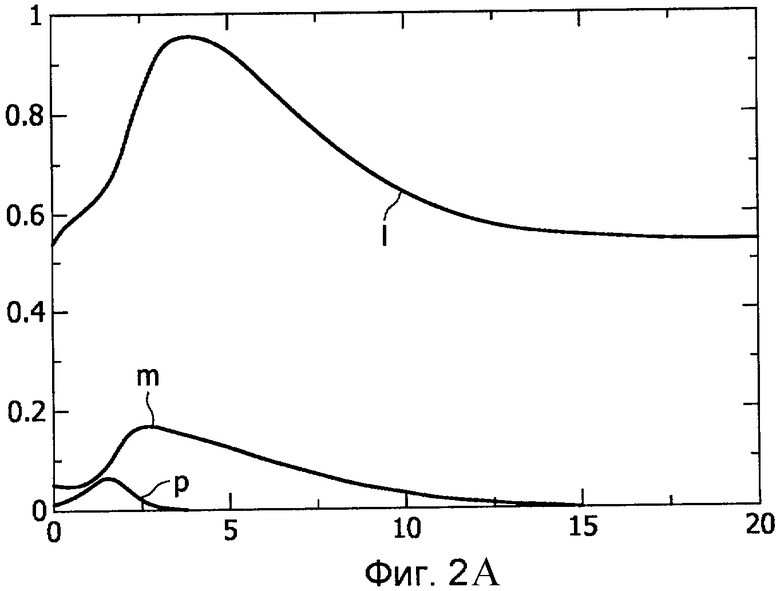
Упомянутые временные графики, соответствующие пяти динамикам, указанным в вышеприведенной таблице, показаны на Фиг.2A-E. Абсцисса представляет время в часах, и ордината представляет уровни патогенных факторов (p), ранний воспалительный отклик (m) и поздний воспалительный отклик (l), соответствующие кривым динамик. Следовательно, Фиг.2A показывает динамику здорового отклика, Фиг.2B показывает хроническое неинфекционное воспаление, Фиг.2C показывает хроническое инфекционное воспаление, Фиг.2D показывает рецидивирующую инфекцию, и Фиг.2E показывает тяжелый иммунодефицит.
Уравнения 1-3 можно решать любым подходящим математическим способом, посредством снабжения модели показателями пациента.
Для примера показа важности снабжения медицинского устройства 100 и модели достаточным числом данных пациента и с достаточной частотой данные p, m и l пациента с Фиг.2A используют для оценки k-параметров в уравнениях 1-3 путем снабжения модели замерами данных p, m и l пациента с Фиг.2A. k-параметры можно оценить используя способ наименьших квадратов или аналогичные способы минимизации/оптимизации/оценки, известные специалисту, для вычисления таких k-значений, которые обеспечивают максимальное согласование данных пациента с моделью. Следовательно, оценка k-параметров соответствует адаптации модели к показателям пациента.
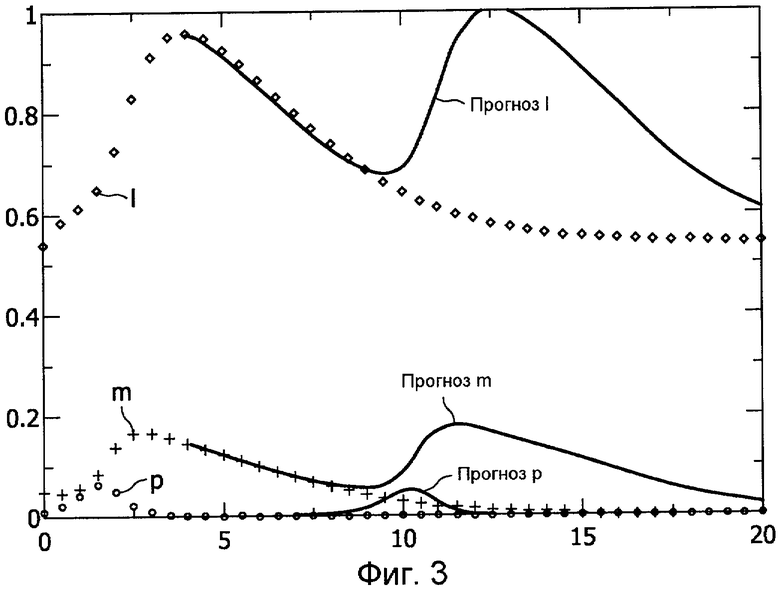
Таким образом, динамику p, m и l на Фиг.2A можно наблюдать как динамику фактических данных пациента реального пациента. В первом примере k-параметры, показанные в нижеприведенной таблице 2, оценивают на основе всего 9 проб, собранных путем отбора данных пациента с Фиг.2A с периодичностью 2 пробы в час. Следовательно, таблица 2 показывает истинные параметры с Фиг.2A и оцененные параметры.
Фиг.3 показывает показатели (p, l, m) пациента c Фиг.2A в сравнении с прогнозируемой динамикой (Xp, Xl, Xm) пациента. Фиг.3 показывает, что прогнозы на ближайшее будущее являются хорошими, но что заметно отклонение, начинающееся с приблизительно 9-го часа, приблизительно, через 5 часов после последнего наблюдения.
Прогнозируемые показатели (Xp, Xl, Xm) пациента определяют посредством снабжения медицинского устройства 100 начальными показателями пациента. Начальные показатели пациента содержат, по меньшей мере, одно значение или набор значений показателей (p, l, m) пациента, указанные точками на Фиг.3. Затем модель адаптируют к начальному, по меньшей мере, одному показателю или набору значений начальных показателей (p, l, m) пациента. Чтобы непрерывно адаптировать модель соответственно текущему состоянию здоровья пациента, медицинское устройство 100 снабжают новыми последними показателями (p, l, m) пациента, которые в комбинации с, по меньшей мере, одним начальным показателем пациента используют для повторной адаптации модели. Соответственно, серию начальных показателей пациента и последних показателей пациента используют для непрерывной адаптации модели посредством непрерывной адаптации k-параметров.
Фиг.3 иллюстрирует важность использования достаточного числа показателей пациента, полученных с достаточно высокой частотой отбора проб. Следовательно, частоту отбора проб следует выбирать с точным учетом самой быстрой ожидаемой динамики заболевания. В примере на Фиг.3 патогенный фактор (p) был, по существу, ликвидирован к, приблизительно, 3-му часу, с последующим снижением иммунного отклика (l и m) на несколько часов после ликвидации. Девять проб, взятых с получасовыми интервалами, смогли собрать основную часть данных динамики, и поэтому оценки и прогнозы были справедливыми. Более сложные модели содержат большее число параметров. Ввиду ограничений, касающихся частоты, с которой можно отбирать кровь из больных пациентов, и скорость, с которой можно получать данные биологических или биомолекулярных измерений, возможно, было бы полезно, если бы медицинское устройство могло снабжать пользователя или клинициста информацией о том, что биологические показатели должны быть предоставлены в медицинское устройство 100, и с какой частотой они должны быть предоставлены, для обеспечения точного прогнозирования динамичного развития заболевания.
Сравнение между спрогнозированными показателями пациента и фактическими показателями пациента, как показано на Фиг.3, показывает важность адаптации модели к текущему состоянию здоровья пациента на основе последних данных пациента. Четко видно, что чем больше число проб для последних данных пациента, которые доступны для адаптации модели к прошлым данным о состоянии здоровья пациента, тем точнее становится модель. Однако поскольку сепсис или другие воспалительные заболевания можно диагностировать только в последней стадии, и поскольку воспалительные заболевания могут развиваться быстро и изменять характер неожиданно, то, с точки зрения клиницистов, может быть полезно непрерывно адаптировать модель к текущему состоянию здоровья пациента на основе самых последних данных пациента. Таким образом, чтобы модель была способна прогнозировать будущие показатели пациента, даже в случае, когда заболевание изменяется неожиданно, используют не только девять проб из примера на Фиг.3, но используют также последующие пробы данных пациента для непрерывного обновления модели. При этом медицинское устройство 100 способно прогнозировать неожиданные изменения показателей пациента, когда, например, клиницист не смог прогнозировать упомянутое неожиданное изменение. Как очевидно, способность содействия клиницисту при прогнозировании упомянутых неожиданных изменений была бы значительным преимуществом.
Поскольку модель уже может быть адаптирована к основной динамике данных пациента, то, в одном варианте осуществления, продолжающуюся адаптацию модели к показаниям пациента можно выполнять с более низкой частотой, при сохранении достаточной точности прогнозов для пациента. Таким образом, в то время, как первые 9 проб получены с частотой 2 пробы в час, продолжающийся ввод показателей пациента в медицинское устройство 100 может быть выполнен с более низкой частотой. Поэтому, в одном варианте осуществления, способ содействия клиницисту содержит этап предложения времени (т.е. значений времени отбора проб) для снабжения медицинского устройства 100 новыми показателями пациента, полученными из биологических/физиологических анализов новых проб. Предлагаемые значения времени для обеспечения новых показателей пациента могут базироваться на скорости изменения конкретных показателей (p, l, m ) пациента или частоте динамики, установленной вычислительным блоком 103, например, с использованием собственных значений модели. В качестве альтернативы или дополнительно, предлагаемые значения времени для обеспечения новых показателей пациента могут быть основаны на показателях, вводимых в пользовательский блок 102 ввода, например, вычислены как компромиссные значения между вычисленными значениями времени и значениями времени, введенными посредством пользовательского блока 102 ввода.
Например, если измеренные показатели пациента, предоставляемые в блок 101 ввода, начинают все ближе подходить к прогнозируемым показателям пациента, то, возможно, показатели пациента достаточно обеспечивать реже, так как прогнозы становятся более точными. Если состояние пациента далеко от прогнозируемой границы (см. Фиг.8, Фиг.9 и сопутствующее описание, касающееся прогнозируемых границ), то конечный результат оказывается менее неопределенным, и обеспечение высокой точности менее важно, и, поэтому, показатели пациента достаточно обеспечивать реже. И, наоборот, если состояние пациента близко к границе между, например, жизнью и смертью, возможно, полезно чаще обеспечивать показатели пациента. Кроме того, если измеренные показатели пациента расходятся с прогнозируемыми показателями пациента, то значения пациента следует чаще предоставлять в медицинское устройство 100, так как степень достоверности клинического прогноза становится менее надежной.
Прогнозы показателей пациента (показанные на Фиг.3 или другие прогнозируемые показатели пациента) можно использовать, чтобы содействовать клиницисту путем адаптации медицинского устройства 100 для обеспечения информации по организации лечения заболевания, определенной из прогнозируемых показателей пациента, например, при наблюдении, что уровень патогенного фактора повышается, и ожидаемый воспалительный отклик не повышается, и, тогда, состояние здоровья пациента может изменяться в сторону конкретного клинического состояния (например, иммунной недостаточности), которое требует конкретного вмешательства (например, лекарственной терапии конкретным антибиотиком). Аналогично, информация по организации лечения заболевания может определяться из прогнозируемых показателей пациента, например, если уровень патогенного фактора, по прогнозу, должен снизиться до нуля, но воспалительный отклик, по прогнозу, должен продолжать подъем выше уровней для здорового состояния, то состояние пациента может изменяться в сторону конкретного клинического состояния (например, гипервоспаления), которое требует конкретного вмешательства (например, противовоспалительных лекарств).
Прогнозы показателей пациента (показанные на Фиг.3 или другие прогнозируемые показатели пациента) можно использовать, чтобы содействовать клиницисту в понимании того, как будет развиваться сепсис, и, на основе такого понимания, клиницист сможет решать, какое вмешательство следует начинать. Однако, при расширении модели для включения взаимосвязи между показателями пациента и лекарствами для вмешательства, клиницист получит возможность прогнозировать эффект разных намеченных вмешательств и поэтому возможность выбирать конкретное вмешательство с требуемым результатом.
Подобная модель, которая включает в себя вмешательства в форме антибиотикотерапии и/или противовоспалительной терапии, описывается уравнениями 4-9.
dp/dt=k p p(1-p)-k pm mp-k pb bp/(c b+b) (4) патогенный фактор (p)
dm/dt=(k mp p+l)m(1-m)-m-k mi im/(c i+i) (5) ранние противовоспалительные отклики (m)
dl/dt=k lm f(m)-k i l (6) поздние противовоспалительные отклики (l)
db/dt=r(t,t start_b ,t stop_b , period b , dose b , duty b)-k b b (7) уровень антибиотика в сыворотке крови (b)
di/dt=r(t,tstart_i, tstop_i, period i , dose i , duty i)-k i i (8) уровень противовоспалительного средства в сыворотке крови (i)
где:
r(t,t start ,t stop , period, dose, duty) (9) генератор режима дозирования является функцией, которая допускает широкий диапазон режимов дозирования.
Функция r может быть, например, генератором прямоугольных импульсов с периодом, равным часам периода (period), амплитудой, равной дозе (dose) (DP на Фиг.4), и, при этом, рабочий цикл (duty) (D) означает время в процентах от периода, в течение которого применяют лекарственную терапию. Весь режим ограничен временным интервалом от t a до t b. Параметр период (period) (P) можно интерпретировать в смысле «доза каждый час в период». Параметры c b и c i являются частью фармакокинетики и подобно k pb, k b, k mi и k i считаются известными свойствами выбранных лекарств. Функция r генератора режима дозирования показана на Фиг.4.
Таким образом, медицинское устройство может снабжаться терапевтическими значениями, например, по меньшей мере, одним из параметров: b, i, доза (dose), период (period), рабочий цикл (duty), t a, t b. Значения могут быть обеспечены настройкой конфигурации пользовательского блока 102 ввода таким образом, чтобы клиницист мог вручную вводить терапевтические значения. Дополнительно или в качестве альтернативы, терапевтические значения могут быть обеспечены из устройств с помощью средства 105 связи.
Упомянутый перечень терапевтических значений нельзя понимать как исключительный перечень, т.е. равным образом применимы другие терапевтические значения. Многие методы терапии, доступные клиницистам, включают в себя средства, нацеленные на специфические пути в отклике иммунной системы, включая метаболические пути коагуляции и арахидоновой кислоты, метаболические пути специфических эндотоксинов (например, LPS), про- и противовоспалительных факторов, антиоксиданты и прочие.
Чтобы пояснить, как расширенную модель, описываемую уравнениями 4-9, можно использовать для содействия клиницисту при выборе подходящего вмешательства, Фиг.5A-B показывают пример антибиотикотерапии, примененной к динамике тяжелого иммунодефицита (показанной на Фиг.2E), и Фиг.6A-B показывают пример противовоспалительной терапии, примененной к динамике хронического неинфекционного воспаления (показанной на Фиг.2B).
В первом сценарии, в котором применяется антибиотикотерапия, предполагается, что быстрого роста численности патогенных факторов в случае иммунодефицита не отмечено до 3-го часа. В этом сценарии патогенный фактор характеризуется таким низким k mp, что не запускает иммунный отклик, т.е. патогенный фактор назван невидимым патогенным фактором.
На основе математической модели, показателей пациента, введенных в блок 101 ввода, блок 104 вывода медицинского устройства 100 может, в одном варианте осуществления, представлять прогноз показателей пациента, как показано на Фиг.2E. Благодаря упомянутому выводу, клиницисту содействуют при выборе из возможных методов терапии. Однако, перед фактическим осуществлением выбранной терапии, клиницисту может потребоваться проверка того, как выбранная терапия влияет на показатели пациента для конкретного пациента. Поэтому медицинское устройство 100 выполнено с возможностью предоставления клиницисту возможности вводить показатели, характеризующие антибиотикотерапию через пользовательский блок 102 ввода.
Таким образом, клиницист может выбрать лекарственную терапию с характеристиками k pb=5, k b=1 и c b=1 (полученными из знаний о патогенном факторе и антибиотике), и, при этом, данные о дозировании лекарства задаются дозой (dose)=2, периодом (period)=2, рабочим циклом (duty)=20, t a=4 и t b=12 представляются в медицинское устройство 100 либо вручную, с использованием пользовательского блока 102 ввода, либо электронными средствами, через средство связи с внешним устройством, например устройством дозирования лекарства.
Медицинское устройство 100 формирует выходные данные, например, как показано на Фиг.5A, посредством блока 104 вывода, предоставляющего клиницисту руководящее указание для понимания терапевтического эффекта от потенциальной лекарственной терапии.
Фиг.5A показывает, что патогенный фактор испытывает воздействие, но не сильное. Второй опытный режим увеличивает рабочий цикл до 100% и дозу до 4, чему соответствуют рабочий цикл (duty)=100 и доза (dose)=4. Как показано на Фиг.5B, данный режим лекарственной терапии более эффективен.
Примеры на Фиг. 5A и 5B показывают важность выбора эффективного вмешательства. В этой связи эффективное вмешательство зависит от данных о дозировании лекарства (дозы (dose), периода (period), рабочего цикла (duty), t a и t b). Таким образом, посредством предоставления клиницисту возможности проверки разных значений лекарственной дозы и разных значений, связанных с распределением времени, т.е. значений периода (period) и рабочего цикла (duty), и, в частности, значения начала терапии, заданного параметром t a, клиницисту позволяют найти наиболее эффективную терапию.
В другом примере с пациентом, страдающим гипервоспалением с последующей иммунной недостаточностью, как известно, очень большое значение для успеха терапии имеет время начала (t a) противовоспалительной терапии. Таким образом, благодаря предоставлению клиницисту возможности проверки разных временных стратегий путем проверки терапевтического эффекта при разных значениях периода (period), рабочего цикла (duty), t a и t b, исключается или, по меньшей мере, снижается риск выбора фатального времени t a начала.
Во втором сценарии противовоспалительная терапия применяется к динамике хронического неинфекционного воспалительного процесса (показанного на Фиг.2B). Посредством применения противовоспалительной терапии с 5-го часа (после того, как патогенный фактор уничтожен обычной иммунной системой) в течение одного часа, с k mi=2, k i=1, c i=1, period i=1, dose=2, duty=100, получен требуемый результат, как показано на Фиг.6A. С предоставлением информации, показанной на Фиг.6A, клиницисту содействуют от медицинского устройства 100 для выполнения упомянутой гипотетической лекарственной терапии. Однако из упомянутых представленных показателей (p, m, l) пациента и терапевтического значения (i) клиницист может сделать выбор для регулировки упомянутого режима дозирования с целью поиска минимального режима, который обеспечивает требуемое ослабление гипервоспаления. Чтобы проверить упомянутый новый режим дозирования с дозой (dose)=0,3 и рабочим циклом (duty)=30, соответствующие значения подают в медицинское устройство 100, которое генерирует результат проверки, аналогичный показанному на Фиг.6B. На Фиг.6B показано, что уточненный режим дозирования благоприятнее, чем режим дозирования, показанный на Фиг.6A.
С медицинским устройством 100 можно применить другие модели, отличающиеся от моделей, описанных уравнениями 1-9. Следовательно, можно применить более сложные модели на основе большего числа переменных величин (p, l, m, b, i) и параметров k, например, можно использовать модели, содержащие 18 переменных величин и 80 параметров, для создания более сложных оценок. Модели могут быть основаны на дифференциальных уравнениях, модели могут включать в себя случайные величины, и модели могут содержать статистические модели.
Фиг.7 показывает пользовательский блок 701-703, 102 ввода и блок 704, 104 вывода, или, точнее, Фиг.7 показывает пользовательский интерфейс 701-703 блока 102 ввода и пользовательский интерфейс 704 блока 104 вывода, при этом пользовательские интерфейсы 701-704 объединены в один пользовательский интерфейс 700. Кроме того, пользовательский интерфейс 700 содержит кнопки 705 для запуска медицинского устройства 100 на считывание показателей пациента из блока 101 ввода и пользовательского блока 102 ввода, для запуска адаптации модели к данным пациента и для запуска формирования выходных сигналов для блока 104 вывода с целью содействия клиницисту при принятии решения по надлежащему вмешательству. Соответственно, пользовательский интерфейс может применяться в связи с медицинским устройством 100 клиницистом или другими пользователями для проверки разных вмешательств.
Графики, показывающие прогнозируемое развитие показателей пациента и предполагаемые режимы дозирования лекарств в виде, показанном на Фиг.5-6, несомненно, служат полезным инструментарием для содействия клиницисту при принятии решения о том, какое вмешательство следует осуществлять, когда следует осуществлять вмешательство (t a), и какими должны быть период дозирования и рабочий цикл (period, duty).
Соответственно, блок 104 вывода в связи с пользовательским интерфейсом 704 выполнен с возможностью вывода информации по организации лечения заболевания для содействия клиницисту. При использовании прогнозируемых показателей пациента можно определять различные виды информации по организации лечения заболевания, например: предложения, касающиеся, по меньшей мере, одного вмешательства, временные данные для содействия клиницисту при выполнении вмешательства, и оценки степени достоверности 1102 (Фиг.11) прогнозируемых показателей 1101 пациента (Фиг.11), позволяющие клиницисту судить о надежности прогнозов.
Кроме того, блок 104 вывода в связи с пользовательским интерфейсом 704 выполнен с возможностью вывода прогнозируемых траекторий (811-813) пациента, областей (801-804) состояния здоровья и вмешательств (820), как показано на Фиг.8A-B.
В одном варианте осуществления изобретения вычислительный блок 103 можно использовать для анализа введенных показателей пациента и данных по терапии с режимами дозирования лекарств, чтобы снабжать клинициста альтернативным или дополнительным инструментарием для содействия клиницисту через блок 104 вывода. Примеры такого инструментария показаны на Фиг.8A-B.
Фиг.8A показывает карту 800 областей (801-803) состояния здоровья для распознавания результатов изменения состояния здоровья в пространстве (p, m) модели, которые были определены посредством снабжения адаптированной модели (например, модели, составленной уравнениями 1-3) данными (p, m и l) пациента, оценками k и, возможно, также данными (b, i) лечения для прогнозирования результатов изменения состояния здоровья.
Для конкретного примера, показанного на Фиг.8A-B, карту 800 определили посредством, во-первых, приравнивания производной от l к нулю (установки уравнения 3 равным нулю) для создания 2-мерной плоскости p-m. Во-вторых, пространство начальных состояний (p, m, l) систематически сканируется, и модель используется для вывода результата по окончательному состоянию здоровья из начальных состояний. Результаты по окончательному состоянию здоровья классифицируются в соответствии с разными определениями состояния здоровья, например динамиками изменения состояния здоровья, отраженными в таблице 1: здоровым откликом, хроническим неинфекционным воспалением, хроническим инфекционным воспалением, рецидивирующей инфекцией и тяжелым иммунодефицитом.
На карте, показанной на Фиг.8A, разные результаты 801-803 изменения состояния здоровья обозначены разными символами, т.е. кружками, точками и т.п. Указаны также области 801-803 разных результатов 801-803 изменения состояния здоровья. На Фиг.8A область 801 относится к желательным здоровым откликам (как показано на Фиг.2A), область 803 относится к хроническому неинфекционному воспалению (как показано на Фиг.2B), и область 802 относится к недостоверной области, в которой модель не способна прогнозировать показатели пациента с достаточной достоверностью.
Фиг.8B показывает карту областей 801-804 состояния здоровья, использующую такую же модель, как на Фиг.8A, но с k pm, увеличенным с 30 до 40 для моделирования повышения эффективности раннего воспаления в ходе борьбы с патогенным фактором. Вследствие повышения k pm область 801 благоприятного результата изменения состояния здоровья расширилась, и появилась новая область 804. Область 804 является нежелательной областью, так как начальные состояния в данной области приводят к динамике с рецидивирующей инфекцией, как показано на Фиг.2D.
Фиг.8B показывает, как можно использовать карту 800 областей состояния здоровья для содействия клиницисту при организации лечения пациента посредством определения для пациента положения текущих показателей 810 пациента на карте и определения траекторий 811-813 результатов изменения состояния здоровья пациента в пространстве (p, m) модели путем снабжения адаптированной модели данными по лечению с целью прогнозирования траекторий. В одном сценарии траектория 811 показывает, что для состояния здоровья пациента прогнозируется развитие в область 801 здорового отклика. В другом сценарии траектория 812 показывает, что для заболевания пациента прогнозируется сначала развитие к области 801 здорового отклика, однако затем заболевание пациента будет развиваться в сторону от области 801 здорового отклика. В третьем сценарии траектория 813 прогнозирует развитие заболевания в нежелательную область рецидивирующей инфекции 804.
Разные траектории могли быть вызваны разными вмешательствами, которые проверяются клиницистом с использованием пользовательского интерфейса 700.
Следует понимать, что карты 800 моделей, включающих в себя больше переменных величин (p, l, m), чем три переменные величины, например 5, 10 или 18 переменных величин, можно визуализировать аналогично Фиг. 8A-B, например, посредством генерации 3 или 4 двумерных карт 800 для визуализации карт модели с 5 переменными величинами.
Области 801-804 состояния здоровья и траектории 811-813 пациента могут служить клиницисту для решения о том, какое вмешательство следует применить. Например, если траектория 811 на Фиг.8B представляет развитие данных (p, l, m) пациента в ответ на конкретную лекарственную терапию, то упомянутая траектория рекомендует клиницисту продолжить запланированную лекарственную терапию и продолжить адаптацию модели к текущему состоянию здоровья пациента на основе самых последних данных (p, l, m) пациента.
В другом сценарии траектория 812 пациента на Фиг.8B информирует клинициста, что в данной точке в момент времени Ta данные пациента будут приближаться к границе области 801 здорового отклика. Расстояние 820 траектории 812 пациента в момент времени Ta от границы области 801 здорового отклика можно использовать для предложения стратегий вмешательства. Например, возможно применение антибиотиков для сдвига p вниз или противовоспалительных средств для сдвига m вниз. Такой сценарий показывает в одном варианте осуществления изобретения, как медицинское устройство 100 может способствовать клиницисту при принятии решения о том, какое вмешательство будет благоприятным для пациента, и о времени вмешательства, то есть вмешательство следует начинать в момент времени Ta для обеспечения максимальной эффективности, или, возможно, вмешательство следует начинать до Ta, чтобы траектория повернула в область, приблизительно, в момент времени Ta подобно тому, как космический аппарат будет прикладывать кратковременную обратную тягу двигателя до входа в гравитационное поле Земли, чтобы двигаться достаточно медленно для попадания в упомянутое поле. Упомянутый пример воплощает пример информации по организации лечения заболевания, содержащей временные данные.
Соответственно, в одном варианте осуществления, карта 800 областей состояния здоровья, траектории пациента, границы или их комбинации воплощают вывод информации по организации лечения в блок 104 вывода.
Фиг.9 показывает пример медицинского устройства 901, 100, содержащего блок 902, 104 вывода. Медицинское устройство 901 снабжается показателями пациента, содержащими биологические и физиологические значения, посредством средства 105 связи. Значения пациента могут быть определены биологическим анализатором 903 и физиологическим анализатором 904, которые снабжаются пробами, взятыми от пациента 905. Соответственно, биологический анализатор 903 и физиологический анализатор 904 являются внешними устройствами, которые обеспечивают показатели пациента в медицинское устройство 901 через средство 105 связи или при посредстве пользовательского блока 102 ввода.
Блок 902 вывода показывает карту 920, аналогичную картам 800, показанным на Фиг. 8A и 8B. Карта 920 показывает область 911 здорового отклика и область 910 нездорового отклика. Показатели пациента от предшествующих трех проб показаны в виде наблюдений 913. При использовании модели, адаптированной к пациенту 905, прогнозируемое течение 914 заболевания, когда не начинают никакого вмешательства, получают посредством вычислительного блока 103. В одном варианте осуществления изобретения медицинское устройство 901 может обладать способностью рекомендации вмешательств(а), которые(ое), вероятно, должны двигать состояние здоровья пациента в область 911 здорового отклика. Рекомендуемое вмешательство может изображаться стрелкой 915, и терапевтический эффект вмешательства показан прогнозируемой кривой 916, которая дает в результате стабильный благоприятный результат 917 изменения состояния здоровья.
Показатели пациента, предоставляемые в блок 101 ввода, могут испытывать воздействие шумов или неопределенностей, например, обусловленных принципами измерений. Кроме того, даже небольшие ошибки показателей пациента, используемых для установки начальных состояний модели, или небольшие ошибки оценок k-параметров (k p , k mp , k lm) могут приводить к сильно различающимся прогнозам результатов из-за нелинейностей модели.
В одном варианте осуществления изобретения допустимые отклонения показателей пациента учитываются в способе, в котором всем показателям пациента и оцененным константам скорости (k-параметрам) на основе показателей пациента свойственна некоторая неопределенность. Знание неопределенности, характерной для технологий измерения, можно использовать для задания двух показателей, высокого (выше обеспечиваемого показателя) и низкого (ниже обеспечиваемого показателя), которые устанавливают обоснованные пределы для вероятного истинного показателя. Аналогичный подход можно принять для оцененных констант скорости, с использованием других критериев, например картины изменения предшествующих оценок, использующей меньшее число наблюдений. Для иллюстрации упомянутого подхода используют просто фиксированную процентную часть (1% вниз и 0,5% вверх) от номинальных значений для формирования упомянутых высоких/низких пар. После этого модель выполняют для каждой комбинации одного из трех значений (высокого, номинального, низкого) для каждой из возмущенных переменных величин (для модели, задаваемой уравнениями 4-9, существует 3 переменных величины (p, l, m) состояния, b=0 и i=0 без какой-либо неопределенности, и 5 констант скорости (k-параметров)). При каждом выполнении модели отслеживают внешнюю огибающую всех вычисленных траекторий.
При использовании описанного подхода графики прогнозируемых траекторий 1101 можно расширять построением верхней и нижней огибающих 1102 вычисленных траекторий (пунктирных линий), как показано на Фиг.11. В показанном случае график относится к случаю гипервоспаления, когда огибающая указывает, что возмущения демонстрируют связанные отклонения от номинальных прогнозов.
Вышеописанные результаты указывают клиницисту, что, хотя время наступления и пик гипервоспаления могут вызывать некоторые сомнения, само событие несомненно (в пределах исполненных возмущений). Следовательно, обеспечение оценок степени достоверности может снабдить клинициста полезными рекомендациями, полученными на основе упомянутых выводов, относительно требуемых методов терапии и их наилучшего планирования во времени.
Соответственно, информация по организации лечения заболевания, представляемая в блок 104 вывода, может, в дополнение к показу прогнозируемых показателей 1101 пациента, показывать оценки степени достоверности 1102, например, в форме огибающих 1102, чтобы визуализировать точность прогнозируемых показателей 1101 пациента.
Фиг.10 показывает этапы способа в соответствии с вариантом осуществления изобретения.
На этапе 1001 медицинское устройство 100 снабжают показателями пациента посредством средства 105 связи с блоком 101 ввода или пользовательским блоком 102 ввода.
На этапе 1002 динамическую модель адаптируют к текущей динамике пациента с использованием множества показателей пациента. В примере адаптация модели содержит оценку k-параметров. В альтернативном варианте осуществления необязательно следует использовать все показатели пациента для адаптации модели к показателям пациента. Например, можно отбрасывать крайние или ненадежные показатели пациента.
На необязательном этапе 1003 прогнозируют ход изменения состояния здоровья пациента, когда не выполняется никаких вмешательств, с использованием адаптированной модели, посредством прогнозирования будущих показателей пациента. За необязательным этапом 1003 может следовать вывод прогнозируемых показателей пациента в блок 104 вывода.
На этапе 1004 динамическую модель непрерывно адаптируют к динамике пациента, с использованием последних показателей пациента и с использованием множества начальных показателей пациента, для получения уточненной модели. Последние показатели пациента предоставлялись в медицинское устройство после начальных показателей пациента. Следует понимать, что динамическую модель повторно адаптируют каждый раз, когда новые показатели пациента предоставляют в блок 101 ввода или пользовательский блок 102 ввода. Непрерывная адаптация продолжается, пока требуется.
На этапе 1005 определяют прогнозируемые показатели пациента с использованием уточненной модели (самой последней адаптированной модели). Прогнозируемые показатели пациента можно, по желанию, использовать для определения хода изменения состояния здоровья пациента, когда не выполняется никаких вмешательств. В альтернативном варианте осуществления прогнозируемые показатели пациента определяют с использованием уточненной модели и терапевтических значений (b, i) вмешательств. Терапевтические значения могут быть значениями лекарственной терапии, которая уже проведена, или терапевтические значения могут быть значениями лекарственной терапии, которая еще не проведена, но проверяется на медицинском устройстве 100 для прогнозирования терапевтического эффекта конкретной лекарственной терапии.
На этапе 1006 в блок 104 вывода медицинского устройства 100 выводят информацию по организации лечения заболевания для содействия клиницисту при организации лечения острого функционального заболевания. Информацию по организации лечения заболевания определяют из прогнозируемых показателей пациента.
Порядок этапов 1001-1006 необязательно должен быть показанным и описанным порядком, например, этап 1006 можно дополнительно выполнять между необязательным этапом 1003 и этапом 1004.
В вариантах осуществления изобретения медицинское устройство может обслуживать несколько пользователей. Сестры могут использовать систему для контроля текущих трендов. Система может помогать клиницистам посредством генерации соответствующего выходного сигнала, например, тревоги, плана терапии или рекомендации по вмешательству. Кроме того, система может прогнозировать будущий тренд пациента на основе текущих и гипотетических вмешательств. Кроме того, администраторы больницы могут использовать отдельный экземпляр системы или совокупность таких систем для поддержки при планировании ресурсов (площадей, клиницистов, оборудования), управления запасами и обеспечения качества, что является лишь немногими примерами.
Выше настоящее изобретение описано на примере конкретных вариантов осуществления, однако предполагается, что изобретение нельзя ограничивать конкретной формой, представленной в настоящей заявке. Более того, объем настоящего изобретения ограничен только прилагаемой формулой изобретения. В формуле изобретения термин «содержащий» не исключает присутствия других элементов или этапов. Кроме того, хотя отдельные признаки могут быть включены в разных пунктах формулы изобретения, упомянутые признаки можно с пользой сочетать, и включение в разные пункты формулы изобретения не подразумевает, что комбинация признаков невозможна и/или не дает преимуществ. В дополнение, ссылки на единственное число не исключают множественного числа. Следовательно, ссылки на единственное число, выражаемые как «первый», «второй» и т.п., не исключают множественного числа. Кроме того, позиции в пунктах формулы изобретения не подлежат толкованию в смысле ограничения объема.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА И СПОСОБ ДЛЯ ОЦЕНКИ ЗДОРОВЬЯ ПАЦИЕНТА НА ОСНОВАНИИ РЕАКЦИИ ВОССТАНОВЛЕНИЯ ПОСЛЕ ПАДЕНИЯ НАСЫЩЕНИЯ КРОВИ КИСЛОРОДОМ | 2013 |
|
RU2659140C2 |
| СИСТЕМА ПОДДЕРЖКИ ПРИНЯТИЯ КЛИНИЧЕСКИХ РЕШЕНИЙ | 2007 |
|
RU2468434C2 |
| ОЦЕНКА И НАБЛЮДЕНИЕ ОСТРОГО ПОВРЕЖДЕНИЯ ЛЕГКИХ (ALI)/СИНДРОМА ОСТРОЙ ДЫХАТЕЛЬНОЙ НЕДОСТАТОЧНОСТИ (ARDS) | 2013 |
|
RU2629799C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ НАСТУПЛЕНИЯ СЕПСИСА У ДЕТЕЙ ПРИ ОСТРЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЯХ | 2014 |
|
RU2562103C1 |
| Способ оценки риска развития венозных тромбоэмболических осложнений у раненых и тяжелопострадавших | 2016 |
|
RU2657196C2 |
| СПОСОБ ПОЭТАПНОГО ОБЗОРА ОБСЛУЖИВАНИЯ ПАЦИЕНТА | 2011 |
|
RU2657856C2 |
| ПРО-АДМ В КАЧЕСТВЕ МАРКЕРА МОНИТОРИНГА ТЕРАПИИ ДЛЯ КРИТИЧЕСКИ БОЛЬНЫХ ПАЦИЕНТОВ | 2018 |
|
RU2782305C2 |
| Способ предоперационного прогнозирования послеоперационной пневмонии в плановой абдоминальной хирургии | 2024 |
|
RU2841149C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОСТРОГО ПОВРЕЖДЕНИЯ ПОЧЕК ПРИ ИНФАРКТЕ МИОКАРДА У МУЖЧИН МОЛОЖЕ 60 ЛЕТ | 2022 |
|
RU2784943C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПАЦИЕНТА, ОСНОВАННЫЙ НА КЛАСТЕРНОМ АНАЛИЗЕ БОЛЬШИХ ДАННЫХ | 2021 |
|
RU2800315C2 |
Настоящее изобретение относится к медицинскому устройству (901, 100) для содействия клиницистам, медсестрам или другим пользователям при выборе вмешательства для лечения пациента, страдающего острым функциональным заболеванием, например, сепсисом. Технический результат - моделирование острых функциональных заболеваний и прогнозирование будущих показателей пациентов при организации лечения заболевания. Медицинское устройство основано на способе, снабжают медицинское устройство начальными показателями пациента, адаптируют модель к динамике пациента с использованием множества начальных показателей пациента, представленных в медицинское устройство, продолжают адаптировать модель к динамике пациента с использованием последних показателей пациента и с использованием множества начальных показателей пациента, для получения уточненной модели, при этом упомянутые последние показатели пациента представлены в медицинское устройство после начальных показателей пациента, определяют прогнозируемые показатели пациента с использованием уточненной модели, обрабатывают допустимые отклонения показателей пациента для оценки степени достоверности прогнозируемых показателей пациента, выводят информацию по организации лечения заболевания и оцененную степень достоверности в блок вывода медицинского устройства. 3 н. и 10 з.п. ф-лы, 18 ил., 2 табл.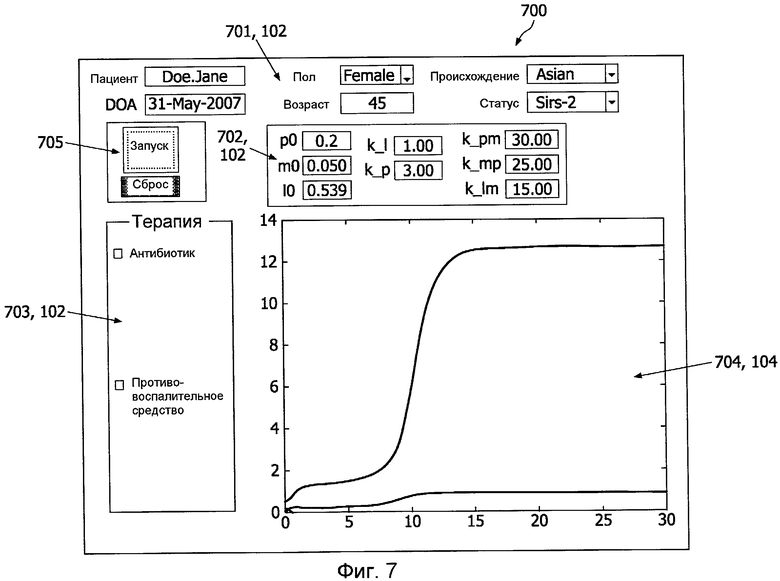
1. Способ содействия клиницисту при организации лечения острого функционального заболевания пациента с использованием медицинского устройства (100), содержащего блок (101) ввода для приема показателей (р, l, m) пациента, характеризующих биологические и/или физиологические показатели пациента, при этом упомянутое медицинское устройство дополнительно содержит вычислительный блок (103) для обработки данных пациента с использованием модели острого функционального заболевания, при этом способ содержит этапы, на которых:
- снабжают медицинское устройство (100) начальными показателями пациента,
- адаптируют модель к динамике пациента с использованием множества начальных показателей пациента, представленных в медицинское устройство,
- продолжают адаптировать модель к динамике пациента с использованием последних показателей пациента и с использованием множества начальных показателей пациента для получения уточненной модели, при этом упомянутые последние показатели пациента представлены в медицинское устройство после начальных показателей пациента,
- определяют прогнозируемые показатели (Хр, Xl, Хm) пациента с использованием уточненной модели,
- обрабатывают допустимые отклонения показателей пациента для оценки степени достоверности (1102) прогнозируемых показателей (1101) пациента,
- выводят информацию по организации лечения заболевания и оцененную степень достоверности (1102) в блок (104) вывода медицинского устройства (100) для содействия клиницисту при организации лечения острого функционального заболевания, при этом информацию по организации лечения заболевания определяют из прогнозируемых показателей пациента.
2. Способ по п.1, в котором информация по организации лечения заболевания содержит вмешательство, при этом вмешательство определяют с использованием прогнозируемых показателей пациента.
3. Способ по п.2, в котором информация по организации лечения заболевания содержит временные данные для выполнения вмешательства, при этом временные данные определяют с использованием прогнозируемых показателей пациента.
4. Способ по п.1, в котором медицинское устройство (100) выполнено с возможностью приема терапевтических значений (b, i, доза (dose), период (period), рабочий цикл (duty), ta, tb) вмешательств, и при этом прогнозируемые показатели пациента определяют с использованием уточненной модели в связи с терапевтическими значениями.
5. Способ по п.1, дополнительно содержащий этап определения времени отбора проб для снабжения медицинского устройства новыми показателями пациента, полученными из биологических и/или физиологических анализов.
6. Способ по п.5, в котором время отбора проб определяют из предыдущих показателей пациента.
7. Способ по п.5, в котором время отбора проб является периодическим с фиксированной частотой.
8. Способ по п.1, дополнительно содержащий этап определения областей (801-804) состояния здоровья для распознавания результатов изменения состояния здоровья в пространстве (р, m) модели посредством снабжения адаптированной модели данными (р, m, l) пациента для прогнозирования результатов изменения состояния здоровья.
9. Способ по п.1, дополнительно содержащий этап определения траекторий (811-813) результатов изменения состояния здоровья пациента в пространстве (р, m) модели.
10. Способ по п.1, в котором блок (104) вывода выполнен с возможностью показа, по меньшей мере, одной информации по организации лечения заболевания, выбранной из перечня, содержащего прогнозируемые траектории (811-813) пациента, области (801-804) состояния здоровья и вмешательства (820), для содействия клиницисту.
11. Способ по п.1, в котором острое функциональное заболевание является воспалительным заболеванием.
12. Медицинское устройство (100) для содействия клиницисту при организации лечения острого функционального заболевания пациента, при этом медицинское устройство содержит блок (101) ввода для приема показателей (р, l, m) пациента, характеризующих биологические и/или физиологические показатели пациента, и вычислительный блок (103) для обработки данных пациента с использованием модели острого функционального заболевания, при этом:
- блок ввода дополнительно выполнен с возможностью его снабжения начальными показателями пациента и последними показателями пациента, представляемыми после начальных показателей пациента,
- вычислительный блок дополнительно выполнен с возможностью адаптации модели к динамике пациента с использованием множества первых показателей пациента и продолжения адаптации модели к динамике пациента с использованием последних показателей пациента и с использованием множества начальных показателей пациента для получения уточненной модели,
- вычислительный блок дополнительно выполнен с возможностью определения прогнозируемых показателей (Хр, Xl, Хm, 1102) пациента с использованием уточненной модели,
- вычислительный блок дополнительно выполнен с возможностью обработки допустимых отклонений показателей пациента для оценки степени достоверности (1102) прогнозируемых показателей (1101) пациента, и причем упомянутое медицинское устройство дополнительно содержит блок (104) вывода, выполненный с возможностью показа информации по организации лечения заболевания и оцененной степени достоверности (1102) для содействия клиницисту при организации лечения острого функционального заболевания, причем информацию по организации лечения заболевания определяют из прогнозируемых показателей пациента.
13. Вычислительный блок, содержащий компьютерную программу, предписывающую процессору выполнять способ по п.1.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЙ БОЛЬНОГО ИНФАРКТОМ МИОКАРДА | 2000 |
|
RU2197173C2 |
Авторы
Даты
2013-02-20—Публикация
2008-07-11—Подача