ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области биофармацевтики, и более конкретно, касается производных соединений рецептора фактора некроза опухоли (TNF-ФНО) и их использования в фармацевтических препаратах.
УРОВЕНЬ ТЕХНИКИ
Фактор некроза опухоли (TNFα) [ФНО-альфа], представитель суперсемейства фактора некроза опухоли, обладает биологической активностью модуляции иммунологической реакции, клеточного апоптоза, клеточной дифференцировки и т.п. TNFα имеет два внутриклеточных рецептора, TNF рецептор 1 (TNFRp55) и TNF рецептор 2 (TNFRp75). Сверхсинтез TNFα является основным механизмом аутоиммунных заболеваний, как например, ревматоидный артрит. Блокирование избыточного TNFα его антагонистами, включающими растворимые TNFRp75:Fc слитые белки, например, этанерцепт [Etanercept], и анти-TNF моноклональные антитела, например, инфликсимаб [Infliximab], было признано в качестве эффективного лечения ревматоидного артрита.
Этанерцепт может связываться как с TNFα, так и с лимфотоксином (LT), но требуется относительно большая клиническая доза, приблизительно 25-50 мг, которая может вызывать покраснение при введении путем подкожной инъекции. Следовательно, существует большая потребность разработки TNFRp75, который может связываться с фактором некроза опухоли и лимфотоксином с высокой аффинностью и, в свою очередь, необходимо разработать TNFRp75:Fc слитый белок в качестве антитела-лекарства.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Одна из целей настоящего изобретения состоит в создании растворимого рецептора, имеющего высокую нейтрализующую активность относительно TNFα и/или лимфотоксина, при этом уменьшается доза растворимого рецептора, необходимая для нейтрализации TNFα, повышается терапевтическое воздействие на аутоиммунные заболевания и снижается стоимость изготовления лекарственного средства.
Другая цель настоящего изобретения состоит в создании слитого белка, образованного между растворимым рецептором с более высокой нейтрализующей активностью и дополнительным аминокислотным фрагментом.
Еще одна цель настоящего изобретения - создание последовательности ДНК, кодирующей растворимый рецептор или слитый белок, указанные выше.
Еще одна цель настоящего изобретения - использование растворимого рецептора, имеющего более высокую нейтрализующую активность относительно TNFα и/или лимфотоксина, или его слитого белка в фармацевтических препаратах.
Целью настоящего изобретения также является создание фармацевтического состава, включающего растворимый рецептор или его слитый белок, указанные выше.
Авторами настоящего изобретения было проведено тщательное исследование структуры TNF рецептора 2, TNFα и LT с помощью моделирования молекулярной структуры и было установлено, что аминокислота в позиции 92 TNF рецептора 2 весьма важна для его связывания с TNFα и LT. Кроме того, авторы выполнили рациональную точечную мутацию в аминокислотной позиции 92 и получили растворимый мутант TNF рецептора 2, который имеет высокую нейтрализующую активность относительно TNFα и лимфотоксина.
В первом аспекте в настоящем изобретении описан растворимый мутант TNFRp75, в котором имеется замещение аминокислоты в аминокислотной позиции 92 последовательности дикого типа (SEQ ID NO.1). Нейтрализующая активность растворимого мутанта TNFRp75 против цитотоксичности TNFα и лимфотоксина увеличивается более чем на 30% по сравнению с диким типом.
В предпочтительном примере осуществления изобретения остаток глутаминовой кислоты (Е) в аминокислотной позиции 92 замещается одним из Asn, His, Ser, Ala, Lys или Gin. То есть аминокислота Е в позиции 92 последовательности, представленной в SEQ ID NO.1, замещается N, H, S, А, K или Q, соответственно. Ниже приведены типичные примеры.
Аминокислотная последовательность мутанта TNFRp75 (Е92Н), представленная в SEQ ID NO.2, в которой позиция 92 - это гистидин (His), а N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Аминокислотная последовательность мутанта TNFRp75 (E92A), представленная в SEQ ID NO.3, в которой позиция 92 - это аланин (Ala), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Аминокислотная последовательность мутанта TNFRp75 (E92N), представленная в SEQ ID NO.4, в которой позиция 92 - это аспарагин (Asn), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Аминокислотная последовательность мутанта TNFRp75 (E92S), представленная в SEQ ID NO.5, в которой позиция 92 - это серин (Ser), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
В некоторых предпочтительных примерах осуществления изобретения триптофан (Tip) в позиции 89 также замещается на Tyr, Phe, His, Lys, Met или Leu, дополнительно к замещению Glu (E) в позиции 92. Ниже приведены типичные примеры.
Аминокислотная последовательность мутанта TNFRp75 (Е92К W89Y), представленная в SEQ ID NO.6, в которой 89 - это тирозин (Tyr), позиция 92 - аспарагин (Asn), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Аминокислотная последовательность мутанта TNFRp75 (E92S, W89Y), представленная в SEQ ID NO.7, в которой позиция 89 - это тирозин (Tyr), позиция 92 - серин (Ser), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Аминокислотная последовательность мутанта TNFRp75 (E92N, W89F), представленная в SEQ ID NO.8, в которой позиция 89 - это фенилаланин (Phe), позиция 92 - аспарагин (Asn), a N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
Во втором аспекте в настоящем изобретении описан слитый белок, включающий растворимый мутант TNFRp75 и дополнительный аминокислотный фрагмент. Вышеупомянутый дополнительный аминокислотный фрагмент способствует усилению устойчивости и увеличению биологического времени полураспада мутанта TNFRp75.
Вышеупомянутый дополнительный аминокислотный фрагмент выбирают из группы, состоящей из константной области (Fc) человеческого иммуноглобулина (IgG) и одной из пяти функциональных областей альбумина.
Вышеупомянутый дополнительный аминокислотный фрагмент находится на С-конце мутанта TNFRp75.
В предпочтительном примере осуществления изобретения вышеупомянутый дополнительный аминокислотный фрагмент представляет собой 232 аминокислотных остатков константной области (Fc) человеческого иммуноглобулина (IgG). Слитый белок образуется растворимым мутантом TNFRp75 и 232 аминокислотами фрагмента Fc на С-конце человеческого IgG, с дополнительным соединяющим фрагментом или без дополнительного соединяющего фрагмента между этими двумя компонентами, предпочтительно без дополнительного соединяющего фрагмента. Ниже приведены типичные примеры:
аминокислотная последовательность TNFRp75 (Е92Н): Fc, представленная в SEQ ID NO.9;
аминокислотная последовательность TNFRp75 (Е92А): Fc, представленная в SEQ ID NO.10;
аминокислотная последовательность TNFRp75 (E92N): Fc, представленная в SEQ ID NO.11;
аминокислотная последовательность TNFRp75 (E92S): Fc, представленная в SEQ ID NO.12;
аминокислотная последовательность TNFRp75 (E92N, W89Y): Fc, представленная в SEQ ID NO.13;
аминокислотная последовательность TNFRp75 (E92S, W89Y): Fc, представленная в SEQ ID NO.14;
аминокислотная последовательность TNFRp75 (E92N, W89F): Fc, представленная в SEQ ID NO.15.
В третьем аспекте в настоящем изобретении описана последовательность ДНК, кодирующая растворимый рецептор или слитый белок, указанные выше. Как хорошо известно в данной области, последовательности ДНК, кодирующие растворимые рецепторы или слитые белки в соответствии с настоящим изобретением, могут изменяться в зависимости от кодон-дегенерации и кодон-смещения различных клеток-хозяев, но эти последовательности ДНК по-прежнему находятся в объеме настоящего изобретения, пока аминокислотные последовательности, кодируемые этими последовательностями ДНК, не изменяются.
В четвертом аспекте в настоящем изобретении описано использование растворимого мутанта TNFRp75 или слитого белка, указанных выше, в фармацевтических препаратах, в частности при лечении заболеваний, ассоциированных со сверхэкспрессией TNFα и/или лимфотоксина, включая, но не ограничиваясь этим, ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой.
В пятом аспекте в настоящем изобретении описан фармацевтический состав, включающий растворимый мутант TNFRp75 или слитый белок, указанные выше.
Мутанты TNFRp75 и их слитые белки в настоящем изобретении обладают повышенной способностью связывания с TNF и лимфотоксином. Например, нейтрализующая активность растворимого TNFRp75 (E92N): Fc относительно TNFα в 1,33 раза больше нейтрализующей активности растворимого TNFRp75: Fc дикого типа (ENBREL производства AMGEN), а нейтрализующая активность относительно LT в 2,77 раз больше нейтрализующей активности растворимого TNFRp75: Fc дикого типа (ENBREL производства AMGEN). Мутант TNFRp75 и его слитый белок в настоящем изобретении пригодны для лечения заболеваний, ассоциированных с TNFα и LT. Благодаря повышенной активности, клиническую дозу можно снизить, чтобы уменьшить вероятность появления покраснения при подкожном введении лекарственного средства. Кроме того, увеличение времени диссоциации в пересчете на TNFα связывание будет эффективно в течение продленного времени действия лекарственного средства.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1-6: Нейтрализация TNFRp75 мутанта: Fc слитого белка против цитотоксичности TNFα или LT28-171, в каждом эксперименте TNFRp75 дикого типа: Fc слитый белок используются в виде контрольного образца.
Фигура 1А: Нейтрализация TNFRp75 (Е92А): Fc слитого белка против цитотоксичности TNFα.
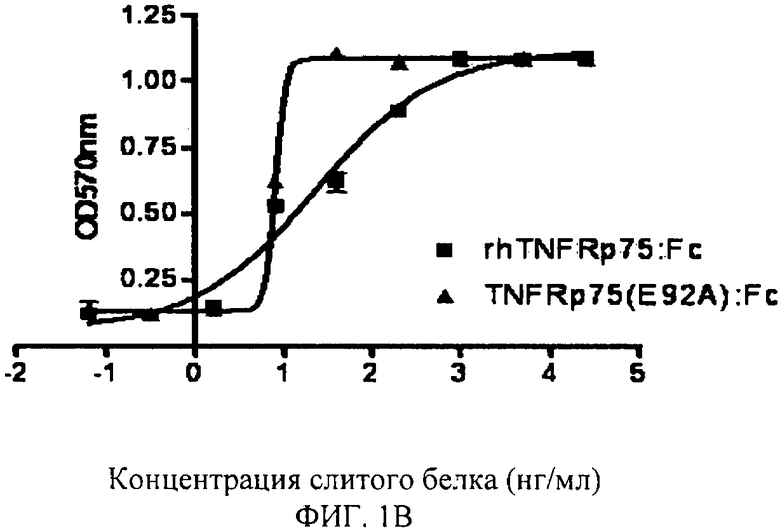
Фигура 1В: Нейтрализация TNFRp75 (Е92А): Fc слитого белка против цитотоксичности LT28-171.
Фигура 2А: Нейтрализация TNFRp75 (Е92Н): Fc слитого белка против цитотоксичности TNFα.
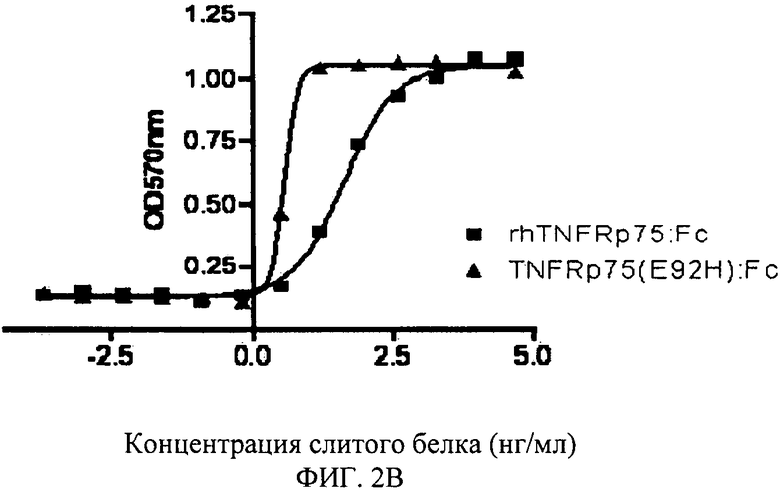
Фигура 2В: Нейтрализация TNFRp75 (Е92Н): Fc слитого белка против цитотоксичности LT28-171.
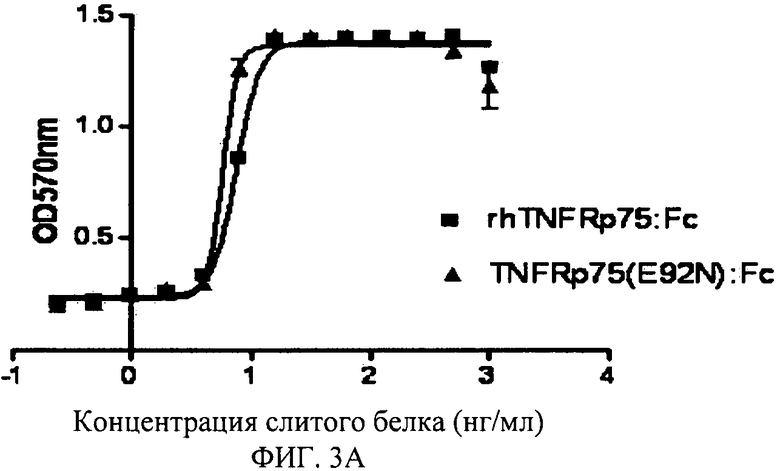
Фигура 3А: Нейтрализация TNFRp75 (E92N): Fc слитого белка против цитотоксичности TNFα.
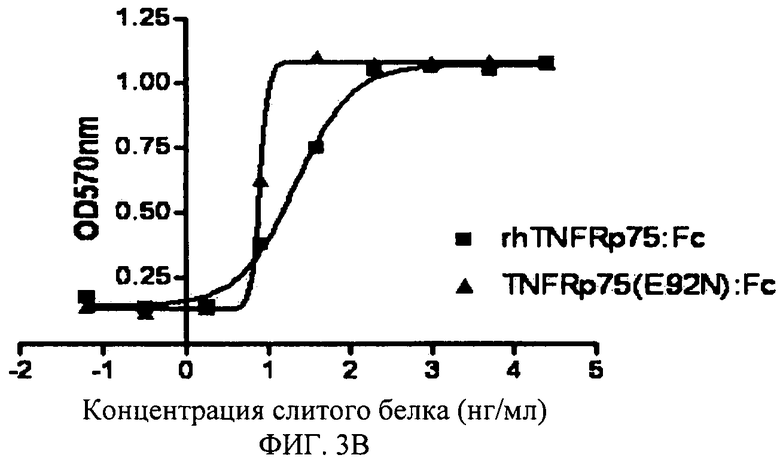
Фигура 3В: Нейтрализация TNFRp75 (E92N): Fc слитого белка против цитотоксичности LT28-171.
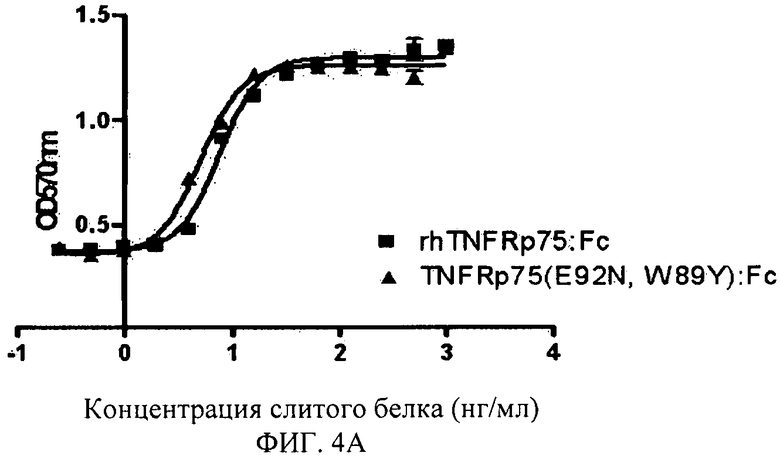
Фигура 4А: Нейтрализация TNFRp75 (E92N, W89Y): Fc слитого белка против цитотоксичности TNFα.
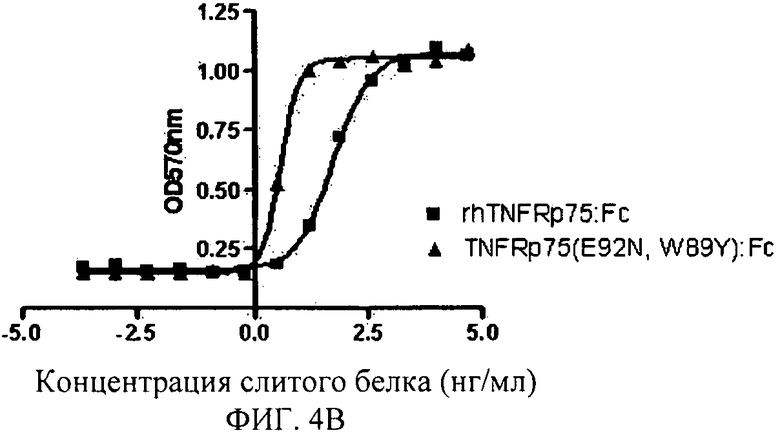
Фигура 4В: Нейтрализация TNFRp75 (E92N, W89Y): Fc слитого белка против цитотоксичности LT28-171.
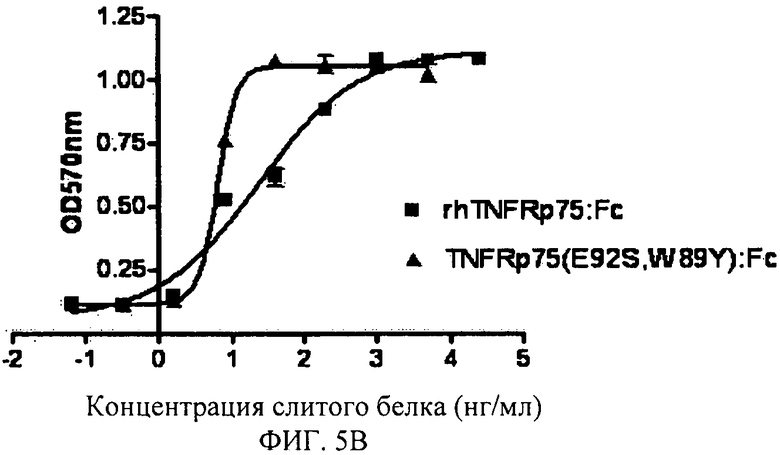
Фигура 5А: Нейтрализация TNFRp75 (E92S, W89Y): Fc слитого белка против цитотоксичности TNFα.
Фигура 5В: Нейтрализация TNFRp75 (E92S, W89Y): Fc слитого белка против цитотоксичности LT2S-171.
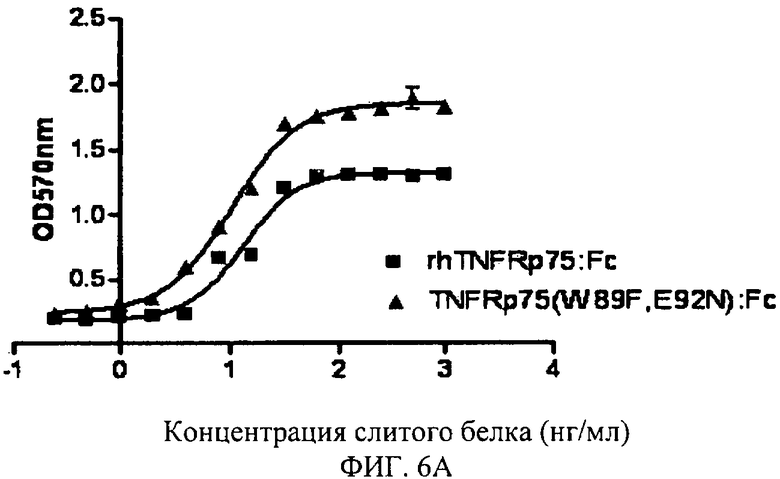
Фигура 6А: Нейтрализация TNFRp75 (E92N - W89F): Fc слитого белка против цитотоксичности TNFα.
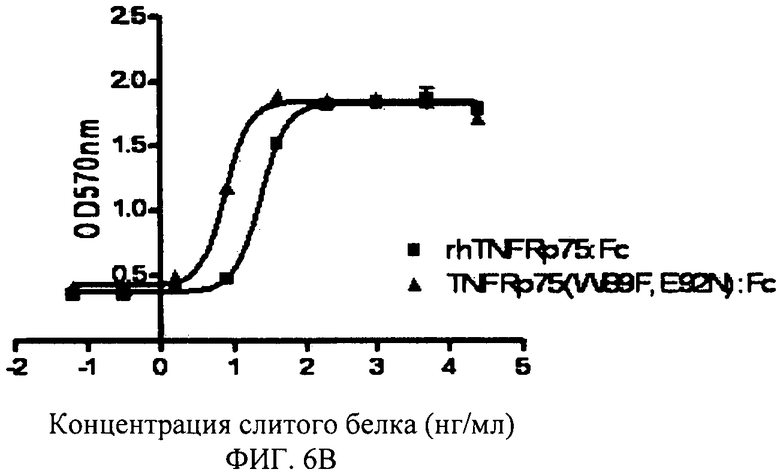
Фигура 6В: Нейтрализация TNFRp75 (E92N, W89F): Fc слитого белка против цитотоксичности LT28-171.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение иллюстрируется со ссылкой на нижеследующие примеры. Следует понимать, что примеры используются только для иллюстрации, но никоим образом не ограничивают объем изобретения. Эксперименты в нижеследующих примерах, в которых не указаны специфические экспериментальные условия, выполнены в обычно применяемых условиях или условиях, предлагаемых изготовителями. Если специально иначе не указано, соотношение и процентное содержание базируются на весе.
В соответствии с использованием в настоящем описании термины «TNF рецептор 2», «TNFRp75» и «TNFRp75 рецептор», которые могут использоваться как взаимозаменяемые, включают TNFRp75 рецептор, полученный от человека, а также его гомологи, полученные от мыши (или крысы), свиньи, лошади или коровы. Предпочтительно, чтобы это был человеческий TNFRp75 рецептор. Аминокислотная последовательность природного человеческого TNFRp75 рецептора дикого типа представлена SEQ ID NO.1.
«Растворимый TNFp75 рецептор» в соответствии с использованием в контексте настоящего изобретения относится к внеклеточной области TNFp75 рецептора, то есть связанному лигандом домену, состоящему из N-концевых аминокислотных остатков 1-257 человеческого TNFp75 рецептора дикого типа, в которых N-концевые аминокислотные остатки 1-22 представляют собой сигнальный пептид.
«Растворимый TNFp75 рецептор» или «растворимый мутант TNFp75 рецептора в настоящем изобретении» в соответствии с использованием в контексте настоящего изобретения означает мутант TNFp75 рецептора, который обладает повышенной способностью связывания с TNF, предпочтительно, как минимум, в 2 раза больше такой способности дикого типа, и обладает повышенной способностью связывания с LT, предпочтительно, как минимум, в 10 раз выше. Такой мутант может быть создан путем вставки, удаления или замещения аминокислоты, предпочтительно путем замещения аминокислоты. Например, Е92Н означает, что в мутанте His замещает Glu в позиции 92 последовательности дикого типа, при нумерации аминокислоты в соответствии с последовательностью широкого типа.
«Замещение аминокислоты» в соответствии с использованием в контексте настоящего изобретения относится к экспериментально индуцированной замене одной или нескольких аминокислот в полипептиде, белке или фрагменте белка другой или несколькими другими аминокислотами при помощи генно-инженерной или искусственной синтетической технологии.
TNFp75 мутантный белок в настоящем изобретении может быть создан синтезированием праймеров в соответствии с последовательностью человеческого растворимого TNFp75 рецептора, уже известной в данной области, а затем амплифицированием кодирующей последовательности растворимого TNFp75 рецептора ПЦР методом; альтернативно, кодирующая последовательность растворимого TNFp75 рецептора может быть синтезирована искусственно. Специалистам в данной области известны технологии генетической модификации кодирующей последовательности растворимого TNFp75 рецептора, как например, технология точечного мутагенеза. Смотри, например, Мутагенез: Практический метод», M.J. McPherson, Ed., (IRL press, Оксфорд, Великобритания (1991), который включает, например, сайт-направленный мутагенез, кассетный мутагенез и мутагенную полимеразную цепную реакцию (ПЦР).
Методы конъюгации фрагмента, кодирующего растворимый TNFp75 рецептор, с другими фрагментами, кодирующими аминокислоты, известны специалистам в данной области. Например, последовательность ДНК, кодирующая слитый белок, можно получить такими способами, как расщепление рестриктивного фермента, сшивание или комплементарные «липкие» концы.
Сайт-направленная мутантная последовательность ДНК, кодирующая мутантный белок в соответствии с настоящим изобретением, полученный как указано выше, затем вставляется в подходящий вектор экспрессии и, в свою очередь, трансформируется в подходящую клетку-хозяина. Наконец, трансформированная клетка-хозяин культивируют, а слитый белок получают путем разделения и очистки.
Векторы экспрессии, используемые в настоящем изобретении, можно выбрать из широкого спектра, как например, коммерческие векторы. Например, выбрали коммерческий вектор, и нуклеотидная последовательность, кодирующая мутантный белок в соответствии с настоящим изобретением, функционально связывается с регулирующей экспрессию последовательностью, тем самым создается вектор экспрессии белка.
«Функционально связанный с» в соответствии с использованием в контексте настоящего изобретения означает такую ситуацию, когда некоторые части линейной последовательности ДНК могут повлиять на активность других частей этой же последовательности ДНК. Например, если ДНК сигнального пептида участвует в секреции пептида как предшественник, она (лидерная последовательность для секреции) «функционально связана с» полипептид-кодирующей ДНК; если промотор управляет транскрипцией последовательности ДНК, она «функционально связана с» кодирующей последовательностью; а если сайт связывания рибосомы находится в позиции, которая обеспечивает его трансляцию, она «функционально связана с» кодирующей последовательностью. Вообще, «функционально связан с» означает соседство; однако, для лидерной последовательности для секреции это означает соседство в рамке считывания.
«Клетки-хозяева» в соответствии с использованием в контексте настоящего изобретения включают эукариотические клетки и прокариотические клетки. Обычно используемые прокариотические клетки включают Е.coli и Bacillus subtilis и т.д. Обычно используемые эукариотические клетки включают клетки дрожжей, клетки насекомых и клетки млекопитающих.
В примере изобретения способ получения растворимого TNFRp75: Fc слитого белка включает следующие стадии:
i. модификация последовательности, кодирующей растворимый TNFp75 рецептор дикого типа, для замены аминокислоты в позиции 92 и конъюгирование модифицированной последовательности с кодирующим Fc фрагментом, таким образом получается ген, кодирующий слитый белок;
ii. клонирование гена, кодирующего модифицированный растворимый TNFp75 рецептор: Fc слитый белок, полученный выше, в плазмиду экспрессии;
iii. трансформация клетки-хозяина плазмидой экспрессии, содержащей ген, кодирующий модифицированный растворимый TNFp75 рецептор: Fc слитый белок;
iv. культивирование трансформированной клетки-хозяина;
v. сбор клетки-хозяина и культурной среды, затем разделение и очистка растворимого TNFp75 рецептора: Fc слитого белка.
Растворимый TNFp75:Fc слитый белок в настоящем изобретении пригоден для лечения заболеваний, ассоциированных с TNF сверхэкспрессией, включающих, но не ограничивающихся этим, ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой и так далее.
Вышеупомянутый растворимый TNFp75:Fc слитый белок в настоящем изобретении может использоваться отдельно или в комбинации с другими препаратами, как например, препараты химиотерапии.
Настоящее изобретение, кроме того, описан фармацевтический состав, включающий эффективное количество одного или нескольких растворимых TNFp75:Fc слитых белков в соответствии с настоящим изобретением, и, как минимум, один фармацевтически приемлемый носитель, разбавитель или инертный наполнитель [эксципиент]. В общем, описанные выше составы можно приготовить смешиванием активного ингредиента и инертного наполнителя, разбавлением активного ингредиента инертным наполнителем или капсулированием активного ингредиента в носителе в форме, например, капсулы или пакетика-саше. Разбавитель может быть твердым, полутвердым или жидким. Состав может быть в форме таблеток, пилюль, порошков, растворов, сиропов и стерильных инъекционных растворов. Подходящие примеры инертных наполнителей могут включать один или несколько агентов из группы, состоящей из лактозы, глюкозы, сахарозы, сорбита, маннита, крахмала, микрокристаллической целлюлозы, поливинилпирролидона, целлюлозы, воды и т.д. Такие составы могут также содержать один или несколько агентов из группы, состоящей из разбавителей, эмульгаторов, консервирующих средств (как например, метил гидроксибензоат и пропил гидроксибензоат), и подслащивающие вещества.
Способы применения растворимого TNFp75:Fc слитого белка и фармацевтический состав в соответствии с настоящим изобретением особо не ограничиваются, они могут быть в виде, подходящем для перорального приема, для парэнтеральной инъекции или для местного применения, например, внутримышечная, внутривенная или подкожная инъекция, ингаляция или аэрозоль. Пероральное введение предпочтительно.
При пероральном применении в форме таблеток или капсул растворимый TNFp75:Fc слитый белок, как правило, вводится в виде однократной дозы в пределах 1-1000 мг для взрослого, имеющего средний вес 60-70 кг, или растворимый TNFp75:Fc слитый белок может вводиться парентерально в виде однократной дозы в пределах 0,1-500 мг. Его можно вводить один раз или несколько раз в сутки. Однократная доза фармацевтического состава обычно включает активный ингредиент в пределах 1-500 мг, обычно 1 мг, 5 мг, 10 мг, 25 мг, 50 мг, 100 мг, 200 мг, 300 мг, 400 мг или 500 мг.
При лечении специфических состояний доза и режим введения активного ингредиента в соответствии с настоящим изобретением будут зависеть от различных факторов, включая вес тела, возраст, пол, симптом, серьезность заболевания, лечение которого проводится, и специфического способа и частоты введения. Соответственно оптимальную дозировку может определить практикующий врач, который лечит конкретного пациента.
Растворимый человеческий TNFp75:Fc слитый белок широкого типа, используемый в настоящем изобретении, получен от AMGEN под торговым названием ENBREL. TNFα, используемый в настоящем изобретении, получен от R&D Company. LT28-171, используемый в настоящем, приготовлен по способу, описанному в китайской заявке №CN00111884.6.
Настоящее изобретение далее иллюстрируется со ссылкой на примеры. Следует понимать, что примеры только иллюстрируют изобретение, но не ограничивают объем изобретения. Эксперименты в нижеследующих примерах, в которых не указаны специфические экспериментальные условия, выполнены в обычно применяемых условиях, например, описанных в работе Sambrook, et al. Molecular clanging: a laboratory manual Самбрук и др., - Молекулярное клонирование: Практикум (New York: Cold Spring Harbor Laboratory Press, 1992), или условиях, предлагаемых изготовителями.
ПРИМЕРЫ
Пример 1. Получение TNFR75 (Е92Н): Fc слитого белка
(1) Создание гена, кодирующего TNFRp75 (E92H):Fc слитый белок.
Мутантная ДНК последовательность, кодирующая растворимый TNF р75 рецептор, была получена с помощью технологии SOE-PCR (сплайсинг перекрывающим удлинением PCR - Splicing by Overlapping Extension PCR), с использованием нуклеотидной последовательности, кодирующей растворимый человеческий TNFRp75: Fc слитый белок дикого типа в виде матрицы. Первая половина фрагмента ДНК, кодирующего растворимый TNF р75 рецептор, который включает сайт мутирования, была амплифицирована при помощи кодирующей ДНК растворимого TNFRp75: Fc слитого белка дикого типа в качестве матрицы и следующих праймеров:
TNFRp75p: aagcttatggctcccgtcgccgtctggg (SEQ ID NO.16) E92HpF1:
TGCTTGAGCTGTGGCTCCCG (SEQ ID NO.1 7)
Затем вторая половина фрагмента ДНК, кодирующего растворимый TNF р75 рецептор, который включает как сайт мутантации, так и фрагмент Fc, была амплифицирована при помощи следующих праймеров:
Fcp: gaattcctatttacccggagacaggg (SEQ ID NO.18)
E92HpR1: CGGGAGCCACAGCTCAAGCAgtgGGGAA (SEQ ID NO.19)
Наконец, фрагмент ДНК, кодирующий TNFRp75 (Е92Н): Fc слитый белок, был амплифицирован PCR [полимеразной цепной реакцией] с использованием двух полученных выше PCR продуктов (то есть первая половина и вторая половина фрагмента ДНК) в качестве матрицы и праймеров TNFRp75 и Fcp.
(2) Структура векторов экспрессии
После проверки секвенированием PCR продукты, полученные как указано выше, расщепили с помощью HindIII и EcoRI, затем вставили в коммерческий вектор экспрессии pcDNA3 (Invitrogen). Расщепление и сшивание выполняли согласно инструкции изготовителя.
(3) Трансфекция
Векторы экспрессии, кодирующие растворимый TNF р75: Fc слитый белок, были трансформированы в DH5α E.coli. Положительные клоны были расширены в 500 мл колбе для лизогенных культур, а затем ДНК извлекли и очистили с помощью набора для сверхчистой очистки плазмидной ДНК (Qiagen) согласно инструкции изготовителя. Плазмидную ДНК, полученную как указано выше, трансфицировали в клетки СНО-K1 (клетки яичника китайского хомячка, полученные от АТСС) с помощью липофектаминного набора производства Invitrogen согласно инструкции изготовителя.
(4) Скрининг клонов
Через 24-48 часов после трансфекции культурную среду заменили на скринирующую среду, содержащую G418 (Geneticin). Скринирующую среду заменяли каждые 3-4 дня, пока не образовались клоны клетки. Когда клоны клетки выросли до размера диаметром 1-2 мм, моноклональные антитела перенесли в 24-луночный планшет. После того, как клетки достигли 50-70% конфлуентности, супернатант в каждой лунке протестировали с помощью анализа ELISA, и клоны с высокой экспрессией TNFRp75 мутанта: Fc слитого белка отобрали для скрининга лекарственным средством. Уровень экспрессии TNFRp75 мутанта: Fc слитого белка в каждом клоне измерили при достижении максимальной концентрации лекарственного средства и два моноклональных клеточных штамма отобрали для хранения посева.
Анализ ELISA выполнили следующим образом:
Антитело (античеловеческое TNFRP75-специфическое моноклональное антитело, R&D Company) разбавили до 1 µг/мл в покрывающем буфере (CBS, рН9.6), нанесли на 96-луночный планшет (100 µл/лунку) и оставили на ночь при 5°С. Жидкость из лунки удалили, лунку промыли с помощью PBST 3 раза. После осушки в планшет добавили блокирующий раствор (1% BSA PBST) в объеме 400 µл/лунку и инкубировали в течение 2 часов при комнатной температуре, а затем промыли с помощью PBST 3 раза и осушили воздухом. Эталонный образец (Amgen, торговое название ENBREL) последовательно разбавили в разбавляющем растворе. Супернатант с экспрессированным белком разбавили до 1 µг/мл и добавили в дубликатные лунки 96-луночного планшета (100 µл/лунку). Планшет инкубировали в течение 1 часа при 37°С. После этого жидкость из лунок удалили, а лунки промыли 3 раза и высушили. Фермент-связанное антитело (HRP-античеловеческое IgG Fc-специфическое антитело, PIERCE) разбавили в разбавляющем растворе до определенной концентрации (1:20000), добавили в 96-луночный планшет (100 µл/лунку) и инкубировали в течение 1 часа при 37°С. Жидкость из лунок затем удалили, а лунки промыли 5 раз и высушили. Полученный смешанный с субстратом раствор добавили в 96-луночный планшет (100 µл/лунку) и инкубировали в течение 10 минут при 37°С. В лунки добавили стоп-реагент (50 µл/лунку) для остановки реакции. Значение оптической плотности [OD] считали при 490 nm, а содержание белка в образце рассчитали в соответствии с калибровочной кривой.
(5) Клеточная культура
1×105/мл клетки амплифицировали в 500-мл колбе для культур при 37°С в течение 3-4 дней. Пассирование: когда плотность клеток достигла 2×105/мл, клетки перенесли в 720-см2 роллерные флаконы и культивировали в течение 3-4 дней. Пассирование: 4×107 клетки перенесли в 1445-см2 роллерные флаконы и культивировали в течение 6 дней. Замена культурной среды: когда клеточная культура достигла платформы, культурную среду заменили на бессывороточную среду (SFM, Gibco Inc). Выход культурной среды: через 6 дней после выращивания в SFM супернатантную жидкость собрали и очистили с помощью Протеин-А афинной хроматографии с получением 8,7 мг TNFRp75 (E92H): Fc слитого белка.
Примеры 2-7. Получение других TNFRp75 мутант: Fc слитых белков
Ниже приведены общие праймеры для создания нуклеотидной последовательности, кодирующей TNFRp75(E92A): Fc, TNFRp75(E92N): Fc, TNFRp75(E92S): Fc, TNFRp75(E92N, W89Y): Fc, TNFRp75(E92S, W89Y): Fc и TNFRp75(E92N, W89F): Fc:
TNFRp75F: aagcttatggctcccgtcgccgtctggg (SEQ ID NO.16)
Fcp: gaattcctatttacccggagacaggg (SEQ ID NO.18)
Специфические праймеры для создания нуклеотидной последовательности, кодирующей TNFRp75(E92A): Fc. TNFRp75(E92N): Fc, TNFRp75(E92S): Fc, TNFRp75(E92Q): Fc, TNFRp75(E92N, W89Y): Fc, TNFRp75(E92S, W89Y): Fc и TNFRp75 (E92N, W89F): Fc приведены в таблице ниже:
Другие процедуры идентичны процедуре, указанной в Примере 1.
Пример 8. Анализ нейтрализующей активности TNFRp75 мутант: Fc слитый белок против LT28-171.
(1) Посев клеток
L929 клетки посеяли в 96-луночный титрационный микропланшет с плотностью 1,0×106 клеток/лунку. В каждую клетку экспериментальной группы добавили актиномицин D, 1 нг/мл LT28-171, и TNFRp75 (E92A):Fc с градиентными концентрациями, а в каждую клетку контрольной группы добавили актиномицин D, 1 нг/мл LT28-171, и rhTNFRp75:Fc дикого типа с градиентными концентрациями. 96-луночные планшеты инкубировали при 37°С, 5% СО2 в течение 24 часов.
(2) Измерение конечной точки
Культурную среду полностью удалили из 96-луночных планшетов. В каждую лунку добавили красильную жидкость в объеме 40 µл. Через 10 минут красильную жидкость удалили, а планшет промыли водой 3 раза, пока используемая вода не обесцветилась.
Остаточную воду оставили для высыхания как можно дальше. В каждую лунку 96-луночного планшета добавили обесцвечивающий раствор в объеме 100 µл/лунку и тщательно смешали. Планшеты считали с помощью фермент-меченого счетчика при 570 nm.
(3) Анализ результатов:
Результаты были автоматически проанализированы с помощью уравнения с четырьмя параметрами в программе обработки данных PraphPad Prism 4.0: ось Х - логарифм концентрации эталонного образца, а ось Y - значение OD570. Концентрация для 50% максимального эффекта (ЕС50) была также обеспечена программой, которая составила 7,93 нг/мл для нейтрализирующей активности TNFRp75 (E92A): Fc относительно LT, и 22,31 нг/мл для нейтрализирующей активности rhTNFRp75:Fc дикого типа относительно LT. Нейтрализующая активность мутанта против LT была увеличена на 291%. Кривая «S», построенная по экспериментальным результатам, показана на Фигуре 1.
Анализ нейтрализующей активности других TNFRp75:Fc мутантов против цитотоксичности LT28-171 был проведен аналогичным образом. Результаты показаны в таблице ниже. Кривая «S», построенная в соответствии с экспериментальными результатами, показана на Фигуре 2-6.
Пример 9. Анализ нейтрализующей активности TNFRp75: Fc мутанта против цитотоксичности TNFα.
L929 клетки посеяли в 96-луночный титрационный микропланшет с плотностью 1,0×106 клеток/лунку. В каждую клетку планшета добавили актиномицин D, 10 нг/мл TNFα и TNFRp75:Fc или их мутанты в градиентных концентрациях. 96-луночные планшеты инкубировали при 37°С, 5% CO2 в течение 24 часов.
Другие процедуры и обработка данных выполняются, как процедуры, описанные для Примера 8.
Результаты показаны в таблице ниже. Ось Х на фигуре - логарифм концентрации (нг/мл) слитого белка, а ось Y - поглощение света при 570 nm.
Кривая «S» построена в соответствии с экспериментальными результатами с помощью программы GraphPad Prism4.0, как показано на Фигуре 1-6.
Пример 10. Измерение константы связывания TNFRp75(E92N,W89Y):Fc для TNFα и LT.
(1) Материалы и приборы:
А. Лиганды TNF-α и LT, рецепторы rhTNFRp75: Fc и TNFRp75(E92N,W89Y):Fc 3,8 мг/мл.
В. HBS-P буфер (10 mM HEPES, 150 тМ NaCl, 3 mM EDTA, 0,005% (объем/объем) сурфактант Р20, рН 7,4).
С. Активирующий агент N-этил-N'-диметиламинопропил карбодиимид (EDC), N-гидроксисукцинимид (NHS), этаноламин и т.д., все приобретены у фирмы Sigma.
D. Приборы для измерения взаимодействия между биологическими макромолекулами: BIAcore3000, карбоксиметилцеллюлозный сенсорный чип (СМ5) (G.E. Inc.), приобретенный у фирмы GE.
(2) Методика
А. Конъюгация rhTNFRp75: Fc
rhTNFRp75: Fc конъюгировали с FC2 каналом СМ5 чипа с помощью метода аминоконъюгации, описанного в программе Wizard, Biacore3000. HBS-P использовали в качестве подвижного буфера, а 1 мг/мл rhTNFRp75: Fc разбавили до конечной концентрации 100 µг/мл в NaAC растворе (10 mM, рН4,0). EDC (0,2М) и NHS (50 mM) смешали в соотношении 1:1, а затем нанесли на поверхность чипа с расходом 10 µл/мин в течение 7 минут. После этого для блокировки активированной поверхности чипа ввели раствор рецептора, а затем ввели этаноламин (1М, рН8,5). Конечный объем конъюгации TNFRp75 составил 7043,6 условных единиц.
В. Конъюгация TNFRp75 (E92N, W89Y): Fc
TNFRp75 (E92N, W89Y): Fc конъюгировали с FC4 каналом СМ5 чипа с помощью метода аминоконъюгации, описанного в программе Wizard, Biacore3000. HBS-P использовали в качестве подвижного буфера, а 3,8 мг/мл TNFRp75 (E92N, W89Y): Fc разбавили до конечной концентрации 100 µг/мл в NaAC растворе (10 mM, рН4,0). EDC (0,2М) и NHS (50 mM) смешали в соотношении 1:1, а затем нанесли на поверхность чипа с расходом 10 µл/мин в течение 7 минут. После этого для блокировки активированной поверхности чипа ввели раствор рецептора, а затем ввели этаноламин (1М, рН8,5). Конечный объем конъюгации TNFRp75 (E92N, W89Y): Fc 6275,0 RU.
С. Первичный скрининг и кинетический анализ rhTNFRp75: Fc
Связывающую активность рецептора TNFRp75: Fc относительно TNF или LT измерили с помощью SPR (поверхностный плазменный резонанс). Лиганды разбавили в HBS-P буфере до концентрации 1 nm или 10 nm соответственно, а затем центрифугировали и инъецировали автоматически, чтобы измерить связывающую активность рецептора TNFRp75 относительно лигандов различных концентраций. Лиганды, продемонстрировавшие связывающую активность, подвергли кинетическому анализу.
Исходный раствор TNFα в концентрации 10 µг/мл (575 nM) последовательно разбавили в HBS-P буфере до 0 nM; 0,3125 nM; 0,625 nM; 1,25 nM; 2,5 nM; 5,0 nM; 10,0 nM и 20,0 nM.
Исходный раствор LT в концентрации 2,25 мг/мл (137 µМ) последовательно разбавили в HBS-P буфере до 0 nM; 0,3125 nM; 0,625 nM; 1,25 nM; 2,5 nM; 5,0 nM; 10,0 nM и 20,0 nM.
Взаимодействие рецептора и лиганда измерили при кинетическом анализе с помощью Wizard, Biacore3000. Все лиганды ввели при расходе 40 µл/мин в течение 1 минуты, диссоциировали в течение 2 мин, а затем 50 mM NaOH и HBS-P буфера ввели при расходе 100 µл/мин в течение 15 сек и 60 сек для регенерации лигандов (50 mM NaOH и HBS-P буфера ввели при расходе 100 µл/мин в течение 10 сек и 30 сек для регенерации при первичном скрининге). Чтобы обеспечить удельную константу скорости, экспериментальные данные адаптировали к 1:1 лангмюровской ассоциативной модели в программном обеспечении анализа Biacore3000.
D. Первичный скрининг и кинетический анализ TNFRp75(E92N, W89Y): Fc
Связывающую активность рецептора TNFRp75(E92N, W89Y): Fc относительно TNF или LT измерили с помощью SPR (поверхностный плазменный резонанс). Лиганды разбавили в буфере HBS-P до концентрации 1 nm или 10 nm соответственно, а затем центрифугировали и инъецировали автоматически, чтобы измерить связывающую активность рецептора TNFRp75(E92N, W89Y): Fc относительно лигандов различных концентраций. Лиганды, продемонстрировавшие связывающую активность, подвергли кинетическому анализу.
Исходный раствор TNFα в концентрации 10 (µг/мл (575 nM) последовательно разбавили в HBS-P буфере до 0 nM; 0,3125 nM; 0,625 nM; 1,25 nM; 2,5 nM; 5,0 nM; 10,0 nM и 20,0 nM.
Исходный раствор LT в концентрации 2,25 мг/мл (137 µM) последовательно разбавили в HBS-P буфере до 0 nM; 0,3125 nM; 0,625 nM; 1,25 nM; 2,5 nM; 5,0 nM; 10,0 nM и 20,0 nM.
Взаимодействие рецептора и лиганда измерили при кинетическом анализе с помощью Wizard, Biacore3000. Все лиганды ввели при расходе 40 µл/мин в течение 1 минуты, диссоциировали в течение 2 мин, а затем 50 mM NaOH и HBS-P буфера введи при расходе 100 µл/мин в течение 15 сек и 60 сек для регенерации лигандов (50 mM NaOH и HBS-P буфера ввели при расходе 100 µл/мин в течение 10 сек и 30 сек для регенерации при первичном скрининге). Чтобы обеспечить удельную константу скорости, экспериментальные данные приспособили к 1:1 лангмюровской ассоциативной модели в программном обеспечении анализа Biacore3000.
(3) Результаты:
А. Кинетические данные связывания rhTNFRp75: Fc для TNFα (аббревиатура TNF) и LT показаны ниже.
В. Кинетические данные связывания TNFRp75(E92N, W89Y):Fc для TNFα (аббревиатура TNF) и LT показаны ниже.
По сравнению с TNFRp75: Fc равновесная константа диссоциации (KD) TNFRp75 (E92N, W89Y) для TNFα или LT показала 2-3-кратное уменьшение, указывающее, что аффинность связывания TNFRp75 (E92N, W89Y) с TNFα или LT увеличилась. Кроме того, константа диссоциации (kd) TNFRp75 (E92N, W89Y) для TNFα была значительно ниже, чем у TNFRp75: Fc, показывая, что комплекс рецептора TNFRp75 (E92N, W89Y) и TNFα более устойчив in vitro, что может улучшить период полувыведения TNFRp75 (E92N, W89Y) in vivo.
Конкретный пример осуществления изобретения, описанный выше, только иллюстрирует изобретение, но не ограничивает объем изобретения. Настоящее изобретение также охватывает функционально эквивалентные способы и компоненты. В свете представленного описания так же как, и прилагаемых рисунков, специалисты в данной области могут легко выполнить различные изменения и модификации, которые также будут относиться к объему изобретения.
























Изобретение относится к области биотехнологии, конкретно к получению рецептора фактора некроза опухоли, и может быть использовано в медицине. Генно-инженерным путем получают мутант TNFRp75, связывающийся с фактором некроза опухоли и лимфотоксином, по существу состоящий из N-концевых 257 аминокислотных остатков TNFRp75, в котором N-концевой остаток Glu92 замещен Asn, His, Ser или Ala и в котором необязательно N-концевой остаток Тгр89 замещен Туг или Phe. На основе полученного мутанта конструируют слитый белок с дополнительным аминокислотным фрагментом, выбранным из константой области человеческого иммуноглобулина и одной из пяти функциональных областей альбумина, который находится на С-конце растворимого мутанта TNFRp75. Полученный мутант TNFRp75 и слитый белок используют в составе фармацевтической композиции для лечения заболеваний, ассоциированных со сверхэкспрессией TNFα, которые включают ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой. Изобретение позволяет получить растворимый мутант TNFRp75, способный с высокой степенью аффинности связываться с фактором некроза опухоли и лимфотоксином. 8 н. и 1 з.п. ф-лы, 12 ил., 10 пр.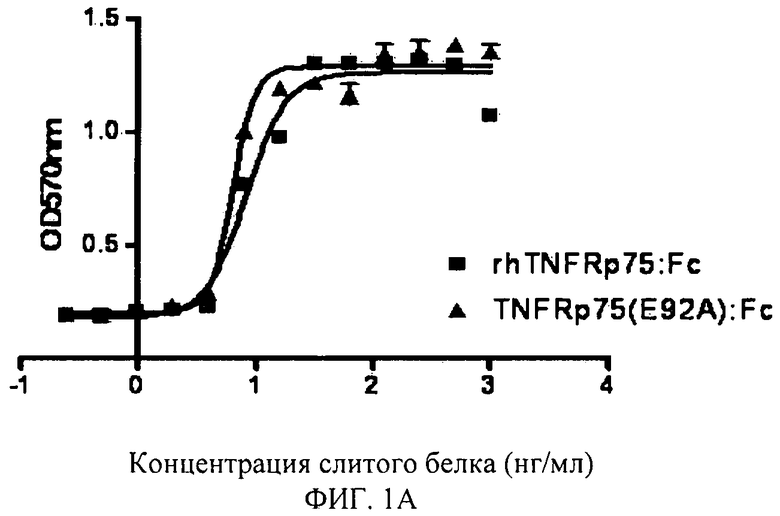
1. Растворимый мутант TNFRp75, связывающийся с фактором некроза опухоли и лимфотоксином, по существу, состоящий из N-концевых 257 аминокислотных остатков TNFRp75, представленных в SEQ ID NO.1, в котором N-концевой остаток Glu92 аминокислотной последовательности, представленной в SEQ ID NO.1, замещен Asn, His, Ser или Ala и в котором необязательно N-концевой остаток Тгр89 замещен Туг или Phe.
2. Слитый белок, связывающийся с фактором некроза опухоли и лимфотоксином, образованный растворимым мутантом TNFRp75 по п.1 и дополнительным аминокислотным фрагментом, который выбирается из группы, состоящей из константой области человеческого иммуноглобулина и одной из пяти функциональных областей альбумина, и находится на С-конце растворимого мутанта TNFRp75.
3. Слитый белок по п.2, в котором дополнительный аминокислотный фрагмент представляет собой 232 аминокислотных остатка константной области человеческого иммуноглобулина.
4. Выделенная молекула ДНК, кодирующая растворимый мутант TNFRp75 по п.1.
5. Выделенная молекула ДНК, кодирующая слитый белок по любому из пп.2 и 3.
6. Применение растворимого мутанта TNFRp75 по п.1 при изготовлении лекарственного средства для лечения заболеваний, ассоциированных со сверхэкспрессией TNFα, которые включают ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой.
7. Фармацевтическая композиция для лечения заболеваний, ассоциированных со сверхэкспрессией TNFα, включающая терапевтически эффективное количество растворимого мутанта TNFRp75 по п.1 и фармацевтически приемлемый носитель, где указанные заболевания, ассоциированные со сверхэкспрессией TNFα, включают ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой.
8. Применение слитого белка по любому из пп.2-3 при изготовлении лекарственного средства для лечения заболеваний, ассоциированных со сверхэкспрессией TNFα, которые включают ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой.
9. Фармацевтическая композиция для лечения заболеваний, ассоциированных со сверхэкспрессией TNFα, включающая терапевтически эффективное количество слитого белка по любому из пп.2 и 3 и фармацевтически приемлемый носитель, где указанные заболевания, ассоциированные со сверхэкспрессией TNFα, включают ревматоидный артрит, псориаз, склеродермию, синдром Шегрена, анкилозирующий спондилит, красную волчанку, дерматомиозит и синдром, сходный с системной красной волчанкой.
| CN 101085813 А, 12.12.2007 | |||
| Способ упрочнения инструмента | 1987 |
|
SU1502632A1 |
| CN 101003575 A, 25.07.2007 | |||
| US 2004170975 A1, 02.09.2004 | |||
| WO 1998049305 A1, 05.11.1998 | |||
| RU 2006101216 A, 20.07.2007. | |||
Авторы
Даты
2013-04-10—Публикация
2009-01-12—Подача