Изобретение относится к способам комплексной обработки воды с помощью аэрозольно-газовой смеси и может быть использовано для обеззараживания питьевой воды в автономных системах водоснабжения (корабельных системах, системах регенерации воды и системах жизнеобеспечения космических кораблей и подводных лодок).
Известен «Способ обработки и дезинфекции воды и/или отработанной воды», включающий подачу дезинфицирующего водного раствора, полученного в результате перемешивания органического кислотного соединения с хлоридом металла в камеру, содержащую воду и/или отработанную воду, причем дезинфицирующий водный раствор получают в результате перемешивания органической оксикислоты или карбоновой кислоты с хлоридом щелочного или щелочноземельного металла при рН, меньшей 7, и при температуре менее по меньшей мере 48,9°С, при этом содержимое камеры изолируют от атмосферы и выдерживают в камере не более 5 мин.
Патент РФ на изобретение №2098360, МПК: C02F 1/76, опубл. 1997.12.10.
Известен «Способ обеззараживания воды» введением в нее гипохлорита натрия, который получают путем растворения в воде поваренной соли и электролизом образовавшегося раствора, причем часть воды, которая идет на производство гипохлорита натрия и составляет 0,04-0,06% от общего объема обеззараживаемой воды, подвергают очистке от органических веществ.
Патент РФ на изобретение №2315004, МПК: C02F 1/76, опубл. 2008.01.20.
Известен «Способ обеззараживания воды», содержащей не менее 0,2% органических примесей, заключающийся в ее обработке реагентом из группы хлора, брома, бромхлорида, гипогалита щелочного или щелочно-земельного металла, галогенированного гидантоина или цианурата и ингибиторами-соединениями азота из группы п-толуолсульфамида, диметилгидантоина, метилэтилгидантоина, циануровой кислоты, карбамида и др., при соотношении хлорсодержащего реагента и соединения азота (0,1-10):1 для снижения содержания органических галогенсодержащих побочных продуктов.
Патент США №5565109, МПК: C02F 1/50, приоритет от 14.10.94 г., опубликован в ИСМ №9 - 1997 г.
Наиболее близким аналогом к способу в предложенном в качестве изобретения техническом решении является «Способ обеззараживания воды», содержащей органические загрязнения, включающий обработку воды гипохлоритом и ингибитором, причем в качестве ингибитора применяют сульфит или сульфид натрия при массовом соотношении последних к единице активного хлора 1,0-1,5 и 0,1-0,2 соответственно, процесс осуществляют в две стадии с обработкой воды ингибитором на первой стадии и гипохлоридом - на второй при поддержании рН, равным 6-9, отношение длительности контактирования обеззараживаемой воды с ингибитором на первой стадии к длительности контактирования воды с гипохлоритом - на второй стадии, равно 1:(15-30), при этом процесс ведут до содержания остаточного активного хлора не ниже 0,6 мг/л. Патент РФ на изобретение №2233801, МПК: C02F 1/50, опубл. 2004.08.10.
Техническим результатом способа является улучшение микробиологических показателей обеззараживаемой воды путем использования аэрозольно-газовой смеси, активными составляющими которой являются монохлорамин и аммиак.
Технический результат достигается тем, что «Способ обеззараживания воды в системах жизнеобеспечения» включает обработку воды хлорсодержащим реагентом при комнатной температуре воздуха и рН водного раствора, равной 8. На первом этапе осуществляют взаимодействие карбамида (NH2)2CO с двутретьосновной солью гипохлорита кальция 3Са(ClO)2 2Са(ОН)2 2H2O в соотношении, равном 1:5. На втором этапе обеззараживают воду полученной на первом этапе аэрозольно-газовой смесью, содержащей аммиак и монохлорамин в соотношении, равном 1:3,5. При этом процесс обеззараживания осуществляют в течение 1,5-2 часов и температуре воды 10-40°С.
Примеры конкретного выполнения способа
Способ обеззараживания воды включает ее обработку аэрозольно-газовой смесью, полученной путем смешения карбамида (NH2)2CO (мочевины) с двутретьосновной солью гипохлорита кальция 3Са(ClO)2 2Са(ОН)2 2H2O в соотношении 1:5.
1. Условия получения аэрозольно-газовой смеси
Основными антимикробными составляющими аэрозольно-газовых смесей, полученных при взаимодействии амидов и гипохлоритов, являются монохлорамин и аммиак. Причем выход монохлорамина зависит от химического состава и весового соотношения компонентов.
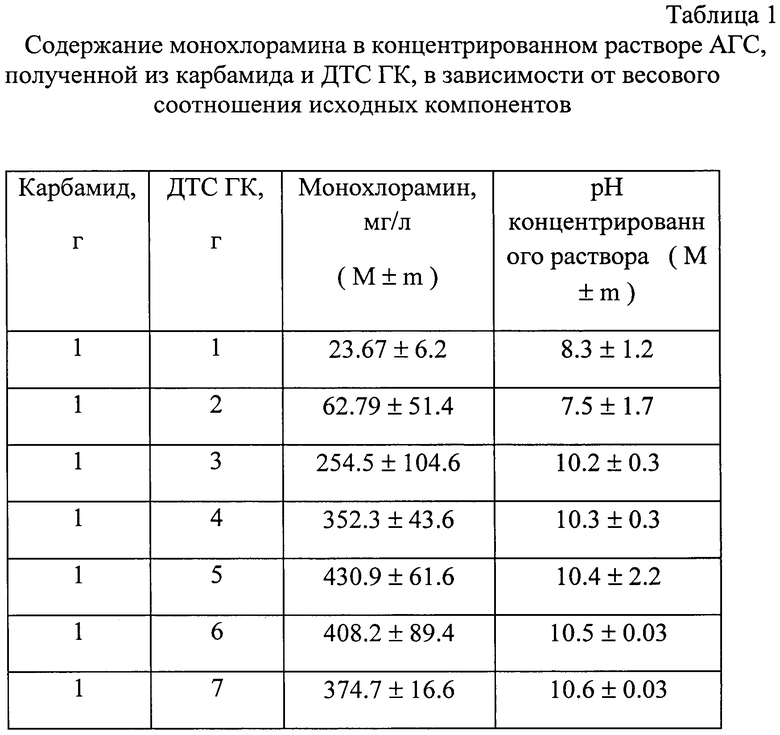
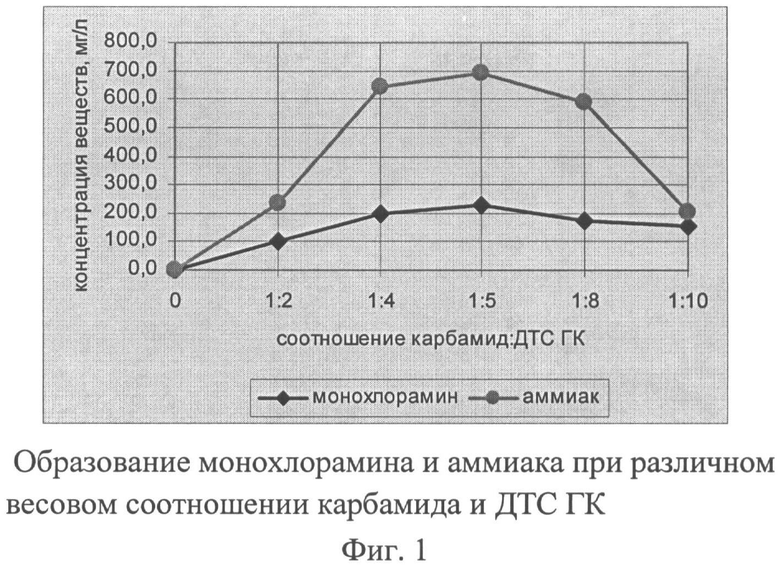
Условия получения аэрозольно-газовой смеси во многом определяют содержание в ней монохлорамина и аммиака, а следовательно ее дезинфицирующие и консервирующие свойства. Исследования показали, что максимальный выход монохлорамина и аммиака достигается при соотношении массы карбамида и ДТС ГК, равном 1:5. Вероятно, при этих условиях наблюдается более полное окисление карбамида. Уменьшение или увеличение соотношения реагентов приводило к уменьшению содержания монохлорамина и аммиака в аэрозольно-газовой смеси - АГС (фиг.1, табл.1). Поэтому соотношение реагентов 1:5 принято нами как основное.
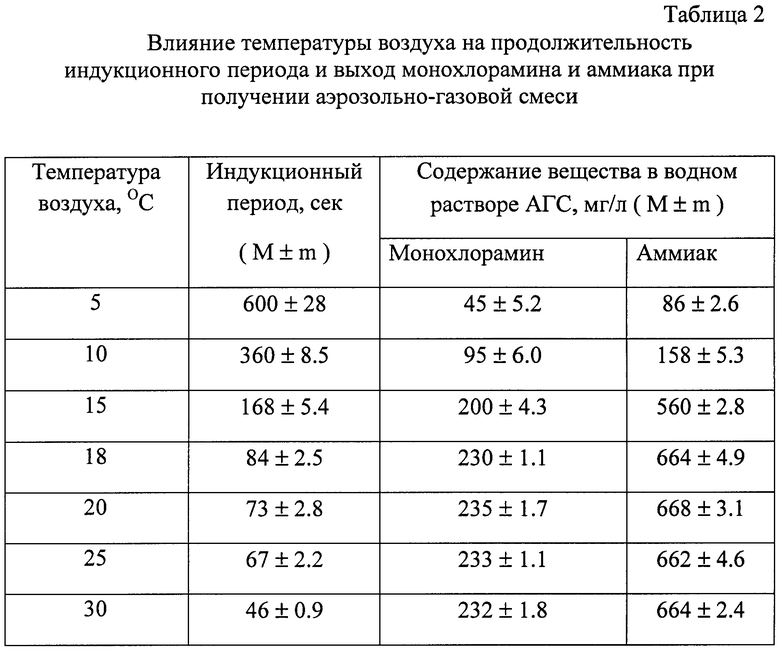
Установлено, что концентрация монохлорамина и аммиака в АГС меняется в зависимости от температуры окружающей среды, при которой происходит взаимодействие реагентов (табл.2).
Снижение температуры воздуха вело к уменьшению содержания монохлорамина и аммиака в АГС. Это, надо полагать, связано с увеличением длительности индукционного периода (периода с момента смешения реагентов до образования АГС), что в свою очередь свидетельствует о "вялом" течении реакции и не полном окислении карбамида.
Повышение температуры воздуха с 5°С до 18°С приводило к заметному увеличению концентрации монохлорамина и аммиака (Р>0.01) и уменьшению длительности индукционного периода. При температуре воздуха выше 18°С индукционный период становился короче, но содержание монохлорамина и аммиака в АГС практически не менялось.
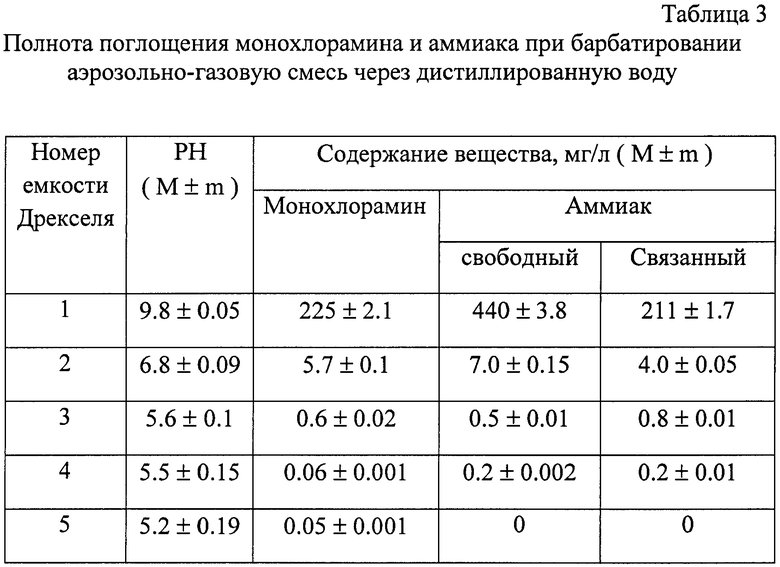
Аэрозольно-газовая смесь хорошо растворяется в воде, на чем основано получение ее водных растворов. Установлено, что при пропускании аэрозольно-газовой смеси через пять емкостей Дрекселя максимальное поглощение монохлорамина и аммиака происходило уже в первой емкости. В последующих емкостях монохлорамин и аммиак обнаруживались в виде следов (табл.3).
С уменьшением содержания монохлорамина и аммиака в каждой из последующих емкостей Дрекселя снижалось и значение рН, что объясняется наличием изоциановой кислоты, которая обнаруживалась при ИК-спектрофотометрии. В последней (пятой) емкости содержание монохлорамина составило всего 0.05 мг/л по сравнению с 225 мг/л в первой емкости.
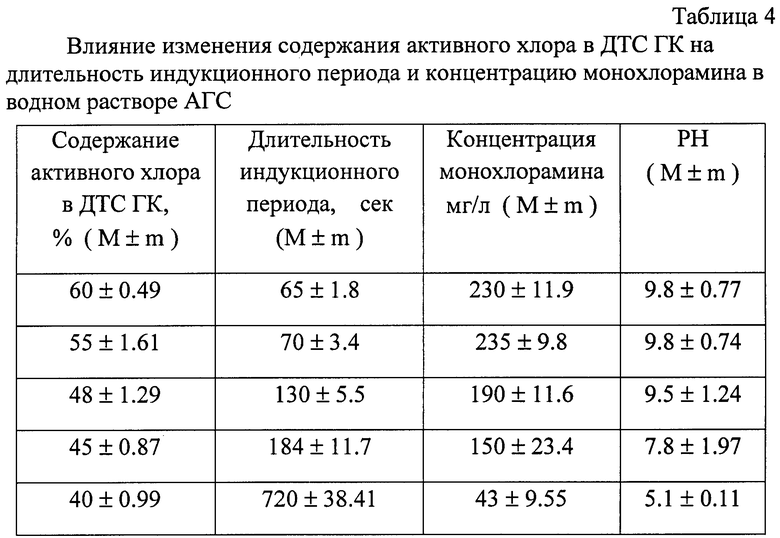
Содержание монохлорамина в АГС и ее концентрированных водных растворах существенно зависит от качества карбамида и двутретьосновной соли гипохлорита кальция 3Са(ClO)2 2Са(ОН)2 2H2O (ДТС ГК). Исследования показали, что снижение процентного содержания активного хлора в ДТС ГК приводило к уменьшению концентрации монохлорамина в АГС. Одновременно отмечалось увеличение длительности индукционного периода (табл.4).
При уменьшении содержания активного хлора в ДТС ГК до 40% растворы АГС приобретали кислый характер (рН 5.1), что объясняется, по-видимому, снижением концентрации аммиака и его соединений в аэрозольно-газовой смеси за счет неполного окисления карбамида.
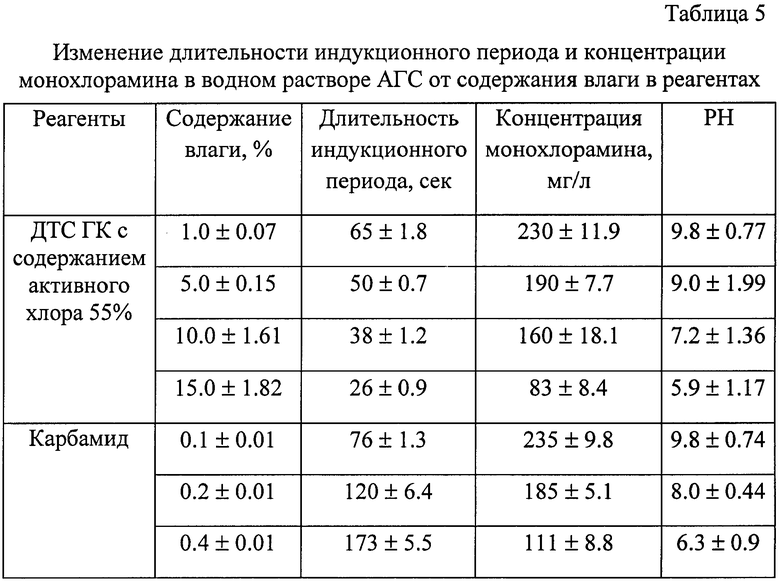
Установлено, что использование для получения АГС влажного карбамида или ДТС ГК изменяло течение реакции и приводило к уменьшению образования монохлорамина. Особенно выражено влияние на этот процесс изменение влажности карбамида (табл.5).
Таким образом, для получения аэрозольно-газовой смеси с максимальным содержанием монохлорамина и аммиака необходимо проведение реакции между карбамидом и ДТС ГК при температуре не ниже 15°С, причем активного хлора в ДТС ГК должно быть не менее 48%, а влажность карбамида - не более 0,1%.
2. Влияние факторов внешней среды на эффективность дезинфекции воды аэрозольно-газовой смесью
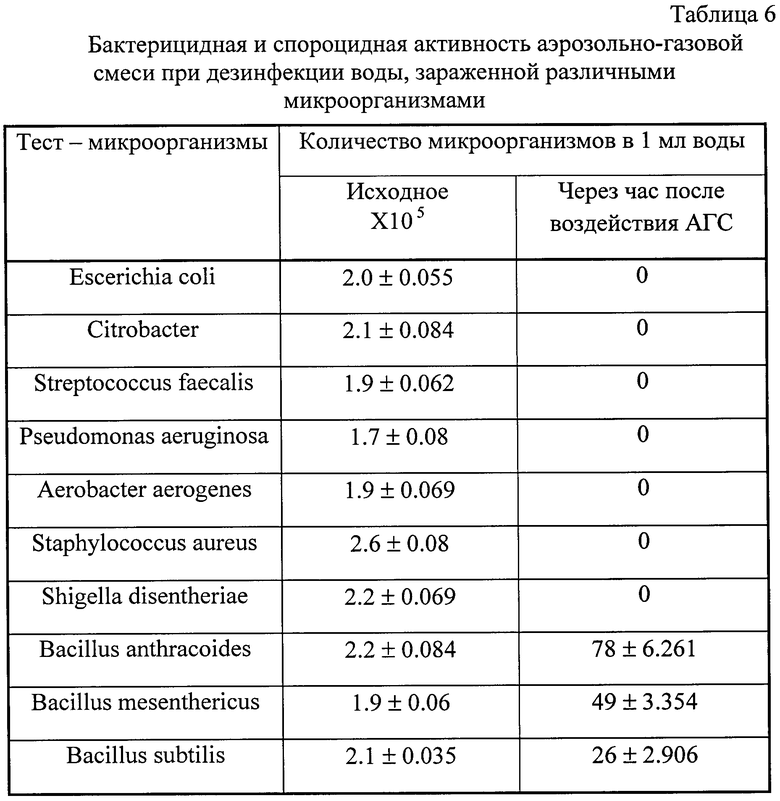
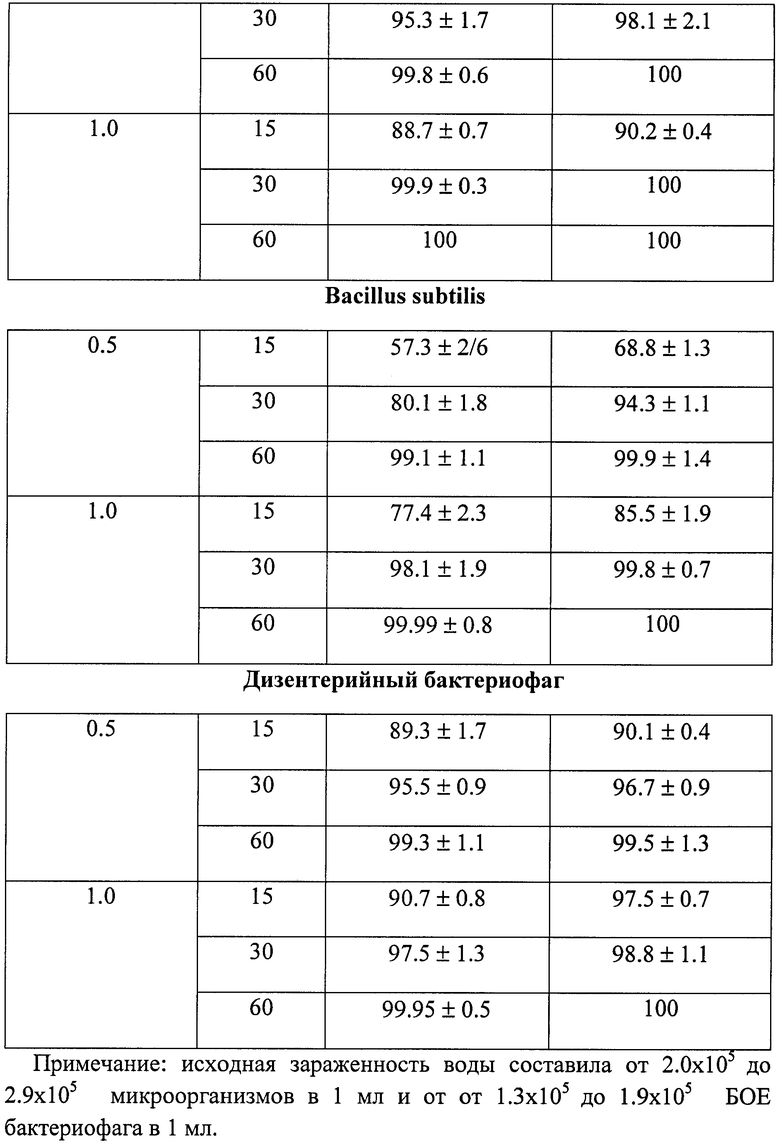
Установлено, что аэрозольно-газовая смесь оказывает эффективное обеззараживающее действие в отношении вегетативных и споровых микроорганизмов. После обеззараживания воды аэрозольно-газовой смесью (концентрация монохлорамина 2.0 мг/л, экспозиция - 1 час) наблюдалась 100% гибель вегетативных микроорганизмов. Количество выживших споровых микроорганизмов при этих же условиях составило 0.01-0.04% (табл.6). Следует отметить, что исходное количество микроорганизмов в сотни раз превышало реальный уровень зараженности воды в системах водообеспечения.
Наибольшей устойчивостью к воздействию аэрозольно-газовой смеси обладают споровые микроорганизмы и особенно антракоидная палочка, которая использована в дальнейшем для исследования эффективности обеззараживания.
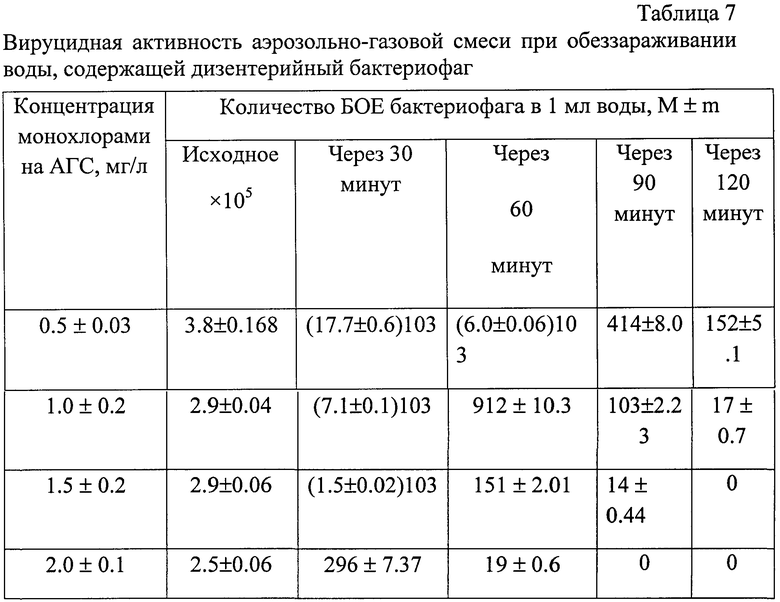
Отмечено значительное снижение количества бляшкообразующих единиц дизентерийного бактериофага после воздействия аэрозольно-газовой смеси. При концентрации монохлорамина в воде 1 мг/л через два часа количество БОЕ дизентерийного бактериофага снизилось на 99.995%. Увеличение концентрации монохлорамина до 1.5-2.0 мг/л приводило к 100% гибели дизентерийного бактериофага (табл.7).
Антимикробная активность аэрозольно-газовой смеси зависит от концентрации ее в воде. Было установлено, что увеличение концентрации АГС в воде, а следовательно монохлорамина и аммиака, приводит к снижению числа выживших микроорганизмов.
Корреляционный анализ зависимости между концентрацией монохлорамина и количеством выживших микроорганизмов показал, что при данном числе степеней свободы с вероятностью (Р<0.001) большей, чем 99,99%, можно утверждать о значительном влиянии концентрации монохлорамина АГС на эффективность обеззараживания (r=0.94±0.05).
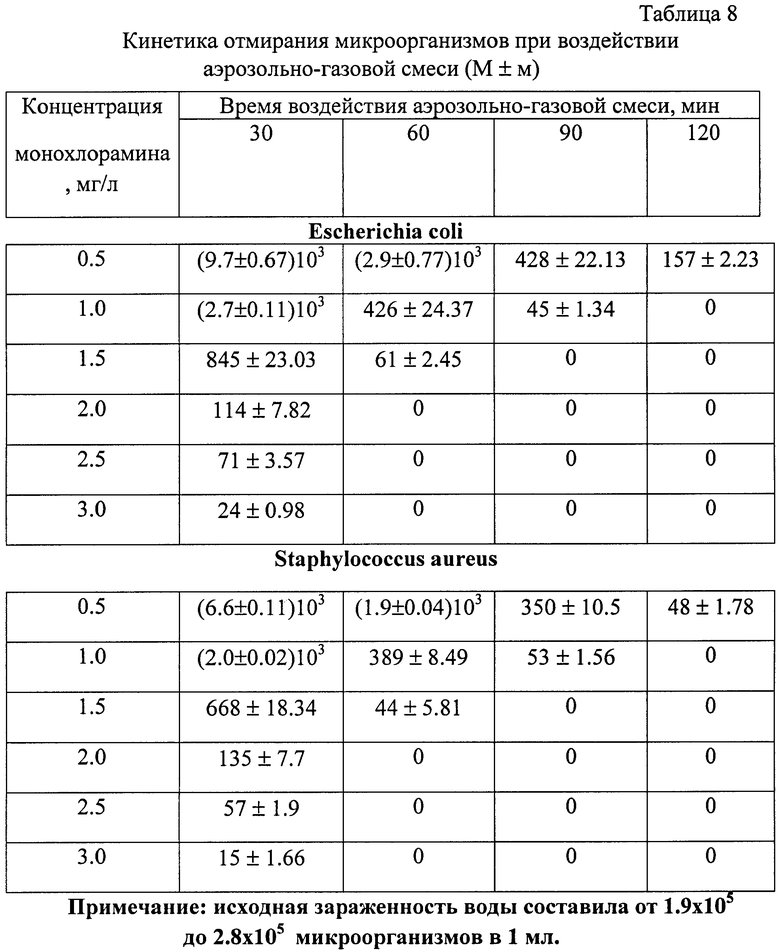
На выживаемость микроорганизмов в воде помимо концентрации АГС существенное влияние оказывает фактор времени. Результаты исследований (табл.7 и 8) свидетельствуют об увеличении эффективности обеззараживания воды при увеличении времени воздействия АГС.
Сочетание факторов времени и концентрации определяет кривые выживаемости микроорганизмов. Причем корреляционная связь между этими факторами и выживаемостью микроорганизмов при обеззараживании воды АГС очень тесная (r=0.95±0.03).
Установлено, что кривые выживаемости микроорганизмов при обеззараживании АГС подчиняются общей закономерности, которую с большой достоверностью (Р<0.001) можно представить в виде уравнения:
Pot=Ph×e-bt,
где Pot - число колинии образующих единиц микроорганизмов, оставшихся в живых после обеззараживания через время t;
Ph - исходное количество микроорганизмов;
е - основание натуральных логарифмов;
t - время воздействия АГС;
b - константа отмирания микроорганизмов.
Зависимость концентрации монохлорамина АГС от времени, необходимого для снижения количества бактерий до заданной величины, выражается уравнением:
Cnt=K,
где С - концентрация монохлорамина АГС;
t - время воздействия АГС;
n - коэффициент поглощения;
K - константа резистентности микроорганизмов к АГС.
Константа резистентности микроорганизмов к АГС рассчитывается по формуле:
lgK=n*lgC+lgt
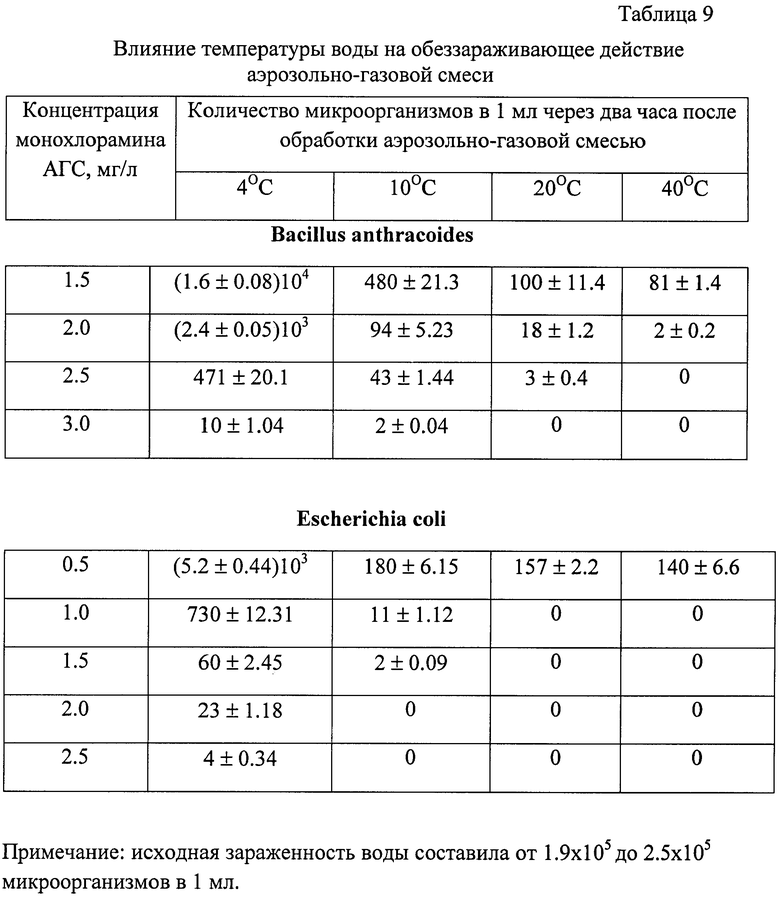
Ослабление бактерицидного действия аэрозольно-газовой смеси наблюдалось при понижении температуры воды (табл.9).
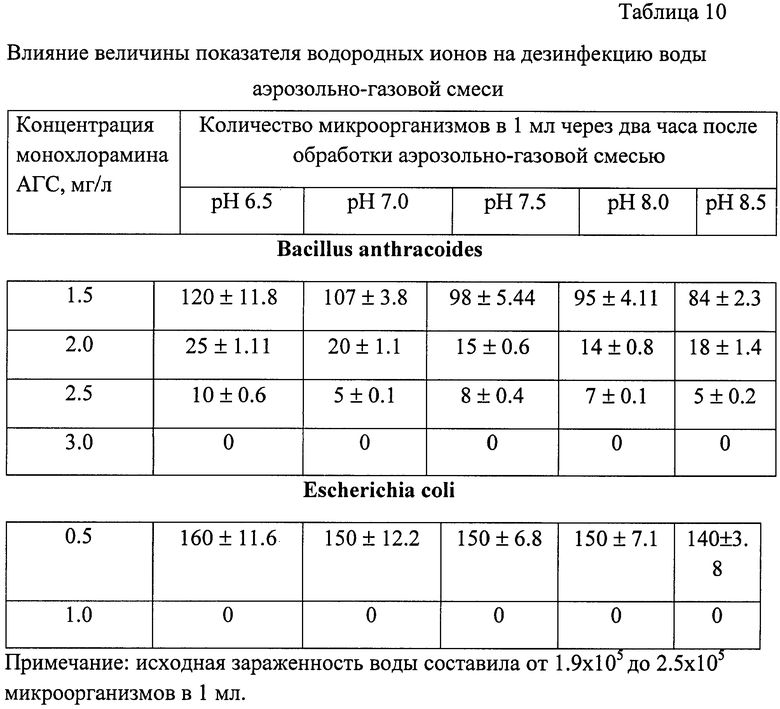
Изменение величины показателя водородных ионов (рН) в пределах, допустимых ГОСТ 2874-82 "Вода питьевая", оказывало незначительное влияние на эффективность обеззараживания воды аэрозольно-газовой смесью. Причем это влияние уменьшалось с увеличением концентрации АГС в воде (табл.10).
Экспериментальные данные, полученные при обеззараживании воды аэрозольно-газовой смесью в лабораторных условиях, были подтверждены результатами дезинфекции воды в полевых условиях.
Установлено, что гигиеническая эффективность обеззараживания воды АГС в резервуарах достигается через час при концентрации монохлорамина 1.5 мг/л.
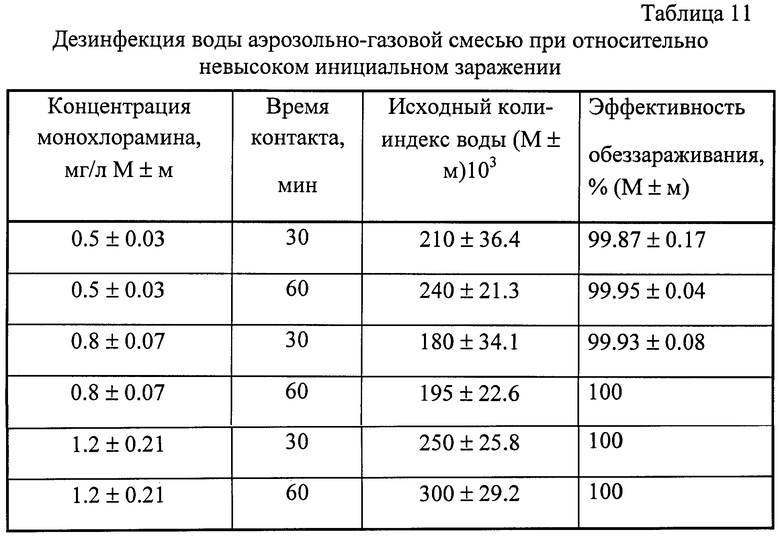
В практических условиях зараженность воды значительно ниже, поэтому для достижения гигиенической эффективности деконтаминации при относительно невысоком инициальном заражении воды кишечной палочкой использовались и меньшие концентрации монохлорамина. Результаты, приведенные в таблице 11, с достаточно высокой степенью надежности свидетельствуют о том, что концентрация монохлорамина 0.8 мг/л при времени контакта 60 минут (или 1.2 мг/л при времени контакта 30 минут) достаточна для освобождения воды от патогенных микроорганизмов кишечной группы.
Результаты проведенных исследований показывают, что аэрозольно-газовая смесь обладает бактерицидными, спороцидными и вирулицидными свойствами. Гигиеническая эффективность обеззараживания воды, зараженной вегетативными микроорганизмами в дозе 2×105 КОЕ/мл, достигается при концентрации монохлорамина 1.5 мг/л, времени контакта 90 минут и температуре не ниже 15°С. В условиях относительно невысокого инициального заражения воды вегетативными микроорганизмами 100% эффективность обеззараживания наблюдается при концентрации монохлорамина 0.8-1.2 мг/л и времени контакта соответственно 30 и 60 минут. Для гигиенической эффективности обеззараживания воды при наличии споровых микроорганизмов необходима концентрация монохлорамина 3.0 мг/л и время контакта 2 часа (таблицы 6, 7, 8, 9, 10 и 11).
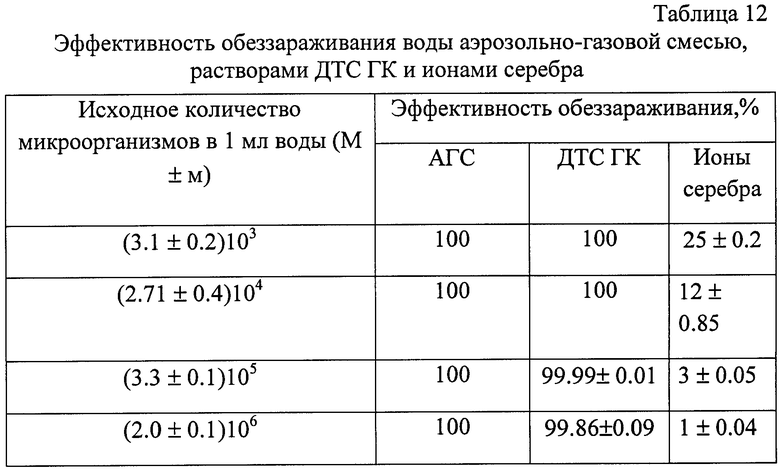
3. Сравнительная устойчивость микроорганизмов при воздействии других дезинфектантов отражена в табл.12.
Результаты сравнительного исследования эффективности деконтаминации воды показали, что аэрозольно-газовая смесь оказывает более выраженное бактерицидное и спороцидное действие по сравнению с ДТС ГК и ионами серебра. При концентрации монохлорамина и ионного серебра в воде 2.0 мг/л эффективность обеззараживания соответственно составляет 100% и 1-25%. Показано, что деконтаминация воды ионами серебра, при высоких уровнях ее заражения, не приводит к снижению числа микроорганизмов до допустимого значения. Для процесса деконтаминации воды ионами серебра характерна выраженная зависимость от величины инициального заражения. В исследуемых концентрациях оптимальное бактерицидное действие ионов серебра наблюдалось при наличии в воде микроорганизмов в количестве 2000±500 м.т./мл.
Установлено также, что спороцидного действия ионы серебра практически не оказывают даже при единичном содержании спор Bac.Anthracoides в воде (табл.13).
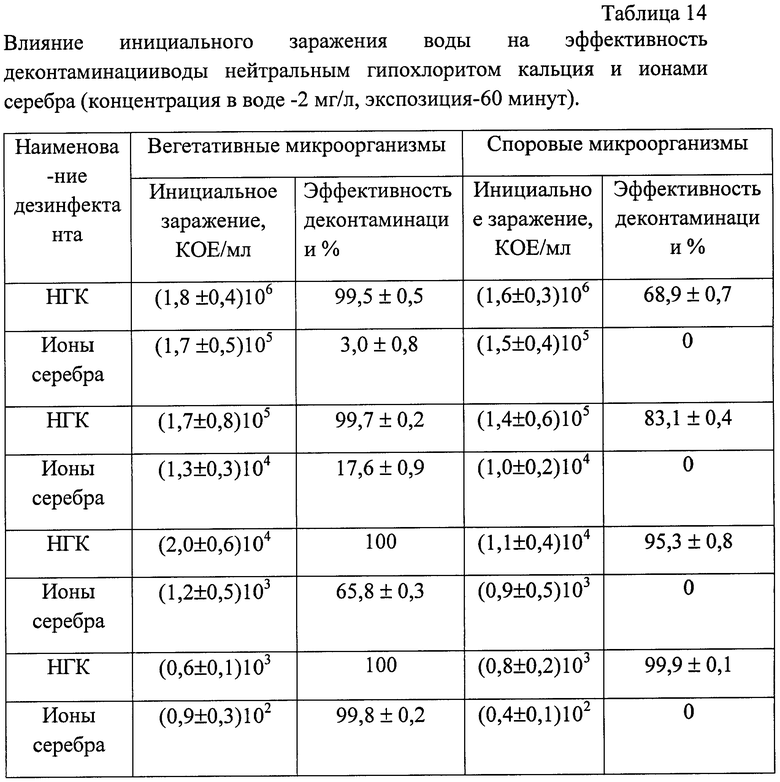
По эффективности обеззараживающего действия ДТС ГК значительно превосходит ионное серебро. При исходной бактериальной нагрузке 1,6-1,8 млн м.т./мл после часовой экспозиции количество микроорганизмов снижается до нескольких десятков и сотен в 1 мл воды, содержащей 2 мг/л остаточного активного хлора. В отличие от ионного серебра нейтральный гипохлорит кальция (НГК) оказывает как бактерицидное, так и спороцидное действие. Причем инициальная бактериальная нагрузка в значительно меньшей степени оказывает влияние на эффективность деконтаминации воды нейтральным гипохлоритом кальция (НГК), чем в случае использования растворов ионного серебра (табл.14).
Деконтаминация воды озонированием показала, что при высоких уровнях инициального заражения озон незначительно превосходит по эффективности аэрозольно-газовую смесь (табл.15). По мере снижения инициальной зараженности воды эффективность озона резко возрастает.
Применение данного изобретения позволит улучшить микробиологические показатели обеззараживаемой воды в системах жизнеобеспечения путем использования аэрозольно-газовой смеси, основными активными составляющими которой являются монохлорамин и аммиак, что позволяет использовать полученную воду в течение длительного срока, а именно более года.

| название | год | авторы | номер документа |
|---|---|---|---|
| ДЕЗИНФИЦИРУЮЩИЙ РАСТВОР | 1994 |
|
RU2077504C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТЬЕВОЙ ВОДЫ | 2001 |
|
RU2182128C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ОЧИСТКИ ПРИРОДНОЙ ВОДЫ | 2016 |
|
RU2617104C1 |
| ВОДНЫЙ РАСТВОР ГИПОХЛОРИТА НАТРИЯ, ОБЛАДАЮЩИЙ ДЕЗИНФИЦИРУЮЩИМ И ОБЕЗЗАРАЖИВАЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2145237C1 |
| СПОСОБ ДЕЗИНФЕКЦИИ ЗАРАЖЕННЫХ ПОВЕРХНОСТЕЙ АВИАЦИОННОЙ ТЕХНИКИ В ВОЗДУХЕ | 2022 |
|
RU2790342C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТЬЕВОЙ ВОДЫ | 2001 |
|
RU2188169C1 |
| СПОСОБ И СОСТАВ ИНДИКАТОРНОЙ РЕЦЕПТУРЫ ДЛЯ ЭКСПРЕСС-ОБНАРУЖЕНИЯ ДЕЗИНФЕКТАНТОВ С ДЕЙСТВУЮЩИМ ВЕЩЕСТВОМ ОКИСЛИТЕЛЬНОГО ХАРАКТЕРА НА ПОВЕРХНОСТЯХ ОБЪЕКТОВ И ВЫЯВЛЕНИЯ ПОЛНОТЫ ДЕЗИНФЕКЦИИ | 2009 |
|
RU2436082C2 |
| БИФУНКЦИОНАЛЬНАЯ РЕЦЕПТУРА ОКИСЛИТЕЛЬНО-НУКЛЕОФИЛЬНОГО ДЕЙСТВИЯ | 2003 |
|
RU2248234C2 |
| СПОСОБ ДЕЗИНФЕКЦИИ ПОМЕЩЕНИЙ | 1999 |
|
RU2171118C2 |
| ТВЕРДАЯ ДОЗИРОВАННАЯ ФОРМА ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА, УПАКОВКА С НЕЙ, СПОСОБ ДЕЗИНФЕКЦИИ | 2004 |
|
RU2277425C2 |
Изобретение относится к способам комплексной обработки воды с помощью аэрозольно-газовой смеси и может быть использовано для обеззараживания питьевой воды в автономных системах водоснабжения (корабельных системах, системах регенерации воды и системах жизнеобеспечения космических кораблей и подводных лодок). Способ включает обработку воды хлорсодержащим реагентом при комнатной температуре воздуха и рН водного раствора, равной 8. На первом этапе осуществляют взаимодействие карбамида (NH2)2CO с двутретьосновной солью гипохлорита кальция 3Са(ClO)2 2Са(ОН)2 2H2O в соотношении, равном 1:5. На втором этапе обеззараживают воду полученной на первом этапе аэрозольно-газовой смесью, содержащей аммиак и монохлорамин в соотношении, равном 1:3,5. При этом процесс обеззараживания осуществляют в течение 1,5-2 часов и температуре воды 10-40°С. Техническим результатом изобретения является улучшение микробиологических показателей обеззараживаемой воды путем использования аэрозольно-газовой смеси, активными составляющими которой являются монохлорамин и аммиак. 15 табл., 1 ил.
Способ обеззараживания воды в системах жизнеобеспечения, включающий обработку воды хлорсодержащим реагентом при комнатной температуре воздуха и рН водного раствора, равной 8, отличающийся тем, что на первом этапе осуществляют взаимодействие карбамида (NH2)2CO с двутретьосновной солью гипохлорита кальция 3Са(ClO)2 2Са(ОН)2 2H2O в соотношении, равном 1:5, а на втором этапе обеззараживают воду полученной на первом этапе аэрозольно-газовой смесью, содержащей аммиак и монохлорамин в соотношении, равном 1:3,5, при этом процесс обеззараживания осуществляют в течение 1,5-2 ч и температуре воды 10-40°С.
| СПОСОБ ОБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2003 |
|
RU2233801C1 |
| СПОСОБ ОБРАБОТКИ И ДЕЗИНФЕКЦИИ ВОДЫ И/ИЛИ ОТРАБОТАННОЙ ВОДЫ (ВАРИАНТЫ) И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1994 |
|
RU2098360C1 |
| СПОСОБ ОБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2006 |
|
RU2315004C1 |
| СПОСОБ ДЕЗИНФЕКЦИИ ХРАНИЛИЩ ДЛЯ ПРОДУКТОВ СЕЛЬСКОГО ХОЗЯЙСТВА | 1993 |
|
RU2074008C1 |
| СРЕДСТВО ДЛЯ ДЕЗИНФЕКЦИИ | 1996 |
|
RU2117491C1 |
| Волновая реечная передача с промежуточными звеньями в виде клиньев | 1980 |
|
SU1043392A1 |
| JP 10043771 А, 17.02.1998. | |||
Авторы
Даты
2013-04-27—Публикация
2011-08-24—Подача