Изобретение относится к области органического синтеза, конкретно к синтезу (E)-4-фенил-3-бутен-2-она (бензальацетона) (I).
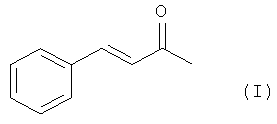
Бензальацетон (I) имеет широкий спектр промышленного применения и используется в качестве вкусовых и ароматических добавок в пищевой промышленности и в парфюмерии [J-М Sauer et al. Drug Metabolism and disposition, vol.25, №.10, p.1184-1190, 1997]; применяется в качестве промежуточного продукта для получения коричной кислоты и бензилацетона (ценный парфюмерный продукт с запахом земляники и жасмина) [Заявка US 2002/0055656 A1, 2002]. Замещенные (E)-4-фенил-3-бутен-2-оны проявляют противовоспалительную, противовирусную и антиоксидантную активность и применяются в фармацевтической промышленности [G.Elias and M.N.A.Rao. European Journal of Medicinal Chemistry, vol.23 (4), p.379-380, 1988; P.C.Kuo et al. Arch. Pharm. Res, vol.28, №5, p.518-528, 2005; M.L.Edwards et al. J. Med. Chem., vol.26, №3, 1983].
Известен способ получения бензальацетона, ферментативным восстановлением 4-фенил-3-бутин-2-она, при помощи редуктазы OYE; в присутствии никотинамидадениндинуклеотидфосфата (NADPH), этилендиаминтетрауксусной кислоты (ЭДТА) в изопропаноле при pH 6,8, 30°C в течение 1 ч при перемешивании. Реакционную смесь экстрагировали хлороформом. Выход продукта не указан [Заявка US 2010/0009421 A1, 2010].
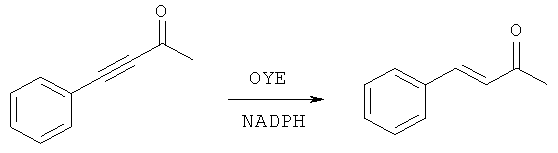
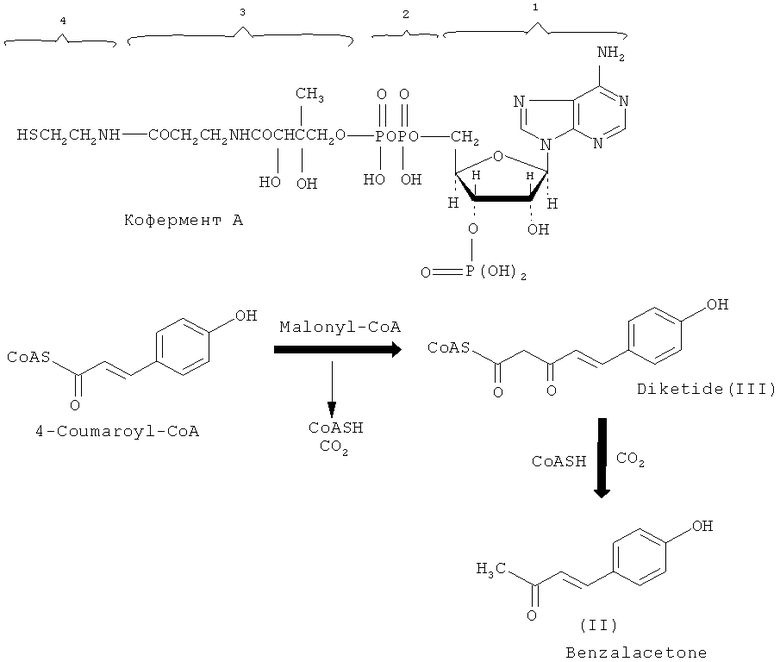
Известен ряд работ, относящихся к способу получения производного бензальацетона 4-(4-гидроксифенил)-бутен-2-она (II), в литературе называемого также «бензальацетон» (Н.Morita et al. PNAS, vol.107, №2, p.669-673, 2010; Y. Shimokawa et al., Bioorganic & Medicinal Chemistry Letters, Vol 20, (17), p.5099-5103, 2010; Патент GB 2416770, 2006; D.Zheng, G.Hrazdina. Archives of Biochemistry and Biophysics, 470, p.139-145, 2008]. Синтез 4-(4-гидроксифенил)-бутен-2-она (II) осуществляют ферментативными методами, а именно конденсацией ферментов 4-кумарил-КоА и молонил-КоА, где 4-кумарил-КоА - остаток кумаровой кислоты + кофермент A, состоящей из остатка адениловой кислоты (1), которая связана пирофосфатной группой (2) с остатком пантотеновой кислоты с молонил-KoA(malonyl-CoA); молонил-КоА - остаток малоновой кислоты+Кофермент A. Образовавшийся в ходе конденсации дикетид (III) далее декарбоксилируют и получают 4-(4-гидроксифенил)-бутен-2-он (II).
Ферментативные методы синтеза могут быть альтернативой химическим методам, но в настоящее время эти методы недостаточно разработаны.
Известен способ получения бензальацетона по реакции Кляйзена-Шмидта - конденсацией бензальдегида с ацетоном в присутствии сильных оснований.
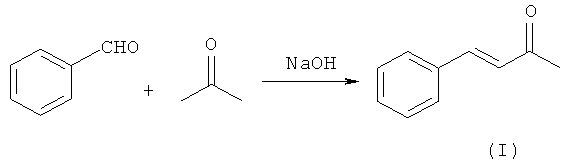
Согласно методике, приведенной в [A.Sethi. Systematic Lab Experiments in organic Chemistry, p.699, 2003; S.Gokksu et al. Turk J. Chem., vol.27, pp.31-34, 2003; M.L.Edwards et al. J. Med. Chem., vol.26, №3, 1983] синтез бензальацетона (I) осуществляют следующим образом: в колбу емкостью 100 мл, снабженную мешалкой и термометром, приливают 10 мл свежеперегнанного бензальдегида и 20 мл ацетона (значительный избыток ацетона приливают для уменьшения образования дибензальацетона). Колбу с реакционной массой держат в холодной водяной бане, затем по каплям при перемешивании добавляют 2,5 мл 10%-ного раствора гидроксида натрия, так, чтобы температура реакционной смеси не поднималась выше 30°C. Потом смесь перемешивают в течение 2 ч при комнатной температуре. После окончания реакции реакционную массу нейтрализуют и разделяют перегонкой в вакууме. Выход целевого продукта составляет 10 г (68,4%).
К недостаткам данного способа можно отнести использование растворов едкого натра и соляной кислоты, необходимость стадии нейтрализации, отмывки реакционной смеси, утилизация больших объемов сточных вод, коррозию оборудования и т.д.
В работе [S.Handayani, I.S.Arty. Journal of Physical Science, vol.19, p.61-68, 2008] бензальацетон (I) получают также конденсацией Кляйзена-Шмидта, но по другой методике, которая заключается в том, что в предварительно подготовленный спиртовой раствор (этанол:вода=1:1) гидроксида натрия, содержащего 0,05 моль NaOH, добавляют бензальдегид (0,02 моль), и перемешивают 10 мин, после этого в смесь приливают по каплям ацетон (0,02 моль) и перемешивают в течение 30 мин. Затем к реакционной массе приливают воду и фильтруют. Дальше продукт очищают перекристаллизацией в этаноле и высушивают. Выход продукта (I) составляет 82%.
Недостатки этого метода: использование большого количества щелочи, что приводит к появлению стадии нейтрализации и отмывки продукта реакции, а также применение большого количества растворителя (этанола) и необходимость его регенерации.
Задачей настоящего изобретения является упрощение способа получения бензальацетона (I).
Решение этой задачи достигается тем, что способ получения бензальацетона (I) осуществляют взаимодействием стирола и уксусного ангидрида в присутствии оксидного алюмо-кремний-циркониевого катализатора. Реакцию проводят при 80-130°C, количестве катализатора 10-50% мас. (в расчете на смесь стирола с уксусным ангидридом, взятых в мольном отношение 1:1) и мольном соотношении стирол:уксусный ангидрид, равном 1:2÷8. Конверсия стирола составляет 53,8-99%. Селективность образования целевого продукта 65-89%. Реакция проходит по схеме:
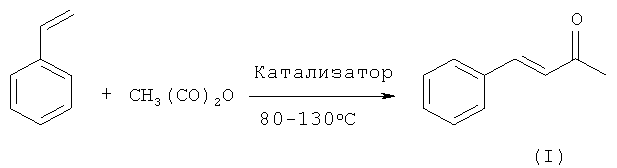
Катализатор представляет собой мезопористый аморфный смешанный элементосиликат, в составе которого содержится алюминий и цирконий, равномерно распределенные в силикатной матрице.
Элементосиликаты известны как активные катализаторы разнообразных реакций: изомеризации парафинов и нафтенов, алкилирования ароматических соединений, гидрокрекинга и др.
Титаносиликатный катализатор, известный как TS-1, используется в промышленном процессе окисления фенола пероксидом водорода.
Использование элементосиликатов для получения бензальацетона не известно.
Преимущества предлагаемого способа
1. Малостадийность.
2. Отсутствие гидроксида натрия.
3. Отсутствие кислых и щелочных стоков.
4. Отсутствие растворителей.
5. Оксидный алюмо-кремний-циркониевый катализатор легко отделяется от реакционной массы и регенерируется, может использоваться многократно.
6. Снижение себестоимости и упрощение технологии за счет уменьшения энерго- и трудозатрат.
Предлагаемый способ получения бензальацетона (I) осуществляют следующим образом.
Используют мезопористый аморфный оксидный алюмо-кремний-циркониевый катализатор, синтезированный по методике, описанной в патенте [пат. РФ 2420455, 2011].
Для получения катализатора смешивают растворы солей алюминия и циркония в этаноле, со спиртовым раствором этилсиликата-40: обрабатывают полученную смесь аммиачной водой; образовавшуюся массу сушат вначале на воздухе при 100-150°C, а затем при 500-650°C. Получают мезопористый алюмоциркониевый катализатор, характеристики которого приведены в таблице.
Синтез бензальацетона проводят в периодическом термостатированном реакторе. В реактор помещают стирол, уксусный ангидрид и катализатор, после чего нагревают до заданной температуры при непрерывном перемешивании реакционной массы. После окончания реакции реакционную массу отделяют от катализатора фильтрованием и перегоняют под вакуумом.
Изобретение иллюстрируется следующими примерами.
Пример 1. Синтез проводят в трехгорлой колбе, снабженной термометром, мешалкой, холодильником. В колбу помещают 1,2 мл (0,01 моль) стирола, 3,8 мл (0,04 моль) уксусного ангидрида, 0,21 г катализатора и нагревают до 80°C. Реакционную массу непрерывно перемешивают в течение 10 ч. После окончания реакции реакционную массу отделяют от катализатора фильтрованием и перегоняют под вакуумом. Целевой продукт - бензальацетон выделяют при 90°C/5 мм рт.ст. Конверсия стирола составляет 53,8%, селективность образования бензальацетона 86,2%.
Примеры 2-8 аналогично примеру 1. Условия и результаты примеров представлены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ (Е)-4-ФЕНИЛ-3-БУТЕН-2-ОНА | 2011 |
|
RU2482105C1 |
| СПОСОБ ПОЛУЧЕНИЯ (Е)-4-ФЕНИЛ-3-БУТЕН-2-ОНА | 2011 |
|
RU2482106C1 |
| Способ приготовления катализатора для селективного гидрирования арабинозы в арабинитол, катализатор, приготовленный по этому способу, и способ селективного гидрирования арабинозы в арабинитол с использованием полученного катализатора | 2022 |
|
RU2784328C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ЭТИЛ-3,5-ДИМЕТИЛПИРИДИНА | 2016 |
|
RU2644166C2 |
| Способ получения 2-метил-3-пропилиндола | 2024 |
|
RU2831365C1 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697875C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИ-ТРЕТ-БУТИЛ-П-БЕНЗОХИНОНА | 2016 |
|
RU2654477C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЗОПОРИСТЫХ АМОРФНЫХ СМЕШАННЫХ ЭЛЕМЕНТОСИЛИКАТОВ | 2009 |
|
RU2420455C1 |
| Способ получения гомо- и соолигомеров α-метилстирола и изопентенов в присутствии мезопористого алюмосиликатного катализатора ASM | 2020 |
|
RU2759627C2 |
| Способ получения 2,2,4-триалкил-2,3-дигидро-1Н-1,5-бензодиазепинов | 2019 |
|
RU2702359C1 |
Изобретение относится к способу получения (Е)-4-фенил-3-бутен-2-она (бензальацетона) (I), который может быть использован в качестве вкусовой и ароматической добавки в пищевой промышленности и в парфюмерии. Способ заключатся во взаимодействии стирола и уксусного ангидрида в присутствии мезопористого аморфного оксидного алюмо-кремний-циркониевого катализатора при мольном соотношении стирол:уксусный ангидрид=1:2÷8, температуре 80-130°С, массовом содержании катализатора 10-50% (в расчете на смесь стирола с уксусным ангидридом, взятых в мольном отношении 1:1). Предлагаемое изобретение позволяет простым и малозатратным способом получить целевой продукт. 1 табл., 8 пр.

Способ получения (Е)-4-фенил-3-бутен-2-она, характеризующийся тем, что взаимодействие стирола и уксусного ангидрида проводят в присутствии мезопористого аморфного оксидного алюмо-кремний-циркониевого катализатора при мольном соотношении стирол : уксусный ангидрид = 1:2-8, температуре 80-130°С, массовом содержании катализатора 10-50% (в расчете на смесь стирола с уксусным ангидридом, взятых в мольном отношении 1:1).
| JP 3261741 A, 21.11.1991 | |||
| DE 3821197 A, 28.12.1989 | |||
| Р.Pawluc et al, One-Pot Synthesis of (E)-Styryl Ketones from Styrenes | |||
| Journal of Organic Chemistry, 2011, 76(15), 6438-6441 | |||
| СПОСОБ ПОЛУЧЕНИЯ α,β -НЕНАСЫЩЕННЫХ КЕТОНОВ АРОМАТИЧЕСКОГО ИЛИ ГЕТЕРОАРОМАТИЧЕСКОГО РЯДА | 1994 |
|
RU2082710C1 |
Авторы
Даты
2013-05-10—Публикация
2011-11-24—Подача