Предлагаемое изобретение относится к области органической химии, в частности, к способу получения 2-метил-3-пропилиндола (1).
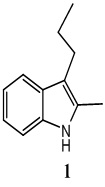
2-Метил-3-пропилиндол используется в виде репеллента в составе морского противообрастающего материала от живых организмов [Патенты JPH10259101A; JP4092621]; для синтеза производных индолов, обладающих антиартериосклеротическими и противовоспалительными действиями [Патент JP2006001926], фотохромных красителей [Патент DE19646820A1].
В литературе [E.B. Landstrom [et al.] // Organic Letters. – 2020. – Vol. 22. – № 16. – P. 6543-6546] описан способ получения 2-метил-3-пропилиндола (1) с помощью водного мицеллярного катализа:
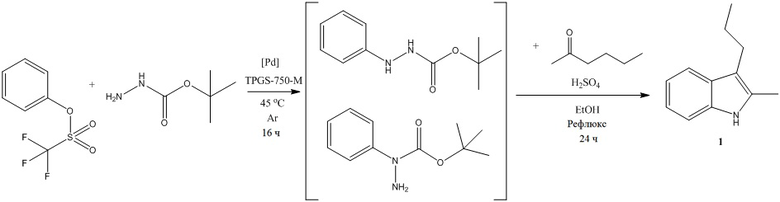
На первой стадии осуществляли взаимодействие фенилтрифторометансульфоната с производным гидразина в присутствии каталитической системы на основе комплекса палладия Pd (0,5 %мол.) с применением фосфина tBuBrettPhos (0,5 ммоль), трет-бутоксида натрия NaOt-Bu (2 ммоль) (45 °С, 16 ч, аргон). В качестве поверхностно-активного вещества использовали производное полиоксиэтанил-α-токоферилсукцината - TPGS-750-M (2 %мас. в H2O). На второй стадии добавляли этанол (0,2 М), серную кислоту и 2-гексанон (производное гидразина: 2-гексанон:H2SO4 = 1:2:3 моль/моль), реакцию проводили в течение 24 ч в условиях кипения. Недостатки вышеописанного способа – использование множества дорогостоящих компонентов, многостадийность и долгий синтез.
Авторы [H.-D. Xia [et al.] // Organic Letters. – 2018. – Vol. 20. – № 13. – P. 4052-4056] синтезировали 2-метил-3-пропилиндол 1 с выходом 80 % двухстадийным синтезом:
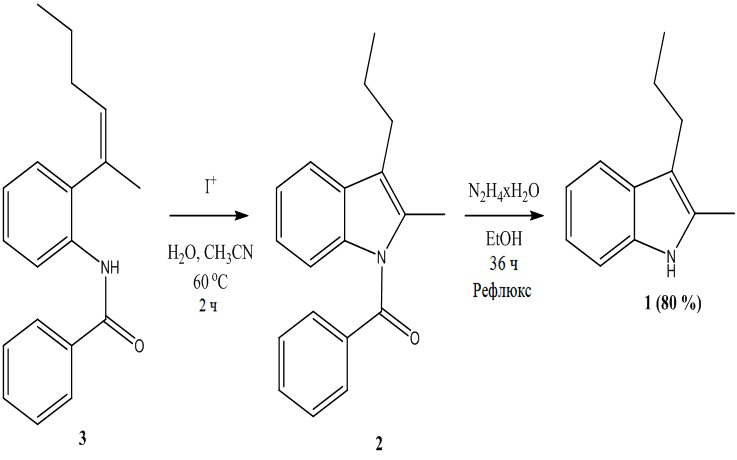
Сначала осуществляли внутримолекулярную конденсацию бензамида 3 с получением производного индола 2 (катализатор на основе гипервалентного йода (фенилйодонио)сульфамат, H2O, CH3CN, 60 °C, 2 ч), затем снимали защиту с азотной группы (катализатор – N2H4⋅H2O, EtOH, 36 ч в условиях кипения). Недостатки данного способа – многостадийный и долгий синтез, использование прекурсора, наркотических и психотропных веществ в качестве растворителя.
Авторы [S. Banerjee, E. Barnea, A.L. Odom // Organometallics. – 2008. – Vol. 27. – Titanium-Catalyzed Hydrohydrazination with Monosubstituted Hydrazines. – № 5. – P. 1005-1014] синтезировали индол 1, исходя из 1-гексина и фенилгидразина, с выходом 87 % с использованием двух катализаторов:
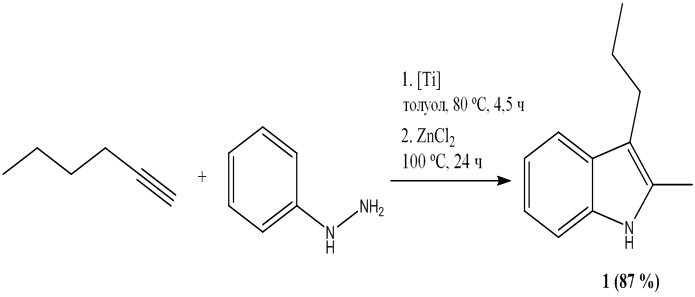
Сначала в качестве катализатора применяли Ti-содержащую каталитическую систему (толуол, 80 °С, 4,5 ч), затем добавляли хлорид цинка ZnCl2 (100 °С, 24 ч). Недостатками данного способа являются: использование сложного комплекса титана в качестве катализатора, сравнительно дорогостоящего и взрывоопасного реагента (1-гексина), ядовитого фенилгидразина, многостадийность, долгий синтез.
Аналогичной реакцией соединение 1 синтезировано с выходом 82 % [N.T. Patil, A. Konala // European Journal of Organic Chemistry. – 2010. – Vol. 2010. – № 35. – P. 6831-6839] в присутствии бинарной каталитической системы, состоящей из металлорганического комплекса золота и п-толуолсульфокислоты Ph3PAuNTf2/pTSA·H2O (толуол, 100 °С). Недостатки данного способа – использование сложного и дорогостоящего комплекса золота в качестве катализатора, сравнительно дорогостоящего и взрывоопасного реагента (1-гексина), ядовитого фенилгидразина.
Традиционным способом синтеза индолов из фенилгидразина и 2-гексанона (реакция Фишера) авторы [J. Selby [et al.] // The Journal of Organic Chemistry. – 2020. – Vol. 85. – № 19. – P. 12227-12242] получали алкилиндол 1 с выходом 87 %:
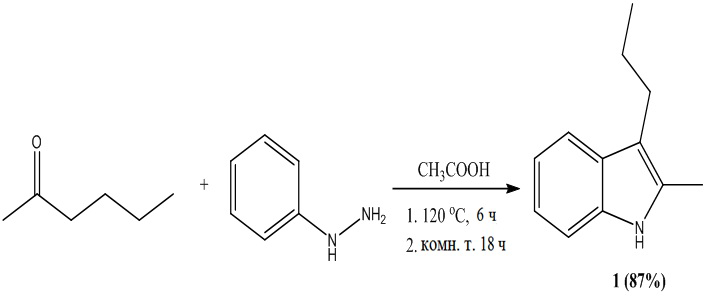
Условия синтеза – катализатор уксусная кислота, 120 °С – 6 ч, затем комнатная температура – 18 ч. Недостатками данного способа являются использование дорогостоящего реагента (2-гексанона), ядовитого фенилгидразина, долгий синтез.
Использование гомогенных катализаторов в вышеперечисленных способах приводит к многостадийности процесса, сложному отделению продуктов от катализаторов, невозможности их повторного использования. Этих недостатков лишены гетерогенные катализаторы.
В работе [L.-L. Cao [et al.] // Tetrahedron Letters. – 2011. – Vol. 52. – № 22. – P. 2837-2839] 2-метил-3-пропилиндол 1 получали восстановлением 2-метил-α-этилиндол-3-метанола под действием катализатора 5% Pd/C, бензойной кислоты в атмосфере водорода в присутствии тетрагидрофурана (ТГФ):
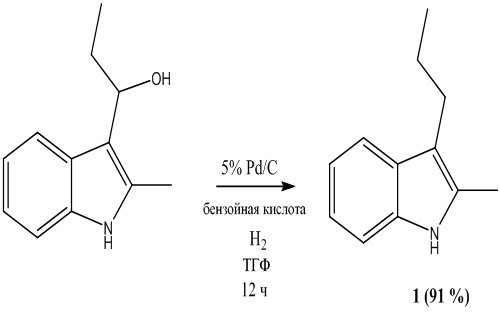
Выход целевого продукта 1 составил 91 %. К недостаткам данного способа можно отнести использование дорогостоящего реагента (2-метил-α-этилиндол-3-метанол), использование водорода, необходимость удаления бензойной кислоты.
2-Метил-3-пропилиндол 1 получали с выходом 62 % в присутствии боргидрида натрия на полимерной основе PS-BH4 [E. Chiurchiù, A. Palmieri, M. Petrini // Arkivoc. – 2019. – Vol. 2019. – № 4. – P. 69-79] разложением сульфопроизводного индола 4 (40 мин, 2 атм, комнатная температура):
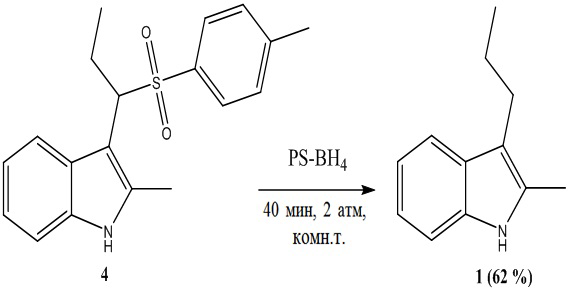
Арилсульфонилалкилпроизводное индола 4 авторы предлагают получать по методике [A. Palmieri, M. Petrini // The Journal of Organic Chemistry. – 2007. – Vol. 72. – № 5. – P. 1863-1866] взаимодействием 2-метилиндола, п-толуолсульфокислоты и альдегида. К недостаткам данного способа относятся многостадийность процесса.
В работе [M.P. Prochazka [et al.] // Acta Chemica Scandinavica. – 1990. – Vol. 44. – P. 610-613] с выходом 86 % синтезировали индол 1 в присутствии порошкообразного цеолита марки Y-82 (Union Carbide) синтезом Фишера. Цеолит (6 г) смешивали с ксилолом (растворитель, 40 мл) в течение 5 мин, затем добавляли 2-гексанон и перемешивали суспензию 1 ч. Добавляли фенилгидразин (2-гексанон: фенилгидразин = 1:1 моль/моль), проводили реакцию в условиях кипения (~130-140 °C) в течение 3 ч. К недостаткам данного способа относится использование больших количеств катализатора, ядовитого фенилгидразина, больших объемов растворителя.
Задачей настоящего изобретения является разработка эффективного гетерогенно-каталитического способа синтеза 2-метил-3-пропилиндола.
Решение этой задачи достигается тем, что синтез алкилиндола (1) осуществляют взаимодействием анилина с 1,2-пропандиолом в присутствии гранулированного цеолита структурного типа FAU в H-форме высокой степени кристалличности, имеющего микро-мезо-макропористую структуру (H-Yh). Реакцию проводят в автоклаве при 260 °С, мольном соотношении анилин : 1,2-пропандиол = 1 : 2-5, в присутствии 5-20 мас.% катализатора H-Yh, в течение 6-9 ч.
Основным продуктом реакции анилина с 1,2-пропандиолом в присутствии цеолитного катализатора H-Yh является 2-метил-3-пропилиндол 1:
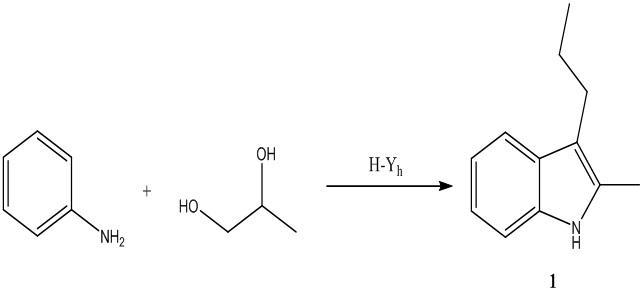
Кроме целевого продукта 1, в реакционной смеси обнаружены 3-метил-2-этилхинолин (Х), 3-метил-2-этил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амин (ТГХА), 3,4-диметил-1-фенилпиррол (П), алкиланилины, продукты превращения спирта. Побочные N-гетероциклические соединения являются ценным сырьем для получения лекарственных препаратов, ингибиторов коррозии, полимеров и т.д. [Vandekerckhove S.; D’hooghe, M. Bioorganic & Medicinal Chemistry, 2015; 23(16), 5098 – 5119; Chitra S.; Saranya J.; Lavanya, K. Corrosion Reviews, 2018; 36(4), 365-371;A. K. D. Diaw; A. Yassar; D. Gningue-Sall; J.-J. Aaron / Arkivoc(2009), 2008(17), 122-144; 8. S. Tarkuc; E. Sahmetlioglu; C. Tanyeli; I.M. Akhmedov; L. Toppare (2006), 51(25), 5412–5419].
С использованием двух недорогих реагентов – 1,2-пропандиола и анилина – в литературе описаны синтезы 3-метилиндола (скатола) [Wenhui L.; Xinghai L.; Dongyan L.; Lei S.; Qi S. Chin. J. Catal, 2009; 30(12), 1287–1290; Yang H.; Wenhui L.; Dongyan L.; Jing L.; Lei S.; Qi S. Journal of Natural Gas Chemistry, 2009;18, 445–448; Патент Китай 107540595, 106278985] и 2-метилиндола [Lee H.; Yi C. S. Organometallics, 2019; 35(11), 1973–1977; Charvieux A.; Hammoud A.A.; Duclos M.-Ch.; Duguet N.; Métay E. Tetrahedron Letters, 2021; 78, 153270; Zhang M.; Xie F.; Wang XiaoTing; Yan F.; Wang T.; Chen M.; Ding Yu. RSC Adv., 2013; 3, 6022–6029]. Упоминания о синтезе 2-метил-3-пропилиндола 1 реакцией 1,2-пропандиола с анилином в литературе отсутствуют.
Цеолит H-Yh синтезирован в виде гранул без связующих веществ; его гранулы представляют собой единые сростки цеолитных кристаллов и обладают степенью кристалличности, близкой к 100%. Пористая структура гранул состоит из микропористой структуры самого цеолита Y и мезопористой структуры, сформировавшейся между сростками кристаллов. Существенным преимуществом цеолита H-Yh перед высокодисперсными цеолитами является то, что он синтезируется в гранулах. Гранулированный катализатор обладает лучшими физическими свойствами: не пылит, не слеживается, легко рассеивается и легко отделяется от реакционной массы фильтрованием (в отличие от высокодисперсного, который быстро забивает фильтр или проходит через полотно фильтра).
Обычно гранулированные цеолиты синтезируют следующим образом: смешивают высокодисперсный цеолит со связующим материалом, а затем полученную смесь формуют в гранулы. Введение связующего материала в состав гранул снижает адсорбционную ёмкость и каталитическую активность цеолитов по сравнению с высокодисперсными цеолитами, а в ряде случаев не удается обеспечить механическую прочность получаемых таким образом гранулированных материалов. Гранулы катализатора H-Yh на 100% состоят из цеолита Y, в них отсутствует связующее вещество.
Цеолит H-Yh имеет комбинированную микро-мезо-макропористую кристаллическую структуру, которая высокостабильна и не разрушается в процессе ионного обмена катионов Na+ на H+.
Использование предлагаемого способа имеет следующие преимущества перед известными способами:
1) Для синтеза используются недорогие, доступные, стабильные реагенты.
2) Реакция проводится в присутствии гетерогенного катализатора – цеолита H-Yh с иерархической пористой структурой.
3) Цеолит используется в виде гранул.
4) Цеолитный катализатор легко отделяется от реакционной массы и может использоваться повторно.
5) Упомянутые выше реакции осуществляются в присутствии растворителей, которые используются в больших объемах, в предлагаемом способе растворитель отсутствует, следовательно, не требуется стадия его отделения и очистки.
Гранулированный цеолитный катализатор H-Yh синтезируют в Na-форме по методу, приведенному в [Travkina O.S, Agliullin M.R, Filippova N.A, Khazipova A.N, Danilova I.G, Grigor'eva N.G, Narender N, Pavlov M.L, Kutepov B.I // RSC Advances. 7 (2017) 32581-32590; Патенты РФ № 2540086, № 2553876]. Путем ионного обмена из раствора NH4NO3 цеолит Na-Yh переводят в NH4-форму; последующей прокалкой при 540 oС в течение 4 ч переводят в Н-форму.
Реакцию проводят в автоклаве при 260 °С, мольном соотношении анилин : 1,2-пропандиол = 1 : 2-5, в присутствии 5-20 % катализатора H-Yh, в течение 6-9 ч.
Продукты реакции экстрагируют хлористым метиленом и анализируют с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) на модульном приборе SHIMADZU со спектрофотометрическим детектором SPD-20a. Условия съемки: колонка – Agilent C18 (4,6⋅250 мм), элюент-CH3CN/H2O - 80/20, скорость подачи элюента - 1 мл/мин.
Изобретение иллюстрируется следующими примерами.
ПРИМЕР 1.
В металлический автоклав загружают 0.2 г (2.2 ммоль) анилина, 0.8 г (11.0 ммоль) 1,2-пропандиола и 0.1 г (10 % мас. в расчете на исходную смесь) цеолита H-Yh, автоклав герметично закрывают и помещают в термостатируемый шкаф. Реакцию проводят при температуре 260°С в течение 6 ч при непрерывном вращении автоклава.
После окончания реакции автоклав охлаждают до комнатной температуры, продукты реакции экстрагируют дихлорметаном, после отгонки растворителя анализируют методом высокоэффективной жидкостной хроматографии.
Конверсия анилина составляет 99 %, селективность образования 2-метил-3-пропилиндола 1 - 55 %.
ПРИМЕРЫ 2-6. Аналогично примеру 1. Условия и результаты примеров представлены в таблице.
Таблица
Синтез 2-метил-3-пропилиндола 1 в присутствии иерархического цеолита H-Yh
(температура 260°С)
%
3-метил-2-этилхинолин (Х), 3-метил-2-этил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амин (ТГХА),
3,4-диметил-1-фенилпиррол (П).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3,4-диметил-1-фенилпиррола | 2023 |
|
RU2830162C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-МЕТИЛ-2-ЭТИЛ-N-ФЕНИЛ-1,2,3,4-ТЕТРАГИДРОХИНОЛИН-4-АМИНА | 2023 |
|
RU2808560C1 |
| Способ получения 2-(4-метилхинолин-2-ил)анилина | 2024 |
|
RU2838488C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-МЕТИЛ-2-ЭТИЛХИНОЛИНА | 2023 |
|
RU2803740C1 |
| Способ получения хинолинов в присутствии иерархического цеолита H-ZSM-5mmm | 2021 |
|
RU2789409C1 |
| Способ получения хинолинов | 2022 |
|
RU2786740C1 |
| Способ получения хинолинов реакцией Скраупа в присутствии иерархического цеолита Н-Ymmm | 2019 |
|
RU2738603C1 |
| Способ получения хинолина реакцией Скраупа в присутствии иерархического цеолита H-ZSM-5mmm | 2020 |
|
RU2740912C1 |
| Способ получения хинолинов в присутствии иерархического цеолита H-Ymmm | 2021 |
|
RU2789408C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ N-ПРОПИЛАНИЛИНА И 2-ЭТИЛ-3-МЕТИЛХИНОЛИНА | 2022 |
|
RU2797946C1 |
Изобретение относится к области органической химии, конкретно к способу получения 2-метил-3-пропилиндола, который находит применение в качестве репеллента в составе морского противообрастающего материала от живых организмов, для синтеза производных индолов и фотохромных красителей. Способ характеризуется тем, что 2-метил-3-пропилиндол получают взаимодействием анилина с 1,2-пропандиолом в присутствии гранулированного цеолита Yh в Н-форме с иерархической пористой структурой, в автоклаве при 260°С, мольном соотношении анилин:1,2-пропандиол = 1:2-5, в присутствии 5-20 мас.% катализатора H-Yh, в течение 6-9 ч. Технический результат – упрощение гетерогенно-каталитического синтеза целевого продукта из доступного и безопасного сырья. 1 табл., 6 пр.
Способ получения 2-метил-3-пропилиндола, характеризующийся тем, что 2-метил-3-пропилиндол получают взаимодействием анилина с 1,2-пропандиолом в присутствии гранулированного цеолита Yh в Н-форме с иерархической пористой структурой, в автоклаве при 260°С, мольном соотношении анилин:1,2-пропандиол = 1:2-5, в присутствии 5-20 мас.% катализатора H-Yh, в течение 6-9 ч.
| Tsuji Y | |||
| et al | |||
| Ruthenium-complex-catalyzed N-heterocyclization | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| The Journal of Organic Chemistry, 52 (9), 1987, 1673-1680 | |||
| Prochazka M.P | |||
| et al | |||
| Enhanced Regioselectivity for Unsymmetrical Ketone Substrates | |||
| Acta Chemica Scandinavica, 44, 1990, | |||
Авторы
Даты
2024-12-04—Публикация
2024-05-07—Подача