ТЕХНИЧЕСКАЯ ОБЛАСТЬ
Настоящее изобретение относится к клеточным линиям, содержащим их композициям для лечения меланом, способам получения композиций и к способам лечения. Более конкретно, изобретение относится к различным клеточным линиям меланомы человека для лечения злокачественных заболеваний, где клеточные линии представляют собой: (a) Mel-XY1 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии (German Collection of Microorganisms and Cell Cultures) DSMZ - Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrabe 7 B 38124 Braunschweig, Germany, 23 марта 2007 года под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ - Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrabe 7 B 38124 Braunschweig, Germany, 23 марта 2007 года под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ - Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrabe 7 B 38124 Braunschweig, Germany, 23 марта 2007 года под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ - Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrabe 7 B 38124 Braunschweig, Germany, 23 марта 2007 года под регистрационным номером DSM ACC2829) или (e) их субпопуляции. Клеточные линии могут быть облученными, с получением, таким образом, популяций с апоптотическим фенотипом и популяций с некротическим фенотипом таких клеточных линий. Композиции могут содержать адъюванты и/или иммуномодуляторы и/или аутологичные дендритные клетки.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В настоящее время предпринято множество попыток и используют множество средств для исследования в области иммунотерапии злокачественных опухолей. Важные существующие данные указывают на центральную роль T-лимфоцитов в эффективных иммунных ответах на злокачественную опухоль (Oliver RT, Nouri AM. T; Cancer Surv 1992; 13:173-204). В связи с этим использовали лечение аллогенными клетками отдельно, с адъювантами или в сочетании с некоторыми цитокинами.
С другой стороны известно, что дендритные клетки (DC) представляют собой антигенпрезентирующие клетки, которые могут инициировать T-клеточный ответ вследствие их исключительной способности стимулировать наивные T-лимфоциты (Schuler G, Steinman RM. J Exp. Med 1997; 186:1183-7, и Banchereau J, Steinman RM. Nature 1998; 392:245-52).
Несколькими авторами на моделях на мышах и у человека было показано, что DC поглощают апоптотические клетки и, таким образом, представляют антигены для образования комплексов HLA класса I/пептиды, позволяющих индукцию цитотоксических T-лимфоцитов (Albert МЛ, Pearce SF, Francisco LM, Sauter B, Roy P, Silverstein RL, Bhardwaj N. J Exp Med. 1998, 188: 1359-1368; Chen Z, Moyana T, Saxena A, Warrington R, Jia Z, Xiang J. Int J Cancer. 2001, 93: 539-548, и Shaif-Muthana M, McIntyre C, Sisley K, Rennie I, Murray A. Cancer Res. 2000, 60: 6441-6447). Для этого процесса существенно, что апоптотические клетки индуцируют созревание дендритных клеток (DC), однако многие авторы информировали, что апоптотические клетки человека не вызывают созревания DC, или индуцируют утрату созревания таких как DC (Pietra G, Mortarini R, Parmiani G, Anichini A. Cancer Res 2001, 61: 8218-8226; Labarriere N, Bretaudeau L, Gervois N, Bodinier M, Bougras G, Diez E, Lang F, Gregoire M, Jotereau F. Int J Cancer 2002, 101: 280-286 и Demaria S, Santori FR, Ng B, Liebes L, Formenti SC, Vukmanovic S. J Leukoc Biol. 2005, 77: 361-368).
В патенте США 6187306, выданном Pardoll et al., описан способ лечения меланомы и защиты от нее, который включает применение по меньшей мере одной или нескольких аллогенных клеточных линий, экспрессирующих иммунодоминантные антигены меланомы, где клеточная линия модифицирована таким образом, чтобы она экспрессировала цитокины, и введение такой трансформированной линии пациенту, имеющему меланому или подверженному риску возникновения заболевания. Несмотря на важность используемой клеточной линии или клеточных линий, которые экспрессируют большинство иммунодоминантных антигенов, не описана новая клеточная линия или сочетание клеточных линий, экспрессирующих большинство таких антигенов. Изобретение включает по существу трансформированные клеточные линии, экспрессирующие цитокины, такие как GM-CSF.
В патенте США 5882654 и патенте США 5840317 описаны облученные клеточные линии меланомы, используемые в качестве аллогенных вакцин. Описанное лечение достигает уровней у пациентов NED ниже 50% (16/37) и демонстрирует эффективную противоопухолевую активность гуморального типа.
В патенте США 2006/0034811, выданном Wallack et al., описаны вакцины, содержащие антигенпрезентирующие клетки, нагруженные лизированными или перфорированными опухолевыми клетками, включающими цитозоль и мембраны. Опухолевые клетки могут представлять собой клетки пациента, клеточные линии или клетки, инфицированные рекомбинантным вирусом осповакцины, кодирующим IL-2. В патенте США 2006/0140983, выданном Palucka et al., описана композиция, индуцирующая иммунитет у пациентов со злокачественной опухолью, которая содержит выделенные и очищенные антигенпрезентирующие клетки, примированные для экспонирования одного или нескольких белков теплового шока, и погибшие опухолевые клетки. Антигенпрезентирующие клетки представляют собой дендритные клетки, и опухолевые клетки могут представлять собой сингенные или аллогенные клетки, например, клеточные линии. В этом документе описана необходимость поглощения белков теплового шока с помощью разрушения опухолевых клеток посредством нагревания. В представленных способах анализа не описано обязательно, что композиция обладает индуцирующей иммунитет активностью у пациентов с меланомой.
В патенте США 6602709, выданном Albert et al., описано применение апоптотических клеток для представления антигенов дендритным клеткам для индукции T-клеток. Способ пригоден для индукции антигенспецифических цитотоксических T-хелперных лимфоцитов. Дендритные клетки примируются апоптотическими клетками или их фрагментами, и они способны процессировать и представлять процессированные антигены, и индуцировать активность цитотоксических T лимфоцитов, которые можно использовать в качестве терапевтических вакцин.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте настоящего изобретения представлено несколько клеточных линий меланомы человека для лечения злокачественных заболеваний, где клеточные линии представляют собой (a) Mel-XY1 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированную Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829) или (e) их субпопуляции. Клеточные линии могут быть облученными, с получением, таким образом, популяций с апоптотическим фенотипом и популяций таких линий с некротическим фенотипом.
В другом аспекте настоящего изобретения представлена композиция для лечения меланомы, где такая композиция содержит по меньшей мере одну аллогенную клеточную линию меланомы, например (a) Mel-XY1 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829) или их сочетания, где такие клеточные линии не способны пролиферировать. Также композиция может содержать эксципиенты, адъюванты, такие как БЦЖ, и иммуномодуляторы, такие как GM-CSF или IFNα. В предпочтительном варианте осуществления композиция содержит сочетание четырех аллогенных клеточных линий меланомы: (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832) и (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии являются облученными и не способны пролиферировать. В другом предпочтительном варианте осуществления представлена композиция по изобретению, содержащая сочетания трех аллогенных клеточных линии меланомы: (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831) и (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), где клеточные линии являются облученными и не способны пролиферировать.
В другом аспекте настоящего изобретения представлена композиция для адъювантного лечения меланомы, где такая композиция содержит по меньшей мере одну аллогенную клеточную линию меланомы, например (a) Mel-XY1 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), и их сочетания, и где такие клеточные линии являются облученными и не способны пролиферировать. Также композиция может содержать эксципиенты, адъюванты, такие как БЦЖ, и иммуномодуляторы, такие как GM-CSF и/или IFNα. В одном предпочтительном варианте осуществления композиция по изобретению содержит сочетание аллогенных клеточных линий меланомы (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832) и (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии являются облученными и не способны пролиферировать. В другом предпочтительном варианте осуществления композиция по изобретению содержит сочетание аллогенных клеточных линий меланомы: (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831) или (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), где такие клеточные линии являются облученными и не способны пролиферировать.
В другом аспекте настоящего изобретения представлена композиция для лечения меланом человека, содержащая зрелые аутологичные дендритные клетки, аутологичные дендритные клетки, нагруженные клетками по меньшей мере аллогенной клеточной линии меланомы человека, апоптотические клетки такой по меньшей мере одной гетерологичной клеточной линии меланомы человека. Клеточная линия меланомы человека представляет собой одну или несколько из следующих линий: (a) Mel-XY1 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829) или (e) их субпопуляции.
В другом аспекте изобретения представлена композиция для адъювантного лечения меланомы человека, содержащая зрелые дендритные клетки, дендритные клетки, нагруженные клетками по меньшей мере одной аллогенной клеточной линии меланомы человека, апоптотические клетки одной гетерологичной клеточной линии меланомы человека и некротические клетки одной гетерологичной клеточной линии меланомы человека. Клеточная линия меланомы представляет собой одну или несколько из следующих клеточных линий: (a) Mel-XY1 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированная в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829) или их субпопуляции.
В другом аспекте настоящего изобретения представлен способ получения композиции, где такой способ осуществляют в следующих стадиях:
a) размораживание и культивирование клеточных линий (a) Mel-XY1 (Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832);
b) смешивание этих трех клеточных линий;
c) облучение этих трех клеточных линий;
d) добавление адъювантов и эксципиентов к смесям клеточных линий. Также способ может включать на стадии a) добавление клеточной линии (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829).
В другой задаче настоящего изобретения представлен способ получения композиции, который включает стадии:
a) размораживания и культивирования клеточных линий (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832) и Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829);
b) смешивания таких клеточных линий;
c) облучения таких клеточных линий;
d) получения аутологичных дендритных клеток; и
e) со-культивирования в течение некоторого времени аутологичных дендритных клеток с облученными клеточными линиями стадии c).
В другом аспекте настоящего изобретения представлен способ индуцирования противоопухолевого иммунного ответа у пациентов, имеющих меланому, который включает введение пациенту, нуждающемуся в этом, эффективного количества сочетания клеточных линий (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831) и (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), где такие клеточные линии не способны пролиферировать. Введение можно проводить вместе с адъювантами и/или иммуномодуляторами.
В другом аспекте настоящего изобретения представлен способ индуцирования противоопухолевого иммунного ответа у пациентов, имеющих меланому, который включает введение пациенту, нуждающемуся в этом, эффективного количества сочетания клеточных линий (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии не способны пролиферировать.
В другом аспекте настоящего изобретения представлен способ индуцирования противоопухолевого иммунного ответа у пациентов, имеющих меланому, который включает введение пациенту, нуждающемуся в этом, эффективного количества аутологичных дендритных клеток, со-культивированных в течение от 6 до 72 часов, и сочетания клеточных линий: (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832), (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии не способны пролиферировать.
ОПИСАНИЕ РИСУНКОВ
На фиг.1 представлен иллюстративный пример результатов гамма-облучения смеси клеточных линий по изобретению в отношении индукции апоптоза и некроза (клетки Apo-Nec). На панели A представлены необлученные клетки, и на панели B представлены клетки после гамма-облучения 70 Грэй и окрашивания аннексином V-FITC и IP (иодидом пропидия). Ранние апоптотические клетки определяют как аннексин V-FITC+/IP-, а некротические клетки были двойными положительными.
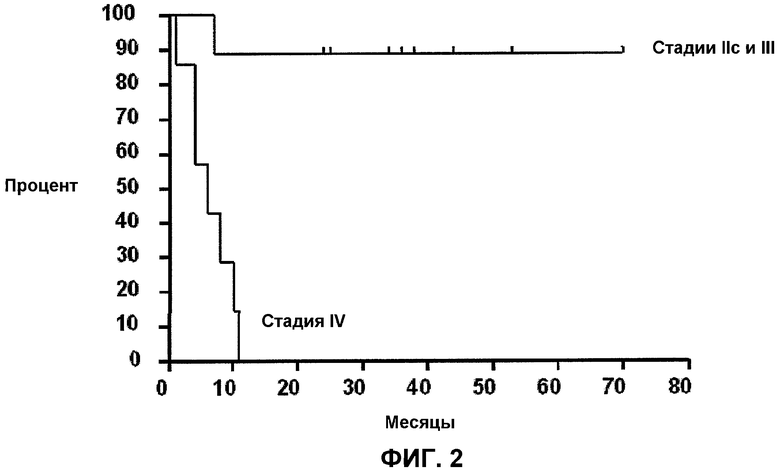
На фиг.2 представлен график Каплана-Мейера для пациентов, которым вводили композицию по изобретению DC/Apo-Nec.
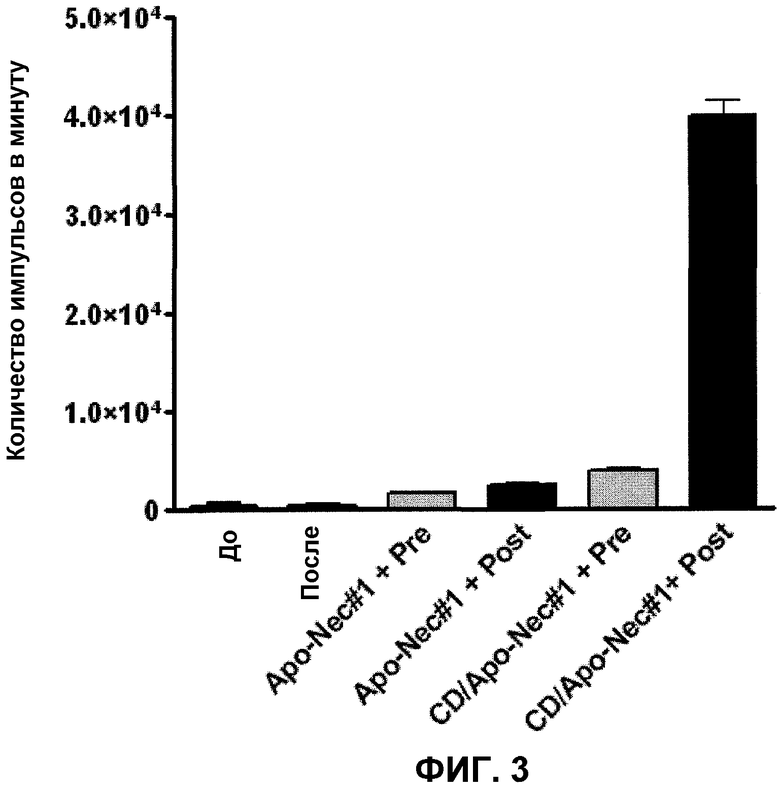
На фиг.3 представлена пролиферация лимфоцитов in vitro в ответ на аутологичные опухолевые клетки, представленные DC. Результаты представлены в качестве средних значений ± SD cpm (число импульсов в минуту) для трех значений. Лимфоциты с фитогемаглютинином (PHA), имеющие более 7×104 cpm, инкубировали в качестве положительных контролей.
На фиг.4 представлено окрашивание тетрамером на антигены Melan A/MART-1 и gp100. На панели A представлены результаты, полученные для образцов PBMN от пациентов с HLA-A*0201, участвующих в тестировании. *ND означает: нет данных вследствие недостаточного количества CD8+ T-клеток в образцах после применения. На панели B показано повышение CD8+ HLA T-лимфоцитов/тетрамерный пептид+ в PBMC от пациента #2. Количества соответствуют проценту CD8+ HLA/тетрамерный пептид+. PBMC с HLA-A*0201 от здоровых доноров окрашивали в качестве контролей.
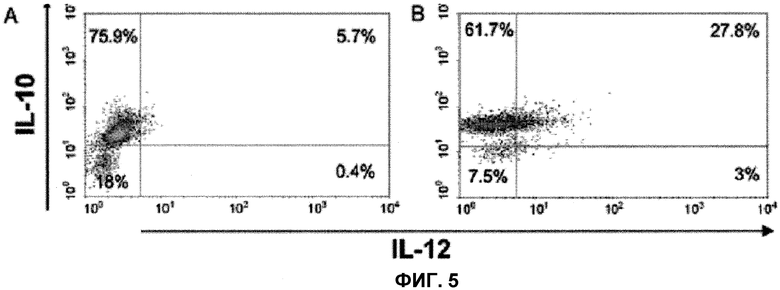
На фиг.5 представлено внутрицитоплазматическое измерение IL-10 и IL-12 в клетках Apo-Nec по изобретению. На панели A представлены результаты FACS для DCin, и на панели B представлены результаты FACS для клеток DC/Apo-Nec.
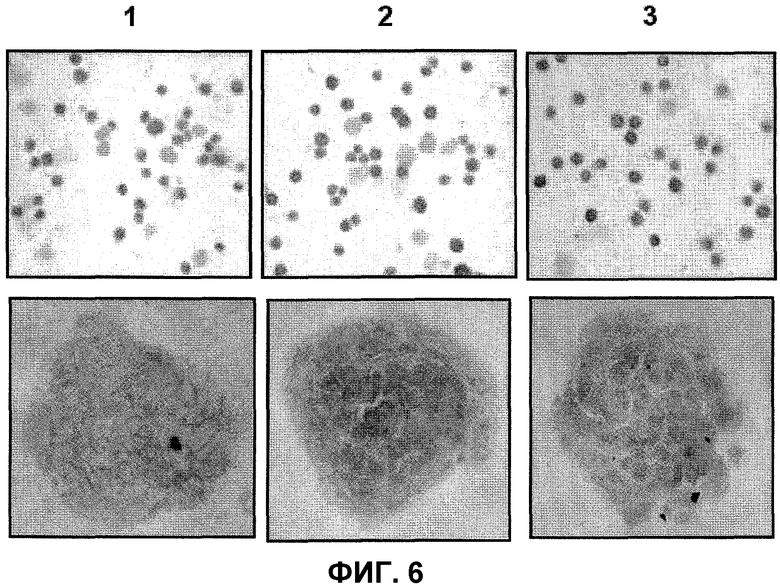
На фиг.6 представлена экспрессия антигена HMB45 и Mart-1 в линии Mel-XY1 и в производных клонах этой клеточной линии. Три верхние панели соответствуют клеточной линии, а три нижние панели соответствуют клонам. Столбец 1 соответствует клеточной линии и контрольным клонам, столбец 2 соответствует клеточной линии с экспрессией HMB45 и клонам соответственно; и столбец 3 соответствует клеточной линии с экспрессией Mart-1 и клонам.
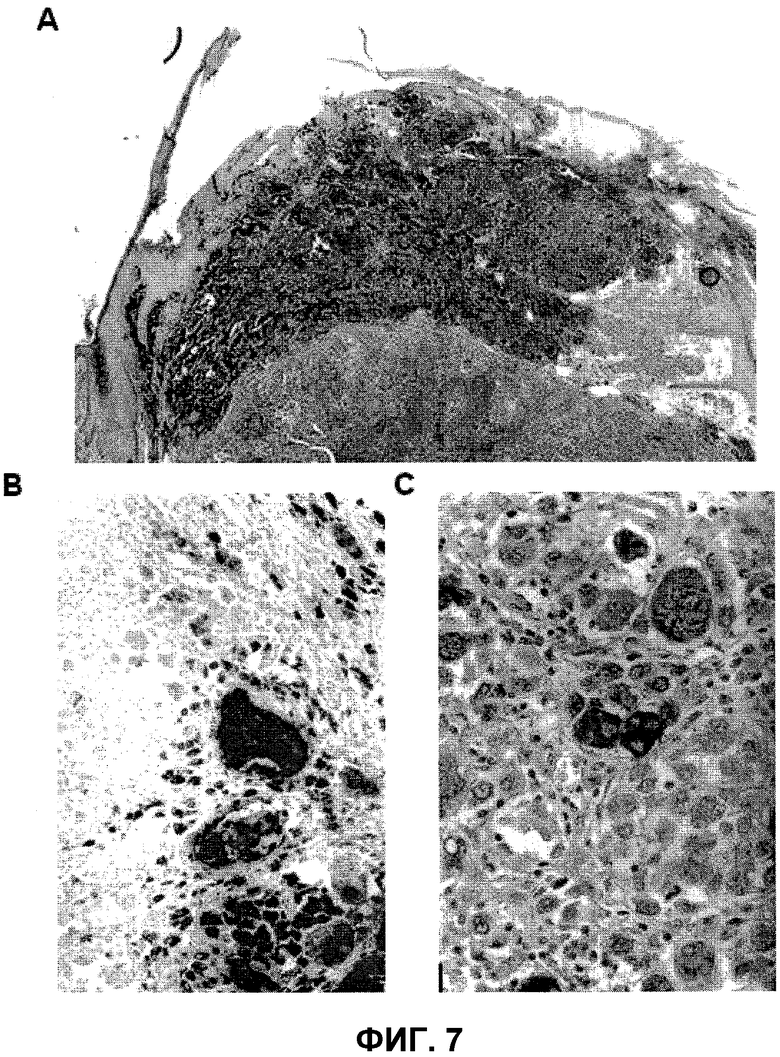
На фиг.7 представлен биоптат меланомы от пациента #100. На панели A представлено изображение с низким увеличением (25X), где можно видеть положительные и отрицательные по Ag gp100 опухолевые клетки; на панели B представлена экспрессия гетерогенного gp100, где можно видеть клетки с высокой, умеренной и нулевой экспрессией (400x); на панели C представлена экспрессия гетерогенного Ag MART-1, где можно видеть клеточный клон с высокой экспрессией, окруженный отрицательными клетками (400x).
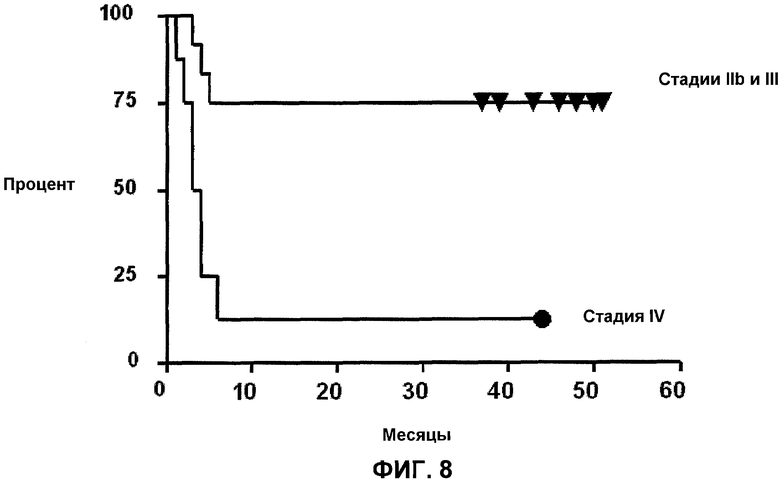
На фиг.8 представлен график Каплана-Мейера для пациентов, которым вводили композицию Apo-Nec по изобретению.
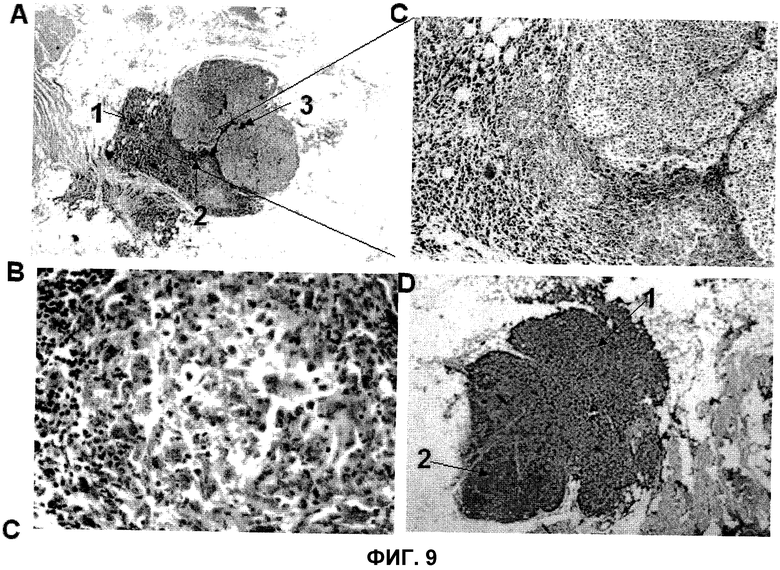
На фиг.9 представлены метастазы в кожу, вырезанные у пациента #200, которому вводили композицию Apo/Nec по изобретению, в дополнение к GM-CSF и БЦЖ. На панели A представлены макрофаги в некротической области опухоли (1), инфильтрированной лимфоцитами, контактирующими с опухолевыми клетками (2), и жизнеспособной области опухоли (3). На панели B представлен фрагмент 100x области с высокой инфильтрацией опухоли, на панели C представлен фрагмент 400x той же области, где наблюдают инфильтрирующие лимфоциты, на панели D представлен фрагмент того же метастаза, где большая его часть является некротизированной с макрофагами, нагруженными меланином (1), и жизнеспособная область (2) (25X).
На фиг.10 представлены изображения компьютерной аксиальной томографии пациента #300, которому вводили композицию Apo-Nec по изобретению в дополнение к БЦЖ. На панели A стрелкой показано расположение метастаза в легком, а на панели B представлено изображение аксиальной томографии, полученное через 5 месяцев.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В этой заявке термины "сочетание" и "смесь" являются взаимозаменяемыми.
Когда в настоящем изобретении приводятся композиции, которые модифицируют иммунную систему у млекопитающих, необходимо понимать, что эти композиции также известны специалисту в данной области как вакцинные композиции, клеточные вакцины или просто вакцины.
Четыре клеточные линии по изобретению были депонированы согласно Будапештскому договору в German Collection of Microorganisms and Cell Cultures DSMZ 23 марта 2007 года под следующими регистрационными номерами: клеточная линия Mel-XY1 DSM ACC2830, линия Mel-XY2 DSM ACC2831, линия Mel-XY3 DSM ACC2832 и линия Mel-XX4 DSM ACC2829.
Результаты анализов по охарактеризации клеточных линий представлены в следующей таблице.
B18/B37
B18/B65
B18
B18/B65(14)
GR52/DR53
DR13
GR52
Из охарактеризации клеточной линии MEL-XY1 следует, что клетки растут в качестве гетерогенного амеланотического клеточного монослоя по размеру и форме, где большинство из них являются кубическими или удлиненными и без отростков. Они являются немного меланотическими при высокой плотности. Клетки MEL-XY1 образуют значительное количество колоний в полутвердом агаре. Клетки MEL-XY1 являются онкогенными у бестимусных мышей (голых) и не образуют метастазы.
Из охарактеризации клеточной линии MEL-XY2 следует, что клетки растут до размеров гетерогенного амеланотического клеточного слоя. Клетки являются небольшими и менее многочисленными, многоядерными и с выступающими ядрами. Также видны клетки с характерными для меланомы дендритными отростками. При росте с высокой плотностью, они могут накапливаться и образовывать микроопухоли. Клетки MEL-XY2 являются онкогенными у бестимусных мышей (голых) и не образуют метастазы.
Из охарактеризации клеточной линии MEL-XY3 следует, что клетки растут в виде монослоя. Клетки являются однотипными, небольшими и частично округлыми. Вырастая с высокой плотностью, они могут скапливаться и образовывать микроопухоли. Клетки MEL-XY3 образуют множество колоний в полутвердом агаре. Клетки MEL-XY3 являются онкогенными у бестимусных мышей (голых) и не образуют метастазы.
Из охарактериации клеточной линии Mel-XX4 следует, что эта клеточная линия растет в виде веретенообразного монослоя с высокой плотностью. При низкой плотности, в ней заметны дендритные отростки, сходные с меланоцитами. Клетки являются меланотическими, и некоторые из них имеют множество ядер с выступающим ядром. Время удвоения популяции составляет 172-173 часов, и они образуют колонии в анализе на мягком агаре.
Когда клеточную линию Mel-XX4 по изобретению трансплантировали голым мышам (с иммунной супрессией), получали опухолевые клеточные линии in vivo. Серийные пассажи от исходных опухолей продемонстрировали, что у 100% животных с трансплантатами в течение первого месяца развились опухоли. Рост опухоли был медленным и через 84 суток достигал среднего значения 372±63 мм3. Клеточная линия Mel-XX4 по изобретению является онкогенной при подкожной инъекции в количестве 3×106 клеток.
Из анализа модального числа хромосом следует следующее: линия MEL-XY1 по изобретению демонстрирует разброс в числе хромосом (между 105 и 110), и, таким образом, четкое модальное число не было ясным (самцы). Линия MEL-XY2 по изобретению демонстрирует бимодальную тенденцию с числами хромосом 89 и 91 (самцы). Клеточная линия MEL-XY3 по настоящему изобретению демонстрирует модальное число (самцы). Наиболее частые изменения числа представляли собой отсутствие хромосом в парах 2 и 6 и дополнительные хромосомы в парах 20 и 22. Клеточная линия MEL-XY4 по изобретению демонстрирует модальное число 57-58 (самки).
Исследовали индукцию гамма-облучением апоптоза в клеточных линиях по изобретению. Применение облучения 50 Грэй было достаточным для тотального подавления клоногенной способности каждой клеточной линии по изобретению в мягком агаре. Не выявили значимых отличий в степени индукции апоптоза/некроза, когда клетки облучали 70 или 100 Грэй. На фиг.1A показано, что необлученные клетки меланомы содержали между 6-9% ранних апоптотических клеток, характеризующихся окраской Anexin-V+/IP- (нижняя правая панель). После облучения при 70 Грэй и культивирования в течение 72 ч, получали 45-53% ранних апоптотических клеток (см. фиг.1 B, нижняя правая панель). Аннексин-V и IP окрашивали некротические клетки с возрастанием от 7,5% в необлученных клетках до приблизительно 15% в облученных клетках (верхние левые панели). Таким образом, в настоящей патентной заявке облученные клетки меланомы по изобретению называют клетками Apo-Nec, и композиция, содержащая одну или несколько из любых из клеточных линий Apo-Nec (Mel-XY1, Mel-XY2, Mel-XY3 и/или Mel-XX4), известна как композиция Apo-Nec.
Облучение клеток позволяет получить клетки, неспособные пролиферировать, пригодные для изготовления композиций, таких как композиция Apo-Nec по изобретению. Специалисту в данной области очевидно, что композиция Apo-Nec по изобретению может содержать любую из клеточных линий по изобретению или их различные сочетания. В предпочтительном варианте осуществления композиция Apo-Nec по изобретению содержит смесь или сочетание клеточных линий Mel-XY1, Mel-XY2 и Mel-XY3. В другом предпочтительном варианте осуществления композиция Apo-Nec по изобретению содержит смесь или сочетание клеточных линий Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4. Смесь предпочтительных клеточных линий Apo-Nec по изобретению обеспечивает сочетание множества антигенов, индуцирующих превосходный противоопухолевый иммунный ответ.
Неожиданно, сочетание опухолевых антигенов, представляемых смесью четырех клеточных линий Apo-Nec по изобретению, индуцирует специфический T-клеточный иммунный ответ против опухоли и позволяет достигнуть отсутствия заболевания у 80% пациентов, при введении им композиции Apo-Nec по изобретению (см. фиг.8).
Линии по изобретению также использовали для получения композиции по изобретению, известной как DC/Apo-Nec, которая содержит по меньшей мере одну из клеточных линий по изобретению и аутологичные дендритные клетки.
В предпочтительном варианте осуществления клеточные линии представляют собой различные сочетания линий Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4. В качестве неограничивающего примера сочетание может содержать смесь клеточных линий Mel-XY1 и Mel-XY2, или смесь линий Mel-XY1, Mel-XX4. В предпочтительном варианте осуществления сочетание клеточных линий содержит смесь клеточных линий Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4; таким образом, присутствуют четыре типа клеток.
В предпочтительном варианте осуществления композиция DC/Apo-Nec по изобретению содержит сочетание облученных клеточных линий Mel-XY1, Mel-XY2, Mel-XY3, Mel-XX4 и аутологичные дендритные клетки.
Конкретное сочетание четырех клеточных линий по изобретению обеспечивает уникальный источник нативных антигенов для нагрузки дендритных клеток, кроме того, предоставляя антигены клоногенных клеток. Необходимо учитывать, что сочетание четырех облученных клеточных линий по изобретению не только обеспечивает конкретное сочетание нативных антигенов, но также содержит конкретное сочетание клеточных популяций, где присутствует приблизительно 50% апоптотических клеток и приблизительно 15% некротических клеток. Это сочетание популяций индуцирует созревание DC.
Исследование I стадии композиции DC/Apo-Nec по изобретению проводили у 16 пациентов с меланомой, характеристики которых представлены в таблице 2.
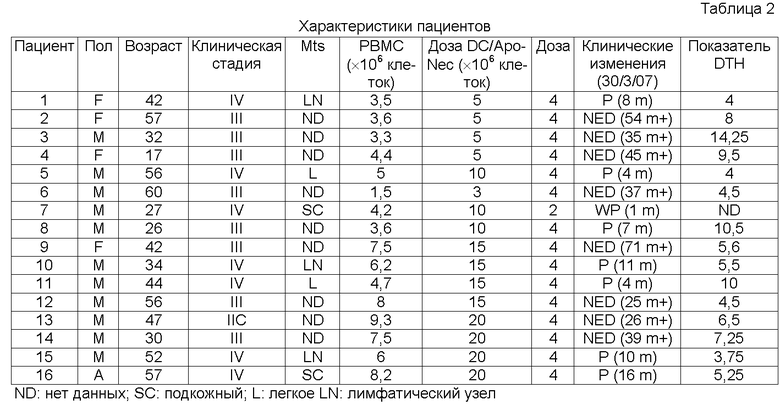
Средний возраст составлял 42 года (в диапазоне от 17 до 60 лет). Введение проводили пяти женщинам и одиннадцати мужчинам. Один из пациентов имел меланому стадии IIC AJCC, восемь имели меланому стадии III, и семь имели меланому стадии IV. Пациенты #5 и #11 подвергались хирургической операции по удалению метастазов в легком; пациент #16 имел подкожные метастазы, и пациентам #1, #10 и #15 была проведена лучевая терапия в подмышечной области после хирургической операции вследствие разрыва капсулы лимфатического узла. Группам из четырех пациентов проводили введение и промывание 5, 10, 15, или 20×106 дендритных клеток (CD), со-культивированных с клетками Apo-Nec (композиция DC/Apo-Nec по изобретению). Каждому пациенту вводили раз в две недели дозу композиции DC/Apo-Nec (0,3 мл) без адъювантов. Пациент #7 был исключен из протокола после второго применения вследствие быстрого прогрессирования заболевания после спортивной травмы на правом бедре и неконтролируемой инфекции; этот пациент не был заменен.
Незрелые дендритные клетки (DCin) продемонстрировали следующий паттерн: 95,1±3,6% были CD14-/CD11c+, и 70±6% были CD1a+. Оцененная чистота составляла приблизительно 60%.
Из 1×108 PBMC, посеянных в бессывороточной среде, получили приблизительно 3×106 DC.
Когда DCin, полученные от пациентов, и клетки, содержащиеся в композиции DC/Apo-Nec по изобретению, охарактеризовали, было выявлено, что 42,3%±13,7 клеток Dcin от пациентов (n=15) были способны фагоцитировать клетки Apo-Nec по изобретению. Фагоцитоз клеток Apo-Nec оценивали с помощью электронной микроскопии, наблюдая целые клетки Apo-Nec или их части в вакуолях DC.
Способность клеток Apo-Nec по изобретению влиять на процесс созревания происходящих из моноцитов клеток DC исследовали посредством измерения специфичных маркеров DC-клеток проточной цитометрией (FACS) (FACSCalibur , BD Biosciences, San Jose, CA). Фагоцитоз клеток Apo-Nec по изобретению привел к зрелому фенотипу DC-клеток по сравнению с контролями, инкубированными с LPS. О зрелости DC-клеток свидетельствовало повышение экспрессии CD83, CD80, CD86, HLA класса I и II и CD40. После фагоцитоза, было выявлено снижение эндоцитоза FITC-Dx, составляющее 75,2%±16, по сравнению с DCin.
Экспрессия рецептора 7 хемокинов (мотив C-C) (CCR7) повышалась в DC после фагоцитоза клеток Apo-Nec по изобретению у всех пациентов, и это было связано с миграцией CD-клеток in vitro в направлении MIP-3β. Клетки DCin (9,6% CCR7+, MFI: 23,3) мигрировали в направлении MIP-1α, но не в направлении MIP-3β; напротив, клетки DC/Apo-Nec (81,8% CCR7+, MFI: 41,2) отчетливо мигрировали в направлении MIP-3β, но не в направлении MIP-1α.
За исключением пациента #6, у которого был показан низкий выход PBMC, и, таким образом, дозу клеток DC/Apo-Nec 10×106 нельзя было получить и необходимо было вводить дозы 3×106 клеток на применение, всем остальным пациентам вводили ожидаемые дозировки композиции DC/Apo-Nec по изобретению: группа 1: 5×106, группа 2: 10×106, группа 3: 15×106 и группа 4: 20×106. Композиция DC/Apo-Nec по изобретению хорошо переносилась, и слабые выявленные случаи токсичности всегда имели степень 1. В областях применения были выявлены слабые местные реакции и DTH, состоящие из эритемы и папул. Ни у одного из пациентов не развивались проявления аутоиммунного заболевания (таблица 3).
5×106
После наблюдения в среднем в течение 41,5 месяцев после хирургической операции (между 25 и 71 месяцами), у пациентов стадии IIC не было выявлено признаков заболевания (NED); 7/8 (87,5%) стадии III пациенты были NED, и у 7/7 пациентов стадии IV было показано прогрессирование заболевания (см. фиг.2).
Реакции DTH оценивали для каждого применения гетерологичных клеток Apo-Nec по изобретению и оценивали интенсивность реакции с помощью показателя DTH, как описано в примерах. Только у 6/15 пациентов была выявлена небольшая реакция DTH перед применением против клеток Apo-Nec по изобретению. В анализах DTH было показано, что применение клеток Apo-Nec индуцирует специфическую реактивность у всех пациентов, поскольку показатель DTH был значимо выше после применения второй дозы композиции DC/Apo-Nec, по сравнению с основными реакциями, наблюдаемыми после первого применения (критерий Манна-Уитни P=0,029, n=15). Показатели DTH были более высокими у пациентов NED, чем у пациентов с прогрессированием заболевания (P=0,28, критерий суммы рангов Манна-Вилкоксона).
Увеличение количества клеток DC/Apo-Nec на применение не приводило к значимому увеличению показателя DTH.
До и после применения не наблюдали гуморального ответа против живых клеток меланомы, содержащихся в композиции по изобретению, оцениваемого анализом FACS. Также оценивали наличие реактивных антител против клеток Apo-Nec в сыворотке до и после применения способом вестерн-блоттинга. У четырех пациентов (#3, #4, # и #16) наблюдали и выявили только слабую полосу белка меланомы (>200 кДа) в сыворотке после применения, и она не была обнаружена в клеточных экстрактах рака молочной железы, используемых в качестве неспецифического контроля.
Аутологичная клеточная линия меланомы была получена для пациента #1, и, таким образом, можно оценить вероятность применения у такого пациента клеток DC/Apo-Nec, индуцирующих пролиферативный ответ лимфоцитов против его собственных клеток. Пролиферацию лимфоцитов оценивали после инкубации лимфоцитов в течение 5 суток до и после применения клеток Apo-Nec#1 (облученных опухолевых клеток от пациента #1, полученных как описано в разделе "Примеры"). На фиг.3 показано, что после применения пролиферация лимфоцитов в ответ на клетки DC/Apo-Nec#1 была более высокой по сравнению с предварительным применением лимфоцитов, что позволяет предположить, что после применения клеток DC/Apo-Nec происходит специфическая иммунизация против опухолевых антигенов, представленных клетками Apo-Nec, которые также присутствуют в опухоли пациента #1.
Семь из 15 пациентов, включенных в исследование, имели гаплотип HLA-A*0201 класса I, и это позволило исследовать ограниченный HLA опухолеспецифический ответ в образцах их собственных PBMC. Ответ против gp100, и специфические CD8+ T-клетки Melan A/MART-1, индуцированные композицией CD/Apo-Nec, оценивали посредством специфического связывания тетрамеров HLA/пептидов и секреции IFN-γ, измеряемой посредством ELISpot непосредственно в образцах периферической крови.
У 5/7 пациентов было получено достаточное количество PBMC до применения (за 7 суток до первого применения) и после применения (через 15 суток после четвертого применения) для анализа присутствия специфических CD8+ T-лимфоцитов, реактивных к gp100, и Melan A/MART-1 посредством окрашивания тетрамерами. Результаты представлены на фиг.4A. У пациентов #2 и #6 значительно повышалась частота специфических к gp100 и Melan A/MART-1 CD8+ T-клеток после применения до уровня более 1%, и они все еще оставались NED (53 и 36 месяцев соответственно, после хирургической операции), а у пациентов #5, #8 и #16 было снижено окрашивание тетрамером перед применением, и у всех из них после применения заболевание прогрессировало (фиг.3A). На фиг.4 B приведен пример с результатами пациента #2. Процентное количество CD8+ T-клеток, распознающих gp100 или пептид Melan A/Mart-1, возрастало после применения от 0,17 и 0,26 до 1,15, и 1,16 соответственно. В проводимом эксперименте не наблюдали реактивности в тех же условиях у здоровых положительных по HLA-A*0201 доноров.
Высвобождение IFN-γ анализировали в ELISpot тотальных PBMC до и после применения после инкубации в течение 24 ч с аутологичными DC-клетками, стимулированными gp100 или Melan A/MART-1, и с использованием пептидов вируса гриппа в качестве контроля (flu58-66). В этом анализе оценку проводили у 5/7 пациентов с HLA-A*0201. Было выявлено, что у двух пациентов (#5 и #16) индуцировался IFN-γ после применения композиции DC/Apo-Nec по изобретению, секретируемый CD8+ T-клетками, специфичными к gp100 и Melan a/MART-1. У пациентов #5 и #16 индуцировались CD8+ T-клетки, секретирующие IFN-γ, с частотами 7-3,5×10-4. У пациента #2 было выявлено большое количество CD8+ T-клеток, специфичных к gp100 и Melan A/MART-1 до и после применения. У этого пациента все еще не было заболевания через 54 месяца после хирургической операции. У пациентов #8 и #15 было показано низкое количество в исходный момент (до применения), и не было выявлено изменений после четырех применений композиции DC/Apo-Nec по изобретению.
Баланс между IL-12 и IL-10 в клетках DC/Apo-Nec по изобретению количественно определяли посредством FACS в различные моменты времени после фагоцитоза, и после обработки в течение 8 часов брефелдином A для внутрицитоплазматического накопления цитокинов. Как представлено на фиг.5, только 6,1% DCin продуцируют IL-12, но через 32 ч. Из со-культуры в 30,8% клеток DC/Apo-Nec была индуцирована продукция IL-12. С другой стороны, 81,6% DCin содержали цитокины в цитоплазме, и они не были модифицированы после фагоцитоза. Двойные положительные клетки, продуцирующие IL-10 и IL-12, составляли 27,8% через 24 часа (см. фиг.5).
Композиция DC/Apo-Nec по изобретению была безопасной и хорошо переносилась пациентами.
Композиция DC/Apo-Nec по изобретению индуцировала клеточные ответы у пациентов, поскольку реакция DTH при использовании клеток Apo-Nec в качестве иммуногенов возрастала у всех пациентов после второго применения, по сравнению с исходными значениями.
85% пациентов (стадия IIc и III), которым вводили композицию DC/Apo-Nec по изобретению, не имели заболевания после наблюдения в среднем в течение 41,5 месяцев, когда им проводили введение после хирургической операции (см. фиг.2). Композиция DC/Apo-Nec по изобретению сама по себе пригодна для лечения пациентов с меланомой и также пригодна в качестве адъюванта после радикальных способов лечения, поскольку она стимулирует иммунный ответ у пациента, где иммунная система устраняет все оставшиеся опухолевые клетки, защищая пациента от возможных рецидивов. Более конкретно, композиция DC/Apo-Nec по изобретению пригодна для лечения пациентов на стадиях IIB, IIC и III, которые обладают меньшей опухолевой массой, и она пригодна в качестве адъюванта после радикальных способов терапии для пациентов на стадии IV.
Специалисту в данной области очевидно, что композицию DC/Apo-Nec по изобретению можно применять для лечения меланомы человека; также ее можно применять в качестве адъюванта вместе с другими способами лечения и в качестве стимулятора иммунной системы, например, в зависимости от стадии у пациента и стадии лечения.
Важной является необходимость указать, что сочетание клеток Apo-Nec по изобретению индуцирует созревание аутологичных DC-клеток. Смесь или сочетание клеток Apo-Nec по изобретению является хорошим источником антигенов меланомы для нагрузки дендритных клеток. Следует отметить, что дендритные клетки созревают только при контакте и фагоцитозе сочетания клеток Apo-Nec по изобретению, без добавления дополнительных стимулов, например таких, как интерлейкин-1, фактор некроза опухоли-α, лиганд CD40 или простагландин E, которые обычно используют в качестве обеспечивающего созревание коктейля. DC, фагоцитирующие клетки Apo-Nec по изобретению, повышают миграцию in vitro в ответ на хемокин MIP-3β и внутриклеточную продукцию IL-12. Клетки DC/Apo-Nec по изобретению способны представлять перекрестные нативные опухолевые антигены специфическим к антигенам CTL.
Как указано выше, фагоцитоз клеток Apo-Nec посредством DCin у каждого пациента индуцировал созревание таких DC.
С другой стороны, клеточные линии по изобретению анализировали в отношении их клоногенной способности. Колонии клеточной линии MEL-XY3 по изобретению в мягком агаре присутствуют, обладая гетерогенной морфологией с низкой адгезией между клетками. Наблюдают низкую долю меланотических колоний. Колонии клеточной линии MEL-XY1 по изобретению в мягком агаре присутствуют в виде компактной морфологии с высокой адгезией между содержащимися в них клетками. Меланотические колонии наблюдают редко.
В качестве способа охарактеризации колоний сравнивали уровни экспрессии антигенов меланомы, нормализованные к экспрессии β-актина, в клеточных линиях по изобретению и в колониях таких клеточных линий в мягком агаре. Результаты охарактеризации клонов представлены в таблице 4 и на фиг.6.
*данные еще не нормализованы
Как можно видеть, в популяции и в каждой клеточной линии по изобретению существует субпопуляция клоногенных клеток, и эти клоногенные клетки также включены в объем настоящего изобретения. Наличие клоногенных клеток может обеспечить у пациента типические антигены недифференцированных клеток, также называемых стволовыми клетками.
Гетерогенность меланомных опухолей является высокой, таким образом, для иммунной терапии является основополагающим применение комплексных смесей антигенов, обеспечиваемых смесью или сочетанием клеточных линий и их субпопуляций. В качестве примера на фиг.7 представлен биоптат первичной меланомы, свидетельствующий о гетерогенности таких опухолей при сравнении экспрессии меланоцитических антигенов дифференцировки.
Когда пациентом вводят композицию Apo-Nec по изобретению вместе с БЦЖ в качестве адъюванта и GM-CSF в качестве иммуномодулятора согласно схеме, описанной ниже в разделе "Примеры", было выявлено, что у 75% пациентов (стадии IIC и III) отсутствовало заболевание при наблюдении максимально в течение 51 месяцев (см. фиг.8), и токсичность был низкой и имела только степень 1.
Представлены иллюстративные результаты от одного пациента с выбранным протоколом. Пациентом #200 является женщина европеоидной расы в возрасте 67 лет, пришедшая в ноябре 2003 года. В июне 2002 года, у нее была проведена хирургическая операция на увеличенном невусе на спине. Гистология выявила меланому кожи, уровня Clark IV, уровня Breslow 5,7 мм. В августе 2002 года, были выявлены некоторые разрастания, которые были удалены. Пациенту вводили Apo-Nec + БЦЖ + GM-CSF, с количеством GM-CSF 600 мкг (на композицию) и лечение закончили с небольшой токсичностью. При последнем клиническом обследовании на спине был выявлен ожидаемый узелок, который был удален, и его микроскопическое изображение представлено на фиг.9. Наблюдали интенсивную лимфоидную инфильтрацию с остающимися жизнеспособными областями опухоли, но также с интенсивным некрозом ткани опухоли и присутствием макрофагов, нагруженных меланином.
В качестве примера также представлены результаты пациента, которому вводили композицию Apo-Nec по изобретению + БЦЖ + IFN-α. Пациентом #300 является мужчина в возрасте 17 лет, который пришел с левой паховой аденопатией. Через два месяца проводили другое вырезание в левой паховой области, где было получено 4/11 узелков с метастазами меланомы. Ему проводили лечение интерлейкином-2 в низких дозах.
Через 14 месяцев после второго удаления был выявлен рецидив в левой паховой связке, и снова провели хирургическую операцию, где было выделено 5/7 узелков с метастазами меланомы. Пациент испытывал боль в спине. Компьютерная аксиальная томография выявила ретроперитонеальную аденопатию, и была проведена химиотерапия по схеме Дартмута. После окончания химиотерапии его начали лечить композицией Apo-Nec по изобретению + БЦЖ. Через 14 месяцев после начала лечения композицией по изобретению был выявлен узелок в левой паховой области. Ему провели хирургическую операцию, и были выявлены метастазы меланомы с выраженной лимфоплазмоцитарной инфильтрацией. Пациента продолжали лечить композицией Apo-Nec+IFN-α. На фиг.10 показана ремиссия узла в левом легком. В настоящее время пациента является здоровым.
Настоящее изобретение относится к клеточным линиям меланомы, которые в сочетании экспрессируют большинство ассоциированных с меланомой антигенов, к композициям, содержащим такие облученные линии, и к композициям, содержащим аутологичные DC, полученные ex vivo, которые фагоцитируют смесь апоптотических/некротических клеток меланомных клеточных линий.
Это изобретение лучше проиллюстрировано с помощью представленных ниже примеров, которые не следует понимать как ограничение его объема. Напротив, должно быть хорошо понятно, что могут быть упомянуты другие варианты осуществления, модификации и эквиваленты, которые после прочтения настоящего описания могут быть предложены специалистом в данной области без отклонения от сущности настоящего изобретения и/или объема прилагаемой формулы изобретения.
Пример 1
Получение, установление и поддержание клеточных линий по изобретению
Mel-XY1: Линия Mel-XY1 была получена от пациента-мужчины европеоидной расы, из метастаза в легком, вторичного по отношению к первичной меланоме на спине. Пациент погиб через два года вследствие метастазов в головной мозг.
Mel-XY2: Возраст пациента, от которого получена линия, составлял 44 года, и он являлся мужчиной европеоидной расы, имеющим изъязвленную меланому на спине (уровень Clark III). Через два года у него одновременно развились подмышечная аденопатия и метастазы в легком. Подмышечная аденопатия была удалена, диссоциирована, и эти клетки дали начало клеточной линии.
Mel-XY3: пациент являлся мужчиной европеоидной расы в возрасте 43 лет, у которого развилась первичная меланома плеча. Через два года появился метастаз в подмышечном лимфатическом узле. Пациенту проводили химиотерапию посредством DTIC без видимого клинического ответа. Подмышечные метастазы удалили, и клетки дали начало клеточной линии Mel-XY3.
Mel-XX4: она была получена при хирургической операции по поводу паховой аденопатии у белой женщины в возрасте 33 лет, где эта аденопатия была диагностирована как метастаз меланомы. Первичная опухоль была неизвестна. Через пятнадцать месяцев пациент имел рецидив в паховом лимфатическом узле. Объемный меланотический узел был удален, нарезан на небольшие фрагменты, жировая и соединительная ткани были удалены, и фрагменты были суспендированы в модифицированной способом Игла среде Дульбекко (DMEM), механически разделены под давлением на нейлоновом сите, и клеточные агрегаты ферментативно обрабатывали в течение ночи при 37°C.
Клетки ресуспендировали в культуральной среде для меланомы, дополненной 10% эмбриональной телячьей сывороткой (FBS) (Natocor, Cordoba, Argentina), высевали в 25-см2 культуральные флаконы и инкубировали при 37°C при увлажнении и в атмосфере 5% CO2-95% в воздухе. Через 24 часа культуральную среду удаляли для устранения неприкрепившихся клеток.
Суспензию клеток пропускали четыре раза через колонки с антифибробластными микросферами (Miltenyi Biotec, Germany). Полученные клетки назвали Mel-XX4.
Поддержание четырех клеточных линий по изобретению (Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4) проводили посредством культивирования в смеси среда для меланомы DMEM:питательная смесь F12 (1:1), дополненной 2 мМ глутамином, 20 нМ селенитом натрия, 100 мкМ аскорбиновой кислотой, 0,3 мг/мл галактозы, 0,15 мг/мл пирувата натрия и 5 мкг/мл инсулина), 100 МЕ/мл пенициллина, 10 мкг/мл стрептомицина, помимо 10% эмбриональной телячьей сыворотки (FBS) (Natocor, Cordoba, Argentina) в лаборатории GMP Centro de Investigaciones Oncologicas-FUCA.
Клоны CTL (ограниченные по HLA A*0201), специфичные к антигенам Melan A/MART-1 (M27: AAGIGILTV) и gp100 (G154: KTWGQYWQV) размножали в среде RPMI с 10% сывороткой человека с инактивированными АВ и антибиотиками, в течение 14-суточных циклов с использованием 30 нг/мл антитела против CD3 (OKT-3, BD Biosciences), и серии 300 МЕ/мл IL-2 (Chiron BV, Amsterdam, Netherlands) каждые 3 суток.
Пример 2
Охарактеризация клеточной линии:
Кинетика роста in vitro:
104 клеток культивировали в лунках 24-луночных планшетов (Corning). Каждые 2-3 суток клетки обрабатывали ЭДТА (0,02%), собирали и посчитывали. Время удвоения популяции оценивали из наклона кривой роста в ходе экспоненциальной фазы.
Клоногенность
Независимый от прикрепления рост клеток определяли способом на мягком агаре (Hamburger, and Slamon, Science 197: 461, 1977). 3-10×103 клеток культивировали в верхнем слое. Планшеты инкубировали в течение 21 суток, а затем подпитывали каждые сутки 50 мкл культуральной среды. Колонии из более чем 36 клеток подсчитывали под микроскопом.
Охарактеризация антигенов меланомы посредством иммуноцитохимии (ICC) и FACS
Для оценки ICC экспоненциально растущие клетки обрабатывали ЭДТА, центрифугировали, фиксировали формальдегидом, погружали в парафин и нарезали на тонкие срезы. В качестве контроля использовали нормальные образцы тканей пациента.
Ткани и клетки анализировали с помощью моноклональных антител (Mabs) против кератинов, виментина и gp100/HMB 45 (Biogenex), MARTl/Melan-A (Dako), и с помощью поликлональных антител против S100 (Biogenex).
Реакции визуализировали с помощью комплексов авидин-биотин (Vectastain ABC). Эндогенные пероксиды блокировали с помощью 0,6% H2O2.
Реакции непрямой иммунофлуоресценции проводили ресуспендированием обработанных ЭДТА клеток. После блокирования нормальной сывороткой козы, разбавленной до 10%, клетки инкубировали с первичными антителами, промывали, инкубировали со вторичными антителами (антитело против иммуноглобулинов козы с FITC (Dako), промывали, фиксировали в 1% параформальдегиде, и анализировали посредством FACS (FACS Vantage SE, Becton-Dickinson, USA). Первичные антитела представляли собой Mab против p53 мыши (DO-7, BD Pharmingen), антитело против GD2 3F8, антитело против GD3 R24. В случае p53, в клетках повышали проницаемость. Антигены лейкоцитов человека (HLA) класса I и класса II типировали посредством PCR-SSP.
Определение ассоциированного с меланомой антигена посредством RT-PCR:
Тотальную РНК экстрагировали с помощью Trizol (Invitrogen). Для инициации синтеза кДНК, к 1-3 мкг РНК добавляли соответствующие праймеры и инкубировали с 200 Е фермента MMLV-RT (Promega), 25-40 E RNAsin (Promega) и 250-500 мкМ dNTP (Invitrogen) в течение 5 мин при 70°С, а затем в течение 60 мин при 42°С. Аликвоты кДНК (2-10 мкл) амплифицировали с помощью ДНК-полимеразы Taq (Invitrogen), с использованием специфических пар праймеров.
Специфические праймеры представлены ниже:
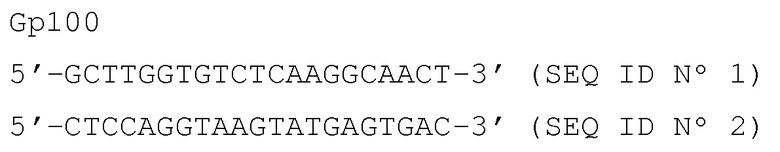
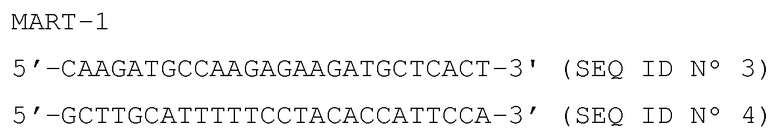
Тирозинкиназа


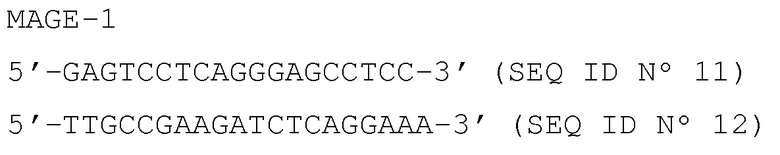
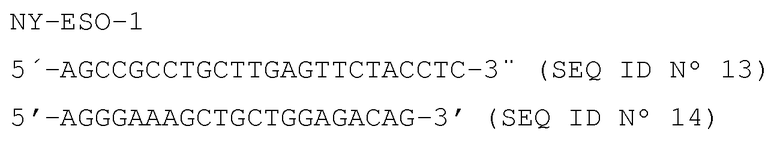
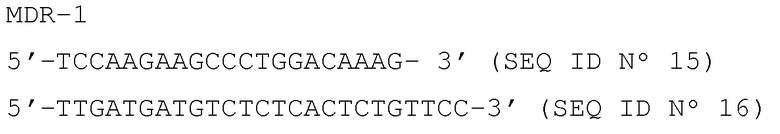
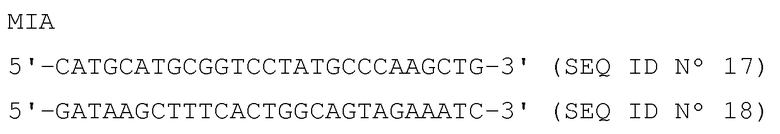
β-актин
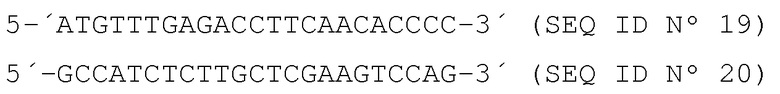
Антисмысловые праймеры представлены в нижней строке. Для детекции тирозина также амплифицировали аликвоту 1/100 от первой реакции PCR со внутренними праймерами (гнездовая PCR).
Продукты PCR анализировали в агарозных гелях и окрашивали бромидом этидия; размер фрагментов вычисляли посредством сравнения с размером, наблюдаемым для маркеров ДНК PM размером 100 п.о. (Promega).
Цитогенетический и цитомолекулярный анализ:
Клетки, соответствующие четырем линиям по изобретению, инкубировали для цитогенетического анализа при экспоненциальном росте в колхицине (0,1 мкг/мл) при 37°С в течение 8-16 ч, собирали с помощью раствора трипсин-ЭДТА и обрабатывали в соответствии со стандартными протоколами. Использовали способ G-полос. Идентификацию хромосом проводили согласно International System for Human Cytogenic Nomenclature (Mitelman, 1995 ISCN.: An International System for Human Cytogenetic Nomenclature, (ed. S Karger, Basel).
Пример 3
Получение дендритных клеток (DC) из моноцитов, их охарактеризация и нагрузка клетками Apo-Nec
Дендритные клетки получали из лейкоцитной пленки или продуктов лейкофереза от здоровых доноров. Периферические мононуклеарные клетки (PBMC) очищали с помощью градиента плотности Fycoll-Hypaque. PBMC суспендировали в свежей бессывороточной среде AIM-VTM (Invitrogen) и оставляли прикрепляться в культуральных флаконах (TPP, Germany). Через 2 ч при 37°C неприкрепившиеся клетки удаляли, и прикрепленные моноциты культивировали в течение 5 суток в AIM-V, дополненной 800 Е/мл rhuGM-CSF и 50 нг/мл IL-4 (Peprotech, Mexico), получая, таким образом, CDin. Изменения фенотипа анализировали под световым микроскопом и с помощью FACS. Для индукции контролируемого созревания DCin добавляли 2 мкг/мл LPS (липополисахариды J5 E. coli, Sigma, St. Louis, CA), и в конце клетки культивировали в течение 48 ч.
Охарактеризацию фенотипа DC-клеток проводили, когда клетки находились в незрелом состоянии (DCin), и после анализа фагоцитоза апоптотических/некротических клеток (клеток Apo-Nec) посредством окрашивания 5×105 клеток антителами, меченными флуорохромами, против антигенов CD14, CD11c, CD1a, HLA класса II, CD80, CD86, CD83, CD40, HLA класса I, и CCR7 (BD Biosciences, San Jose, CA) с помощью анализа FACS (Becton Dickinson, San Jose, CA). Соответствующие изотипические контроли представляли собой IgG2a крысы с PE, и IgG1 и IgG2a мыши (BD Biosciences, San Jose, CA). Также анализировали экспрессию CD83 в DC, фагоцитирующих клетки Apo/Nec с использованием немеченого моноклонального антитела против CD83 (IgG1), и соответствующего изотипического антитела в качестве контроля; для проявления использовали антитело против IgG1 мыши-PerCP (BD Biosciences, San Jose, CA).
Способность DC к эндоцитозу оценивали посредством инкубации 1 x 106 DC с 1 мг/мл декстрана, конъюгированного с FITC (Dx-FITC) (Sigma, St Louis, CA) в течение 30 мин при 37°С. После инкубации клетки промывали посредством PBS и анализировали с помощью FACS. Контроли включали DC, инкубированные с Dx-FITC в течение 30 мин при 4°С для ингибирования процесса эндоцитоза; с другой стороны, в анализе базовым считали включение в 0 момент времени. Включение DX-FITC (эндоцитоз) количественно определяли посредством FACS.
Оценка фагоцитоза DC-клеток:
Клетки DCin со-культивировали с клетками Apo-Nec (полученными, как показано выше) в свежей среде AIM-V в различные моменты времени. В некоторых способах анализа DC окрашивали красным цветом с помощью PKH26, и клетки Apo-Nec окрашивали зеленым цветом с помощью PKH67 (Sigma, St. Louis, CA). Анализ посредством FACS проводили после со-культивирования, и процентное количество DC, фагоцитирующих клетки Apo-Nec, определяли как процентное количество двойных положительных клеток. Для каждого цвета получали соответствующие контроли. Контроль неспецифического связывания клеток Apo-Nec с DC проводили посредством инкубации клеток при 4°С в течение тех же периодов времени.
Миграция DC in vitro:
Миграцию DC in vitro анализировали до и после со-культивирования с клетками Apo-Nec с использованием 48-луночной камеры для хемотаксиса (AP 48 Neuroprobe Inc., Gaithersburg, MD). 10 нг/мл MIP-1α или MIP-3β (Peprotech, Rocky Hill, NJ, USA), разбавленного в RPMI, помещали в нижний отдел. Базовую миграцию анализировали помещением в нижнюю камеру RPMI. DC высевали в верхнюю камеру (3×104 CD/лунка) в RPMI. Между верхней и нижней камерой помещали поликарбонатную мембрану с размером пор 5 мкм (Neuroprobe, Inc., Bethesda, MD). Через 90 мин при 37°С, клетки с верхней стороны мембраны удаляли, и мигрировавшие клетки, прикрепленные к нижней стороне мембраны, окрашивали 10% красителем Гимза, разбавленным в нейтральной воде. Мембраны сушили на воздухе, помещали на предметное стекло с помощью канадского бальзама, и с использованием микроскопа количественно определяли длины миграции. Анализировали пять полей на лунку с 40X увеличением, и анализировали по 3 лунки/условие. Статистический анализ проводили с помощью критерия Стьюдента.
Электронная микроскопия:
Процесс фагоцитоза также исследовали с помощью электронной микроскопии. Образцы со-культуры фиксировали с помощью 2,5% глутаральдегида в 0,1 M фосфатном буфере, и после фиксации проводили окрашивание 1% тетроксидом осмия, их промывали два раза дистиллированной водой, и подвергали контрастному окрашиванию 5% ацетатом уранила в течение 2 ч. После промывания и дегидратации, образцы погружали в смолу (Durkupan). Получали ультратонкие срезы (70-90 нм), помещали на медные сита и подвергали контрастному окрашиванию с помощью цитрата свинца Рейнольда. Сита анализировали с помощью трансмиссионного электронного микроскопа Zeiss 109. Альтернативно, для получения изображений полных ячеек получали тонкие срезы (0,5 мкм) на ультрамикротоме (Reichert-Jung), окрашивали 0,4% толуидином синим, 0,1M карбонатным буфером, помещали на Durkupan, и анализировали с помощью светового микроскопа (1000x). Изображения получали с помощью цифровой камеры Sony Cybershot Digital (5 Мегапикселей), и обрабатывали с помощью программы Adobe photoshop 6.0.
Анализ перекрестного представления in vitro, секреция IFN-γ:
Очищали 98% CD14+ моноцитов от доноров с HLA A*0201 с использованием микросфер против CD14 (Miltenyi Biotec, Germany), и дифференцировали в клетки DCin посредством культивирования в течение 5 суток, как описано выше. Клетки DCin инкубировали с клетками Apo-Nec в течение 6, 12, 24 и 48 ч, и повергали воздействию специфичных к MelanA/MART-1, или gp100 клонов CTL в 1 мл среды AIMV в течение ночи. Секрецию IFN-γ в супернатант определяли в трех параллельных анализах способом ELISA (OptEIA IFN-γ, Pharmingen BD Biosciences, San Diego, CA) в соответствии с инструкциями поставщика. Для каждого эксперимента получали калибровочную кривую, и концентрацию в образце вычисляли с использованием дважды логарифмического регрессионого анализа, и с использованием программного обеспечения Cembal 2.2. Контроли включали: DC плюс 20 мкг/мл пептидов MART-1 или gp100, жизнеспособные клеточные линии меланомы с HLA A*0201+, экспрессирующие антигены MART-1 и gp100 (положительные контроли) или клетки DC, культивированные с неспецифическими пептидами, и жизнеспособные клеточные линии меланомы с HLA A*0201+, не экспрессирующие соответствующие антигены (отрицательные контроли).
Определение внутрицитоплазматических цитокинов IL-10 и IL-I2:
DC, меченные PKH26 (красный) со-культивировали с клетками Apo-Nec, меченными PKH67, в различные моменты времени (6, 12, 24 и 48 ч). Измерение накопленных цитокинов проводили способом внутриклеточной иммунофлуоресценции после блокирования их продукции брефелдином A (8 ч) после культивирования (Golgi Plug, BD Biosciences, San Jose CA). Повышали проницаемость клеток с помощью 0,05% сапонина, и окрашивали с помощью антитела против IL10 (изотип IgG2a крысы)-APC, и антитела против субъединицы p40-p70 IL12 (изотип IgG1 мыши)-PerCp (BD Biosciences, San Jose, CA). Популяцию с двойной окраской PKH26/PKH67 отбирали для исследований посредством FACS, и цитокины оценивали в такой популяции в эксперименте с помощью четырех цветов. Со-культуру при 4°С использовали в качестве контроля.
Пример 4
Получение композиций по изобретению и схемы применения:
Композиция Apo-Nec:
Облучение клеточных линий:
Четыре клеточных линии по изобретению (Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4) облучали гамма-излучением при 70 Грэй (Siemens, Instituto Alexander Fleming, Buenos Aires, Argentina), а затем клетки замораживали (50% DMEM, 40% альбумин человека и 10% DMSO) в жидком азоте до применения.
В день применения клеток их размораживали, промывали и изготавливали в виде доз композиции с 5 - 10×106 клеток каждой выделенной клеточной линии по изобретению или их сочетания, ресуспендируя их в среде DMEM.
300 мкл инъецировали внутрикожно.
Композиция DC/Apo-Nec:
Получение апоптотических/некротических опухолевых клеток:
Облученные и замороженные клетки (Mel-XY1, Mel-XY2, Mel-XY3 и Mel-XX4), как описано выше, размораживали и высевали в среде для меланомы плюс 10% эмбриональная телячья сыворотка до завершения апоптотического процесса. После культивирования в течение 72 ч клетки открепляли со дна флаконов, промывали, подсчитывали и ресуспендировали в свежей бессывороточной среде AIMVTM (therapeutic grade, GIBCO, Invitrogen Corporation, Grand Island, N.Y). Апоптоз и некроз анализировали способом связывания аннексина-V FITC и включения иодида пропидия (IP) (набор для детекции апоптоза с помощью аннексина-V, BD Biosciences, San Jose, CA), и анализировали посредством FACS. Клоногенные анализы в мягком агаре проводили в шести экземплярах (1,5×104 клеток/лунка) для анализа способности к пролиферации в облученных клетках по сравнению с необлученными контрольными клетками.
5, 10, 15 и 20×106 DC, в соответствии с каждой дозой для пациентов, со-культивировали с клетками Apo-Nec в среде AIMV в течение 48 ч при 37°С. В день применения со-культивированные клетки центрифугировали со скоростью 1200 об/мин в течение 5 мин, ресуспендировали в среде DMEM (300 мкл) и инъецировали внутрикожно в одну из четырех конечностей с интактным дренажем лимфатических узлов.
Контроль качества и анализы стерильности проводили для всех препаратов композиции.
Пример 5
Схема исследования у пациентов и критерии селекции
Исследования у пациентов проводили для оценки токсичности, выживаемости и иммунного ответа на лечение. Исследования были одобрены Institutional Revision Council of Instituto Alexander Fleming и этической комиссией. Критериями выживаемости были (a) кожная меланома, подтвержденная гистологией, на стадиях IIB, IIC, III или IV (AJCC); (b) пациенты с минимальным или не поддающимся детекции заболеванием (ND) после хирургической операции, обследованные с помощью компьютерной аксиальной томографии, и показателями фермента лактатдегидрогеназы (LDH). В исследование могли быть включены пациенты с неизвестной первичной меланомой; (c) возраст между 15 и 60 лет; (d) ожидаемая продолжительность жизни >6 месяцев; (e) результат (ECOG) 0 или 1; (f) пациенты стадии III, которых ранее лечили IFN-α, у которых лечение было закончено или прекращено вследствие прогрессирования заболевания, токсичности или любой другой клинической причины, или пациенты, у которых не начинали лечение IFN-α за шесть месяцев до хирургической операции; (g) надлежащий венозный доступ для процедуры лейкофереза, (h) лабораторные критерии включения представляли собой: гемоглобин > 10 г%; количество лейкоцитов >4800/мм3, тромбоциты > 150000/мм3; общий и прямой билирубин, щавелевоуксусные трансаминазы, глутамин-пируватные трансаминазы <1,5 раз выше наибольшего значения нормы; LDH <450 мЕ/мл; i) отсутствие беременности, с β-HCG в сыворотке, определенным за одну неделю до каждого применения у женщин в доменопаузальном периоде; (i) креатинин < 1,4 мг%; (k) отсутствие химиотерапевтической, лучевой терапии или биологической терапии в течение предшествующего месяца; (k) отсутствие лечения кортикостероидами или нестероидными противовоспалительными средствами (AINE); (l) отсутствие активных метастазов в головном мозге; (m) нормальная ЭКГ; (n) все пациенты должны были подписать информированное согласие.
Оценка пациентов и схема лечения:
Базовую оценку пациента проводили за 35 суток до первого применения. Клиническая оценка включала полный клинический анамнез, физикальный осмотр, электрокардиограмму (ECG), компьютерную аксиальную томографию (грудь, живот, таз и головной мозг), определение стадии опухоли, размера опухоли и документирование областей заболевания, химический анализ крови и гематологический анализ. Отобранных пациентов подвергали лейкоферезу для получения PBMC, в целях получить DC.
Пациентам проводили 4 введения DC/Apo-Nec с интервалами в 2 недели. Инокуляцию проводили внутрикожно (300 мкл), и при каждой дозе проводили тест DTH, состоящий в инокуляции в верхнее плечо между 5 и 20×106 клеток DC/Apo-Nec без адъюванта. Показатели жизнедеятельности и кожные реакции DTH анализировали через 2, 24 и 48 ч после применения. Состояние пациента исследовали на 70 сутки посредством брюшной ультразвуковой эхографии и рентгена грудной полости и протокол завершали на 75 сутки клиническим обследованием.
Для применения клеток Apo/Nec по изобретению пациентам проводили внутрикожную инъекцию (id) в одну конечность с интактными лимфатическими узлами. Двадцати (20) пациентам вводили дозу rhGM-CSF 400 мкг (100 мкг в сутки, четверо суток). В день применения, 0,1 мл hGM-CSF смешивали с Apo-Nec (16×106 облученных клеток в 0,3 мл) и БЦЖ (1×106 колониеобразующих единиц) в 0,05 мл. В ходе следующих 3 суток, 0,1 мл rhGM-CSF инъецировали внутрикожно в область применения. Каждому пациенту проводили 4 введения, разделенных 3 неделями, а затем 1 введение композиции каждые два месяца в течение года, 1 введение композиции каждые три месяца на второй год, а затем продолжали 1 введением композиции каждые 6 месяцев.
Статистический анализ:
Все неблагоприятные результаты классифицировали согласно общим критериям токсичности National Cancer Institute (NCI).
Оцениваемую группу определили как все пациенты, которым проведено четыре введения. Поскольку большинство данных от пациентов не подчинялись нормальному распределению, общие данные анализировали с использованием критерия суммы рангов Вилкоксона. Значения DTH для различных групп, в которых вводили различные количества DCs/Apo-Nec, сравнивали между каждой группой с одной переменной с помощью ANOVA и критерия множественных сравнений Даннета. Значимым считали значение P<0,05.
Способы оценки иммунного ответа подвергнутых лечению пациентов:
Для оценки иммунного ответа пациента получали сыворотку за 7 суток до введения (предварительная сыворотка), и на 15 сутки после окончания введения (конечная сыворотка), и образцы хранили при -80°С. Клетки PBMC очищали с помощью градиента Ficoll-Hypaque и последующего центрифугирования после лейкофереза (до применения), или из 100 мл крови, полученной через 15 суток после последней дозы (после применения), PBMC замораживали в 50% DMEM, 40% альбумине человека и 10% DMSO до применения в иммунологических анализах. Типирование HLA-A*0201 проводили после инкубации образцов пациента с моноклональными антителами против HLA*A0201 мыши, конъюгированными с FITC (BD-Pharmingen, San Jose, CA).
Реакция DTH:
В каждый день введения проводили тестирование DTH на предплечье с помощью 2×106 клеток Apo-Nec, и реакцию оценивали через 2, 24 и 48 ч после применения. Были приняты следующие показатели интенсивности DTH: 0: эритема <0,5 см; 1: розеола 0,5-1,0 см; (2) розеола 1,0-2,0 см; 3: розеола >2,0 см, или папулезная эритема <1,5 см; 4: папулезная эритема >1,5 см. Конечный DTH соответствует сумме всех отдельных интенсивностей DTH/4.
Анализ пролиферации:
PBMC до и после применения композиции получали с помощью градиента плотности Ficoll-Hypaque, и хранили замороженными в жидком азоте до применения. Клетки размораживали для анализа и инкубировали в среде AIM-V (Gibco, Grand Island, NY) в течение 1 ч при 37°С. 5×105 клеток высевали в 96-луночные планшеты в присутствии или отсутствии фитогемагглютинина (PHA) (5 мкг/мл) (Gibco, Grand Island, NY) и инкубировали при 37°С в течение 72 ч. В течение последних 16 ч клетки обрабатывали (3H)dThd (Amersham, 1 мкКи/лунка), и после лизиса клеток с помощью жидкостного сцинтилляционного счетчика измеряли включенную в ДНК радиоактивность (Cell Harvester, Nunc, Rochester, NY).
Определение цитокинов:
Концентрации IL-10 и IL-12 в сыворотке пациентов определяли до применения (сыворотка перед применением) и через две недели после четвертого применения (сыворотка после применения). Сыворотку замораживали при -80°С до проведения анализа ELISA (OptEIA IL-10 и IL-12, BD Biosciences, San Diego, CA). Для каждого анализа получали калибровочную кривую, и концентрацию в образце вычисляли посредством дважды логарифмического регрессионного анализа с использованием программного обеспечения Cembal 2.2.
Измерение IFN-γ способом ELISpot:
Клетки CD14+ очищали в качестве стимуляторов из PBMC положительных по HLA-A2 пациентов с использованием микросфер, покрытых антителами против CD14 (Miltenyi Biotec, Paris, France), культивировали в течение 5 суток в синтетической среде SYN-H (AbCys, Paris, France) с 100 нг/мл GM-CSF, и 20 нг/мл IL-4, и подвергали созреванию с помощью 10 мкг/мл LPS в течение дополнительных 48 ч. Зрелые DC обрабатывали в течение 1 ч при 37°C 10 мкг/мл соответствующего пептида, разбавленного в среде SYH-H, промывали и смешивали с PBMC до достижения соотношения E/T пациентов, равного 10:1, с использованием всего 105 CD8+ лимфоцитов/лунка.
96-луночные планшеты покрывали нитроцеллюлозой (MAIPS 450; Millipore, Bedford, MA) в течение ночи при 4°C с 10 мкг/мл mAb человека против IFN-γ (Mabtech, Nacka, Sweden) в карбонат-бикарбонатном буфере, pH 9,6, промывали и блокировали средой IMDM+10% сывороткой человека с Ат (Biowest, Nuaille, France) в течение 1 ч при 37°C. Эффекторные клетки высевали в 100 мкл среды, и добавляли клетки-мишени до достижения соотношения E/T, составляющего 10:1, всего в количестве 200 мкл/лунка. После инкубации в течение 24 ч, лунки промывали 5 раз 0,1% Tween-20 в PBS. Планшеты инкубировали в течение 2 ч при комнатной температуре с 1 мкг/мл биотинилированных mAb мыши против IFN-γ человека (Mabtech) в PBS/HSA (0,4 г/л). После нескольких промываний 0,1% Tween-20 в PBS, добавляли 1:1000 щелочную фосфатазу-стрептавидин (Mabtech) в PBS/HSA, и инкубировали в течение 1 ч при комнатной температуре. Затем планшеты промывали, и добавляли синий субстрат, представляющий собой 5-бром-4-хлор-3-индолфосфат/нитротетразолий, на 30 минут при комнатной температуре (Mabtech). Проявление цвета останавливали промыванием планшетов водой. После высыхания CD8+ T-клетки, секретирующие IFN-γ, подсчитывали, визуализировали посредством цветного пятна на нитро-целлюлозной мембране, с использованием автоматической считывающий системы с визуализацией для ELISpot (AID, Strassberg, Germany).
Окрашивание тетрамерами HLA/пептидами:
Для идентификации колоний CD8+ T-лимфоцитов, специфичных к MART-1 (AAGIGILTV) или gp-100 (KTWGQYWQV), использовали тетрамеры HLA-A0201, конъюгированные с PE (фикоэритрином), или APC (аллофикоцианином), соответственно. Процесс окрашивания проводили при 37°С в течение 15 минут и клетки сразу помещали на лед. Затем образцы инкубировали с антителом против CD8 с FITC (BD Biosciences, San Jose CA) при 4°C в течение дополнительных 40 минут, и анализировали посредством FACS. Положительные контроли получали с помощью клонов CTL (ограниченных по HLA A*0201), специфичных к антигенам MART-1 (M27: AAGIGILTV) и gp100 (G154: KTWGQYWQV), размножаемых 14-суточными циклами в среде RPMI в присутствии антител против CD3 (OKT-3, BD Biosciences) в количестве 30 нг/мл, и серии IL-2 (Chiron BV) 300 МЕ/мл каждые 3 суток с 10% сывороткой человека с инактивированными AB и антибиотиками. Отрицательные контроли представляли собой образцы PBMC от здоровых доноров с HLA-A0201.
Определение гуморального ответа:
Жизнеспособные клетки, содержащие клетки Apo-Nec, смешивали в равных соотношениях, блокировали 10% сывороткой кролика в течение 30 мин, и инкубировали с сывороткой до и после применения, разбавленной 1/10 на 1 ч при 4°С. Затем их промывали и клетки инкубировали с антителом против иммуноглобулина человека (IgG+A+M), полученного у кроликов (DakoCytomation, Glostrup, DK) в течение 1 ч при 4°C. Клетки промывали, фиксировали в 1% параформальдегиде и анализировали посредством FACS. Альтернативно сначала повышали проницаемость клеток с помощью сапонина в количестве 0,05% (Sigma-Aldrich, Saint Louis, MO) в PBS на стадии блокирования, и добавляли 0,05% сапонин/PBS после стадии реакции. В качестве первого антительного контроля использовали нормальную сыворотку.
Из клеточных линий Apo-Nec по изобретению получали экстракты белка. Клеточные осадки замораживали при -80°C, размораживали и обрабатывали в течение 20 мин при 4°C лизирующим буфером (50 мМ Tris-CIH, pH 7,5, 1% NP4O, 150 мМ NaCl, 5 мМ ЭДТА и 1 мМ PMSF). Суспензию гомогенизировали с помощью Polytron (Brinkmann Instruments, USA), и центрифугировали в течение 40 мин при 10000 g. Супернатант хранили в качестве аликвот, замороженных при -20°C. Концентрацию белка измеряли способом Лоури. Аналогично получали экстракты клеточной линии карциномы молочной железы человека IIB-BR-G.
Белковые экстракты (50 мкг) анализировали в градиенте 3%-12% SDS-PAGE, и переносили на нитроцеллюлозную мембрану (размер пор 0,45 мкм, Sigma-Aldrich, Saint Louis, MO, USA). После блокирования 3% обезжиренным коровьим молоком (Moliko, Argentina), их инкубировали в течение ночи при 4°C с сывороткой пациента, разбавленной 1/10. После нескольких промываний мембраны инкубировали с антителами человека против IgG+A+M, полученными у козы, конъюгированными с пероксидазой хрена (HRP) (Zymed, San Francisco, CA), и проявленными с помощью 4-Cl-нафтола и H2O2.
Гистопатологический анализ метастазов меланомы:
Погруженные в парафин биоптаты использовали для анализа лимфоидных клеток и инфильтрации DC-клеток. От трех до пяти срезов окрашивали гематоксилином/эозином или подвергали иммунному окрашиванию антителами против CD4 (клон 1F6), против CD8 (клон C8E-144b), против CD20 (клон L26), против CD1a (клон 010) (DakoCytomation, Glostrup, DK) и против CD57 (клон NK1, Zymed, San Francisco, CA), и проявляли реагентом ABC, и диаминобензидином (DAB), или Novared в качестве субстрата (Vectastain, Vector, Burlingame, CA). В качестве контроля проводили реакции без первичных антител. Срезы анализировали с помощью микроскопа Olympus BX40.




Изобретение относится к области биотехнологии, конкретно к клеточным технологиям, и может быть использовано в медицине. Клеточные линии меланомы человека, такие как Mel-XY1, депонированная в DSMZ под №DSM ACC2830, Mel-XY2, депонированная в DSMZ под №DSM ACC2831, Mel-XY3, депонированная DSMZ под №DSM ACC2832, и Mel-ХХ4, депонированная DSMZ под № DSM ACC2829, облучают для получения популяций с апоптотическим и некротическим фенотипом. Полученные клеточные линии используют в различных сочетаниях для лечения злокачественных заболеваний, а именно для лечения меланомы человека. Также указанные популяции облученных клеток сокультивируют с аутологичными дендритными клетками для последующего совместного введения пациенту, страдающему меланомой. Изобретение позволяет индуцировать стойкий противораковый иммунный ответ у млекопитающего, страдающего меланомой. 8 н. и 13 з.п. ф-лы, 4 табл., 10 ил., 5 пр.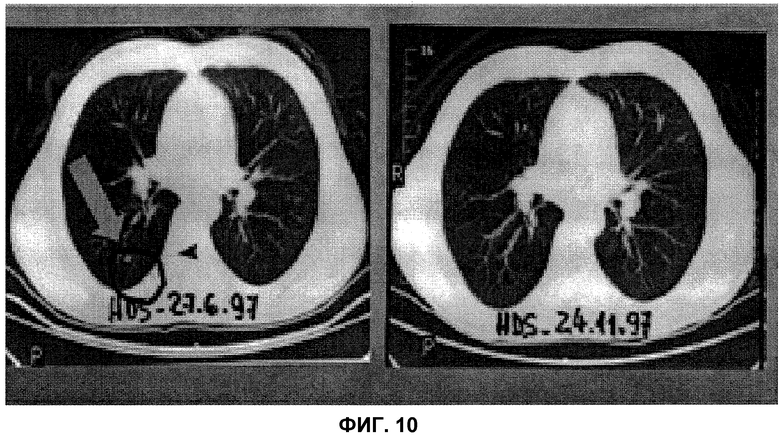
1. Сочетание клеточных линий меланомы человека для лечения злокачественных заболеваний, отличающееся тем, что такое сочетание включает клеточную линию (a) Mel-XY1 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2832) и (d) Mel-XX4 (депонированную в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии являются облученными и не способны пролиферировать.
2. Сочетание клеточных линий по п.1, отличающееся тем, что клеточные линии a), b), c) и d) содержат популяцию клеток с апоптотическим фенотипом.
3. Сочетание клеточных линий по п.2, отличающееся тем, что популяция апоптотических клеток содержит от 35% до 60% таких клеток.
4. Сочетание клеточных линий по п.1, отличающееся тем, что клеточные линии a), b), c) и d) содержат популяцию клеток с некротическим фенотипом.
5. Сочетание клеточных линий по п.4, отличающееся тем, что популяция некротических клеток содержит от 10% до 25% таких клеток.
6. Композиция для лечения меланомы, отличающаяся тем, что она содержит сочетание аллогенной клеточной линии меланомы (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM АСС2832), (d) Mel-ХХ4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829), где такие клеточные линии являются облученными и не способны пролиферировать.
7. Композиция для лечения меланомы, отличающаяся тем, что она содержит зрелые аутологичные дендритные клетки, аутологичные дендритные клетки, нагруженные сочетанием гетерологичных клеточных линий меланомы человека, апоптотические клетки такого сочетания гетерологичной клеточной линии меланомы человека и некротические клетки такого сочетания гетерологичной клеточной линии меланомы человека, где сочетание клеточных линий состоит из (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM АСС2832) и (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829).
8. Композиция по п.7, отличающаяся тем, что зрелые дендритные клетки имеют фенотип CD 14-, CD11c+, CD1a+ и CD83+.
9. Способ получения композиции по п.6, характеризующийся стадиями:
a) размораживания и культивирования клеточных линий (a) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Mel-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM АСС2832); (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829);
b) облучения этих клеточных линий;
c) добавления адъювантов и/или иммуномодуляторов для смешивания клеточных линий.
10. Способ по п.9, отличающийся тем, что клетки облучают при 50-100 Грэй.
11. Способ по п.9, отличающийся тем, что адъювант представляет собой БЦЖ.
12. Способ по п.9, отличающийся тем, что иммуномодулятор выбран из группы, включающей GM-CSF, G-CSF, IFNα, циклофосфамид и их смеси.
13. Способ получения композиции по п.7, характеризующийся стадиями:
a) размораживания и культивирования клеточных линий (а) Mel-XY1 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2830), (b) Ме1-XY2 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2831), (c) Mel-XY3 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM АСС2832); и (d) Mel-XX4 (депонированной в Коллекции Микроорганизмов и Клеточных Культур Германии DSMZ под регистрационным номером DSM ACC2829);
b) облучения этих клеточных линий;
c) получения аутологичных дендритных клеток; и
d) сокультивирования в течение некоторого времени аутологичных дендритных клеток с клеточными линиями, облученными на стадии b).
14. Способ по п.13, отличающийся тем, что клетки облучают при 50-100 Грэй.
15. Способ по п.13, отличающийся тем, что сокультивирование проводят при температуре от 35 до 39°C, и в течение периода времени от 6 до 72 ч.
16. Способ по п.13, отличающийся тем, что на стадии d) соотношение между аутологичными дендритными клетками и клеточными линиями составляет от 1:1 до 3:1.
17. Способ по п.13, отличающийся тем, что дендритные клетки стадии d) содержат незрелые дендритные клетки.
18. Способ по п.9 или 13, отличающийся тем, что он включает стадию смешивания клеточных линий.
19. Применение сочетания клеточных линий меланомы человека по п.1 для получения композиции для индуцирования противоопухолевого иммунного ответа у млекопитающего, имеющего меланому.
20. Применение сочетания клеточных линий меланомы человека по п.1 для получения композиции для лечения млекопитающего, имеющего меланому.
21. Применение сочетания клеточных линий меланомы человека по п.1 для получения композиции для адъювантного лечения млекопитающего, имеющего меланому.
| THUMANN P | |||
| et al., Antigen loading of dendritic cells with whole tumor cell preparations, J | |||
| Immunol | |||
| Methods, 2003, v.277, n.1-2, p.1-16 | |||
| LONGHI PAULA et al., Preclinical studies of a human vaccine based on dendritic cells loaded with apoptotic/necrotic melanoma cells, Proc | |||
| Amer | |||
| Assoc | |||
| Cancer Res., 2004, v.45, p.292 | |||
| GOLDSZMID R.S | |||
| et al., |
Авторы
Даты
2013-06-10—Публикация
2008-04-11—Подача