Изобретение относится к области медицины и может быть использовано в функциональной диагностике, кардиологии, гериатрии и для оценки возрастных изменений сердечно-сосудистой системы человека, проведения мониторинга биологического старения сердечно-сосудистой системы.
В настоящее время существует множество способов определения биологического возраста человека, использующих разнообразные показатели, закономерно изменяющиеся с возрастом: физиологические и патологические, функциональные и морфологические, клинико-лабораторные, биохимические, психологические, нервно-психические и ряд других. Для оценки биологического возраста человека предложено более 100 маркеров возрастных изменений.
Оценка старения организма человека в существующих способах проводится по величине отклонения индивидуального биологического возраста (БВ) человека от его календарного возраста (KB), при этом определяется повышенный риск раннего развития возрастной патологии, который влияет на качество и продолжительность жизни.
Определение БВ и индивидуальной скорости старения особо актуально для оценки и прогнозирования риска развития наиболее распространенных хронических заболеваний современного человека, сцепленных с онтогенетическим развитием и процессами старения человека: артериальная гипертония, ишемическая болезнь сердца, ожирение, сахарный диабет 2-го типа, атеросклероз и др.
Известен способ определения биологического возраста человека и скорости старения (RU №2387374, А61В 5/107, опубл. 27.01.2010), позволяющий прогнозировать риск развития наиболее распространенных хронических заболеваний современного человека, связанных с нарушением обмена веществ, а также определять влияния экологических факторов (природных и антропогенных) на скорость старения организма человека.
Известен способ определения скорости старения сердечно-сосудистой системы человека (RU №2193341, А61В 5/02, опубл. 27.11.2002), позволяющий определить биологический возраст сердечно-сосудистой системы и скорость старения сердечно-сосудистой системы.
Этот известный способ определения скорости старения сердечно-сосудистой системы человека основан на определении должного биологического возраста сердечно-сосудистой системы по формуле ДБВ ССС=(КВинд-КВсред)R2+КВсред, где ДБВ ССС - должный биологический возраст сердечно-сосудистой системы, КВинд - индивидуальный календарный возраст, КВсред - средний календарный возраст у обследуемых, R - множественный коэффициент корреляции, и биологического возраста сердечно-сосудистой системы, включающий измерение систолического артериального давления, затем проводят регрессионный анализ, рассчитывают биологический возраст сердечно-сосудистой системы по формулам для мужчин и женщин и находят разницу между биологическим возрастом сердечно-сосудистой системы и должным биологическим возрастом сердечно-сосудистой системы, при этом для определения биологического возраста сердечно-сосудистой системы дополнительно проводят исследование центральной гемодинамики, микроциркуляции, подсчитывают общий коньюнктивальный индекс, сердечный индекс и индекс экономичности работы сердца и рассчитывают биологический возраст сердечно-сосудистой системы по формулам для мужчин БВ ССС мужчин=0,19·АДС+2,98·КИ-7,23·СИ+26,45, для женщин БВ ССС женщин =0,38·АДС+3,07·КИ-4,77·СИ-1,24·ИЭРС, и при разнице биологического возраста сердечно-сосудистой системы и должного биологического возраста сердечно-сосудистой системы ниже 6,3 года определяли замедление скорости старения сердечно-сосудистой системы, от -6,3 до +5,5 лет - среднюю скорость старения сердечно-сосудистой системы, а выше +5,5 лет - увеличение скорости старения сердечно-сосудистой системы.
Данный способ принят в качестве прототипа для заявленного изобретения.
Недостатком известных способов является отсутствие системного и комплексного подхода при оценке возрастных изменений сердечно-сосудистой системы организма человека, невозможность проведения углубленного патогенетического анализа с возрастными изменениями в других органах и системах организма человека, определении темпов старения сердечнососудистой системы при различных метаболических нарушениях.
В связи с указанными недостатками существующие в настоящее время способы не позволяют разрабатывать алгоритмы терапии и оценивать эффективность проводимого медикаментозного и немедикаментозного лечения.
Настоящее изобретение направлено на достижение технического результата, заключающегося в повышении достоверности и объективности оценки возрастных изменений сердечно-сосудистой системы организма человека за счет учета показателя лодыжечно-плечевого индекса, как биомаркера в кровеносных сосудах и региональных сосудистых бассейнах, в совокупности с морфологическими (структурными) и функциональными (динамическими) показателями скорости старения сердечно-сосудистой системы.
Новым в заявленном способе является то, что применяется системный подход с изучением пятидесяти (50) показателей (маркеров) - коэффициентов скорости старения сердечно-сосудистой системы и биологического возраста, которые основаны на оценке возрастных изменений показателей в различных возрастных группах, т.е. в любом возрасте (табл.1).
Для решения этой задачи в заявленном способе для оценки возрастных изменений сердечнососудистой системы используется данные, полученные при одновременной неинвазивной регистрации показателей артериального давления (АД) (систолическое АД (САД), диастолическое АД (ДАД), пульсовое АД (ПАД) в 4-х местах (левое и правое плечо, левая и правая лодыжка), определение лодыжечно-плечевого индекса (ЛПИ), скорости распространения пульсовой волны (СПВ) в левой и правой половинах туловища, а также при проведении ЭхоКГ для ультразвукового исследования (УЗИ) сердца, при определении уровня изменения показателей САД, ДАД, ПАД, ЛПИ, СПВ, при определении биофизических и биохимических показателей.
На основании полученных данных (50 маркеров) проводят диагностику поражения органов-мишеней у больных с артериальной гипертензией (АГ), судят об атеросклеротических и других изменениях кровеносного сосуда, состоянии центральной и периферической гемодинамики, изменении геометрии сердца, работе всей сердечно-сосудистой системы в целом и при нарушении делают вывод о степени возрастных изменениях сердечно-сосудистой системы.
Указанные признаки являются существенными и взаимосвязаны с образованием устойчивой совокупности существенных признаков, достаточной для получения требуемого технического результата.
Кроме того, очень важным в заявленном способе является возможность разрабатывать алгоритмы терапии и оценивать эффективность проводимого медикаментозного и немедикаментозного лечения во времени с заданным интервалом и под контролем 50 биопоказателей (биомаркеров).
30,0-34,9
Артериальная гипертензия (АГ) - одна из основных причин сердечно-сосудистых осложнений (ССО) и смерти от них. В поддержании нормального уровня артериального давления (АД) принимают участие различные органы и системы - сердечно-сосудистая (ССС), центральная нервная (ЦНС) и эндокринная, почки. Особую роль в этом процессе играют почки, контролирующие не только объем и распределение циркулирующей в организме жидкости, но и активно влияющие на тонус сосудов. С одной стороны, заболевания почек существенно отражаются на уровне АД, способствуя развитию или усугублению АГ, с другой - почки крайне чувствительны к патологии ССС. АГ приводит к значительному ухудшению функции почек как органа-мишени, что в свою очередь дополнительно ухудшает контроль АД, замыкая тем самым порочный круг. Другой наиболее частой причиной развития осложнений со стороны почек является сахарный диабет (СД). Между СД, почками и сердечно-сосудистой патологией существуют тесные взаимосвязи. Наиболее частыми причинами прогрессирующего нарушения функции почек являются именно АГ и СД. Достаточная доказательная база подтверждает, что своевременное выявление поражения почек при АГ или СД и использование нефропротективных подходов в схеме лечения таких больных улучшают прогноз, снижают сердечно-сосудистую заболеваемость (ССЗ) и смертность.
Сердечно-сосудистую систему (ССС) следует рассматривать как ведущую в реализации физиологических (непосредственно связанных с механизмами старения) и патологических детерминант смерти индивидуума. Ее состояние в значительной мере лимитирует продолжительность жизни человека, поэтому определение возрастных изменений ССС является важной задачей современной геронтологии и клинической гериатрии. С помощью 50 биопоказателей (биомаркеров) имеется возможность оценить эффективность лечебно-профилактических мероприятий у больных с ССЗ, состояние здоровья населения при массовых обследованиях и профилактических осмотрах. Вышеуказанный алгоритм может определять и скорость старения ССС, что позволяет выявить лиц с ускоренным темпом ее старения и индивидуализировать лечебные мероприятия у этого контингента больных, использовать данный способ для прогнозирования их результатов.
Это повышает объективность способа и дает возможность с большей достоверностью характеризовать скорость старения ССС.
При определении возрастных изменений ССС организма человека осуществляют одновременное измерение системного АД на левом и правом плече, левой и правой лодыжке для определения значений ЛПИ в левой и правой половине туловища, СПВ в левой и правой половинах туловища, а также дополнительно проводят ЭКГ и ЭхоКГ сердца, определяют биофизические и биохимические показатели (маркеры), что позволяет верифицировать структурно-функциональные и метаболические изменения, как в локальных кровеносных сосудах, так и региональных сосудистых бассейнах, состояния центральной и периферической гемодинамики, изменения геометрии сердца, и работы всей ССС в целом, а также проводить контроль и мониторинг эффективности медикаментозной и немедикаментозной терапии у больных с АГ, МС, атеросклерозом и другими сосудистыми заболеваниями.
Авторы на основании 15 летних клинических наблюдений в Центре Артериальной Гипертонии г.Самара (ЦАГИС), а также клинических, физиологических, биохимических и биофизических клинико-экспериментальных исследований в Самарском государственном медицинском университете, Гериатрическом научно-практическом центре Самарской области, а затем и в Самарском областном гериатрическом центре утверждают, что повышение объективности и информативности способа оценки возрастных изменений сердечно-сосудистой системы человека достигается за счет системного подхода в оценке всех 50 биопоказателей (биомаркеров), оптимальные значения которых получены опытным путем, и которые изменяются с возрастом в зависимости от базовых генетических, физиологических и патофизиологических показателей, а также влияние на характер их изменений - образ жизни, качество употребления питьевой воды и питания в целом, наличие вредных привычек и воздействие окружающей среды, длительность воздействия хронического стресса и нарушение биоритмов сна (бодрствования), что оказывают влияние на скорость старения ССС.
Определение, оценка и характеристика 50 биопоказателей (биомаркеров) в способе оценки возрастных изменений сердечно-сосудистой системы человека следующая:
1) Календарный (паспортный) возраст (KB) - исчисляется от момента рождения и устанавливается на основании свидетельства о рождении, а после 14 лет согласно паспорта гражданина. Единица измерения - лет.
2) Биологический возраст (БВ) - характеризует темпы развития (старения), уровень жизнеспособности и общего здоровья организма, а также является интегральным показателем уровня индивидуального здоровья человека, характеризующим функциональные, резервные, регуляторные и адаптационные особенности организма. В норме соответствует КВ. Если БВ меньше KB, это говорит о большей продолжительности жизни. Если возрасты равны, то в организме человека протекает нормальный физиологический процесс, если же БВ больше KB, это может быть признаком преждевременного старения. В предлагаемом способе можно установить причину и системный характер (БВ<KB>БВ), как превышения БВ по сравнению с KB, так и его уменьшение (ревитализацию, омоложение). Единица измерения - лет.
3) Коэффициент полиморбидности - это наличие нескольких заболеваний у одного больного, который характеризует возрастные патологические изменения в различных физиологических системах, обусловленные разными причинами, обычно тесно связанными с изменениями возрастного характера. В норме при соответствии KB и БВ, коэффициент полиморбидности меньше 1. Во всех возрастных группах, когда БВ больше KB, то коэффициент полиморбидности всегда больше 1. Сроки начала заболеваний, формирующих синдромы полиморбидности, и их хронизация приходятся на молодой (30-45 лет) и средний (46-60 лет) возраст, а результат их суммарного накопления, период яркой клинической демонстрации начинают проявляться в пожилом (61-75 лет) возрасте, дальнейшие прожитые годы лишь добавляют количество болезней. У долгожителей 76-100 лет и старше коэффициент полиморбидности меньше 3,5, так как старые люди (76-90 лет) и долгожители (старше 91 года) более активны, меньше болеют хроническими заболеваниями, которые протекают у них менее агрессивно, с более мягкими осложнениями, реже обращаются за медицинской помощью. Предлагаемый способ оценки возрастных изменений сердечно-сосудистой системы человека позволяет определить развитие полиморбидности путем причинно-следственной трансформации, в следствии системного развития атеросклероза сосудов и диагностики следующих заболеваний: артериальная гипертония, ишемическая болезнь сердца, дисциркуляторная энцефалопатия, атеросклероз сосудов нижних конечностей, атеросклероз сосудов желудочно-кишечного тракта (преимущественно тонкого и толстого кишечника). У лиц старших возрастных групп (пожилом возрасте старше 60 лет) коэффициент полиморбидности больше 3,5 свидетельствует о преждевременном старении. Единица измерения - условных единиц (количество заболеваний).
4) Курение - является фактором риска (ФР) развития сердечно-сосудистых заболеваний (ССЗ), а также раннего и ускоренного развития атеросклероза сосудов. Стаж курильщика (лет) и количество выкуренных сигарет в сутки, свидетельствует о тяжести данного ФР в развитии ССЗ. Единица измерения - сигарета/лет.
5) Потребление алкоголя - является ФР развития ССЗ, а также раннего и ускоренного развития атеросклероза сосудов. Стаж злоупотребления алкоголем (лет) и количество (грамм) употребления алкоголя из расчета качественного этанола (этилового спирта, винного спирта, алкоголя) в сутки, для мужчин больше 30 грамм/сутки, и для женщин больше 25 грамм/сутки свидетельствует о тяжести данного ФР в развитии ССЗ. В норме для мужчин меньше 30 грамм/сутки, а для женщин меньше 25 грамм/сутки этанола. Единица измерения - грамм/сутки (г/сут) употребления этанола.
6) Потребление поваренной соли - является ФР развития ССЗ, а также раннего и ускоренного развития повышенной вариабельности кардиосинхронизированного механизма сосудов. Употребления поваренной соли более 5 грамм в сутки, для мужчин и для женщин, свидетельствует о тяжести данного ФР в развитии ССЗ, и прежде всего артериальной гипертонии. В норме для мужчин и для женщин употребление поваренной соли составляет менее 5 грамм/сутки. Единица измерения -грамм/сутки (г/сут).
7) Физическая активность (ФА) - показатель физической активности человека, и как следствие выраженность развития гиподинамии - ФР развития ССЗ и преждевременного старения сердечнососудистой системы организма человека. ФА, менее 30 минут в сутки и расстояние, которое человек преодолевает (ходьба, медленный и умеренный бег), менее 3 километров в сутки характеризуют развитие гиподинамии и фактора ускоренного старения сосудов человека. В норме ФА составляет более 30 минут и 3 километров. Единица измерения - время минут (мин) и расстояние - километров (км). Положительный эффект, связанный с увеличением ФА, очевиден и многообразен: снижение риска инфаркта миокарда и мозгового инсульта; снижение АД; увеличение фибринолитической активности крови; улучшение контроля СД; повышение толерантности к глюкозе; улучшение липидного профиля; уменьшение массы тела; повышение стрессоустойчивости; уменьшение тяжести депрессии; улучшение функции дыхания; уменьшение остеоартритических болей и риска остеопороза; улучшение качества жизни.
8) Индекс массы тела (ИМТ) - характеризует увеличение массы висцерального жира, снижение чувствительности периферических тканей к инсулину и гиперинсулинемию, которые вызывают нарушение углеводного, липидного, пуринового обменов, а также раннее развитие артериальной гипертонии (АГ). В норме ИМТ составляет от 18,5 до 24,9 кг/м2, показатель менее 18,5 свидетельствует о дефиците массы тела, от 25,0-29,9 предожирение, 30,0-34,9 ожирение I ст., 35,0-39,9 ожирение II ст., от 40,0 и более - ожирение III ст. Степень ожирение и дислипидемия характеризуют выраженность метаболического синдрома (МС), который в 3-6 раз повышает риск развития сахарного диабета (СД) типа 2 и АГ, ассоциируется с большей частотой распространения поражения органов мишеней (ПОМ), увеличивает риск сердечно-сосудистых осложнений (ССО) и структуру смертности от болезней системы кровообращения (БСК). Смертность населения в РФ от БСК за последние 5 лет составляет от 56 до 59% (в структуре от всех причин). Кроме того, ИМТ влияет на выбор тактики и стратегии лечения ССЗ, медикаментозной и немедикаментозной терапии, времени и продолжительности комбинированной терапии.
9) Серотонин - является предшественником мелатонина, образующегося в эпифизе (шишковидная или пинеальная железа, по строению и функции эпифиз относится к железам внутренней секреции). Один из основных нейромедиаторов по химическому строению относится к биогенным аминам. Серотонин играет важную роль в процессах свертывания крови. Тромбоциты крови содержат значительные количества серотонина и обладают способностью захватывать и накапливать серотонин из плазмы крови. Серотонин повышает функциональную активность тромбоцитов и их склонность к агрегации и образованию тромбов. Стимулируя специфические серотониновые рецепторы в печени, серотонин вызывает увеличение синтеза печенью факторов свертывания крови. Выделение серотонина из поврежденных тканей является одним из механизмов обеспечения свертывания крови по месту повреждения. Серотонинергическая система контролирует интенсивность мозгового кровообращения. Он повышает проницаемость сосудов, усиливает хемотаксис и миграцию лейкоцитов в очаг воспаления, увеличивает содержание эозинофилов в крови, усиливает дегрануляцию тучных клеток и высвобождение других медиаторов аллергии и воспаления. Эпифиз также является регулятором циркодианных ритмов, поскольку опосредованно связан со зрительной системой. Под влиянием солнечного света в дневное время в эпифизе вырабатывается серотонин, а в ночное время - мелатонин. Оба гормона сцеплены между собой, поскольку серотонин является предшественником мелатонина. Единица измерения, нормальные и патологические изменения серотонина показаны в табл.1. Кроме того, экспериментальные данные и клинические исследования свидетельствуют об участии серотонина в патогенезе острых нарушений мозгового кровообращения, в частности ишемических инсультов. Серотонин контролирует цикл сон-бодрствование, регулирует дельта-сон, инициирует фазу быстрого сна. Дисметаболизм серотонина усугубляет течение и тяжесть ССЗ и ССО, так как ведет к расстройству цикла сон - бодрствование, вызывает депрессию. Кроме того, патологические показатели серотонина в организме человека влияют на выбор тактики и стратегии лечения ССЗ, медикаментозной и немедикаментозной терапии, времени и продолжительности комбинированной терапии.
10) Мелатонин - нейрогормон. Эпифиз выделяет в кровоток «гормон молодости» серотонин, который является производным незаменимой аминокислоты триптофана. В темноте серотонин перерабатывается в способствующий сну нейрогормон мелатонин. Секреция мелатонина подчинена суточному ритму и зависит от освещенности - избыток света снижает его образование, а уменьшение освещенности увеличивает синтез и секрецию гормона. У человека на ночные часы приходится две трети суточной продукции мелатонина. С возрастом эпифиз инволюирует и выработка мелатонина снижается. Единица измерения, нормальные и патологические изменения мелатонина показаны в табл.1. У больных ИБС со стенокардией ночная продукция мелатонина значительно снижена. Причем, чем тяжелее форма ИБС, тем ниже уровень мелатонина. Особенно низок уровень мелатонина у больных с высоким риском возникновения инфаркта миокарда и летального исхода. Специфические рецепторы к мелатонину есть в гладкомышечных клетках и эндотелии кровеносных сосудов. Мелатонин ингибирует агрегацию тромбоцитов, обеспечивает кардиопротекторный эффект. В настоящее время бесспорным является нарушение временной организации гемодинамики, проявляющееся феноменом внутреннего и внешнего десинхроноза циркадианных и циркасептанных ритмов показателей гемодинамики, у больных АГ. При применении препаратов мелатонина больными АГ отмечается эффект снижения уровня диастолического артериального давления (ДАД) в среднем на 30 мм рт. ст. Подобный эффект, но выраженный гораздо меньше, наблюдается и у здоровых добровольцев. Очевидно, что фармакологическое действие мелатонина напрямую зависит от исходного тонуса сосудов. Т.о мелатонин - во-первых, благодаря синхронизирующим свойствам, способен ликвидировать рассогласование циркадианных ритмов. Во-вторых, у ряда больных АГ имеет место гиперреактивность гипофиз-адреналовой системы, функцию которой ограничивает мелатонин. Кроме того, мелатонин активирует дофаминэргические и ГАМК - эргические механизмы, ослабленные при АГ. В-третьих, в развитии АГ играет роль снижение продукции ПГЕ2 и других депрессоров. А мелатонин обладает свойством стимулировать синтез ПГЕ2, простациклина. И, наконец, мелатонин контролирует активность Са2+ каналов, нарушение деятельности которых считается одним из ключевых моментов патогенеза АГ. Содержание мелатонина в крови напрямую зависит от уровня заболеваемости - чем выше уровень мелатонина, тем ниже уровень заболеваемости с возрастом (рис.1.7) и имеет клиническое значение (рис.1.5) в хронобиологии и хрономедицине (Кузнецов С.И., Романчук П.И., Шишин Г.Г. Артериальная гипертония и артериальная гипотония: инновации комбинированной терапии. - Научно-методическое пособие. - Самара. 2011. - 288 с.; Романчук П.И., Никитин О.Л. Артериальная гипертония и активное долголетие: системокомплекс инноваций восстановительной медицины. - Научно-практическое пособие. - Самара. 2010. - 340 с.; Анисимов В.Н. Молекулярные и физиологические механизмы старения: В 2 т. - 2-е изд., перераб. и доп. - СПб.: Наука, 2008. - Т.1. - 448 с.; Анисимов В.Н. Молекулярные и физиологические механизмы старения: В 2 т. - 2-е изд., перераб. и доп. - СПб.: Наука, 2008. - Т.2. - 434 с.).
11) Кортизол - является наиболее биологически активным глюкокортикоидным гормоном. Кортизол секретируется наружным слоем (корой) надпочечников под воздействием адренокортикотропного гормона (АКТГ). Секреция АКТГ, в свою очередь, стимулируется соответствующим рилизинг-фактором гипоталамуса. Кортизол является регулятором углеводного обмена организма, а также принимает участие в развитии стрессовых реакций. Для кортизола характерен суточный ритм секреции: максимальная концентрация отмечается в утренние, а минимальная концентрация в вечерние часы. Чем выше уровень содержание кортизола, тем ниже уровень мелатонина, и наоборот. Выделившийся в кровь кортизол достигает клеток-мишеней (в частности, клеток печени). Благодаря своей липофильной природе легко проникает через клеточную мембрану в цитоплазму и ядро, где связывается со специфическими рецепторами. Гормон-рецепторный комплекс является фактором транскрипции, активирует транскрипцию определенных участков ДНК. В результате синтез глюкозы в гепатоцитах усиливается, тогда как в мышцах снижается распад глюкозы. В клетках печени глюкоза запасается в виде гликогена. Эффект кортизола состоит в сохранении энергетических ресурсов организма. По принципу негативной обратной регуляции повышение уровня кортизола в крови снижает секрецию кортиколиберина (а значит, и АКТГ). Единица измерения, нормальные и патологические изменения кортизола показаны в табл.1. Кортизол на 50% снижает содержание фермента теломеразы во время стресса, по сравнению с физиологическими условиями пребывания человека. Теломерная ДНК является важным хромосомным элементом, синтезируемым копированием последовательности РНК, т.е. обратной транскрипцией. Чем больше защита длины теломер, с помощью фермента теломеразы, тем выше способность к постоянному делению теломер, а значит к увеличению продолжительности жизнедеятельности организма человека. Т.о., теломераза - не лекарство от старости, а фермент, решающий «проблему концевой репликации ДНК». Установлена связь между длиной теломер и следующими заболеваниями (синдромами): АГ, СД, МС. Прекращение работы теломеразы, отмечаемое в подавляющем большинстве дифференцированных соматических клеток, является, по-видимому, одним из необходимых условий на пути достижения биологической целесообразности -смерти.
12) Сахарный диабет (СД): сахарный диабет первого и второго типа. Сахарный диабет 1-го типа (инсулинозависимый диабет, ювенильный диабет) - заболевание эндокринной системы, характеризующееся абсолютной недостаточностью инсулина, вызванной деструкцией бета-клеток поджелудочной железы. Диабет 1 типа может развиться в любом возрасте, однако наиболее часто заболевают лица молодого возраста (дети, подростки, взрослые люди моложе 30 лет). В клинической картине преобладают классические симптомы: жажда, полиурия, потеря веса, кетоацидотические состояния. В основе патогенетического механизма развития диабета 1 типа лежит недостаточность выработки инсулина эндокринными клетками (β-клетки островков Лангерганса поджелудочной железы), вызванное их разрушением под влиянием тех или иных патогенных факторов (вирусная инфекция, стресс, аутоиммунные заболевания и другие). Диабет 1 типа составляет 10-15% всех случаев диабета, чаще развивается в детском или подростковом периоде. Для этого типа диабета характерно появление основных симптомов, которые быстро прогрессируют с течением времени. Основным методом лечения являются инъекции инсулина, нормализующие обмен веществ пациента. В отсутствие лечения диабет 1 типа быстро прогрессирует и приводит к возникновению тяжелых осложнений, таких как кетоацидоз и диабетическая кома, заканчивающиеся смертью больного. Сахарный диабет 2-го типа (инсулиннезависимый диабет) - метаболическое заболевание, характеризующееся хронической гипергликемией, развивающейся в результате нарушения секреции инсулина или механизмов его взаимодействия с клетками тканей. Этот тип заболевания обусловлен снижением чувствительности тканей к действию инсулина (инсулинорезистентность), который на начальных стадиях заболевания синтезируется в нормальных или даже повышенных количествах. Диета и снижение массы тела пациента в некоторых случаях помогают нормализовать углеводный обмен и снизить синтез глюкозы в печени из неуглеводистого сырья. Со временем избыточная секреция инсулина истощает β-клетки поджелудочной железы, что делает необходимыми инъекции инсулина. Диабет 2 типа составляет 85-90% от всех типов сахарного диабета и наиболее часто развивается у людей старше 40 лет и, как правило, ассоциирован с ожирением. Заболевание прогрессирует медленно. Для него характерны второстепенные симптомы, кетоацидоз развивается редко. С течением времени развиваются осложнения: микро- и макроангиопатия, нефро- и нейропатия, ретинопатия и другие. Сахарный диабет 2-го типа является наследственным заболеванием. Подавляющее большинство лиц с этим типом заболевания имеет избыточную массу тела. Само по себе ожирение является одним из серьезных факторов риска развития сахарного диабета 2-го типа. Диагноз Сахарный диабет 2-го типа устанавливается если: концентрация глюкозы в капиллярной крови натощак >6,1 ммоль/л, через 2 часа после приема пищи (постпрандиальная гликемия)>11,1 ммоль/л; концентрация глюкозы в крови при проведении глюкозотолерантного теста превышает 11,1 ммоль/л. Сахарный диабет 2-го типа увеличивает темпы преждевременного старения сердечно-сосудистой системы организма человека, в результате диабетической микро- и макроангиопатии - нарушении проницаемости сосудов, повышении их ломкости, повышении склонности к тромбозам, к развитию атеросклероза сосудов. У 30-40% больных СД 1 типа и более чем у 70-80% пациентов с СД 2 типа наблюдается преждевременная инвалидизация и ранняя смерть от ССО. Установлено, что повышение диастолического АД на каждые 6 мм рт.ст. увеличивает риск развития ИБС на 25%, а риск развития ОНМК - на 40%. При СД 2 типа риск развития ИБС и ОНМК повышаются в 2-3 раза, почечной недостаточности - в 15-20 раз, слепоты - в 10-20 раз, гангрены - в 20 раз. При сочетании СД и АГ риск этих осложнений возрастает еще в 2-3 раза даже при условии удовлетворительной компенсации углеводного обмена. Т.о., коррекция АГ является задачей не менее важной, чем компенсация метаболических нарушений и должна проводиться одновременно с ней. По числу входящих в него основных факторов риска развития ИБС (абдоминальное ожирение, нарушенная толерантность к глюкозе или СД 2 типа, дислипидемия и AГ), МС называют смертельным квартетом. МС объединяет ряд метаболических и клинико-лабораторных изменений: абдоминальное ожирение; инсулинорезистентность; гиперинсулинемия; нарушенная толерантность к глюкозе/СД 2 типа; артериальная гипертония; дислипидемия; нарушение гемостаза; гиперурикемия; микроальбуминурия. Лечение АГ при наличии СД проводится одновременно с сахароснижающей терапией, постоянно и пожизненно. И первым пунктом в лечении АГ, как любого хронического заболевания, является отнюдь не лекарственная терапия. Установлено, что до 30% АГ являются натрий-зависимыми, поэтому из рациона таких пациентов полностью исключается поваренная соль, в т.ч. в продуктах питания, где очень много скрытых солей (майонезы, заправки к салатам, сыры, консервы), которые также должны быть ограничены. Следующим пунктом для решения этой проблемы является снижение массы тела при наличии ожирения. У больных с ожирением, имеющих СД 2 типа, АГ или гиперлипидемию, снижение массы тела примерно на 5% от исходного веса приводит к: улучшению компенсации СД; снижению АД на 10 мм рт.ст.; улучшению липидного профиля; снижению риска преждевременной смерти на 20%. Снижение веса является сложной задачей и для больного, и для врача, поскольку от последнего требуется много терпения, чтобы объяснить пациенту необходимость этих немедикаментозных мер, пересмотреть его привычный рацион питания, выбрав оптимальный, рассмотреть варианты регулярной (регулярность является обязательным условием) физической нагрузки (ФА). От пациента же требуется понимание и терпение для того, чтобы начать все это применять в жизни.
13) Гипергликемия натощак и нарушения толерантности к глюкозе (НТГ). Единицы измерения, нормальные и патологические изменения показаны в табл.1. В случаях, когда концентрация глюкозы в капиллярной крови натощак >6,1 ммоль/л, а через 2 часа после приема пищи (постпрандиальная гликемия) >11,1 ммоль/л; концентрация глюкозы в крови при проведении глюкозотолерантного теста (НТГ) превышает 11,1 ммоль/л, то устанавливается диагноз: Сахарный диабет 2-го типа. Актуальность и целесообразность контроля данных биохимических показателей (маркеров) связана с развитием МС и тяжестью течения АГ, а главное - выраженными сердечно-сосудистыми и церебро-васкулярными осложнениями. Нормализация данных показателей является надежным средством в профилактике преждевременного старения сердечно-сосудистой системы.
14) Объем талии при отсутствии метаболического синдрома (МС). Единицы измерения, нормальные и патологические изменения показаны в табл.1. Информативный показатель для определения ССР и способа оценки возрастных изменений сердечно-сосудистой системы человека. Кроме того, влияет на выбор тактики и стратегии лечения ССЗ, медикаментозной и немедикаментозной терапии, времени и продолжительности комбинированной терапии.
15) Объем талии при наличии МС. Единицы измерения, нормальные и патологические изменения показаны в табл.1. МС характеризуется увеличением массы висцерального жира, снижением чувствительности периферических тканей к инсулину и гиперинсулинемией, которые вызывают нарушение углеводного, липидного, пуринового обменов и развитие АГ. Наличие МС в 3-6 раз повышает риск развития СД типа 2 и АГ, ассоциируется с большей частотой распространения ПОМ, увеличивает риск ССО и смерти от них. Основой лечения пациента с МС являются немедикаментозные мероприятия, направленные на снижение массы тела, изменение стереотипов питания и повышение физической активности, т.е. формирование здорового ОЖ. При недостаточной эффективности немедикаментозных методов лечения или наличии показаний возможна медикаментозная или хирургическая коррекция веса тела. Обязательной является коррекция имеющихся нарушений углеводного, липидного и пуринового обменов. Выбор тактики ведения больных с МС индивидуален и зависит от степени ожирения, наличия или отсутствия АГ и других проявлений МС (Диагностика и лечение артериальной гипертензии. Российские рекомендации (третий пересмотр). - ВНОК. - М., 2008 // приложение 2 к журналу «Кардиоваскулярная терапия и профилактика», 2008; 7 (6); Национальные клинические рекомендации, Всероссийское научное общество кардиологов, Москва, 2009. - 392 с.; Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр), 2010).
16) Микроальбуминурия (МИ) - повышенная потеря альбумина из плазмы крови через эндотелий и потому определяется как четкий маркер развития системной эндотелиальной дисфункции и является важнейшим ранним признаком поражения почек, отражающим начальные стадии патологии сосудов (эндотелиальной дисфункции, атеросклероза), и неизменно коррелирует с увеличением ССЗ и смертности. Единицы измерения, нормальные и патологические изменения МИ показаны в табл.1. Как показывают клинические исследования, уже самые небольшие уровни повышения экскреции альбумина с мочой четко ассоциируются со значительным возрастанием риска кардиоваскулярных событий, в том числе фатальных, а прогрессирующее со временем увеличение уровня МИ однозначно указывает на ухудшение состояния сосудов и, соответственно, обусловливает дополнительное повышение риска. В связи с этим МИ признана независимым фактором ССР и наиболее ранним (доклиническим) признаком поражения таких уязвимых органов-мишеней, как почки. В 1999 г. ВОЗ определила МИ как один из компонентов МС, что отражало существенный вклад этого фактора риска в кардиоваскулярную заболеваемость и смертность у больных СД.
17) Скорость клубочковой фильтрации (СКФ) - оценка поражения почек (ПОМ при АГ), за счет уменьшение СКФ<60 мл/мин/1,73 м2 (MDRD формула) или снижение клиренса креатинина <60 мл/мин (формула Кокрофта-Гаулта). СКФ является показателем функции почечной ткани, этот параметр играет важную роль для терапевтических целей и при дозировке лекарственных препаратов, выводимых с мочой. Для достижения целевого уровня АД при поражении почек часто требуется комбинированная терапия, включающая диуретик (при нарушении азотовыделительной функции почек - петлевой диуретик) и/или антагонисты кальция. У больных с поражением почек, особенно при СД, с учетом повышенного риска развития ССО часто показана комплексная терапия - антигипертензивными препаратами, статины, антиагреганты и диетотерапия.
18) Отношение альбумин/креатинин - чем выше было соотношение альбумин/креатинин в группе контроля, тем выше ССР: с каждым десятикратным увеличением этого показателя относительный риск комбинированной первичной конечной точки возрастал на 57%, уровень сердечно-сосудистой смертности - на 97,7%, смертности от всех причин - на 75,2%, инсульта - на 51%, инфаркта миокарда - на 45%. Единицы измерения, нормальные и патологические изменения, соотношение альбумин/креатинин показаны в табл.1.
19) Сывороточный креатинин - у здоровых людей концентрация креатинина в плазме крови практически постоянна и не зависит ни от потребления воды, ни от физической нагрузки, ни от скорости выделения мочи. Повышенные значения креатинина в плазме всегда указывают на пониженное выделение, т.е. на нарушение функции почек. Клиренс креатинина позволяет оценить скорость гломерулярной фильтрации, что позволяет лучше распознавать почечные заболевания и наблюдать за работой почек. Ключевой детерминантой ухудшения функции почек является повышение систолического артериального давления (САД). При гипертоническом нефроангиосклерозе первичным звеном считается повреждение клубочковых эндотелиоцитов, что происходит следующим образом. При повышении САД, активации симпатоадреналовой (САС) и ренин-ангиотензин-альдостероновой системы (РААС) происходит констрикция приносящей артерии клубочка с уменьшением эффективного почечного кровотока (ЭПК) и образованием ангиотензина - АII (ведущий фактор), который вызывает спазм выносящей артерии клубочка и способствует развитию внутриклубочковой гипертензии с последующей гиперфильтрацией и повышенной проницаемостью для белка. В дальнейшем гиперфильтрация усугубляется, уменьшается приток крови в клубочковые капилляры, что сопровождается развитием гломерулярной ишемии, длительное существование которой приводит к апоптозу эндотелиоцитов и в конечном итоге определяет развитие нефроангиосклероза. Единицы измерения, нормальные и патологические изменения сывороточного креатинина показаны в табл.1.
20) Дислипидемия - это нарушение соотношения разных видов липидов (жироподобных веществ) в крови человека. Основные липиды, присутствующие в крови человека - это триглицериды и холестерин в разных соединениях (липопротеиды) высокой, низкой и очень низкой плотности. Между повышенным уровнем общего холестерина в крови и риском развития ИБС существует четкая положительная связь. Дислипидемия - это наследственное или приобретенное состояние, характеризующиеся нарушением образования, обмена и выведения из циркуляции липопротеидов и жиров, что приводит к повышению или снижению их содержания в крови. Соответственно выявить дислипидемию можно только после биохимического анализа крови - липидного спектра или липидограммы. Существенную роль в развитии атеросклеротического процесса играет соотношение компонентов общего холестерина (ОХС) и ЛПВП (липопротеинов высокой плотности), с этой целью используют индекс атерогенности (ИА). Вычисляют ИА по следующим формулам: ИА (усл. ед.)=(ОХС - ХС ЛПВП)/ХС ЛПВП. В норме ИА должен быть не более 4. Если он выше нормы, то это говорит о том, что скорость развития атеросклероза увеличена, как и риск развития осложнений. Также необходимо сказать, что ЛПВП являются «полезными» и замедляют прогрессирование атеросклероза, чем их больше, тем лучше. Снижение ЛПВП даже при нормальном уровне ОХС и его фракций ведет к прогрессированию атеросклероза. (Диагностика и лечение метаболического синдрома. Российские рекомендации (второй пересмотр).- ВНОК. - М., 2009 // приложение 2 к журналу «Кардиоваскулярная терапия и профилактика», 2009; 8 (6). Единицы измерения, нормальные и патологические изменения липидного спектра (липидограммы) показаны в табл.1. Профилактика дислипидемии: диета, психологические методы отказа от курения, от чрезмерного употребления алкоголя, увеличение ФА, использование биологически активных добавок, а в случае неэффективности немедикаментозной терапии - лекарственные препараты и методы гравитационной хирургии крови. Существует три способа снизить уровень ОХС в организме: 1) соблюдать строгую диету с ограничением животных жиров, вести правильный образ жизни (отказ от курения и алкоголя, физкультура, полноценный сон, отсутствие стрессов). Но даже при соблюдении всех требований можно не достичь результата особенно при наличии заболеваний, нарушающих обмен веществ, в том числе липидов, в организме - при коллагенозах (системной красной волчанке), гипотиреозе, заболеваниях почек, подагре, сахарном диабете, ожирении и др.; 2) Снижение уровня холестерина с помощью лекарственных средств - никотиновой кислоты, статинов, гепарина и др., возможно, но также имеет свои минусы. Статины снижают уровень холестерина в крови, но не влияют на холестерин, содержащийся в стенке сосуда. Действие препарата отсрочено - эффект становится заметным через 3-4 недели от начала приема. Прием статинов должен быть пожизненным, при прекращении приема лекарств холестерин тут же увеличивается снова. При длительном приеме возможно развитие побочных эффектов в виде диспептических расстройств, кожной сыпи, зуда, и более редких, но и более серьезных - симптомов миопатии, требующих отмены препарата из-за опасности развития рабдомиолиза (острого некроза скелетных мышц) и почечной недостаточности. Кроме того, статины могут взаимодействовать с другими лекарствами, которые требуются больному, меняя их и собственные свойства; 3) экстракорпоральное очищение крови от «плохого» холестерина с помощью гравитационной хирургии крови для коррекции дислипидемии применяют современные эффективные и безопасные методики - криоаферез и каскадную фильтрацию плазмы.
21) Сердечно-сосудистый риск (ССР). Стратификации риск ССО определяется врачом после завершения полного обследования пациента. В зависимости от степени повышения АД, наличия ФР, ПОМ и АКС («Фремингемская модель») все больные АГ могут быть отнесены к одной из четырех групп риска: низкого, среднего, высокого и очень высокого риска. По «Фремингемской модели» низкому риску соответствует вероятность развития ССО и смерти от них в течение ближайших 10 лет <15%, среднему риску - 15-20%, высокому - 20-30% и очень высокому риску >30%. При оценке величины риска по Европейской модели SCORE учитываются пол, возраст, статус курения, величина АД и ОХС. Для РФ по системе SCORE низкому риску соответствует вероятность смерти в течение ближайших 10 лет <5%, среднему риску - 5-9%, высокому - 10-14% и очень высокому риску >15%. Особого внимания требуют пациенты с высоким и очень высоким риском развития ССО как по «Фремингемской модели», так по системе SCORE. Систему стратификации риска SCORE у больных, имеющих высоко вероятные ПОМ и АКС, целесообразно использовать как предварительную с последующим уточнением величины риска по методу стратификации, основанному на «Фремингемской модели» после проведения дополнительного обследования. Оценка ССР и системная оценка возрастных изменений сердечно-сосудистой системы организма человека имеет большое значение при выборе тактики лечения больных (стартовая терапия АГ, определение целевого уровня АД и конечных целей лечения, необходимость назначения комбинированной терапии, потребность в статинах и других негипотензивных препаратах), которая зависит от начального общего ССР (Национальные клинические рекомендации, Всероссийское научное общество кардиологов, Москва, 2009. - 392 с.; Кузнецов С.И., Романчук П.И., Шишин Г.Г. Артериальная гипертония и артериальная гипотония: инновации комбинированной терапии. - Научно-методическое пособие. - Самара. 2011. - 288 с.).
22) Ассоциированные клинические состояния (АКС) - это состояния, обусловленные наличием следующих патологических состояний: церебро-васкулярные болезни (ЦВБ) - ишемический и геморрагический мозговой инсульт, транзиторная ишемическая атака (ТИА); заболевания сердца - инфаркт миокарда (ИМ), стенокардия, коронарная реваскуляризация, хроническая сердечная недостаточность (ХСН), заболевания почек - диабетическая нефропатия, почечная недостаточность: сывороточный креатинин >133 мкмоль/л (1,5 мг/дл) для мужчин и >124 мкмоль/л (1,4 мг/дл) для женщин; заболевания периферических артерий - расслаивающая аневризма аорты, симптомное поражение периферических артерий; гипертоническая ретинопатия - кровоизлияния или экссудаты, отек соска зрительного нерва. Величина АД является важнейшим, но далеко не единственным фактором, определяющим тяжесть АГ, ее прогноз и тактику лечения. Большое значение имеет оценка общего ССР, степень которого зависит от величины АД, а также наличия или отсутствия ФР, ПОМ, АКС. Кроме того, АКС существенно влияет на формулирование диагноза АГ и проведение комбинированной терапии, оценку и прогноз, возрастание или, наоборот, снижение (ревитализации, обратного развития, омоложения) степени возрастных изменений сердечно-сосудистой системы, а главное возможность оценки стабилизации патологического процесса (ремиссии заболевания) и его влияние на коэффициент полиморбидности.
23) Поражение органов мишеней (ПОМ) - системная оценка изменения органов и систем организма у больных с ССЗ, которая характеризует: 1) возрастное (патологическое изменение) органов при хроническом повышении АД, влиянии ФР, МС и АКС; 2) наличие недостаточно проведенной ранней диагностики и неэффективного лечения ССЗ; 3) преждевременное старение организма человека, и прежде всего сердечно-сосудистой системы. К ПОМ относятся: патологическое изменение сосудов мозга, мозгового кровотока, возникновение церебрального атеросклероза и дисциркуляторной энцефалопатии; патологические изменение сосудов глаз (глазного дна), поражение сердца - гипертрофия левого желудочка (ГЛЖ) это изменение на ЭКГ: признак Соколова-Лайона >38 мм, Корнельское произведение >2440 мм χ мс, изменение на ЭхоКГ: ИММЛЖ ≥125 г/м2 для мужчин и ≥110 г/м2 для женщин; поражение сосудов - ультразвуковые (УЗ) признаки утолщения стенки артерии (ТИМ>0,9 мм) или атеросклеротические бляшки магистральных сосудов, скорость пульсовой волны от сонной к бедренной артерии >12 м/с, лодыжечно/плечевой индекс <0,9; поражение почек - небольшое повышение сывороточного креатинина: 115-133 мкмоль/л (1,3-1,5 мг/дл) для мужчин или 107-124 мкмоль/л (1,2-1,4 мг/дл) для женщин, низкая СКФ<60 мл/мин/ 1,73 м2 (MDRD формула) или низкий клиренс креатинина <60 мл/мин (формула Кокрофта-Гаулта), МАУ 30-300 мг/сут; отношение альбумин/креатинин в моче ≥22 мг/г (2,5 мг/ммоль) для мужчин и ≥31 мг/г (3,5 мг/ммоль) для женщин.
24) Суточное мониторирование АД (СМАД) - это автоматизированное измерение (мониторирование) АД по установленной программе периодов и интервалов измерения (например: 1-й период с 8 ч до 22 ч, интервал между измерениями 30 мин; 2-й период с 22 до 8 ч, интервал между измерениями 60 мин). С практической точки зрения наибольший интерес представляет оценка различий между дневным и ночным АД - степень ночного снижения (СНС) или суточный индекс (СИ, %). Суточный индекс рассчитывается отдельно для систолического и диастолического АД по формуле: СИ=100% × (АД д - АД н)/АД д) где АДд - среднее АД в период бодрствования, АДн - среднее АД в период сна. Существенную роль играет одновременная системная оценка СНС и СИ, так СНС нормальный (Dippers) и СИ 10-22%, СНС недостаточный (Non-dippers) и СИ<10%, СНС избыточный (Over-dippers) и СИ>22%, СНС устойчиво повышенный (Night-peakers) и СИ<0. Повышенная вариабельность АД обычно ассоциируется с ПОМ. Нарушения циркадного ритма АД чаще встречаются у больных с нарушениями толерантности к углеводам, сахарным диабетом I и II типов, у нормотоников с неблагоприятной наследственностью по АГ, у лиц с симптоматической АГ (феохромоцитома, почечные гипертензии и т.д.). Нарушения циркадного ритма с недостаточным снижением АД в ночное время ассоциируются с большей частотой перенесенных инсультов, более частым развитием ГЛЖ, более частой и выраженной МИА. У женщин с недостаточным снижением АД в ночное время чаще развивается ИБС и выше смертность от инфаркта миокарда. Все вышеперечисленные параметры СМАД используются как в диагностике АГ, в оценке антигипертензивной терапии, в стратегии ранней диагностики ФР, ПОМ и ССР у больных с ССЗ, так и в выработке алгоритма лечения (комбинированного лечения с использованием принципов хронобиологии и хрономедицины) и преждевременного старения.
25) Систолическое артериальное давление (САД) на левом плече. Показатели САД в норме от 100 до 140 мм рт.ст., ниже указанных границ - гипотония, а выше - гипертония. Классификация АГ по уровню САД (мм рт.ст) следующая: оптимальное - <120, нормальное 120-129, высокое нормальное 130-139, АГ 1-й степени - 140-159, АГ 2-й степени 160-179, АГ 3-й степени - ≥180, Изолированная систолическая гипертония (степени 1-3 в зависимости от уровней САД) - ≥140.
26) Диастолическое артериальное давление (ДАД) на левом плече. Показатели ДАД в норме от 60 до 90 мм рт.ст., ниже указанных границ - гипотония, а выше - гипертония. Классификация АГ по уровню ДАД (мм рт.ст) следующая: оптимальное - <80, нормальное 80-84, высокое нормальное 85-89, АГ 1-й степени - 90-99, АГ 2-й степени 100-109, АГ 3-й степени - ≥110, Изолированная систолическая гипертония при показателях ДАД<90.
27) Пульсовое артериальное давление (ПАД) на левом плече. Показатели ПАД в норме от 30 до 60 мм рт.ст., патологические показатели ПАД<30 и >60. ПАД позволяет на доклинической стадии выявить пациентов с гемодинамически значимой патологией артерий нижних конечностей, повышенным риском наличия атеросклеротических поражений в каротидном и коронарном артериальных бассейнах, а также позволяет определить ФР развития ССО.
САД на правом плече характеризует системный уровень вариабельности систолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии. Патологическое САД является ФР развития ССЗ и ССО.
28) ДАД на правом плече характеризует системный уровень вариабельности диастолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии. Патологическое САД является ФР развития ССЗ и ССО.
29) ПАД на правом плече характеризует вариабельность кардиосинхронизированного механизма сосудистой регуляции, жесткости артерий, является показателем (маркером) гемодинамически значимой патологии артерий нижних конечностей, повышенным риском наличия атеросклеротических поражений в каротидном и коронарном артериальных бассейнах, а также позволяет определить ФР развития ССО.
30) САД на левой лодыжке характеризует системный уровень вариабельности систолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии артерий нижних конечностей. Патологическое САД является ФР развития ССЗ и ССО.
31) ДАД на левой лодыжке характеризует системный уровень вариабельности систолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии артерий нижних конечностей. Патологическое ДАД является ФР развития ССЗ и ССО.
32) ПАД на левой лодыжке характеризует вариабельность кардиосинхронизированного механизма сосудистой регуляции, жесткости артерий, является показателем (маркером) гемодинамически значимой патологии артерий нижних конечностей, повышенным риском наличия атеросклеротических поражений в каротидном и коронарном артериальных бассейнах, а также позволяет определить ФР развития ССО.
33) САД на правой лодыжке характеризует системный уровень вариабельности систолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии артерий нижних конечностей. Патологическое САД является ФР развития ССЗ и ССО.
34) ДАД на правой лодыжке характеризует системный уровень вариабельности систолического АД в региональном сосудистом бассейне. Используется для диагностики АГ, ЛПИ, СПВ и для сравнительной оценки гемодинамической значимой сосудистой патологии артерий нижних конечностей. Патологическое ДАД является ФР развития ССЗ и ССО.
35) ПАД на правой лодыжке характеризует вариабельность кардиосинхронизированного механизма сосудистой регуляции, жесткости артерий, является показателем (маркером) гемодинамически значимой патологии артерий нижних конечностей, повышенным риском наличия атеросклеротических поражений в каротидном и коронарном артериальных бассейнах, а также позволяет определить ФР развития ССО.
36) Лодыжечно-плечевой индекс (ЛПИ) левая половина туловища отражает степень стеноза или окклюзии артерий нижних конечностей при атеросклеротической облитерации. При ЛПИ<0,90 делается заключение о наличии заболеваний периферических артерий (ЗПА), при ЛПИ 0,9-0,99 констатируется его пограничное снижение, ЛПИ 1-1,09 соответствует нижнему нормальному значению, ЛПИ 1,10-1,29 - нормальному, и ЛПИ >1,30 - повышенному значению. ЛПИ - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со суточным профилем АД по данным СМАД (СНС и СИ), СПВ, а также САД, ДАД, ПАД в регионарных сосудистых бассейнах. Частота случаев выявления ИБС, нарушений мозгового кровообращения и доклинического атеросклероза существенна у больных со сниженным ЛПИ, особенно при величинах ЛПИ менее 0,9, указывающих на наличие ЗПА. Кроме того, при сниженных значениях ЛПИ диагностируется повышение толщины комплекса интима-медиа сонных артерий, а повышение частоты выявления коронарного кальция как при сниженных (менее 0,9), так и при повышенных (более 1,3) значениях ЛПИ (Волобуев А.Н., Петров Е.С., В.А.Кондурцев, П.И.Романчук. О некоторых подходах к лечению первичной артериальной гипертонии // ВРАЧ, - М., 2011. - С.20-22.; Национальные рекомендации по ведению пациентов с сосудистой артериальной патологией (Российский согласительный документ). Часть 1. Периферические артерии. - М.: Изд-во НЦССХ им. А.Н.Бакулева РАМН, 2010. - 176 с.; Рогоза А.Н., Балахонова Т.В. и др., Современные методы оценки состояния сосудов у больных артериальной гипертонией, - М.: Издательский дом «Атмосфера», 2008. - 72 с.; Диагностика и лечение больных с заболеваниями периферических артерий. Рекомендации Российского общества ангиологов и сосудистых хирургов. Москва, 2007 г., 127 с.).
37) ЛПИ правая половина туловища - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи с суточным профилем АД по данным СМАД (СНС и СИ), СПВ, а также САД, ДАД, ПАД в регионарных сосудистых бассейнах. Нормальные показатели ЛПИ в границах <0,8 и >1,4. Если ЛПИ>0,9, то повреждения магистральной артерии нет, но сохраняется риск тромботических осложнений. Если ЛПИ<0,9, то необходимо выполнить или ультразвуковое исследование артериальное, или компьютерную томографическую ангиографию. ЛПИ выше 1,4 тоже говорит о поражении артерий. Это значит, что стенка сосуда потеряла эластичность и наполнена кальцием, при этом диагностируется патологическое сужение сосудов. ЛПИ меньше 0,8 говорит о начале развития заболевания периферических сосудов нижних конечностей. ЛПИ ниже 0,5 свидетельствует о выраженном сужении периферических сосудов. ЛПИ ниже 0,3 означает критическую ишемию в конечностях, которая может привести к ампутации.
38) Скорость пульсовой волны (СПВ) от сонной артерии к левой бедренной в норме составляет <12 м/с. СПВ>12 м/с характеризует жесткость стенок артерий. Для более жестких стенок артерий характерна большая СПВ. Как показатель наиболее простого раннего обнаружения атеросклеротических заболеваний СПВ позволяет мониторировать степень развития атеросклероза у пациентов с АГ, дислипемией, СД, ИМ и МИ. СПВ имеет широкое применение для оценки эффективности лечения при наблюдении за пациентом во времени. СПВ - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД ДАД, ПАД в регионарных сосудистых бассейнах.
39) СПВ от сонной артерии к правой бедренной в норме составляет <12 м/с. СПВ>12 м/с характеризует жесткость стенок артерий. СПВ - диагностический показатель, который позволяет мониторировать степень развития атеросклероза у пациентов с АГ, дислипемией, СД, ИМ и МИ. СПВ имеет широкое применение для оценки эффективности лечения при наблюдении за пациентом во времени. СПВ - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД, ДАД, ПАД в регионарных сосудистых бассейнах.
40) СПВ между левым предплечьем и левой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД. ДАД, ПАД в регионарных сосудистых бассейнах. В возрасте до 29 лет нормальные показатели в границах 11,3±0,9. Патологическое значение >12,2.
41) СПВ между правым предплечьем и правой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД. ДАД, ПАД в регионарных сосудистых бассейнах. В возрасте до 29 лет нормальные показатели в границах <13,5. Патологическое значение >13,5.
42) СПВ между левым предплечьем и левой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД. ДАД, ПАД в регионарных сосудистых бассейнах. В возрасте от 30 до 49 лет нормальные показатели в границах 11,5±0,9. Патологическое значение >12,4.
43) СПВ между правым предплечьем и правой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД. ДАД. ПАД в регионарных сосудистых бассейнах. В возрасте от 30 до 49 лет нормальные показатели в границах ≥13,5 и ≤14,5. Патологическое значение >14,5.
44) СПВ между левым предплечьем и левой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД. ДАД, ПАД в регионарных сосудистых бассейнах. В возрасте от 50 лет и старше нормальные показатели в границах 12,5±1,4. Патологическое значение >14,0.
45) СПВ между правым предплечьем и правой лодыжкой - биопоказатель (биомаркер) для системной оценки возрастных изменений сердечно-сосудистой системы человека во взаимосвязи со ЛПИ, суточным профилем АД по данным СМАД (СНС и СИ), а также САД, ДАД, ПАД в регионарных сосудистых бассейнах. В возрасте от 50 лет и старше нормальные показатели в границах ≥14,5 и ≤15,0. Патологическое значение >15,0.
46) Ультразвуковые признаки (УЗ) признаки утолщения стенки артерии - (ТИМ). В норме ТИМ<0,9 мм. Патологическое значение ТИМ>0,9 мм является ФР ССЗ и ССО, а также диагностическим признаком наличия атеросклеротической бляшки магистральных сосудов.
47) Гипертрофия левого желудочка (ГЛЖ) по данным электрокардиограммы (ЭКГ) (признак Соколова-Лайона) в норме составляет <38 мм. Патологическое значение признака Соколова-Лайона >38 мм по данным ЭКГ является ФР ССЗ и ССО, а также диагностическим признаком ПОМ (гипертрофия левого желудочка сердца).
48) Фракция выброса (ФВ) при ультразвуковом исследовании (УЗИ) сердца Эхокардиография (ЭхоКГ) в норме составляет более 55,0%. Основным показателем, характеризующим систолическую функцию сердца, является величина сердечного выброса (или минутный объем крови - МО) - это количество крови, выбрасываемой желудочком в минуту. В норме эта величина варьирует в широких пределах: при необходимости сердечный выброс может увеличиваться в 3-5 раз по сравнению с покоем. Сердечный выброс рассчитывается следующим образом:
МО(л/мин)=УО(л) ЧСС (уд/мин),
где МО - минутный объем крови (сердечный выброс), УО - ударный объем, ЧСС - частота сердечных сокращений.
УО является производными МО и ЧСС. УО - количество крови, выбрасываемой желудочком в магистральный сосуд при каждом сокращении: 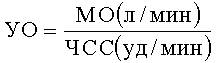
ФВ - отношение УО к КДО (в %): 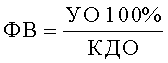
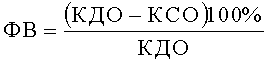
ФВ - существенный интегральный показатель систолической функции сердца, указывающий какая часть КДО выбрасывается из желудочков во время их систолы. ФВ менее 50,0% свидетельствует о снижении систолической функции сердца и развитии хронической сердечной недостаточности (ХСН).
49) Индекс массы миокарда левого желудочка (ИММЛЖ) при УЗИ сердца (ЭхоКГ) в норме составляет: для мужчин ИММЛЖ <125 г/м2, для женщин ИММЛЖ <110 г/м2. Патологическое значение ИММЛЖ ≥125 г/м2 для мужчин и ИММЛЖ ≥110 г/м2 для женщин по данным ЭхоКГ является ФР ССЗ и ССО, а также диагностическим признаком ПОМ (гипертрофия левого желудочка сердца).
На основе полученных одновременно данных проводят оценку (САД/ДАД/ПАД/ЛПИ/СПВ/ТИМ/ИММЛЖ), их взаимосвязи, а также биофизических и биохимических показателей (маркеров) для ранней диагностики поражения органов-мишеней у больных с АГ, оценивают атеросклеротические и другие изменения кровеносного сосуда, состояние центральной и периферической гемодинамики, изменение геометрии сердца, работы всей сердечнососудистой системы в целом.
При клиническом применении разработанной на основе способа компьютерной программы с углубленной оценкой возрастных изменений сердечно-сосудистой системы, способ позволяет верифицировать структурно-функциональные и метаболические изменения как в локальных кровеносных сосудах, так и региональных сосудистых бассейнах, состояние центральной и периферической гемодинамики, изменение геометрии сердца и работу всей сердечно-сосудистой системы в целом, а также проводить контроль и мониторинг эффективности медикаментозной и немедикаментозной терапии у больных с артериальной гипертонией, метаболическим синдромом, атеросклерозом и другими сосудистыми заболеваниями.
Приведенные в табл.1 исследования необходимы и достаточны для решения поставленной технической задачи:
Рост пульсового давления к периферии кровообращения у здоровых людей есть следствие активной работы гладких мышц сосудов под управлением кардиоваскулярного рефлекса, обеспечивающего регуляторную функцию артерий. При нарушении системы регуляции артерий, прежде всего модулирующей части кардиоваскулярного рефлекса, возникает определенный индивидуальный баростатус пациента, страдающего первичной артериальной гипертонией.
Физические факторы: отражение пульсовой волны от бифуркаций сосудов и тенденция к образованию ударной волны играют незначительную роль в повышении пульсового давления в направлении микроциркуляторного сосудистого русла.
Снижение лодыжечно-плечевого индекса α относительно нормы является важным маркером нарушения рефлекторной регуляторной функции артерий и может свидетельствовать о возможном начале развития первичной артериальной гипертонии. Сохранение отношения пульсового давления, измеренного на голени к пульсовому давлению, измененному на плече, в норме представляет собой диагностический показатель, позволяющий исключить диагноз первичная артериальная гипертония II и III стадий, даже если абсолютные значения артериального давления находятся в пределах, соответствующих этим стадиям заболевания.
Значение лодыжечно-плечевого индекса меньше единицы у больных с повышенным артериальным давлением дает дополнительные основания для применения хирургического метода лечения артериальной гипертонии. Сохранение лодыжечно-плечевого индекса в норме - исключает применение данного метода лечения.
Скорость распространения пульсовой волны (СПВ) является независимым предиктором ишемической болезни сердца (ИБС) и инсультов у практически здоровых людей. Повышение артериального давления во время систолы сопровождается растяжением эластических стенок сосудов - пульсовыми колебаниями поперечного сечения или объема. Пульсовые колебания давления и объема распространяются с гораздо большей скоростью, чем скорость кровотока. Скорость распространения пульсовой волны зависит от растяжимости сосудистой стенки и отношения толщины стенки к радиусу сосуда, поэтому данный показатель используют для характеристики упруго-эластических свойств и тонуса сосудистой стенки. При снижении растяжимости стенки с возрастом (атеросклероз) и при повышении тонуса мышечной оболочки сосуда скорость распространения пульсовой волны увеличивается. В норме у взрослых людей скорость распространения пульсовой волны в сосудах эластического типа равна 5-8 м/с, в сосудах мышечного типа - 6-10 м/с.
Для определения скорости распространения пульсовой волны одновременно регистрируют две сфигмограммы (кривых пульса): один датчик пульса устанавливают над проксимальным, а другой - над дистальным отделами сосуда. Так как для распространения волны по участку сосуда между датчиками требуется время, то его и рассчитывают по запаздыванию волны дистального участка сосуда относительно волны проксимального. Определив расстояние между двумя датчиками, можно рассчитать скорость распространения пульсовой волны.
Тяжесть клинических проявлений и прогноз больных с артериальной гипертонией определяется не только степенью повышения артериального давления (АД), но и в значительной мере поражением органов-мишеней, в том числе наличием гипертрофии миокарда левого желудочка (ГЛЖ). ГЛЖ представляет собой физиологическую реакцию сердца на увеличение постнагрузки на левый желудочек, связанное с повышением общего периферического сосудистого сопротивления. Она характеризуется гипертрофией миоцитов, повышением содержания коллагена и фиброзом миокарда. Данные изменения способствуют повышению потребности миокарда в кислороде, а, следовательно, развитию ишемии, изменению систолической и диастолической функций, аритмии. В настоящее время ГЛЖ рассматривают как независимый предиктор ранней сердечно-сосудистой заболеваемости и смертности. У пациентов с АГ, и имеющих ГЛЖ, риск развития сердечно-сосудистых событий достоверно выше по сравнению с больными АГ без ГЛЖ.
Развитие ГЛЖ связано с различными генетическими, демографическими, клиническими и биохимическими факторами. Демографические факторы и образ жизни, ассоциированные с развитием ГЛЖ, включают возраст, пол, физическую активность, расу, ожирение, чувствительность к соли, количество потребляемого алкоголя. Известно, что в возрасте до 55 лет ГЛЖ несколько чаще наблюдается у мужчин, чем у женщин, однако в дальнейшем ее частота у лиц разного пола примерно одинакова. Число больных с ГЛЖ увеличивается с возрастом. Важное значение для развития ГЛЖ имеет тяжесть клинического течения АГ, среди пациентов с АГ 3 степени (АД 180/110 мм рт.ст. и выше) ГЛЖ встречается в 2 раза чаще, чем при АГ 1 степени (АД 140-159/90-99 мм рт.ст.). Кроме степени повышения АД, важную роль в развитии ГЛЖ играет избыточный утренний подъем АД. Значительное повышение АД в утренние часы ассоциировано с развитием ГЛЖ как у леченных, так и у нелеченных больных АГ. Развитию ГЛЖ также способствуют гемодинамические факторы: нагрузка давлением и объемом, изменение структуры артерий, нарушения реологических свойств крови. Для диагностики ГЛЖ могут использоваться различные методы: рентгенография, электрокардиография (ЭКГ), эхокардиография (ЭхоКГ), радиоизотопная вентрикулография, компьютерная томография, магнитно-резонансная томография. Наибольшее клиническое значение в настоящее время имеют ЭКГ и ЭхоКГ. При ЭхоКГ рассчитывают индекс массы миокарда левого желудочка (ИММЛЖ), который является более чувствительным и специфичным методом оценки поражения сердца. Верхнее значение нормы для этого показателя составляет 124 г/м2 для мужчин и 109 г/м2 для женщин. По соотношению толщины задней стенки левого желудочка (ТЗСЛЖ) и его радиуса (РЛЖ), а также с учетом величины ИММЛЖ можно определить тип ремоделирования левого желудочка.
Важной характеристикой системных изменений при атеросклерозе является увеличение толщины комплекса интима-медиа (ИТМ) крупных периферических, и в частности - сонных артерий. Индекс интима-медиа в настоящее время является ключевым показателем развития атеросклеротического процесса и ремоделирования сосудов, измеряемым и мониторируемым при проведении ультразвукового исследования (УЗИ) сосудов.
Полученные при клинических исследованиях значения измеряемых показателей и их взаимосвязь позволяют одновременно проводить раннюю диагностику поражения органов-мишеней у больных с АГ, атеросклеротические и другие изменения кровеносного сосуда, состояние центральной и периферической гемодинамики, изменение геометрии сердца, работы всей сердечно-сосудистой системы в целом.
В настоящее время предлагаемый способ оценки возрастных изменений сердечно-сосудистой системы организма человека имеет достаточно оснований для клинического применения в практическом здравоохранении, широкого внедрения в алгоритмы профилактических обследований, профосмотров и обследований пациентов медицинских учреждений для системной оценки возрастных изменений сердечно-сосудистой системы человека - как надежных, воспроизводимых показателей, позволяющих на доклинической стадии выявить пациентов с гемодинамически значимой патологией артерий нижних конечностей, повышенным риском наличия атеросклеротических поражений в каротидном и коронарном артериальных бассейнах, а также уточнить риски развития сердечно-сосудистых осложнений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НЕИНВАЗИВНОЙ ОЦЕНКИ РАБОТЫ КАРДИОСИНХРОНИЗИРОВАННОГО МЕХАНИЗМА В КРОВЕНОСНЫХ СОСУДАХ И РЕГИОНАЛЬНЫХ СОСУДИСТЫХ БАССЕЙНАХ | 2011 |
|
RU2463948C1 |
| Способ прогнозирования наличия остеопороза по уровню артериальной жесткости у пациентов высокого риска сердечно-сосудистых осложнений | 2020 |
|
RU2746837C1 |
| СПОСОБ ДИЕТИЧЕСКОГО И ПРОФИЛАКТИЧЕСКОГО ПИТАНИЯ ПРИ ВОЗРАСТНЫХ ИЗМЕНЕНИЯХ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ЧЕЛОВЕКА | 2012 |
|
RU2483745C1 |
| Способ прогнозирования наличия артериальной гипертензии у мужчин с низким или умеренным сердечно-сосудистым риском | 2023 |
|
RU2813029C1 |
| СПОСОБ ПЕРСОНИФИЦИРОВАННОЙ ПРОФИЛАКТИКИ ЭСТРОГЕНЗАВИСИМЫХ ЗАБОЛЕВАНИЙ У ЗДОРОВЫХ ЖЕНЩИН И ЖЕНЩИН С ФАКТОРАМИ СЕРДЕЧНО-СОСУДИСТОГО РИСКА В ВОЗРАСТЕ 45-60 ЛЕТ | 2013 |
|
RU2527357C1 |
| СПОСОБ ОЦЕНКИ ВАЗОМОТОРНОЙ ФУНКЦИИ ЭНДОТЕЛИЯ С ПРИМЕНЕНИЕМ ОБЪЕМНОЙ СФИГМОГРАФИИ | 2010 |
|
RU2428924C1 |
| Способ отбора пациентов с факторами риска (ФР) развития сердечно-сосудистых заболеваний (ССЗ) для проведения повторных курсов комплексных профилактических программ | 2021 |
|
RU2757967C1 |
| Способ прогнозирования очень высокого риска возникновения сердечно-сосудистого заболевания у мужчин европейской популяции в возрасте 40-60 лет | 2020 |
|
RU2748715C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ ПРИ ОЖИРЕНИИ | 2014 |
|
RU2546433C1 |
| Способ диагностики состояния сердечно-сосудистой системы с помощью аппаратно-программного комплекса | 2018 |
|
RU2738862C2 |
Изобретение относится к области медицины, а именно к кардиологии. Определяют биофизические и биохимические показатели организма человека. Осуществляют одновременное измерение системного артериального давления на левом и правом плече, левой и правой лодыжке для определения значений лодыжечно-плечевого индекса в левой и правой половине туловища и скорости распространения пульсовой волны в левой и правой половинах туловища. Возрастные изменения сердечно-сосудистой системы организма человека оценивают по величине лодыжечно-плечевого индекса и показателям измерений в момент регистрации этого импульса, а также по показателям состояния центральной и периферической гемодинамики, изменении геометрии сердца, работе сердечно-сосудистой системы и темпе возрастных изменений и их взаимосвязи. Способ позволяет осуществить системную и комплексную оценку возрастных изменений сердечно-сосудистой системы организма человека, провести углубленный патогенетический анализ возрастных изменений, а также определить темп старения сердечно-сосудистой системы при различных нарушениях. 1 табл.
Способ оценки возрастных изменений сердечно-сосудистой системы организма человека, заключающийся в определении биофизических и биохимических показателей организма человека, при котором дополнительно проводят ЭКГ и ЭхоКГ сердца, и по отклонениям указанных показателей и показаний измерений ЭКГ и ЭхоКГ сердца судят о структурно-функциональных и метаболических изменениях в локальных кровеносных сосудах, региональных сосудистых бассейнах, отличающийся тем, что осуществляют одновременное измерение системного артериального давления на левом и правом плече, левой и правой лодыжке для определения значений лодыжечно-плечевого индекса в левой и правой половине туловища и скорости распространения пульсовой волны в левой и правой половинах туловища, а возрастные изменения сердечно-сосудистой системы организма человека оценивают по величине лодыжечно-плечевого индекса и указанным показателям измерений в момент регистрации этого импульса, а также по показателям состояния центральной и периферической гемодинамики, изменению геометрии сердца, работе сердечно-сосудистой системы, темпу возрастных изменений и их взаимосвязи.
| СПОСОБ ОПРЕДЕЛЕНИЯ СКОРОСТИ СТАРЕНИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ЧЕЛОВЕКА | 1999 |
|
RU2193341C2 |
| НАГНЕТАТЕЛЬНЫЙ ВОЗДУШНЫЙ ПОРШНЕВОЙ НАСОС К ВОЛНОВОМУ ДВИГАТЕЛЮ | 1930 |
|
SU21851A1 |
| ВОЙТЕНКО В.П | |||
| и др | |||
| Методика определения биологического возраста человека | |||
| Геронтология и гериатрия | |||
| Биологический возраст | |||
| Наследственность и старение | |||
| - Киев, 1984, с.133-137 | |||
| EDWERD G | |||
| AKATTA, Changes in cardiovascular function with aging, European Heart Journal, 1190, Volume 11, Issue suppl C, p.22. | |||
Авторы
Даты
2013-06-27—Публикация
2012-03-30—Подача