Изобретение относится к области биологии, медицины, ветеринарии и может быть использовано для проведения исследования биологической активности веществ в биологии, медицине и ветеринарии.
Известен способ (1] определения биологической активности вещества. Недостатком способа является существенная ограниченность области применения. Причиной ограниченности является использование в качестве тестирующего только одного вида клеточного материала - длительной культуры костного мозга. Эта ограниченность не позволяет выполнить комплексное определение биологической активности вещества на клетках животных и человека, например раковых клетках. Кроме того, использование только одного типа клеточного тестирующего материала принципиально не позволяет моделировать взаимодействие здоровых и раковых клеток, которое происходит в организме больного животного или человека.
Известен способ [2] определения биологической активности вещества. Недостатком способа является использование двух идентичных клеточных линий, отличающихся по активности только одного гена. Способ не позволяет моделировать процессы взаимодействия пораженной заболеванием клетки со здоровыми клетками организма, которые отличаются по характеру экспрессии множества генов, в результате чего клетки существенно отличаются по своей физиологии и, соответственно, воздействию на окружающие их клетки.
Наиболее близким по существу предполагаемого изобретения, прототипом, является известный способ определения биологической активности вещества [3]. Недостатком прототипа является существенная ограниченность применения. Способ [3] не позволяет проводить исследование биологической активности вещества на клеточных культурах, которые моделируют взаимодействие различных клеточных популяций в организме. Таким образом, с помощью способа [3] нельзя предсказать результат взаимодействия различных здоровых клеток организма с пораженными заболеванием клетками на биологическую активность тестируемого вещества на каждую клеточную популяцию, например раковых клеток.
Целью предполагаемого изобретения является повышение достоверности результата определения биологической активности веществ и расширение области применения способов определения биологической активности веществ.
Цели достигают тем, что выделяют клетки из биологических тканей человека или животных, проводят мечение культур клеток. Мечение выполняют с использованием флюоресцентаого красителя. Меченые культуры клеток совместно ко-культивируют с немеченными пораженными заболеванием клетками. К ко-культуре добавляют исследуемое вещество, осуществляют анализ жизнеспособности определенной популяции клеток в ко-культуре, по результатам анализа определяют биологическую активность исследуемого вещества по отношению к определенной клеточной популяции в ко-культуре здоровых и пораженных заболеванием клеток. Определение биологической активности применяют для выявления противораковых свойств исследуемого вещества по отношению к определенной клеточной популяции в ко-культуре здоровых и пораженных заболеванием клеток.
Сущность предполагаемого изобретения иллюстрирует пример осуществления. предлагаемого способа для оценки биологической активности, в частности цитотоксичности (клеточной токсичности) вещества. Под определением ВЕЩЕСТВО подразумеваются любые субстанции, например материалы, препараты, их компоненты естественного и искусственного происхождения. Осуществление способа производят последовательно, например, в три этапа.
Первый этап
Выбирают биологические ткани, подвергаемые действию испытываемого на биологическую активность вещества, из которых (биологических тканей) выделают и метят испытуемые клетки.
Выделение клеток осуществляют известными способами, например из зачатков зубов человека. Для этого пульпу зуба измельчают, например, стерильным хирургическим скальпелем. Измельченную ткань помещают в емкость для культивирования клеток, например в лунку культурального планшета, и инкубируют в среде DMEM (фирма-производитель красителей - Sigma, Великобритания) с добавлением 10% телячьей эмбриональной сыворотки, при температуре 37°C, во влажной атмосфере, содержащей 5% СО2. Через 1…2 недели наблюдается рост клеток вокруг кусочков зубной ткани. Данные клетки анализируют с использованием стандартных методов проточной цитофлюорометрии [4] для определения их принадлежности к искомым мезенхимальным стволовым клеткам (далее по тексту - МСК).
Мечение культур клеток осуществляют известным способом, например с использованием флюоресцентных in vitro красителей [5]. Для осуществления предлагаемого способа используют, например, две клеточные культуры:
1) мезенхимальные стволовые клетки человека (полученные вышеупомянутым путем);
2) раковые клетки нейробластомы линии SH-SY5Y.
Клетки, например МСК, метят флюоресцентным красителем РКН67 зеленого спектра свечения (фирма-производитель красителей - Sigma, Великобритания). Для этого клетки переводят в суспензию, например, с помощью обработки ферментом трипсин в растворе Версена (фирма-производитель красителей - Sigma, Великобритания). Клетки перемешивают пипетированием и переносят в другую, чистую, пробирку. К клеточной суспензии добавляют культуральную среду DMEM. Клетки осаждают на дне пробирки центрифугированием, например - в течение 5 мин при 1400 об/мин на центрифуге LMC-3000 (фирма-производитель BioSan, Латвия). Клеточный осадок ресуспензируют в буферном растворе «Diluent С» [5], после чего к клеточной суспензии добавляют краситель РКН67, разведенный в буферном растворе «Diluent С». Клеточную суспензию перемешивают пипетированием и инкубируют 5 минут при комнатной температуре, например - при 20…25°C. Процесс мечения клеток останавливают добавлением 1 мл телячьей эмбриональной сыворотки и культуральной среды, например DMEM с добавлением 10% телячьей эмбриональной сыворотки. Клетки осаждают на дне пробирки центрифугированием, например - в течение 10 мин при 1400 об/мин на центрифуге LMC-3000 (фирма-производитель BioSan, Латвия). Клеточный осадок повторно ресуспензирутот в питательной среде, например в питательной среде DMEM с добавлением 10% телячьей эмбриональной сыворотки. Клетки осаждают на дне пробирки центрифугированием, например - в течение 5 мин при 1400 об/мин на центрифуге LMC-3000 (фирма-производитель BioSan, Латвия). Клетки ресуспензируют, например - в питательной среде DMEM с добавлением 10% телячьей эмбриональной сыворотки. Затем проводят оценку количества, концентрации и жизнеспособности клеток, например - окраской трипановым синим и подсчетом окрашенных (мертвых) и неокрашенных (живых) клеток в камере Горяева. Таким путем завершают получение меченой клеточной культуры и приступают ко второму этапу.
Второй этап
Клетки МСК, меченые, например РКН67, и немеченые клетки SH-SY5Y в оптимальном соотношении, например в соотношении 1:1, вносят в лунки культурального планшета и приступают к совместному культивированию (далее по тексту ко-культивирование). Ко-культуры выращивают на культуральной среде, например DMEM с добавлением 10% телячьей эмбриональной сыворотки при температуре 37°C во влажной атмосфере, содержащей 5% СО2. При культивировании раковые клетки SH-SY5Y образуют самоорганизующиеся структуры, напоминающие метастазы опухолей в тканях организма. Таким путем завершают получение ко-культуры клеток для определения биологической активности исследуемого вещества и выполняют третий этап.
Третий этап
Биологическую активность вещества определяют на основании жизнеспособности клеточных популяций в ко-культуре. Берут вещество, биологическую активность которого по отношению к одной из клеточной популяций требуется определить, например пероксид водорода. Пероксид водорода добавляют до конечной концентрации 100…500 мкМ и ко-культуру инкубируют 20 часов в культуральной среде DMEM с добавлением 10% телячьей эмбриональной сыворотки, при температуре 37°C, во влажной атмосфере, содержащей 5% СО2. Биологическую активность исследуемого вещества определяют, например, с помощью проточной флуоресцентной цитометрии [4], например с окраской пропидием иодида. Этот способ определения биологической активности основан на способности пропидия иодида окрашивать ядра только мертвых клеток (красная флюоресценция). Каждая культура клеток состоит из живых и определенного процента мертвых клеток (умирающих в силу естественных причин). Применение окрашивания пропидием иодида позволяет определить процент мертвых клеток в культуре. Увеличение или снижение процента мертвых клеток свидетельствует о понижении или увеличении жизнеспособности клеточной культуры, что соответственно является следствием биологической активности исследуемого вещества.
Приведенный для примера способ с использованием проточный цитометрии позволяет проводить подсчет отдельных клеток, имеющих различные спектры флюоресценции. Определение жизнеспособности клеток меченой популяции проводят по формуле:
Ж=100 - (K1×100/K2), где
Ж - процент жизнеспособных клеток;
K1 - количество (численность) клеток, меченых зеленым флюоресцентным красителем РКН67 и красным флюоресцентным красителем пропидиум иодидом;
K2 - количество (численность) клеток, меченых зеленым флюоресцентным красителем РКН67.
Анализ жизнеспособности клеток не меченой популяции осуществляется по аналогичной формуле, в которой значения K1 и K2 соответствуют аналогичным параметрам клеток, не меченых зеленым флюоресцентным красителем РКН67.
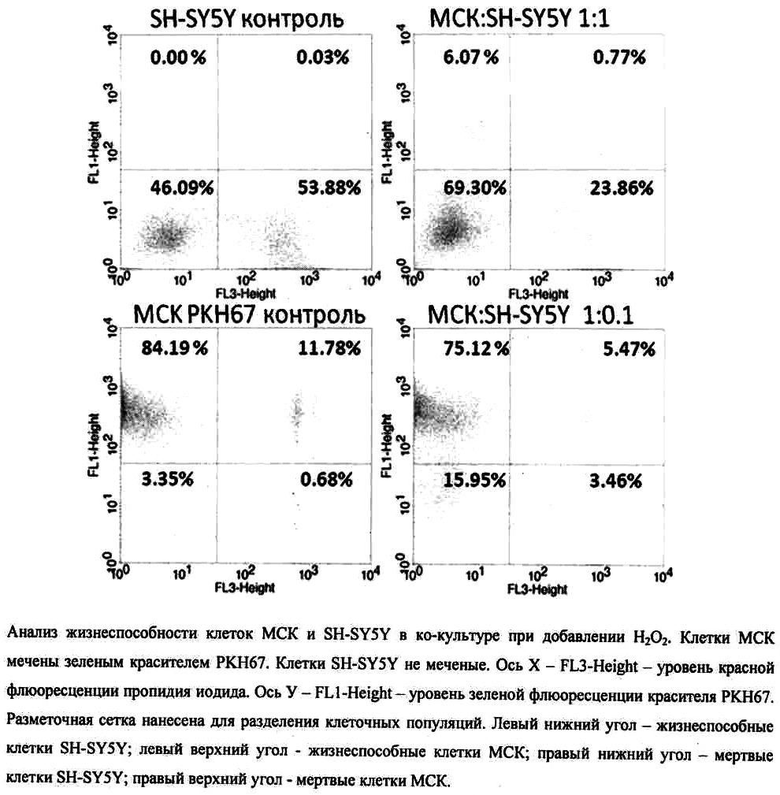
Результат определения биологической активности исследуемого вещества - перикиси водорода H2O2 - иллюстрирует Фиг., отражающий анализ жизнеспособности клеток МСК и SH-SY5Y в ко-культуре при добавлении Н2О2. Клетки МСК мечены зеленым красителем РКН67. Клетки SH-SY5Y не меченые. Ось Х - FL3-Height - уровень красной флюоресценции пропидия иодида. Ось У - FL1-Height - уровень зеленой флюоресценции красителя РКН67. Разметочная сетка нанесена для разделения клеточных популяций. Левый нижний угол - жизнеспособные клетки SH-SY5Y; левый верхний угол - жизнеспособные клетки МСК; правый нижний угол - мертвые клетки SH-SY5Y; правый верхний угол - мертвые клетки МСК.
Проводя сравнение не подверженного воздействию исследуемого препарата контрольного образца с опытными образцами, подвергшимися воздействию исследуемого вещества в различных концентрациях, в условиях культивирования клеток в виде чистых отдельных культур или в виде ко-культуры делают заключение о влиянии исследуемого препарата на биологические функции определенной клеточной популяции.
Таким образом, пример показывает достижимость цели изобретения - определение цитотоксичности (частный случай биологической активности) вещества к определенной клеточной популяции (SH-SY5Y) в ко-культуре (МСК+раковые клетки SH-SY5Y).
Предлагаемый способ применяют, кроме показанного в примере, и для иных клеточных популяций в ко-культуре, например для определения биологической активности исследуемого вещества на пораженные заболеванием клетки, например раковые. Для этого процедуру мечения и определения жизнеспособности меченых клеток проводят с раковыми клетками с использованием способа, описанного выше для МСК.
Описанный способ определения биологической активности вещества, основанный на ко-культивироваяии здоровых и пораженных заболеванием клеток, обладает преимуществом перед известными способами. Предлагаемый способ позволяет определить биологическую активность вещества по отношению к определенной, заранее выбранной, клеточной популяции, например к раковым и/или стволовым клеткам. Использование в качестве объекта тестирования ко-культуры здоровых и пораженных заболеванием клеток позволяет повысить достоверность определения биологической активности путем моделирования межклеточных взаимодействий, например условий, в которых раковые клетки находятся в тканях организма.
Моделирование процесса взаимодействия потенциально-лекарственного вещества с клетками биологических тканей, например больного пациента, вне организма пациента позволяет существенно повысить результативность поиска и применения оптимального, наиболее подходящего в конкретной ситуации лекарственного препарата. Например, таким моделированием удается выявить препарат, обладающий низкой цитотоксичностью по отношению к здоровым клеткам и обладающий высокой цитотоксичностью к пораженным заболеванием клеткам, например обладающий противораковым эффектом.
Такой подбор наиболее эффективного лечебного препарата до максимально возможного повышает результативность лечебного процесса.
Общепринятое использование для определения биологической активности вещества отдельных чистых культур клеток не позволяет проводить точную оценку терапевтических параметров, так как при тесном взаимодействии здоровые и пораженные заболеванием клетки могут изменять физиологический статус соседних клеток, меняя их чувствительность к лекарственным препаратам. Предлагаемый способ, в отличие от общепринятых, позволяет моделировать физиологические взаимодействия здоровых и пораженных заболеванием клеток вне организма, в культуре клеток, что недостижимо при применении прототипа.
Проведенные ранее эксперименты показали, что клетки, выделяемые из зачатков зубов человека по описанному в примере способу, аналогичны мезенхимным стволовым клеткам (МСК) (6). Известно, что помимо зачатков зубов, МСК выделяют из костного мозга, жировой ткани, хрящей, пуповины и пуповинной крови, плаценты, пульпы зубов и других тканей человека и животных (7, 8). Эти клетки обладают схожими свойствами, такими как иммунофенотип, и способностью к дифференцировке в остеогенном, хондрогенном и адипогенном направлении. Таким образом, приведенный пример осуществления предлагаемого способа не ограничивает применение иных (по сравнению с приведенными в примере) культур клеток, а также способов мечения клеточных популяций и способов определения биологического эффекта исследуемого вещества на здоровые и раковые клетки.
Приведенный пример применения предполагаемого изобретения показывает его полезность для исследования биологической активности лекарственных препаратов в медицине. Применение предлагаемого способа особо полезно при разработке in vitro тест-систем повышенной эффективности для поиска (скрининга) новых веществ, обладающих лекарственным действием.
Предлагаемое изобретение удовлетворяет критериям новизны, так как при определении уровня техники не обнаружено средство, которому присущи признаки, идентичные (то есть совпадающие по исполняемой ими функции и форме выполнения этих признаков) всем признакам, перечисленным в формуле изобретения, включая характеристику назначения.
Предлагаемый способ имеет изобретательский уровень, поскольку не выявлены технические решения, имеющие признаки, совпадающие с отличительными признаками данного изобретения, и не установлена известность влияния отличительных признаков на указанный технический результат.
Заявленное техническое решение применимо в промышленном поиске биологически активных веществ, обладающих определенными терапевтическими, лекарственными, свойствами, и применять выявленный таким путем биологически активный препарат в деятельности организаций здравоохранения, например для лечения онкологических заболеваний, посредством использования известных стандартных технических устройств и оборудования. Это соответствует критерию «промышленная применимость», предъявляемому к изобретениям.
Использованные источники
1. Способ определения биологической активности вещества для доклинических испытаний. Заявка RU 2002113711.
2. Targeted methods of drug screening using co-culture methods. US Patent 6518035.
3. Method of Testing the Safety and Efficacy of a Drug. US Patent 20070172814.
4. Dean PN, Hoffman RA. Overview of flow cytometry instrumentation. Curr Protoc Cytom. 2007 Jan; Chapter 1:Unit1.1.
5. Stable cell membrane labelling. Horan PK, Slezak SE. Nature. 1989 July 13; 340(6229): 167-8.
6. Isolation and characterization of stem cells derived from human third molar tooth germs of young adults: implications in neo-vascularization, osteo-, adipo- and neuro-genesis. Yalvac ME, Ramazanoglu M, Rizvanov AA, Sahin F, Bayrak OF, Salli U, Palotas A, Kose GT. Phannacogenomics J. 2010 Apr; 10(2): 105-13.
7. Tamok, A., Ulrich, H. and Bocsi, J. Phenotypes of stem cells from diverse origin // Cytometry A. - 2010. - 1: Vol.77. - p.6-10.
8. Webster RA, Blaber SP, Herbert BR, Wilkins MR, Vesey G. The role of mesenchymal stem cells in veterinary therapeutics - a review. N Z Vet J. 2012 Sep; 60(5):265-72.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА НА ОСНОВЕ ВЕЗИКУЛ КЛЕТОК ЧЕЛОВЕКА | 2015 |
|
RU2605853C1 |
| Способ скрининга противоопухолевых препаратов in vitro на многокомпонентной клеточной тест-системе | 2018 |
|
RU2695568C1 |
| Генетическая кассета, содержащая кодон-оптимизированные нуклеотидные последовательности генов TRAIL, PTEN и IFNβ-1, и фармацевтическая композиция для лечения онкологических заболеваний | 2020 |
|
RU2757502C1 |
| Применение мембранных везикул мультипотентных стромальных клеток, индуцированных цитохалазином В, для восстановления и повышения митохондриальной функции | 2019 |
|
RU2727540C1 |
| Носитель для культивирования клеток человека и животных | 2017 |
|
RU2663131C1 |
| Генно-клеточный везикулярный терапевтический препарат и способ терапии рассеянного склероза посредством трансплантации генно-клеточного везикулярного терапевтического препарата | 2021 |
|
RU2762855C1 |
| Способ увеличения пролиферативного потенциала трехмерных опухолевых клеточных культур | 2021 |
|
RU2782600C1 |
| АНТИРЕТРОВИРУСНЫЕ ПРЕПАРАТЫ НА ОСНОВЕ ПРОИЗВОДНЫХ АЗИДОТИМИДИНА | 2014 |
|
RU2561501C1 |
| Способ терапии болезни Тея-Сакса и болезни Сандхоффа с помощью генетически модифицированных мезенхимных стволовых клеток человека со сверхэкспрессией β-гексозаминидазы A | 2020 |
|
RU2748383C1 |
| СПОСОБ НАРАЩИВАНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ В ЗОНАХ ДЕФЕКТА АЛЬВЕОЛЯРНОГО ОТРОСТКА ЧЕЛЮСТИ | 2014 |
|
RU2570034C1 |
Настоящее изобретение относится к медицине и описывает способ определения биологической активности вещества, заключающийся в том, что выделяют клетки из биологических тканей человека или животных, проводят мечение с использованием флюоресцентного красителя, ко-культивируют с пораженными заболеванием клетками, к ко-культуре добавляют исследуемое вещество, определяют биологическую активность исследуемого вещества, анализируя жизнеспособность определенной клеточной популяции в ко-культуре здоровых и пораженных заболеванием клеток по увеличению или снижению процента мертвых клеток. Изобретение обеспечивает повышение достоверности результата определения биологической активности веществ и расширение области применения способов определения биологической активности веществ. 1 з.п. ф-лы, 1 ил.
1. Способ определения биологической активности вещества заключается в том, что выделяют клетки из биологических тканей человека или животных, проводят мечение с использованием флюоресцентного красителя, ко-культивируют с пораженными заболеванием клетками, к ко-культуре добавляют исследуемое вещество, определяют биологическую активность исследуемого вещества анализируя жизнеспособность определенной клеточной популяции в ко-культуре здоровых и пораженных заболеванием клеток по увеличению или снижению процента мертвых клеток.
2. Способ определения биологической активности по п.1 применяют для выявления противораковых свойств исследуемого вещества по отношению к определенной клеточной популяции в ко-культуре здоровых и пораженных заболеванием клеток.
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ВЕЩЕСТВА | 1992 |
|
RU2008680C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ВЕЩЕСТВА | 2000 |
|
RU2176390C1 |
| Николаенко М.Н | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Автореферат диссертации, 2007. | |||
Авторы
Даты
2013-09-10—Публикация
2009-09-11—Подача