Предлагаемое изобретение относится к медицине и может быть использовано в остеологии, дентальной имплантологии, пластической и реконструктивной хирургии, челюстно-лицевой хирургии, травматологии и ортопедии, ветеринарной медицине.
В настоящее время стало возможным получать из организма взрослого человека, животных (костный мозг, подкожно-жировая клетчатка, дерма) его собственные (ауто-) стволовые клетки, длительно культивировать с сохранением их первоначального фенотипа, наращивать в огромных количествах, направлять их на определенный путь развития (дифференцировка) в специализированные клетки, создавать трехмерные структуры, соответствующие условиям тканевого окружения, получать клеточно-тканевые трансплантаты на основе биодеградируемых материалов.
Все это способствует разработке новых технологий клеточной и тканевой терапии, которые помогут решить проблему лечения ряда тяжелых заболеваний животных и человека.
Известно большое количество способов пластики костных дефектов альвеолярного отростка челюстей, однако применяемые материалы не всегда удовлетворяют предъявляемым к ним требованиям. Стволовые клетки могут восстановить практически любое повреждение, превращаясь на месте в необходимые организму клетки (костные, гладкомышечные, печеночные, клетки сердечной мышцы или даже нервные) и стимулируя внутренние резервы организма к регенерации (восстановлению) органа или ткани. (Интернет-ресурс http://gulnara-wellness.blogspot.ru/2011_05_01_archive.html ПРИНЦИПИАЛЬНОЕ ОТЛИЧИЕ ПРИМЕНЕНИЯ КЛЕТОЧНОЙ ТЕРАПИИ СТВОЛОВЫМИ КЛЕТКАМИ В КЛИНИЧЕСКОЙ ОНКОЛОГИИ, 31 мая 2011 г. «Здоровье и Молодость»).
Из исследованного уровня техники заявителем выявлены различные способы наращивания костной ткани альвеолярных отростков челюстей, некоторые из них совпадают с заявленным техническим решением по назначению, другие по наличию некоторых совпадающих признаков.
Из исследованного уровня техники выявлено изобретение по патенту №2389442 «Способ лечения хронического остеомиелита с дефектом кости», сущность которого заключается в том, что способ лечения хронического остеомиелита длинных трубчатых костей с дефектом кости, включающий имплантацию аутологичных клеток костного мозга в остеомиелитический очаг, отличающийся тем, что берут у пациента костный мозг, выделяют мононуклеарные клетки костного мозга, после культивирования в течение 3-5 суток первый имплантат, представляющий суспензию неприлипающей фракции мононуклеарных клеток костного мозга в количестве 300-500·106 клеток, вводят в мягкие ткани в области очага, далее прилипающую фракцию культивируют в течение 3-4 недель и второй имплантат, являющийся суспензией мезенхимальных стромальных клеток костного мозга в количестве 10-15·106 клеток, вводят непосредственно в остеомиелитический очаг.
Детальнее известный способ лечения хронического остеомиелита длинных трубчатых костей с нарушением остеорегенерации возможно охарактеризовать тем, что проводят трехкратную трансплантацию в область остеомиелитического очага аутологичных стромальных стволовых клеток.
При этом стромальные стволовые клетки получают из аспирата костного мозга путем культивирования с удалением неприлипающей фракции.
После наращивания необходимого количества клеток их индуцируют в остеогенном направлении путем дополнительного культивирования в остеогенной среде в течение 21 суток, далее полученные клетки в количестве 300-500·106 клеток вводят в остеомиелитический очаг трехкратно с интервалом в 1 неделю.
При этом следует отметить, что известный способ имеет ряд существенных недостатков, а именно:
- длительное культивирование клеток in vitro может приводить к нежелательным изменениям генотипа, в том числе к онкогенным мутациям;
- длительная культивация требует значительных материальных затрат, временной промежуток между забором костного мозга и трансплантацией клеток порядка 2-х месяцев обременителен для больного;
- трехкратное введение клеток в очаг повышает инвазивность лечения и увеличивает риск рецидива инфекционного процесса.
Из исследованного уровня техники заявителем выявлен патент №2240135 «Культура клеток, содержащая клетки-предшественники остеогенеза, имплантат на ее основе и его использование для восстановления целостности кости», указанный способ восстановления целостности кости, предусматривающий использование культуры клеток костного мозга млекопитающих, содержащей клетки-предшественники остеогенеза.
Сущность известного способа заключается в том, что культура клеток, содержащая клетки-предшественники остеогенеза, характеризующаяся тем, что она представляет собой клетки стромального и лимфо-макрофагального ряда костного мозга млекопитающих, культивированные в питательной среде с 10% бычьей эмбриональной сывороткой в течение 4-7 дней с использованием в качестве индукторов остеогенеза - инсулина, дексаметазона и β-глицерофосфата с 24-часовой обработкой 5-азацитидином в середине цикла и формирующие монослойную культуру с адгезивной способностью не менее 4·104 клеток/см2.
Таким образом, клетки стромального и лимфомакрофагального ряда костного мозга культивируют в индукционной остеогенной среде до формирования монослойной культуры на аллогенном деминерализованном костном матриксе и губке из биодеградируемого материала и вносят в костный дефект, достигая реваскуляризации с помощью костного аутотрансплантата.
Недостатками известного способа является:
- сложная подготовка трансплантата костного мозга для широкого клинического использования;
- высокий риск развития осложнений в донорской зоне;
- длительный срок лечения и наступления полезного результата;
- потенциальный риск спонтанной онкогенетической трансформации при пересадке культивированных «взрослых» стволовых клеток человека (Singh et al. 2004), передача вирусов (Ogle et al. 2005).
Кроме этого, заявителем выявлен способ реконструкции альвеолярных отростков челюстей, защищенный патентом №2163099.
Сущность известного способа характеризуется тем, что реконструкция альвеолярных отростков челюстей, включающая скелетирование альвеолярных отростков в области дефектов костной ткани, декортикацию, наложение минерального компонента кости в смеси с декальцинированной костью, отличается тем, что после декортикации на костное ложе укладывают морфогенетический белок, затем минеральный компонент кости, в качестве которого используют неорганический костный матрикс и декальцинированную кость в виде лиофилизированной костной стружки и изолируют от мягких тканей твердой мозговой оболочкой.
Таким образом, указанный способ включает использование костного морфогенетического белка в качестве стимулятора остеогенеза с целью сокращения сроков заживления костной раны, а также послеоперационной раны, получения полноценного костного регенерата в более короткие сроки, с нужным объемом и наименьшим количеством послеоперационных осложнений.
Недостатком данного способа является то, что, как указано в патенте, непосредственно костный морфогенетический белок «укладывают» на костное ложе. Отсутствие какого-либо носителя, например, в виде гранул, остеопластических материалов, мембраны и т.д. не позволяет в полной мере придать объем (форму) костному морфогенетическому белку, что впоследствии будет приводить к его (костный морфогенетический белок) растеканию и диффузии в окружающие ткани, вследствие чего ожидаемый положительный результат наращивания кости под действием костного морфогенетического белка не достигается в полной мере.
Кроме этого, заявителем из исследованного уровня техники выявлен способ «Экспериментально-клинического обоснования применения пористых материалов на основе сплава никелида-титана для наращивания объема костной ткани в зонах дентальной имплантации» (Автореферат диссертации на соискание ученой степени кандидата медицинских наук Азизовой Дины Анваровны ВАК РФ 14.01.14), который заключается в наращивании костной ткани с применением пористой никелид-титановой мембраны, изготовленной по форме альвеолярного гребня, где в полость подмембранного пространства помещают никелид-титановые гранулы в смеси с факторами роста («Гамалант»), далее рана ушивается.
Недостатком известного способа является использование в качестве факторов роста ксеногенного материала, который способен вызывать реакции отторжения, что приводит к рискам развития осложнений.
Кроме указанного, известный способ может привести к выраженным иммунологическим проблемам, а именно к спонтанной онкогенетической трансформации, при этом указанный способ не исключает возможность передачи вирусов. К недостаткам указанного способа можно отнести, в том числе, и сложность получения факторов роста. При этом следует отметить факт того, что для обеспечения полноценного объема костной ткани требуется длительный период в интервале до шести месяцев, что является весьма затратным в материальном плане.
Наиболее близким аналогом изобретения, совпадающим по назначению и количеству совпадающих признаков, выбранным заявителем в качестве прототипа, является «Способ костной пластики в эксперименте» по патенту №2336841.
Способ костной пластики в эксперименте, включающий имплантацию фибробластоподобных клеток, отличающийся тем, что жировую ткань, полученную из подкожно-жирового слоя путем аспирации, подвергают ферментативной обработке раствором коллагеназы, центрифугируют, в полученную фракцию фибробластоподобных клеток в качестве индуктора остеогенной дифференцировки добавляют костную крошку в пропорции 1 объем крошки на 4 объема клеточной фракции и непосредственно после приготовления вводят аутологичную смесь в область костного дефекта.
Более детально способ осуществляют следующим образом. Под местной анестезией выполняют шприцевую липоаспирацию. Полученную жировую ткань интенсивно промывают стерильным физиологическим раствором от примеси крови и анестетика, далее путем ферментативной диссоциации жировой ткани и центрифугирования выделяют стромальную фракцию с преобладанием фибробластоподобных клеток. Далее из места имеющегося костного дефекта выполняют забор костной крошки. В стромальную клеточную фракцию добавляют костную крошку в пропорции 1:4 и этой смесью заполняют дефект кости. Фиксацию "трансплантата" осуществляют с помощью окружающих мягких тканей, проницаемых нерезорбируемых или резорбируемых материалов.
Недостатками известного способа являются:
- дополнительная травма челюстно-лицевой области во время забора костной крошки из края костного дефекта, т.к. в процессе сбора костной крошки увеличивается сам дефект альвеолярного отростка и тем самым возрастает объем дефекта для костной регенерации;
- в случае наличия недостаточности костной ткани в области, например, обширного дефекта, реализовать известный способ практически не представляется возможным;
- большой временной интервал роста костной ткани.
Заявленное техническое решение направлено на устранение недостатков прототипа и получение менее травматичного и более технологичного способа наращивания костной ткани, который впоследствии возможно развить и для областей восстановительной хирургии не только в области стоматологии, но и в травматологии и ортопедии в целом.
Заявленное техническое решение иллюстрируется Фото 1-3, на которых представлены основные этапы реализации заявленного способа, выполненные на экспериментальном животном (собаке).
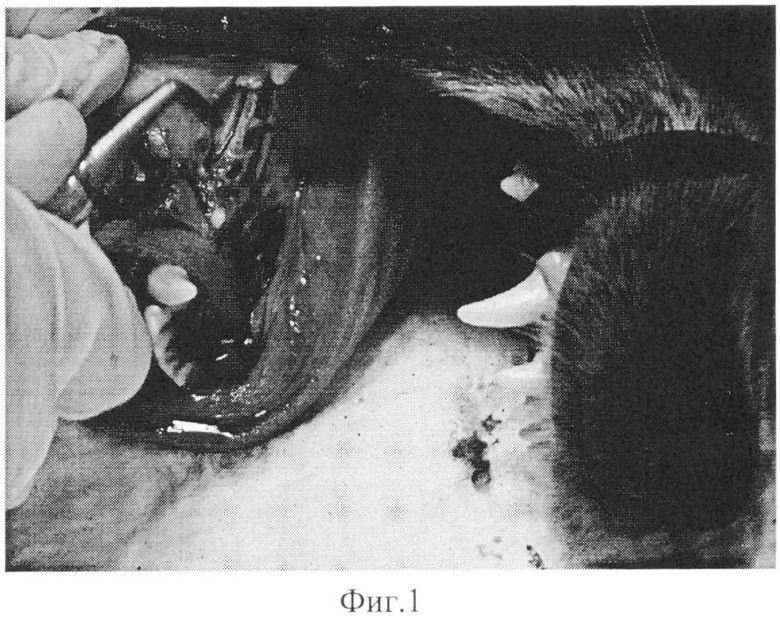
На Фото 1 представлен этап создания области дефекта (удаление зубов).
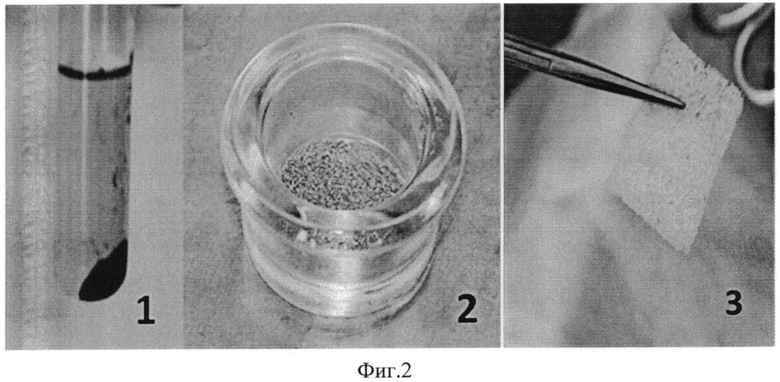
На Фото 2 представлены собственно материалы, используемые в заявленном способе, а именно под цифрой 1 представлена стромально-васкулярная фракция, под цифрой 2 представлены никелид-титановые гранулы, под цифрой 3 представлен собственно ксеногенный костный матрикс (мембрана).
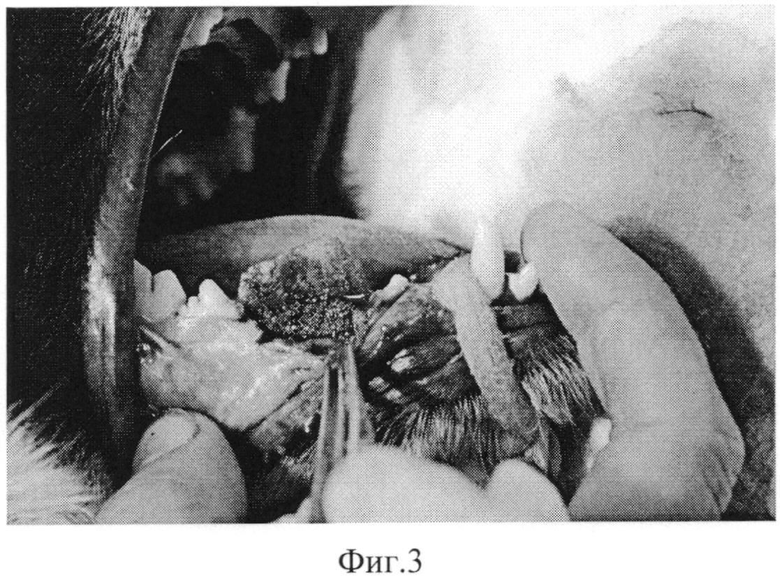
На Фото 3 приведен этап заполнения дефекта альвеолярного отростка.
Сущность заявленного способа заключается в наращивании объема костной ткани в зонах дефекта альвеолярного отростка челюсти, включаюет забор из передней брюшной стенки методом липосакции жировой ткани, последующую ее ферментизацию с добавлением коллагеназы, центрифугирование и получение стромально-васкулярной фракции, при этом в качестве остеокондуктивного материала используют пористые никелид-титановые гранулы, которые насыщают клетками полученной стромально-васкулярной фракции и размещают в зоне дефекта, с последующим приданием требуемого объема восстанавливаемой костной ткани с помощью ксеногенного костного матрикса, который также укладывают в зону дефекта с последующим ушиванием раны.
В заявленном техническом решении после проведения ферментной обработки жировой ткани из нее получают клетки стромально-васкулярной фракции (СВФ) известным в целом методом.
Краткая сущность заявляемого технического решения заключается в том, что полученные известным методом клетки стромально-васкулярной фракции жировой ткани (далее СВФЖТ) доставляют в зону дефекта альвеолярного отростка с помощью никелид-титановых гранул с приданием требуемого объема, с последующим закрытием области дефекта ксеногенным костным матриксом (мембраной) и ушиванием раны.
При этом в качестве остеокондуктивного материала заявителем вместо применения своей (пациента) костной крошки, факторов роста (ксеногенного происхождения) использован никелид-титановый порошок (в виде гранул), пропитанный стромально-васкулярной фракцией (собственными стволовыми клетками, полученными из жировой ткани), и ксеногенный костный матрикс (мембрана).
Таким образом, заявленное техническое решение предназначено для создания костной ткани для последующей дентальной имплантации.
Для реализации заявленного способа производится забор жировой ткани путем липосакции из передней брюшной стенки живота (животного, человека). Из забранной жировой ткани производится выделение клеток стромально-васкулярной фракции (СВФ). Для этого жировую ткань трижды промывают в физиологическом растворе в стерильных условиях. Далее производится ферментизация жировой ткани с добавлением коллагеназы. Одновременно с выделением клеток создается дефект альвеолярного отростка челюсти. Клетки СВФ (в обобщенном виде применим термин стволовые клетки) совместно с остеокондуктивными материалами (пористые никелид-титановые гранулы, ксеногенный костный матрикс (мембрана)) трансплантируются в зону дефекта альвеолярного отростка. Перспективность использования стволовых клеток жировой ткани обусловлена, в первую очередь, доступностью биологического материала и легкостью выращивания в условиях культивирования in vitro.
Целью заявленного способа является устранение недостатков прототипа, а именно:
- исключение дополнительной травмы челюстно-лицевой области во время забора костной крошки из края костного дефекта, т.к. в процессе сбора костной крошки увеличивается сам дефект альвеолярного отростка и тем самым возрастает объем дефекта для костной регенерации;
- обеспечение возможности регенерации костной ткани даже в случаях полного или частичного отсутствия костной ткани;
- значительное сокращение временного интервала полного восстановления роста костной ткани;
- возможность формирования и наращивание объема костной ткани в зонах дентальной имплантации альвеолярных отростков челюстей (кости) на основе адресной доставки стволовых клеток, совместно с остеокондуктивными материалами;
- обеспечение возможности наращивания костной ткани требуемой формы и размеров.
Указанная цель достигается выполнением следующей последовательности выполнения операций:
1. Забор жировой ткани.
2. Получение стромальной-васкулярной фракции.
3. Создание модели беззубого участка непосредственно после удаления зубов.
4. Заполнение дефекта костной ткани стромально-васкулярной фракцией с остеокондуктивными материалами (пористые никелид-титановые гранулы, ксеногенный костный матрикс).
5. Ушивание раны.
Проведение эксперимента сопровождали рентгенологическими исследованиями и клиническими наблюдениями. Через 1, 3, 6 мес производили забор никелид-титановых костных блоков, которые в дальнейшем подвергались гистологическим наблюдениям.
Для морфологического исследования процессов, протекающих вокруг пористых материалов, из сплава никелида титана предварительно удаляли пористый порошок, используя методику глубокого травления по Миргазизову, препараты костных блоков декальцинировали, делали парафиновые срезы и окрашивали гематоксилином и эозином и по Ван-Гизону.
В предлагаемом способе остеогенная трансформация (пролиферация и дифференцировка) пересаженной клеточной фракции происходит in vivo под влиянием комплекса естественных остеоиндукторов. При осуществлении данного способа не проводят культивирование тканей, которое связано с риском инфицирования клеточной популяции, контаминации чужеродным материалом животного происхождения из питательной среды, непредсказуемого изменения свойств клеток (Wang Y., Huso D.L., Harrington J., Kellner J., Jeong D.K., Turney J., McNiece I.K. Outgrowth of a transformed cell population derived from normal human BM mesenchymal stem cell culture // Cytotherapy - 2005 - Vol 7(6) - P. 509-519.).
Известно, что стромально-васкулярная фракция жировой ткани содержит истинные «покоящиеся» мезенхимальные стволовые клетки, которые имеют характеристики, аналогичные свойствам стромальных клеток костного мозга: обладают высокой пролиферативной активностью, способны к самоподдержанию и мультилинейной (в том числе, остеогенной) дифференцировке (Zuk Р.А., Zhu М., Ashjan P. et al. Human adipose tissue is a source of multipotent stem cells // Mol. Biol. Cell - 2002 - Vol. 13 - P. 4279-4295; Mizuno H. Versatility of adipose tissue as a source of stem cells // J Nippon Med Sch. - 2003 - Vol. 70(5) - P. 428-431).
По результатам экспериментального исследования удалось добиться полного сегментарного наращивания костной ткани в области искусственно созданных дефектов в эксперименте на собаках.
Через 1 мес во всех наблюдениях дефект челюсти был закрыт грубоволокнистой костью с балочным строением, по периферии выявлялись многоядерные остеокласты, в межбалочных пространствах выявлялись кровеносные сосуды.
Через 3 мес наблюдается формирование зрелой кости и восстановление мягких тканей с нормальным многослойным плоским неороговевающим эпителием. Новообразованная костная ткань имела ячеистый вид, поскольку образовалась вокруг гранул никелид-титанового порошка, удаленных путем травления.
Через 6 мес имело место заживление путем формирования пластинчатых костных структур с хорошо развитой системой гаверсовых каналов.
Таким образом, полученные результаты демонстрируют целесообразность применения предлагаемого способа костной пластики для устранения дефектов кости. Способ характеризуется малой травматичностью, иммунологической безупречностью, онкогенной безопасностью, не требует существенных материальных затрат и может быть применен в практической медицине.
Предлагаемое изобретение удовлетворяет критериям новизны, так как при определении уровня техники не обнаружено средство, которому присущи признаки, идентичные (то есть совпадающие по исполняемой ими функции и форме выполнения этих признаков) всем признакам, перечисленным в формуле изобретения, включая характеристику назначения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ наращивания объема костной ткани гребня альвеолярного отростка челюсти | 2016 |
|
RU2645963C2 |
| Способ изготовления многокомпонентного остеогенного трансплантата при хирургическом устранении врождённых и приобретённых дефектов кости челюстей | 2021 |
|
RU2778353C2 |
| Способ предотвращения неконтролируемого изменения объёма остеогенного трансплантата в послеоперационном периоде после устранении врождённых и приобретённых дефектов кости челюстей | 2021 |
|
RU2778352C2 |
| Многокомпонентный остеогенный трансплантат для хирургического устранения врождённых и приобретённых дефектов кости челюстей | 2021 |
|
RU2766978C1 |
| УСТРОЙСТВО ДЛЯ ВОССТАНОВЛЕНИЯ УТРАЧЕННОЙ КОСТНОЙ ТКАНИ ВОКРУГ ОБНАЖЕННОЙ ПОВЕРХНОСТИ ИМПЛАНТАТА И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2015 |
|
RU2604049C1 |
| Устройство с памятью формы для дистракции костной ткани гребня альвеолярного отростка и способ его использования перед протезированием на имплантатах | 2019 |
|
RU2713939C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОСТИ АЛЬВЕОЛЯРНОГО ГРЕБНЯ ЧЕЛЮСТИ И ТКАНЕЙ ПАРОДОНТА С РЕДУЦИРОВАННЫМ РЕГЕНЕРАТОРНЫМ ПОТЕНЦИАЛОМ | 2006 |
|
RU2320285C2 |
| СПОСОБ АДРЕСНОЙ ДОСТАВКИ ОСТЕОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ФАКТОРЫ РОСТА И РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ, В ОБЛАСТЬ ДЕФЕКТА АЛЬВЕОЛЯРНОЙ КОСТИ | 2011 |
|
RU2469676C1 |
| Способ регенерации костной ткани челюстей | 2019 |
|
RU2709723C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ДЕСНЫ В ОБЛАСТИ ОБНАЖЕННОЙ ПОВЕРХНОСТИ ИМПЛАНТАТА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2015 |
|
RU2597145C1 |
Изобретение относится к медицине, в частности к остеологии, и касается наращивания объема костной ткани в зонах дефекта альвеолярного отростка челюсти. Способ включает забор из передней брюшной стенки методом липосакции жировой ткани, последующую ее ферментизацию с добавлением коллагеназы, центрифугирование и получение стромально-васкулярной фракции. В качестве остеокондуктивного материала используют пористые никелид-титановые гранулы. Последние насыщают клетками полученной стромально-васкулярной фракции и размещают в зоне дефекта. Придают требуемый объем восстанавливаемой костной ткани с помощью ксеногенного костного матрикса, который также укладывают в зону дефекта с последующим ушиванием раны. Способ обеспечивает наращивание костной ткани при малой травматичности, иммунологической безупречности, онкогенной безопасности, при этом не требует существенных материальных затрат. 3 ил.
Способ наращивания объема костной ткани в зонах дефекта альвеолярного отростка челюсти, включающий забор из передней брюшной стенки методом липосакции жировой ткани, последующую ее ферментизацию с добавлением коллагеназы, центрифугирование и получение стромально-васкулярной фракции, отличающийся тем, что в качестве остеокондуктивного материала используют пористые никелид-титановые гранулы, которые насыщают клетками полученной стромально-васкулярной фракции и размещают в зоне дефекта, с последующим приданием требуемого объема восстанавливаемой костной ткани с помощью ксеногенного костного матрикса, который также укладывают в зону дефекта с последующим ушиванием раны.
| СПОСОБ АДРЕСНОЙ ДОСТАВКИ ОСТЕОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ФАКТОРЫ РОСТА И РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ, В ОБЛАСТЬ ДЕФЕКТА АЛЬВЕОЛЯРНОЙ КОСТИ | 2011 |
|
RU2469676C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ В ЭКСПЕРИМЕНТЕ | 2006 |
|
RU2336841C2 |
| СПОСОБ СТИМУЛЯЦИИ ФОРМИРОВАНИЯ ФИБРОЗНО-ХРЯЩЕВОГО РЕГЕНЕРАТА КОСТНОЙ МОЗОЛИ У МЛЕКОПИТАЮЩИХ | 2011 |
|
RU2461621C1 |
| Затвор к щелевым разбрасывающим сыпучее вещество приспособлениям | 1930 |
|
SU25004A1 |
| АЗИЗОВА Д.А | |||
| Экспериментально-клинического обоснования применения пористых материалов на основе сплава никелида-титана для наращивания объема костной ткани в зонах дентальной имплантации | |||
| Автореферат диссертации на соискание ученой степени | |||
Авторы
Даты
2015-12-10—Публикация
2014-06-16—Подача