Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет относительно заявки США №12/212131, поданной 22 сентября 2008 года, и заявки США №12/001951, поданной 12 декабря 2007 года. Полнота каждой из этих заявок включена в настоящий документ посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к алкилированным 1,3-бензолдиаминам, а более конкретно, к алкилированным N1,N3-дициклоалкил-1,3-бензолдиаминам, и способам их получения. Подобные алкилированные 1,3-бензолдиамины можно использовать, например, в качестве антиокислителей, стабилизаторов и антиозонантов для смазочных материалов, реагентов для электроники, уретанов, средств для защиты урожая, фармацевтических препаратов, красителей и тонеров.
Уровень техники
Смазочные материалы, такие, как смазочные материалы, используемые в разнообразных механизмах, подвержены окислительной деградации во время хранения, транспортировки и использования, в частности, когда подобные смазочные материалы подвергают действию высоких температур и внешней среды, содержащей каталитическое количество железа, что в высокой степени активизирует их окисление. Такое окисление, если с ним не бороться, способствует образованию коррозионных кислотных продуктов, углеродистых отложений, нагарообразований, смол и других нерастворимых в масле продуктов и может привести к потере указанных физических и трибологических свойств данных смазочных материалов. Подобные продукты окисления могут привести к образованию вредных отложений на важных деталях двигателя, таких, как поршни, втулки поршней, клапаны и толкатели клапанов. Поэтому существует установившаяся практика включать в смазочные материалы присадки для сдерживания образования отложений и антиокислители для предотвращения, по крайней мере, до некоторой степени, окисления, чтобы повысить период эксплуатационной долговечности смазочных материалов.
Композиции смазочных материалов, содержащие различные вторичные диариламины в качестве антиокислителей, широко известны в данной области. Известно также использование 1,4-бензолдиаминов, что показано в патентах США №2718501, 2883362, 3211793, 3304285 и 5711767, публикациях США №№2006/0128574, 2006/0189824 и 2007/0006855, GB1296592 и GB0835826 и JP59020392, полное содержание и раскрытие которых включено здесь ссылкой. В большинстве случаев 1,4-бензолдиамины использовали в качестве стабилизаторов моторных масел и антиозонантов и антиокислителей для резины. Было описано несколько 1,3-бензолдиаминов, применимых для использования в качестве антиокислителей.
В патенте США №2541642 описаны метафенилендиамин, N1,N3-диметилметафенилендиамин и лаурилметафенилендиамин в качестве антиокислителей, применимых для композиций смазочных масел, для использования в условиях, в которых может иметь место катализируемая железом окислительная реакция. Аналогичным образом описаны N,N'-диметилортофенилендиамин, N,N'-дициклогексилпарафенилендиамин и различные ди- и тетра-н-алкилпарафенилендиамины.
В патенте США № 2857424 описано получение солей щавелевой кислоты стабилизирующих топливо N,N'-диалкилпарафенилендиаминов в качестве способа сделать присадки менее токсичными. Описано получение оксалатной соли N,N'-дициклогексилпарафенилендиамина. Предполагается получение оксалатных солей других, точно не установленных дициклоалкилорто-, мета- и парафенилендиаминов.
Obester, A.E. et al., 45 CAN. J. CHEM. 195-201 (1967), в качестве части программы поиска антиозонантов для резины получил 39 новых фенилендиаминов, не являющихся сенсибилизаторами, или дерматотоксичными. В некоторых соединениях атом азота N'-фенилендиамина различным образом конденсирован с пирролидиновым, пиперидиновым, гексаметилениминовым (гомопиперидиновым), морфолиновым, или 2,6-диметилморфолиновым циклом. В каждом случае получали N-циклогексильное соединение.
В патенте США № 3402201 в качестве стабилизатора для органических материалов, в частности, резины, описан N,N'-дициклооктил-п-фенилендиамин, и приводится пример его использования в качестве стабилизатора бензина. Предполагается аналогичное использование N,N'-дициклооктил-о- и м-фенилендиаминов.
Makogon A. N. et. al., 12 KHIMICHESKAYA PROMYSHLENNOST, SERIYA: METODY ANALIZA I KONTROLYA KACHESTVA PRODUKTSII V KHIMICHESKOI PROMYSHLENNOSTI 18-21 (1980) описывает характеристику продуктов реакции N,N'-диалкилпарафенилендиаминов, полученных каталитическим окислением 4-аминодифениламина С7-С9 спиртами.
В патенте США №4487759 описано использование некоторых третичных фенилендиаминов, имеющих структуру:
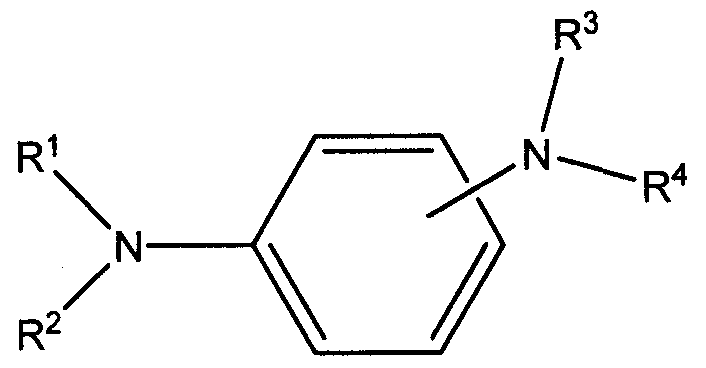
В частности, N,N',N'-триалкил-N-фенилпарафенилендиамины (например, N,N'-дидецил-N'-октил-N-фенилпарафенилендиамин) используют в качестве светостабилизаторов для ненасыщенных феромонов насекомых, которые содержатся в микроинкапсулированной системе доставки.
В патенте США №5207939 и 5312461 описаны некоторые продукты реакции основания Манниха моно-, или диалкилфенилендиаминов, альдегида, или кетона и стерически затрудненного фенола, которые можно использовать в антиокислительном количестве в смазочных маслах, густых смазках и топливных композициях. Конкретно, соединения данных фенилендиаминов имеют формулу:
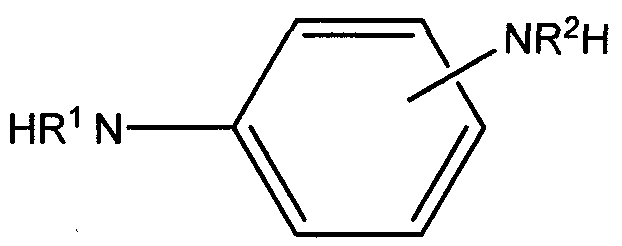
В японском патенте №59-020392 описана смазочная композиция, содержащая N,N'-дивторбутилпарафенилендиамин для штамповки масляных баков. Данная смазочная композиция смазки включает также стерически затрудненный фенольный антиокислитель.
Вышеупомянутые раскрытия включены здесь в виде ссылки.
Несмотря на то, что известно, что фенилендиамины эффективны в качестве антиокислителей, было найдено, что данные соединения коммерчески невыгодны, поскольку присутствие подобных соединений, при использовании их в количествах, которые обычно используются для обеспечения антиокислительной активности, оказывает неблагоприятные воздействия в отношении поршневых отложений и борьбы с нагарообразованием, а также проявляет агрессивные свойства по отношению к фторкаучуковым материалам для герметизации двигателя. Эти неблагоприятные воздействия особенно очевидны в случае фенилендиаминовых соединений с большим содержанием азота (соединений со сравнительно небольшим количеством гидрокарбильных заместителей). В недавних спецификациях смазочных масел для смазочных масел для дизельных двигателей легковых автомобилей (PCDO), установленных фирмами-производителями комплектного оборудования (OEMs), требовались сниженные концентрации фосфорсодержащего смазочного материала (например, менее 800 ч. на млн.). В настоящее время в спецификациях смазочных масел для смазочных масел для сверхмощных дизельных двигателей (HDD) отсутствует ограничение содержания фосфора, хотя предполагается, что в следующем поколении спецификации смазочных материалов (например, API CJ-4) оно будет. Ожидаемые пределы содержания фосфора (такие, как 1200 ч. на млн., или менее) и сокращения допустимых количеств сульфатированной золы (SASH) и серы ограничат количество диалкилдитиофосфата цинка (ZDDP), одного из наиболее рентабельных противоизносных/антиокислительных соединений, которые может использовать составитель смазочных материалов.
Изложение сущности настоящего изобретения
В первом аспекте настоящего изобретения предоставлен способ алкилирования соединения 1,3-бензолдиамина, включающий введение во взаимодействие первого карбонильного соединения с соединением 1,3-бензолдиамина, с образованием промежуточного соединения, где первое карбонильное соединение замещено по соответствующим атомам азота 1,3-бензолдиамина, и введение во взаимодействие второго карбонильного соединения с данным промежуточным соединением в присутствии водорода и катализатора гидрирования, с получением алкилированного 1,3-бензолдиамина, где второе карбонильное соединение замещено по центральному ароматическому циклу алкилированного 1,3-бензолдиамина. Первое и второе карбонильные соединения выбирают из числа альдегидов и кетонов.
Во втором аспекте настоящего изобретения предоставлено соединение, имеющее общую формулу:
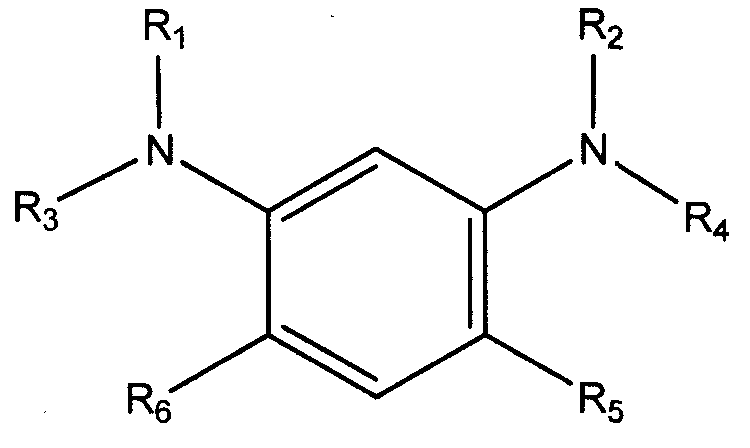
в которой R1 и R2 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло; R3 и R4 независимо выбирают из группы, состоящей из водорода, С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила и С5-С20 гетероцикло; и R5 и R6 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом.
В третьем аспекте настоящего изобретения предоставлено соединение, имеющее общую формулу:
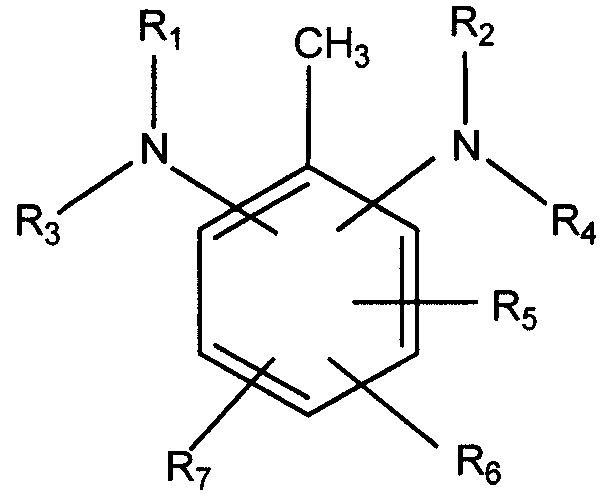
R1 и R2 независимо выбирают из группы, состоящей из С1-С36 алкила, С2-С36 алкенила, С4-С36 циклоалкила, С5-С36 арила, С5-С36 гетероцикло, структуры:
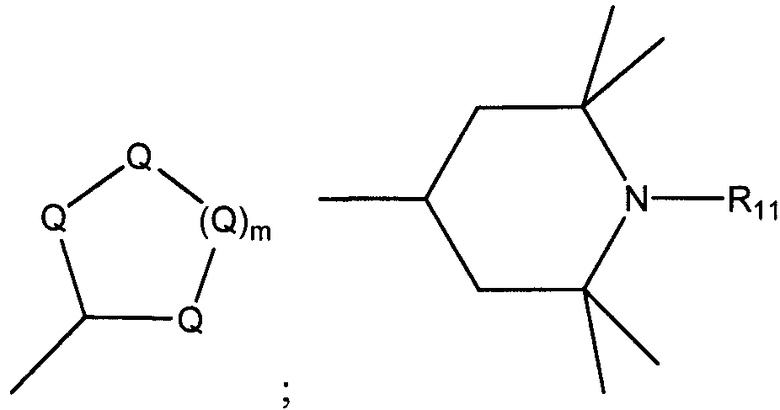 ; и -R12CO2R13;
; и -R12CO2R13;
R3 и R4 независимо выбирают из группы, состоящей из водорода, С1-С36 алкила, С2-С36 алкенила, С4-С36 циклоалкила, С5-С36 арила, С5-С36 гетероцикло, структуры:
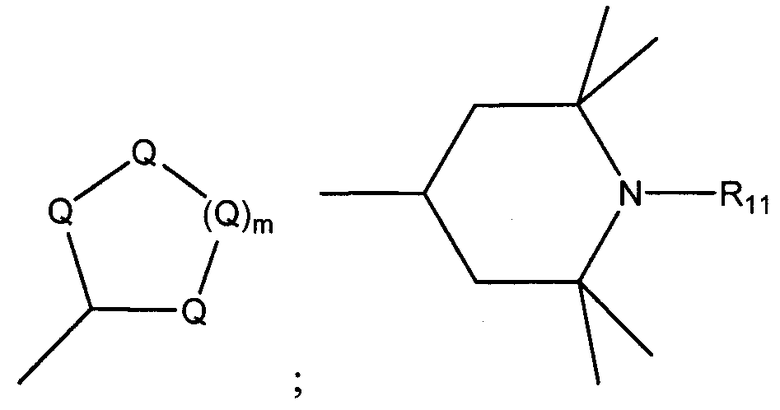 ; и -R12CO2R13;
; и -R12CO2R13;
в которых m является целым числом от 1 до 8, а каждый Q представляет собой С(R9)(R10), где каждый R9 и R10 независимо выбирают из группы, состоящей из водорода, галогена, С1-С36 алкила, С2-С36 алкенила, С4-С36 циклоалкила, С5-С36 арила и С5-С36 гетероцикло;
где R11 выбирают из группы, состоящей из водорода, кислорода, галогена, Н, С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арил, С5-С20 гетероцикло; и
где R12 представляет собой С1-С20 алкильную, или алкенильную группу, а R13 выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арил, С5-С20 гетероцикло; при условии, что R12 не является -СН2СН2-, или -СН2СН(СН3)-; а
R5, R6, и R7 независимо выбирают из группы, состоящей из С1-С36 алкила, С2-С36 алкенила, С4-С36 циклоалкила, С5-С36 арила, С5-С36 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5, R6, R7 и R8 не является водородом,
при условии, что амины расположены в центральном ароматическом цикле в 1,3-положении друг относительно друга.
В одном из вариантов осуществления 1,3-бензолдиамин получают из толуолдиамина, выбранного из группы, состоящей из 2,4-толуолдиамина, 2,6-толуолдиамина и 2,5-толуолдиамина.
В четвертом аспекте настоящего изобретения предоставлен способ алкилирования соединения 1,3-бензолдиамина, включающий предоставление карбонильного соединения, выбранного из группы, состоящей из альдегида общей формулы:
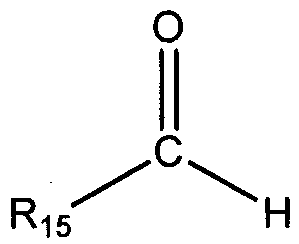
и кетона общей формулы:
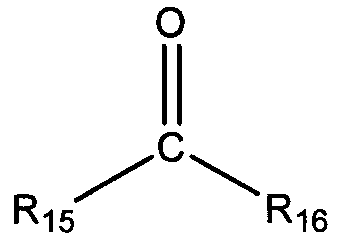
в которых R15 и R16 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло и циклического соединения, полученного путем конденсации R15 и R16 с образованием С4-С20 циклоалкила, С5-С20 арила, или С5-С20 гетероцикло; и введение во взаимодействие данного карбонильного соединения с соединением 1,3-бензолдиамина в присутствии водорода и катализатора гидрирования с получением структуры общей формулы:
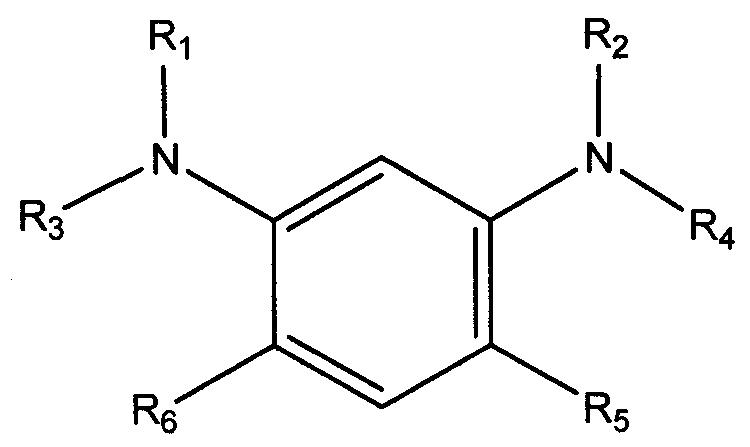
в которой R1 и R2 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло; R3 и R4 независимо выбирают из группы, состоящей из водорода, С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила и С5-С20 гетероцикло; и R5 и R6 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом.
В пятом аспекте настоящего изобретения предоставлен способ алкилирования соединения 1,3-бензолдиамина, включающий предоставление первого карбонильного соединения, выбранного из группы, состоящей из альдегида общей формулы:
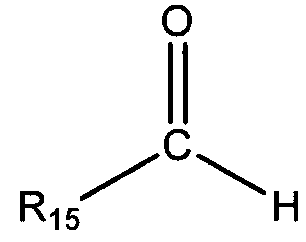
и кетона общей формулы:
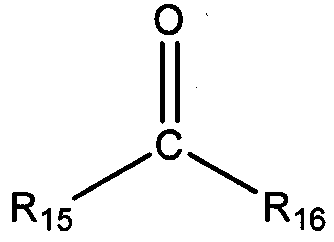
в которых R15 и R16 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло и циклического соединения, полученного путем конденсации R15 и R16 с образованием С4-С20 циклоалкила, С5-С20 арила, или С5-С20 гетероцикло;
предоставление второго карбонильного соединения, выбранного из альдегида общей формулы:
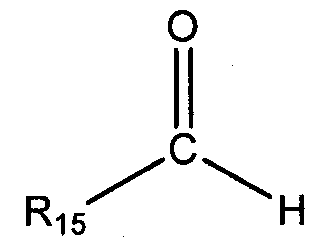
и кетона общей формулы:
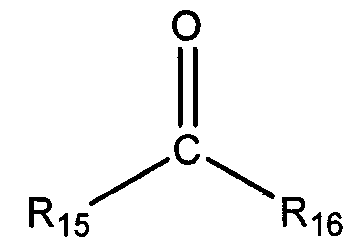
в которых R15 и R16 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло и циклического соединения, полученного путем конденсации R15 и R16 с образованием С4-С20 циклоалкила, С5-С20 арила, или С5-С20 гетероцикло, где первое карбонильное соединение отличается от второго карбонильного соединения; введение во взаимодействие первого карбонильного соединения с соединением 1,3-бензолдиамина в присутствии водорода и катализатора гидрирования с получением промежуточного соединения, имеющего общую формулу, выбранную из группы, состоящей из:
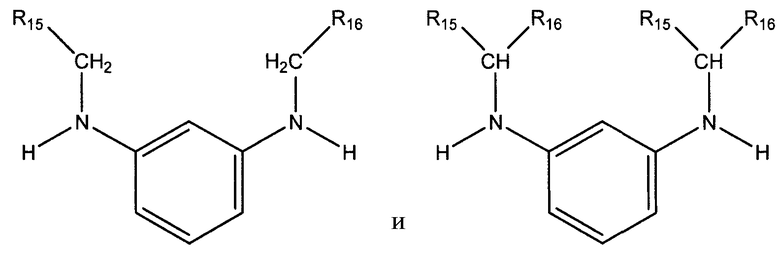 и
и
введение во взаимодействие второго карбонильного соединения с данным промежуточным соединением в присутствии водорода и катализатора гидрирования с получением соединения алкилированного 1,3-бензолдиамина, имеющего общую формулу, выбранную из группы, состоящей из:
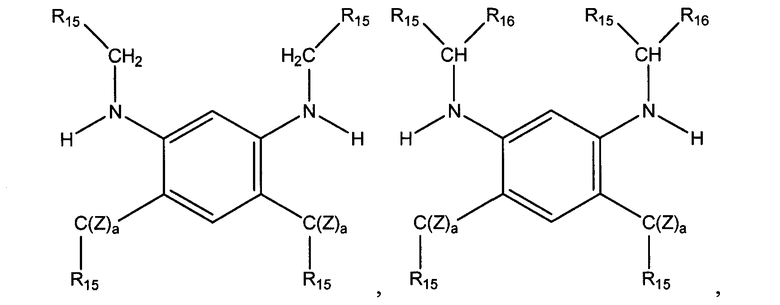
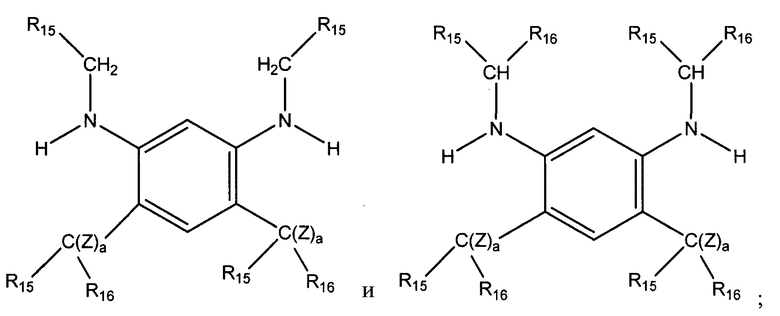
в которых Z=H, а а=0, 1, или 2.
В шестом аспекте настоящего изобретения предоставлена композиция смазочного масла, включающая: по меньшей мере, один базовый компонент смазочной вязкости в количестве от 80 масс.% до 99,99 масс.% из расчета на общую массу композиции, и антиокислитель в количестве от 0,01 масс.% до 6 масс.% из расчета на общую массу композиции, по меньшей мере, при этом данный антиокислитель включает, по меньшей мере, одно соединение структуры (I), имеющее общую формулу:
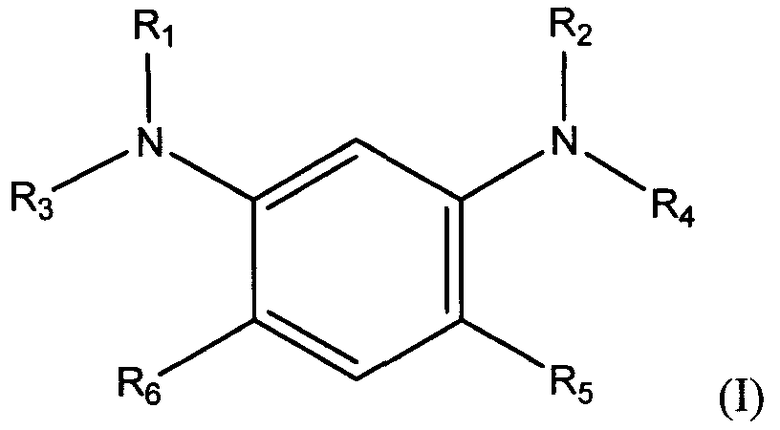
в которой R1 и R2 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила, С5-С20 гетероцикло; R3 и R4 независимо выбирают из группы, состоящей из водорода, С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила и С5-С20 гетероцикло; а R5 и R6 независимо выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арил, С5-С20 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом.
В седьмом аспекте настоящего изобретения предоставлен N1,N3-диалкил-4,6-диалкил-1,3-бензолдиамин. В одном из вариантов осуществления N1,N3-диалкил-4,6-диалкил-1,3-бензолдиамин включает N1,N3-дициклогексил-4,6-диалкил-1,3-бензолдиамин, такой, как N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамин.
В восьмом аспекте настоящего изобретения предоставлена композиция смазочного масла, включающая: по меньшей мере, один базовый компонент смазочной вязкости в количестве от 80 масс.% до 99,99 масс.% из расчета на общую массу композиции, и N1,N3-дициклоалкил-4,6-диалкил-1,3-бензолдиамин в количестве от 0,01 масс.% до 6 масс.% из расчета на общую массу композиции.
Подробное описание предпочтительных вариантов осуществления
Введение
В целом, настоящее изобретение относится к алкилированным 1,3-бензолдиаминам и способу алкилирования 1,3-бензолдиаминов. В одном из вариантов осуществления 1,3-бензолдиамин алкилируют альдегидом, или кетоном в присутствии восстановителя с получением вторичных аминогрупп. Необязательно, 1,3-бензолдиамин вводят во взаимодействие с альдегидом, или кетоном с использованием каталитического гидрирования. В любом случае, происходит селективное алкилирование атомов азота 1,3-бензолдиамина, а не его бензольного компонента. После этого полученный продукт N1,N3-диалкилированного-1,3-бензолдиамина вводят во взаимодействие с альдегидом, или кетоном с использованием каталитического гидрирования. Несмотря на то, что можно было бы аналогичным образом ожидать, что на стадии второго алкилирования будут алкилироваться аминные группы N1,N3-диалкилированного-1,3-бензолдиамина, к удивлению и неожиданно было найдено, что в отличие от стадии первого алкилирования, на стадии второго алкилирования происходит селективное алкилирование центрального ароматического кольца алкилированного-1,3-бензолдиамина. Таким образом, в данном способе предпочтительно образуются N1,N3-диалкилированные-4,6-диалкилированные-1,3-бензолдиамины, а не N1,N1,N3,N3-алкилированные-1,3-бензолдиамины.
Новые алкилированные бензолдиамины
В соответствии с вариантами осуществления настоящего изобретения, значительное сдерживание количества отложений было найдено не только в случае 1,4-замещенных бензолдиаминов, но также и для 1,2- и 1,3-замещенных бензолдиаминов. Кроме того, было найдено, что бензолдиамины с замещением в центральном ароматическом кольце являются высокоактивными агентами для сдерживания образования отложений.
В целом, композиции в соответствии с вариантами осуществления изобретения включают жидкость, подлежащую окислительному разложению, и количество, по меньшей мере, одной присадки на основе N-замещенного бензолдиамина, достаточное для стабилизации данной жидкости в отношении образования отложений. В одном из вариантов осуществления N-замещенный бензолдиамин находится в форме свободного основания, или растворимой в масле соли. Добавка на основе N-замещенного бензолдиамина имеет формулу:
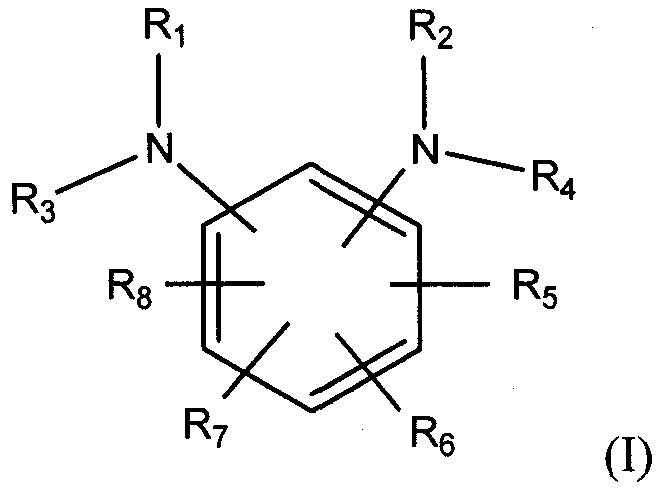
R1 и R2 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С36 алкила, линейного или разветвленного С2-С36 алкенила, замещенного или незамещенного С4-С36 циклоалкила, замещенного или незамещенного С5-С36 арила, замещенного или незамещенного С5-С36 гетероцикло, структуры:
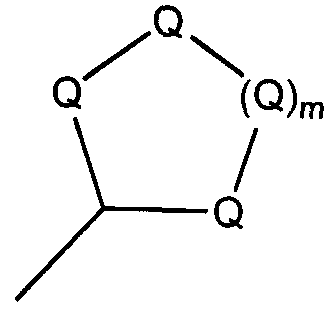
m является целым числом от 1 до 8, а каждый Q представляет собой (С)(R9)(R10), где каждый R9 и R10 независимо выбирают из группы, состоящей из водорода, галогена, линейного или разветвленного С1-С36 алкила, линейного или разветвленного С2-С36 алкенила, замещенного или незамещенного С4-С36 циклоалкила, замещенного или незамещенного С5-С36 арила и замещенного или незамещенного С5-С36 гетероцикло;
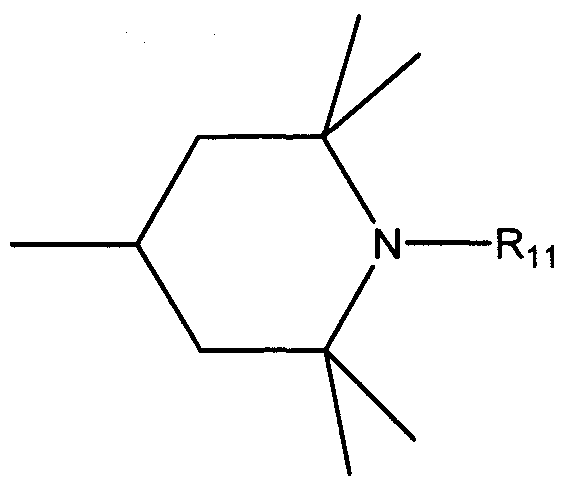
в которой R11 выбирают из группы, состоящей из водорода, кислорода, галогена, Н, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло; и
-R12CO2R13, где R12 представляет собой линейную, или разветвленную С1-С20 алкильную, или алкенильную группу, а R13 выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло; при условии, что R12 не является -СН2СН2-, или -СН2СН(СН3)-.
R3 и R4 независимо выбирают из группы, состоящей из водорода, линейного или разветвленного С1-С36 алкила, линейного или разветвленного С2-С36 алкенила, замещенного или незамещенного С4-С36 циклоалкила, замещенного или незамещенного С5-С36 арила, замещенного или незамещенного С5-С36 гетероцикло, структуры:
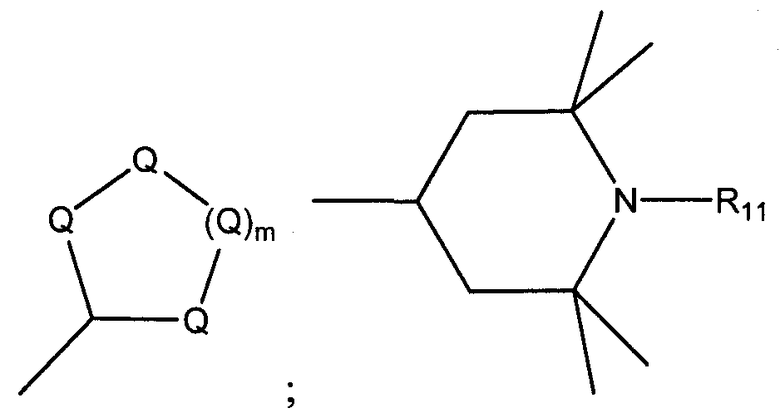
в которых Q, m и R11 определены выше, и -R12CO2R13, где R12 и R13 определены выше.
R5, R6, R7 и R8 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С36 алкила, линейного или разветвленного С2-С36 алкенила, замещенного или незамещенного С4-С36 циклоалкила, замещенного или незамещенного С5-С36 арила, замещенного или незамещенного С5-С36 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5, R6, R7 и R8 не является водородом.
В одном из вариантов осуществления амины расположены в центральном ароматическом кольце в 1,3-положении друг относительно друга.
Циклоалкильная, арильная и гетероциклильная группы могут быть замещены атомами галогена, линейным или разветвленным С1-С20 алкилом и линейным или разветвленным С2-С20 алкенилом. В одном из вариантов осуществления циклоалкильная, арильная и гетероциклильная группы могут быть замещены линейными или разветвленными С1-С12 алкильными группами. Атомы галогена можно выбрать из группы, состоящей из F, Cl, Br и I.
В одном из вариантов осуществления алкильная, алкенильная, циклоалкильная, арильная, или гетероциклильная группы могут содержать один, или более гетероатомов, выбранных из группы, состоящей из N, O и S.
Репрезентативные примеры алкильных групп для использования здесь в качестве любой из R групп включают, например, радикал с линейной или разветвленной углеводородной цепью, содержащий от 1 до 36, например, от 1 до 20 атомов углерода, например, метил, этил, н-пропил, 1-метилэтил (изопропил), н-бутил, изобутил, вторбутил, 1,3-диметилбутил, 1,4-диметилпентил, н-пентил, изопентил, 1,5-диметилгексил и гексил, и так далее, их смеси и изомеры и тому подобное.
Репрезентативные примеры алкенильных групп для использования здесь в качестве любой из R групп включают, например, радикал с линейной или разветвленной углеводородной цепью, содержащий от 2 до 36, например, от 2 до 20 атомов углерода, например, этилиден, пропенил, 2-метилпропенил, бутенил, пентенил, гексенил, и так далее, их смеси и изомеры и тому подобное. Подобные алкенильные группы могут также включать аллил и метилаллил. Алкенильная группа может иметь одну, или более двойных связей и может включать диалкенильные группы, триалкенильные группы, тетраалкенильные группы и так далее.
Репрезентативные примеры циклоалкильных групп для использования здесь в качестве любой из R групп включают, например, замещенные или незамещенные циклы, содержащие от 4 до 36, например, от 4 до 20 атомов углерода, например, циклобутил, циклопентил, циклогексил, н-метилциклогексил, н-диметилциклогексил, н-этилциклогексил, циклогептил, циклооктил и так далее, их смеси и изомеры и тому подобное.
Репрезентативные примеры арильных групп для использования здесь в качестве любой из R групп включают, например, замещенные или незамещенные ароматические циклы, содержащие от 5 до 36, например, от 5 до 20 атомов углерода, например, фенил, н-метилфенил, н-диметилфенил, н-этилфенил, бензил, нафтил, тетрагидронафтил, инденил, дифенил и так далее, их смеси и изомеры и тому подобное.
Репрезентативные примеры гетероциклических групп для использования здесь в качестве любой из R групп включают, например, замещенные, или незамещенные циклы, содержащие от 5 до 36, например, от 5 до 20 атомов углерода, например, фурфурил и тетрагидрофурфурил.
В одном из вариантов осуществления имеется алкилированный 1,3-бензолдиамин формулы:
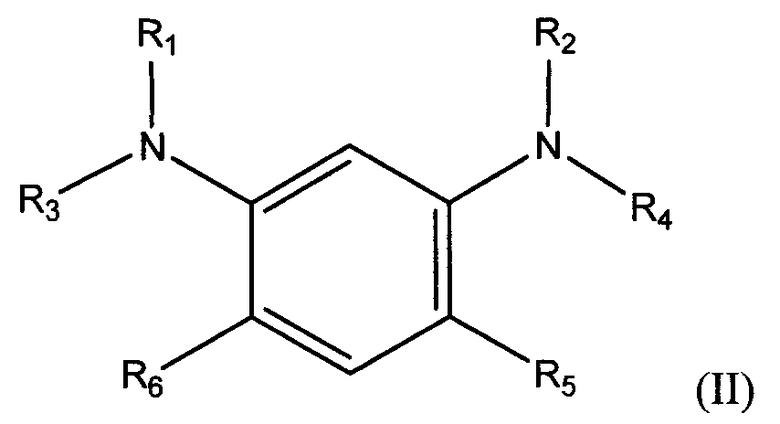
в которой R1 и R2 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло; R3 и R4 независимо выбирают из группы, состоящей из водорода, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила и замещенного или незамещенного С5-С20 гетероцикло; а R5 и R6 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом. В одном из вариантов осуществления R3 и R4 предпочтительно являются водородом.
В одном из вариантов осуществления R5 и R6 представляют собой один и тот же заместитель, такой, как линейная, или разветвленная алкильная группа, содержащая от 3 до 6 атомов углерода, или алкилзамещенная арильная группа, содержащая от 5 до 8 атомов углерода. Аналогичным образом, R3 и R4 могут представлять собой один и тот же заместитель, такой, как циклогексил, или 1,3-диметилбутил, и R5 и R6 могут представлять собой один и тот же заместитель, такой, как водород.
Предпочтительно, алкилированный 1,3-бензолдиамин имеет, или имеет в среднем, содержание азота от около 2 до около 15 массовых процентов (масс.%), например, от около 5 до около 11 масс.%, от около 5,5 до около 10,5 масс.% из расчета на общую массу алкилированного 1,3-бензолдиамина.
В одном из вариантов осуществления алкилированный 1,3-бензолдиамин настоящего изобретения имеет общую формулу:
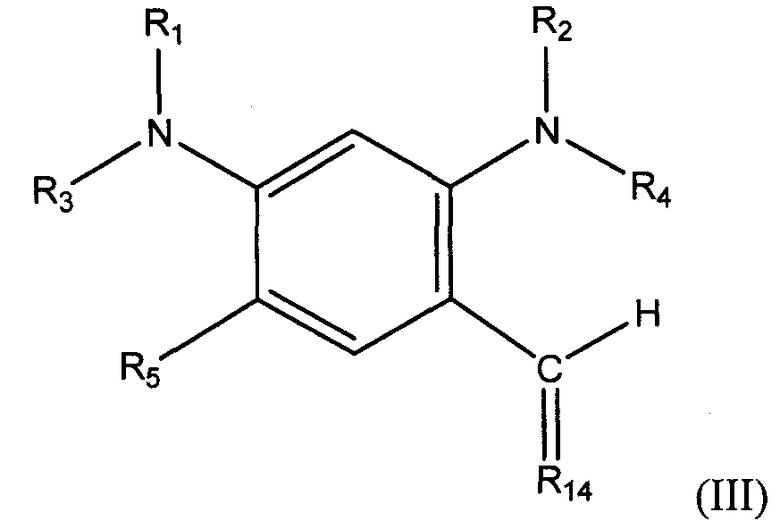
в которой R1, R2, R3, R4 и R5 определены выше, а R14 выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арил и С5-С20 гетероцикло.
В одном из вариантов осуществления алкилированный 1,3-бензолдиамин настоящего изобретения имеет общую формулу, выбранную из группы, состоящей из:
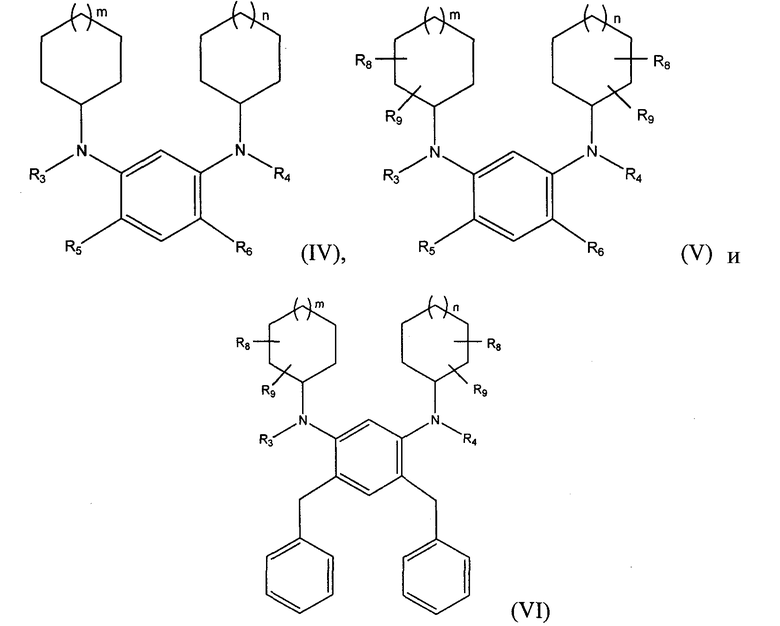
в которых m и n независимо равны 0, 1, 2, или 3, R3, R4, R5 и R6 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом; а R8 и R9 независимо выбирают из группы, состоящей из водорода, галогена, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила и замещенного или незамещенного С5-С20 гетероцикло. В одном из вариантов осуществления R5 и R6 оба не являются водородом. Либо один, либо оба R8 и R9 могут являться галогеном.
В следующем варианте осуществления алкилированный 1,3-бензолдиамин настоящего изобретения имеет общую формулу:
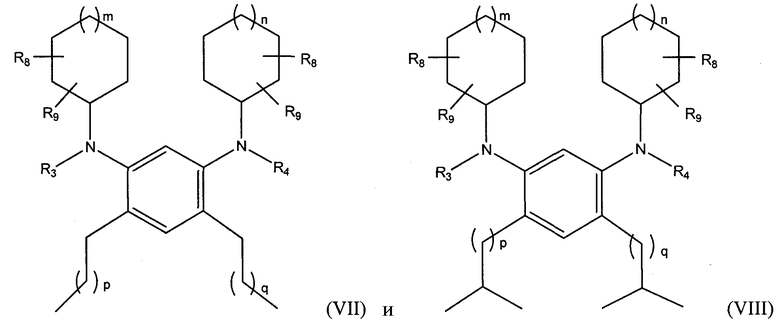
в которых m и n независимо представляют собой целые числа, равные 0, 1, 2, или 3, p и q независимо представляют собой целые числа от 0 до 18, а R3, R4, R8 и R9 независимо выбирают из группы, состоящей из водорода, галогена, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, и замещенного или незамещенного С5-С20 гетероцикло. Либо один, либо оба R8 и R9 могут являться галогеном.
В следующем варианте осуществления алкилированный 1,3-бензолдиамин настоящего изобретения имеет общую формулу, выбранную из группы, состоящей из:
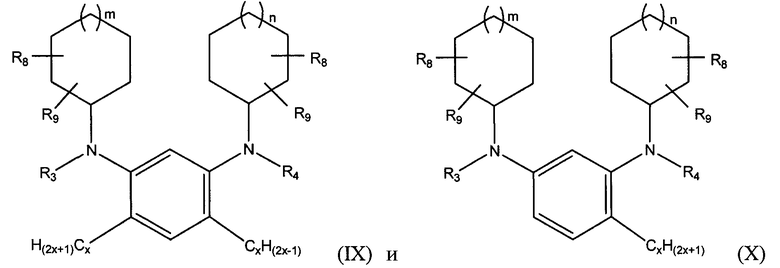
в которых m и n независимо равны 0, 1, 2, или 3, х является целым числом от 2 до 18, а R3, R4, R8 и R9 независимо выбирают из группы, состоящей из водорода, галогена, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло.
В следующем варианте осуществления алкилированный 1,3-бензолдиамин настоящего изобретения имеет общую формулу, выбранную из группы, состоящей из:
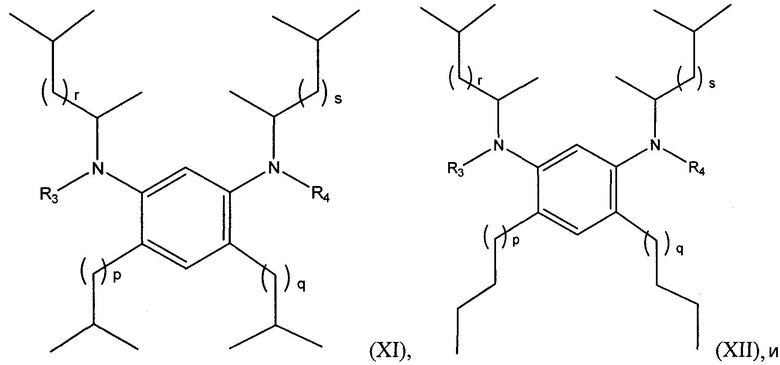
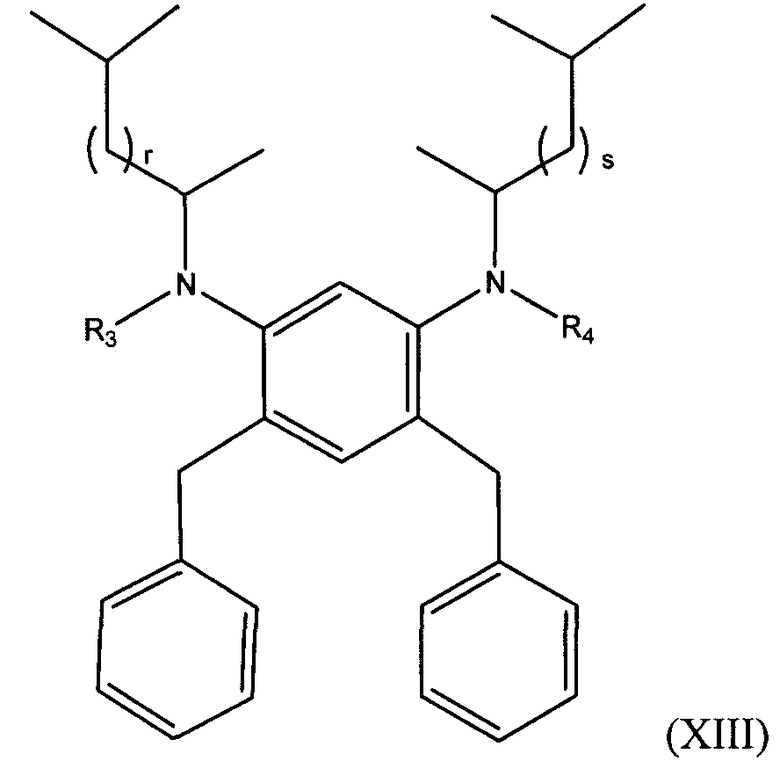
в которых p и q независимо представляют собой целые числа от 0 до 18, r и s независимо представляют собой целые числа, равные 1, или 2, а R3 и R4 независимо выбирают из группы, состоящей из водорода, галогена, линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, замещенного или незамещенного С4-С20 циклоалкила, замещенного или незамещенного С5-С20 арила, замещенного или незамещенного С5-С20 гетероцикло.
Следует понимать, что алкилированный 1,3-бензолдиамин настоящего изобретения может иметь общую формулу, выбранную из группы, состоящей из формулы (I)-(XIII).
В иллюстративном варианте осуществления алкилированный 1,3-бензолдиамин представляет собой бензолдиамин одной из следующих формул:
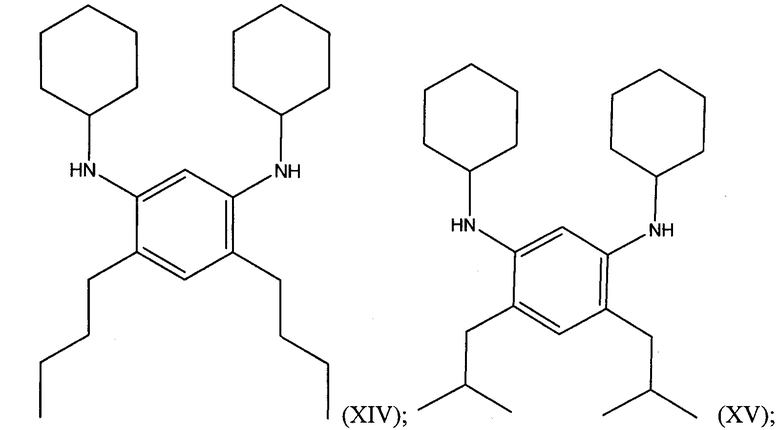
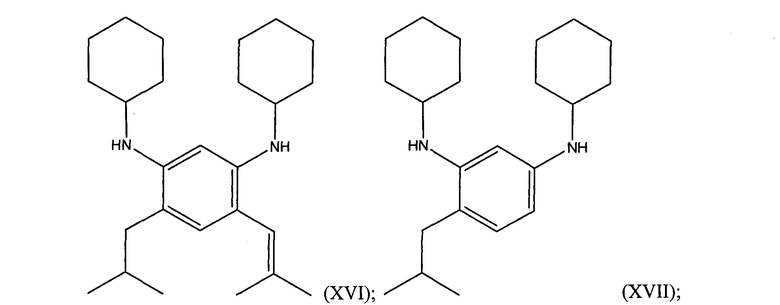
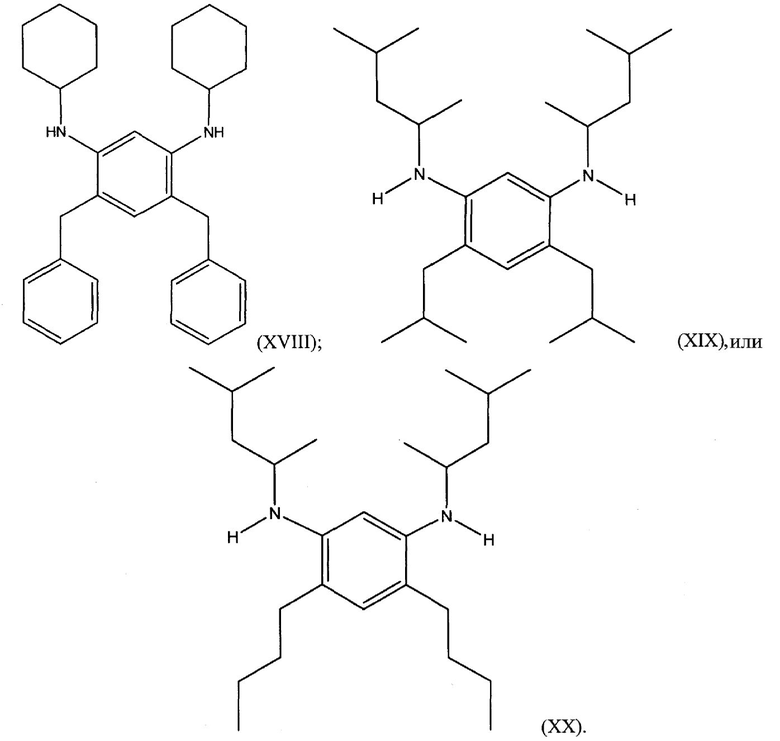
Алкилированные 1,3-бензолдиамины могут включать N1,N3-диалкил-4,6-диалкил-1,3-бензолдиамин, такой, как N1,N3-дициклогексил-4,6-диалкил-1,3-бензолдиамин, или N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамин. 4,6-Диалкильный заместитель выбирают из группы, состоящей из С1-С20 алкила, С2-С20 алкенила, С4-С20 циклоалкила, С5-С20 арила и С5-С20 гетероцикло.
Иллюстративные алкилированные 1,3-бензолдиамины настоящего изобретения включают, но не ограничиваются: N1,N3-дициклогексил-4-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этенил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропенил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутенил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутенил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептенил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бензил-1,3-бензолдиамином, N1,N3-дициклогексил-4-фурфурил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-диметил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-диэтил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дипропил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дибутил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутенил-6-изобутил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дигептил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-диэтенил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дипропенил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-диизобутенил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дибутенил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дигептенил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дибензил-1,3-бензолдиамином, N1,N3-дициклогексил-4,6-дифурфурил-1,3-бензолдиамином, N1,N3-дициклопентил-4-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-этил-1,3-бензолдиамином, N1,N3-дициклопентил-4-пропил-1,3-бензолдиамином, N1,N3-дициклопентил-4-бутил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутил-1,3-бензолдиамином, N1,N3-дициклопентил-4-гептил-1,3-бензолдиамином, N1,N3-дициклопентил-4-этенил-1,3-бензолдиамином, N1,N3-дициклопентил-4-пропенил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутенил-1,3-бензолдиамином, N1,N3-дициклопентил-4-бутенил-1,3-бензолдиамином, N1,N3-дициклопентил-4-гептенил-1,3-бензолдиамином, N1,N3-дициклопентил-4-бензил-1,3-бензолдиамином, N1,N3-дициклопентил-4-фурфурил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-диметил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-диэтил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дипропил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дибутил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-диизобутил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутенил-6-изобутил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дигептил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-диэтенил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дипропенил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-диизобутенил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дибутенил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дигептенил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дибензил-1,3-бензолдиамином, N1,N3-дициклопентил-4,6-дифурфурил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бензил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-фурфурил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диметил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диэтил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дипропил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-6-изобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дигептил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диэтенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дипропенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диизобутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дигептенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибензил-1,3-бензолдиамином и N1,N3-(1,3-диметилбутил)-4,6-дифурфурил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бензил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-фурфурил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диметил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диэтил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дипропил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-6-изобутил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дигептил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диэтенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дипропенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-диизобутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибутенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дигептенил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4,6-дибензил-1,3-бензолдиамином и N1,N3-(1,3-диметилбутил)-4,6-дифурфурил-1,3-бензолдиамином.
В одном из вариантов осуществления изобретение направлено на композицию, включающую смесь двух, или более алкилированных 1,3-бензолдиаминов, выбранных из структур и соединений, указанных выше. Подобные смеси могут включать два различных алкилированных 1,3-бензолдиаминов в массовом соотношении, составляющем, например, от 5:4 до 4:1, например, от 5:3 до 3:1, или примерно 2:1. В иллюстративном варианте осуществления, данная смесь содержит N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамин и N1,N3-дициклогексил-4-изобутенил-6-изобутил-1,3-бензолдиамин в массовом соотношении от 5:4 до 4:1, например, от 5:3 до 3:1, или примерно 2:1.
В различных вариантах осуществления настоящее изобретение направлено на новые соединения алкилированных 1,3-бензолдиаминов, полученные из толуолдиаминов. Подходящие толуолдиамины включают 2,6-толуолдиамин, 2,4-толуолдиамин и 2,5-толуолдиамин. В таких вариантах осуществления толуолдиамин имеет общую формулу:
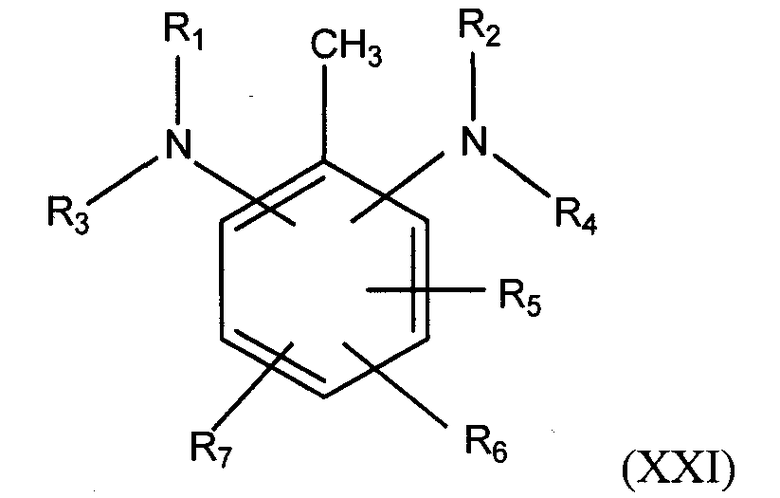
в которой R1, R2, R3, R4, R5, R6 и R7 определены выше, при условии, что амины расположены в центральном ароматическом кольце в 1,3-положении друг относительно друга.
В одном из вариантов осуществления соединение алкилированного бензолдиамина получено из 2,6-толуолдиамина(2-метил-1,3-бензолдиамина) и имеет общую формулу:
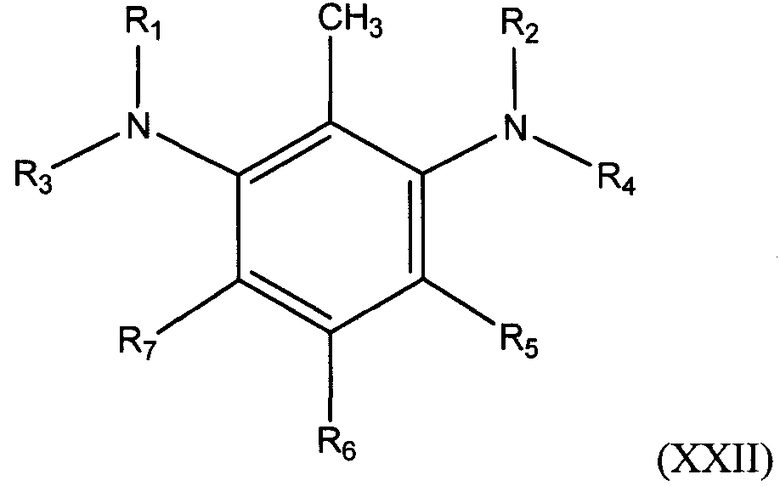
в которой R1, R2, R3, R4, R5, R6 и R7 определены выше.
В одном из вариантов осуществления соединение алкилированного бензолдиамина получено из 2,4-толуолдиамина(4-метил-1,3-бензолдиамина) и имеет общую формулу:
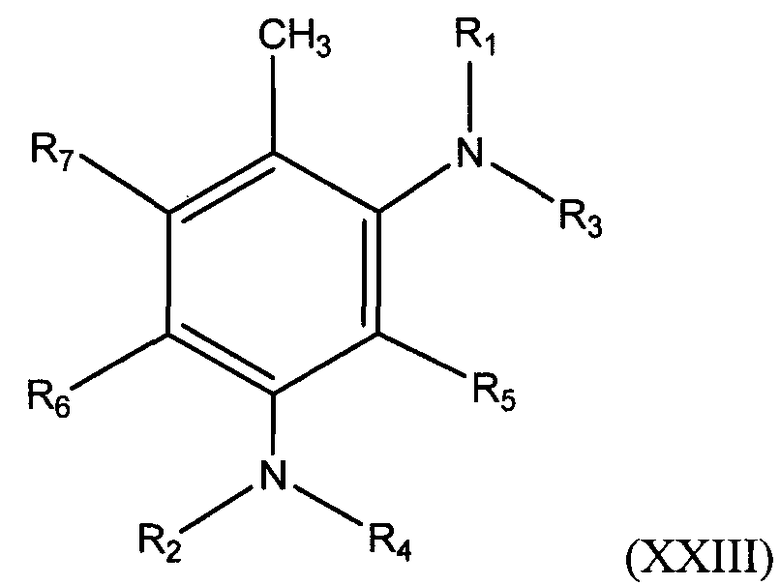
в которой R1, R2, R3, R4, R5, R6 и R7 определены выше.
В иллюстративном варианте осуществления алкилированный 1,3-бензолдиамин, полученный из толуола, представляет собой 1,3-бензолдиамин, имеющий следующую формулу:
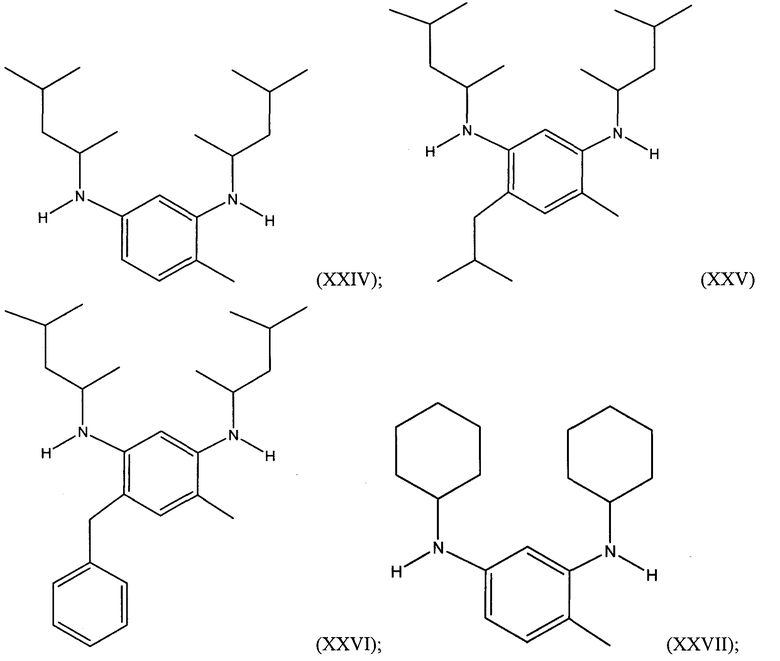
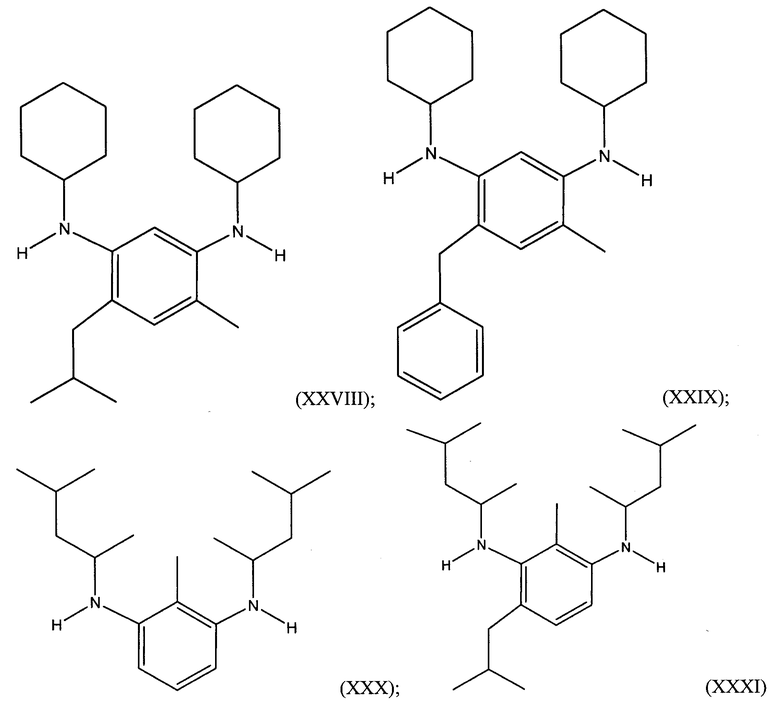
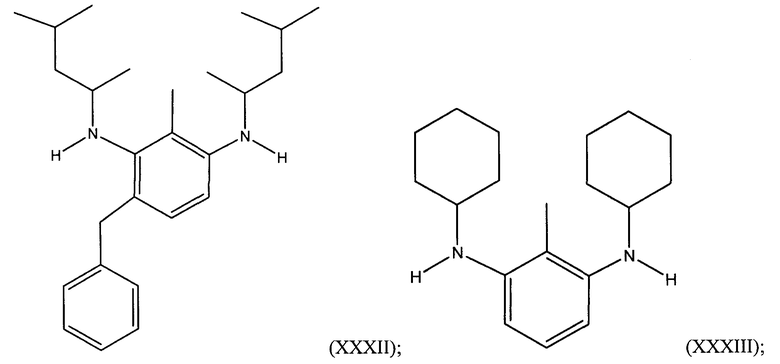
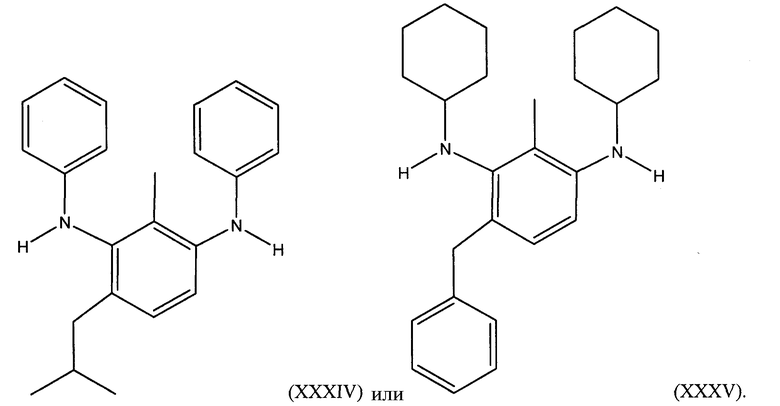
Иллюстративные алкилированные 1,3-бензолдиамины настоящего изобретения, полученные из толуола, включают, но не ограничиваются: N1,N3-дициклогексил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этенил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропенил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутенил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутенил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептенил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бензил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-фурфурил-2-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-этенил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-пропенил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-изобутенил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бутенил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-гептенил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-бензил-6-метил-1,3-бензолдиамином, N1,N3-дициклогексил-4-фурфурил-6-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-пропил-2-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-бутил-2-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутил-2-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутенил-2-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-пропил-4-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-бутил-4-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутил-4-метил-1,3-бензолдиамином, N1,N3-дициклопентил-4-изобутенил-4-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этенил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропенил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутенил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептенил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бензил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-фурфурил-2-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-этенил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-пропенил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-изобутенил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бутенил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-гептенил-6-метил-1,3-бензолдиамином, N1,N3-(1,3-диметилбутил)-4-бензил-6-метил-1,3-бензолдиамином и N1,N3-(1,3-диметилбутил)-4-фурфурил-6-метил-1,3-бензолдиамином.
Способы получения алкилированных 1,3-бензолдиаминов
В целом, настоящее изобретение относится также к способам получения алкилированных 1,3-бензолдиаминов. В одном из вариантов осуществления данный способ включает алкилирование N,N'-диалкилированного-1,3-бензолдиамина. Стадия алкилирования предпочтительно включает введение во взаимодействие N,N'-диалкилированного-1,3-бензолдиамина с карбонильным соединением, то есть альдегидом, или кетоном, и водородом в условиях каталитического гидрирования, эффективных для селективного алкилирования бензольного кольца N,N'-диалкилированного-1,3-бензолдиамина, предпочтительно, в его 4 и/или 6 положениях.
Использованный здесь термин алкилировать, или алкилирование, относится к добавлению заместителя, который содержит, главным образом, углеводородную структуру. Это включает, но не ограничивается, добавлением алкильной группы, алкенильной группы, циклоалкильной группы, арильной группы, или гетероциклильной группы. В одном из вариантов осуществления алкилирование может относиться к добавлению циклоалкильной или арильной группы, которая замещена алкильной группой и/или содержит один или более атомов галогена, или гетероатомов.
Способ получения 1,3-бензолдиаминов хорошо известен и может включать нитрование бензола азотной кислотой с последующим гидрированием. В одном из вариантов осуществления изобретение направлено на многостадийный способ алкилирования, в котором исходят из 1,3-бензолдиамина. В данном варианте осуществления 1,3-бензолдиамин алкилируют на стадии первого алкилирования, получая N,N'-диалкилированный-1,3-бензолдиамин путем восстановления каждого амина. Затем полученный N,N'-диалкилированный-1,3-бензолдиамин алкилируют на стадии второго алкилирования, вводя во взаимодействие N,N'-диалкилированный-1,3-бензолдиамин с карбонильным соединением с использованием каталитического гидрирования для селективного алкилирования бензольного кольца N,N'-диалкилированного-1,3-бензолдиамина, предпочтительно в его 4 и/или 6 положениях, получая конечный продукт N,N'-диалкилированного-4-алкилированного-1,3-бензолдиамина, или продукт N,N'-диалкилированного-4,6-диалкилированного-1,3-бензолдиамина.
На стадии первого алкилирования промежуточное соединение алкилированного 1,3-бензолдиамина можно получить при использовании либо восстановительного алкилирования, либо алкилирования путем каталитического гидрирования. Способы восстановительного алкилирования 1,3-бензолдиамина карбонильным соединением описаны у Abdel-Majid, A. F. et al., 61 J. ORG. CHEM. 3849-62 (1996), полнота которого включена путем ссылки. Специалисты в данной области поймут, что для достижения желательной реакции при варьировании исходных веществ может потребоваться корректировка стехиометрических соотношений, продолжительности реакции и температуры реакции.
Подходящие восстановители для подобных способов восстановительного алкилирования включают, например, триацетоксиборгидрид натрия (STAB-H), цианоборгидрид натрия, комплекс боран-пиридин, Ti(OiPr)4/NaBH3CN, Zn/AcOH, NaBH4/Mg(ClO4)2, Zn(BH4)2/ZnCl2 и боргидридные обменные смолы. В одном из вариантов осуществления на стадии первого алкилирования используют STAB-H.
В таких способах восстановительного алкилирования карбонильное соединение может включать альдегид общей формулы:
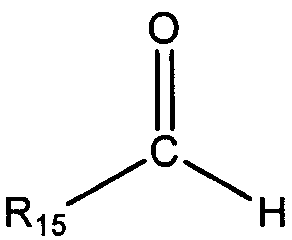
или кетон общей формулы:
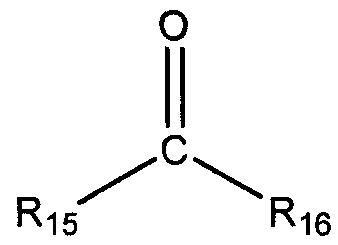
в которых R15 и R16 выбирают из любого R1-R8, определенного выше. В одном из вариантов осуществления R15 и R16 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, С4-С20 циклоалкила (например, циклобутила, циклопентила, циклогексила, циклогептила, циклооктила), С5-С20 арила и С5-С20 гетероцикло. Необязательно, R15 и R16 конденсированы с образованием циклического соединения, такого, как С4-С20 циклоалкил, С5-С20 арил, или С5-С20 гетероцикло. Иллюстративное циклическое соединение включает циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. В одном из вариантов осуществления кетон может представлять собой метилизобутилкетон (MIBK), метилизоамилкетон (MIAK), циклопентанон, или циклогексанон.
В некоторых вариантах осуществления в способе восстановительного алкилирования можно использовать один, или более растворителей. Подходящие растворители включают, например, ксилолы, 1,2-дихлорэтан, тетрагидрофуран и ацетонитрил. Растворители можно удалить из реакционной смеси, например, выпариванием при помощи роторного испарителя, или другим стандартным методом отделения.
Температура и продолжительность смешения могут изменяться в широких пределах в зависимости от использованных соединений. Например, к смеси 1,3-бензолдиамина и альдегида/кетона можно прибавлять восстановитель при температуре от 25°С до 80°С, например, от 40°С до 50°С, или примерно при 35°С, в течение от 1 часа до 10 часов, например, от 2 до 8 часов, или от 3 до 5 часов.
В другом варианте осуществления стадия первого алкилирования включает каталитическое гидрирование, при котором 1,3-бензолдиамин вводят во взаимодействие с карбонильным соединением, то есть альдегидом, или кетоном, в присутствии водорода и катализатора гидрирования, вместо описанного выше способа восстановительного алкилирования. В данном варианте осуществления 1,3-бензолдиамин и карбонильное соединение взаимодействуют в присутствии водорода и катализатора гидрирования. По аналогии со способом восстановительного алкилирования, можно синтезировать 1,3-бензолдиамины, алкилированные по атомам азота (то есть содержащие вторичные амины).
При таком каталитическом гидрировании карбонильное соединение может включать альдегид общей формулы
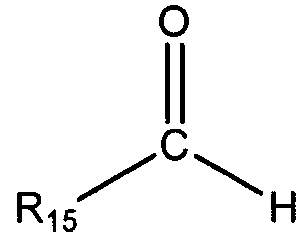
или кетон общей формулы:
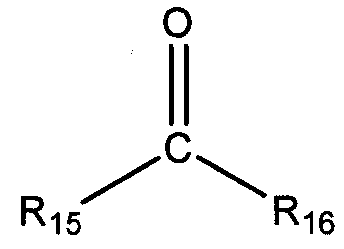
в которых R15 и R16 выбирают из любого R1-R8, определенного выше. В одном из вариантов осуществления R15 и R16 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, С4-С20 циклоалкила (например, циклобутила, циклопентила, циклогексила, циклогептила, циклооктила), С5-С20 арила и С5-С20 гетероцикло. Необязательно, R15 и R16 конденсированы с образованием циклического соединения, представляющего собой С4-С20 циклоалкил, С5-С20 арил, или С5-С20 гетероцикло, например, циклобутила, циклопентила, циклогексила, циклогептила, циклооктила. В одном из вариантов осуществления кетон может представлять собой MIBK, MIAK, циклопентанон, или циклогексанон.
Подходящие катализаторы гидрирования включают платиновые, палладиевые, родиевые, рутениевые, осмиевые, иридиевые, или никелевые катализаторы. В одном из вариантов осуществления катализатор включает катализатор на носителе. Носитель катализатора может включать, например, уголь, оксид алюминия, оксид кремния, алюмосиликаты и так далее.
Каталитическое гидрирование предпочтительно проводят в реакторе под избыточным давлением. В одном из вариантов осуществления избыточное давление в реакторе составляет 100-30000 килопаскаль (кПа) водорода, например, 500-10000 кПа, или 3500-5000 кПа.
Температура каталитического гидрирования предпочтительно изменяется в интервале от 20°С до 300°С, например, от 80°С до 250°С, или от 120°С до 220°С.
Как указывалось выше, на стадии первого алкилирования альдегид, или кетон селективно присоединяется к первичным аминогруппам 1,3-бензолдиамина и дает промежуточное соединение вторичного амина. Можно было бы ожидать, что последующее алкилирование данного промежуточного соединения, либо путем восстановительного алкилирования, либо путем гидрирования, аналогичным образом привело бы к селективному присоединению по положениям азота N,N'-диалкилированных-1,3-бензолдиаминов с образованием третичных аминов.
Однако, в настоящее время, к удивлению, и неожиданно было найдено, что каталитическое гидрирование промежуточного соединения N,N'-диалкил-1,3-бензолдиамина с карбонильным соединением, то есть альдегидом, или кетоном, приводит к селективному алкилированию бензольной группы, а не алкилированию аминогрупп, как показано далее в синтезе сравнения. В частности, алкилирование протекает специфично по 4 и/или 6 положениям центральной ароматической группы.
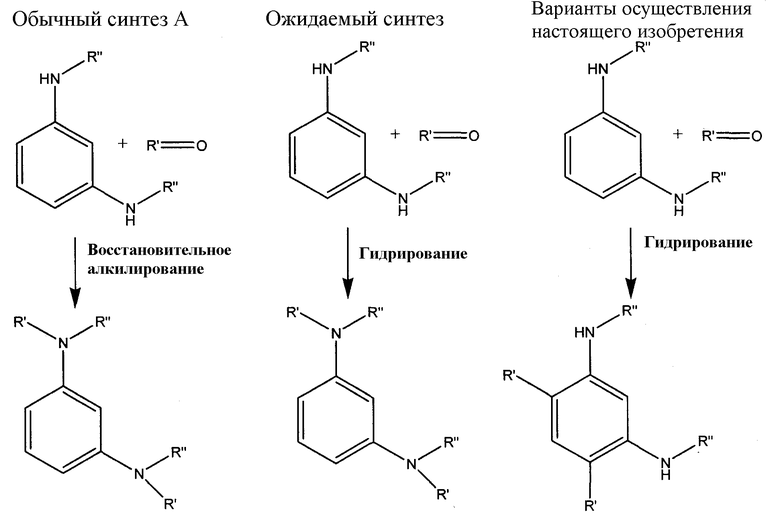
R' и R'' представляют собой любой подходящий заместитель из данной заявки.
Подходящие карбонильные соединения для каталитического гидрирования промежуточного соединения N,N'-диалкил-1,3-бензолдиамина включают альдегиды и кетоны со следующими структурами:
альдегид общей формулы
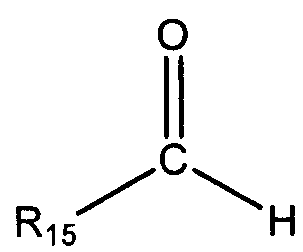
и кетон общей формулы:
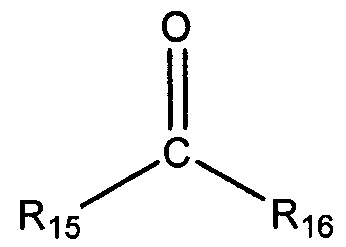
в которых R15 и R16 выбирают из любого R1-R8, определенного выше. В одном из вариантов осуществления R15 и R16 независимо выбирают из группы, состоящей из линейного или разветвленного С1-С20 алкила, линейного или разветвленного С2-С20 алкенила, С4-С20 циклоалкила (например, циклобутила, циклопентила, циклогексила, циклогептила, циклооктила), С5-С20 арила и С5-С20 гетероцикло. Необязательно, R15 и R16 конденсированы с образованием циклического соединения, например, циклобутила, циклопентила, циклогексила, циклогептила, циклооктила.
Молярные соотношения альдегида или кетона и промежуточного соединения N,N'-диалкил-1,3-бензолдиамина могут составлять от 5:1 до 1:5, например, от 3:1 до 1:3, или от 2:1 до 1:2.
При подобном каталитическом гидрировании подходящие катализаторы гидрирования включают платиновые, палладиевые, родиевые, рутениевые, осмиевые, иридиевые или никелевые катализаторы. В одном из вариантов осуществления катализатор включает катализатор на носителе. Носитель катализатора может включать, например, уголь, оксид алюминия, оксид кремния, алюмосиликаты и так далее.
Каталитическое гидрирование промежуточного соединения предпочтительно проводят в реакторе под избыточным давлением, давление в котором предпочтительно выше 220 кПа, например, выше 375 кПа, или выше 650 кПа. В выражении через интервалы в реактор необязательно нагнетают давление от 100-30000 кПа водорода, например, 500-10000 кПа, или 3500-5000 кПа.
Температура каталитического гидрирования предпочтительно изменяется в интервале от 20°С до 300°С, например, от 80°С до 250°С, или от 120°С до 220°С. В одном из вариантов осуществления каталитическое гидрирование для алкилирования центрального ароматического компонента данного промежуточного соединения можно проводить при более высокой температуре, чем каталитическое гидрирование для алкилирования первичных аминов. Более высокая температура может быть больше на величину от 10°С до 100°С, например, от 25°С до 75°С, или от 40°С до 60°С.
В одном из вариантов осуществления взаимодействие карбонильных соединений с 1,3-бензолдиамином включает два отдельных процесса каталитического гидрирования. Подобный способ может включать предоставление первого и второго карбонильных соединений из числа определенных выше формул альдегида и кетона, где первое карбонильное соединение отличается от второго карбонильного соединения. В одном из вариантов осуществления первое карбонильное соединение может представлять собой кетон, такой, как MIBK, MIAK, циклопентанон, или циклогексанон, а второе карбонильное соединение может представлять собой альдегид, такой, как изобутиральдегид, или бутиральдегид. Первое карбонильное соединение вводят во взаимодействие с соединением 1,3-бензолдиамина в определенных выше условиях каталитического гидрирования с получением промежуточного соединения, выбранного из группы, состоящей из:
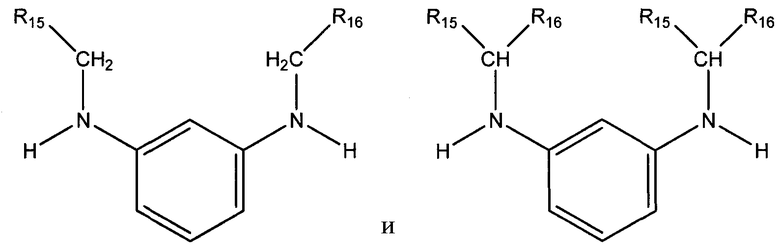
в которых R15 и R16 определены выше. Как показано, данное промежуточное соединение включает две вторичных аминогруппы. Затем второе карбонильное соединение вводят во взаимодействие с данным промежуточным соединением в определенных выше условиях каталитического гидрирования с получением соединения алкилированного 1,3-бензолдиамина общей формулы, выбранной из группы, состоящей из:
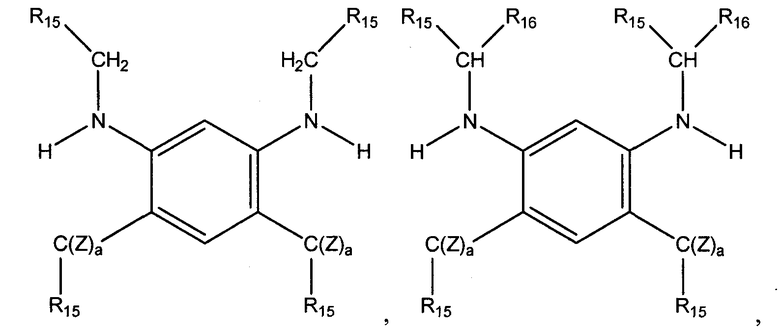
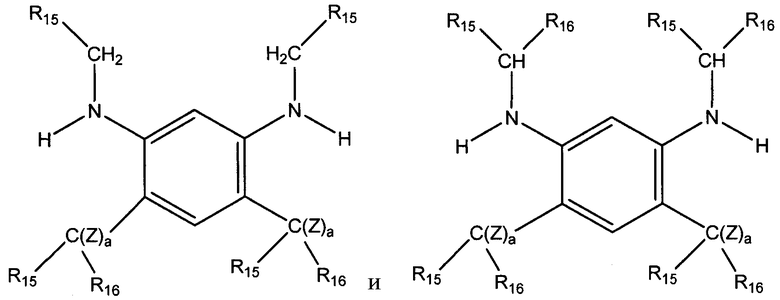
в которых R15 и R16 определены выше, Z=H, а а=0, 1, или 2. Следует понимать, что когда а равно 0, или 1, между С и соответствующей R группой может быть кратная связь.
В некоторых вариантах осуществления в способе изобретение происходит селективное алкилирование только по 4 положению, а не и по 4, и по 6 положениям бензольной группы. Селективному алкилированию по 4 положению может благоприятствовать, например, снижение количества альдегида, или кетона, доступного для взаимодействия с N,N'-диалкил-1,3-бензолдиамином. Например, молярные соотношения альдегида или кетона и N,N'-диалкил-1,3-бензолдиамина меньшие 2:1, например, меньшие 1,5:1, или меньшие 1,2:1, могут благоприятствовать моноалкилированию больше, чем диалкилированию. В выражении в виде интервалов, молярные соотношения альдегида или кетона и N,N'-диалкил-1,3-бензолдиамина могут составлять от 2:1 до 1:2, например, от 1,5:1 до 3:4, или от 1,2:1 до 5:6. Более низкие температуры и меньшая продолжительность реакции, например, менее 3, менее 2, или менее 1 часа, также могут благоприятствовать моноалкилированию.
В одном из вариантов осуществления толуолдиамин также может образовывать алкилированный 1,3-бензолдиамин при использовании а) восстановительного алкилирования, или каталитического гидрирования с алкилированием соответствующих аминогрупп толуолдиамина, и b) каталитического гидрирования с алкилированием центрального ароматического кольца при использовании карбонильных соединений описанного выше толуолдиамина. Для получения алкилированных 1,3-бензолдиаминов можно использовать 2,4-толуолдиамин и 2,6-толуолдиамин, и их смеси, необязательно содержащие 2,5-толуолдиамин.
В некоторых вариантах осуществления способы данного изобретения могут приводить к образованию двойных связей в алкильной группе, присоединяемой к N,N'-диалкилированному-1,3-бензолдиамину. Образованию ненасыщенных алкильных групп может благоприятствовать, например, снижение парциального давления водорода, доступного для взаимодействия, и/или уменьшение продолжительности реакции, или температуры в реакционном сосуде. Конкретный используемый катализатор также может оказать влияние на насыщение.
Применения
Композиции настоящего изобретения можно включить во множество продуктов, например, с целью улучшения устойчивости к окислению, и/или для предотвращения разложения, или образования отложений. В предпочтительном варианте осуществления одну, или более композиций алкилированных-1,3-бензолдиаминов изобретения можно включить в жидкость, которая иначе подверглась бы окислительному разложению. Таким образом, в одном из вариантов осуществления данное изобретение направлено на жидкость, например, смазочную жидкость, включающую базовый компонент и стабилизирующее количество, по меньшей мере, одной композиции алкилированных-1,3-бензолдиаминов настоящего изобретения. Предпочтительно, данная жидкость содержит алкилированный-1,3-бензолдиамин в количестве, достаточном для стабилизации данной жидкости в отношении образования отложений, относительно такой же композиции без алкилированного-1,3-бензолдиамина.
В одном из вариантов осуществления данное изобретение направлено на жидкость, например, композицию смазочного масла, включающую, по меньшей мере, один базовый компонент, например, базовый компонент смазочной вязкости, в количестве от 45 до 99,99 масс.%, например, от 80 до 99,95 масс.%, или от 90 до 99 масс.%, из расчета на общую массу данного базового компонента и алкилированного-1,3-бензолдиамина. Жидкость также включает одно, или более соединений алкилированного-1,3-бензолдиамина настоящего изобретения в количестве от 0,01 до 6 масс.%, например, от 0,05 до 4 масс.%, или от 1 до 3 масс.%, из расчета на общую массу данного базового компонента и алкилированного-1,3-бензолдиамина. Разумеется, в данную жидкость могут быть также включены другие присадки, как описано далее. В одном из иллюстративных примеров вариантов осуществления базовый компонент присутствует в количестве от 80 до 99,99 масс.%, а соединение - в количестве от 0,01 до 6 масс.%, при этом соединение имеет формулу:
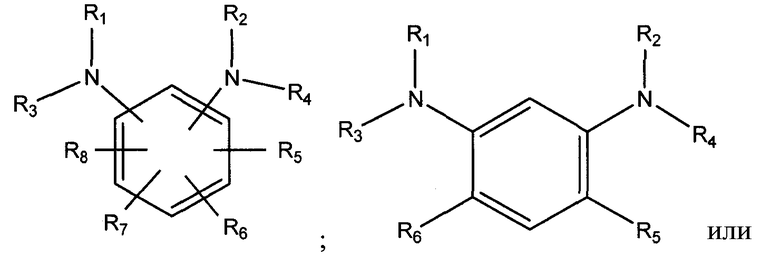
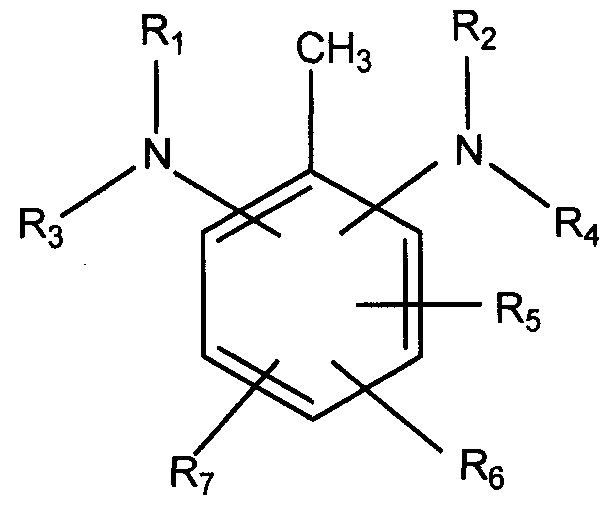
в которой каждый из R1, R2, R3, R4, R5, R6, R7 и R8 определен выше.
В другом иллюстративном примере варианта осуществления данное изобретение направлено на жидкость, например, композицию смазочного масла, включающую базовый компонент и N1,N3-дициклоалкил-4,6-диалкил-1,3-бензолдиамин. Базовый компонент предпочтительно присутствует в данной жидкости в количестве от 80 до 99,99 масс.%, из расчета на общую массу базового компонента и N1,N3-дициклоалкил-4,6-диалкил-1,3-бензолдиамина. N1,N3-дициклоалкил-4,6-диалкил-1,3-бензолдиамин предпочтительно присутствует в данной жидкости в количестве от 0,01 до 6 масс.%, из расчета на общую массу базового компонента и N1,N3-дициклоалкил-4,6-диалкил-1,3-бензолдиамина.
В подобных вариантах осуществления в композиции смазочного масла алкилированный 1,3-бензолдиамин присутствует в достаточном количестве для того, чтобы стабилизировать данную жидкость в отношении образования отложений. Например, имитационная проверка термоокисления моторного масла при средних-высоких температурах (MHT-TEOST) указывает на то, что подобные композиции смазочных масел могут образовывать от 1 до 70 мг, например, от 5 до 55 мг, или от 5 до 35 мг отложений. Отложения в количестве более 70 мг, как правило, отражают нежелательно высокий уровень образования отложений, тогда как значения менее 55 мг обычно считаются приемлемыми для большинства применений. Необязательно жидкости, например, композиции смазочного масла различных вариантов осуществления данного изобретения, образуют менее 50 мг отложений, например, менее 30 мг отложений, или менее 20 мг отложений, при определении методом MHT-TEOST, ссылка на который приведена выше.
Подходящие базовые компоненты для композиций смазочной вязкости выбирают из группы, состоящей из моторных масел, трансмиссионных жидкостей, гидравлических жидкостей, трансмиссионных масел, цилиндровых масел для судовых двигателей, компрессорных масел, низкотемпературных смазок, авиационных турбинных масел, масел для газовых турбин и их смеси.
Соединения настоящего изобретения улучшают устойчивость к окислению органических веществ, которые подвергаются окислительному, термическому и/или вызванному светом разложению. Данные органические вещества могут быть природными, или синтетическими. Данные органические вещества могут включать «функциональные жидкости», смазочные масла, консистентные смазки и топлива, а также трансмиссионные жидкости для автоматического и ручного управления, жидкость для рулевого управления с усилителем, гидравлические жидкости, масла для газовых турбин, компрессорные смазки, автомобильные и промышленные смазочные материалы для трансмиссий и теплообменные масла. Композиции смазочных масел, применимые для практического осуществления настоящего изобретения, включают основное количество масла смазочной вязкости и минорное количество, по меньшей мере, одного соединения бензолдиамина, содержащего один, или более циклоалкильных заместителей у каждого атома азота.
Масла смазочной вязкости, применимые в контексте настоящего изобретения, можно выбрать из природных смазочных масел, синтетических смазочных масел и их смесей. Смазочное масло может различаться по вязкости от минеральных масел легкого дистиллята до тяжелых смазочных масел, таких, как масла для бензиновых двигателей, минеральные смазочные масла и дизельные масла для сверхмощных двигателей. В целом, вязкость данных масел изменяется в интервале от около 2 сантистокс до около 40 сантистокс, в особенности от около 4 сантистокс до около 20 сантистокс при определении при 100°С.
Дизельное топливо представляет собой горючее на основе нефти, особенно горючее масло на основе среднего дистиллята. Такое дистиллятное горючее масло обычно кипит в интервале от 110°С до 500°С, например, от 150°С до 400°С. Данное горючее масло может включать атмосферный дистиллят или вакуумный дистиллят, крекинг-газойль или смесь в любом соотношении фракции прямой гонки и термического и/или нефтезаводского потоков, таких, как крекинг- и гидрокрекинг-дистилляты.
Другие примеры дизельного топлива включают топливо Фишера-Тропша. Топливо Фишера-Тропша, известное также как топливо FT, включает топливо, описанное как топливо газ-в-жидкость (GTL), топливо биомасса-в-жидкость (BTL) и топливо на основе превращения угля. Для получения такого топлива сначала получают синтетический газ (СО+Н2), а затем превращают его в нормальные парафины методом Фишера-Тропша. После этого нормальные парафины можно модифицировать такими методами, как каталитический крекинг/реформинг, или изомеризация, гидрокрекинг и гидроизомеризация, получая ряд углеводородов, таких, как изопарафины, циклопарафины и ароматические соединения. Полученное FT топливо можно использовать как таковое, или в сочетании с другими топливными компонентами и видами топлива. Подходит также дизельное топливо, полученное из растительного, или животного сырья. Такое топливо можно использовать как таковое, или в сочетании с другими видами топлива.
Предпочтительно, содержание серы в дизельном топливе составляет, по большей части, 0,05 массовых %, более предпочтительно, по большей части, 0,035 массовых %, особенно, по большей части, 0,015 массовых %. Также подходит топливо с еще более низким содержанием серы, такое, как топливо с содержанием серы менее 50 ч. на млн. по массе, предпочтительно, менее 20 ч. на млн., например, 10 ч. на млн., или менее.
Масла и жиры, полученные из растительного, или животного сырья, находят все больше применений в качестве топлива и, в частности, в качестве частичной, или полной замены топлива на основе полученного из нефти горючего на основе среднего дистиллята, такого, как дизельное топливо. Обычно подобные виды топлива известны как «биотопливо», или «биодизельное топливо». Биотопливо можно получить из многих видов сырья. В ряду наиболее распространенных алкиловые, часто метиловые эфиры жирных кислот, экстрагированные из растений, такие, как рапс, подсолнечник и так далее. Эти виды топлива часто называют FAME (метиловые эфиры жирных кислот).
Природные масла включают животные масла и растительные масла (например, лярдовое масло, касторовое масло), сжиженные нефтяные масла и подвергшиеся гидроочистке, обработанные растворителем, или обработанные кислотой минеральные масла парафинового, нафтенового, или смешанного парафино-нафтенового типов. Масла смазочной вязкости, полученные из угля, или сланца, также служат в качестве применимых базовых масел. Другими примерами масел и жиров, полученных из животного, или растительного сырья, являются рапсовое масло, кориандровое масло, соевое масло, хлопковое масло, подсолнечное масло, касторовое масло, оливковое масло, арахисовое масло, кукурузное масло, миндальное масло, косточковое пальмовое масло, кокосовое масло, горчичное масло, масло ятрофы, говяжий жир и рыбьи жиры. Другие примеры включают масла, полученные из зерновых, джута, кунжута, ши, земляного ореха, и льняное масло, и могут быть получены из них способами, которые известны в данной области. Рапсовое масло, которое представляет собой смесь жирных кислот, частично этерифицированных глицерином, доступно в большом количестве, и может быть получено простым способом путем выжимания рапса. Также подходят регенерированные масла, такие, как использованные кухонные масла.
Подходящие примеры алкиловых эфиров жирных кислот могут включать промышленные смеси этилового, пропилового, бутилового, и в особенности, метиловых эфиров жирных кислот, содержащих от 12 до 22 атомов углерода. Например, лауриновая кислота, миристиновая кислота, пальмитиновая кислота, пальмитолеиновая кислота, стеариновая кислота, олеиновая кислота, элаидиновая кислота, петроселиновая кислота, рицинолеиновая кислота, элеостеариновая кислота, линолевая кислота, линоленовая кислота, эйкозановая кислота, гадолеиновая кислота, докозановая кислота, или эруковая кислота применимы и имеют йодное число от 50 до 150, в особенности, от 90 до 125. Смеси с частично выгодными свойствами представляют собой смеси, содержащие, в основном, то есть, по меньшей мере, 50 масс.%, метиловых эфиров жирных кислот с количеством атомов углерода от 16 до 22 и 1, 2, или 3 двойными связями. Предпочтительными низшими алкиловыми эфирами жирных кислот являются метиловые эфиры олеиновой кислоты, линолевой кислоты, линоленовой кислоты и эруковой кислоты.
Промышленные смеси установленного типа получают, например, расщеплением и этерификацией животных и растительных жиров путем их переэтерификации более низкими алифатическими спиртами. Для получения алкиловых эфиров жирных кислот выгодно исходить из жиров и масел, которые содержат низкие концентрации насыщенных кислот, менее 20%, и которые имеют йодное число менее 130. Подходят смеси следующих сложных эфиров, или масел, например, рапсовое, подсолнечное, кориандровое, касторовое, соевое, арахисовое, хлопковое, говяжий жир и так далее. Предпочтительными являются алкиловые эфиры жирных кислот на основе нового ряда рапсового масла, компонент жирной кислоты которого включает более 80 масс.% ненасыщенных жирных кислот с 18 атомами углерода.
Особенно предпочтительными являются масла, которые можно использовать в качестве биотоплива. Полагают, что биотопливо, то есть топливо, полученное из животного, или растительного сырья, наносит меньший ущерб окружающей среде при сгорании и получается из возобновляемых источников. Сообщалось, что при сгорании эквивалентного количества топлива на основе нефтяного дистиллята, например, дизельного топлива, образуется меньше двуокиси углерода и образуется очень мало двуокиси серы. В качестве замены дизельному топливу можно использовать некоторые производные растительного масла, например, производные, полученные омылением и повторной этерификацией одноатомного алкилового спирта.
Предпочтительными видами биотоплива являются производные растительных масел, среди которых особенно предпочтительными видами биотоплива являются производные алкиловых эфиров рапсового масла, хлопкового масла, соевого масла, подсолнечного масла, оливкового масла, или пальмового масла, при этом особенно предпочтительным является метиловый эфир рапсового масла, либо сам по себе, либо в смеси с производными других растительных масел, например, смесей в любом соотношении метилового эфира рапсового масла и метилового эфира пальмового масла.
В настоящее время биотопливо наиболее употребительно в сочетании с маслами на основе нефти. Настоящее изобретение применимо к смесям биотоплива и горючего на основе нефти в любом соотношении. Например, из растительного, или животного сырья можно получить, по меньшей мере, 5%, предпочтительно, по меньшей мере, 25%, более предпочтительно, по меньшей мере, 50%, и наиболее предпочтительно, по меньшей мере, 95 массовых % масла.
Синтетические смазочные масла включают углеводородные масла и галогензамещенные углеводородные масла, такие, как полимеризованные и сополимеризованные олефины (например, полибутилены, полипропилены, сополимеры пропилен-изобутилена, хлорированные полибутилены, поли(1-гексены), поли(1-октены), поли(1-децены)), алкилбензолы (например, додецилбензолы, тетрадецилбензолы, динонилбензолы, ди(2-этилгексил)бензолы), полифенилы (например, бифенилы, терфенилы, алкилированные полифенолы) и алкилированные дифениловые простые эфиры и алкилированные дифенилсульфиды, и их производные, аналоги и гомологи. Кроме того, применимы синтетические масла, полученные из способа превращения газа в жидкость из углеводородов, синтезированных по Фишеру-Тропшу, которые обычно называют базовыми маслами газ-в-жидкость, или “GTL”.
Алкиленоксидные полимеры и сополимеры и их производные, в которых терминальные гидроксильные группы модифицированы получением сложного эфира, получением простого эфира и так далее, составляют следующий класс известных синтетических смазочных масел. Их примерами являются полиоксиалкиленовые полимеры, полученные полимеризацией этиленоксида, или пропиленоксида и алкиловых и ариловых простых эфиров полиоксиалкиленовых полимеров (например, метилполиизопропиленгликолевый эфир с молекулярной массой 1000, или дифениловый эфир полиэтиленгликоля с молекулярной массой от 1000 до 1500) и их сложные эфиры моно- и поликарбоновых кислот, например, эфиры уксусной кислоты, смешанные эфиры С3-С8 жирных кислот, и диэфир С13 оксокислоты и тетраэтиленгликоля.
Следующий подходящий класс синтетических смазочных масел включает эфиры дикарбоновых кислот (например, фталевой кислоты, янтарной кислоты, алкилянтарных кислот и алкиленянтарных кислот, малеиновой кислоты, азелаиновой кислоты, субериновой кислоты, себациновой кислоты, фумаровой кислоты, адипиновой кислоты, димера линолевой кислоты, малоновой кислоты, алкилмалоновых кислот, алкенилмалоновых кислот) и ряда спиртов (например, бутилового спирта, гексилового спирта, додецилового спирта, 2-этилгексилового спирта, этиленгликоля, моноэфира диэтиленгликоля, пропиленгликоля). Конкретные примеры подобных сложных эфиров включают дибутиладипат, ди(2-этилгексил)себацат, ди-н-гексилфумарат, диоктилсебацат, диизооктилазелат, диизододецилазелат, диоктилфталат, дидецилфталат, диэйкозилсебацат, 2-этилгексиловый диэфир димера линолевой кислоты, и сложный эфир, полученный при взаимодействии одного моля себациновой кислоты с двумя молями тетраэтиленгликоля и двумя молями 2-этилгексановой кислоты.
Сложные эфиры, применимые в качестве синтетических масел, включают также эфиры, полученные из С5-С12 монокарбоновых кислот и полиолов, и сложных эфиров полиолов, таких, как неопентилгликоль, триметилолпропан, пентаэритрит, дипентаэритрит и трипентаэритрит.
Следующий подходящий класс синтетических смазочных материалов составляют масла на основе силикона, такие, как полиалкил-, полиарил-, полиалкокси- или полиарилоксисиликоновые масла и силикатные масла; такие масла включают тетраэтилсиликат, тетраизопропилсиликат, тетра-(2-этилгексил)силикат, тетра-(4-метил-2-этилгексил)силикат, тетра-(п-третбутилфенил)силикат, гекса-(4-метил-2-этилгексил)дисилоксан, поли(метил)силоксаны и поли(метилфенил)силоксаны. Прочие синтетические смазочные масла включают жидкие эфиры фосфорсодержащих кислот (например, трикрезилфосфат, триоктилфосфат, диэтиловый эфир децилфосфоновой кислоты) и полимерные тетрагидрофураны.
Масла смазочной вязкости могут включать базовый компонент I группы, II группы или III группы, или смеси базовых масел упомянутых выше базовых компонентов. Предпочтительно, масло смазочной вязкости представляет собой базовый компонент II группы, или III группы, или их смесь, или смесь базового компонента I группы и одного, или более из II группы, или III группы. Предпочтительно, основное количество масла смазочной вязкости представляет собой базовый компонент II группы, III группы, IV группы, или V группы, или их смесь. Базовый компонент, или смесь базовых компонентов предпочтительно имеет содержание насыщенных продуктов, по меньшей мере, 65%, более предпочтительно, по меньшей мере, 75%, такое, как по меньшей мере, 85%. Наиболее предпочтительно, базовый компонент, или смесь базовых компонентов, имеет содержание насыщенных продуктов более 90%. Предпочтительно, содержание серы в масле, или смеси масел составит менее 1%, предпочтительно, менее 0,6% и наиболее предпочтительно, менее 0,4 массовых %.
Предпочтительно, летучесть масла, или смеси масел, определенная при помощи пробы на летучесть методом Ноака (ASTM D5880), меньше, или равна 30%, предпочтительно, меньше, или равна 25%, более предпочтительно, меньше, или равна 20%, предпочтительно, меньше, или равна 16%. Предпочтительно, индекс вязкости (VI) масла, или смеси масел, составляет, по меньшей мере, 85, предпочтительно, по меньшей мере, 100, наиболее предпочтительно, по меньшей мере, от около 105 до 140.
Определения базовых компонентов и базовых масел в данном изобретении аналогичны определениям, приведенным в публикации Американского нефтяного института (API) “Engine Oil Licensing and Certification System”, Industry Services Department (14th ed., December 1996), Addendum 1, December 1998. В данной публикации проведена категоризация базовых компонентов следующим образом.
(а) базовые компоненты I группы содержат менее 90 процентов насыщенных продуктов и/или более 0,03 процентов серы и имеют индекс вязкости, больший, или равный 80, и меньший 120 при использовании методов тестирования, определенных в таблице 1.
(b) базовые компоненты II группы содержат больше, или равно 90 процентов насыщенных продуктов и меньше, или равно 0,03 процентов серы и имеют индекс вязкости, больший, или равный 80, и меньший 120 при использовании тестовых методов, определенных в таблице 1.
(с) базовые компоненты III группы содержат больше, или равно 90 процентов насыщенных продуктов и меньше, или равно 0,03 процентов серы и имеют индекс вязкости, больший, или равный 120 при использовании тестовых методов, определенных в таблице 1.
(d) базовые компоненты IV группы представляют собой полиальфаолефины (РАО).
(е) базовые компоненты V группы включают все остальные базовые компоненты, не включенные в I, II, III, или IV группы.
Для того чтобы композиции данного изобретения могли соответствовать конкретным требованиям, в них можно включить дополнительные присадки. Примеры присадок, которые можно включить в композиции смазочных масел, представляют собой диспергаторы, моющие присадки, ингибиторы коррозии металла, присадки, понижающие температурную зависимость вязкости, ингибиторы коррозии, ингибиторы окисления, модификаторы трения, другие диспергаторы, противовспенивающие вещества, противоизносные вещества и депрессорные присадки, понижающие температуру застывания. Некоторые из них подробно обсуждаются далее.
Кроме того, композиции смазочных масел настоящего изобретения могут содержать один, или более беззольных диспергаторов, которые эффективно снижают образование отложений при использовании в бензиновых и дизельных двигателях при добавлении к смазочным маслам. Беззольные диспергаторы, применимые в композициях настоящего изобретения, включают маслорастворимую полимерную длинноцепную структуру, содержащую функциональные группы, способные связываться с частицами, подлежащими диспергированию. Обычно подобные диспергаторы включают аминные, спиртовые, амидные, или сложноэфирные полярные группы, связанные с полимерным каркасом, часто через мостиковую группу. Беззольный диспергатор можно выбрать, например, из маслорастворимых солей, сложных эфиров, аминоэфиров, амидов, имидов и оксазолинов длинноцепных углеводородзамещенных моно- и поликарбоновых кислот, или их ангидридов, тиокарбоксилатных производных длинноцепных углеводородов, длиннноцепных алифатических углеводородов, содержащих полиаминные группы, непосредственно связанные с ними, и продуктов конденсации Манниха, полученных конденсацией длинноцепного замещенного фенола с формальдегидом и полиалкиленполиамином.
Предпочтительные диспергаторы включают полиальфа-олефиновые диспергаторы, модифицированные полиаминами, в частности, диспергаторы на основе этилен/бутен альфа-олефина и полиизобутилена. Особенно предпочтительными являются беззольные диспергаторы, полученные из полиизобутилена, замещенного группами ангидрида янтарной кислоты, и введенного во взаимодействие с полиэтиленаминами, например, полиизобутиленсукцинимидом, полиэтилендиамином, тетраэтиленпентамином, или полиоксиалкиленполиамином, например, полиоксипропилендиамином, триметилоламинометаном, гидроксисоединением, например, пентаэритритом, и их комбинации. Одной из особенно предпочтительных комбинаций диспергатора является сочетание (А) полиизобутилена, замещенного группами янтарного ангидрида, и введенного во взаимодействие с (В) гидроксисоединением, например, пентаэритритом, (С) полиоксиалкиленполиамином, например, полиоксипропилендиамином, или (D) полиалкилендиамином, например, полиэтилендиамином и тетраэтиленпентамином при использовании от около 0,3 до около 2 моль (В), (С) и/или (D) на моль (А). Другая предпочтительная комбинация диспергатора включает сочетание (А) ангидрида полиизобутенилянтарной кислоты и (В) полиалкиленполиамина, например, тетраэтиленпентамина, и (С) полиатомного спирта, или полигидроксизамещенного алифатического первичного амина, например, пентаэритрита, или трисметилоламинометана, как описано в патенте США №3632511.
Следующий класс беззольных диспергаторов включает продукты конденсации оснований Манниха. Как правило, эти продукты получают конденсацией примерно одного моля алкилзамещенного моно-, или полигидроксибензола с карбонильным соединением (соединениями) (например, формальдегидом и параформальдегидом) в количестве примерно от 1 до 2,5 моль, и полиалкиленполиамином в количестве примерно от 0,5 до 2 моль, как описано, например, в патенте США № 3442808. Подобные продукты конденсации оснований Манниха могут включать полимерный продукт катализируемой металлоценом полимеризации в качестве заместителя в бензольной группе, или можно вводить во взаимодействие с соединением, содержащим подобный полимер, замещенный по ангидриду янтарной кислоты образом, аналогичным описанному в патенте США № 3442808. Примеры функционализированных и/или модифицированных функциональными группами полимеров с использованием систем на основе металлоценовых катализаторов описаны в публикациях, определенных выше.
Впоследствии диспергатор можно подвергнуть повторной обработке при помощи ряда стандартных способов повторной обработки, таких, как борирование, как, в общих чертах, обучают в патентах США №№ 3087936 и 3254025. Борирование диспергатора легко осуществить, обрабатывая ацильный азотсодержащий диспергатор соединением бора, таким, как оксид бора, галогенид бора, кислоты бора и эфиры борных кислот, в количестве, достаточном для получения от около 0,1 до около 20 атомных долей бора на каждый моль ацилированной азотной композиции. Применимые диспергаторы содержат от около 0,5 до около 2,0 масс.%, например, от около 0,05 до около 0,7 масс.% бора. Предполагается, что бор, присутствующий в продукте в виде полимеров дегидратированной борной кислоты (главным образом, (НВО2)3), связывается с имидами и диимидами диспегатора в виде солей аминов, например, метаборатной соли диимида. Борирование можно осуществить, прибавляя от около 0,5 до 4 масс.%, например, от около 1 до около 3 масс.% (из расчета на массу ацильного азотсодержащего соединения) соединения бора, предпочтительно, борной кислоты, обычно в виде суспензии, к ацильному азотсодержащему соединению, и нагревая при перемешивании при температуре от около 135°С до около 190°С, например, от около 140°С до около 170°С, в течение от около одного до около пяти часов с последующей отгонкой азота. Альтернативным образом, обработку бором можно проводить, добавляя борную кислоту в горячую реакционную смесь соединения дикарбоновой кислоты и амина при одновременном удалении воды. Можно также использовать другие общеизвестные методы обработки после реакций.
Диспергатор можно также дополнительно подвергнуть последующей обработке при помощи реакции с так называемым «закрывающим агентом». Обычно азотсодержащие диспергаторы «закрывали», чтобы уменьшить неблагоприятное воздействие, которое подобные диспергаторы оказывают на фторкаучуковые элементы герметизации двигателя. Известно множество «закрывающих агентов» и способов. Из числа известных «закрывающих агентов» наиболее подходящими являются те, которые переводят основные аминогруппы диспергатора в не основные группы (например, амидо, или имидогруппы). Взаимодействие азотсодержащего диспергатора и алкилацетоацетата (например, этилацетоацетата (ЕАА)) описано, например, в патентах США №№4839071, 4839072 и 4579675. Взаимодействие азотсодержащего диспергатора с муравьиной кислотой описано, например, в патенте США №3185704. Продукты реакции азотсодержащего диспергатора с другими подходящими закрывающими агентами описаны в патенте США №4663064 (гликолевая кислота), патентах США №№4612132, 5334321, 5356552, 5716912, 5849676 и 5861363 (алкил- и алкиленкарбонаты, например, этиленкарбонат), патенте США №5328622 (моноэпоксид), патенте США №5026495, патентах США №№5085788, 5259906, 5407591 (поли (например, бис)-эпоксиды) и патенте США №4686054 (ангидрид малеиновой кислоты, или ангидрид янтарной кислоты). Приведенный выше список не является исчерпывающим и специалистам в данной области известны другие способы закрывания азотсодержащих диспергаторов.
Для достаточного сдерживания образования отложений на поршнях, азотсодержащий диспергатор можно добавить в количестве, при котором получат композицию смазочного масла с содержанием азота от около 0,03 масс.% до около 0,15 масс.%, предпочтительно, от около 0,07 масс.% до около 0,12 масс.%.
Металлсодержащие, или образующие золу детергенты, действуют и как детергенты для уменьшения количества, или удаления отложений, и как нейтрализаторы кислот, или ингибиторы коррозии, уменьшая, таким образом, износ и коррозию, и продлевая срок службы двигателя. Как правило, детергенты содержат полярную голову и длинный гидрофобный хвост, при этом полярная голова включает соль металла с кислотным органическим соединением. Данные соли могут содержать, главным образом, стехиометрическое содержание металла, в этом случае их обычно описывают как нормальные, или нейтральные соли, и обычно имели бы общее щелочное число, или TBN (которое можно определить при помощи ASTM D2896) от 0 до 80. Большое количество основания металла можно ввести при реакции избытка соединения металла (например, оксида, или гидроксида) с кислотным газом (например, двуокисью углерода). Полученный сверхосновный детергент содержит нейтрализованный детергент в качестве внешнего слоя мицеллы основания металла (например, карбоната). Такие сверхосновные детергенты могут иметь TBN, равное 150, или больше, и обычно имеют TBN, составляющее от 250 до 450, или больше.
Детергенты, подходящие для использования, включают маслорастворимые нейтральные, или сверхосновные сульфонаты, феноляты, сульфированные феноляты, тиофосфонаты, салицилаты, нафтенаты, и другие маслорастворимые карбоксилаты металла, в частности, щелочных, или щелочноземельных металлов, например, натрия, калия, лития, кальция и магния. Наиболее употребительными металлами являются кальций и магний, оба из которых могут присутствовать в моющих присадках, используемых в смазочном материале, и смеси кальция и/или магния и натрия. Особенно подходящими металлсодержащими детергентами являются нейтральные и сверхосновные сульфонаты кальция с TBN, составляющим от 20 до 450 TBN, и нейтральные и сверхосновные феноляты кальция и сульфированные феноляты с TBN, составляющим от 50 до 450. Можно использовать сочетания детергентов, либо сверхосновных, либо нейтральных, либо и тех, и других.
Сульфонаты можно получить из сульфокислот, которые обычно получают сульфированием алкилзамещенных ароматических углеводородов, таких, как углеводороды, полученные фракционированием нефти, или алкилированием ароматических углеводородов. Примеры включают углеводороды, полученные алкилированием бензола, толуола, ксилола, нафталина, дифенила, или их галогенсодержащих производных, таких, как хлорбензол, хлортолуол и хлорнафталин. Алкилирование можно осуществить в присутствии катализатора при помощи алкилирующих агентов, содержащих от около 3 до более, чем 70 атомов углерода. Алкиларилсульфонаты обычно содержат от около 9 до около 80, или более атомов углерода, предпочтительно, от около 16 до около 60 атомов углерода на алкилзамещенную ароматическую группу.
Маслорастворимые сульфонаты, или алкиларилсульфокислоты можно нейтрализовать оксидами, гидроксидами, алкоголятами, карбонатами, карбоксилатами, сульфидами, гидросульфидами, нитратами, боратами и эфирами металла. Количество соединения металла выбирают, принимая во внимание желательное TBN конечного продукта, но обычно оно изменяется в интервале от около 100 до 220 масс.% (предпочтительно, по меньшей мере, 125 масс.%) от стехиометрически требуемого количества.
Соли металла с фенолами и сульфированными фенолами получают реакцией с соответствующим соединением металла, таким, как оксид, или гидроксид, и нейтральными, или сверхосновными продуктами, которые можно получить методами, известными в данной области. Сульфированные фенолы можно получить, вводя фенол во взаимодействие с серой, или серусодержащим соединением, таким, как сероводород, моногалогенид серы, или дигалогенид серы, получая продукты, которые обычно представляют собой смеси соединений, в которых два, или более фенола связаны мостиковым образом серусодержащими мостиками.
Дигидрокарбилдитиофосфатные соли металла часто используют в качестве противоизносных и антиокислительных агентов. Металл может представлять собой щелочной, или щелочноземельный металл, или алюминий, свинец, олово, молибден, марганец, никель, или медь. Наиболее употребительны в смазочном масле цинковые соли в количестве от 0,1 до 10 масс.%, предпочтительно, от 0,2 до 2 масс.%, из расчета на общую массу композиции смазочного масла. Их можно получить по известным методикам, получая сперва дигидрокарбилдитиофосфорную кислоту (DPPA), как правило, реакцией одной или более молекул спирта, или фенола с P2S5, а затем нейтрализуя полученный DPPA соединением цинка. Например, дитиофосфорную кислоту можно получить, вводя во взаимодействие смеси первичных и вторичных спиртов. Альтернативным образом, можно получить сложные дитиофосфорные кислоты, в которых гидрокарбильные группы одной имеют полностью вторичный характер, а гидрокарбильные группы другой имеют полностью первичный характер. Для получения данной цинковой соли можно было бы использовать любое основное, или нейтральное соединение цинка, но в большинстве случаев используют оксиды, гидроксиды и карбонаты. Промышленные присадки часто содержат избыток цинка вследствие использования избытка основного соединения цинка в реакции нейтрализации.
Предпочтительные дигидрокарбилдитиофосфаты цинка представляют собой маслорастворимые соли дигидрокарбилдитиофосфорных кислот, и могут включать диалкилдитиофосфаты цинка. Настоящее изобретение может особенно подходить в случае использования для смазочных композиций для дизельных автомобильных двигателей, в которых концентрация фосфора составляет от около 0,02 до около 0,12 масс.%, например, от около 0,03 до около 0,10 масс.%, или от около 0,05 до около 0,08 масс.%, из расчета на общую массу композиции, и композиций для сверхмощных дизельных двигателей, в которых концентрация фосфора составляет от около 0,02 до около 0,16 масс.%, например, от около 0,05 до около 0,14 масс.%, или от около 0,08 до около 0,12 масс.%, из расчета на общую массу композиции. В одном из предпочтительных вариантов осуществления в композициях смазочного масла содержится диалкилдитиофосфат цинка, полученный преимущественно (например, более, чем на 50 мол.%, например, более, чем на 60 мол.%) из вторичных спиртов.
Следующее представляет собой иллюстративные примеры подобных противоизносных присадок и является коммерчески доступным от Lubrizol Corp.: Lubrizol 677А, Lubrizol 1095, Lubrizol 1097, Lubrizol 1360, Lubrizol 1395, Lubrizol 5139 и Lubrizol 5604, в числе прочих; и от Ciba-Geigy: Irgalube 353.
Противоокислительные присадки или антиокислители снижают тенденцию минеральных масел к разложению при эксплуатации. Доказательством окислительного разложения может являться наличие осадка в смазке, нагароподобных отложений на металлических поверхностях, и рост вязкости. Такие противоокислительные присадки включают стерически затрудненные фенолы, соли щелочноземельных металлов алкилфенолтиоэфиров, содержащих предпочтительно от С5 до С12 алкильные боковые цепи, нонилфенолсульфид кальция, маслорастворимые феноляты и сульфированные феноляты, фосфорсульфированные или сульфированные углеводороды, эфиры фосфористой кислоты, тиокарбаматы металлов, маслорастворимые соединения меди, описанные в патенте США № 4867890, и молибденсодержащие соединения.
Типичные маслорастворимые ароматические амины, содержащие, по меньшей мере, две ароматические группы, связанные непосредственно с одним аминным атомом азота, включают от 6 до 16 атомов углерода. Данные амины могут содержать более двух ароматических групп. Соединения, содержащие, в целом, по меньшей мере, три ароматические группы, в которых две ароматические группы связаны ковалентной связью, или атомом, или группой (например, атомом кислорода, или серы, или -СО-, -SO2-, или алкиленовой группой), а две непосредственно связаны с одним атомом азота амина, также считаются ароматическими аминами, содержащими, по меньшей мере, две ароматические группы, непосредственно связанные с атомом азота. Ароматические кольца обычно замещены одним, или более заместителями, выбранными из алкильной, циклоалкильной, алкокси, арилокси, ацильной, ациламино, гидроксильной и нитро-групп.
Обычно используют комбинацию ряда антиокислителей. В одном из предпочтительных вариантов осуществления, композиции смазочного масла, помимо соединения (соединений) бензолдиамина, добавленных для улучшения вызванного наличием сажи увеличения вязкости, содержит от около 0,1 до около 1,2 масс.% аминного антиокислителя, и от около 0,1 до около 3 масс.% фенольного антиокислителя. В другом предпочтительном варианте осуществления композиции смазочного масла настоящего изобретения содержат от около 0,1 до около 1,2 масс.% аминного антиокислителя, и от около 0,1 до около 3 масс.% фенольного антиокислителя, и соединение молибдена в количестве, которое обеспечивает содержание молибдена в композиции смазочного масла в количестве от около 10 до около 1000 ч. на млн. Предпочтительно, композиции смазочного масла, применимые для практического осуществления настоящего изобретения, в частности, композиции смазочного масла, применимые для практического осуществления настоящего изобретения, для которых требуется содержание не более 1200 ч. на млн. фосфора, содержат беззольные антиокислители, отличающиеся от бензолдиаминов, в количестве от около 0,1 до около 5 масс.%, предпочтительно, от около 0,3 масс.% до около 4 масс.%, более предпочтительно, от около 0,5 масс.% до около 3 масс.%. В том случае, когда требуется меньшее содержание фосфора, содержание беззольного антиокислителя, отличающегося от бензолдиамина, предпочтительно, соответственно возрастет.
Следующее представляет собой примеры антиокислителей на основе вторичных диариламинов, и является коммерчески доступным от Chemtura Corporation: Naugalube™ 438, Naugalube 438L, Naugalube 640, Naugalube 635, Naugalube 680, Naugalube AMS, Naugalube APAN, Naugard PANA, Naugalube 403, Naugalube 410 и Naugalube 420; и от Ciba-Geigy: Irganox™ L 06 и Irganox L 57. Следующее представляет собой пример антиокислителей на основе замещенных фенолов, которые коммерчески доступны от Crompton Corporation: Naugard™ BHT, Antioxidant 431 и Naugalube 531; и от Ciba-Geigy: Irganox™ L 115, Irganox L 115, Irganox L 118, Irganox L 135 и Irgalube F 10A.
Репрезентативные примеры модификаторов вязкости представляют собой полиизобутилен, сополимеры этилена и пропилена, полиметакрилаты, сополимеры метакрилата, сополимеры ненасыщенной дикарбоновой кислоты и винильного соединения, сополимеры стирола и акриловых сложных эфиров, и частично гидрированные сополимеры стирола/изопрена, стиролбутадиена, и изопрена/бутадиена, а также частично гидрированные гомополимеры бутадиена и изопрена.
Диспергирующая присадка, понижающая температурную зависимость вязкости, действует и как присадка, понижающая температурную зависимость вязкости, и как диспергатор. Примеры диспергирующих присадок, понижающих температурную зависимость вязкости, включают продукты реакции аминов, например, полиаминов, с гидрокарбилзамещенными моно-, или дикарбоновыми кислотами, в которых гидрокарбильный заместитель содержит цепь достаточной длины для придания данным соединениям свойств, понижающих температурную зависимость вязкости. Как правило, диспергирующая присадка, понижающая температурную зависимость вязкости, может представлять собой, например, полимер С4-С24 ненасыщенного сложного эфира винилового спирта, или С3-С10 ненасыщенной монокарбоновой кислоты, или С4-С10 дикарбоновой кислоты, с ненасыщенным азотсодержащим мономером, содержащим от 4 до 20 атомов углерода; полимер С2-С20 олефина и ненасыщенной С3-С10 моно- или дикарбоновой кислоты, нейтрализованной амином, гидроксиамином или спиртом; или полимер этилена и С3-С20 олефина, введенный далее во взаимодействие либо путем прививания к нему С4-С20 ненасыщенного мономера, либо путем прививания на полимерный каркас ненасыщенной кислоты, а затем введения во взаимодействие групп карбоновой кислоты с амином, гидроксиамином, или спиртом.
Кроме того, можно включить модификаторы трения и агенты для экономии топлива, совместимые с другими ингредиентами конечного масла. Примеры подобных веществ включают моноэфиры глицерина и высших жирных кислот, например, глицеринмоноолеат, эфиры длинноцепных поликарбоновых кислот и диолов, например, эфир бутандиола и димеризованной ненасыщенной жирной кислоты, соединения оксазолина, и алкоксилированные алкилзамещенные моноамины, диамины и алкиловые аминоэфиры, например, этоксилированный амин из животного сала и этоксилированный аминоэфир из животного сала.
Другие известные модификаторы трения включают маслорастворимые молибденорганические соединения. Кроме того, подобные модификаторы трения на основе молибденорганических соединений придают композиции смазочного масла антиокислительные и противоизносные свойства. Примеры таких малорастворимых молибденорганических соединений включают дитиокарбаматы, дитиофосфаты, дитиофосфинаты, ксантаты, тиоксантаты, сульфиды и так далее, и их смеси. Особенно предпочтительными являются дитиокарбаматы, диалкилдитиофосфаты, алкилксантаты и алкилтиоксантаты молидбена.
Помимо этого, соединение молибдена может быть кислым соединением молибдена. Данные соединения будут взаимодействовать с основным соединением азота, как определено по методике титрования D-664, или D-2896 теста ASTM, и обычно являются шестивалентными. В их число входят молибденовая кислота, молибдат аммония, молибдат натрия, молибдат калия и другие молибдаты и прочие молибденовые соли щелочных металлов, например, гидромолибдат натрия, MoOCl4, MoO2Br2, Mo2O3Cl6, триоксид молибдена, или похожие кислые соединения молибдена.
В число соединений молибдена, применимых в композициях данного изобретения, входят молибденорганические соединения формулы: Mo(ROCS2)4 и Mo(RSCS2)4, в которых R представляет собой органическую группу, выбранную из группы, состоящей из алкила, арила, аралкила и алкоксиалкила, содержащую, как правило, от 1 до 30 атомов углерода, предпочтительно, от 2 до 12 атомов углерода, и наиболее предпочтительно, алкил, содержащий от 2 до 12 атомов углерода. Особенно предпочтительными являются диалкилдитиокарбаматы молибдена.
Следующую группу молибденорганических соединений, применимых в смазочных композициях данного изобретения, составляют трехъядерные соединения молибдена, особенно соединения формулы Mo3SkLnQz и их смеси, где L являются независимо выбранными лигандами, содержащими органогруппы с числом атомов углерода, достаточным для того, чтобы данное соединение растворялось или диспергировалось в масле, n составляет от 1 до 4, k изменяется от 4 до 7, Q выбирают из группы нейтральных электронодонорных соединений, таких, как вода, амины, спирты, фосфины и простые эфиры, а z изменяется в интервале от 0 до 5 и включает нестехиометрические значения. В числе всех органогрупп лиганда должен присутствовать, по меньшей мере, всего 21 атом углерода, например, по меньшей мере, 25, по меньшей мере, 30, или, по меньшей мере, 35 атомов углерода.
Следующее является примером молибденовых присадок для модификации трения и коммерчески доступно от R. T. Vanderbilt Company, Inc.: Molyvan™ A, Molyvan L, Molyvan 807, Molyvan 865B, Molyvan 822, Molyvan 855, в числе прочего. Следующее также является примером подобных присадок и коммерчески доступно от Asahi Denka Kogyo K.K.: SAKURA-LUBE™ 100, SAKURA-LUBE 165, SAKURA-LUBE 300, SAKURA-LUBE 310G, SAKURA-LUBE 321, SAKURA-LUBE 474, SAKURA-LUBE 600, SAKURA-LUBE 700, в числе прочего. Следующее также является примером подобных присадок и коммерчески доступно от Akzo Nobel Chemicals GmbH: Ketjen-Ox™ 77M, Ketjen-Ox 77TS, в числе прочего. Примером таких присадок является также Naugalube MolyFM, коммерчески доступный от Chemtura Corporation.
Депрессорные присадки, понижающие температуру застывания, известные также как присадки, улучшающие текучесть смазочного масла (LOFI), понижают минимальную температуру, при которой жидкость будет течь, или может быть налита. Подобные присадки хорошо известны. Типичными такими присадками, улучшающими низкотемпературную текучесть жидкости, являются сополимеры С8-С18 диалкилфумарата/винилацетата и полиметакрилаты. Регулирование вспенивания можно обеспечить при помощи антивспенивателя полисилоксанового типа, например, силиконового масла, или полидиметилсилоксана. Примером депрессорной присадки, понижающей температуру застывания, является полиметакрилат и так далее.
Некоторые из упомянутых выше присадок могут обеспечить ряд эффектов, так, например, одна присадка может действовать в качестве диспергатора-ингибитора окисления. Данный подход хорошо известен и не нуждается здесь в дальнейшей разработке.
Примеры ингибиторов окисления включают комплексы аминов, соединения на основе бензотриазола, толилтриазола, тиадиазола и имидазола, и так далее. Следующее является примером ингибиторов коррозии и коммерчески доступно от King Industries, Inc.: K-Corr™ 100A2.
Примеры присадок, понижающих температурную зависимость вязкости (V.I.), включают сополимеры олефинов, диспергирующие сополимеры олефинов, сополимеры этилен-α-олефинов, в которых α-олефин может представлять собой пропилен, 1-бутен или 1-пентен, или их гидриды, полиизобутилены или их гидриды, гидрированные сополимеры стирол-диенов, сополимеры стирол-ангидрида малеиновой кислоты и полиалкилстиролы и так далее.
Примеры антивспенивателей включают полисилоксан, силиконы, такие, как диметилсиликон и фторсиликон и так далее. Следующее является примером антивспенивателя и коммерчески доступно от Munzing/Ultra Additives; Foam Ban™ MS-575.
В настоящем изобретении может потребоваться включить присадку, которая поддерживает стабильность вязкости смеси. Так, несмотря на то, что при помощи присадок, содержащих полярные группы, достигается подходящая низкая вязкость на стадии предварительного смешивания, было замечено, что у некоторых композиций повышалась вязкость при их хранении в течение длительных периодов времени. Присадки, эффективные для регулирования повышения данной вязкости, включают длинноцепные углеводороды, функционализированные реакцией с моно-, или дикарбоновыми кислотами или ангидридами, которые используют при получении беззольных диспергаторов, описанных здесь ранее.
В случае, когда смазочные композиции содержат одну, или более вышеупомянутых присадок, каждую присадку обычно смешивают с базовым компонентом в количестве, которое дает возможность данной присадке обеспечить свое требуемое действие. Репрезентативные эффективные количества подобных присадок, при использовании в картерных смазках, приведены ниже. Все приведенные значения даны в виде массового процента активного ингредиента.
Предпочтительно, содержание серы в полностью составленных композициях смазочного масла для дизельного двигателя легкового автомобиля (PCDO) настоящего изобретения составляет примерно менее 0,4 масс.%, такое, как примерно меньше 0,35 масс.%, более предпочтительно, примерно меньше 0,03 масс.%, такое, как примерно меньше 0,15 масс.%. Предпочтительно, летучесть по методу Ноака полностью составленной PCDO (масло смазочной вязкости плюс все присадки) будет не более 13, например, не более 12, предпочтительно, не более 10. Полностью составленные PCDOs настоящего изобретения предпочтительно содержат не более 1200 ч. на млн. фосфора, например, не более 1000 ч. на млн. фосфора, или не более 800 ч. на млн. фосфора. Предпочтительно, содержание сульфатированной сажи в полностью составленных PCDOs настоящего изобретения составляет примерно 1,0 масс.%, или меньше.
Предпочтительно, содержание серы в полностью составленных композициях смазочного масла для сверхмощного дизельного двигателя (HDD) настоящего изобретения составляет примерно менее 1,0 масс.%, такое, как примерно меньше 0,6 масс.%, более предпочтительно, примерно меньше 0,4 масс.%, например, примерно меньше 0,15 масс.%. Предпочтительно, летучесть по методу Ноака полностью составленной композиции смазочного масла HDD (масло смазочной вязкости плюс все присадки) будет не больше 20, например, не больше 15, предпочтительно, не больше 12. Полностью составленные композиции смазочного масла HDD настоящего изобретения предпочтительно содержат не больше 1600 ч. на млн. фосфора, например, не больше 1400 ч. на млн. фосфора, или не больше 1200 ч. на млн. фосфора. Предпочтительно, содержание сульфатированной сажи (SASH) в полностью составленных композициях смазочного масла HDD настоящего изобретения составляет примерно 1,0 масс.%, или меньше.
Может быть желательно, хотя и не существенно, получить один, или более концентратов присадок, содержащих присадки (данные концентраты иногда называют пакетами присадок), при помощи которых к маслу можно одновременно добавить несколько присадок для получения композиции смазочного масла. В концентрате для получения композиции смазочного масла настоящего изобретения может, например, содержаться от около 0,1 до около 16 масс.% алкилированного-1,3-бензолдиамина настоящего изобретения, от около 10 до около 40 масс.% азотсодержащего диспергатора, от около 2 до около 20 масс.% аминного антиоксиданта и/или фенольного антиоксиданта, соединения молибдена, или его смеси, от около 5 до 40 масс.% детергента, и от около 2 до около 20 масс.% дигидрокарбилдитиофосфата металла.
В конечной композиции можно использовать от 5 до 25 масс.%, предпочтительно, от 5 до 18 масс.%, обычно, от 10 до 15 масс.% данного концентрата, при этом остаток представляет собой масло смазочной вязкости и модификатор вязкости.
Все значения, выраженные здесь в массовых процентах (если не указано иначе), основаны на содержании присадки в активном ингредиенте (A.I.) и/или на общей массе какого-либо комплекта присадок, или состава, который будет представлять собой сумму массы A.I. каждой присадки плюс масса всего масла, или разбавителя.
Помимо смазок, алкилированные-1,3-бензолдиамины настоящего изобретения можно использовать с реагентами для электроники, уретанами, средствами для защиты урожая, фармацевтическими препаратами, красителями и тонерами.
Примеры
Пример 1 - Восстановительное алкилирование 1,3-бензолдиамина циклогексаноном
Реакционную круглодонную колбу на 2000 мл снабжали верхнеприводной мешалкой, термопарой и входным клапаном для азота. В сосуд загружали 40,1 г 1,3-бензолдиамина, 800 мл тетрагидрофурана, 400 мл ксилола, 96 мл циклогексанона и 21 мл ледяной уксусной кислоты. В течение 3,5 часов прибавляли триацетоксиборгидрид натрия, 160,0 г, по мере чего температура реакционной смеси повышалась от 38°С до 65°С. Реакционную смесь перемешивали при 65°С в течение 2 ч. Реакционную смесь экстрагировали 320 г 25%-ного раствора гидроксида натрия и три раза промывали водой. Растворитель удаляли выпариванием на роторном испарителе, получая 96,4 г твердого вещества темного цвета, которое перекристаллизовывали из изопропанола, получая кристаллы светло-коричневого цвета, т.пл. 84-86°С. Кристаллы продукта содержали N1,N3-дициклогексил-1,3-бензолдиамин.
1H ЯМР: δ 7,93 т, J=7,8 Гц (1H), 6,95 дд, J1=7,8 Гц, J2=2,3 Гц, (2H), 5,83 т, J=2,2 Гц (1H), 3,42 ушир.с (2H, в состоянии обмена с CD3OD), 3,20 м, (2H), 2,1-1,1 (20H).
13C ЯМР: δ 148,86, 130,24, 103,03, 128,704, 51,92, 33,92, 26,27, 25,35.
Пример 2 - Каталитическое гидрирование 1,3-бензолдиамина циклогексаноном
В автоклав из нержавеющей стали на 1 л загружали 108,1 г 1,3-бензолдиамина, 294,0 г циклогексанона и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,233 кПа (600 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 160°С в течение 4 часов. Реакционную массу охлаждали, получая 272 г густой суспензии серого цвета, содержащей сырой N1,N3-дициклогексил-1,3-бензолдиамин, который вводили во взаимодействие без дополнительной очистки.
Пример 3 - Каталитическое гидрирование 1,3-бензолдиамина метилизобутилкетоном
В автоклав из нержавеющей стали на 1 л загружали 108,1 г 1,3-бензолдиамина, 300,6 г метилизобутилкетона (MIBK), толуол и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 160°С в течение 9 часов. Реакционную массу охлаждали, разбавляли толуолом и фильтровали. Растворитель удаляли выпариванием на роторном испарителе, получая 242,2 г красновато-коричневой жидкости, содержащей 78% сырого N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина. Сырое вещество перед использованием очищали перегонкой в вакууме.
Пример 4 - Каталитическое гидрирование N1,N3-дициклогексил-1,3-бензолдиамина, полученного в примере 1
В автоклав из нержавеющей стали на 1 л загружали 263,0 г реакционной смеси N1,N3-дициклогексил-1,3-бензолдиамина, полученной, как описано в примере 1, 59,5 г бутиральдегида и дополнительное количество 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,647 кПа (660 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 4 часов и выдерживали при 180°С в течение 17 часов. N1,N3-дициклогексил-4,6-дибутил-1,3-бензолдиамин имел приведенные ниже характеристики.
1H ЯМР: δ 6,68 с (1H), 6,04 с (1H), 3,30 ушир. (2H, в состоянии обмена с CD3OD), 3,28 м (2H; появляется при 3,12 при добавлении CD3OD), 2,36 т, J=7,7 Гц (4H), 2,10 м (4H) 1,8-1,2 (24H), 0,96 т, J=7,2 Гц (6H).
13C ЯМР: δ 144,0, 130,6, 115,2, 96,3, 52,4, 34,1, 31,9, 30,5, 26,4, 25,3, 23,1, 14,4.
Пример 5 - Каталитическое гидрирование N1,N3-дициклогексил-1,3-бензолдиамина, полученного в примере 2
К 272 г N1,N3-дициклогексил-1,3-бензолдиамина, полученного, как описано в примере 2, прибавляли 151,4 г изобутиральдегида и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 5 часов. Реакционную массу охлаждали и фильтровали. Полученную жидкость разделяли и отбрасывали водную фазу. Летучие вещества удаляли из органической фазы, получая 361 г вязкой жидкости коричневого цвета, которая затвердевала при стоянии.
В результате перекристаллизации из этилацетата получали продукт почти белого цвета, т.пл. 92-94°С, содержащий 42% N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамина наряду с 35% N1,N3-дициклогексил-4-изобутенил-6-изобутил-1,3-бензолдиамина, что определяли методом GC/MS.
N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамин подвергали дополнительной очистке обработкой бромом в тетрагидрофуране. После обработки водным раствором тиосульфата натрия продукт растворяли в гексане. Продукт получали хроматографией на силикагеле при использовании смеси 19:1 гексан/этилацетат.
1Н ЯМР: δ 6,58 с (1H), 6,02 с (1H), 3,30 ушир. (2H, в состоянии обмена с CD3OD), 3,30 м (2H; появляется при 3,15 при добавлении CD3OD), 2,22 д, J=7,2 Гц (4 H), 2,1-1,2 (22H), 0,91 д, J=6,6 Гц (12H).
13C ЯМР: δ 144,0, 133,5, 114,1, 96,3, 52,4, 40,7, 34,1, 28,6, 27,5, 25,3, 23,1.
ИК 3420 см-1 сл-ср (N-H).
Пример 6 - Каталитическое гидрирование N1,N3-дициклогексил-1,3-бензолдиамина, полученного в примере 2
К N1,N3-дициклогексил-1,3-бензолдиамину, полученному, как описано в примере 2, прибавляли 59,5 г бутиральдегида и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,647 кПа (660 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 4 часов и выдерживали при 180°С в течение 17 часов. Реакционную массу охлаждали и фильтровали и удаляли летучие вещества выпариванием на роторном испарителе. N1,N3-дициклогексил-4-бутил-1,3-бензолдиамин содержался в реакционной массе и был выделен колоночной хроматографией в виде масла, чистота 93,5% по данным анализа GCMS. Он имел приведенные ниже характеристики.
1H ЯМР: δ 6,80 д, J=7,8 Гц (1H), 5,93 м, (2H), 3,62 ушир.с (2H), 3,21 м, (2H), 2,33 т, J=1,1 Гц (2H), 2,05 м, (4H), 1,8-1,1 (20H), 0,932 т, J=7,2 Гц, (3H).
ИК: 3248 см-1 ср, острый (N-H).
Пример 7 - Каталитическое гидрирование N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученного в примере 3
В автоклав из нержавеющей стали на 1 л загружали 68,1 г реакционной смеси N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученной, как описано в примере 3, 54,0 г изобутиральдегида, 300 мл толуола и дополнительное количество 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 4 часов и выдерживали при 180°С в течение 17 часов. Реакционную массу охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе. Жидкая смесь продукта содержала 74% желательного N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамина. Другой компонент с наибольшим содержанием присутствовал в количестве 6% (GC). Данное соединение N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамина имело приведенные ниже характеристики.
1H ЯМР: δ 6,58 с (1H), 5,99 с (1H), 6,00 с (1H), 3,55 м (2H), 3,15 ушир. (2H, в состоянии обмена с CD3OD), 2,21 д, J=7,2 Гц (4H), 1,78 м (4H), 1,54 м (2H), 1,26 м (2H), 1,18 д, J=6,0 Гц (6H), 0,96 д, J=6,0 Гц (6H), 0,92 д, J=6,0 Гц (12H).
ИК: 3434 см-1 ср, острый (N-H).
Пример 8 - Каталитическое гидрирование N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученного в примере 3
В автоклав из нержавеющей стали на 1 л загружали 68,1 г реакционной смеси N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученной, как описано в примере 3, 54,0 г бутиральдегида, 300 мл толуола и дополнительное количество 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 4 часов и выдерживали при 180°С в течение 14 часов. Реакционную массу охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе. Жидкая смесь продукта содержала 72% желательного N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамина. Другой компонент с наибольшим содержанием присутствовал в количестве 6% (GC). Данное соединение N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамина имело приведенные ниже характеристики.
1H ЯМР: δ 6,68 с (1H), 6,00 с (1H), 3,72 м (2H), 3,35 ушир. (2H, в состоянии обмена с CD3OD), 2,52 м (4H), 1,94 м (2H), 1,72 м (4H), 1,58 м (4H), 1,47 м (2H), 1,36 д, J=6,3 Гц (6H), 1,13 м, (18H).
ИК: 3435 см-1 ср, (N-H).
Пример 9 - Каталитическое гидрирование N,N'-дициклогексил-1,3-бензолдиамина, полученного в примере 2 с использованием бензальдегида
В автоклав из нержавеющей стали на 1 л загружали 65,0 г реакционной смеси N1,N3-дициклогексил-1,3-бензолдиамина, полученной, как описано в примере 2, 79,5 г бензальдегида, 300 мл толуола и дополнительное количество 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 4 часов и выдерживали при 180°С в течение 4 часов. Реакционную смесь охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе. Продукт перекристаллизовывали из смеси 4:1 гексан/этилацетат, получая кристаллы бежевого цвета, т.пл. 152-154°С. Данное соединение N1,N3-дициклогексил-4,6-дибензил-1,3-бензолдиамина имело приведенные ниже характеристики.
1H ЯМР: δ 7,25 м (10H), 6,78 с (1H), 6,00 с (1H), 3,80 с (4H), 3,3 ушир.с (2H, в состоянии обмена с CD3OD), 3,17 м (2H), 1,8-1,0 (20H).
13C ЯМР: δ 145,39, 141,16, 128,74, 128,73, 126,30, 113,22, 96,21, 51,83, 38,06, 33,40, 26,25, 24,8.
ИК: 3424 см-1 ср, острый, (N-H).
Пример 10 - Каталитическое гидрирование N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученного в примере 3, с использованием бензальдегида
В автоклав из нержавеющей стали на 1 л загружали 69,0 г реакционной смеси N1,N3-(1,3-диметилбутил)-1,3-бензолдиамина, полученной, как описано в примере 3, 79,5 г бензальдегида, 300 мл толуола и дополнительное количество 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4,578 кПа (650 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 0,6 часов и выдерживали при 180°С в течение 6 часов. Реакционную смесь охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе. Продукт перекристаллизовывали из изопропанола, получая кристаллы желто-коричневого цвета, т.пл. 130-132°С. Данное соединение N1,N3-(1,3-диметилбутил)-4,6-дибензил-1,3-бензолдиамина имело приведенные ниже характеристики.
1H ЯМР: δ 7,12 м (10H), 6,77 с (1Н), 5,98 с (1H), 3,79 с (4H), 3,40 м (2H; появляется при 3,15 при добавлении CD3OD), 3,15 ушир. (2H, в состоянии обмена с CD3OD), 1,4-0,6 (10H), 1,01 д, J=6,0 Гц (6H), 0,82 д, J=6,3 Гц (6H), 0,79 д, J=6,3 Гц (6H).
13C ЯМР: δ 145,7, 141,2, 134,0, 128,72, 128,71, 126,3, 112,8, 95,3, 47,1, 46,6, 38,0, 25,1, 23,2, 22,9, 21,5.
ИК: 3419 см-1 ср, (N-H).
Пример 11 - Каталитическое гидрирование соединения, полученного из 2,4-толуолдиамина
В автоклав из нержавеющей стали на 1 л загружали 122 г 2,4-толуолдиамина, 294 г циклогексанона и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 5090 кПа (722 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 160°С в течение 3 часов. Реакционную массу охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе, получая 278,7 г вязкой коричневой жидкости, содержащей сырой N1,N3-дициклогексил-4-метил-1,3-бензолдиамин (88% требуемого продукта по данным GC). Дополнительные летучие вещества удаляли отгонкой в вакууме при 205°С, 13 торр, получая 271,6 г 92%-ного N1,N3-дициклогексил-4-метил-1,3-бензолдиамина.
Затем 71,5 г указанного выше N1,N3-дициклогексил-4-метил-1,3-бензолдиамина помещали в автоклав из нержавеющей стали на 1 л вместе с 54 г изобутиральдегида, 300 мл толуола и 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 4240 кПа (602 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 180°С в течение 0,8 часов и выдерживали при 180°С в течение 7 часов. Реакционную смесь охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе, получая 87,5 г вязкой коричневой жидкости. Данные TEOST для полученной реакционной смеси приведены в таблице 5.
Сырой продукт очищали хроматографией на оксиде алюминия при использовании 98:2 гексан:оксид алюминия, выделяя соединение N1,N3-дициклогексил-4-изобутил-6-метил-1,3-бензолдиамина, имевшее характеристики, приведенные далее. В данном веществе содержалось 38% сырой реакционной смеси по данным GC.
1H ЯМР: δ 6,64 с (1H), 6,02 с (1H), 3,24 ушир. (4H; с CD3OD 2H обменом, и иное 2H появляется как 3,15 тт, J1=9,9, J2=3,5 Гц) 2,22 д, J=7,2 Гц (2H), 2,01 с (3H), 2,1-1,1 (21H), 0,92 д, J=7,2 Гц (6H).
3C ЯМР: δ 144,33, 144,26, 132,7, 114,3, 96,0, 52,4, 52,2, 40,4, 33,9, 28,6, 26,3, 25,2, 23,1, 20,9, 16,8, 14,3.
ИК: 3426 см-1 (ср).
В результате той же хроматографической очистки выделяли также соединение N1,N3-дициклогексил-N'-изобутил-4-изобутил-6-метил-1,3-бензолдиамина, имевшее характеристики, приведенные далее. В данном веществе содержалось 16% реакционной смеси по данным GC.
1H ЯМР: δ 6,77 с (1H), 6,44 с (1H), 3,24 ушир. (2H; обменивается с CD3OD 1H, и иное 1H появляется при 3,16 тт, J1=10, J2=4 Гц), 2,76 д, J=7,2 Гц (2 H), 2,60 м (1H), 2,25 д, J=7,2 Гц, 2,15 с (3H), 2,1-1,1 (22H), 0,94 д, J=7,2 Гц (6H), 0,81 д, J=7,2, (6H).
13C ЯМР: δ 148,53, 142,8, 133,2, 123,0, 120,47, 107,44, 62,9, 53,9, 52,4, 40,7, 33,8, 30,0 28,3, 26,63, 26,58, 25,2, 23,2, 21,1, 17,9.
ИК: 3426 см-1 (ср).
Пример 12 - Каталитическое гидрирование соединения, полученного из 2,4-толуолдиамина
Затем 71,5 г N1,N3-дициклогексил-4-метил-1,3-бензолдиамина, описанного в примере 11, помещали в автоклав из нержавеющей стали на 1 л вместе с 79,5 г бензальдегида, 300 мл толуола и дополнительным количеством 2,0 г влажного (в том виде, в котором получали) катализатора из сульфидированной платины на угле. В автоклав нагнетали 3375 кПа (536 фунтов/кв. дюйм) водорода. Реакционную смесь нагревали до 160°С в течение 1,4 часов и выдерживали при 160°С в течение 1 часа. Реакционную смесь охлаждали и фильтровали, а летучие вещества удаляли выпариванием на роторном испарителе, получая 97,4 г жидкости красного цвета. В соединении N1,N3-дициклогексил-4-бензил-6-метил-1,3-бензолдиамина содержалось 69% реакционной смеси по данным GC. Данные TEOST для полученной реакционной смеси приведены в таблице 5.
1H ЯМР: δ 7,24 м (5H), 6,64 с (1H), 6,02 с (1H), 3,78 с (2H), 3,26 тт, J1=10, J2=4 Гц (1H), 3,18 тт, J1=10, J2=4 Гц (1H), 3,0 ушир. (2H, обменивается с CD3OD), 2,04 с (3H), 2,1-1,1 (20H).
13C ЯМР: δ 145,1, 144,8, 141,2, 133,1, 128,86, 128,75, 128,72, 126,3, 113,6, 110,3, 96,1, 52,3, 52,0, 39,9, 34,0, 33,4, 26,4, 26,3, 25,3, 24,9, 16,8.
ИК: 3417 см-1 (ср).
Сравнительный пример А
3-Горлую колбу на 100 мл снабжали верхнеприводной мешалкой, термопарой и вводом азота. В колбу помещали 2,10 г N1,N3-дициклогексил-1,3-бензолдиамина, полученного, как описано в примере 1, 18 мл тетрагидрофурана, 9 мл ксилола и 1,4 мл изобутиральдегида. Смесь нагревали до 52°С и прибавляли триацетоксиборгидрид натрия, 2,06 г, в течение 1,3 часа и перемешивали реакционную смесь в течение 30 минут. Реакционную смесь нагревали до 70°С и добавляли еще 1,39 г триацетоксиборгидрида натрия. Реакционную смесь перемешивали при 70°С в течение 1 ч. Прибавляли еще 0,7 мл изобутиральдегида и 1,04 г триацетоксиборгидрида натрия и перемешивали реакционную смесь в течение 0,7 ч. Реакционную смесь растворяли в ксилоле, экстрагировали водным гидроксидом натрия и дважды промывали водой. Растворитель удаляли выпариванием на роторном испарителе, получая 2,70 г темного масла коричневато-оранжевого цвета. Это масло хроматографировали на оксиде алюминия с использованием гексана.
1H ЯМР: δ 7,03 м (1H), 6,244 с (1H), 6,240 д, J=6,6 Гц (2H), 3,38 м (2H), 2,88 д, J=6 Гц (4H), 1,94 кажущийся септет, J=6,9 Гц (2H) 1,8-1,1 (20H), 0,90 д, J=6,6 Гц (12H).
13C ЯМР: δ 150,78, 129,00, 106,05, 104,11, 60,97, 52,79, 31,44, 26,91, 26,77, 26,35, 21,06.
ИК: N-H отсутствует при 3400 см-1.
По сравнению с примерами 4 и 5 в сравнительном примере А, (N1,N3-дициклогексил-N1,N3-диизобутил-1,3-бензолдиамин) превращал вторичные амины в третичные амины. В сравнительном примере А алкилирования бензола не происходило.
Сравнительный пример В
3-Горлую колбу на 100 мл снабжали верхнеприводной мешалкой, термопарой и вводом азота. В колбу помещали 4,20 г N1,N3-дициклогексил-1,3-бензолдиамина, полученного, как описано в примере 1, 26 мл тетрагидрофурана, 13 мл ксилола и 5,62 г триацетоксиборгидрида натрия. Реакционную смесь нагревали до 40°С и добавляли 2,4 мл гептальдегида в течение 40 минут. Реакционную смесь перемешивали еще в течение 70 минут. Прибавляли еще 0,4 мл гептальдегида и перемешивали реакционную смесь в течение 80 минут. Реакционную смесь растворяли в ксилоле, экстрагировали водным гидроксидом натрия и дважды промывали водой. Растворитель удаляли выпариванием на роторном испарителе, получая 5,60 г масла коричневато-оранжевого цвета. Это масло хроматографировали на оксиде алюминия с использованием смеси 98:2 гексан/этилацетат.
1H ЯМР: δ 7,03 т, J=8,1 Гц (1H), 6,08 м (3H), 3,52 м (2H), 3,10 м (4H), 1,8-1,1 (40H), 0,89 т, J=6,6 Гц (6H).
13C ЯМР: 150,11, 129,73, 101,77, 97,92, 57,80, 45,79, 32,28, 31,21, 30,46, 29,58, 27,69, 26,66, 26,33, 22,92, 14,36.
ИК: N-H отсутствует при 3400 см-1.
По сравнению с примерами 4 и 5 в сравнительном примере В, (N1,N3-дициклогексил-N1,N3-дигептил-1,3-бензолдиамин) превращал вторичные амины в третичные амины. В сравнительном примере В алкилирования бензола не происходило.
Примеры 13-21
Имитационная проверка термо-окисления моторного масла (TEOST)
Состав моторного масла, использованный в данных тестах, включал следующие компоненты, которые являются коммерчески доступными. В контексте настоящего изобретения нет никакого особенного ограничения в отношении типа и точного состава материалов. Иллюстративный тестовый состав является полностью составленным маслом II группы, за исключением АО, составленный с обычными промышленными присадками, описанными выше. Значительное снижение количества отложений, возникающих при использовании циклоалкилбензолдиамина, в соответствии с практикой данного изобретения, было убедительно показано на примере состава моторного масла при помощи имитационной проверки термо-окисления моторного масла при средней-высокой температуре (МНТ-TEOST). Данный тест представляет собой тест с ускоренным окислением. В данном тесте определяют массу отложений, образованных на специально созданном стальном стержне, путем непрерывного воздействия повторяющегося пропускания 8,5 г тестируемого масла в термоокислительных и каталитических условиях. Использованный прибор был произведен Tannas Co. и имел типовую воспроизводимость, равную 0,15(х+16) мг, где х является средним двух или более повторных результатов теста. Условия теста TEOST приведены в таблице 4. Чем меньше количество полученных отложений, тем выше устойчивость масла к окислению.
Вторичный диариламин, использованный в тесте, представлял собой сложную смесь преимущественно моно-, ди- и тринонилдифениламинов, продаваемую в настоящее время под торговым обозначением Naugalube™ 438L, которая коммерчески доступна от Chemtura Corporation. В приведенной далее таблице 5 представлены результаты МНТ-TEOST для масел, содержащих замещенный бензолдиамин из примеров 4-10.
N1,N3-дициклогексил-4,6-дибутил-1,3-бензолдиамин
N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамин
N1,N3-дициклогексил-4-бутил-1,3-бензолдиамин
N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамин
N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамин
N1,N3-дициклогексил-4,6-дибензил-1,3-бензолдиамин
N1,N3-(1,3-диметилбутил)-4,6-дибензил-1,3-бензолдиамин
N1,N3-дициклогексил-4-изобутил-6-метил-1,3-бензолдиамин
N1,N3-дициклогексил-4-бензил-6-метил-1,3-бензолдиамин
Сравнительные примеры С-G
В сравнительном примере С содержание антиокислителя из основания вторичного амина составляло лишь 0,75% от уровня обработки, при отсутствии циклоалкилбензолдиаминовой, сдерживающей образование отложений/антиокислительной, присадки. В сравнительном примере D содержание вторичного амина составляло 1,25%, с заменой дополнительного вторичного дифениламина на сдерживающую образование отложений/антиокислительную присадку на основе бензолдиамина. В сравнительном примере Е содержание антиокислителя из основания вторичного амина составляло 0,75% от уровня обработки, при этом 0,5% антиоксилителя Naugalube™ 531 заменяли на сдерживающую образование отложений/антиокислительную присадку на основе циклоалкилбензолдиамина. Антиокислитель Naugalube™ 531 представляет собой смесь С7-С9 эфиров 3,5-дитретбутилгидроксикоричной кислоты и коммерчески доступен от Chemtura Corporation. В сравнительном примере F содержание антиокислителя из основания вторичного амина составляло 0,75% от уровня обработки, при этом 0,5% антиоксилителя Flexzone™ 4L заменяли на сдерживающую образование отложений/антиокислительную присадку на основе циклоалкилбензолдиамина. Антиокислитель Flexzone™ 4L представляет собой N,N'-бис(метилпентил)парабензолдиамин и коммерчески доступен от Chemtura Corporation. Сравнительный пример G представлял собой наработку иллюстративного тестового состава, полученного без добавления антиокислителя. Результаты МНТ-TEOST представлены в приведенной далее таблице 6.
Количество отложений, полученное в примерах 13-21 изобретения, значительно меньше количества отложений, полученного в сравнительных примерах C-G. Это показывает, что композиции смазочного масла, содержащие соответствующие смеси сочетаний сдерживающих образование отложений/антиокислительных присадок настоящего изобретения, обладают превосходящей устойчивостью к окислению, приводящей к образованию небольших количеств отложений при МНТ-TEOST.
В свете множества изменений и модификаций, которые можно произвести, не выходя из принципов, лежащих в основе настоящего изобретения, следует обратиться к прилагаемой формуле изобретения для понимания рамок защиты, предоставляемых изобретением. Однако то, что заявители предоставляют в своем изобретении, не нужно рассматривать как ограниченное конкретными описанными вариантами осуществления, поскольку данные описанные варианты осуществления считаются иллюстративными, а не ограничивающими. Специалист может произвести изменения, не выходя из сущности данного изобретения. Раскрытия всех патентов, статей и других материалов, описанных здесь, настоящим включены во всей своей полноте в данное описание в виде ссылки. Композиции, описанные как «включающие» большое количество определенных компонентов, следует рассматривать как включающие композиции, полученные при смешивании определенного множества определенных компонентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФОСФИТНЫЕ СТАБИЛИЗАТОРЫ ОСНОВНЫХ КОМПОНЕНТОВ СМАЗОЧНЫХ МАСЕЛ И ТЕРМОПЛАСТИЧЕСКИХ ПОЛИМЕРОВ | 2009 |
|
RU2500683C2 |
| ПОЛИАМИДНЫЕ КОМПОЗИЦИИ С УЛУЧШЕННЫМИ ОПТИЧЕСКИМИ СВОЙСТВАМИ | 2013 |
|
RU2637556C2 |
| СТАБИЛИЗИРОВАННЫЕ КАУЧУКИ | 2015 |
|
RU2672709C1 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2742578C2 |
| ПРОИЗВОДНЫЕ БЕНЗО[1,3]ДИОКСИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ LPAR5 АНТАГОНИСТОВ | 2013 |
|
RU2647727C2 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2597918C2 |
| ПРИМЕНЕНИЕ РЕАГЕНТОВ-СОБИРАТЕЛЕЙ МЕТАЛЛОВ ДЛЯ УДАЛЕНИЯ ОСТАТКОВ РУТЕНИЯ | 2014 |
|
RU2631506C2 |
| ОЛИГОМЕРНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИЯ, СПОСОБ СТАБИЛИЗАЦИИ И ОЛИГОМЕРНЫЕ ПРОДУКТЫ | 1993 |
|
RU2130461C1 |
| АНТИОКСИДАНТЫ | 2009 |
|
RU2496768C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА И ПРОМЕЖУТОЧНОЕ ВЕЩЕСТВО | 2003 |
|
RU2314294C2 |
Изобретение относится к новому способу получения алкилированного 1,3-бензолдиамина структурной формулы II. Соединение алкилированного 1,3-бензолдиамина используют в качестве сдерживающих рост отложений присадок для смазочных масел для органических материалов, включающих смазочное масло, бензин и дизельное топливо. Способ алкилирования соединения 1,3-бензолдиамина включает введение во взаимодействие первого карбонильного соединения с соединением 1,3-бензолдиамина с образованием промежуточного соединения, где первое карбонильное соединение замещено по соответствующим атомам азота 1,3-бензолдиамина, и введение во взаимодействие второго карбонильного соединения с данным промежуточным соединением в присутствии водорода и катализатора гидрирования с образованием алкилированного 1,3-бензолдиамина, где второе карбонильное соединение замещено по центральному ароматическому циклу алкилированного 1,3-бензолдиамина. Алкилированный 1,3-бензолдиамин имеет структуру (II) общей формулы:
 , в которой R1 и R2 независимо выбирают из группы, состоящей из водорода, С1-С20алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила; R3 и R4 независимо выбирают из группы, состоящей из С1-С20алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила; a R5 и R6 независимо выбирают из группы, состоящей из н-пропила, 1-метилэтила, н-бутила, изобутила, втор-бутила, 1,3-диметилбутила, 1,4-диметилпентила, н-пентила, изопентила, 1,5-диметилгексила, гексила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила, циклооктила и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом. Способ позволяет повысить селективность алкилирования по аминогруппам и по бензольному кольцу, получаемые соединения позволяют улучшить устойчивость к окислению смазочных веществ и топлива. 4 з.п. ф-лы, 6 табл. 21 пр.
, в которой R1 и R2 независимо выбирают из группы, состоящей из водорода, С1-С20алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила; R3 и R4 независимо выбирают из группы, состоящей из С1-С20алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила; a R5 и R6 независимо выбирают из группы, состоящей из н-пропила, 1-метилэтила, н-бутила, изобутила, втор-бутила, 1,3-диметилбутила, 1,4-диметилпентила, н-пентила, изопентила, 1,5-диметилгексила, гексила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила, циклооктила и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом. Способ позволяет повысить селективность алкилирования по аминогруппам и по бензольному кольцу, получаемые соединения позволяют улучшить устойчивость к окислению смазочных веществ и топлива. 4 з.п. ф-лы, 6 табл. 21 пр.
1. Способ алкилирования соединения 1,3-бензолдиамина, включающий: введение во взаимодействие первого карбонильного соединения с соединением 1,3-бензолдиамина с образованием промежуточного соединения, где первое карбонильное соединение замещено по соответствующим атомам азота 1,3-бензолдиамина, и введение во взаимодействие второго карбонильного соединения с данным промежуточным соединением в присутствии водорода и катализатора гидрирования с образованием алкилированного 1,3-бензолдиамина, где второе карбонильное соединение замещено по центральному ароматическому циклу алкилированного 1,3-бензолдиамина, в котором алкилированный 1,3-бензолдиамин имеет структуру (II) общей формулы:
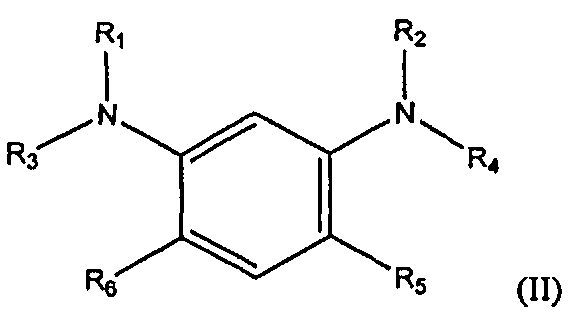
в которой R1 и R2 независимо выбирают из группы, состоящей из водорода, С1-С20алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила;
R3 и R4 независимо выбирают из группы, состоящей из С1-С20 алкила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила и циклооктила; а
R5 и R6 независимо выбирают из группы, состоящей из н-пропила, 1-метилэтила, н-бутила, изобутила, втор-бутила, 1,3-диметилбутила, 1,4-диметилпентила, н-пентила, изопентила, 1,5-диметилгексила, гексила, 2-метилпропенила, бензила, циклопентила, циклогексила, циклогептила, циклооктила и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом.
2. Способ по п.1, в котором
R1 и R2 независимо выбирают из группы, состоящей из водорода, С1-С20алкила, 2-метилпропенила, бензила и циклогексила.
3. Способ по п.1, в котором
R3 и R4 выбирают из группы, состоящей из циклогексила и 1,3-диметилбутила.
4. Способ по п.1, в котором
R5 и R6 независимо выбирают из группы, состоящей из н-пропила, 1-метилэтила, н-бутила, изобутила, втор-бутила, 1,3-диметилбутила, н-пентила, изопентила, гексила, 2-метилпропенила, бензила, циклогексила и водорода, при условии, что, по меньшей мере, один из R5 и R6 не является водородом.
5. Способ по п.1, в котором алкилированный 1,3-бензолдиамин выбирают из группы, состоящей из N1,N3-дициклогексил-4,6-дибутил-1,3-бензолдиамина, N1,N3-дициклогексил-4,6-диизобутил-1,3-бензолдиамина, N1,N3-дициклогексил-4-бутил-1,3-бензолдиамина, N1,N3-(1,3-дициклогексил-4,6-дибензил-1,3-бензолдиамина, N1,N3-(1,3-диметилбутил)-4,6-диизобутил-1,3-бензолдиамина, N1,N3-(1,3-диметилбутил)-4,6-дибутил-1,3-бензолдиамина, N1,N3-(1,3-диметилбутил)-4,6-дибензил-1,3-бензолдиамина и N1,N3-дициклогексил-4-изобутенил-6-изобутил-1,3-бензолдиамина.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| US 5041668 А, 20.08.1991 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| МЕМБРАНА АЭРАТОРА | 2010 |
|
RU2451642C9 |
| Весосортировочный автомат | 1978 |
|
SU699349A2 |
| DVOLAITZKY MAYA ет al | |||
| Stable N,N'-di-tert-butyl-m-phenylenebisnitroxide - unexpected occurrences of ground-state singlets Angew | |||
| Chem | |||
| Int Ed | |||
| Речной батометр | 1921 |
|
SU992A1 |
| US 4900868 A, 13.02.1990 | |||
| СМАЗОЧНОЕ МАСЛО ДЛЯ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 1989 |
|
RU2051170C1 |
| RU 2010128617 А, 12.12.2007. | |||
Авторы
Даты
2013-09-20—Публикация
2008-12-01—Подача