Настоящее изобретение относится к некоторым карбоксамидным производным, к способам их получения, к содержащим их инсектицидным, акарицидным, моллюскоцидным и нематоцидным композициям и к способам их применения для борьбы с насекомыми-, клещами-, моллюсками- и нематодами-вредителями и их уничтожения.
Производные ароматических амидов, обладающие инсектицидной способностью, раскрыты, например, в WO 05/021488 и JP 2006/225340.
Согласно изобретению неожиданно было установлено, что некоторым карбоксамидные производные, которые содержат по меньшей мере одну цианогруппу, тиоцианатную группу, аминотиокарбонил, N-C1-C4-алкиламинотиокарбонил или N,N-ди-C1-C4-алкиламинотиокарбонил в качестве заместителя в центральном ароматическом кольце, обладают инсектицидной способностью.
Поэтому настоящее изобретение относится к соединению формулы (I):
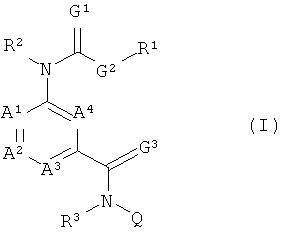
в которой
A1, A2, A3 и A4 независимо друг от друга обозначают C-R4, C-R5 или азот при условии, что по меньшей мере один из A1, A2, A3 и A4 обозначает C-R4 и не более двух из A1, A2, A3 и A4 обозначают азот;
R1 обозначает C1-C6-алкил, C1-C6-галогеналкил, C2-C6-алкенил, C2-C6-галогеналкенил, C2-C6-алкинил, C2-C6-галогеналкинил, C3-C8-циклоалкил, C3-C8-галогенциклоалкил, или
-Е1-Z1-R6, где
Е1 обозначает C1-C4-алкилен, C2-C4-алкенилен, C3-C4-алкинилен, C1-C4-галогеналкилен, C2-C4-галогеналкенилен или C3-C4-галогеналкинилен,
Z1 обозначает -O-, -S-, -SO- или -SO2-, и
R6 обозначает водород, C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C2-C6-галогеналкинил, или
-Е2-R7, где
Е2 обозначает C1-C4-алкилен, C2-C4-алкенилен, C3-C4-алкинилен, C1-C4-галогеналкилен, C2-C4-галогеналкенилен или C3-C4-галогеналкинилен, и R7 обозначает C3-C8-циклоалкил, C3-C8-галогенциклоалкил, цианогруппу, нитрогруппу, гидроксигруппу или фенил или фенил, содержащий от 1 до 5 заместителей R8, которые могут быть одинаковыми или разными, или пиридил или пиридил, содержащий от 1 до 4 заместителей R9, которые могут быть одинаковыми или разными, или тиофенил, или тетрагидрофуранил;
R2 и R3 независимо друг от друга обозначают водород, C1-C4-алкил, C2-C4-алкенил, C2-C4-алкинил, C1-C4-алкилкарбонил, C1-C4-галогеналкилкарбонил, гидроксигруппу, C1-C4-алкилкарбонилоксигруппу, арилкарбонилоксигруппу или арилкарбонилоксигруппу, где арильное кольцо содержит от 1 до 5 заместителей, независимо выбранных из группы, включающей галоген, C1-C4-алкил, C1-C4-галогеналкил, C1-C4-алкоксигруппу или C1-C4-галогеналкоксигруппу;
G1, G2 и G3 независимо друг от друга обозначают кислород или серу;
каждый R4 независимо обозначает цианогруппу, тиоцианатную группу, аминотиокарбонил, N-C1-C4-алкиламинотиокарбонил или N,N-ди-C1-C4-алкиламинотиокарбонил;
каждый R5 независимо обозначает водород, галоген, C1-C4-алкил, C1-C4-галогеналкил или C1-C4-алкоксигруппу;
каждый R8 независимо обозначает галоген, C1-C6-алкил, C1-C6-галогеналкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, цианогруппу, нитрогруппу, гидроксигруппу, C1-C4-алкилкарбонил, C1-C4-галогеналкилкарбонил, C1-C4-алкилкарбонилоксигруппу, C1-C4-алкоксикарбонил или пентафторсульфанил;
каждый R9 независимо обозначает галоген, C1-C6-алкил, C1-C6-галогеналкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, цианогруппу, нитрогруппу, гидроксигруппу, C1-C4-алкилкарбонил, C1-C4-галогеналкилкарбонил, C1-C4-алкилкарбонилоксигруппу, C1-C4-алкоксикарбонил или пентафторсульфанил; и
Q обозначает фрагмент формулы (II) или (III)
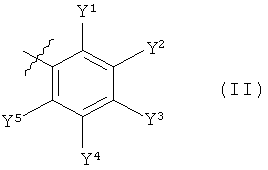
 ,
,
в которых
Y1, Y2, Y4 и Y5 независимо друг от друга обозначают водород, галоген, C1-C6-алкил, C1-C6-галогеналкил, C1-C4-алкокси-C1-C4-алкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, пентафторсульфанил, цианогруппу или нитрогруппу при условии, что не более, чем один из Y1 и Y5 обозначает водород, и
Y3 обозначает C1-C6-галогеналкил, C1-C6-галогеналкоксигруппу, C1-C6-гидроксигалогеналкил, C1-C6-галогеналкилтиогруппу, C1-C6-галогеналкилсульфинил, C1-C6-галогеналкилсульфонил или пентафторсульфанил, или
Y6, Y7 и Y9 независимо друг от друга обозначают водород, C1-C6-алкил, C1-C6-галогеналкил, C1-C4-алкокси-C1-C4-алкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, пентафторсульфанил, цианогруппу или нитрогруппу при условии, что не более, чем один из Y и Y обозначает водород, и
Y8 обозначает C1-C6-галогеналкил, C1-C6-галогеналкоксигруппу, C1-C6-гидроксигалогеналкил, C1-C6-галогеналкилтиогруппу, C1-C6-галогеналкилсульфинил, C1-C6-галогеналкилсульфонил или пентафторсульфанил;
или его соли или N-оксиду.
Соединения формулы (I) могут существовать в виде разных геометрических или оптических изомеров или в разных таутомерных формах. В объем настоящего изобретения входят все такие изомеры и таутомеры и их смеси во всех соотношениях, а также изотопозамещенные формы, такие как дейтерированные соединения.
Каждый алкильный фрагмент, по отдельности или в виде части большей группы (такой как алкоксигруппа, алкоксикарбонил, алкилкарбонил или алкилен), обладает линейной или разветвленной цепью и означает, например, метил, этил, н-пропил, н-бутил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил. Алкильные группы предпочтительно представляют собой C1-C6-алкильные группы, более предпочтительно - C1-C4- и наиболее предпочтительно - C1-C3-алкильные группы. Примерами алкиленовых групп являются метилен, этилен, н- и изопропилен и н-, втор-, изо- и трет-бутилен.
Алкенильные и алкинильные фрагменты (по отдельности или в виде части большей группы, такой как алкенилоксигруппа, алкинилоксигруппа, алкенилен или алкинилен) могут находиться в виде линейных или разветвленных цепей и алкенильные фрагменты, если это является подходящим, могут находиться в (E)-или (Z)-конфигурации. Примерами являются винил, аллил и пропаргил. Алкенильные и алкинильные группы предпочтительно представляют собой C2-C6-алкенильные и алкинильные группы, более предпочтительно - C2-C4- и наиболее предпочтительно - C2-C3, алкенильные и алкинильные группы.
Галоген обозначает фтор, хлор, бром или йод.
Галогеналкильные группы (по отдельности или в виде части большей группы, такой как галогеналкоксигруппа или галогеналкилтиогруппа) представляют собой алкильные группы, которые замещены одним или большим количеством одинаковых или разных атомов галогенов и представляют собой, например, -CF3, -CF2Cl, -CH2CF3 или -CH2CHF2. Перфторалкильные группы (по отдельности или в виде части большей группы, такой как перфторалкилтиогруппа) представляют собой особый тип галогеналкильной группы; они представляют собой алкильные группы, которые полностью замещены атомами фтора, и представляют собой, например, -CF3, -CF2CF3 или -CF(CF3)2.
Гидроксигалогеналкильные группы (по отдельности или в виде части большей группы, такой как гидроксигалогеналкоксигруппа или гидроксигалогеналкилтиогруппа) представляют собой галогеналкильные группы, которые замещены одним или большим количеством гидроксигрупп, например 1,1,1,3,3,3-гексафтор-2-гидрокси-проп-2-ил.
Галогеналкенильные и галогеналкинильные группы (по отдельности или в виде части большей группы, такой как галогеналкенилоксигруппа или галогеналкинилоксигруппа) представляют собой алкенильные и алкинильные группы соответственно, которые замещены одним или большим количеством одинаковых или разных атомов галогенов и представляют собой, например, -CH=CF2, -CCl=CClF или -CClC≡CH.
Циклоалкильные группы могут находиться в моно- или бициклической форме и необязательно могут быть замещены одной или большим количеством метильных групп. Циклоалкильные группы предпочтительно содержат от 3 до 8 атомов углерода, более предпочтительно - от 3 до 6 атомов углерода. Примерами моноциклических циклоалкильных групп являются циклопропил, 1-метилциклопропил, 2-метилциклопропил, циклобутил, циклопентил и циклогексил.
Галогенциклоалкильные группы представляют собой циклоалкильные группы, которые замещены одним или большим количеством одинаковых или разных атомов галогенов и необязательно могут быть замещены одной или большим количеством метильных групп. Примерами моноциклических галогенциклоалкильных групп являются 2,2-дихлорциклопропил, 2,2-дихлор-1-метилциклопропил и 2-хлор-4-фторциклогексил.
В контексте настоящего описания термин "арил" означает кольцевую систему, которая может быть моно-, би- или трициклической. Примеры таких колец включают фенил, нафталинил, антраценил, инденил и фенантренил. Предпочтительной арильной группой является фенил.
Предпочтительные значения A1, A2, A3, A4, R1, R2, R3, G1, G2, G3, R4, R5, Q, Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 в любой комбинации являются такими, как приведенные ниже.
Предпочтительно, если A1 обозначает C-R4 или C-R5.
Предпочтительно, если A2 обозначает C-R4 или C-R5. Предпочтительно, если A3 обозначает C-R4 или C-R5.
Предпочтительно, если A4 обозначает C-R4 или C-R5.
Предпочтительно, если один, два или три из A1, A2, A3 и A4 обозначают C-R4, более предпочтительно, если один или два из A1, A2, A3 и A4 обозначают C-R4, наиболее предпочтительно, если один из A1, A2, A3 и A4 обозначает C-R4.
Предпочтительно, если R1 обозначает C1-C6-алкил, C1-C6-галогеналкил, C2-C6-алкенил, C2-C6-галогеналкенил, C2-C6-алкинил, C2-C6-галогеналкинил, C3-C8-циклоалкил, C3-C8-галогенциклоалкил или циано-C1-C4-алкилен, более предпочтительно - C1-C6-алкил, C1-C6-галогеналкил, C2-C6-алкенил или циано-C1-C4-алкилен, наиболее предпочтительно - метил, этил, 2-фторэтил, 2-хлорэтил, 2-бромэтил, 2-йодэтил, 2-цианоэтил, 2,2-дифторэтил, 2,2-дихлорэтил, 2,2,2-трифторэтил, 2,2,2-трихлорэтил, 2,2,2-трибромэтил, пропил, 3-фторпропил, 3-хлорпропил, 3-бромпропил, 1,2-дифторпроп-2-ил, 1,3-дифторпроп-2-ил, 1,3-дихлорпроп-2-ил, 1-хлор-3-фторпроп-2-ил, 3,3,3-трифторпропил, бутил, 4,4,4-трифторбутил или винил.
Предпочтительно, если R2 обозначает водород, метил, этил, аллил, пропаргил, ацетил, 3,3,3-трихлорпропионил, гидроксигруппу, ацетилоксигруппу или бензоилоксигруппу.
Более предпочтительно, если R2 обозначает водород, метил, этил, аллил, пропаргил, ацетил или гидроксигруппу.
Еще более предпочтительно, если R2 обозначает водород, метил или этил.
Еще более предпочтительно, если R2 обозначает водород или метил.
Наиболее предпочтительно, если R2 обозначает водород.
Предпочтительно, если R3 обозначает водород, метил, этил, аллил, пропаргил, ацетил, гидроксигруппу, ацетилоксигруппу или бензоилоксигруппу.
Более предпочтительно, если R3 обозначает водород, метил, этил, аллил, пропаргил, ацетил или гидроксигруппу.
Еще более предпочтительно, если R3 обозначает водород, метил или этил.
Еще более предпочтительно, если R3 обозначает водород или метил.
Наиболее предпочтительно, если R3 обозначает водород.
Предпочтительно, если G1 обозначает кислород.
Предпочтительно, если G2 обозначает кислород.
Предпочтительно, если G3 обозначает кислород.
Предпочтительно, если каждый R4 независимо обозначает цианогруппу, тиоцианатную группу или аминотиокарбонил, более предпочтительно - цианогруппу или тиоцианатную группу, наиболее предпочтительно - цианогруппу.
Предпочтительно, если каждый R5 независимо обозначает водород, фтор, хлор, бром, метил, трифторметил или метоксигруппу.
Более предпочтительно, если каждый R5 независимо обозначает водород, фтор, хлор, бром, метил или трифторметил.
Еще более предпочтительно, если каждый R5 независимо обозначает водород, фтор, метил или трифторметил.
Еще более предпочтительно, если каждый R5 независимо обозначает водород или фтор.
Наиболее предпочтительно, если каждый R5 обозначает водород.
Предпочтительно, если Q обозначает фрагмент формулы (II).
Предпочтительно, если Y1 обозначает цианогруппу, галоген, метил, этил, трифторметил или метоксиметил.
Более предпочтительно, если Y1 обозначает цианогруппу, бром, хлор, метил, этил, трифторметил или метоксиметил.
Еще более предпочтительно, если Y1 обозначает бром, хлор, метил, этил или метоксиметил.
Еще более предпочтительно, если Y1 обозначает бром, метил или этил.
Еще более предпочтительно, если Y1 обозначает метил или этил.
Наиболее предпочтительно, если Y1 обозначает метил.
Предпочтительно, если Y2 обозначает водород, хлор, фтор или метил.
Наиболее предпочтительно, если Y2 обозначает водород.
Предпочтительно, если Y3 обозначает гептафторпропил, гептафторпроп-2-ил, гептафторпропилтиогруппу, гептафторпропилсульфинил, гептафторпропилсульфонил, гептафторпроп-2-илтиогруппу, гептафторпроп-2-илсульфинил, гептафторпроп-2-илсульфонил или нонафторбут-2-ил.
В одном варианте осуществления Y3 обозначает C2-C6-перфторалкил, более предпочтительно, если Y3 обозначает гептафторпроп-2-ил или нонафторбут-2-ил.
В одном варианте осуществления Y3 обозначает гептафторпроп-2-ил.
В одном варианте осуществления Y3 обозначает нонафторбут-2-ил.
Предпочтительно, если Y4 обозначает водород, хлор, фтор или метил.
Наиболее предпочтительно, если Y4 обозначает водород.
Предпочтительно, если Y5 обозначает цианогруппу, галоген, метил, этил или трифторметил.
Более предпочтительно, если Y5 обозначает цианогруппу, бром, хлор, метил, этил или трифторметил.
Еще более предпочтительно, если Y5 обозначает бром, хлор, метил или этил.
Еще более предпочтительно, если Y5 обозначает бром, метил или этил.
Еще более предпочтительно, если Y5 обозначает метил или этил.
Наиболее предпочтительно, если Y5 обозначает метил.
Предпочтительно, если Y6 обозначает цианогруппу, галоген, метил, этил, трифторметил или метоксиметил.
Более предпочтительно, если Y6 обозначает цианогруппу, бром, хлор, метил, этил, трифторметил или метоксиметил.
Еще более предпочтительно, если Y6 обозначает бром, хлор, метил, этил или метоксиметил.
Еще более предпочтительно, если Y6 обозначает бром, метил или этил.
Еще более предпочтительно, если Y6 обозначает метил или этил.
Наиболее предпочтительно, если Y6 обозначает метил.
Предпочтительно, если Y7 обозначает водород, хлор, фтор или метил.
Наиболее предпочтительно, если Y6 обозначает водород.
Предпочтительно, если Y8 обозначает гептафторпропил, гептафторпроп-2-ил, гептафторпропилтиогруппу, гептафторпропилсульфинил, гептафторпропилсульфонил, гептафторпроп-2-илтиогруппу, гептафторпроп-2-илсульфинил, гептафторпроп-2-илсульфонил или нонафторбут-2-ил.
В одном варианте осуществления Y8 обозначает C2-C6-перфторалкил, более предпочтительно, если Y8 обозначает гептафторпроп-2-ил или нонафторбут-2-ил.
В одном варианте осуществления Y8 обозначает гептафторпроп-2-ил.
В одном варианте осуществления Y8 обозначает нонафторбут-2-ил.
Предпочтительно, если Y9 обозначает цианогруппу, галоген, метил, этил, трифторметил или метоксиметил.
Более предпочтительно, если Y9 обозначает цианогруппу, бром, хлор, метил, этил, трифторметил или метоксиметил.
Еще более предпочтительно, если Y9 обозначает бром, хлор, метил, этил или метоксиметил.
Еще более предпочтительно, если Y9 обозначает бром, метил или этил.
Еще более предпочтительно, если Y9 обозначает метил или этил.
Наиболее предпочтительно, если Y9 обозначает метил.
Предпочтительным вариантом осуществления являются соединения формулы (Ia), в которой A1 обозначает C-CN и A2, A3, A4 обозначают CH.
Предпочтительным вариантом осуществления являются соединения формулы (Ib), в которой A обозначает C-CN и A1, A3 и A4 обозначают CH.
Предпочтительным вариантом осуществления являются соединения формулы (Ic), в которой A обозначает C-CN и A1, A2 и A4 обозначают CH.
Предпочтительным вариантом осуществления являются соединения формулы (Id), в которой A4 обозначает C-CN и A1, A2 и A3 обозначают CH.
В предпочтительном варианте осуществления Q2 обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-этил-6-метил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-диэтил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-метоксиметил-6-метил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-бром-6-метил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-бром-6-этил-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-дихлор-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-дибром-4-(гептафторпроп-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-диметил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-этил-6-метил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-диэтил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-метоксиметил-6-метил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-бром-6-метил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2-бром-6-этил-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-дихлор-4-(нонафторбут-2-ил)-фенил.
В предпочтительном варианте осуществления Q2 обозначает 2,6-дибром-4-(нонафторбут-2-ил)-фенил.
В одном варианте осуществления настоящего изобретения R2 и R3 независимо друг от друга обозначают водород, C1-C4-алкил или C1-C4-алкилкарбонил. Предпочтения для R2 и R3 являются такими же, как указанные для соединений формулы (I), за тем исключением, что R2 и R3 не могут обозначать аллил, пропаргил, гидроксигруппу, ацетилоксигруппу или бензоилоксигруппу.
В одном варианте осуществления настоящего изобретения каждый R5 независимо обозначает водород, галоген, C1-C4-алкил или трифторметил. Предпочтения для R5 являются такими же, как указанные для соединений формулы (I), за тем исключением, что R не может обозначать метоксигруппу.
В одном варианте осуществления настоящего изобретения Y1, Y2, Y4 и Y5 независимо друг от друга обозначают водород, галоген, C1-C6-алкил, C1-C6-галогеналкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, пентафторсульфанил, цианогруппу или нитрогруппу при условии, что не более, чем один из Y1 и Y5 обозначает водород. Предпочтения для Y1, Y2, Y4 и Y5 являются такими же, как указанные для соединений формулы (I), за тем исключением, что Y1 не может обозначать метоксиметил.
В одном варианте осуществления настоящего изобретения Y6, Y7 и Y9 независимо друг от друга обозначают водород, C1-C6-алкил, C1-C6-галогеналкил, C1-C6-алкоксигруппу, C1-C6-галогеналкоксигруппу, C1-C6-алкилтиогруппу, C1-C6-галогеналкилтиогруппу, C1-C6-алкилсульфинил, C1-C6-галогеналкилсульфинил, C1-C6-алкилсульфонил, C1-C6-галогеналкилсульфонил, пентафторсульфанил, цианогруппу или нитрогруппу при условии, что не более чем один из Y6 и Y9 обозначает водород. Предпочтения для Y6, Y7 и Y9 являются такими же, как указанные для соединений формулы (I), за тем исключением, что Y6 не может обозначать метоксиметил.
Соединения, приведенные ниже в таблицах 1-35, иллюстрируют соединения, предлагаемые в настоящем изобретении.
Таблица 1
В таблице 1 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в представленной ниже таблице.
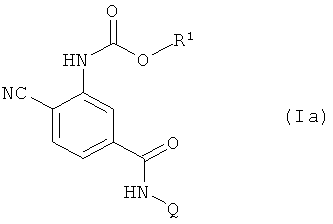
Таблица 2
В таблице 2 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-этил-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 3
В таблице 3 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-диэтил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 4
В таблице 4 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-метоксиметил-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 5
В таблице 5 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-бром-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 6
В таблице 6 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-бром-6-этил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 7
В таблице 7 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-дихлор-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 8
В таблице 8 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-дибром-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 9
В таблице 9 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-диметил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 10
В таблице 10 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-этил-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 11
В таблице 11 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-диэтил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 12
В таблице 12 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-метоксиметил-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 13
В таблице 13 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-бром-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 14
В таблице 14 приведены 24 соединения формулы (Ia), в которой Q обозначает 2-бром-6-этил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 15
В таблице 15 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-дихлор-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 16
В таблице 16 приведены 24 соединения формулы (Ia), в которой Q обозначает 2,6-дибром-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 17
В таблице 17 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил и R1 обладает
значениями, приведенными в таблице 1.

Таблица 18
В таблице 18 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-этил-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 19
В таблице 19 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-диэтил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 20
В таблице 20 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-метоксиметил-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 21
В таблице 21 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-бром-6-метил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 22
В таблице 22 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-бром-6-этил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 23
В таблице 23 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-дихлор-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 24
В таблице 24 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-дибром-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 25
В таблице 25 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-диметил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 26
В таблице 26 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-этил-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 27
В таблице 27 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-диэтил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 28
В таблице 28 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-метоксиметил-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 29
В таблице 29 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-бром-6-метил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 30
В таблице 30 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2-бром-6-этил-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 31
В таблице 31 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-дихлор-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 32
В таблице 32 приведены 24 соединения формулы (Ia'), в которой Q обозначает 2,6-дибром-4-(нонафторбут-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
Таблица 33
В таблице 33 приведены 24 соединения формулы (Ib), в которой Q обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил и R1 обладает значениями, приведенными в таблице 1.
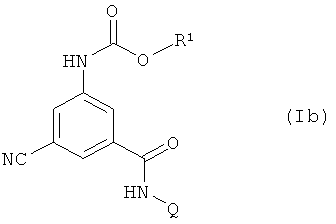
Таблица 34
В таблице 34 приведены 24 соединения формулы (Ic), в которой Q обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил и R1 обладает
значениями, приведенными в таблице 1.
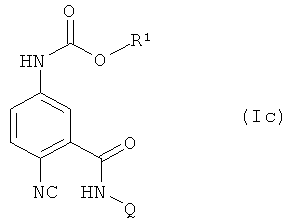
Таблица 35
В таблице 35 приведены 24 соединения формулы (Id), в которой Q обозначает 2,6-диметил-4-(гептафторпроп-2-ил)-фенил и R1 обладает
значениями, приведенными в таблице 1.

Соединения, предлагаемые в настоящем изобретении, можно получть по различным методикам.
1) Соединения формулы (I), в которой G1, G2 и G3 обозначают кислород, можно получить путем обработки соединения формулы (II), в которой G обозначает кислород, хлорформиатом формулы R1-OCOCl.
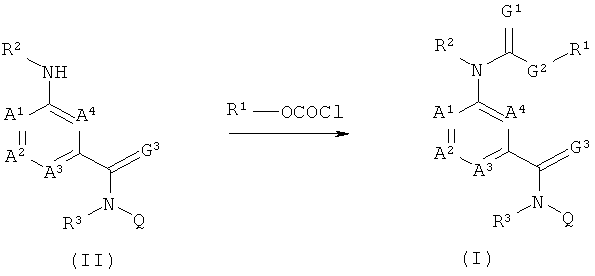
Такие реакции обычно проводят в щелочной среде (например, в присутствии пиридина, триэтиламина, 4-(диметиламино)-пиридина или диизопропилэтиламина), необязательно в присутствии нуклеофильного катализатора, такого как гидроксибензотриазол. Альтернативно, реакцию можно провести в двухфазной системе, содержащей органический растворитель, предпочтительно - этилацетата, и водного растворителя, предпочтительно -раствора гидрокарбоната натрия. Многие хлорформиаты имеются в продаже. Альтернативно, диэфир дикарбоновой кислоты, (R1-OCO)2O, или 1-[(метоксикарбонил)окси]-сукцинимид, R1-OCO-сукцинимид, можно использовать вместо хлорформиат R1-OCOCl.
2) Соединения формулы (II), в которой G обозначает кислород, можно получить путем обработки соединений формулы (III), в которой R обозначает OH, C1-C6-алкоксигруппу или Cl, F или Br с амином формулы NHR3Q.

Если R обозначает ОН такие реакции обычно проводят в присутствии реагента сочетания, такого как ДКК (N,N'-дициклогексилкарбодиимид), ЭДК (1-этил-3-[3-диметиламино-пропил]карбодиимидгидрохлорид) или BOP-Cl (хлорангидрид бис(2-оксо-3-оксазолидинил)фосфоновой кислоты), в присутствии основания, такого как пиридин, триэтиламин, 4-(диметиламино)-пиридин или диизопропилэтиламин, и необязательно в присутствии нуклеофильного катализатора, такого как гидроксибензотриазол. Если R обозначает Cl, такие реакции обычно проводят в щелочной среде (например, в присутствии пиридина, триэтиламина, 4-(диметиламино)-пиридина или диизопропилэтиламина), также необязательно в присутствии нуклеофильного катализатора. Альтернативно, реакцию можно провести в двухфазной системе, содержащей органический растворитель, предпочтительно - этилацетата, и водного растворителя, предпочтительно - раствора гидрокарбоната натрия. Кроме того, реакцию можно провести только с субстратом и реагентом в подходящем растворителе, таком как тетрагидрофуран. Если R обозначает C1-C6-алкоксигруппу, то иногда можно превратить сложный эфир непосредственно в амид путем совместного нагревания эфира и амина в термической реакции.
3) Галогениды кислот формулы (III), в которой G1 обозначает кислород и R обозначает Cl, F или Br, можно получить из карбоновых кислот формулы (III), в которой G1 обозначает кислород и R обозначает ОН, при стандартных условиях, таких как обработка тионилхлоридом или оксалилхлоридом.
4) Карбоновые кислоты формулы (III), в которой G1 обозначает кислород и R обозначает ОН, можно получить из сложных эфиров формулы (III), в которой G1 обозначает кислород и R обозначает C1-C6-алкоксигруппу. Специалисту в данной области техники известно, что существует много методик гидролиза таких эфиров, зависящих от характера алкоксигруппы. Одной широко использующейся методикой проведения такого превращения является обработка эфира гидроксидом щелочного металла, таким как гидроксид натрия, в растворителе, таком как этанол и/или вода.
5) Соединения формулы (III), в которой R обозначает C1-C6-алкоксигруппу, можно получить из соединений формулы (IV) последовательной обработкой спиртом формулы R2-ОН в кислой среде и последующим образованием связи N-R2. Специалисту в данной области техники известно, что существует много опубликованных методик образования этой связи, зависящих от характера заместителя R2.
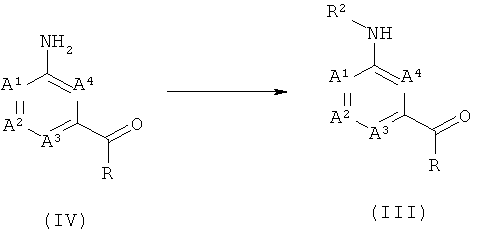
Альтернативно, можно использовать реакции на основе продуктов окисления спирта, таких как соответствующий альдегид и кетон, или на основе в большей степени активированных аналогов спиртов, таких как соответствующий галогенид или сульфонат. Например, восстановительное аминирование можно провести путем обработки амина альдегидом или кетоном и восстановительным реагентом, таким как цианоборогидрид натрия или борогидрид натрия. Альтернативно, алкилирование можно провести путем обработки амина алкилирующим реагентом, таким как алкилгалогенид, необязательно в присутствии основания. Альтернативно, арилирование можно провести путем обработки амина арилгалогенидом или -сульфонатом в присутствии подходящей системы катализатор/лиганд, часто - комплекса палладия(0). Соединения формулы (IV) и спирты формулы R2-ОН являются известными соединениями или их можно получить по методикам, известным специалисту в данной области техники.
6) Соединения формулы (I), в которой G1 и G3 обозначают серу и G2 обозначает кислород, можно получить из соединения формулы (I), в которой G1, G2 и G3 обозначают кислород, путем обработки реагентом, переносящим тиогруппу, таким как реагент Лавессона или пентасульфид фосфора.
7) Альтернативный синтез соединений формулы (II), в которой G3 обозначает кислород и R2 обозначает водород, можно провести путем восстановления нитросоединений формулы (VI), в которой G3 обозначает кислород.
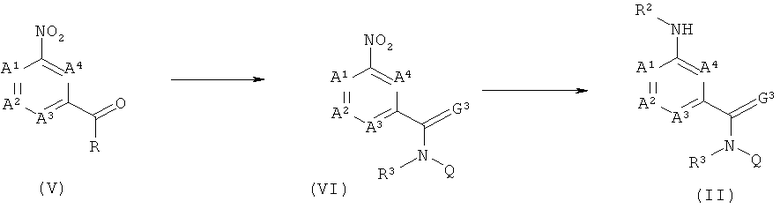
В литературе описано много методик проведения такого превращения, таких как обработка хлоридом олова в кислой среде или гидрирование при катализе благородным металлом, таким как палладий на угле.
8) Соединения формулы (VI), в которой G обозначает кислород, можно получить из соединений формулы (V), в которой R обозначает ОН, C1-C6-алкоксигруппу или Cl, F или Br, путем обработки амином формулы NHR3Q при стандартных условиях, описанных в разделе 2). Соединения формулы (V) являются известными или их можно получить по методикам, известным специалисту в данной области техники.
9) Соединения формулы (I), в которой G3 обозначает серу и G1 и G2 обозначают кислород, можно получить путем обработки соединений формулы (II), в которой G3 обозначает кислород, путем обработки реагентом, переносящим тиогруппу, таким как реагент Лавессона или пентасульфид фосфора, и затем превратить в соединения формулы (I), в которой G3 обозначает серу и G1 и G2 обозначают кислород, как это описано в разделе 1).
10) Соединения формулы (I), в которой G обозначает кислород или серу, G2 и G3 обозначают кислород и R2 обозначает водород, можно получить путем обработки соединения формулы (VII), в которой G обозначает кислород или серу, спиртом формулы R1-ОН.
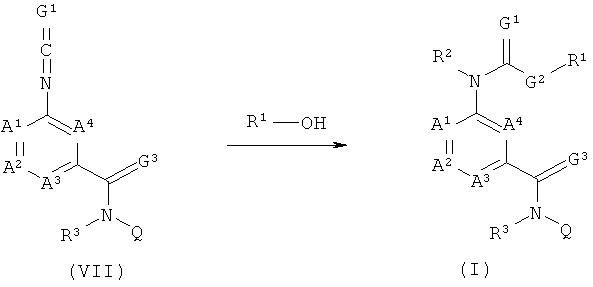
Такие реакции обычно проводят или в самом спирте в качестве растворителя, или в инертном растворителе, таком как дихлорметан, тетрагидрофуран или толуол, необязательно в присутствии основного катализатора (например, в присутствии пиридина, триэтиламина, 4-(диметиламино)-пиридина или диизопропилэтиламина).
11) Соединения формулы (I), в которой G1 обозначает кислород или серу, G2 обозначает серу, G3 обозначает кислород и R2 обозначает водород, можно получить путем обработки соединения формулы (VII), в которой G1 обозначает кислород или серу, меркаптаном формулы R1-SH.

Такие реакции обычно проводят в инертном растворителе, таком как дихлорметан, тетрагидрофуран или толуол, необязательно в присутствии основного катализатора (например, в присутствии пиридина, триэтиламина, 4-(диметиламино)-пиридина или диизопропилэтиламина).
12) Соединения формулы (I), в которой G1 обозначает кислород или серу, G2 и G3 обозначают кислород и R2 обозначает водород, можно получить путем обработки соединения формулы (IX), в которой G1 обозначает кислород или серу, G2 обозначает кислород, R2 обозначает водород и R обозначает ОН, C1-C6-алкоксигруппу или Cl, F или Br, амином формулы NHR3Q при стандартных условиях, описанных в разделе 2).
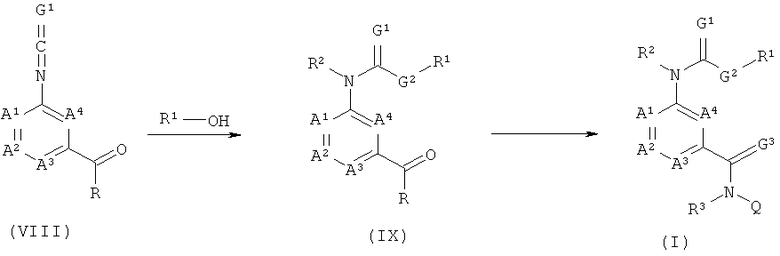
Соединения формулы (IX), в которой G1 обозначает кислород или серу, G2 обозначает кислород и R2 обозначает водород, можно получить из соединений формулы (VIII) по реакции со спиртами формулы R1-ОН, как это описано в разделе 10).
13) Соединения формулы (VII), в которой G1 обозначает кислород или серу, можно получить путем обработки соединения формулы (II), в которой R2 обозначает водород, фосгеном или оксалилхлоридом для соединений формулы (VII), в которой G1 обозначает кислород, или тиофосгеном для соединений формулы (VII), в которой G1 обозначает серу.
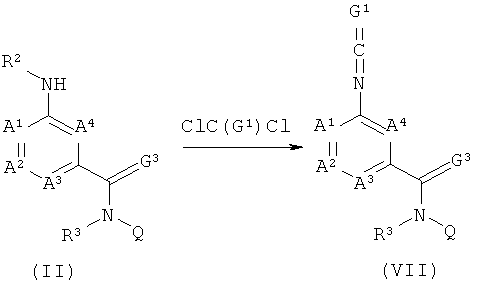
Такие реакции обычно проводят или в инертном растворителе, таком как дихлорметан или толуол, или в двухфазной системе, состоящей из воды и инертного растворителя, необязательно в присутствии основного катализатора (например, в присутствии пиридина, триэтиламина, 4-(диметиламино)-пиридина или диизопропилэтиламина или карбоната, такого как карбонат кальция или гидрокарбонат натрия). Аналогичным образом, соединения формулы (VIII), в которой G1 обозначает кислород или серу, можно получить из соединений формулы (IV).
14) Соединения формулы (V) в которой R4 обозначает цианогруппу, можно получить из соединения формулы (V), в которой LG обозначает галоген, такой как фтор или хлор, по реакции с цианидом, таким как цианид калия, необязательно в присутствии основания, такого как карбонат калия.

Замещение галогена цианидом также можно провести для промежуточных продуктов формулы (VI). В обоих случаях наличие нитрогруппы облегчает замещение отщепляющейся группы цианидным ионом. Аналогичным образом, соединения формулы (V) или (VI), в которой R4 обозначает тиоцианатную группу, можно получить из соединения формулы (V') или (VI'), в которой LG обозначает галоген, такой как йод, фтор или хлор, по реакции с тиоцианатом, таким как тиоцианат калия или тиоцианат меди, как это описано, например, в публикации Journal of the Chemical Society, Chemical Communications, (2), 81-2; 1989 или Synthetic Communications, 10(8), 633-6; 1980.
15) Соединения формулы (V), в которой R обозначает цианогруппу, можно получить, например, из соединения формулы (V), в которой LG обозначает аминогруппу, по реакции с цианидом, таким как цианид меди, по реакции диазотирования. Замещение амина цианидом также можно провести для промежуточных продуктов формулы (VI).
16) Соединения формулы (I), в которой R4 обозначает цианогруппу, можно получить, например, из соединения формулы (II), (III), (IV), (V), (I), (IX), (V), которые содержат галоген в центральном кольце, по реакции с цианидом металла, таким как цианид меди, цианид цинка, или цианид калия, необязательно в присутствии подходящего палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий, и необязательно в присутствии галогенида металла, такого как йодид меди или йодид цинка, в подходящем растворителе, таком как N,N-диметилформамид или N-метилпирролидин. Такие реакции описаны, например, в публикации Organic Process Research & Development (2006), 10(3), 553-555, Synlett (2006), (1), 65-68, Journal of Medicinal Chemistry (2004), 47(8), 1969, Synthetic Communications (1994), 24(6), 887-90, Tetrahedron (2001), 57(8), 1581 и WO 2004067528.
16) Соединения формулы (II), в которой G1 и G2 обозначают кислород и R4 обозначает тиоцианатную группу, можно получить, например, путем обработки соединения формулы (II), в которой R2 обозначает водород и R4 обозначает водород, тиоцианатом в присутствии галогена или эквивалента галогена (N-хлорсукцинимид, N-бромсукцинимид), как это описано, например, в публикации Pest Management Science, 59(1), 25-35; 2003 или Inorganic Chemistry, 44(6), 1837-1845; 2005.
17) Соединения формулы (I), в которой G1 и G2 обозначают кислород и R4 обозначает аминотиокарбонил, можно получить, например, путем обработки соединения формулы (V) или (VI), в которой R4 обозначает цианогруппу, с помощью P4S10 или H2S, как это описано, например, в публикации Journal of Fluorine Chemistry (2006), 127(1), 63-67, и Synthesis (2006), (2), 224-226 или Synthetic Communications (2003), 33(24), 4279-4284. Альтернативно, соединения формулы (I), в которой G1 и G2 обозначают кислород и R4 обозначает аминотиокарбонил можно получить, например, путем обработки соединения формулы (I), в которой R4 обозначает цианогруппу, по реакции с гидросульфидом натрия и хлоридом магния, как это описано, например, в публикации Synthetic Communications (2005), 35(5), 761-764.
18) Соединения формулы (I), в которой G1 и G2 обозначают кислород и R обозначает N-C1-C4-алкиламинотиокарбонил или N,N-ди-C1-C4-алкиламинотиокарбонил, можно получить, например, путем обработки соединения формулы (I), в которой R обозначает аминотиокарбонил, электрофильным реагентом, как это описано, например, в публикации Tetrahedron Letters (1988), 29(15), 1755-8 или, например, путем обработки соединения формулы (I), в которой R4 обозначает аминокарбонил, электрофильным реагентом, как это описано, например, в публикациях Tetrahedron Letters (2000), 41(25), 4933, Journal of Medicinal Chemistry (1975), 18(9), 926, Chemical Communications (Cambridge, United Kingdom) (2006), (23), 2483, Organometallics (2004), 23(8), 1649-1651, Tetrahedron Letters (1994), 35(20), 3313-14, Bulletin of the Chemical Society of Japan (1985), 58(3), 838-43, с последующей обработкой реагентом, переносящим тиогруппу, таким как реагент Лавессона или пентасульфид фосфора.
Соединения формулы (I) можно использовать для борьбы с нашествиями указанных ниже вредителей-насекомых и их уничтожения, таких как чешуекрылые, двукрылые, полужесткокрылые, бахромчатокрылые, прямокрылые, тараканы, жесткокрылые, блохи, перепончатокрылые и термиты, а также другие беспозвоночные вредители, например клещи, нематоды и моллюски. Насекомые, клещи, нематоды и моллюски ниже в настоящем изобретении будут называться вредителями. Вредители, с которыми можно бороться и которых можно уничтожать путем применения соединений, предлагаемых в настоящем изобретении, включают вредителей, связанных с земледелием (этот термин включает выращивание урожая для получения пищевых продуктов и продуктов из волокон), плодоводством и животноводством, домашними животными, лесоводством и хранением продуктов растительного происхождения (таких как плоды, зерно и древесина); вредителей, связанных с повреждением искусственных сооружений и передачей болезней человеку и животным; а также раздражающих вредителей (таких как мухи).
Примеры видов вредителей, бороться в которыми можно с помощью соединений формулы (I), включают Myzus persicae (тля), Aphis gossypii (тля), Aphis fabae (тля), Lygus spp. (клопы), Dysdercus spp. (клопы), Nilaparvata lugens (дельфацид), Nephotettixc incticeps (пикадка), Nezara spp. (щитники), Euschistus spp. (щитники), Leptocorisa spp. (щитники), Frankliniella occidentalis (thrip), Thrips spp. (трипсы), Leptinotarsa decemlineata (колорадский жук), Anthonomus grandis (долгоносик хлопковый), Aonidiella spp. (червецы), Trialeurodes spp. (белокрылки), Bemisia tabaci (белокрылка), Ostrinia nubilalis (мотылек кукурузный), Spodoptera littoralis (гусеница совки хлопковой), Heliothis virescens (гусеница табачной листовертки-почкоеда), Helicoverpa armigera (коробочный червь), Helicoverpa zea (коробочный червь), Sylepta derogata (листовертка хлопковая), Pieris brassicae (капустница), Plutella xylostella (моль капустная), Agrotis spp. (совки), Chilo suppressalis (сверлильщик рисовый стеблевой), Locusta migratoria (саранча), Chortiocetes terminifera (саранча), Diabrotica spp. (листоеды), Panonychus ulmi (клещ красный плодовый), Panonychus citri (клещик красный цитрусовый), Tetranychus urticae (клещ двупятнистый паутинный), Tetranychus cinnabarinus (клещ паутинный красный), Phyllocoptruta oleivora (клещ ржавчинный (ржавый) цитрусовый), Polyphagotarsonemus latus (широкий клещ), Brevipalpus spp.(плоские клещи), Boophilus microplus (клещ боофилюс), Dermacentor variabilis (иксодовый клещ собачий), Ctenocephalids felis (блоха кошачья), Liriomyza spp. (минирующие мушки), Musca domestica (муха комнатная), Aedes aegypti (комар), Anopheles spp. (кровососущие комары), Culex spp. (кровососущие комары), Lucillia spp. (мясные мухи), Blattella germanica (таракан), Periplaneta americana (таракан), Blatta orientalis (таракан), термиты семейства Mastotermitidae (например, Mastotermes spp.), семейства Kalotermitidae (например, Neotermes spp.), семейства Rhinotermitidae (например Coptotermes formosanus, Reticulitermes flavipes, R. speratu, R. virginicus, R. hesperus и R. santonensis) и семейства Termitidae (например, Globitermes sulphurous), Solenopsis geminata (огненный муравей), Monomorium pharaonis (фараонов муравей), Damalima spp. и Linognathus spp. (пухоеды и вши соответственно), Meloidogyne spp. (корневые нематоды), Globodera spp. и Heterodera spp.(гетеродериды), Pratylenchus spp. (повреждающие растения нематоды), Rhodopholus spp. (банановые норовые или сверлящие нематоды), Tyienchulus spp. (цитрусовые нематоды), Haemonchus contortus (гемонхус), Caenorhabditis elegans (уксусная нематода), Trichostrongylus spp. (желудочно-кишечные нематоды) и Deroceras reticulatum (слизень).
Поэтому настоящее изобретение относится к способу борьбы с насекомыми, клещами, нематодами и моллюсками или их уничтожения, который включает нанесение инсектицидно, акарицидно, нематоцидно или моллюскоцидно эффективного количества соединения формулы (I) или композиции, содержащей соединение формулы (I), на вредителей, на очаг вредителей, предпочтительно - на растения или на растения, подверженные нашествию вредителей. Соединения формулы (I) предпочтительно использовать против насекомых, клещей или нематод.
При использовании в настоящем изобретении термин "растение" включает сеянцы, кустарники и деревья.
Для нанесения соединения формулы (I) в виде инсектицида, акарицида, нематоцида или моллюскоцида на вредителей, на очаг вредителей или на растения, подверженные нашествию вредителей, соединение формулы (I) обычно вносят в композицию, которая в дополнение к соединению формулы (I) включает подходящий инертный разбавитель или носитель и необязательно поверхностно-активное вещество (ПАВ). ПАВ являются химикатами, которые способны изменять свойства границы раздела (например, границ раздела жидкость/твердое вещество, жидкость/воздух или жидкость/жидкость) путем снижения поверхностного натяжения, что приводит к изменениям других свойств (например, диспергирования, эмульгирования и смачивания). Предпочтительно, чтобы все композиции (и твердые, и жидкие препараты) включали, в мас.%, от 0,0001 до 95%, более предпочтительно - от 1 до 85%, например от 5 до 60% соединения формулы (I). Композицию обычно применяют для борьбы с вредителями таким образом, чтобы соединение формулы (I) наносилось в количестве, составляющем от 0,1 г до 10 кг на гектар, предпочтительно - от 1 г до 6 кг на гектар, более предпочтительно - от 1 г до 1 кг на гектар.
При использовании для протравливания семян соединение формулы (I) применяется в количестве, составляющем от 0,0001 до 10 г (например, 0,001 г или 0,05 г), предпочтительно - от 0,005 до 10 г, более предпочтительно - от 0,005 до 4 г на 1 кг семян.
Другой вариант выполнения настоящего изобретения относится к инсектицидной, акарицидной, нематоцидной или моллюскоцидной композиции, включающей инсектицидно, акарицидно, нематоцидно или моллюскоцидно эффективное количество соединения формулы (I) и его подходящий носитель или разбавитель. Композиция предпочтительно является инсектицидной, акарицидной, нематоцидной или моллюскоцидной композицией.
Композиции можно выбрать из целого ряда препаратов, включая порошки для опыления (ПО), растворимые порошки (РП), растворимые в воде гранулы (ВГ), диспергирующиеся в воде гранулы (ДГ), смачивающиеся порошки (СП), гранулы (ГР) (с медленным или быстрым выделением), растворимые концентраты (РК), смешивающиеся с маслом жидкости (МЖ), жидкости сверхмалого объема (ЖС), эмульгирующиеся концентраты (ЭК), диспергирующиеся концентраты (ДК), эмульсии (и масло-в-воде (ЭМ), и вода-в-масле (ЭВ)), микроэмульсии (МЭ), концентраты суспензий (СК), аэрозоли, препараты для мелкокапельного опрыскивания/фумигации, капсулированные суспензии (КС) и препараты для обработки семян. Выбранный тип композиции в любом случае будет зависеть от конкретного назначения и физических, химических и биологических характеристик соединения формулы (I).
Порошки для опыления (ПО) можно получить путем смешивания соединения формулы (I) с одним или большим количеством твердых разбавителей (например, природными глинами, каолином, пирофиллитом, бентонитом, оксидом алюминия, монтмориллонитом, кизельгуром, мелом, диатомовой землей, фосфатами кальция, карбонатами кальция и магния, серой, гидроксидом кальция, разными типами муки, тальком и другими органическими и неорганическими твердыми носителями) и механического размола смеси в тонкоизмельченный порошок.
Растворимые порошки (РП) можно получить путем смешивания соединения формулы (I) с одним или большим количеством растворимых в воде неорганических солей (таких как бикарбонат натрия, карбонат натрия или сульфат магния) или с одним или большим количеством растворимых в воде органических твердых веществ (таких как полисахарид) и, необязательно, с одним или большим количеством смачивающих агентов, с одним или большим количеством диспергирующих агентов или смесью таких агентов для улучшения диспергируемости/растворимости в воде. Затем смесь размалывают в тонкоизмельченный порошок. Аналогичные композиции также можно гранулировать с получением растворимых в воде гранул (ВГ).
Смачивающиеся порошки (СП) можно получить путем смешивания соединения формулы (I) с одним или большим количеством твердых разбавителей или носителей, с одним или большим количеством смачивающих агентов, с одним или большим количеством диспергирующих агентов и, необязательно, с одним или большим количеством суспендирующих агентов для облегчения диспергирования в жидкостях. Затем смесь размалывают в тонкоизмельченный порошок. Аналогичные композиции также можно гранулировать с получением диспергирующихся в воде гранул (ВГ).
Гранулы (ГР) можно получить или путем гранулирования смеси соединения формулы (I) с одним или большим количеством порошкообразных твердых разбавителей или носителей, или из предварительно сформованных не содержащих активного ингредиента гранул путем абсорбции соединения формулы (I) (или его раствора в подходящем агенте) в пористом гранулированном материале (таком как пемза, аттапульгитовые глины, фуллерова земля, кизельгур, диатомовая земля или размолотые кукурузные кочерыжки) или путем адсорбции соединения формулы (I) (или его раствора в подходящем агенте) в твердом наполнителе (таком как песок, силикаты, неорганические карбонаты, сульфаты или фосфаты) с проведением сушки в случае необходимости. Агенты, которые обычно применяются для содействия абсорбции или адсорбции, включают растворители (такие как алифатические и ароматические нефтяные растворители, спирты, простые эфиры, кетоны и сложные эфиры) и склеивающие агенты (такие как поливинилацетаты, поливиниловые спирты, декстрины, сахара и растительные масла). В гранулы также можно включить одну или большее количество других добавок (например, эмульгирующий агент, смачивающий агент или диспергирующий агент).
Диспергирующиеся концентраты (ДК) можно получить путем растворения соединения формулы (I) в воде или органическом растворителе, таком как кетон, спирт или простой эфир гликоля. Эти растворы могут содержать поверхностно-активное вещество (например, для улучшения разбавления водой или предотвращения кристаллизации в баке для опрыскивания).
Эмульгирующиеся концентраты (ЭК) или эмульсии масло-в-воде (ЭМ) можно получить путем растворения соединения формулы (I) в органическом растворителе (необязательно содержащем один или большее количество смачивающих агентов, один или большее количество эмульгирующих агентов или смесь таких агентов). Подходящие для использования в ЭК органические растворители включают ароматические углеводороды (такие как алкилбензолы или алкилнафталины, примерами которых являются SOLVESSO 100, SOLVESSO 150 и SOLVESSO 200; SOLVESSO является зарегистрированным товарным знаком), кетоны (такие как циклогексанон или метилциклогексанон) и спирты (такие как бензиловый спирт, фурфуриловый спирт или бутанол), N-алкилпирролидоны (такие как N-метилпирролидон или N-октилпирролидон), диметиламиды жирных кислот (такие как диметиламид жирной кислоты C8-C10) и хлорированные углеводороды. Готовый ЭК может самопроизвольно эмульгироваться при добавлении к воде с образованием эмульсии, обладающей достаточной стабильностью, чтобы с помощью подходящего оборудования было возможно проведение опрыскивания. Получение ЭМ включает получение соединения формулы (I) в виде жидкости (если при комнатной температуре оно не является жидкостью, то его можно расплавить при подходящей температуре, обычно ниже 70°C) или раствора (путем растворения в подходящем растворителе) с последующим эмульгированием полученной жидкости или раствора в воде, содержащей одно или большее количество ПАВ, при большом сдвиговом усилии, с получением эмульсии. Подходящие для использования в ЭМ растворители включают растительные масла, хлорированные углеводороды (такие как хлорбензолы), ароматические растворители (такие как алкилбензолы или алкилнафталины) и другие подходящие органические растворители, которые обладают низкой растворимостью в воде.
Микроэмульсии (МЭ) можно получить путем смешивания воды со смесью одного или большего количества растворителей с одним или большим количеством ПАВ для обеспечения самопроизвольного образования термодинамически стабильной изотропной жидкости. Соединение формулы (I) первоначально содержится или в воде, или в смеси растворитель/ПАВ. Подходящие для использования в МЭ растворители включают описанные выше для применения в ЭК или ЭМ. МЭ может представлять собой систему масло-вводе или вода-в-масле (определить тип имеющейся системы можно путем измерения электропроводности) и она может быть подходящей для смешивания растворимых в воде и растворимых в масле пестицидов в одном и том же препарате. МЭ пригодна для разбавления водой, в которой она остается микроэмульсией или образует обычную эмульсию масло-в-воде.
Концентраты суспензий (СК) могут включать водные или неводные суспензии тонкоизмельченных твердых частиц соединения формулы (I). СК можно получить путем размола на шаровой или бисерной мельнице твердого соединения формулы (I) в подходящей среде, необязательно с одним или большим количеством диспергирующих агентов и получить тонкоизмельченную суспензию соединения. В композицию можно включить один или большее количество смачивающих агентов и можно включить суспендирующий агент для снижения скорости оседания частиц. Альтернативно, соединение формулы (I) можно подвергнуть сухому размолу и прибавить к воде, содержащей описанные выше агенты, и получить искомый готовый продукт.
Аэрозольные препараты включают соединение формулы (I) и подходящий пропеллент (например, н-бутан). Соединение формулы (I) также можно растворить или диспергировать в подходящей среде (например, в воде или смешивающейся с водой жидкости, такой как н-пропанол) и получить композиции для использования в не находящихся под давлением емкостях для распыления, действующих с помощью ручных насосов
Соединение формулы (I) можно в сухом виде смешать с пиротехнической смесью и получить композицию, пригодную для образования в закрытом пространстве дыма, содержащего соединение.
Капсулированные суспензии (КС) можно получить способом, сходным со способом получения препаратов ЭМ, но с включением дополнительной стадии полимеризации, так чтобы образовалась водная дисперсия капелек масла, в которой каждая капелька масла капсулирована с помощью полимерной оболочки и содержит соединение формулы (I) и необязательно его носитель или разбавитель. Полимерную оболочку можно получить с помощью межфазной реакции поликонденсации или по методике коацервации. Композиции могут использоваться для регулируемого выделения соединения формулы (I) и их можно использовать для обработки семян. Соединение формулы (I) также можно включить в биологически разлагающуюся полимерную матрицу и обеспечить медленное, регулируемое выделение соединения.
Композиция может включать одну или большее количество добавок для улучшения биологических рабочих характеристик композиции (например, путем улучшения смачивания, удерживания или распределения на поверхностях; стойкости к воздействию дождя на обработанные поверхности; или впитывания или подвижности соединения формулы (I)). Такие добавки включают поверхностно-активные вещества, добавки для опрыскивания на основе масел, например некоторых минеральных масел или натуральных растительных масел (таких как соевое масло и рапсовое масло), и их смеси с другими усиливающими биологическое воздействие вспомогательными веществами (ингредиентами, которые могут содействовать воздействию соединения формулы (I) или изменять его воздействие).
Соединение формулы (I) также можно приготовить для применения в качестве средства обработки семян, например, в виде порошкообразной композиции, такой как порошок для сухой обработки семян (ПС), растворимый в воде порошок (ВП) или диспергирующийся в воде порошок для обработки взвесью (ДП), или в виде жидкой композиции, такой как текучий концентрат (ТК), раствор (PC) или капсулированная суспензия (КС). Получение композиций ПС, ВП, ДП, ТК и PC является очень сходным с получением описанных выше композиций ПО, РП, СП, СК и ДК соответственно. Композиции для обработки семян могут включат агент, способствующий адгезии композиции к семенам (например, минеральное масло или пленкообразующее защитное вещество).
Смачивающие агенты, диспергирующие агенты и эмульгирующие агенты могут представлять собой ПАВ катионогенного, анионогенного, амфотерного или неионогенного типа.
Подходящие ПАВ катионогенного типа включают четвертичные аммониевые соединения (например, цетилметиламмонийбромид), имидазолины и соли аминов.
Подходящие анионогенные ПАВ включают соли щелочных металлов жирных кислот, соли алифатических моноэфиров серной кислоты (например, лаурилсульфат натрия), соли сульфированных ароматических соединений (например, додецилбензолсульфонат натрия, додецилбензолсульфонат кальция, бутилнафталинсульфонат и смеси диизопропил- и триизопропилнафталинсульфонатов натрия), сульфаты простых эфиров, сульфаты простых эфиров спиртов (например, лаурет-3-сульфат натрия), карбоксилаты простых эфиров (например, лаурет-3-карбоксилат натрия), фосфатные сложные эфиры (продукты реакции одного или большего количества жирных спиртов с фосфорной кислотой (преимущественно сложные моноэфиры) или с пентаоксидом фосфора (преимущественно сложные диэфиры), например, продукты реакции лаурилового спирта с тетрафосфорной кислотой; эти продукты также могут быть этоксилированы), сульфосукцинаматы, сульфонаты парафинов или олефинов, таураты и лигносульфонаты.
Подходящие ПАВ амфотерного типа включают бетаины, пропионаты и глицинаты.
Подходящие ПАВ неионогенного типа включают продукты конденсации алкиленоксидов, таких как этиленоксид, пропиленоксид, бутиленоксид, или их смесей с жирными спиртами (такими как олеиловый спирт или цетиловый спирт) или с алкилфенолами (такими как октилфенол, нонилфенол или октилкрезол); частичные сложные эфиры, полученные из жирных кислот с длинными цепями или ангидридов гексита; продукты конденсации указанных частичных сложных эфиров с этиленоксидом; блок-полимеры (включающие этиленоксид и пропиленоксид); алканоламины; обычные сложные эфиры (например, полиэтиленгликолевые эфиры жирных кислот); оксиды аминов (например, лаурилдиметиламиноксид); и лецитины.
Подходящие суспендирующие агенты включают гидрофильные коллоиды (такие как полисахариды, поливинилпирролидон или натриевая соль карбоксиметилцеллюлозы) и набухающие глины (такие как бентонит или аттапульгит).
Соединение формулы (I) можно вносить любыми известными способами применения пестицидных соединений. Например, его можно нанести, одно или в композиции, на вредителей или на очаг вредителей (такой как местообитание вредителей или на выращиваемое растение, подверженное заражению врредителями), на любую часть растения, включая листву, стебли, ветви или корни, на семена перед их высеванием или на другие среды, в которых произрастает или должно быть посеяно растение (такие как почва, окружающая корни, почва в целом, вода для затопления или гидропонные системы выращивания) непосредственно или его можно вносить путем разбрызгивания, опыления, наносить погружением, вносить в виде препарата, представляющего собой крем или пасту, вносить в виде паров или вносить путем распределения композиции (такой как гранулированная композиция или композиция, упакованная в растворимый в воде пакет) в почве или в водной среде или включения в нее.
Соединение формулы (I) также можно ввести в растения путем инъекции или опрыскивания растительного покрова с использованием электродинамических методик опрыскивания или других малообъемных методик или внести с помощью наземных или авиационных систем орошения.
Композиции для применения в качестве водных препаратов (водных растворов или дисперсий) обычно поставляются в виде концентрата, содержащего значительную долю активного ингредиента, и перед применением концентрат прибавляют к воде. Эти концентраты, которые могут представлять собой ДК, СК, ЭК, ЭМ, МЭ ВГ, РП, СП, ДГ и КС, часто должны выдерживать хранение в течение продолжительных периодов времени и после такого хранения после прибавления к воде должны быть способны образовывать водные препараты, которые остаются однородными в течение времени, достаточного для того, чтобы их можно было вносить с помощью обычного оборудования для разбрызгивания. Такие водные препараты могут содержать разные количества соединения формулы (I) (например, от 0,0001 до 10 мас.%) в зависимости от цели их применения.
Соединение формулы (I) можно применять в смесях с удобрениями (например, азот-, калий- или фосфорсодержащими удобрениями). Подходящие типы препаратов включают гранулы удобрения. Предпочтительно, чтобы смеси содержали до 25 мас.% соединения формулы (I).
Поэтому настоящее изобретение также относится к композиции удобрения, содержащей удобрение и соединения формулы (I).
Композиции, предлагаемые в настоящем изобретении, могут содержать другие соединения, обладающие биологической активностью, например микроудобрения или соединения, обладающие фунгицидной активностью или обладающие регулирующей рост растения, гербицидной, инсектицидной, нематоцидной или акарицидной активностью.
Соединение формулы (I) может являться единственным активным ингредиентом композиции или оно может быть смешано с одним или большим количеством дополнительных активных ингредиентов, таких как пестицид, фунгицид, синергетик, гербицид или регулятор роста растений, если это целесообразно. Дополнительный активный ингредиент может: давать композицию, обладающую более широким спектром активности или повышенной устойчивостью в очаге распространения; усиливать воздействие или дополнять воздействие (например, путем увеличения скорости воздействия или преодоления невосприимчивости) соединения формулы (I); или способствовать преодолению или предупреждению развития резистентности по отношению к отдельным компонентам. То, какой конкретный дополнительный активный ингредиент будет использоваться, зависит от назначения композиции. Примерами подходящих пестицидов являются следующие:
а) пиретроиды, такие как перметрин, циперметрин, фенвалерат, эсфенвалерат, дельтаметрин, цигалотрин (в частности, лямбда-цигалотрин), бифентрин, фенпропратрин, цифлутрин, тефлутрин, безопасные для рыб пиретроиды (например, этофенпрокс), натуральный пиретрин, тетраметрин, s-биоаллетрин, фенфлутрин, праллетрин и 5-бензил-3-фурилметил-(Е)-(1R,3S)-2,2-диметил-3-(2-оксотиолан-3-илиденметил)циклопропанкарбоксилат;
b) фосфорорганические соединения, такие как профенофос, сулпрофос, ацефат, метилпаратион, азинфос-метил, деметон-s-метил, гемтенофос, тиометон, фенамифос, монокротофос, профенофос, триазофос, метамидофос, диметоат, фосфамидон, малатион, хлорпирифос, фосалон, тербуфос, фенсульфотион, фонофос, форат, фоксим, пиримифос-метил, пиримифос-этил, фенитротион, фостиазат и диазинон;
c) карбаматы (включая арилкарбаматы), такие как пиримикарб, тиазамат, клоэтокарб, карбофуран, фуратиокарб, этиофенкарб, алдикарб, тиофурокс, карбосульфан, бендиокарб, фенобукарб, пропоксур, метомил и оксамил;
d) бензоилмочевины, такие как дифлубензурон, трифлумурон, гексафлумурон, флуфеноксурон и хлорфлуазурон;
e) органические соединения олова, такие как цигексатин, фенбутатиноксид и азоциклотин;
f) пиразолы, такие как тебуфенпирад и фенпироксимат;
g) макролиды, такие как авермектины и милбемицин, например, абамектин, эмамектинбензоат, ивермектин, милбемицин, спиносад и азадирахтин;
h) гормоны и феромоны;
i) хлорорганические соединения, такие как эндосульфан, бензолгексахлорид, ДДТ, хлордан и диэлдрин;
j) амидины, такие как хлордимеформ и амитраз;
k) фумиганты, такие как хлорпикрин, дихлорпропан, метилбромид и метам:
l) неоникотиноиды, такие как имидаклоприд, тиаклоприд, ацетамиприд, нитенпирам, динотефуран и тиаметоксам;
m) диацилгидразины, такие как тебуфенозид, хромафенозид и метоксифенозид;
n) дифениловые эфиры, такие как диофенолан и пирипроксифен;
о) индоксакарб;
р) Хлорфенапир;
q) пиметрозин;
r) спиротетрамат, спиродиклофен или спиромезифен; или
s) флубендиамид и ринаксипир.
В дополнение к основным классам пестицидов, перечисленным выше, в композициях можно использовать другие пестициды, воздйествующие на определенных вредителей, если это целесообразно для применения композиции по назначению. Например, для риса можно использовать инсектициды, селективные для конкретных культур, например специфичные по отношению к стеблевым пилильщикам инсектициды (такие как картап) или специфичные для амбаров инсектициды (такие как бупрофезин). Альтернативно, в композицию также можно включать инсектициды или акарициды, специфичные для конкретных видов/стадий развития насекомых (например, акарицидные оволарвициды, такие как клофентезин, флукбензимин, гекситиазокс или тетрадифон; акарицидные мотилициды, такие как дикофол или пропаргит; акарициды, такие как бромпропилат или хлорбензилат; или регуляторы роста, такие как гидраметилнон, циромазин, метопрен, хлорфлуазурон или дифлубензурон).
Примерами фунгицидных соединений, которые можно включать в композицию, предлагаемую в настоящем изобретении, являются (Е)-N-метил-2-[2-(2,5-диметилфеноксиметил)фенил]-2-метоксииминоацетамид (SSF-129), 4-бром-2-циано-N,N-диметил-6-трифторметилбензимидазол-1-сульфонамид, α-[N-(3-хлор-2,6-ксилил)-2-метоксиацетамидо]-γ-бутиролактон, 4-хлор-2-циано-N,N-диметил-5-п-толилимидазол-1-сульфонамид (IKF-916, цианамидазосульфамид), 3-5-дихлор-N-(3-хлор-1-этил-1-метил-2-оксопропил)-4-метилбензамид (RH-7281, зоксамид), N-аллил-4,5,-диметил-2-триметилсилилтиофен-3-карбоксамид (MON65500), N-(1-циано-1,2-диметилпропил)-2-(2,4-дихлорфенокси)пропионамид (AC382042), N-(2-метокси-5-пиридил)-циклопропанкарбоксамид, ацибензолар (CGA245704), аланикарб, алдиморф, анилазин, азаконазол, азоксистробин, беналаксил, беномил, билоксазол, битертанол, бластицидин S, бромуконазол, бупиримат, каптафол, каптан, карбендиазим, карбендиазимхлоргидрат, карбоксин, карпропамид, карвон, CGA41396, CGA41397, хинометионат, хлорбензтиазон, хлороталонил, хлорозолинат, клозилакон, содержащие медь соединения, такие как оксихлорид меди(II), оксихинолат меди(II), сульфат меди(II), таллат меди(II) и бордосская жидкость, циамидазосульфамид, циазофамид (IKF-916), цимоксанил, ципроконазол, ципродинил, дебакарб, ди-2-пиридилдисульфид-1,1'-диоксид, дихлофлуанид, дикломезин, диклоран, диэтофенкарб, дифеноконазол, дифензокват, дифлуметорим, O,O-диизопропил-S-бензилтиофосфат, димефлуазол, диметконазол, диметоморф, диметиримол, диниконазол, динокап, дитианон, додецилдиметиламмонийхлорид, додеморф, додин, догуадин, эдифенфос, эпоксиконазол, этиримол, этил-(Z)-N-бензил-N([метил(метилтиоэтилиденаминооксикарбонил)амино]тио)-β-аланинат, этридиазол, фамоксадон, фенамидон (RPA407213), фенаримол, фенбуконазол, фенфурам, фенгексамид (KBR2738), фенпиклонил, фенпропидин, фенпропиморф, фентинацетат, фентингидроксид, фербам, феримзон, флуазинам, флудиоксонил, флуметовер, флуороимид, флуквинконазол, флусилазол, флутоланил, флутриафол, фолпет, фуберидазол, фуралаксил, фураметпир, гуазатин, гексаконазол, гидроксиизоксазол, гимексазол, имазалил, имибенконазол, иминоктадин, иминоктадинтриацетат, ипконазол, ипробенфос, ипродион, ипроваликарб (SZX0722), изопропанилбутилкарбамат, изопротиолан, касугамицин, крезоксим-метил, LY 186054, LY 211795, LY 248908, манкозеб, манеб, мефеноксам, мепанипирим, мепронил, металаксил, метконазол, метирам, метирам-цинк, метоминостробин, миклобутанил, неоасозин, диметилдитиокарбамат никеля, нитротал-изопропил, нуаримол, офурац, ртутьорганические соединения, оксадиксил, оксасульфурон, оксолиновая кислота, окспоконазол, оксикарбоксин, пефуразоат, пенконазол, пенкикурон, феназиноксид, фосетил-Al, фосфорсодержащие кислоты, фталид, пикоксистробин (ZA1963), полиоксин D, полирам, пробеназол, прохлораз, процимидон, пропамокарб, пропиконазол, пропинеб, пропионовая кислота, пиразофос, пирифенокс, пириметанил, пироквилон, пироксифур, пирролнитрин, четвертичные аммониевые соединения, хинометионат, хиноксифен, хинтозен, сипконазол (F-155), пентахлорфенат натрия, спироксамин, стрептомицин, сера, тебуконазол, теклофталам, текназен, тетраконазол, тиабендазол, тифлузамид, 2-(тиоцианметилтио)бензотиазол, тиофанат-метил, тирам, тимибенконазол, толклофос-метил, толилфлуанид, триадимефон, триадименол, триазбутил, триазоксид, трициклазол, тридеморф, трифлоксистробин (CGA279202), трифорин, трифлумизол, тритиконазол, валидамицин A, вапам, винклозолин, зинеб и зирам.
Соединения формулы (I) можно смешивать с почвой, торфом или другими средами для укоренения с целью защиты растений от распространяемых семенами, передаваемых через почву или листовых грибковых болезней.
Примеры синергистов, подходящих для применения в композициях, включают пиперонилбутоксид, сесамекс, сафроксан и додецилимидазол.
То, какие гербициды и регуляторы роста растений окажутся подходящими дял включения в композиции, будет зависеть от объекта воздействия и необходимого эффекта.
Примером селективного гербицида для риса, который можно включить, является пропанил. Примером регулятора роста растений, предназначенного для хлопка, является PIX™.
Некоторые смеси могут включать активные ингредиенты, которые обладают существенно иными физическими, химическими или биологическими характеристиками, так что сами по себе они нелегко включаются в такой же обычный тип препарата. В таких случаях можно получить другие типы препаратов. Например, если один активный ингредиент представляет собой нерастворимое в воде твердое вещество, а другой - нерастворимую в воде жидкость, все же можно диспергировать каждый активный ингредиент в одной и той же непрерывной водной фазе путем диспергирования твердого активного ингредиента в виде суспензии (с использованием методики, аналогичной применяющейся для получения СК), но диспергирования жидкого активного ингредиента в виде эмульсии (с использованием методики, аналогичной применяющейся для получения ЭМ). Полученная композиция представляет собой препарат суспензия-эмульсия (СЭ).
Приведенные ниже примеры иллюстрируют, но не ограничивают настоящее изобретение.
Примеры получения
Пример I1: Получение 4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамида
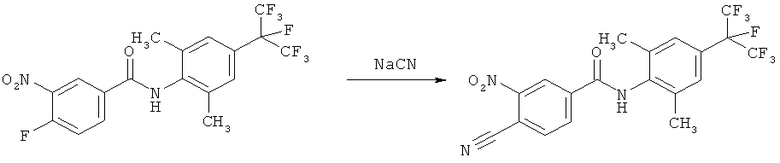
К раствору N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-4-фтор-3-нитробензамида (2,008 г, 4,4 ммоля) (получали в соответствии с WO 05/073165) в N,N-диметилформамиде (25 мл) добавляли цианид натрия (0,237 г, 4,84 ммоля). Реакционную смесь перемешивали при температуре окружающей среды в течение 48 ч. Затем добавляли воду (20 мл) и органическую фазу 3 раза экстрагировали этилацетатом (3×100 мл). Объединенные органические экстракты промывали водой и рассолом, сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат 1:4) и получали 4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамид (1,0 г, выход 49%). 1H-ЯМР (400 МГц, CDCl3): 8,85 (d, 1H), 8,38 (q, 1H), 8,11 (d, 1H), 7,55 (s, 1H), 7,40 (s, 2H), 2,33 (s, 6H) част./млн.
Аналогичные методики использовали для получения следующих соединений:
4-Циано-N-[2,6-диэтил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 8,84 (s, 1H), 8,38 (q, 1H), 8,10 (d, 1H), 7,57 (bs, 1H), 7,43 (s, 2H), 2,68 (q, 4H), 1,24 (t, 6H) част./млн.
4-Циано-N-[2-метоксиметил-6-метил-4-(1,2,2,2-тетрафтор- 1-трифторметилэтил)-фенил]-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 9,18 (s, 1H), 8,88 (s, 1H), 8,39 (d, 1H), 8,11 (d, 1H), 7,55 (s, 2H), 7,40 (s, 1H), 4.55 (s, 2H), 3,45 (s, 3H), 2,39 (s, 3H) част./млн.
N-[2-Бром-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-4-циано-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 8,88 (s, 1H), 8,40 (d, 1H), 8,11 (d, 1H), 7,78 (s, 2H), 7,52 (s, 1H), 2,44 (s, 3H) част./млн.
N-[2-Бром-6-этил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-4-циано-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 8,87 (s, 1H), 8,39 (d, 1H), 8,10 (d, 1H), 7,80 (s, 1H), 7,74 (s, 1H), 7,56 (s. 1H), 2,77 (q, 2H), 1,29 (t, 3H) част./млн.
4-Циано-N-[2,6-дибром-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамид. Соединение использовали на следующей стадии без дополнительной очистки.
4-Циано-N-[2-этил-6-метил-4-(1,2,2,3,3,3-гексафтор-1-трифторметилпропил)-фенил]-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 8,86 (s, 1H), 8,39 (q, 1H), 8,10 (d, 1H), 7,80 (s, 1H), 7,39 (s, 2H), 2.68 (q, 2H), 2,32 (s, 3H), 1,20 (t, 3H) част./млн.
4-Циано-Н-[2,6-диэтил-4-(1,2,2,3,3,3-гексафтор-1-трифторметилпропил)-фенил]-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 8,84 (s, 1H), 8,38 (q, 1H), 8,11 (d, 1H), 7,63 (s, 1H), 7,26 (s, 2H), 2,67 (q, 4H), 1.23 (t, 6H) част./млн. 2-Циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-5-нитробензамид. 1Н-ЯМР (400 МГц, CDCl3): 8,81 (m, 1H), 8,69 (m, 1H), 8,33 (d, 1H), 7,49 (s, 2H), 2,21 (s, 6H) част./млн.
2-Циано-N-[2,6-диэтил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамид. 1H-ЯМР (400 МГц, CDCl3): 10,67 (s, 1H), 8,58 (d, 1H), 8,40 (d, 1H), 8,02 (t, 1H), 7,49 (s, 2H), 2,53 (q, 4H), 1,17 (t, 6H) част./млн.
Пример I2: Получение 3-амино-4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамида

4-Циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-нитробензамид (1,0 г, 2,16 ммоля) (пример I1) растворяли в диметиловом эфире диэтиленгликоля ("диглим") (25 мл) и добавляли хлорид олова (1,229 г, 6,48 ммоля). Смесь охлаждали до 0°C и медленно добавляли водный раствор хлористоводородной кислоты (концентрированная) (4 мл). Реакционную смесь перемешивали при 80°C в течение 0,5 ч. Добавляли водный раствор гидроксида натрия (30 мас.%) (80 мл) для доведения значения рН до 7-8. Водную фазу 3 раза экстрагировали этилацетатом (200 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат от 1:1 до 0:1) и получали 3-амино-4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид (0,48 г, выход 51%). 1H-ЯМР (400 МГц, CDCl3): 7,54 (s, 1H), 7,49 (d, 2H), 7,36 (m, 3H), 7.15 (q, 1H), 2,3 (s, 6H) част./млн.
Аналогичные методики или хорошо известные методики, такие как гидрирование в присутствии палладиевого катализатора, как описано, например, в публикации Journal of Medicinal Chemistry (2005), 48(24), 7560 или в публикации Journal of Medicinal Chemistry (2005), 48(6), 1729, или восстановление с помощью гидросульфита натрия в двухфазной системе в присутствии тетрабутиламмонийбромида в качестве межфазного катализатора, как описано, например, в публикации Journal of Medicinal Chemistry (2006), 49(3), 955-970, использовали для получения следующих соединений:
3-Амино-4-циано-N-[2,6-диэтил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 7,53 (d, 1H), 7,40 (s, 2H), 7,33 (m, 2H), 4,65 (bs, 2H), 2,67 (q, 4H), 1,19 (t, 6H) част./млн.
3-Амино-4-циано-N-[2-метоксиметил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 8,78 (s, 1H), 7,53 (m, 2H), 7,38 (s, 1H), 7,18 (d, 1H), 4.65 (s, 2H), 4,49 (s, 2H), 3,40 (s, 3H), 2,38 (s, 3H) част./млн.
3-Амино-N-[2-бром-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-4-цианобензамид. 1H-ЯМР (400 МГц, CDCl3): 7,72 (s, 1H), 7,60 (s, 1H), 7,54 (d, 1H), 7,50 (s, 1H), 7,35 (s, 1H), 7,21 (d, 1H), 4,65 (s, 2H), 2,40 (s, 3Н) част./млн.
3-Амино-N-[2-бром-6-этил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-4-цианобензамид. 1H-ЯМР (400 МГц, ацетон d6): 7,70 (s, 1H), 7,54 (s, 1H), 7,46 (d, 1H), 7,39 (s, 1H), 7,18 (d, 1H), 5,70 (s, 2H), 2,70 (q, 2H), 1,10 (t, 3H) част./млн.
3-Амино-4-циано-N-[2,6-дибром-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 8,88 (s, 2H), 7,63 (s, 1H), 7,54 (d, 1H), 7,35 (s, 1H), 7,21 (d, 1H), 4,67 (bs, 2H) част./млн.
3-Амино-4-циано-N-[2-этил-6-метил-4-(1,2,2,3,3,3-гексафтор-1-трифторметилпропил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 7,53 (d, 1H), 7,33 (m, 4H), 7.15 (q, 1H), 4,64 (bs, 2H), 2,67 (q, 2H), 2,33 (s, 3H), 1,21 (t, 3Н) част./млн.
3-Амино-4-циано-N-[2,6-диэтил-4-(1,2,2,3,3,3-гексафтор-1-трифторметилпропил)-фенил]-бензамид. lH-ЯМР (400 МГц, CDCl3): 7,74 (d, 1H), 7,38 (s, 2H), 7,34 (m, 2H), 7,15 (q, 1H), 4,66 (bs, 2H), 2,66 (q, 4H), 1,21 (t, 6H) част./млн.
5-Амино-2-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 7,7 (s, 1H), 7,43 (s, 2H), 7,14 (d, 1H), 7,98 (m, 1H), 4,3 (s, 2H), 2,2 (s, 6H) част./млн.
3-Амино-2-циано-N-[2,6-диэтил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид. 1H-ЯМР (400 МГц, CDCl3): 7,5-7,44 (m, 4H), 7,28 (s, 1H), 6,94 (d, 1H), 5,60 (s, 2H), 2,50 (q, 4H), 1,13 (t, 6H) част./млн.
Пример P1: Получение 3-амино-4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамида (соединение №A1, приведенное в таблице A)
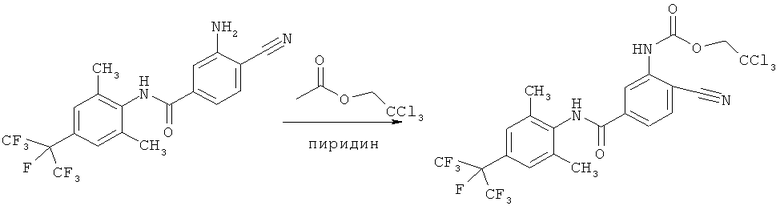
3-Амино-4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид (пример 12) (199 мг, 0,46 ммоля) растворяли в тетрагидрофуране (5 мл), затем при температуре окружающей среды добавляли пиридин (0,074 мл, 0,92 ммоля). При интенсивном перемешивании при температуре окружающей среды добавляли трихлорметилхлорформиат (0,066 мл, 0,48 ммоля). Реакционную смесь перемешивали при температуре окружающей среды в течение 16 ч. Добавляли смесь этилацетата (50 мл) и водного раствора гидрокарбоната натрия (насыщенный). Фазы разделяли и водную фазу дважды экстрагировали этилацетатом (50 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат 2:1) и получали соединение №A1, приведенное в таблице A (0,125 мг, выход 45%).
Аналогичные методики использовали для получения следующих соединений:
Соединения №A4, A7 и от A9 до A14, приведенные в таблице A, соединение №C1, приведенное в таблице C и соединение №D1, приведенное в таблице D. Соединение №A5 получали в виде побочного продукта в ходе синтеза соединения №A4 и соединение №A8 получали в виде побочного продукта в ходе синтеза соединения №A7.
Пример I3: Получение 4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-метиламинобензамида
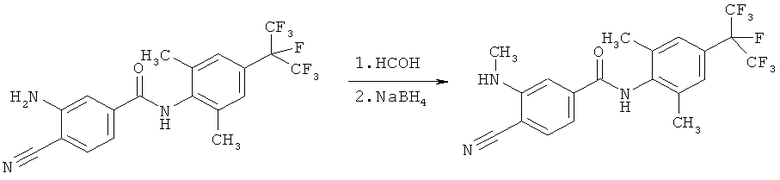
3-Амино-4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид (3,01 г, 6,95 ммоля) (пример 12) растворяли в ацетонитриле (50 мл) и последовательно добавляли водный раствор формальдегида (36,5% мас./об.) (0,64 мл, 6,95 ммоля) и уксусную кислоту (30 мл). Реакционную смесь перемешивали при температуре окружающей среды в течение 45 мин. Затем добавляли борогидрид натрия (0,44 г, 6,95 ммоля) и повторно добавляли уксусную кислоту (5 мл). Реакционную смесь перемешивали и концентрировали. Остаток растворяли в этилацетате и раствор промывали водным раствором гидроксида натрия (1 н.). Водную фазу 3 раза экстрагировали этилацетатом (200 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат 1:5) и получали 4-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-метиламинобензамид (1,80 г, выход 58%). Т.пл. (температура плавления) 204-206°C. 1H-ЯМР (400 МГц, CDCl3): 7,53 (d, 1H), 7,37 (s, 3H), 7,23 (s, 1H), 7,10 (q, 1H), 5,88 (d, 1H), 3,02 (d, 3H), 2,35 (s, 6H) част./млн. Методику, описанную в примере P1, затем использовали для получения соединения №A3, приведенного в таблице A.
Аналогичную методику использовали для получения следующего соединения:
4-Циано-N-[2,6-диэтил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-метиламинобензамид. Т.пл. 199-202°C. 1H-ЯМР (400 МГц, CDCl3): 7,53 (d, 1H), 7,40 (s, 2H), 7,31 (s, 1H), 7,23 (s, 1H), 7,08 (q, 1H), 5,88 (d, 1H), 3,02 (d, 3Н), 2,69 (q, 4H), 1,24 (t, 6H) част./млн. Методику, описанную в примере Р1, затем использовали для получения соединения №A6, приведенного в таблице A.
Аналогичную методику использовали для получения следующего соединения:
4-Циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-3-этиламино-бензамид получали с использованием ацетальдегида в качестве реагента. 1H-ЯМР (400 МГц, CDCl3): 7,52 (d, 1H), 7,37 (s, 2H), 7,35 (s, 1H), 7,23 (s, 1H), 7,08 (m, 1H), 4,69 (t, 1H), 3,35 (m, 2H), 2,35 (s, 6H), 1,24 (t, 3Н) част./млн. Методику, описанную в примере Р1, затем использовали для получения соединения №A2, приведенного в таблице A.
Пример I4: Получение 3-циано-5-нитробензойной кислоты
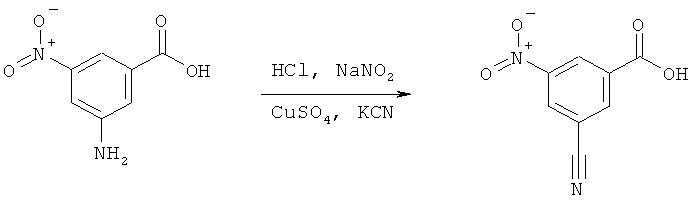
Раствор 1: 3-Амино-5-нитробензойную кислоту (10 г, 54,9 ммоля) растворяли в водном растворе хлористоводородной кислоты (концентрированная) (55 мл) и разбавляли водой (200 мл). При 0-5°C добавляли раствор нитрита натрия (3,788 г, 54,90 ммоля) в воде (30 мл). Раствор 2: К раствору гидрата сульфата меди (28,786 г, 115,29 ммоля) в воде (120 мл) добавляли раствор цианида калия (27,528 г, 422,73 ммоля) в воде (30 мл).
Раствор 2 нагревали до 65°C. Значение рН раствора 1 доводили до 6-7 путем добавления при 0-50C водного раствора карбоната натрия (насыщенный). Раствор 1 при 65°C по каплям добавляли к раствору 2. Реакционную смесь кипятили с обратным холодильником в течение 40 мин. Реакционной смеси давали охладиться до температуры окружающей среды и ее подкисляли путем добавления водного раствора хлористоводородной кислоты (2 н.). Водную фазу экстрагировали этилацетатом (3×200
мл) и объединенные органические экстракты промывали водным раствором фосфита натрия (насыщенный), водой и рассолом и концентрировали и получали 3-циано-5-нитробензойную кислоту (7,2 г, выход 68%), которую использовали без дополнительной очистки. 1Н-ЯМР (400 МГц, ДМСО-d6): 9,0 (s, 1Н), 8,82 (s, 1H), 8,70 (s, 1H) част./млн.
Пример I5: Получение 3-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-5-нитробензамида
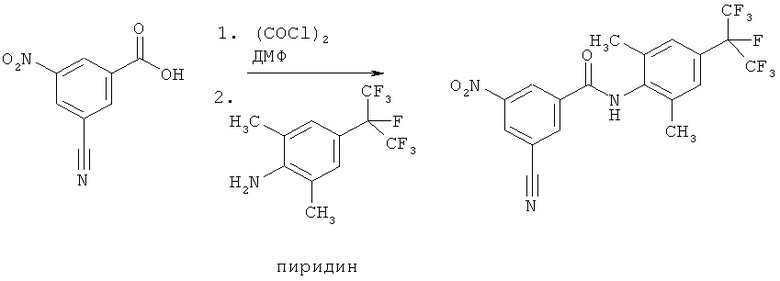
К суспензии 3-циано-5-нитробензойной кислоты (пример 14) (7,2 г, 37,5 ммоля) в дихлорметане (40 мл) при температуре окружающей среды добавляли оксалилхлорид (3,808 мл, 45 ммолей), затем N,N-диметилформамид ("ДМФ") (0,2 мл). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч и затем кипятили с обратным холодильником в течение 3 ч. Реакционной смеси давали охладиться до температуры окружающей среды и затем концентрировали. Остаток суспендировали в тетрагидрофуране (50 мл). 2,6-Диметил-4-(гептафторпроп-2-ил)-анилин (9,761 г, 33,7 ммоля) (получали в соответствии с ЕР 1006102) растворяли в тетрагидрофуране (50 мл) и добавляли пиридин (6,035 мл, 75 ммолей). Смесь охлаждали до 0°C и добавляли раствор 2-фтор-5-нитробензоилхлорида. Реакционную смесь перемешивали при температуре окружающей среды в течение 12 ч. Затем добавляли водный раствор гидрокарбоната натрия (насыщенный) (100 мл) и органическую фазу дважды экстрагировали этилацетатом (2×200 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат 6:1) и получали 3-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-5-нитробензамид (12 г, выход 77%). 1Н-ЯМР (400 МГц, CDCl3): 8,99 (m, 1H), 8,72 (m, 1H), 8,6 (m, 1H), 7,80 (s, 1H), 7,4 (s, 2H), 2,33 (s, 6H) част./млн.
Пример I5: Получение 5-амино-3-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамида
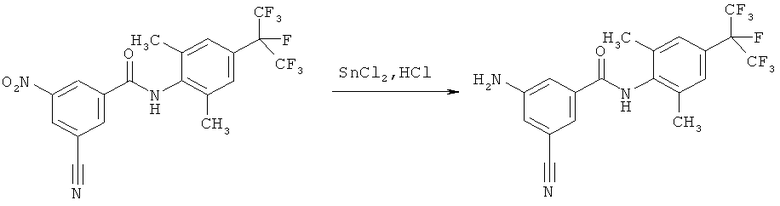
3-Циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-5-нитробензамид (12,0 г, 25,9 ммоля) (пример 15) растворяли в изопропаноле (200 мл) и добавляли хлорид олова (14,73 г, 77,7 ммоля). Смесь охлаждали до 0°C и медленно добавляли водный раствор хлористоводородной кислоты (концентрированная) (30 мл). Реакционную смесь перемешивали при 80°C в течение 0,5 ч. 1/3 Общего объема изопропанола выпаривали. К концентрированной смеси добавляли воду (100 мл) и водный раствор гидроксида натрия (4н.) для доведения значения рН смеси до 7-8. Водную фазу 3 раза экстрагировали этилацетатом (3×200 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: циклогексан/этилацетат от 4:1 до 0:1) и получали 5-амино-3-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид (10,6 г, выход 94,4%). 1H-ЯМР (400 МГц, CDCl3): 7,47 (s, 1H), 7,44 (s, 2H), 7,36 (s, 2H), 7,07 (s, 1H), 4,11 (bs, 2H), 2,32 (s, 6H) част./млн.
Пример Р2: Получение 3-амино-5-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамида (соединение №B1, приведенное в таблице B)

3-Амино-5-циано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилэтил)-фенил]-бензамид (пример 15) (199 мг, 0,46 ммоля) растворяли в тетрагидрофуране (3 мл), затем при температуре окружающей среды добавляли пиридин (0,117 мл, 1,45 ммоля). При интенсивном перемешивании при температуре окружающей среды добавляли трихлорметилхлорформиат (0,070 мл, 0,48 ммоля). Смесь перемешивали при температуре окружающей среды в течение 2 ч. Добавляли смесь этилацетата (50 мл) и водного раствора гидрокарбоната натрия (насыщенный). Фазы разделяли и водную фазу дважды экстрагировали этилацетатом (50 мл). Объединенные органические экстракты сушили над сульфатом натрия и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (элюент: циклогексан/этилацетат 2:1) и получали соединение №В1, приведенное в таблице В (210 мг, выход 74%).

Обозначения: s = синглет; m = мультиплет.
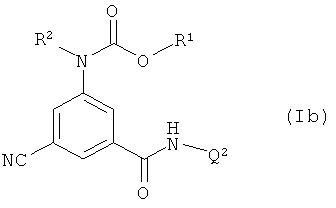
Обозначения: s = синглет; m = мультиплет.


Биологические примеры
Этот пример иллюстрирует пестицидные/инсектицидные характеристики соединения формулы (I). Описанные ниже исследования проводили для следующих вредителей:
Spodoptera littoralis (гусеница совки египетской хлопковой)
Диски из листьев хлопка помещали на агар в 24-луночные планшеты для микротитрования и опрыскивали исследуемыми растворами при дозе внесения, равной 200 част./млн. После сушки диски из листьев заражали личинками 5 Li. Образцы исследовали на гибель, поведение при кормлении и регулирование роста через 3 дня после обработки (ДПО). Указанные ниже соединения обеспечивали уничтожение не менее 80% Spodoptera littoralis: A1, A2, A3, A4, A5, A6, A7, A8, A11, A12, A13, A14, B1, D1.
Heliothis virescens (гусеница листовертки-почкоеда табачной):
Яйца (0-24-часовые) помещали на искусственный корм в 24-луночные планшеты для микротитрования и с помощью пипетки обрабатывали исследуемыми растворами при дозе внесения, равной 200 част./млн. После инкубационного периода длительностью 4 дня образцы исследовали на гибель яиц, гибель личинок и регулирование роста. Указанные ниже соединения обеспечивали уничтожение не менее 80% Heliothis virescens: A1, A2, A3, A4, A5, A6, A7, A8, A11, A12, A13, A14, B1.
Plutella xylostella (моль капустная):
24-Луночные планшеты для микротитрования (ПМТ) с искусственным кормом с помощью пипетки обрабатывали исследуемыми растворами при дозе внесения, равной 18 част./млн. После сушки ПМТ заражали личинками (L2) (7-12 на лунку). После инкубационного периода длительностью 6 дней образцы исследовали на гибель личинок и регулирование роста. Указанные ниже соединения обеспечивали уничтожение не менее 80% Plutella xylostella: A1, A2, A3, A4, A6, A7, A8, A11, A12, A13, A14, B1.
Diabrotica balteata (блошка длинноусая):
24-Луночные планшеты для микротитрования (ПМТ) с искусственным кормом с помощью пипетки обрабатывали исследуемыми растворами при дозе внесения, равной 200 част./млн (концентрация в лунках составляла 18 част./млн). После сушки ПМТ заражали личинками (L2) (6-10 на лунку). После инкубационного периода длительностью 5 дней образцы исследовали на гибель личинок и регулирование роста. Указанные ниже соединения обеспечивали уничтожение не менее 80% Diabrotica balteata: A1, A2, A3, A4, A5, A6, A7, A8, A11, A12, A13, A14, B1.
Myzus persicae (тля персиковая):
Диски из листьев полсолнечника помещали на агар в 24-луночные планшеты для микротитрования и опрыскивали исследуемыми растворами при дозе внесения, равной 200 част./млн. После сушки диски из листьев заражали популяцией тлей смешанного возраста. После инкубационного периода длительностью 6 ДПО образцы исследовали на гибель. Указанные ниже соединения обеспечивали уничтожение не менее 80% Myzus persicae: A12.
Thrips tabaci (трипс луковый):
Диски из листьев полсолнечника помещали на агар в 24-луночные планшеты для микротитрования и опрыскивали исследуемыми растворами при дозе внесения, равной 200 част./млн. После сушки диски из листьев заражали популяцией популяцией трипсов смешанного возраста. После инкубационного периода длительностью 7 дней образцы исследовали на гибель насекомых. Указанные ниже соединения обеспечивали уничтожение не менее 80% Thrips tabaci: A8, A11, A12, A14.
Tetranychus urticae (клещ двупятнистый паутинный)
Диски из листьев бобов помещали на агар в 24-луночные планшеты для микротитрования и опрыскивали исследуемыми растворами при дозе внесения, равной 200 част./млн. После сушки диски из листьев заражали популяцией клещей смешанного возраста. Через 8 дней диски исследовали на гибель яиц, гибель личинок и гибель взрослых особей. Указанные ниже соединения обеспечивали уничтожение не менее 80% Tetranychus urticae: A11.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ БЕНЗАМИДЫ ДЛЯ БОРЬБЫ С ЧЛЕНИСТОНОГИМИ | 2014 |
|
RU2713949C2 |
| ЗАМЕЩЕННЫЕ БЕНЗАМИДЫ ДЛЯ БОРЬБЫ С ЧЛЕНИСТОНОГИМИ | 2014 |
|
RU2712092C2 |
| МЕСТНО ВВОДИМЫЙ СОСТАВ ДЛЯ БОРЬБЫ С ПАРАЗИТАМИ ЖИВОТНЫХ И ИХ ПРОФИЛАКТИКИ | 2018 |
|
RU2786638C2 |
| БИСАМИДНЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНСЕКТИЦИДНЫХ СОЕДИНЕНИЙ | 2008 |
|
RU2515966C2 |
| ПРОИЗВОДНЫЕ 2-ИМИНООКСИФЕНИЛУКСУСНОЙ КИСЛОТЫ И СРЕДСТВО, СОДЕРЖАЩЕЕ ЭТИ СОЕДИНЕНИЯ | 1996 |
|
RU2170229C2 |
| ИМИНООКСИМЕТИЛЕНАНИЛИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), СРЕДСТВА ДЛЯ БОРЬБЫ С ВРЕДИТЕЛЯМИ, СПОСОБ БОРЬБЫ С ВРЕДИТЕЛЯМИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1995 |
|
RU2143423C1 |
| ЦИКЛИЧЕСКИЕ АЗАИНДОЛ-3-КАРБОКСАМИДЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 2009 |
|
RU2487874C2 |
| ЗАМЕЩЕННЫЕ БЕНЗИЛАМИНОПИПЕРИДИНЫ И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ЛЕЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2152930C2 |
| ДИГИДРОПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2086548C1 |
| ПРОИЗВОДНЫЕ 3-(3-АРИЛОКСИФЕНИЛ)-1-(ЗАМЕЩЕННЫЙ МЕТИЛ)-S-ТРИАЗИН-2,4,6-ТРИОНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ, СПОСОБ ПОДАВЛЕНИЯ НЕЖЕЛАТЕЛЬНЫХ ВИДОВ РАСТЕНИЙ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2159769C2 |
Изобретение относится к новым соединениям формулы (I), которые могут найти применение для борьбы с насекомыми или клещами. В формуле
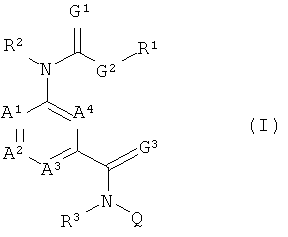
A1, A2, A3 и A4 независимо друг от друга обозначают C-R4 или C-R5, при условии что только один из A1, A2, A3 и A4 обозначает C-R4; R1 обозначает C1-C6-алкил или C1-C6-галогеналкил; R2 обозначает водород, C1-C4-алкил или C1-C4-галогеналкилкарбонил; R3 обозначает водород; G1, G2 и G3 обозначают кислород; R4 обозначает цианогруппу; R5 обозначает водород; Q обозначает фрагмент формулы 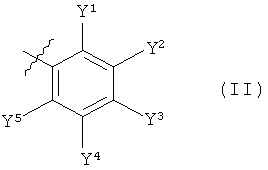 или
или 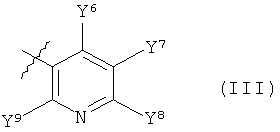
где Y1 и Y5 независимо друг от друга обозначают галоген, C1-C6-алкил или C1-C4-алкокси-C1-C4-алкил; Y2, Y4 обозначают водород; Y3 обозначает C1-C6-перфторалкил; Y6, Y7 и Y9 независимо друг от друга обозначают водород, C1-C6-алкил, и Y8 обозначает C1-C6-галогеналкил. Изобретение относится также к инсектицидной или акарицидной композиции и способу борьбы с насекомыми или клещами. 3 н. и 2 з.п. ф-лы, 5 табл., 8 пр.
1. Соединение формулы (I):

в которой
A1, A2, A3 и A4 независимо друг от друга обозначают C-R4 или C-R5, при условии что только один из A1, A2, A3 и A4 обозначает C-R4;
R1 обозначает C1-C6-алкил или C1-C6-галогеналкил;
R2 обозначает водород, C1-C4-алкил или C1-C4-галогеналкилкарбонил;
R3 обозначает водород;
G1, G2 и G3 обозначают кислород;
R4 обозначает цианогруппу;
R5 обозначает водород;
Q обозначает фрагмент формулы (II) или (III)

 ,
,
где Y1 и Y5 независимо друг от друга обозначают галоген, C1-C6-алкил или C1-C4-алкокси-C1-C4-алкил;
Y2, Y4 обозначают водород;
Y3 обозначает C1-C6-перфторалкил;
Y6, Y7 и Y9 независимо друг от друга обозначают водород, C1-C6-алкил, и
Y8 обозначает C1-C6-галогеналкил.
2. Соединение по п.1, в котором R2 обозначает водород, метил, этил.
3. Соединение по п.1, в котором Q обозначает фрагмент формулы (II).
4. Способ борьбы с насекомыми или клещами и их уничтожения, который включает нанесение на вредителей, на очаг вредителей или на растения, подверженные нашествию вредителей, инсектицидно или акарицидно эффективного количества соединения формулы (I) по п.1.
5. Инсектицидная или акарицидная композиция, включающая инсектицидно или акарицидно эффективное количество соединения формулы (I) по п.1.
| Щеточно-коллекторный узел электрической машины | 1989 |
|
SU1661886A2 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| ИНСЕКТИЦИДНЫЕ АНТРАНИЛАМИДЫ | 2001 |
|
RU2278852C2 |
Авторы
Даты
2013-09-20—Публикация
2008-02-26—Подача