Изобретение относится к медицине, а именно к хирургии. Данный способ может быть использован в трансплантологических центрах.
Особенности хирургической техники таковы, что для трансплантации почки необходимо временное прекращение кровотока в ней. Это неизбежно приводит к ишемической, а позднее и реперфузионной травмам различной степени тяжести. Вследствие этого, значительная часть почечных аллотрансплантатов начинает нормально функционировать не сразу. Тяжелые травмы в результате ишемии/реперфузии встречаются в 20-30% случаев и сопровождаются выраженным канальцевым некрозом и острой почечной недостаточностью трансплантата, в связи с чем возникает необходимость в продолжении диализа в послеоперационном периоде.
Известен способ коррекции реперфузионной травмы аллопочки (Ржевская О.Н. и др. Применение вазапростана в комплексной терапии острого канальцевого некроза после пересадки почки. «Вестник трансплантологии искусственных органов», №5, 2006, с.21-22), включающий медикаментозную терапию вазапростаном в послеоперационном периоде по специальной схеме.
Недостатком этого способа является его недостаточная эффективность, поскольку осуществляется только коррекция уже развившихся нарушений, при этом не происходит уменьшение реперфузионной травмы непосредственно после возобновления кровотока в трансплантате.
Известен способ коррекции реперфузионной травмы аллопочки, включающий проведение экстракорпоральной детоксикации после включения аллопочки в кровоток, медикаментозную терапию (Патент РФ №2213583, МПК A61M 1/38, публ. 2003, прототип).
Недостатком данного метода является то, что при плазмаферезе неизбежно происходит удаление белков плазмы и возникает необходимость в их восполнении - переливании свежезамороженной плазмы человека или раствора альбумина, что сопровождается риском заражения вирусными гепатитами, а также развития аллергических реакций. Сложно поддерживать постоянную терапевтическую концентрацию препаратов: компонентов иммуносупрессии, наркозных компонентов, антибиотиков, необходимых в интра- и ближайшем послеоперационном периоде. Все это уменьшает эффективность и безопасность этого способа.
Задачей предложенного способа является устранение указанных недостатков, улучшение результатов трансплантации почки путем уменьшения степени тяжести реперфузионной травмы, снижения иммуногенности трансплантата во время операции, в том числе и в раннем послеоперационном периоде, когда трансплантат наиболее уязвим. Помимо этого селективная сорбция оказывает меньшее воздействие на гемодинамику и лучше переносится пациентом.
Для этого при коррекции реперфузионной травмы аллопочки, включающей проведение экстракорпоральной детоксикации после включения аллопочки в кровоток, медикаментозную терапию, предложено в качестве экстракорпоральыой детоксикации проводить селективную сорбцию цитокинов в течение 6-8 часов начиная с момента включения аллопочки в кровоток. Причем медикаментозную терапию необходимо осуществлять одновременно с процессом селективной сорбции. При этом в интра- и послеоперационном периоде осуществляют контроль концентрации провоспалительпых цитокинов в крови, а именно: до начала операции, а также после операции делают, по меньшей мере, 3 измерения концентрации провоспалительпых цитокинов в крови через каждые 4-6 часов, и при регистрации роста концентрации цитокинов в двух измерениях подряд после операции до величины в 1,5 и более раза превышающей значение, полученное до операции, проводят повторный сеанс селективной сорбции.
Предложенный способ позволяет значительно улучшить результаты аллотрансплантации почек путем:
- уменьшения степени тяжести реперфузионной травмы почечного трансплантата, что увеличивает число нормально функционирующих нефронов, снижает выраженность острого канальцевого некроза;
- уменьшения иммуногенности трансплантата и снизить риск развития острого отторжения в раннем послеоперационном периоде.
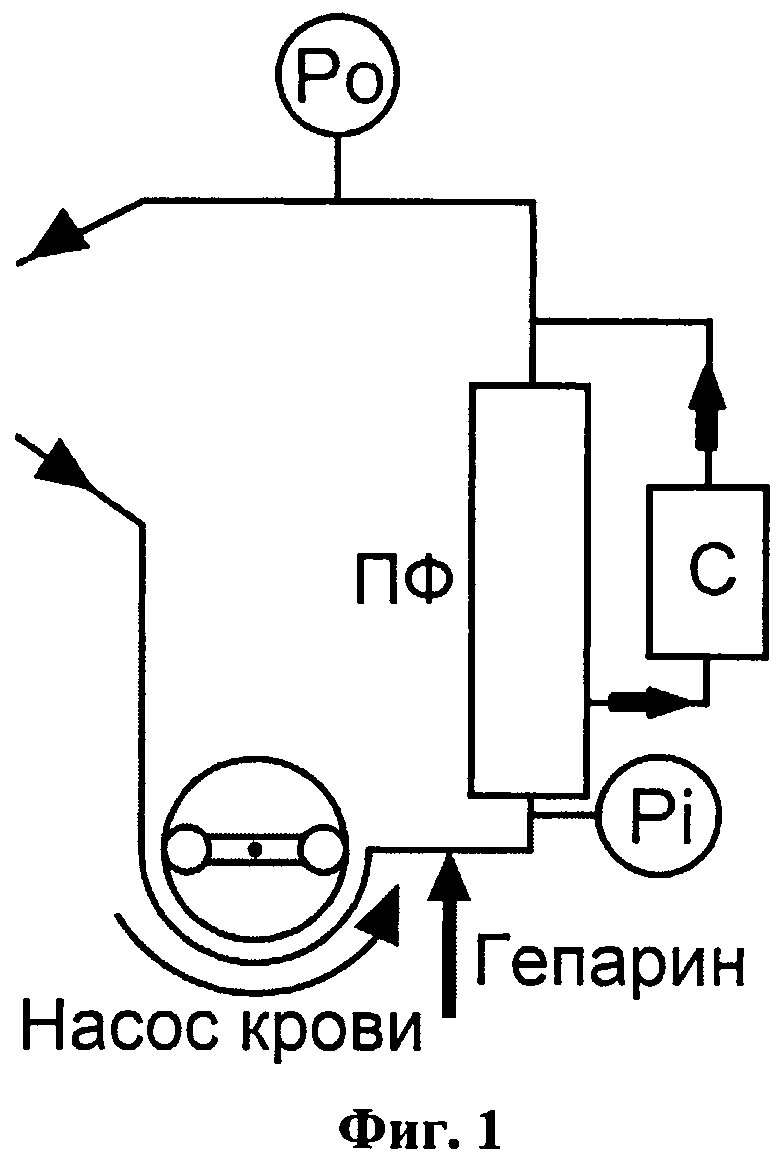
На фиг.1 представлена схема экстракорпорального контура, где Pi - датчик давления крови до плазмофильтра, Ро - датчик давления после плазмофильтра, ПФ - плазмофильтр, С - сорбционная колонка.
Способ осуществляется следующим образом.
В процессе предоперационного обследования измеряют концентрацию цитокинов в крови. Проводят операцию трансплантации почки по стандартной методике. После возобновления кровотока в донорской почке непосредственно в артерию трансплантата вводят ряд препаратов, улучшающих кровоток в трансплантате и одновременно проводят селективную сорбцию цитокинов в течение 6-8 часов.
Сосудистый доступ обеспечивается путем пункции артериовенозной фистулы или имплантации временного сосудистого доступа - двухпросветного диализного катетера. Экстракорпоральный контур заполняется кровью реципиента, и после формирования сосудистых анастомозов начинается экстракорпоральная гемоперфузия со скоростью 100-180 мл/мин. В плазмофильтре (ПФ) происходит сепарация плазмы и клеток крови. После плазмофильтра плазма поступает в сорбционную колонку (С) со скоростью 30-40 мл/мин. После сорбционной колонки плазма вновь соединяется с клетками крови и возвращается в сосудистое русло реципиента. С целью своевременной диагностики тромбоза колонки осуществляют контроль давления в экстракорпоральном контуре посредством до плазмофильтра Pi и после плазмофильтра с помощью Ро.
В ближайшем послеоперационном периоде осуществляют контроль концентрации цитокинов, как минимум, 3 раза каждые 4-6 часов.
При регистрации роста концентрации цитокинов до величины в 1,5 и более раза превышающей значение, полученное до операции, в двух измерениях подряд после операции, проводят повторный сеанс селективной сорбции.
В послеоперационном периоде назначают введение препаратов, улучшающих тканевой метаболизм и тканевую реперфузию (рибоксин, витамин Е, кокарбоксилаза, вазапростан, аденозинтрифосфат, пентоксифиллин). Коррекция дозы этих препаратов производится лечащим врачом индивидуально.
Пример 1.
Больной К., 42 года, поступил в хирургическое отделение трансплантологии и диализа с диагнозом хронический гломерулонефрит, терминальная стадия хронической почечной недостаточности, состояние на программном гемодиализе для трансплантации донорской почки. У больного до операции определен уровень провоспалительного цитокина - интерлейкина-6, который составил 45 пг/мл. Операция выполнена по стандартной методике.
Во время операции, после возобновления кровотока в донорской почке, начата экстракорпоральная селективная сорбция цитокинов. Процедура продолжалась 6 часов. Уровень интерлейкина-6 снизился на 42% и составил 19 пг/мл. В артерию трансплантата болюсно ввели нифедипин и папаверин, внутривенно капельно вводился реополиглюкин.
С первых суток в течение десяти дней больной помимо антибиотиков и иммуносупрессии ежедневно получал рибоксин, витамин Е, кокарбоксилазу, вазапростан, аденозинтрифосфат, пентоксифиллин. Через 6 и 12 часов концентрация интерлейкина-б составила 41 и 55 пг/мл соответственно, а через 18 часов - 74 пг/мл, т.е. увеличилась в 1,8 раза по отношению к концентрации до операции. Через 22 часа - 82 пг/мл, т.е. увеличилось в 2 раза по сравнению с концентрацией до операции.
С целью коррекции возвратной гиперцитокинемии, проведен второй сеанс селективной сорбции цитокинов, который длился 8 часов. У больного отмечена первичная функция трансплантата. Несмотря на 18-часовую «холодовую» ишемию, с первых суток отмечена высокая концентрацию креатинина в моче и стабильное снижение концентрации креатинина в крови. Диурез на первые сутки составил 600 мл, на вторые - 1200 мл, на третьи и далее - более 2 л.
На шестые сутки отмечена нормализация азотемии. При амбулаторном наблюдении у нефролога - функция трансплантата стабильная, удовлетворительная. Эпизодов отторжения за двухлетний период наблюдения не отмечено.
Пример 2.
Больная Л., 46 лет, с диагнозом хронический гломерулонефрит, терминальная стадия хронической почечной недостаточности, состояние на программном гемодиализе, была госпитализирована в хирургическое отделение трансплантологии и диализа для трансплантации донорской почки. В анамнезе у больной была трансплантация донорской почки 2 года до настоящей госпитализации, однако, в связи с некупируемым кризом отторжения трансплантат был удален через 35 дней после трансплантации.
У больной до операции определен уровень провоспалительного цитокина - фактора некроза опухоли-α (ФНОα) - 4,0 пг/мл. Были сформированы сосудистые анастомозы по стандартной методике. Время «холодовой» ишемии составило 16 часов. После возобновления кровотока в почке начата селективная сорбция цитокинов. В артерию трансплантата болюсно введены дилтиазем и папаверин, внутривенно капельно вводился реополиглюкин. Процедуру сорбции селективной цитокинов проводили 8 часов. Через 6 часов после операции концентрация ФНОα составила 4,4 пг/мл, а через 10 и 14 часов - 6,4 и 8,1 пг/мл соответственно.
Больной проведен второй сеанс селективной сорбции цитокинов в течение 8 часов. Диурез на первые сутки составил 3200 мл, на вторые 2200 мл, далее диурез колебался в зависимости от объема вводимой жидкости.
Нормализация азотемии наступила на шестые сутки после операции. В связи с тем, что трансплантация была повторная, больная имела высокий риск развития отторжения в раннем послеоперационном периоде. Однако за три года послеоперационного наблюдения эпизодов отторжения не отмечено, функция трансплантата остается стабильной.
Всего предлагаемый метод применен у 16 больных. Для сравнительной оценки эффективности предложенного метода проведен анализ результатов лечения больных без применения селективной сорбции цитокинов для коррекции реперфузионнного повреждения (группа сравнения). При применении предложенного метода первичная функция отмечена у 14 больных из 16 (в группе сравнения - у 15 больных из 25), сутки нормализации азотемии - 8±2,1 (в группе сравнения - 14,2±5,1), число кризов отторжения в течение двух лет - 1 у 16 больных (в группе сравнения - 9 у 25 больных), выживаемость трансплантатов в течение двух лет - 15 из 16 (в группе сравнения - 21 из 25).
Способ апробирован в отделе трансплантологии, нефрологии и хирургической гемокоррекции ГБУЗ МО МОНИКИ им. М.Ф. Владимирского. Полученный хорошие результаты, а также высокая безопасность позволяют рекомендовать его для широкого применения.
В результате применения предложенного метода достигается более ранняя реабилитация реципиентов почечного аллотрансплантата, меньшая потребность в заместительной почечной терапии в ближайшем послеоперационном периоде, меньшая частота кризов отторжения в раннем послеоперационном периоде, большая выживаемость трансплантатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОРРЕКЦИИ РЕПЕРФУЗИОННОЙ ТРАВМЫ АЛЛОПОЧКИ | 2002 |
|
RU2213583C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОТТОРЖЕНИЯ ПОЧЕЧНОГО ТРАНСПЛАНТАТА | 2013 |
|
RU2508924C1 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ИНТЕНСИВНОЙ ТЕРАПИИ У ТЯЖЕЛООБОЖЖЕННЫХ И КРАЙНЕ ТЯЖЕЛООБОЖЖЕННЫХ | 2020 |
|
RU2751014C1 |
| СПОСОБ ЛЕЧЕНИЯ СЕПСИСА ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ И ЗАБРЮШИННОГО ПРОСТРАНСТВА | 2012 |
|
RU2500434C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ОТТОРЖЕНИЯ ПОЧКИ ДО ЕЕ ТРАНСПЛАНТАЦИИ | 2018 |
|
RU2671637C1 |
| Способ профилактики отторжения трансплантата трупной почки | 2018 |
|
RU2688172C1 |
| Способ профилактики отторжения пересаженного органа | 1986 |
|
SU1424854A1 |
| Способ коррекции реперфузионно-ишемического повреждения при резекции почки по поводу локализованного рака в условиях тепловой ишемии | 2019 |
|
RU2732765C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАЧАЛЬНОЙ ФУНКЦИИ ПОЧЕЧНОГО АЛЛОТРАНСПЛАНТАТА В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ | 2013 |
|
RU2523663C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕПЕРФУЗИОННЫХ ПОВРЕЖДЕНИЙ ДОНОРСКИХ ОРГАНОВ | 2011 |
|
RU2487704C2 |
Изобретение относится к медицине, а именно к хирургии и транспалнтологии, и может быть использовано при оперативных вмешательствах по поводу трансплантации почки. Для этого после включения аллопочки в кровоток проводят экстракорпоральную детоксикацию, в качестве которой применяют селективную сорбцию цитокинов. Детоксикацию проводят в течение 6-8 часов, начиная с момента включения аллопочки в кровоток. Одновременно с процессом селективной сорбции осуществляют медикаментозную терапию. В ходе проведения мероприятий осуществляют контроль концентрации провоспалительных цитокинов в крови до начала операции и после. При этом после операции делают, по меньшей мере, 3 измерения концентрации цитокинов в крови через каждые 4-6 часов. При регистрации роста концентрации цитокинов после операции в двух измерениях подряд в 1,5 раза и более превышающей значение, полученное до операции, проводят повторный сеанс селективной сорбции. Способ обеспечивает улучшение результатов трансплантации почки за счет снижения реперфузионной травмы, иммуногенности трансплантата, в том числе и в раннем послеоперационном периоде, а также позволяет поддерживать постоянную терапевтическую концентрацию препаратов. 1 ил., 2 пр.
Способ коррекции реперфузионной травмы аллопочки, включающий проведение экстракорпоральной детоксикации после включения аллопочки в кровоток, медикаментозную терапию, отличающийся тем, что в качестве экстракорпоральной детоксикации проводят селективную сорбцию цитокинов в течение 6-8 ч, начиная с момента включения аллопочки в кровоток, причем медикаментозную терапию осуществляют одновременно с процессом селективной сорбции, при этом осуществляют контроль концентрации провоспалительных цитокинов в крови до начала операции, а также после операции, причем после операции делают, по меньшей мере, 3 измерения концентрации цитокинов в крови через каждые 4-6 ч и при регистрации роста концентрации цитокинов в двух измерениях подряд после операции до величины в 1,5 раза и более превышающей значение, полученное до операции, проводят повторный сеанс селективной сорбции.
| СПОСОБ КОРРЕКЦИИ РЕПЕРФУЗИОННОЙ ТРАВМЫ АЛЛОПОЧКИ | 2002 |
|
RU2213583C1 |
| АФФИННЫЙ СОРБЕНТ ДЛЯ УДАЛЕНИЯ ФАКТОРА НЕКРОЗА ОПУХОЛИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2123860C1 |
| US 20060129082 A1, 15.06.2006 | |||
| КРСТИЧ М | |||
| и др | |||
| Уросепсис до и после аллогенной трансплантации почки | |||
| Патогенетические аспекты | |||
| - Врач, №11, 2011, с.53-55 | |||
| СИНЮТИН А.А | |||
| Влияние послеоперационного плазмафереза на функцию и внутриорганный кровоток почечного аллотрансплантата | |||
| Автореферат | |||
Авторы
Даты
2013-10-10—Публикация
2012-05-23—Подача