Предлагаемое изобретение относится к медицине, в частности к иммунологическим лабораторным исследованиям в трансплантологии и может быть использовано как критерий прогноза степени риска отторжения почки до ее трансплантации.
Клиническая трансплантология является одним из оптимальных способов лечения заболеваний почек, не поддающихся традиционным способам. Однако пересадка тканей или органов от одного индивидуума другому, генетически отличающемуся, вызывает реакцию отторжения пересаженного биологического материала. Поэтому отторжение является одной из основных причин ограниченной выживаемости трансплантата. Известно, что иммунологическая реакция на донорский орган включает комплекс последовательных клеточных и молекулярных процессов, которые суммарно обуславливают клиническую картину отторжения (Taniguchi М, Rebellato LM, Cai J, Hopfield J, et al.. Higher risk of kidney graft failure in the presence of anti-angiotensin II type-1 receptor antibodies. Am J Transplant. - 2013. - №13. - p. 2577-2589). На сегодняшний день нет никаких сомнений в неудовлетворенной медицинской потребности диагностики повреждения трансплантата, чтобы обеспечить более персонализированный терапевтический подход (Volk HD, Sawitzki В, Reinke P. Molecular analysis of renal allograft biopsies-more than a nice toy for researchers? Am J Transplant. -2013. - №13. - p. 539-540).
В последние годы уделяется большое внимание биохимическим, иммунологическим, молекулярногенетическим исследованиям, благодаря чему удалось получить представление о процессах, лежащих в основе повреждения трансплантата при отторжении.
Аналогом данной заявки является способ мониторинга состояния пациента после трансплантации органа (патент РФ на изобретение № 2560705, опубликованный в 2015 г. Хубутия М.Ш., Пинчук А.В., Евсеев А.К., Гольдин М.М.). Способ основан на электрохимическом методе определения патологических состояний при помощи измерения редокс потенциалов (РП) плазмы крови. При этом ежедневно определяют РП плазмы крови пациента с помощью платинового электрода относительно хлорсеребряного электрода. Платиновый электрод предварительно обрабатывают с помощью катодно-анодного сканирования в растворе неорганического восстановителя в циклическом потенциодинамическом режиме. Проводят ежедневный мониторинг величины РП плазмы крови пациента и выявляют изменения величин РП в одном направлении за сутки или несколько суток. При выявлении изменения РП более 25 мВ за сутки или несколько суток судят о наличии дисфункции трансплантата или высоком риске развития криза отторжения трансплантата.
Недостатками способа являются:
1) Наличие специального прибора для определения редокс потенциала, с платиновым электродом.
2) Необходимость предварительной трудоемкой обработки электрода с помощью катодно-анодного сканирования в водном растворе 0,1 М Na2SO3 в циклическом потенциодинамическом режиме перед каждым измерением.
3) Для мониторинга необходимо осуществлять забор крови у трансплантированных пациентов ежедневно.
За ближайший аналог принят способ диагностики отторжения почечного аллотрансплантата (патент РФ на изобретение №2430370, публикация 2009 г. Васильченко И.А., Метелин В.Б., Цалман А.Я., Ватазин А.В.). Способ диагностики отторжения почечного аллотрансплантата включает определение фазовой высоты РН живых лимфоцитов периферической крови методом фазово-интерференционной микроскопии. По полученным результатам рассчитывают функциональную активность лимфоцитов по формуле: FA=(k3n3+k2n2+k1n1+k0n0)/n, где n - число лимфоцитов в выборке, n3 - число лимфоцитов с РН≤1,5 мкм, n2 - число лимфоцитов с 1,5 мкм ≤ РН ≤ 2 мкм, n1 - число лимфоцитов с 2 мкм≤РН≤2,5 мкм, n0 - число лимфоцитов с РН ≥ 2,5 мкм, k3, k2, k1, k0 - коэффициенты активности лимфоцитов. Если FA=1,8-2,0, то диагностируют отторжение почечного трансплантата.
Основным недостатком данного способа является неспецифичность метода, так как повышение функциональной активности лимфоцитов может быть связано не только с отторжением, но и с ишемическим и реперфузионным повреждением ткани, воспалительными и инфекционными процессами и т.д. Так же способ требует высокой квалификации персонала и дополнительного оборудования.
Задачи: снижение риска потери трансплантата; повышение чувствительности и специфичности способа диагностики предикторов отторжения; упрощение способа, не требующего дополнительного оборудования и специального обучения персонала, сокращение материальных затрат.
Сущностью предложенного изобретения является определение уровня концентрации комплекса цитокинов до трансплантации и по уровню полученных значений прогнозирование степени риска отторжения.
Технический результат: способ при использовании позволяет снизить риск отторжения аллотрансплантата почки, определив уровень риска отторжения до трансплантации. Это дает возможность в период предоперационной подготовки реципиента, провести профилактическое лечение и предотвратить потерю трансплантата, улучшить его функции после трансплантации и таким образом повлиять на благоприятный исход трансплантации. Предлагаемое в данном способе иммунологическое исследование уровня цитокинов, является простым в исполнении, минимально инвазивным и занимает на 20% меньше времени по сравнению с известным аналогом.
Для осуществления этого способа предложено всем пациентам при постановке в лист ожидания, параллельно с выявлением HLA антител, из того же образца крови выполнять первичное иммунологическое определение уровня цитокинов в крови: IL-1RA, IL-2, IL-6, Eotaxin, МСР-1, MIP-1alpha, MIP-1beta, SDF-1alpha, GM-CSF, BDNF, LIF. Исследование методом мультиплексного анализа на сформированной для этого исследования мультиплексной панели Simplex ProcartaPlex (например, eBioscience, США). Для этого в лунки иммунологического планшета вносят по 25 мкл аналита и по 25 мкл смеси микросфер, покрытых специфичными антителами. Далее, для первичного исследования предлагается инкубировать при t 24°С на шейкере в течение 60 мин, при 500 об/мин и далее при t 4°С всю ночь, для увеличения чувствительности теста. После отмывки добавляют по 25 мкл смеси детекторных антител, затем выполняют инкубацию при t 24°С в течение 30 мин и промывку. Затем в каждую лунку добавляют по 50 мкл стрептавидина-фикоэритрина в качестве флуоресцентного красителя и инкубируют при t 24°С в течение 30 мин.
Детекцию результатов мультиплексного анализа выполняют с использованием двухлазерной системы с цифровой обработкой сигналов на проточном флуоресцентном анализаторе (например, Luminex 100/200 Luminex Corporation, США).
Повторное исследование проводят непосредственно перед трансплантацией, параллельно с постановкой кросс-матча, из одного и того же образца крови, забранного в день трансплантации. При повторном исследовании, после смешивания аналита и смеси микросфер, рекомендуется инкубировать при t 24°С на шейкере 60 мин, при 500 об/мин, для сокращения времени исследования и далее продолжить протокол с сохранением тех же условий.
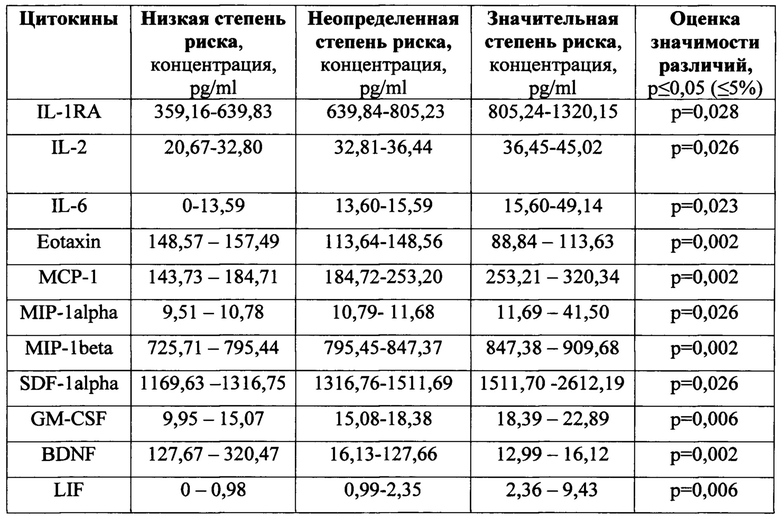
По результатам производят оценку риска отторжения (см. таблицу) и предоперационное прогнозирование возможности развития отторжения после трансплантации почки. Причем риском отторжения является изменение концентрации не менее трех маркеров острого отторжения.
Степени риска отторжения почки по результатам концентрации цитокинов у пациентов с хронической почечной болезнью (ХПБ) перед трансплантацией.
В периферической крови 51 реципиентов аллотрансплантата почки перед трансплантацией и в различные сроки после трансплантации (7, 30, 90 и 180 дней) оценивали содержание 47 цитокинов: IL-12p70, IL-13, IL-1b, IL-2, IL-4, IL-5, IL-6, IL-18, IL-10, IL-17A, IL-21, IL-22, IL-23, IL-27, IL-9, IL-31, IL-15, IL-1a, IL-1RA, IL-7, IL-33; IFN-alpha, IFN-gamma, TNF-alpha, TNF-beta, Eotaxin, GRO-alpha, IL-8(CXCL8), IP-10, MCP-1, MIP-1alpha, MIP-1beta, MIG, SDF-1alpha, RANTES; GM-CSF, NGF-beta, BDNF, EGF, FGF-2, HGF, LIF, PDGF-BB, PIGF-1, SCF, VEGF-A, VEGF-D, методом мультиплексного анализа и технологии хМАР (принцип проточной цитометрии).
Всем реципиентам был проведен скрининг предсуществующих HLA-антител перед трансплантацией и антитела не были выявлены, что свидетельствует об отсутствии иммунизации антигенами главного комплекса гистосовместимости ранее.
У 34 пациентов наблюдалось не осложненное течение послеоперационного периода на протяжении 180 дней, у 8 - выработались HLA-антитела без клинических проявлений отторжения, а у 9 пациентов в послеоперационном периоде наблюдалась дисфункция трансплантата - острые отторжения (подтвержденные иммуногистохимическим исследованием) и выявлялись HLA-антитела. Контрольную группу составили 20 человек (здоровые доноры крови), обоего пола, возраст - 18-50 лет.
Наряду с определением концентрации цитокинов реципиентам проводили стандартные исследования: OAK, биохимические, ИГХ, бактериологические исследования.
В результате проведенного исследования выявлены прогностически значимые маркеры острого отторжения трансплантата почки - IL-1RA, IL-2, IL-6, Eotaxin, МСР-1, MIP-1alpha, МIР-1beta, SDF-1alpha, GM-CSF, BDNF, LIF, так как они продемонстрировали достоверные изменения концентрации у реципиентов с кризами отторжения еще до трансплантации. А так же были разработаны критерии риска отторжения для пациентов с ХПБ перед трансплантацией.
В таблице представлены значения критериев риска для каждого цитокина. За пороговые значения концентраций низкой степени риска приняты результаты, полученные у реципиентов почки до трансплантации, впоследствии не имевших отторжений в 100% случаев. Критерии значительной степени риска - это результаты реципиентов почки до трансплантации, впоследствии имевших отторжения в 89% случаев. Промежуточные значения - неопределенный риск отторжения, который составляет 19%.
На основании полученных данных был рассчитан относительный риск (RR) развития отторжения. У пациентов, имевших достоверные повышения или понижения уровня данных цитокинов в крови до трансплантации, отторжения наблюдается в 13,4 раза чаще. Показатель относительного риска свидетельствует о наличии прямой связи (р<0,05) между концентрацией цитокинов до трансплантации и вероятностью отторжения. Число больных, которых необходимо лечить (NNT) - 1,729.
Пример 1.
Реципиенту Д., мужчина, 30 лет с диагнозом хронический гломерулонефрит, хроническая почечная болезнь (ХПБ) С5 перед трансплантацией было выполнено иммунологическое исследование уровня цитокиновых маркеров отторжения и получены результаты: IL-1RA - 359,16 пг/мл, IL-2 - 20,67 пг/мл, IL-6 - 0 пг/мл, Eotaxin - 149,0 пг/мл, МСР-1 - 157,35 пг/мл, MIP-1alpha - 9,50 пг/мл, MIP-1beta - 725,71 пг/мл, SDF-1alpha - 1182,12 пг/мл, GM-CSF - 10,01 пг/мл, BDNF - 127,67 пг/мл, LIF - 0 пг/мл. Концентрация маркеров: IL-1RA, IL-2, IL-6, MIP-1alpha, MIP-1beta, BDNF, LIF - соответствовала минимальным значениям низкой степени риска. Посттрансплантационный период действительно протекал без осложнений, трансплантат функционирует 2 года.
Пример 2.
Больная К., женщина 26 лет. Диагноз: хронический интерстициальный нефрит, ХПБ С5, находилась на программном гемодиализе (ПГД) с 2013 года. Исследование уровня цитокинов накануне трансплантации показало следующие результаты: IL-1RA - 425,71 пг/мл, IL-2 - 32,8 пг/мл, IL-6 - 13,59 пг/мл, Eotaxin - 157,4 пг/мл, МСР-1 - 180,54 пг/мл, MIP-1alpha - 10,05 пг/мл, MIP-1beta - 784,26 пг/мл, SDF-1alpha - 1127,82 пг/мл, GM-CSF - 15,07 пг/мл, BDNF - 320,47 пг/мл, LIF - 0,97 пг/мл. Концентрация пяти маркеров: IL-2, IL-6, Eotaxin, GM-CSF, BDNF была на уровне верхних значений низкой степени риска. Согласно этим данным есть основание предположить о нормальном приживлении трансплантата, что и было подтверждено записями в истории болезни. Трансплантат продолжает функционировать.
Пример 3.
Больная Р., женщина 44 лет. Диагноз: сахарный диабет 1 типа, комбинированная нефропатия. ХБП С5. ПГД с 2010 г. После проведения иммунологического исследования уровня цитокинов, получены результаты: IL-1RA - 564,79 пг/мл, IL-2 - 34,56 пг/мл, IL-6 - 13,60 пг/мл, Eotaxin - 151,24 пг/мл, МСР-1 - 168,39 пг/мл, MIP-1alpha - 10,79 пг/мл, MIP-1beta - 795,45 пг/мл, SDF-1alpha - 1316,76 пг/мл, GM-CSF - 12,58 пг/мл, BDNF - 1176,51 пг/мл, LIF - 1,23 пг/мл. После сравнения данных с табличными значениями, установили, что: IL-6, MIP-1alpha, MIP-1beta, SDF-1alpha соответствовали нижней границе неопределенной степени риска. Посттрансплантационный период действительно протекал без осложнений, трансплантат функционирует 2,1 года.
Пример 4.
Было выполнено иммунологическое исследование уровня цитокиновых маркеров отторжения пациенту О., мужчина 46 лет. Диагноз: периодическая болезнь (Средиземноморская лихорадка), абдоминальная форма. ХБП С5.ПГД с 2013 г. Исследование выполнялось в день трансплантации за 8 часов до операции. Результаты продемонстрировали следующие показатели: IL-1RA - 345,08 пг/мл, IL-2 - 26,63 пг/мл, IL-6 - 15,58 пг/мл, Eotaxin - 150,73 пг/мл, МСР-1 - 1184,21 пг/мл, MIP-1alpha - 11,68 пг/мл, MIP-1beta - 847,37 пг/мл, SDF-1alpha - 1423,79 пг/мл, GM-CSF - 13,41 пг/мл, BDNF - 127,66 пг/мл, LIF - 0 пг/мл. Сопоставив полученные результаты с табличными значениями, установили, что: IL-6, MIP-1alpha, MIP-1beta, BDNF имели пограничные значения неопределенной степени риска. Посттрансплантационный период протекал без осложнений. Через три месяца после трансплантации у пациента были обнаружены анти-HLA антитела к антигенам гистосовместимости второго класса 15%. Согласно записям в истории болезни было проведено лечение ритуксимабом в дозировке 1 мг/кг веса, а так же плазмаферез и корректировка доз иммуносупрессоров. Через шесть месяцев антитела были на уровне 1%. Трансплантат продолжает функционировать. Данный пример иллюстрирует возможность проявления иммунной реакции и при неопределенной степени риска.
Пример 5.
Больной О., м. 46 лет, поступил в больницу с диагнозом хронический гломерулонефрит, ХПБ С5, находящийся на ПГД с 2013 г. За шесть часов до трансплантации было выполнено иммунологическое исследование уровня цитокиновых маркеров отторжения и получены результаты: IL-1RA - 362,73 пг/мл, IL-2 - 45,02 пг/мл, IL-6 - 49,14 пг/мл, Eotaxin - 154,16 пг/мл, МСР-1 - 320,34 пг/мл, MIP-1alpha - 41,5 пг/мл, MIP-1beta - 909,68 пг/мл, SDF-1alpha - 1283,4 пг/мл, GM-CSF - 10,71 пг/мл, BDNF - 16,12 пг/мл, LIF - 1,13 пг/мл. Концентрация шести маркеров (IL-2, IL-6, МСР-1, MIP-1alpha, MIP-1beta, BDNF) соответствовала верхним границам значительной степени риска. Интраоперационно проведена перфузия аутоплазмы и плазмаферез. Так же, за два часа до трансплантации был введен симулект 20 мг внутривенно, капельно для профилактики острого отторжения. Повторное введение выполнили на четвертые сутки после трансплантации. Трансплантат сохраняет свою функцию на протяжении 2,5 лет.
Пример 6.
Пациенту Б., м. 31 год, с диагнозом хронический гломерулонефрит, гипертонический вариант, ХПБ С5, ПГД с 2001г было проведено иммунологическое исследование уровня цитокиновых маркеров отторжения. Проведенный анализ полученных результатов показал наличие четырех цитокинов с высоким риском отторжения: МСР-1 - 253,21 пг/мл,, MIP-1alpha - 11,69 пг/мл, MIP-1beta - 847,38 пг/мл, SDF-1alpha - 1511,7 пг/мл. Было решено, проводить интраоперационную профилактику острого отторжения симулектом по стандартной схеме с проведением плазмафереза. Посттрансплантационный период протекал без осложнений. Трансплантат функционирует 2,2 года.
Приведенные данные доказывают, что предлагаемый способ позволяет определить степень риска острого отторжения до трансплантации и дают возможность провести профилактическое лечение, благодаря чему улучшить результаты трансплантации почки. Данный способ может быть применен в обычных лабораториях медицинских учреждений, выполняющих трансплантацию почки.
Изобретение относится к медицине и может быть использовано как критерий прогноза степени риска отторжения почки до ее трансплантации. В крови реципиента до хирургического вмешательства определяют в комплексе уровень концентрации цитокинов: IL-1RA, IL-2, IL-6, Eotaxin, МСР-1, MIP-1alpha, MIP-1beta, SDF-1alpha, GM-CSF, BDNF, LIF и по уровню значений цитокинов прогнозируют низкую степень риска отторжения, неопределенную или значительную. Способ позволяет предотвратить потерю трансплантата, проведя профилактическое лечение. 1 табл., 5 пр.
Способ прогнозирования риска отторжения почки до ее трансплантации, включающий анализ крови реципиента, отличающийся тем, что в крови реципиента до хирургического вмешательства определяют в комплексе уровень концентрации цитокинов: IL-1RA, IL-2, IL-6, Eotaxin, МСР-1, MIP-1alpha, MIP-1beta, SDF-1alpha, GM-CSF, BDNF, LIF и пo таблице в описании по уровню значений цитокинов прогнозируют низкую степень риска отторжения, неопределенную или значительную при условии совпадения не менее трех полученных значений в соответствующей графе.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ХРОНИЧЕСКОГО ОТТОРЖЕНИЯ ПОЧЕЧНОГО ТРАНСПЛАНТАТА | 1991 |
|
RU2018843C1 |
| WO2012136585 A1, 11.10.2012 | |||
| АЛЕКСЕЕВ А.В | |||
| и др | |||
| Современные биомаркеры острого повреждения почек | |||
| Практическая медицина | |||
| Современные вопросы диагностики, N 03, 2014, с.3-10 | |||
| CHAIR D.A | |||
| et al | |||
| Guideline ERBP, Nephrol Dial Transplant (2013), N 28, c.1-71. | |||
Авторы
Даты
2018-11-06—Публикация
2018-01-09—Подача