Предпосылки создания изобретения
Глюкагоноподобный пептид-1 (ГПП-1, GLP-1) впервые был открыт в 1987 году и идентифицирован как глюкозозависимый кишечный гормон-пептид. Пептид ГПП-1 (GLP-1) передает сигналы через рецепторы, сопряженные с G белками (GPCR), и стимулирует β-клетки островков секретировать инсулин, ингибируя секрецию глюкагона, опорожнение желудка и секрецию желудочной кислоты, и влияет на другие физиологические функции.
Эксендины представляют собой пептиды (J. Biol. Chem. 1999, 265, 20259-20262; J. Biol. Chem. 1992, 267 (257?), 7402-7405), обнаруженные в выделениях слюнных желез ящериц- ядозубов Gila monster и Heloderma horridum. Эти эксендины, как показано на примере эксендина-4, высокогомологичны ГПП-1 (GLP-1) [7-36]. Ранее было показано, что эксендины могут связываться с ГПП-1 (GLP-1) рецепторами и вызывать аналогичный фармалогический эффект, такой как стимуляция секреции инсулина, эффективное регулирование уровня сахара в крови после приема пищи, снижение уровня гликозилирования гемоглобина и ингибирование опорожнения желудка. Опыты на животных показали, что продолжительное применение пептидов ГПП-1 (GLP-1) рецепторов может эффективно уменьшать резистентность к инсулину, что может привести к реверсии ухудшения сахарного диабета. Кроме того, было найдено, что ряд инсулинотропных агонистов, таких как ГПП-1 (GLP-1) и эксендин-4, могут стимулировать регенерацию β-клеток островков (Nat. Biotech. 2005, 23, 857-861) и ослаблять неалкогольную жировую болезнь печени (Hepatology 2006, 43, 173-181). Эти открытия делают такие пептиды основной целью в исследовании диабета и адипоза. Wu Dengxi и Sun Yukun (китайский патент ZL01112856) модифицировали эксендин-4 и получили ряд аналогов эксендина-4 с теми же функциями, что и нативный эксендин-4. Недавно на рынок Соединенных Штатов поступило новое лекарство на основе эксендина, эксендин-4 (Byetta®). Это лекарство было разработано совместно фирмами Amylin и Eli Lilly и его требуется вводить два раза в день в виде инъекций. Лекарство привлекло к себе внимание специалистов в области терапии диабета и адипоза. Однако, клинические исследования показали, что, примерно, у 41% пациентов вырабатываются антитела против эксендина-4 после 30 недель лечения таким лекарством (Diabetes Care, 2004,27, 2628-2635).
Белковые/пептидные лекарства обычно имеют недостатки, такие как короткий период полужизни в крови, плохая физическая и химическая стабильность, ежедневно требуются многократные инъекции таких лекарств, это вызывает боль и приносит неудобства пациентам. Как продлить период полужизни этих лекарств - это было задачей биотехнологии в течение долгого времени. До настоящего времени не найдено приемлемого для всех решения этой проблемы.
Метод ПЭГ-модификации появился в 1970-х годах и был применен в технологии приготовления белковых/пептидных лекарств. Когда некоторые белки/пептиды модифицировались с помощью линейного или разветвленного ПЭГ, модификация могла придать следующие признаки белку/пептиду: (1) повышение физической и химической устойчивости; (2) снижение иммуногенности; (3) повышение устойчивости к расщеплению протеазами; (4) увеличение периода полужизни вследствие повышения ПЭГ молекулярной массы, что приводит к снижению почечного клиренса; и (5) повышению растворимости лекарства и повышению проницаемости клеточных мембран для: лекарства. Согласно исследованиям A. Yang and К. Precourt эксендин-4 преимущественно метаболизируется и выводится почками (почечный клиренс). Ввиду этого для модификации эксендинов они применяли ПЭГ с молекулярной массой от 500 до 20000 Да (китайский патент CN1372570A), чтобы понизить эффект почечного клиренса.
Однако, основным недостатком ПЭГ технологии является то, что после модификации биоактивность модифицированного лекарства обычно заметно падает. Halm Tsubery et al. применяли 9-гидроксиметил-7-сульфофлуорен-Н-гидроксисукцинимид (FMS) для активации конденсации ПЭГ с эксендином-4, а затем группы ПЭГ отщепляли от эксендина гидролизом in vivo. Таким образом биоактивность эксендина-4 восстанавливалась. Хотя этот метод решает проблему низкой активности благодаря ПЭГ-модификации, после гидролиза in vivo высвобождается немодифицированный эксендин-4 и проблема иммуногенности в связи с частыми инъекциями остается нерешенной (J. Biol. Chem. 2004, 279, 38118-38124).
Имеющиеся у известных эксендинов и аналогов эксендинов недостатки включают короткие интервалы между введением доз, продуцирование антител у пациентов после инъекций в течение длительного времени и снижение биоактивности после модификации с помощью ПЭГ. Эти недостатки делают затруднительным применения эксендинов и аналогов эксендинов на практике, и требуется введение больших доз эксендинов или аналогов эксендинов, что в значительной мере препятствует применению эксендинов.
Сущность изобретения
Некоторые варианты изобретения включают эксендин или аналоги эксендина, модифицированные одной или более молекул или одним или более производных полиэтиленгликоля (ПЭГ). Некоторые варианты изобретения включают ПЭГ-модифицированные эксендины или аналоги эксендинов, имеющие одно или более ПЭГ-производных, связанных с одной или более аминокислот эксендина или аналогов или производных эксендина. ПЭГ-производные могут иметь линейную или разветвленную структуру. В некоторых вариантах изобретения ПЭГ-производные могут иметь разветвленную структуру, например такую, как представленная в любой из Формул (I-IV) по данному описанию. Некоторые варианты изобретения включают композиции, включающие ПЭГ-модифицированный эксендин или аналог эксендина, способы получения или введения таких модифицированных эксендинов или аналогов эксендинов и их различное применение, например, для лечения диабета. ПЭГ-модифицированные эксендины или аналоги эксендинов проявляют улучшенные и неожиданные свойства и характеристики, например, такие как продолжительный период полужизни в крови, высокая биоактивность и/или низкая иммуногенность.
Краткое описание Фигур
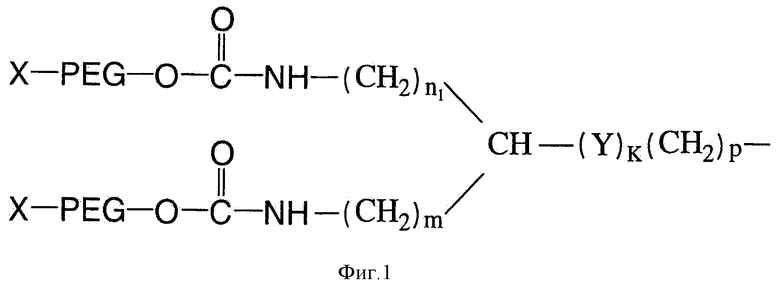
На Фигуре 1 представлена структура Формулы I разветвленных ПЭГ-производных.
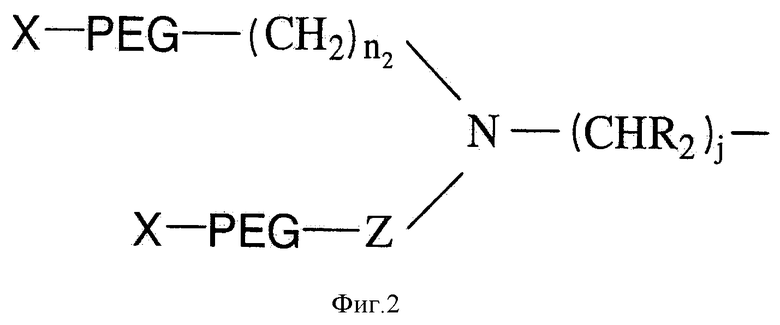
На Фигуре 2 представлена структура Формулы III разветвленных ПЭГ-производных.
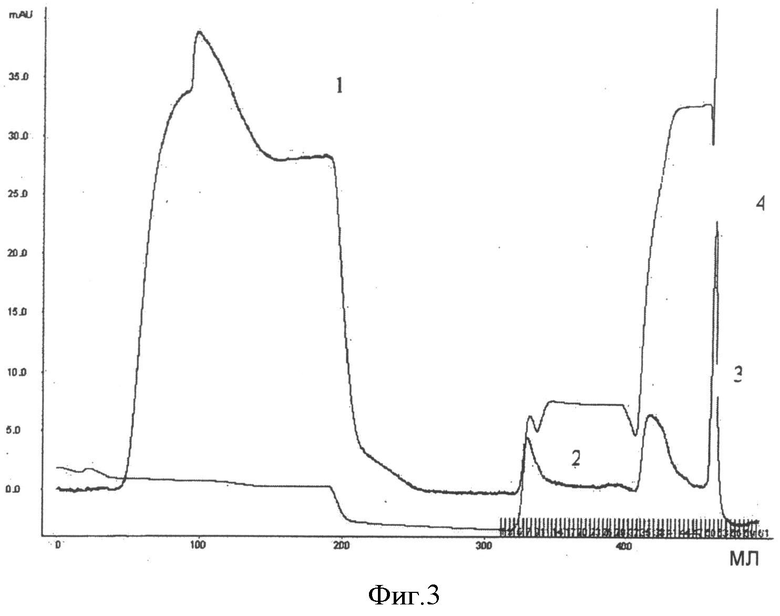
На Фигуре 3 показаны результаты хроматографии после разделения и очистки модифицированного с помощью ПЭГ производного аналога эксендина-4, (Формула IV), имеющего молекулярную массу 40000 Да (Дальтон). Цифрой 1 показан пик (максимум) поглощения при нанесении образца; цифрой 2 показан пик поглощения во время элюции для модифицированных многократными ПЭГ-частицами производных аналогов эксендина-4; цифрой 3 показан пик поглощения во время элюции для модифицированных единичными ПЭГ-производными аналогов эксендина-4; цифрой 4 показан пик поглощения во время элюции для немодифицированного аналога эксендина-4.
На Фиг.4 показана электрофоретограмма модифицированного единичным ПЭГ производным аналога эксендина-4 (Формула IV), имеющего молекулярную массу 40000 Да, причем на дорожке 1 видна полоса аналога эксендина-4, модифицированного единичным ПЭГ-производным.
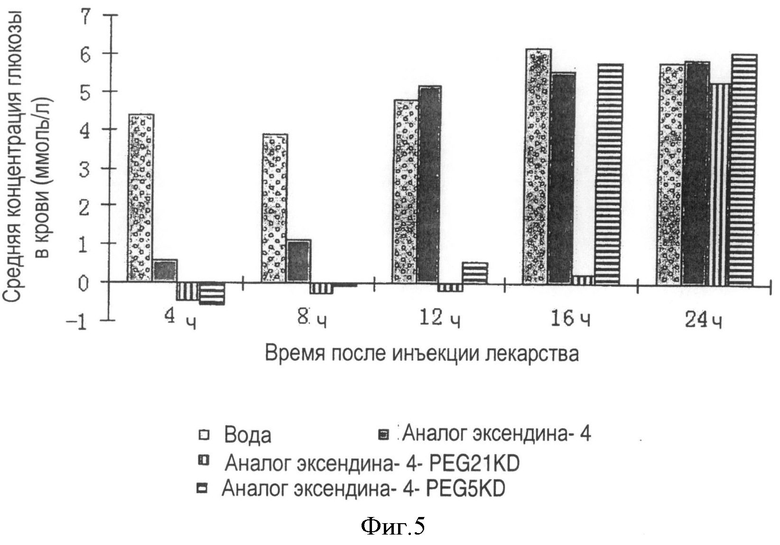
На Фигуре 5 показаны результаты 24-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных единичным ПЭГ-производным с молекулярной массой 5000 и 21000 Да, соответственно.
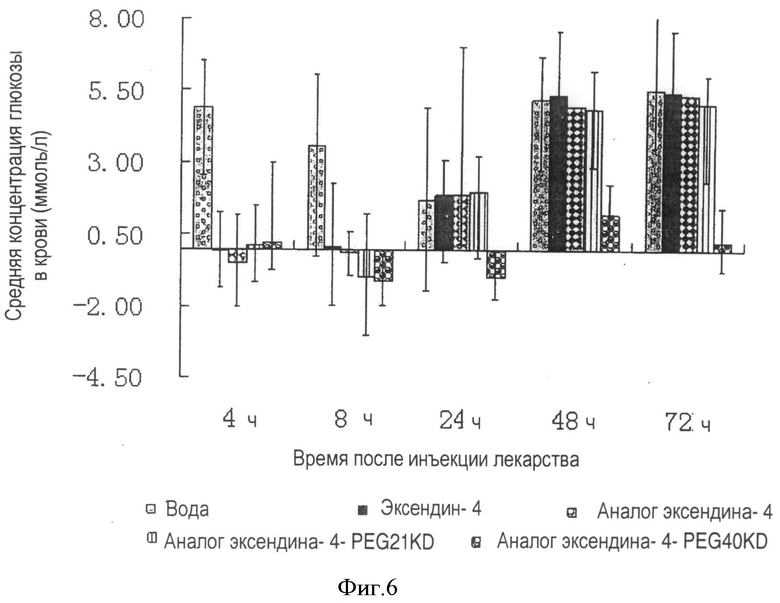
На Фигуре 6 показаны результаты 72-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных линейным единичным линейным или разветвленным ПЭГ-производным (Формула IV), с молекулярной массой 21000 и 40000 Да.
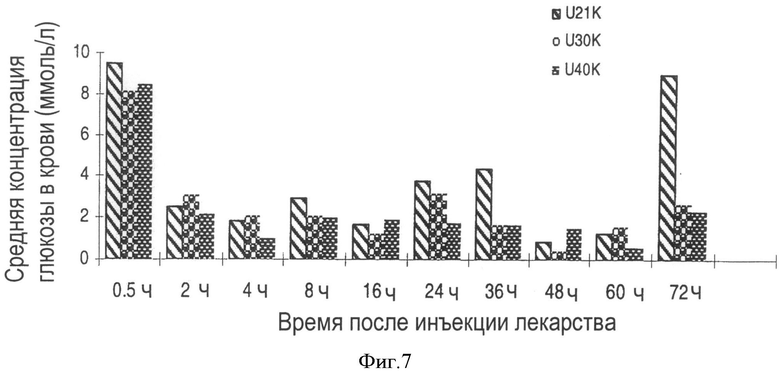
На Фигуре 7 показаны результаты 72-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных единичными ПЭГ-производными (Формула II) с молекулярной массой 21000 Да (U21K), 30000 Да (U30K) и 40000 Да (U40K), соответственно.
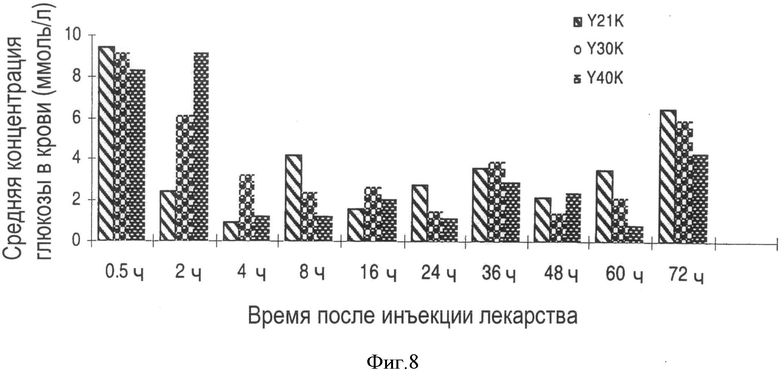
На Фигуре 8 показаны результаты 72-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных единичными ПЭГ-производными (Формула IV) с молекулярной массой 21000 Да (Y21K), 30000 Да (УЗОК) и 40000 Да (Y40K), соответственно.
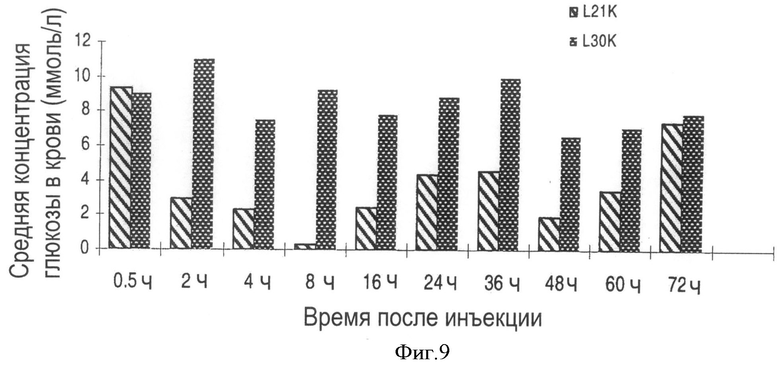
На Фигуре 9 показаны результаты 72-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных единичными линейными ПЭГ-производными с молекулярной массой 21000 Да (L21K) и 30000 Да (L30K), соответственно.
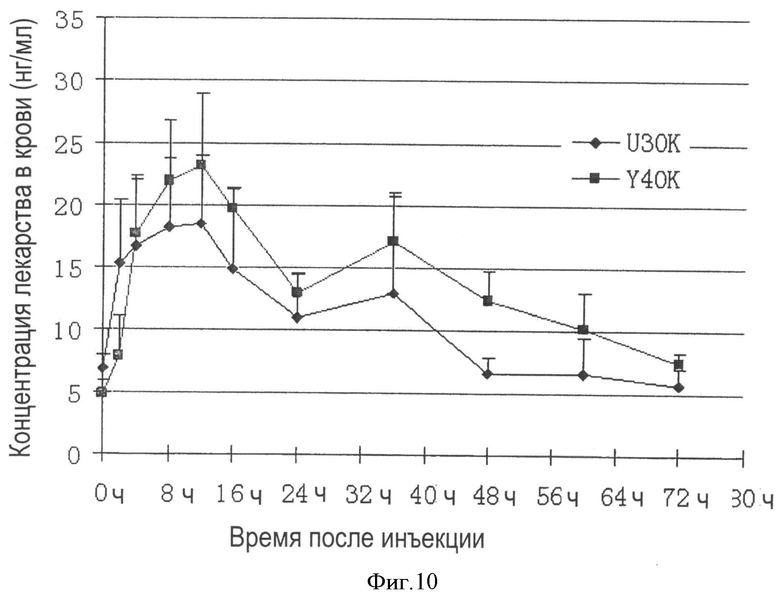
На Фигуре 10 показаны результаты 72-часового испытания на животных лекарственного действия аналогов эксендина-4, модифицированных единичными ПЭГ-производными (Формула II) с молекулярной массой 30000 Да (U30K) и ПЭГ-производными (Формула IV) с молекулярной массой 40000 Да (Y40K), соответственно.
Подробное описание изобретения ПЭГ-модификация
Предполагается, что приводимое ниже описание изобретения дается только для иллюстрации различных вариантов изобретения. В силу этого конкретные обсуждаемые модификации не следует рассматривать как ограничивающие объем изобретения. Для специалиста в данной области техники очевидным является то, что можно осуществить различные эквиваленты, изменения и модификации, не отступая от объема изобретения, и понятно, что такие эквивалентные варианты изобретения должны быть включены в данное описание.
Некоторые варианты изобретения включают эксендины или аналоги эксендинов, модифицированные одной или более молекул ПЭГ-производного. В некоторых вариантах изобретения применяются новые ПЭГ-модификации эксендинов и/или аналогов эксендинов для того, чтобы получить ПЭГ-модифицированные эксендины или аналоги эксендинов, которые проявляют улучшенные и неожиданные свойства и характеристики, например, такие как продолжительный период полужизни в крови, высокая биоактивность и/или низкая иммуногенность.
ПЭГ-производные различного химического строения (структуры) могут оказывать различное действие на биоактивность пептидов, модифицированных такими ПЭГ-производными или молекулами. ПЭГ-производные могут иметь линейную или разветвленную структуру. Разветвленные структуры включают, например, двойные (дважды) разветвленные цепи, а также многократно разветвленные цепи. ПЭГ-производные, имеющие двойные разветвленные цепи, включают, но без ограничения, например, структуры, изображенные ниже Формулами I, II, III и IV.
В некоторых вариантах изобретения разветвленные ПЭГ-производные могут включать, но без ограничения, например, структуру, изображенную ниже Формулой I:
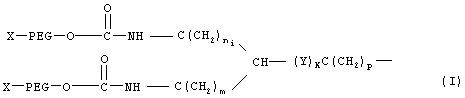
где Х обозначает водород или защитную группу. Защитной группой может быть любая группа, которая способна реагировать со свободной гидроксильной группой ПЭГ-производного и в то же время может предотвратить ее последующую реакцию с другими группами. Примеры защитных групп включают, но без ограничения, например, алкильные группы, такие как метил, диметил, этил, пропил и изопропил.
Далее, PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число; n1 обозначает целое число от 0 до 5; m обозначает целое число от 0 до 5; Y обозначает О, S, SO, SO2 или NR1, где R1 обозначает водород или замещенную или незамещенную (C1-C8) алкильную группу или замещенную или незамещенную циклоалкильную группу; k обозначает 0 или 1; и p обозначает целое число от 0 до 6. ПЭГ-производное, имеющее структуру, представленную Формулой I, можно синтезировать обычными химическими методами. Например, метод синтеза ПЭГ-производного, имеющего структуру, представленную Формулой I, описан в патенте США No. 6566506.
В некоторых вариантах изобретения ПЭГ-производное, применяемое в данном описании, которое содержит разветвленную структуру Формулы I, имеет конкретную структуру, представленную ниже Формулой II:
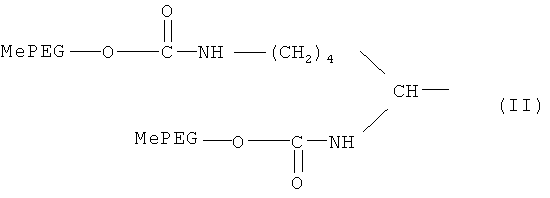
где PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число и Me обозначает метальную группу.
В некоторых вариантах изобретения разветвленное ПЭГ-производное имеет конкретную структуру, представленную ниже Формулой III:
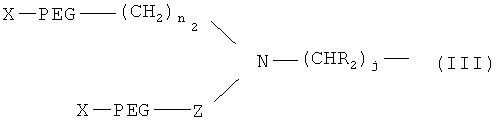
где Х обозначает водород или защитную группу; PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число; n2 обозначает целое число от 0 до 10; Z обозначает группу, выбранную из: (CH2)i, (СН2)iOCO, (CH2)iNHCO или (CH2)iCO, где i обозначает целое число от 0 до 10; R2 обозначает водород, замещенную или незамещенную (C1-C12) алкильную группу, замещенную арильную, арилалкильную или гетероалкильную группу; и j обозначает целое число от 1 до 12. Вышеуказанное ПЭГ производное Формулы III можно синтезировать обычными химическими методами, один из которых представлен в китайском патенте No. ZL03801105.0.
В некоторых вариантах изобретения ПЭГ-производное, применяемое по данному описанию, которое содержит разветвленную структуру Формулы III, имеет представленную ниже структуру Формулы IV:
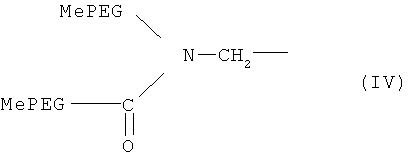
где PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число и Me обозначает метальную группу.
Молекулярная масса ПЭГ-производных может влиять на биоактивность ПЭГ-модифицированных пептидов. В некоторых вариантах изобретения молекулярная масса используемого ПЭГ-модифицированного производного составляет около 200 Да или выше. Предпочтительно, молекулярная масса составляет около 5000 Да или выше или около 20000 Да или выше. В некоторых вариантах изобретения молекулярная масса используемого ПЭГ-модифицированного производного находится в диапазоне, примерно, от 5000 Да, примерно, до 50000 Да. Предпочтительно, молекулярная масса используемого ПЭГ-модифицированного производного находится в диапазоне, примерно, от 5000 Да, примерно, до 50000 Да, или от 20000 Да до 45000 Да, или от 20000 Да до 40,000 Да. Если не указано иначе, молекулярные массы ПЭГ-производных, указываемые в данном описании, представляют собой средние молекулярные массы (Mn), определяемые методом гельпроникающей хроматографии (GPC) (Dong Yanming, Guidebook of Macromolecule Analysis, Beijing, China Petrochemical Press, 2004, 416-427). ПЭГ-производные с различной молекулярной массой можно либо приобрести от поставщиков, либо синтезировать обычными методами, известными в соответствующей области техники.
В некоторых вариантах изобретения ПЭГ-производные имеют разветвленные структуры с молекулярными массами выше 20000 Да. Предпочтительно, используемые разветвленные ПЭГ-производные имеют молекулярную массу выше 20000 Да, примерно, до 50000 Да, или от 20000 Да до 45000 Да, или от 20000 Да до 40,000 Да.
ПЭГ-модификацию эксендинов или аналогов эксендинов проводят, связывая активированные ПЭГ-производные с боковой цепью аминокислотного остатка или с N-концом или с С-концом аминокислот эксендинов или аналогов эксендинов. Например, ПЭГ-производные, содержащие различные активированные группы, могут связываться с различными боковьми цепями, с N-концом или с С-концом аминокислот или конкретной аминокислоты. Группы аминокислот, которые могут связываться химической связью с активированными ПЭГ-производными, включают, но без ограничения, α-аминогруппы на N-конце, ε-аминогруппы боковой цепи лизинового остатка, иминогруппы на имидазолильной группе боковой цепи гистидинового остатка пептидов, карбоксильный конец пептидов, карбоксильные группы боковых цепей аспарагиновой и глутаминовой кислоты, гидроксильные группы боковых цепей серина и треонина, меркаптогруппы боковой цепи цистеина и т.д. Обычно такие химические связи образуются в результате электрофильных и нуклеофильных реакций. Например, связь ПЭГ производного, активированного с помощью N-гидроксилсукцинимида, с α-аминогруппами на N-конце, ε-аминогруппами боковой цепи лизина и свободными аминогруппами, такими как иминогруппы на имидазолильных группах боковой цепи гистидина образуется с помощью таких реакций. Кроме того, ПЭГ, содержащие альдегидные активные группы, могут специфически связываться с N-концом пептидов по реакции восстановительного алкилирования. Действительно, некоторые варианты изобретения включают методы связывания ПЭГ-производных с эксендинами или аналогами эксендинов за счет различных активных групп и получающиеся при этом ПЭГ-модифицированные эксендины или аналоги эксендинов. ПЭГ-производные с различными активными группами можно приобрести от поставщиков или синтезировать обычными методами, известными в соответствующей области техники.
Некоторые варианты изобретения включают эксендины или аналоги эксендинов, конденсированные с одним или более ПЭГ-производных, в которых число ПЭГ-производных, связанных с эксендинами или аналогами эксендинов, зависит от числа свободнорадикальных групп в эксендинах или аналогах эксендинов, активных групп в ПЭГ-производном и/или молекулярной массы ПЭГ-производного. Обычно чем больше свободнорадикальных групп в эксендинах или аналогах эксендинов, тем большее число молекул ПЭГ-производных с ними связывается. Также обычно, чем больше молекулярная масса ПЭГ-производного, тем меньшее число молекул ПЭГ-производных связывается с пептидами. В некоторых вариантах изобретения эксендины или аналоги эксендинов модифицируются с помощью одной, двух, трех или четьфех молекул ПЭГ-производных. Предпочтительно, эксендин или аналог эксендина модифицируется с помощью одной или двух молекул ПЭГ-производных.
Смеси, образующиеся при связывании ПЭГ-производных с эксендинами или аналогами эксендинов, можно эффективно разделять обычными способами, например, ионообменной хроматографией, гель-фильтрацией или обращенно-фазовой хроматографией. Ионообменная хроматография может включать анионообменную и катионообменную хроматографии. Различные методы ионообменной хроматографии могут оказывать различное влияние на результаты разделения и очистки. Так как различные эксендины или аналоги эксендинов содержат различное число аминокислот и различные виды аминокислот и, следовательно, имеют различные молекулярные массы, окончательная молекулярная масса эксендинов или аналогов эксендинов, модифицированных ПЭГ-производными, представляет собой общую молекулярную массу ПЭГ-производных и эксендинов или аналогов эксендинов. После разделения, очистки и замены буферных растворов ПЭГ-модифированные эксендины или аналоги эксендинов можно обрабатывать далее для приготовления фармацевтических композиций.
Эксендины или аналоги эксендинов
Эксендины или аналоги эксендинов по данному описанию представляют собой пептиды или производные пептидов, имеющие аминокислотную последовательность, гомологичную или идентичную участку целой последовательности нативных эксендинов. Эксендины или аналоги эксендинов могут связываться с ГПП-1 (GLP-1) рецепторами и стимулировать каскад передач сигналов в клетке. Такие пептиды можно получать твердофазным химическим синтезом или генной инженерией (методами рекомбинантной ДНК) с последующим разделением и очисткой.
Эксендины или аналоги эксендинов по данному описанию включают, но без ограничения, нативные эксендин-3 и эксендин-4. Нативный эксендин-3 имеет следующую аминокислотную последовательность:
[His-Ser-Asp-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-Val-Arg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-OH] (SEQ ID NO: 1).
Нативный эксендин-4 имеет следующую аминокислотную последовательность:
[His-Gly-Glu-Giy-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-Val-Arg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-NH2] (SEQ ID NO: 2).
В некоторых вариантах изобретения эксендины или аналоги эксендинов включают, но без ограничения, пептидные аналоги, полученные заменой, добавлением или делецией аминокислот в аминокислотных последовательностях нативных эксендина-3 и эксендина-4. Аминокислотные замены в эксендине-3 и эксендине-4 включают замены на природные аминокислоты, а также на неприродные аминокислоты. Неприродные аминокислоты включают, но без ограничения, азетидинкарбоновую кислоту, 2-аминогександиовую кислоту, 3-аминогександиовую кислоту, β-лактамовую кислоту, аминопропионовую кислоту, 2-аминомасляную (аминобутановую) кислоту, 4-аминомасляную кислоту, 6-аминогексановую кислоту, 2-аминогептановую кислоту, 2-амино-2-метилпропановую кислоту, 3-амино-2-метилпропановую кислоту, 2-аминогептандиовую кислоту, 2-амино-3,3-диметилбутановую кислоту, десмозин, 2,2-диаминогептандиовую кислоту, 2,3-диаминопропановую кислоту, N-этилглицин, N-этиласпарагин, гомопролин, гидроксилизин, аллогидроксилизин, 3-гидроксипролин, 4-гидроксипролин, изодесмозин, аллоизолейцин, N-метилаланин, N-метилглицин, N-метилизолейцин, N,N-метилпентилглицин, N-метилвалин, нафталанин, норвалин, норлейцин, орнитин, пентилглицин, пипеколовую кислоту и тиопролин. Предпочтительно, аналоги эксендинов включают одну, две, три, четыре или пять аминокислотных замен.
В некоторых вариантах изобретения аналоги эксендинов включают пептидные аналоги, полученные добавлением к последовательностям или отнятием от последовательностей нативного эксендина-3 или эксендина-4 одной или более аминокислот. Предпочтительно, аналоги эксендинов включают пептидные аналоги, полученные добавлением к последовательностям или удалением из последовательностей нативного эксендина-3 или эксендина-4 от одной до двадцати аминокислот. В некоторых вариантах изобретения аналоги эксендинов включают пептидные аналоги, полученные добавлением к последовательностям или удалением из последовательностей нативного эксендина-3 или эксендина-4 от одной до пятнадцати аминокислот, или добавлением к последовательностям или удалением из последовательностей нативного эксендина-3 или эксендина-4 от одной до десяти аминокислот, или добавлением к последовательностям или удалением из последовательностей нативного эксендина-3 или эксендина-4 от одной до пяти аминокислот.
Аналоги эксендина могут иметь обратимое или необратимое химическое блокирование или химическую модификацию на N-конце, С-конце или в боковых цепях. Например, С-конец эксендина или аналога эксендина может быть амидированным.
В некоторых вариантах изобретения эксендины или аналоги эксендинов содержат аминокислотные последовательности SEQ ID NO: 1-265. Предпочтительно, эксендины или аналоги эксендинов содержат аминокислотные последовательности SEQ ID NO: 1-2 или аминокислотные последовательности SEQ ID NO: 3-229, или аминокислотные последовательности SEQ ID NO: 230-265.
Активность ПЭГ-модифицированных эксендинов или аналогов эксендинов по данному описанию можно проверять на клеточном уровне с помощью анализа, описанного Gong Qiuhong et. al. (Chinese Journal of Incretion and Metaboly, 2004, 20, 559-560). Вкратце, анализ проводят, добавляя глюкозу и ПЭГ-модифицированные эксендины или аналоги эксендинов в различных концентрациях к INS-1 клеткам, инкубируют в течение 4 часов, определяют количество инсулина в супернатанте с помощью радиоиммуноанализа и, наконец, анализируют количество инсулина в INS-1 клетках методом RT-ПЦР с помощью полуколичественного анализа. С помощью вышеуказанного метода можно проводить скрининг в больших масштабах активности модифицированных ПЭГ-производными эксендинов или аналогов эксендинов,. Такой скрининг можно также проводить, определяя изменение уровня сахара в крови мышей (например, мышей С57 или db/db) в различные временнЫе точки после введения дозы.
Фармацевтические композиции и их применение
Некоторые варианты изобретения включают фармацевтические композиции или соединения, содержащие ПЭГ-модифицированные эксендины или аналоги эксендинов по данному описанию. Модифицированные ПЭГ-производными эксендины или аналоги эксендинов по данному описанию могут реагировать с различными неорганическими и органическими кислотами или щелочами с образованием солей. Такие соли включают соли, полученные с органическими и неорганическими кислотами, причем органические и неорганические соли включают, но без ограничения, соляную кислоту, бромистоводородную кислоту, серную кислоту, фосфорную кислоту, трифторуксусную кислоту, уксусную кислоту, муравьиную кислоту, метнсульфокислоту, толуолсульфокислоту, малеиновую кислоту, фумаровую кислоту и камфорсульфокислоту. Соли, полученные из щелочей, включают, но без ограничения, соли аммония, соли щелочных металлов (например, натриевые и калиевые соли) и соли щелочноземельных металлов (например, кальциевые и магниевые соли). Предпочтительные соли включают, например, ацетаты, гидрохлориды и трифторацетаты. Соли можно получать обычными методами. Например, такие соли можно получать по реакции эксендинов или аналогов эксендинов с одним или более эквивалентов соответствующей кислоты или щелочи в растворителе или в среде, в которой полученная соль нерастворима, или в таком растворителе, как вода, которую удаляют в вакууме или лиофилизацией, или заменой ионов в имеющейся соли на другой ион на подходящей ионообменной смоле.
В некоторых вариантах изобретения ПЭГ-модифицированные эксендины или аналоги эксендинов по данному описанию можно также приготовить в качестве фармацевтически приемлемых солей (например, в виде соли, образующейся в результате присоединения кислоты) и/или их комплексов. Приготовление таких солей может содействовать применению в фармакологии за счет изменения физических или химических характеристик композиции, не препятствуя проявлению физиологического действия композиции. Примеры применимых изменений физических свойств включают снижение температуры плавления, что способствует чресслизистому введению, или повышение растворимости, что облегчает введение более высоких концентраций лекарства.
Фармацевтически приемлемые соли включают, например, соли присоединения кислот, такие как соли: сульфат, гидрохлорид, фосфат, сульфамат, ацетат, цитрат, лактат, тартрат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, циклогесилсульфамат и соль хинной кислоты (хиннат). Фармацевтически приемлемые соли можно также получать с органическими и неорганическими кислотами, такими как хлористоводородная (соляная) кислота, серная кислота, фосфорная кислота, сульфаминовая кислота, уксусная кислота, лимонная кислота, молочная кислота, винная кислота, малоновая кислота, метансульфокислота, этансульфокислота, бензолсульфокислота, п-толуолсульфокислота, циклогексилсульфаминовая кислота и хинная кислота. Такие соли можно получать по реакции эксендинов или аналогов эксендинов с одним или более эквивалентов соответствующей кислоты или щелочи в растворителе или в среде, в которой полученная соль нерастворима, или в таком растворителе, как вода, которую удаляют в вакууме или лиофилизацией, или заменой ионов в имеющейся соли на другой ион на подходящей ионообменной смоле.
Чтобы было проще вводить композицию субъекту, можно также использовать носители или эксципиенты. Примеры носителей и эксципиентов включают, например, карбонат кальция, фосфат кальция, различные сахара (например, лактозу, глюкозу или сахарозу) или различные виды крахмала, производные целлюлозы, желатин, растительные масла (например, кунжутное масло, арахисовое масло, оливковое масло), полиэтиленгликоли и физиологически совместимые растворители. Композиции или фармацевтические композиции можно вводить различными путями, включая, например, внутривенный, интраперитонеальный (внутрибрюшинный), подкожный и внутримышечный, пероральный, топический и трансмукозальный (чресслизистый) пути введения.
При желании можно повысить вязкость растворов композиций по изобретению с помощью загустителей, таких как метилцеллюлоза. Их можно приготовить в виде эмульсий (например, вода-в-масле или масло-в-воде). Можно применять любые фармацевтически приемлемые эмульгаторы, известные в уровне техники, включая порошок аравийской камеди, неионное поверхностно- активное вещество (например, Твин) или ионное поверхностно- активное вещество (например, алкоголяты полиалкиленоксидсульфатов или сульфонатов, такие как Тритон).
Композиции можно стерилизовать обычными методами стерилизации или фильтрованием. Композиции могут содержать фармацевтически приемлемые вспомогательные вещества, которые имеют характеристики, тождественные требуемым физиологическим характеристикам, такие как рН буферизующие агенты. Применимые буферы включают, например, ацетатный буфер (ацетат натрия/уксусная кислота). Суппозиторий или препарат с замедленным высвобождением можно использовать с тем, чтобы в кровотоке в течение многих часов или дней после трансдермальной инъекции или доставки сохранялись фармацевтически эффективные количества препарата.
Заданную изотоничность можно получать, используя хлорид натрия или другие фармацевтически приемлемые агенты, такие как глюкоза, борная кислота, тартрат натрия, пропиленгликоль, полиолы (например, манит и сорбит) или другие неорганические или органические растворители. Для буферов, содержащих ион натрия, предпочтительным является хлорид натрия.
В одном варианте изобретения для пациента с массой тела около 70 кг эффективная дозировка соединения составляет, примерно, от 0.01 или, примерно, от 0.03 мг, примерно, до 5 мг в день, предпочтительно, от 0.01 мг, примерно, до 0.5 мг в день, более предпочтительно, от 0.01 или, примерно, от 0.1 мг, примерно, до 1 мг в день, предпочтительно, и вводится в виде одной или более доз. Точную дозу может определить лечащий врач, она должна лежать в указанных интервалах и зависит также от возраста, веса и симптомов у отдельного пациента.
В некоторых вариантах изобретения ПЭГ-модифицированный эксендин или аналог эксендина по данному описанию можно вводить субъекту для лечения сахарного диабета. В некоторых вариантах изобретения введение соединения следует начинать в момент проявления симптомов сахарного диабета или непосредственно после того, как диагностирован сахарный диабет. Необязательно, как указано в других вариантах изобретения, соединение можно вводить до проявления симптомов, в качестве профилактического лечения.
Хотя соединения обычно применяются для лечения людей, их можно применять также для лечения сходных или идентичных заболеваний у других позвоночных, таких как другие приматы, сельскохозяйственные животные (например, свиньи, крупный рогатый скот и домашняя птица), домашние или спортивные животные (например, лошади, собаки и кошки).
Нижеприведенные примеры даны для того, чтобы лучше проиллюстрировать заявляемое изобретение и не предполагают ограничивать объем изобретения. Когда упоминаются конкретные материалы, это делается лишь с целью иллюстрацию, а не с целью ограничить изобретение. Специалист в данной области техники может разработать эквивалентные способы или реагенты без осуществления данного изобретения и не выходя за его объем. Понятно, что можно осуществить много вариантов процедур по данному описанию, оставаясь в пределах настоящего изобретения. Изобретатели полагают, что такие варианты входят в объем настоящего изобретения.
Примеры
Линейное ПЭГ-производное с молекулярной массой 5000 Да получают от Sigma-Aldrich Corporation. Другие ПЭГ-производные, применяемые по данному описанию, получают от Beijing JenKem Technology Co., Ltd.
Хроматографы А, В Double-Pump АКТА purifier, применяемые для ионообменной хроматографии, и другие колонки получают от General Electric. Соответствующие реагенты поставляет фирма Sigma-Aldrich. Нативный эксендин-4 и и его аналоги, применяемые в Примерах 3-9, получают от фирмы Chengdu Sheimuo Science and Technology Co. Ltd.
Пример 1. Твердофазный синтез аналогов эксендина-4
В Примере 1 представлен способ твердофазного синтеза аналога эксендина-4, имеющего следующую аминокислотную последовательность:
[His-Gly-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Arg-Glu-Glu-Glu-Ala-Val-Lys-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-OH] (SEQ ID NO: 232).
(1) Аминокислотные остатки:
Где:
Fmoc обозначает 9-флуоренилметоксикарбонил;
BOC обозначает трет-бутоксикарбонил;
Trt обозначает трифенилметил;
OtBu обозначает трет-бутиловый эфир;
tBu обозначает трет-бутил.
(2) Прибор и реагенты для синтеза
Пептидный синтез проводят в пептидном синтезаторе Peptide Synthesizer 433А (Applied Biosystem, USA).
В данном синтезе используют следующие реагенты: N-метилпирролидон, хлористый метилен, гексагидропиридин, метанол, диметиламинопиридин/ DMF (ДМФА), N,N-диизопропилэтиламин/ NMP, HBTU 100 ммолей/0.5 М НОВТ в ДМФА, N,N-дициклогексилкарбодиимид/ NMP.
Где:
DMF (ДМФА) обозначает N,N-диметилформамид,
NMP обозначает N-метилпирролидон,
НОВТ обозначает 1- гидроксибензотриазол,
HBTU обозначает гексаметилфторфосфат 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония.
(3) Процедуры
а. Синтез
Количества реагентов, используемых в синтезе, описанном ниже, берут из расчета 0.25 ммоля. Взвешивают 0.25 г НМР смолы и помещают в реакционный сосуд синтезатора. Взвешивают 1 ммоль различных аминокислот, имеющих защитные группы, и размещают в синтезаторе в порядке аминокислотной последовательности заданного производного инсулинотропного пептида от С- конца к N-концу. При комнатной температуре 25°С под контролем компьютерной программы автоматически осуществляют реакции снятия защитной группы Fmoc, активации остатка и связывания активированного остатка с НМР смолой. Такие реакции повторяют до тех пор, пока не будет синтезирован целый пептид. По завершении синтеза смолу, связанную с синтезированным пептидом, имеющим защитные группы в боковых аминокислотных цепях, сушат воздухом в пептидном синтезаторе, а затем взвешивают.
б. Снятие защитных групп и отщепление от смолы
Смолу, связанную с синтезированным пептидом, имеющим защитные группы, помещают в колбу Эрленмейера, закрывают пробкой и добавляют отщепляющий реагент, показанный ниже.
Эту реакцию проводят при температуре 30°С в течение шести часов при постоянном перемешивании. Затем смесь фильтруют, водные фильтраты объединяют и смолу промывают небольшим количеством трифторуксусной кислоты (ТФК, TFA). Промывочный раствор смешивают с объединенными водными фильтратами. Затем для преципитации к смеси прибавляют эфир и выпавшие осадки промывают небольшим количеством эфира. Осадки сушат в сушильном шкафу, получают сырой продукт.
в. Выделение и очистка методом ВЭЖХ и лиофилизация
Сырой продукт выделяют и очищают препаративной ВЭЖХ, а затем лиофилизируют, получая конечный продукт. Молекулярную массу продукта анализируют с помощью хроматографии и масс- спектрометрии. Теоретическая (вычисленная) молекулярная масса синтезированного пептида равна 4300.6, а найденная молекулярная масса равна 4316.7.
Аналогично, специалист в данной области техники может использовать вышеописанный метод для синтеза других эксендинов или аналогов эксендинов.
Пример 2. Получение аналога эксендина-4 методами генной инженерии (методами рекомбинантной ДНК)
В данном примере описан способ получения аналога эксендина-4, имеющего нижеприведенную аминокислотную последовательность, метами рекомбинантной ДНК:
[His-Gly-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-Glu-Glu-Glu-Ala-Val-Lys-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-Arg-OH] (SEQ ID NO: 251).
А. Исходя из аминокислотных последовательностей аналога эксендина, который нужно получить, синтезируют следующие фрагменты гена:
(1) 5' ААТ ТСС ATG САС GGC GAA АСС ТТС АСС AGC GAT CTG AGC ААА CAG CTG GAA GAA GAA GCG GTT АА (SEQ ID NO: 266)
(2) 5' ACTG ТТС АТС GAA TGG CTG ААА AAC GGC GGC CCG AGC AGC GGC CCG CCG CCG CCG AGC CGT TAG A (SEQ ID NO: 267)
(3) 5' AGCTT СТА ACG GCT CGG CGG CGG CGC GCT GCT CGG GCC GCC GTT TTT CAG CCA ТТС GAT GA (SEQ ID NO: 268)
(4) 5' ACAG TTT AAC CGC ТТС ТТС ТТС CAG CTG TTT GCT CAG АТС GCT GGT GAA GGT GCC ТТС GCC GTG CAT GG (SEQ ID NO: 269)
Б. Клонирование
Лигирование: Берут две пробирки. В одну пробирку помещают фрагменты гена (1) и (4) и смешивают. В другую пробирку помещают фрагменты гена (2) и (3) и смешивают. В каждую пробирку помещают буфер для полинуклеотидкиназы, полинуклеотидкиназу и аденозинтрифосфат (АТФ, АТР). Реакционные смеси инкубируют при 37°С в течение 60 минут, при этом происходит фосфорилирование 5' конца фрагментов гена. Обе пробирки помещают в водяную баню при 95°С и инкубируют 10 минут. Затем пробирки оставляют охлаждаться на воздухе до комнатной температуре. В каждую пробирку добавляют буфер для Т4 лигазы и Т4 лигазу и смеси инкубируют в течение ночи при 16°С, что способствует лигированию фрагментов гена.
Плазмида: Плазмиду, содержащую промотор Lac (промотор PL, контролируемую которым экспрессию можно регулировать, меняя температуру, или Тас промотор), расщепляют рестриктазами EcoR I и Hind III и экстрагируют раствором фенол/хлороформ. Смесь центрифугируют и водную фазу объединяют. Водную фазу экстрагируют хлороформом и трижды центрифугируют. К полученной водной фазе добавляют изопропанол (выпадает осадок), центрифугируют и осадок сушат на воздухе.
Расщепленную плазмиду и дотированный фрагмент гена смешивают. К смеси прибавляют буфер для Т4 лигазы и Т4 лигазу и инкубируют при комнатной температуре 3-4 часа.
Культивирование клеток- хозяев: Клетки Е. Coli JM103 инкубируют при 37°С в LB бульоне, содержащем 10 г пептона, 5 г дрожжевого экстракта и 5 г NaCl, при встряхивании в течение 4 часов. Бактериальные культуры центрифугируют и осадок обрабатывают раствором CaCli и хранят при 4°С для дальнейшего использования.
Трансформация: Клонированную плазмиду трансформируют в клетки- хозяева Е. Coli JM103. Трансформированные бактериальные клетки инкубируют в бане со льдом в течение 30 минут, а затем инкубируют при 42°С 2 минуты. Бактериальные клетки засевают в плашке с агаром, содержащей ампициллин, и инкубируют в течение ночи при 37°С. Колонии, выращенные на агаре, отбирают в качестве позитивных клонов, содержащих рекомбинантные плазмиды.
В. Ферментация
Штамм выбранный бактериальной клетки-хозяина, содержащей заданную плазмиду, инкубируют при встряхивании в LB-бульоне. К культуральной жидкости прибавляют 0.5 мМ изопропил бета-D-тиогалактопиранозида (EPTG) для того, чтобы индуцировать экспрессию заданного пептида. Инкубируют в течение ночи, бактериальные клетки собирают центрифугированием. Экспрессированные пептиды идентифицируют электрофорезом в полиакриламидном геле (PAGE), содержащем 12% SDS.
Г. Тельца включения
Десять колб, каждая из которых содержит 300 мл бактериальных культу, инкубируют при встряхивании в указанных выше условиях. После индукции экспрессии белка к культуральной жидкости прибавляют раствор для лизиса (20 мМ раствор фосфатного буфера, содержащий 1% NaCl, pH 7.5) и лизоцим и инкубируют при 30°С 30 минут, а затем центрифугируют, собирая преципитаты (осадки). Собранные преципитаты обрабатывают 6М раствором гуанидина гидрохлорида (Gu.HCl) для растворения телец включения. Раствор центрифугируют и полученный супернатант подвергают диализу, удаляя Gu.HCl. Осадки, образующиеся в результате диализа, трижды промывают 20 мМ раствором фосфатного буфера (рН 7.5), содержащим 1% NaCl и 0.1% Твин 80, получают тельца включения.
Д. Разрушение
Тельца включения растворяют в 0.8 М растворе мочевины. Затем к раствору прибавляют соляную кислоту и цианогенбромид. Конечная концентрация соляной кислоты в растворе составляет 50 мМ. Раствор перемешивают в темноте под азотом в течение 2 часов для разрушения телец включения. Для контроля за процессом используют ВЭЖХ анализ.
Е. Очистка.
После разрушения телец включения сырой продукт получают хроматографией на Сефарозе G-25. Далее сырой продукт очищают с помощью ВЭЖХ, получают конечный продукт. Аналогично продукту, полученному химическим синтезом, молекулярная масса полученного пептида, полученная методом масс-спектрометрии, соответствует вычисленной молекулярной массе.
Пример 3. Эксендин-4, модифицированный с помощью линейных метоксипроизводных полиэтиленгликоля (мПЭГ, mPEG) (Mf: 5000 Да)
В каждую из трех пробирок помещают по 1.0 мг эксендина-4 и растворяют в фосфатном буфере с различным рН, соответственно. В каждую пробирку прибавляют по 5.8 мг активированного N-гидроксисукцинимидом мПЭГ (Mf: 5000 Да). Смесь встряхивают на качалке, один час при комнатной температуре. Полученные продукты анализируют, определяя количество немодифицированного эксендина-4 на ВЭЖХ хроматографе Agilent 1100 (условия анализа: растворитель А: 0.1% фосфорная кислота; растворитель В: 0.1% фосфорная кислота +80% ацетонитрила; градиент: 35%-70% растворителя В/25 минут). Ниже показаны результаты:
Влияние различных значений рН на ПЭГилирование эксендина-4
Отгонкой ацетонитрила из раствора, полученного при разделении обращенно-фазовой хроматографией (см. выше), получают раствор (рН 3-4), содержащий мПЭГ-модифицированный эксендин-4.
Пример 4. Аналоги эксендина, модифицированные линейными мПЭГ-производными (Mn: 21000 Да).
1.0 мг аналога эксендина-4 смешивают с 2.0 мл фосфатного буфера (рН 4.5), содержащего NaBH3CN. 5.0 мг активированных альдегидом мПЭГ-производных с молекулярной массой 21000 Да смешивают с аналогом эксендина-4 и встряхивают на качалке при комнатной температуре в течение ночи. Реакционную смесь очищают на хроматографе Agilent 1100 на колонке Zorbax SB-300 для полупрепаративной хроматографии (условия анализа: растворитель А: 0.1% фосфорная кислота; растворитель В: 0.1% фосфорная кислота +80% ацетонитрила; градиент: 35%- 70% растворителя В/25 минут). При этом получают аналог эксендина-4, модифицированный мПЭГ на N-конце.
Из полученного выше раствора на роторном испарителе отгоняют ацетонитрил, обессоливающую колонку используют для замены (задерживания) буфера, полученный модифицированный эксендин-4 затем растворяют в фосфатном буфере (рН 7.0-8.0) с 0.001-1.0% (вес/об) 3-метилфенола,
Пример 5. Аналог эксендина, модифицированный мПЭГ-производными (Mn: 40000 Да), имеющий структуру Формулы IV
1.0 мг аналога эксендина-4 (SEQ ID NO: 251) прибавляют к 4.0 мл фосфатного буфера (рН 7.0). 280 мг активированного N-гидроксисукцинимидом мПЭГ (mPEG)-производного (Формулы IV) с молекулярной массой 40000 Да смешивают с полученным выше аналогом эксендина-4 и проводят реакцию, встряхивая на качалке один час при комнатной температуре. Затем к реакционной смеси прибавляют 200 мл буфера BistTris (рН 7.0) в химическом стакане на 250 мл для последующего использования.
Анионообменную колонку DEAE FF или ANX FF уравновешивают буфером BisTris (рН 7.0). Разбавленную реакционную смесь наносят на анионообменную колонку, абсорбируя целевое вещество на ионообменной смоле. Один или ряд модифицированных аналогов эксендина-4 элюируют в линейном градиенте NaCl в различных концентрациях и элюат собирают с помощью коллектора фракций. Немодифицированный пептид эксендин-4 элюируют с помощью 1М NaCl. Элюированные фракции, полученные в процессе разделения и очистки, показаны на Фигуре 3, где цифрами 2, 3 и 4 показаны пики элюции модифицированного множеством мПЭГ аналога эксендина-4, модифицированного единичным мПЭГ аналога эксендина-4 и немодифицированного аналога эксендина-4, соответственно. Модифицированный аналог эксендина-4 подвергают электрофорезу в геле SDS-PAGE. Молекулярная масса модифицированного аналога эксендина-4 (с вычисленной молекулярной массой 44300 Да), найденная методом SDS-PAGE, немного выше 43000 Да (Фигура 4), это показывает, что полученный продукт на самом деле является модифицированным единичным мПЭГ-производным (Mn: 40000 Да) аналогом эксендина-4.
Объединенный элюат, содержащий модифицированный единичным мПЭГ-производным аналог эксендина-4, упаривают на ультрафильтрационной установке (центрифужная пробирка для ультрафильтрации или ультрафильтрационное устройство). Концентрированный раствор переносят в колонку для обессоливания, чтобы заменить на ацетатный буфер. Наконец, к ацетатному буферу, содержащему модифицированный аналог эксендина-4, прибавляют агент, корректирующий изотоничность (такой как маннит и 0.9% NaCl), и 0.001-1.0% (вес/об) антибактериального агента (такой как 3 метилфенол).
Пример 6. 24-часовое испытание лекарственного действия аналогов эксендинов, модифицированных единичными мПЭГ-производными (Mf: 5000 Да и Mn: 21000 Да)
Подопытное животное: мыши С57, 20 г+/-2 г, 8 мышей в каждой группе, всего 4 группы.
Контрольная группа 1: Каждой мыши подкожно инъецируют стерильную воду.
Контрольная группа 2: Каждой мыши подкожно инъецируют 0.025 мкг аналога эксендина-4.
Группа, получающая лекарство, 1: Каждой мыши подкожно инъецируют 0.625 мкг аналога эксендина-4, модифицированного единичными мПЭГ-производными (Mf: 5000 Да).
Группа, получающая лекарство, 2: Каждой мыши подкожно инъецируют 0.625 мкг аналога эксендина-4, модифицированного единичными мПЭГ-производными (Mn: 21000 Да).
Пробы крови берут в каждой группе мышей через 4, 8, 12, 16 и 24 часа после инъекции лекарства. За 30 минут до взятия образца крови каждой мыши в живот инъецируют 200 мкл 20% раствора глюкозы. Уровни сахара в крови определяют, используя набор реагентов для определения глюкозы (Shanghai ShenSuo Reagents Co., Ltd.). Как показано на Фигуре 5, аналоги эксендина-4, модифицированные мПЭГ-производными (Mn: 21000 Да) сохраняют активность через 16 часов после инъекции. Активный период для аналога эксендина-4, модифицированного мПЭГ-производными (Mf: 5000 Да), составляет 12-16 часов после инъекции лекарства. Немодифицированные аналоги эксендина-4 сохраняют активность менее 12 часов. Период эффективного снижения уровня сахара в крови является более продолжительным при использовании аналогов эксендина-4, модифицированных линейными мПЭГ производными с более высокой молекулярной массой, чем при использовании аналогов эксендина-4, модифицированных линейными мПЭГ производными с более низкой молекулярной массой.
Пример 7. 72-часовое испытание лекарственного действия аналогов эксендинов, модифицированных линейными мПЭГ (Mn=21000 Да) и разветвленными мПЭГ, имеющими структуру Формулы IV (Mn=40000 Да)
Подопытное животное: мыши С57, 20 г+/-2 г, 8 мышей в каждой группе, всего 5 групп.
Контрольная группа 1: Каждой мыши подкожно инъецируют стерильную воду.
Контрольная группа 2: Каждой мыши подкожно инъецируют 0.025 мкг пептида эксендина-4.
Контрольная группа 3: Каждой мыши подкожно инъецируют 0.025 мкг пептида эксендина.
Группа, получающая лекарство, 1: Каждой мыши подкожно инъецируют 0.625 мкг аналога эксендина-4, модифицированного мПЭГ (Mn: 21000 Да).
Группа, получающая лекарство, 2: Каждой мыши подкожно инъецируют 0.625 мкг аналога эксендина-4, модифицированного мПЭГ (Mn: 40000 Да).
Пробы крови берут в каждой группе мышей через 4, 8, 24, 48 и 72 часа после инъекции лекарства. За 30 минут до взятия образца крови каждой мыши в живот инъецируют 200 мкл 20% раствора глюкозы. Уровни сахара в крови определяют, используя набор реагентов для определения глюкозы. Как показано на Фигуре 6, аналог эксендина-4, модифицированный разветвленными мПЭГ-производными (Mn: 40000 Да), сохраняют активность, по меньшей мере, 72 часа после инъекции лекарства. Активный период для аналога эксендина-4, модифицированного линейными мПЭГ-производными (Mn: 21000 Да), составляет около 24 часов после инъекции лекарства.
Пример 8. 72-часовое испытание лекарственного действия аналогов эксендинов, модифицированных единичными мПЭГ-производными
Образцы для испытания: всего 8 образцов, аналоги эксендина-4, модифицированные единичными мПЭГ-производными (Формулы II) с молекулярными массами 21000 Да, 30000 Да, 40000 Да, соответственно; аналоги эксендина-4, модифицированные единичными мПЭГ-производными (Формулы IV) с молекулярными массами 21000 Да, 30000 Да, 40000 Да, соответственно; аналоги эксендина-4, модифицированные линейными мПЭГ-производными с молекулярными массами 21000 Да и 30000 Да, соответственно.
Подопытное животное: мыши С57, 20 г+/-2 г, 3 группы; 24 мыши в каждой подопытной группе.
Так как животные могут не выдержать частого отбора проб, мы разработали схему отбора образцов в подопытных группах в разное время после инъекции. Ниже дается схема отбора проб после инъекции:
Каждую из подопытных групп делят на 8 подгрупп.Каждая подгруппа включает
3 мышей. В начале испытания мышам в каждой подгруппе инъецируют различные модифицированные аналоги эксендина-4, которые обозначают L21K, L30K (модификация одиночными линейными мПЭГ (mPEG)-производными с молекулярными массами 21000 Да и 30000 Да, соответственно); Y21K, УЗОК, Y40K (модификация одиночными линейными мПЭГ (mPEG)- производными, имеющими структуру Формулы IV и молекулярные массы 21000 Да, 30000 Да и 40000 Да, соответственно), U21K, U30K, U40K (аналоги эксендина-4, модифицированные одиночными мПЭГ, имеющими структуру Формулы II и молекулярные массы 21000 Да, 30000 Да и 40000 Да, соответственно). Каждый из различных мПЭГ-модифицированных аналогов эксендина-4 содержит 0.625 мкг аналогов эксендина-4. Непосредственно после инъекции лекарства мышам в брюшную полость инъецируют 200 мкл 20% раствора глюкозы. Через полчаса у всех мышей берут пробы крови. Последующий отбор проб крови проводят в соответствии со схемой, представленной в вышеприведенной таблице. За полчаса до отбора каждой пробы в брюшную полость мышей инъецируют 200 мкл 20% раствора глюкозы. На Фигурах 7-9 показано, что структура молекулы и молекулярная масса ПЭГ-производных оказывают огромное влияние на биоактивность аналогов эксендина-4. Биоактивность аналогов эксендина-4, модифицированных единичным мПЭГ, имеющим структуру Формулы II, сохраняется высокой в течение более продолжительного времени, чем биоактивность аналогов эксендина-4, модифицированных ПЭГ, имеющими структуру Формулы IV и линейными ПЭГ, в испытании в течение 72 часов после введения лекарства. В случае аналогов эксендина-4, модифицированных единичным ПЭГ, имеющими такую же разветвленную структуру, чем больше их молекулярная масса, тем более высокую биоактивность при снижении уровня сахара в крови они проявляют в течение 72 часов. L30K не проявляет заметной биоактивности через 72 часа после введения лекарства, это показывает, что более высокая молекулярная масса линейного ПЭГ отрицательно влияет на биоактивность модифицированного аналога эксендина-4.
Пример 9. Фармакокинетический анализ аналогов эксендина-4, модифицированных единичным ПЭГ.
Подопытное животное: мыши SD самцы, 250-300 г, 2 группы, по 4 мыши в каждой группе.
Группа, получающая лекарство, 1: Каждой мыши инъецируют аналоги эксендина-4 (SEQ ID NO: 251), модифицированные единичными мПЭГ-производными (Формула II, Mn: 30000 Да), содержащие 4.375 мкг аналогов эксендина-4 (U30K).
Группа, получающая лекарство, 2: Каждой мыши инъецируют аналоги эксендина-4 (SEQ ID NO: 251), модифицированные единичными мПЭГ-производными (Формула IV, Mn: 40000 Да), содержащие 4.375 мкг аналогов эксендина-4 (Y30K).
Пробы крови берут в каждой группе мышей через 0, 2, 4, 8, 12, 16, 24, 36, 48, 60 и 72 час после инъекции лекарства. Концентрацию эксендина-4 в крови определяют, используя набор для ферментативного иммуноанализа (EIA) от Phoenix Pharmaceuticals Inc. California, USA. Данные анализируют с помощью Pharmaceutical Kinetics Software 1.0.2 (Shanghai Hongneng Software со. Ltd), результаты представлены на Фигуре 10. Время абсорбции половины U30K, составляет 10.78 час, а время элиминирования половины U30K, составляет 21.44 час. Время абсорбции половины Y40K, составляет 5.53 час, а время элиминирования половины Y30K, составляет 40.77 час. Время, за которое достигается максимальная (пик) концентрация обоих образцов в крови, составляет около 12 часов после инъекции лекарства. Максимальная (пик) концентрация обоих образцов в крови составляет около 20 нг/мл.
Как сказано выше, предполагается, что вышеприведенное описание лишь иллюстрирует различные варианты, настоящего изобретения. Конкретные модификации, обсуждаемые выше, не предполагаются как ограничение объема изобретения. Для специалиста в данной области техники очевидно, что можно осуществить различные эквиваленты, изменения и модификации, не отступая от объема изобретения, и понятно, что такие эквивалентные варианты изобретения непременно входят в данное описание.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ КОМПОЗИЦИИ АГОНИСТОВ ЭКСЕНДИНА И СПОСОБЫ ИХ ВВЕДЕНИЯ | 2000 |
|
RU2242244C2 |
| НОВЫЙ ВАРИАНТ ЭКСЕНДИНА И ЕГО КОНЪЮГАТ | 2010 |
|
RU2528734C2 |
| Сайт-специфически монопегилированные аналоги эксендина и способ их получения | 2012 |
|
RU2625015C2 |
| СТАБИЛИЗИРОВАННЫЕ СОЕДИНЕНИЯ ЭКСЕНДИНА-4 | 2003 |
|
RU2376314C2 |
| АНАЛОГИ ГЛЮКАГОНА, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ И СТАБИЛЬНОСТЬЮ В БУФЕРАХ С ФИЗИОЛОГИЧЕСКИМИ ЗНАЧЕНИЯМИ Ph | 2009 |
|
RU2560254C2 |
| АНАЛОГИ ГЛЮКАГОНА, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ В БУФЕРАХ С ФИЗИОЛОГИЧЕСКИМ ЗНАЧЕНИЕМ pH | 2008 |
|
RU2477286C2 |
| КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ АГОНИСТ РЕЦЕПТОРА GLP-1 И АГОНИСТ ГЛЮКАГОНОВОГО РЕЦЕПТОРА, И ЕЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2719144C2 |
| ПЕПТИДНЫЕ ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ С ПОВЫШЕННОЙ ЭФФЕКТИВНОСТЬЮ ПРОТИВ ИНСУЛИНОРЕЗИСТЕНТНОСТИ | 2012 |
|
RU2602801C2 |
| ДВОЙНЫЕ АГОНИСТЫ GLP1/GIP ИЛИ ТРОЙНЫЕ АГОНИСТЫ GLP1/GIP/ГЛЮКАГОНА | 2013 |
|
RU2652783C2 |
| СПОСОБЫ ПОДАВЛЕНИЯ ГЛЮКАГОНА | 2000 |
|
RU2247575C9 |































































Изобретение относится к области биохимии. Предложен ПЭГ-модифицированный эксендин или аналог эксендина, содержащий одно или более ПЭГ-производных (варианты). Одно или более ПЭГ-производных имеют разветвленную структуру (I) или (III), как указано в формуле. Молекулярная масса указанных одного или более ПЭГ-производных составляет от 5000 Да до 40000 Да. Также предложены композиция и способ лечения сахарного диабета с применением указанного ПЭГ-модифицированного эксендина или аналога эксендина. Предложенные ПЭГ-модифицированные эксендины или аналоги эксендинов имеют продолжительный период полужизни в крови, высокую биоактивность и низкую иммуногенность. 5 н. и 20 з.п. ф-лы, 10 ил., 3 табл., 9 пр.
1. ПЭГ-модифицированный эксендин или аналог эксендина, содержащий одно или более ПЭГ-производных, связанных с одной или более аминокислотами указанного эксендина или аналога эксендина, причем аналоги эксендина выбраны из группы, состоящей из: нативного эксендина-3; нативного эксендина-4; пептидов, полученных путем замены, добавления или удаления одного или более аминокислотных остатков к или из аминокислотных последовательностей нативного эксендина-3 или нативного эксендина-4; их пептидных аналогов, полученных путем обратимого или необратимого блокирования или модификации N-конца, С-конца и/или боковых цепей пептидов, и причем указанные одно или более ПЭГ-производных имеют разветвленную структуру, изображенную формулой I, а молекулярная масса указанных одного или более ПЭГ-производных составляет от приблизительно 5000 до приблизительно 40000 Да:
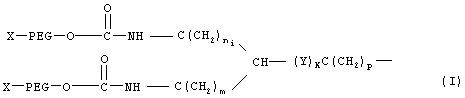
где Х обозначает водород или защитную группу; PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число; ni обозначает целое число от 0 до 5; m обозначает целое число от 0 до 5; Y обозначает О, S, SO, SO2 или NR1, где R1 обозначает водород или незамещенную (C1-C8) алкильную группу или незамещенную циклоалкильную группу; k обозначает 0 или 1 и р обозначает целое число от 0 до 6.
2. ПЭГ-модифицированный эксендин или аналог эксендина по п.1, отличающийся тем, что указанные одно или более ПЭГ-производных имеют разветвленную структуру, представленную формулой II
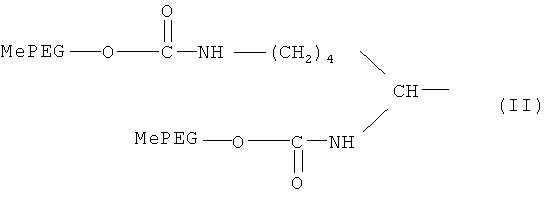
где PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число и Me обозначает метильную группу.
3. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, представленную в SEQ ID NO: 1.
4. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, представленную в SEQ ID NO: 2.
5. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, выбранную из SEQ ID NO: 3 - SEQ ID NO: 229.
6. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2 отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, выбранную из SEQ ID NO: 230 - SEQ ID NO: 265.
7. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что указанные одно или более ПЭГ-производных имеют молекулярную массу от приблизительно 20000 до приблизительно 40000 Да.
8. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что указанные одно или более ПЭГ-производных имеют молекулярную массу более 20000 Да.
9. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, отличающийся тем, что указанные одно или более ПЭГ-производных активируют для связывания с указанным эксендином или аналогом эксендина с помощью N-гидроксисукцинимида.
10. ПЭГ-модифицированный эксендин или аналог эксендина по пп.1 и 2, содержащий одно, два, три или четыре разветвленных ПЭГ-производных.
11. ПЭГ-модифицированный эксендин или аналог эксендина по п.10, содержащий одно разветвленное ПЭГ-производное.
12. ПЭГ-модифицированный эксендин или аналог эксендина, содержащий одно или более ПЭГ-производных, связанных с одной или более аминокислотами указанного эксендина или аналога эксендина, причем аналоги эксендина выбраны из группы, состоящей из: нативного эксендина-3; нативного эксендина-4; пептидов, полученных путем замены, добавления или удаления одного или более аминокислотных остатков к или из аминокислотных последовательностей нативного эксендина-3 или нативного эксендина-4; их пептидных аналогов, полученных путем обратимого или необратимого блокирования или модификации N-конца, С-конца и/или боковых цепей пептидов, и причем указанные одно или более ПЭГ-производных имеют разветвленную структуру, изображенную формулой III, а молекулярная масса указанных одного или более ПЭГ-производных составляет от приблизительно 5000 до приблизительно 40000 Да:
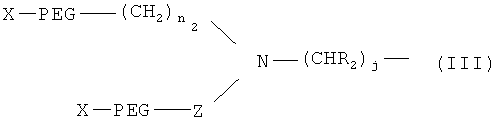
где X обозначает водород или защитную группу; PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число; n2 обозначает целое число от 0 до 10; Z обозначает группу, выбранную из: (СН2)i, (СН2)iOCO, (CH2)iNHCO или (СН2)iCO, где i обозначает целое число от 0 до 10; R2 обозначает водород, незамещенную (C1-C12) алкильную группу, арильную, арилалкильную или гетероалкильную группу и j обозначает целое число от 1 до 12.
13. ПЭГ-модифицированный эксендин или аналог эксендина по п.12, отличающийся тем, что указанные одно или более ПЭГ-производных имеют разветвленную структуру, представленную формулой IV
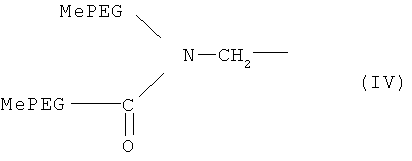
где PEG (ПЭГ) обозначает -O(CH2CH2O)q-, q обозначает целое положительное число и Me обозначает метильную группу.
14. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, представленную в SEQ ID NO: 1.
15. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, представленную в SEQ ID NO: 2.
16. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, выбранную из SEQ ID NO: 3 - SEQ ID NO: 229.
17. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что эксендин или аналог эксендина имеет аминокислотную последовательность, выбранную из SEQ ID NO: 230 - SEQ ID NO: 265.
18. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что указанные одно или более ПЭГ-производных имеют молекулярную массу от приблизительно 20000 до приблизительно 40000 Да.
19. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что указанные одно или более ПЭГ-производных имеют молекулярную массу более 20000 Да.
20. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, отличающийся тем, что указанные одно или более ПЭГ-производных активируют для связывания с указанным эксендином или аналогом эксендина с помощью N-гидроксисукцинимида.
21. ПЭГ-модифицированный эксендин или аналог эксендина по пп.12 и 13, содержащий одно, два, три или четыре разветвленных ПЭГ-производных.
22. ПЭГ-модифицированный эксендин или аналог эксендина по п.21, содержащий одно разветвленное ПЭГ-производное.
23. Композиция для лечения сахарного диабета, содержащая модифицированные ПЭГ-производными эксендины или аналоги эксендинов по любому из пп.1, 2, 12 и 13.
24. Применение ПЭГ-модифицированного эксендина или аналога эксендина по любому из пп.1, 2, 12 и 13 для получения лекарства для предупреждения или лечения сахарного диабета.
25. Способ лечения сахарного диабета, заключающийся во введении субъекту композиции по п.23.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| WO 03076490 A1, 18.09.2003 | |||
| Электропривод постоянного тока | 1986 |
|
SU1372570A1 |
| US 6924264 B1, 02.08.2005 | |||
| НОВЫЕ КОМПОЗИЦИИ АГОНИСТОВ ЭКСЕНДИНА И СПОСОБЫ ИХ ВВЕДЕНИЯ | 2000 |
|
RU2242244C2 |
Авторы
Даты
2013-11-20—Публикация
2007-11-13—Подача