ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение имеет отношение к способам модифицированного продуцирования гликопротеинов в растениях. Настоящее изобретение также предполагает использование растений с модифицированным продуцированием гликопротеинов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Иммуноглобулины (ИгГ) - это сложные гетеромиллиметровые белки с характерной аффинностью для конкретных антигенных аналогов различной природы. В настоящее время регулярное изолирование клеточных линий, образующих ИгГ, и появление технологий для ориентированной на ИгГ эволюции, а также молекулярной инженерии серьезно повлияло на их развитие в качестве биотерапии и на общий рынок продукции медико-биологических исследований. Терапевтические моноклональные ИГГ (моноклональные антитела (МКА)) доминируют на существующем рынке новых противовоспалительных и противораковых средств терапии. А в настоящее время сотни новых потенциальных лечебных препаратов находятся на стадии исследований и клинических испытаний с целью улучшения их свойств или определения новых направлений их применения. Годовая потребность рынка МКА колеблется в пределах от нескольких грамм (диагностика), нескольких килограмм (антитоксины) до одной или нескольких сотен килограммов (биозащита, противораковые, противоинфекционные, противовоспалительные препараты).
Несмотря на то, что культивирование клеток СНО продолжает оставаться предпочтительным основным производством промышленного масштаба, общепризнано, что для того чтобы МКА достигли своего полного влияния на рынок продукции медико-биологических исследований, необходимо создать резервные производственные мощности. Поскольку мощности, необходимые для производства этих культур, не могут быть легко реконструированы по масштабу, расходы на их возведение и содержание являются слишком высокими и постоянно увеличиваются, а их легализация в соответствии с правилами организации производства и контроля качества лекарственных средств (GMP) пока занимает в среднем три года после их создания. Даже на ранних стадиях развития выбор клеточных линий СНО с приемлемым результатом на выходе и эффективностью производства остается дорогостоящим и длительным процессом. Новые производственные мощности, которые снизят растущие расходы (более высокий выход продукции, более простые технологии и инфраструктуры), имеют более короткое время ввода в эксплуатацию, являются легко перераспределяемыми, в то время как соблюдение действующих на данный момент свойств воспроизводимости, качества и безопасности находящихся в обращении систем клеточных культур, вероятно, будет значительно влиять на разработку МКА и вакцин для рынка продукции медико-биологических исследований на каждый стадии развития.
Растения являются удобными «хозяевами» для получения МКА и ряда других белков, применяемых в настоящее время в биологических научных исследованиях (см. Ко и Koprovski, 2005; Ма с соавт., 2005; Yusibov с соавт., 2006 для обзоров последних результатов). Получение МКА происходило в стабильных линиях трансгенных растений с выходом до 200 мг/кг сырой массы (СМ) и путем переходной экспрессии в объемах до 20 мг/кг CM (Kathuria, 2002). В отчете Giritch с соавт. (2006) упоминаются уровни экспрессии величиной 200-300 мг/кг листовой массы для ИГГ, один из упомянутых уровней составляет максимум 500 мг/кг, достигнут путем использования системы переходной экспрессии.
Процесс N-гликолизации у растений и млекопитающих различен. Последние шаги N-гликолизации в клетке млекопитающих присоединяют β1,4 галактозу, α1,6 фукозу (бета-1,4 галактозу, альфа1,6 фукозу) и конечные остатки сиаловой кислоты к сложным гликанам. Однако в растениях добавляются остатки β1,3 галактозы, α1,3 фукозы (бета-1,3 галактозы, альфа1,3 фукоза), α1,4 фукозы и β1,2 ксилозы (альфа1,4 фукоза и бета1,2 ксилоза). Альфа1,3 фукоза и бета1,2 ксилоза, являются компонентами глико-эпитопов ряда растительных аллергенов. Эти остатки считаются потенциально иммуногенными (аллергенными), и их появление в лечебных белках, включая антитела, считается нежелательным.
Присоединение последовательности KDEL к С-концу пептида обычно используется для обеспечения извлечения пептида из клетки Гольджи с его возвращением в ЭР (эндоплазматический ретикулом). Такой подход был применен для получения нефукозилированного и нексилозилированного антитела при использовании агроинфильтрации листьев табака (Sriraman с соавт., 2004). Однако присоединенный KDEL-пептид является потенциальным аллергеном, поэтому данный подход имеет ограниченное применение в продуцировании лечебных белков.
Контроль присоединения α1,3 фукозы (альфа1,3 фукозы) и β1,2 ксилозы (бета1,2 ксилозы) был также достигнут путем модифицирования экспрессии фукозилтрансферазы и ксилозилтрансферазы. Мутанты, неспособные присоединять α1,3 фукозу и β1,2 ксилозу к сложным гликанам, были получены из мха (Physcomitrella patens; Koprivova с соавт., 2004) и Arabidopsis thaUana (Strasser с соавт., 2004). Частичное ингибирование экспрессии фукозилтрансферазы и ксилозилтрансферазы растения было также достигнуто путем экспрессии РНК-ингибирования (РНК/нацеленное на гены α1,3 фукозилтрансферазы и β1,2 ксилозилтрансферазы в Lemna minor Кокс с соавт., 2006 г.). Однако полное ингибирование этой ферментативной активности оказывает вредное воздействие на некоторые виды растений, поскольку они мешают нормальному течению ключевых, связанных с развитием событий, например формирование пыльцы или завязывание семян. Вызванная РНК-ингибированием специфичная деградация иРНК (информационной РНК) не может оставаться стабильной длительное время, и она не может быть применена к широкому спектру базирующихся на растениях платформ, используемых для получения лечебных препаратов, поскольку, как сообщалось в отчетах, она чувствительна к воздействию факторов окружающей среды.
Патент WO 03/078637 содержит описание применения галактозилтрансферазы человека для ускорения присоединения конечной β1,4 галактозы (GalT) к гликанам растения. Экспрессия галактозы и направление ее действия на цис Гольджи путем использования синтеза с трансмембранным доменом ксилозилтрансферазы привела к присоединению конечной галактозы и уменьшению специфических остатков в растении, несущем N-гликаны (см. также Bakker с соавт., 2006). Разведение таких растений, содержащих рекомбинантный ИГГ, привело к значительному, но переменному снижению гликанов, включающих в себя фукозу и ксилозу.
Прикрепление остатка бета-1,4-связанного N-ацетилглюкозамина (GlnANc) к бета-связанной маннозе для получения деленной пополам GlcNac ускоряется N-ацетилглюкозаминилтрансферазой III (GnT-III; EC 2.4..1.144). Введение данного энзима было описано Rouwendal с соавт. в 2007 г., а растения, экспрессирующие белки, содержали GnT-III со сложными N-гликанами, были поделены пополам и несли два остатка GlnAc.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение имеет отношение к способам модифицирования продуцирования гликопротеина в растениях. Настоящее изобретение также предлагает растения с модифицированным продуцированием гликопротеина.
Целью настоящего изобретения является предложение усовершенствованного способа модифицирования образования гликопротеина в растениях.
Предлагается нуклеиновая кислота, имеющая нуклеотидную последовательность (А), содержащую нуклеотиды 1-1077 последовательности SEQ ID NO. 17 (GNT1-GalT; фиг.5d) или содержащую нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-1077 последовательности SEQ ID NO. 17, что подтверждается путем использования следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11, где нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка.
Также предлагается нуклеиновая кислота, имеющая нуклеотидную последовательность (В), содержащую первую последовательность нуклеиновой кислоты, имеющей нуклеотиды 5-1198 последовательности SEQ ID NO. 14 (GalT), или содержащую нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 5-1198 последовательности SEQ ID NO. 14, что подтверждается путем использования следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11, где первая последовательность нуклеиновой кислоты кодирует белок, который модифицирует гликозилирование целевого белка, а первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты, содержащей 35S, или пластоцианин, промотер.
Настоящее изобретение описывает нуклеиновую кислоту, имеющую нуклеотидную последовательность, содержащую нуклеотиды 1-1641 последовательности SEQ ID NO. 26 (GNT1-GnT-III) или содержащую нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-1641 последовательности SEQ ID NO. 26, что подтверждается путем использования следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11, где нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка.
Также приводится описание нуклеиновой кислоты, имеющей нуклеотидную последовательность, содержащую первую последовательность нуклеиновой кислоты, имеющей нуклеотиды 1-1460 последовательности SEQ ID NO. 16 (GnT-III) или содержащую нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-1460 последовательности SEQ ID NO. 16, что подтверждается путем использования следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11, где первая последовательность нуклеиновой кислоты кодирует белок, который модифицирует гликозилирование целевого белка, а первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты, содержащей 35S, или промотер пластоцианина.
Кроме того, предлагается растение, растительная клетка и семя, содержащие нуклеотидные последовательности (А), (В), (С) или (D), рассмотренные выше.
Настоящее изобретение также имеет отношение к составному (гибридному) белку GNT1-GalT, содержащему CTS домен N-ацетилглюкозаминилтрансферазы, слитый с каталитическим доменом бета 1,4 галактозилтрансферазы, а также содержащий последовательность SEQ ID NO. 18. Аминокислотная последовательность последовательности SEQ ID NO. 18 может быть закодирована нуклеотидной последовательностью SEQ ID NO. 17.
Также предлагается растение, растительная клетка или семя, содержащее только что упомянутый составной белок. Кроме того, предлагается растение, растительная клетка или семя, содержащее нуклеиновую кислоту, имеющую последовательность SEQ ID NO. 17.
Настоящее изобретение включает в себя составной (гибридный) белок GNT1- GnT-III, содержащий CTS домен N-ацетилглюкозаминилтрансферазы, слитый с каталитическим доменом N-ацетилглюкозаминилтрансферазы III, а также содержащий аминокислотную последовательность SEQ ID NO. 20, Аминокислотная последовательность последовательности SEQ ID NO. 21 может быть закодирована нуклеотидной последовательностью SEQ ID NO. 26.
Также предлагается растение, растительная клетка или семя, содержащее только что упомянутый составной белок. Кроме того, предлагается растение, растительная клетка или семя, содержащее нуклеиновую кислоту, имеющую нуклеотидную последовательность SEQ ID NO. 26.
В соответствии с настоящим изобретением предлагается способ (1) синтезирования целевого белка, содержащего экспрессию в пределах растения или части растения, нуклеотидную последовательность, кодирующую первую нуклеотидную последовательность, кодирующую составной белок GNT1-GalT, содержащий CTS домен N-ацетилглюкозаминилтрансферазы (GNT1), слитый с каталитическим доменом бета 1,4 галактозилтрансферазы (GalT), первую нуклеотидную последовательность, функционально связанную с первой регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка. Вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, и экспрессию первой и второй нуклеотидных последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным N-гликозилированием.
Как изложено выше, первая нуклеотидная последовательность и вторая нуклеотидная последовательность могут быть экспрессированы в растении неустойчиво, или они могут быть экспрессированы стабильно. Далее, первая регуляторная область может быть первым тканеспецифичным промотором, а вторая регуляторная область является вторым тканеспецифичным промотором. Как первый, так и второй промоторы могут быть промоторами пластоцианина.
В настоящем изобретении также предлагается способ (2) синтезирования целевого белка. Данный способ аналогичен по описанию способу 1, при этом целевой белок может быть антителом. Если целевой белок является антителом, то вторая нуклеотидная последовательность, кодирующая целевой белок, содержит нуклеотидную последовательность 2А, функционально связанную с регуляторной областью 2А, которая является активной в пределах растения, а также вторая нуклеотидная последовательность 2В, функционально связанная с регуляторной областью 2В, которая является активной в растении, а также продукт, кодируемый каждой из последовательностей 2А и 2В, объединяются для получения белка. Регуляторная область 2А может быть промотором пластоцианина, а регуляторная область 2В может быть также промотором пластоцианина.
В настоящем изобретении также предлагается рассмотренный выше способ (1) или способ (2), где третья нуклеотидная последовательность экспрессируется в растении. Третья нуклеотидная последовательность, кодирующая суппрессора сайленсинга (подавителя механизма «выключения» генов), функционально связана с третьей регуляторной областью, являющейся активной в растении. Третьей нуклеотидной последовательностью, кодирующей суппрессора сайленсинга, может быть, например, HcPro, TEV-p1/HC-Pro? BYV-p21, TBSV-p19, TCV-CP, CMV-2b, PVX-p25, PVM-p11, PVS-p11, BScV-p16, CTV-p23, GLRaV-2 p24, GBV-p14, HLV-p10, GCLV-p16 или GVA-p10. Третий тканевый промотер может быть промотором пластоцианина.
В настоящем изобретении предлагается система экспрессии растения для сушки экспрессии целевого белка в растении, где целевой белок содержит модифицированный паттерн гликозилирования. Например, целевой белок содержит редуцированные фукозилированные, ксилозилированные или одновременно фукозилированные и ксилозилированные N-гликаны. В качестве варианта, целевой белок может содержать модифицированный паттерн гликозилирования, при котором в протеине отсутствуют фукозилированные, ксилозилированные или одновременно фукозилированные и ксилозилированные остатки, а сам белок демонстрирует увеличенное галатолизирование. Кроме того, может произойти присоединение терминальной галактозы, что приведет к снижению или исчезновению фукозилирования и ксилозилирования целевого белка при сравнении с таким же целевым белком, полученным в диком растении.
В настоящем изобретении предлагается способ (3) синтезирования целевого белка с модифицированным профилем N-гликозилирования, содержащим коэкспрессирующую в пределах растения, части растения или растительной клетке нуклеотидной последовательности, кодирующей первую нуклеотидную последовательность, кодирующую составной белок, GNT1-GnT-III, содержащую CTS домен N-ацетилглюкозаминилтрансферазы (GNT1), слитый с каталитическим доменом N-ацетилглюкозаминилтрансферазы III (GnT-III), первую нуклеотидную последовательность, функционально связанную с первой регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка. Вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, и коэкспрессию первой и второй нуклеотидных последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным профилем N-гликозилирования.
Первая нуклеотидная последовательность и вторая нуклеотидная последовательность, рассмотренные выше (способ 3), могут находиться в растении временно или они могут быть экспрессированы стабильно. Более того, первая регуляторная область является, возможно, первым тканеспецифичным промотором, а вторая регуляторная область является вторым тканеспецифичным промотором. Любой из первого и второго тканеспецифичных промоторов может быть промотором пластоцианина.
Также представлен способ (4) синтезирования целевого белка с модифицированным профилем N-гликозилирования, содержащий коэкспрессирующую в пределах растения, части растения или растительной клетке нуклеотидную последовательность, кодирующую первую нуклеотидную последовательность, кодирующую составной белок, GNTI-GalT, содержащий CTS домен N-ацетилглюкозаминилтрансферазы (GNT1), слитый с каталитическим доменом бета 1,4 галактозилтрансферазы (GalT), первую нуклеотидную последовательность, функционально связанную с первой регуляторной областью, являющейся активной в растении, вторую нуклеотидную последовательность, кодирующую бета 1,4 галактозилтрансферазы, вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, третью нуклеотидную последовательность, кодирующую целевой белок, третья нуклеотидная последовательность функционально связана с третьей регуляторной областью, являющейся активной в растении, и коэкспрессию первой, второй и третьей последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным профилем N-гликозилирования.
Первая нуклеотидная последовательность и вторая нуклеотидная последовательность, рассмотренные выше (4), могут находиться в растении временно или они могут быть экспрессированы стабильно. Более того, первая регуляторная область может быть первым тканеспецифичным промотором, а вторая регуляторная область является вторым тканеспецифичным промотором. Любой из первого и второго тканевых промоторов может быть промотором пластоцианина.
В настоящем изобретении предлагается способ (5) синтезирования целевого белка с модифицированным профилем N-гликозилирования, содержащий коэкспрессирующую в пределах растения, части растения или растительной клетке нуклеотидной последовательности, кодирующей первую нуклеотидную последовательность, кодирующую составной белок, GNTI-GnT-III, содержащий CTS домен N-ацетилглюкозаминилтрансферазы (GNT1), слитый с каталитическим доменом N-ацетилглюкозаминилтрансферазы III (GnT-III), указанная первая нуклеотидная последовательность, функционально связана с первой регуляторной областью, являющейся активной в растении; вторую нуклеотидную последовательность N-ацетил глюкозаминил трансферазы III, указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении; и третью нуклеотидную последовательность, кодирующую целевой белок, указанная третья нуклеотидная последовательность функционально связана с третьей регуляторной областью, являющейся активной в растении; а также коэкспрессию первой, второй и третьей последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным профилем N-гликозилирования.
Первая нуклеотидная последовательность, вторая нуклеотидная последовательность и третья нуклеотидная последовательность, рассмотренные выше (5), могут находиться в растении временно или они могут быть экспрессированы стабильно. Более того, первая, вторая и третья регуляторные области являются, возможными тканевыми промоторами. Например, любой из тканевых промоторов может быть промотором пластоцианина.
[0030] В соответствии с рассмотренными в описании способами белок может быть получен таким образом в больших количествах. В нем отсутствуют гликаны, которые, как известно, участвуют в реакциях гиперчувствительности или, другими словами, в аллергических реакциях. Это достигается коэкспрессией гликоинженерных энзимов вместе с целевым белком, в результате получается белок, который является менее иммуногенным, чем белок, полученный в диком растении.
Как рассматривается в настоящем описании, возможно использование упрощенных систем экспрессии для получения целевого белка, применяющих систему транзиентной экспрессии. Однако указанные способы могут использоваться с применением стабильных систем преобразования. По этой причине настоящее изобретение не ограничено использованием только систем транзиентной экспрессии.
Используя транзиентную коэкспрессию, рассматриваемая в настоящем описании система избегает длительных периодов продуцирования, а также процесса отбора элитных мутантов и гликоинженерных трансгенных линий и их последующего использования в качестве родительских клеточных линий (например, как это описано Bakker с соавт., 2005). Система также позволяет предотвратить побочные проблемы, зачастую связанные с мутантами и гликоинженерными растениями относительно продуктивности, пыльцевой продуктивности, завязывания семян (Bakker с соавт., 2005), а также относительно жизнеспособности (Boisson с соавт., 2005). Как поясняется в настоящем описании, коэкспрессия целевого белка с модифицированной химерной человеческой галактозилтрансферазой не влияла на кинетику производства и количества получаемого продукта
Система транзиентной экспрессии, рассматриваемая в настоящем описании, обеспечивает уровни экспрессии, достигающие 1,5 г высококачественного антитела на килограмм массы сырой ткани листьев, что превышает известный по отчетам уровень аккумулирования любого антитела в растениях при помощи других систем экспрессии, включая системы, базирующиеся на многих вирусах и трансгенных растениях.
Изложенная в настоящем описании методика, например, включающая в себя экспрессию Galt или Galt-GNT1, может быть также применена к устойчиво трансформированным растениям. Наряду с демонстрацией многих преимуществ настоящее изобретение не ограничивается только системами транзиентной экспрессии,
Данное краткое изложение сущности изобретения не излагает в обязательном порядке все отличительные признаки настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Указанные и прочие признаки настоящего изобретения станут более очевидными из последующего описания, в котором приведены ссылки на прилагаемые чертежи.
На фиг.1А показан базирующийся на пластоцианине кластер, собранный для экспрессии С5-1. R610 содержит нуклеотидную последовательность, кодирующую С5-1 LC, С5-1 HC-KDTL; R612 содержит нуклеотидную последовательность, кодирующую С5-1 LC и С5-1 НС, где С5-1 LC: последовательность кодирования легкой цепи С5-1; С5-1 НС: последовательность кодирования тяжелой цепи С5-1. На фиг.1В показана нуклеотидная последовательность для промотора пластоцианина и 5'-НТО (нетранслируемой области) (SEQ ID NO:23), сайт инициирования транскрипции показан полужирным шрифтом, а кодон инициирования трансляции подчеркнут. На фиг.1C показана нуклеотидная последовательность для пластоцианина 3'-НТО и терминатора (SEQ ID NO:24), терминатор подчеркнут.
На фиг.2 показано накопление антитела С5-1 в листьях Nicotiana benthamiana, пропитанных R610 и R612 (полигенные экспрессирующие кластеры, базирующиеся на пластоцианине) с и без коэкспрессии суппрессора сайленсинга HcPro. Представленные величины соответствуют среднему уровню аккумулирования и стандартному отклонению, полученным в результате 6 измерений на трех растениях (с инфильтрацией при помощи шприца) или 6 измерений на отдельных партиях приблизительно 12 инфильтрованных растений (250 г).
На фиг.3 показан блот-анализ белка накопления С5-1 антитела в экстрактах, инфильтрованных при помощи шприца растений и растений с вакуумной инфильтрацией. На фиг.3А показан иммуноблотинг конъюгированных с пероксидазой антител козы против иммуноглобулинов мыши (IgG (H+L)) на экстрактах из растений, инфильтрованных с применением R612 (для секреции, дорожки 1) или R610 (для удержания ЭР (эндоплазматического ретикулома), дорожки 2). C1: 100 нг коммерческого иммуноглобулина мыши IgG1 (Sigma M9269), загруженного для контроля электрофоретической подвижности; С2: 12 мкг общих белков, извлеченных из биомассы, инфильтрованной мыльнянкой лекарственной (пустой вектор). С3: 100 нг коммерческого иммуноглобулина мыши IgG1 (Sigma M9269), добавленного в 12 мкг общих белков, извлеченных из биомассы, инфильтрованной мыльнянкой лекарственной (пустой вектор). На фиг.3В показан иммуноблотинг активности с применением конъюгированных с пероксидазой иммуноглобулинов человека IgG1 на экстрактах из растений, инфильтрованных с применением R612 (для секреции, дорожки 1) или R610 (для удержания ЭР (эндоплазматического ретикулома), дорожки 2). C1: 2 мкг контрольного антитела С5-1, рафинированного из гибридомы (Хауди с соавт., 1997 г.); С2: 75 мкг общего белка, извлеченного из биомассы, инфильтрованной мыльнянкой лекарственной (пустой вектор).
На фиг.4 показан анализ антител, рафинированных из растений, инфильтрованных с применением R612 (для секреции, дорожки 1) или R610 (для удержания ЭР, дорожки 2). На фиг.4А показан анализ методом электрофореза в полиакриламидном геле (SDS-PAGE) суммарных экстрактов и рафинированных белков, выполняемый в невосстановительных условиях. На фиг.4В показан анализ SDS-PAGE рафинированных антител, выполняемый в восстановительных условиях. На фиг.4С показан иммуноблотинг активности рафинированных антител, выполняемый с применением конъюгированных с пероксидазой ИгГ1 человека. На фиг.4D показано сравнение загрязнителей в 6 партиях рафинированных антител С5-1 из различных инфильтрованных культур. С: 2,5 мкг коммерческого иммуноглобулина мыши ИгГ1 (Sigma M9269), загруженного для контроля электрофоретической подвижности.
На фиг.5 представлены примеры полигенных кластеров, собранных для экспрессии нативной (R622) и гибридной (R621) версий галактозилтрансферазы. GNT1-CTS: CTS домен N-ацетилглюкозаминилтрансферазы I; GalT-Cat: каталитический домен человеческой β1,4 галактозилтрансферазы; GalT (R622): человеческая (31,4 галактозилтрансфераза. На фиг.5В показана нуклеотидная последовательность (SEQ ID NO: 14) для GalT (UDP-GakbetaGlcNac бета 1,4 галактозилтрансферазы полипептид 1, бета 1,4 галактозилтрансферазы I), сайт инициирования АТГ подчеркнут; трансмембранный домен подчеркнут и выделен курсивом; последовательность, выделенная полужирным шрифтом, соответствует каталитическому домену человеческой бета 1,4 галактозилтрансферазы (human beta 1,4GalT); FLAG-эпитоп выделен курсивом. На фиг.5С показана аминокислотная последовательность (SEQ ID NO: 15) для GalT (UDP-Gal:betaGlcNac бета 1,4 галактозилтрансферазы полипептид 1, бета 1,4 галактозилтрансферазы I). Трансмембранный домен подчеркнут и выделен курсивом; последовательность, выделенная полужирным шрифтом, соответствует каталитическому домену человеческой бета 1,4 галактозилтрансферазы; FLAG эпитоп выделен курсивом. На фиг.5D показана нуклеотидная последовательность (SEQ ID NO: 17) GNTIGalT, сайт инициирования АТГ подчеркнут; трансмембранный домен (CTS) подчеркнут и выделен курсивом; последовательность, выделенная полужирным шрифтом, соответствует каталитическому домену человеческой бета 1,4 галактозилтрансферазы (human beta 1,4GalT); FLAG эпитоп выделен курсивом. На фиг.5Е показана аминокислотная последовательность (SEQ ID NO: 18) GNTIGalT, трансмембранный домен (CTS) подчеркнут и выделен курсивом; последовательность, выделенная полужирным шрифтом, соответствует каталитическому домену человеческой бета 1,4 галактозилтрансферазы (human beta 1,4GalT); FLAG эпитоп выделен курсивом. На фиг.5F показана нуклеотидная последовательность домена CTS (внутриклеточный концевой элемент, трансмембранный домен, межзональная область) N-ацетилглюкозаминтрансферазы (GNT1; SEQ ID NO: 21). На фиг.5G аминокислота последовательности, нацеленной на капсиду (CTS) (SEQ ID NO: 22). На фиг.5Н показана последовательность нуклеиновой кислоты Gntl-Gnt III (SEQ ID NO: 26). На фиг.5I показана аминокислотная последовательность Gntl-Gnt III (SEQ ID NO: 20). На фиг.5J показана последовательность нуклеиновой кислоты Gnt III (SEQ ID NO: 16). На фиг.5K показана аминокислотная последовательность Gnt III (SEQ ID NO: 19).
На фиг.6 показан профиль экстрактов, полученных из экспрессирующих антитела С5-1 растений и либо окрашенных для выделения белка, либо для проведения иммуноблотинга. На верхней панели показан окрашенный по классу «Кумасси» полиакридамидный гель (ПААГ). Вторая сверху панель показывает определение аффинности агглютинина Erythrina cristagali (ECA), который связывает конкретно β1,4 галактозу. Третья сверху панель показывает иммуноблотинг с использованием антител против α1,3 фукозы. Нижняя панель показывает иммуноблотинг с использованием антител против β1,2 ксилозы. R612: С5-1 экспрессирует в одиночку; R612+R622: С5-1 коэкспрессирует (коинфильтрирует) с GalT; R612+R621: С5-1 коэкспрессирует с GNT1-GalT.
На фиг.7 показана MALDI-TOF масс-спектрометрия для определения N-гликозилирования типичного гликопептида EEQFNSTFR (SEQ ID NO: 13) С5-1 антитела, изолированного от растений, инфильтрованных Nicotina benthamiana при помощи шприца, с применением ряда моделей. N-гликозирование гликопептида было определено после сепарации на препаративном высокоэффективном жидкостном хроматографе (ВЭЖХ). Аналогичные результаты были получены после проведения вакуумной инфильтрации. На фиг.7А показана MALDI-TOF масс-спектрометрия типичного гликопептида вслед за экспрессией R612: (С5-1; см. фиг.1). На фиг.7В показана MALDI-TOF масс-спектрометрия типичного гликопептида вслед за экспрессией С5-1 (R612; см. фиг.1) совместно с естественным GalT (R622; см. фиг.5). На фиг.7С показана MALDI-TOF масс-спектрометрия типичного гликопептида вслед за экспрессией С5-1 (R612; см. фиг.1) вместе с GNTIGalT (R621, см. фиг.5). На фиг.7С - вкладыш, соответствующий увеличенному виду m/z 2650-2800 спектра, показано (стрелкой) отсутствие основного комплексного иона J, обнаруженного в растении R612. A: GlcNAcMan3GlcNac2; В: Man5GlcNac2; С: GalGlcNAcMan3GlcNAc2; D: GlcNAc2Man3GlcNac2; E: Man6GlcNac2;:F: GalGlcNAcMan3(Xyl)GlcNAc2; G: GlcNAcMan5GlcNac2; H: GlcNAc2Man5(Fuc)GlcNAc2; I: Man7GlcNac2; J: GlcNAc2Man3(Xyl)(Fuc)GlcNAc2; K: GalGlcNAcMan5GlcNAc2; L: Man8GlcNac2; M: Man9GlcNac2.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение имеет отношение к способам модифицирования продуцирования гликопротеинов в растениях. Настоящее изобретение также предлагает растения с модифицированным продуцированием гликопротеинов.
В настоящем изобретении содержится описание системы экспрессии в растениях для управления экспрессией целевого белка в растении. При использовании описанной системы экспрессии целевой белок, имеющий модифицированный паттерн гликозилирования, например, с редуцированным фукозилированием, ксилозилированием или одновременно фукозилированием и ксилозилированием, могут быть получены N-гликаны. В альтернативном варианте может быть получен целевой белок, имеющий модифицированный паттерн гликозилирования, где белок не имеет фукозилирования, ксилозилирования или того и другого одновременно, а также содержит повышенное галатолизирование. Кроме этого, как указывается в описании, модуляция посттрансляционных модификаций, например присоединение концевой галактозы, приводит к уменьшению фукозилирования и ксилозилирования экспрессированного белка, целевого. Например, целевой белок может содержать менее 10% продуктов фукозилирования и ксилозилирования (т.е. менее 10% остатков N-гликанов фукозилированы и ксилозилированы), или менее 5% продуктов фукозилирования и ксилозилирования (т.е. менее 5% остатков N-гликанов фукозилированы и ксилозилированы), или менее 1% продуктов фукозилирования и ксилозилирования (т.е. менее 1% остатков N-гликанов фукозилированы и ксилозилированы) от примерно 0,1 до примерно 2% остатков N-гликанов фукозилированы и ксилозилированы, от примерно 0,5 до примерно 1,5% остатков N-гликанов фукозилированы и ксилозилированы, или от примерно 0,7 до примерно 1% остатков N-гликанов фукозилированы и ксилозилированы, при сравнении с аналогичным целевым белком, полученным в диком растении. Таким образом, целевой белок может быть произведен в больших количествах и не содержать гликаны, которые могут вызвать реакции повышенной чувствительности или могут каким-либо образом участвовать в аллергических реакциях.
[0046] Неограничительный пример целевого белка, подлежащего экспрессированию, включает сложный белок, например антитело. Экспрессия такого сложного белка внутри агроинфильтрованного растения, например Nicotina benthamiana, достигала уровня продуцирования белка в 1,5 г/кг массы сырой ткани (около 25% TSP (transferred solid phase = перенесенная фаза с иммобилизованными антителами). Были достигнуты уровни в 558 и 757 мг/кг/массы сырой ткани для форм целевого белка, секретированных и с удержанием ЭР, соответственно. В предложенном неограничительном примере указанный уровень экспрессии был достигнут для антитела, этот уровень в три раза выше, чем уровень, достигнутый для антитела, полученного с применением многовирусной системы транзиентной экспрессии (Girth с соавт., 2006).
[0047] Влияние разницы между растением и типичным животным N-гликозилированием было основной проблемой, вызвавшей решение использовать растения для производства лекарственных средств. Образование гликанов в растениях может вызвать сокращение наполовину жизнедеятельности выращенного в растении белка в кровотоке, или указанные гликаны могут спровоцировать у пациентов аллергические реакции.
Присутствие основных α1,3 фукозы и β1,2 ксилозы в гликопротеинах, полученных из растений, был воспринят промышленностью как нормативный вызов, так как они были также обнаружены в некоторых растительных аллергенах. В дополнение к этому, в настоящее время документально подтверждено, что удаление коровой фукозы, даже α1,6 фукозы, которая может быть обнаружена в иммуноглобулинах из клеток СНО, увеличит активность антителозависимой клеточнозависимой цитотоксичности (ADCC). Признаком рассмотренной в описании системы является возможность выполнения модуляции посттрансляционных модификаций, например устойчивое присоединение терминальной галактозы и уменьшение фукозилирования и ксилозилирования (при сравнении с аналогичным белком, полученным в диком растении). В альтернативном варианте уровень фукозилирования может быть понижен при одновременном увеличении объема галактозилирования (опять же при сравнении с аналогичным белком, полученным в диком растении).
Изменение объема фукозилирования, ксилозилирования или галактозилирования может быть определено путем применения любого подходящего способа, например использования антител против α1,3 фукозы для обнаружения наличия или отсутствия иммуносигналов о фукозе (фукозилирования), антител против β1,2 ксилозы для обнаружения ксилозилирования, или наличия, или отсутствия иммуносигналов о ксилозе, например, как показано на фиг.6. В альтернативном варианте может быть применена MALDI-TOF масс-спектрометрия для определения N-гликозилирования профиля белка или части белка, как показано на фиг.7. Может быть также использован другой известный специалисту в данной области знаний способ определения N-гликозилирования профиля белка или части белка.
Как подробно рассмотрено ниже, была использована система агроинфильтрации, базирующаяся на вакуумировании, которая была признана подходящей для получения целевого белка, например антитела с точки зрения количеств, качества и воспроизводимости. Переход к масштабируемой технологии инфильтрации позволяет получать ежедневно граммы указанного антитела внутри небольшой экспериментальной установки, что дает возможность использовать такую систему транзиентной экспрессии с целью получения материалов для клинических исследований в пределах чрезвычайно короткого временного графика и для поставки лицензированной продукции на рынок в количестве, достигающем несколько килограммов в год. Высококачественные антитела были получены из подвергнутых инфильтрации листьев после единственной операции аффинной хроматографии. Однако следует понимать, что рассмотренный в описании способ может быть также применен к стабильно трансформированным растениям.
Посттранскрипционный сайленсинг генов (ПТСГ) может быть применен для ограничения экспрессии трансгенов в растениях, а также коэкспрессии суппрессора сайленсинга, например, но, не ограничиваясь этим, HcPro из вируса картофеля Y может быть использован для противодействия специфичному разрушению трансгена иРНК (Brigneti с соавт., 1998). Альтернативные суппрессоры известны из существующего уровня техники и могут быть использованы так, как изложено в настоящем описании (Chiba с соавт., 2006, Virology 346; 7-14; включен в описание в виде ссылки), например, но, не ограничиваясь этим, вирус гравировки табака TEV-p1/HC-Pro (Tobacco etch virus-p1/HC-Pro), BYV-p21, p19 вируса кустистой карликовости томата (TBSV р19), капсида протеина вируса курчавости томата (TCV-CP), вирус мозаики огурца 2b (CMV-2b), p25 вируса картофеля Х (PVX-p25), p11 вируса картофеля М (PVM-p11), p11 вируса картофеля S (PVS-p11), р16 вируса ожога черники (BScV-p16), p23 вируса тристеца цитрусовых (CTV-p23), p24 вируса скручивания листьев винограда-2 (Grapevine leafroll-associated virus-2) (GLRaV-2 p24), p10 вируса винограда A (GVA-p10), p14 вируса винограда В (GVB-p14), p10 латентного вируса борщевика (Heracleum latent vims) (HLV-p10), or р16 общего латентного вируса чеснока (Garlic common latent virus) (GCLV-pl6). Таким образом, суппрессор сайленсинга, например HcPro, TEV-p1/HC-Pro, BYV-p21, TBSV-p19, TCV-CP, CMV-2b, PVX-p25, PVM-p11, PVS-p11, BScV-p16, CTV-p23, GLRaV-2 p24, GBV-p14, HLV-p10, GCLV-p16 или GVA-p10, может быть коэкспрессирован либо с GalT. GNT1-GalT, GnT-III, GNT1-GnT-III, либо в указанной выше комбинации, чтобы дополнительно обеспечить высокие уровни получения белка в растениях.
Окрашивание по классу «Кумасси» очищенных продуктов, полученных путем использования транзиентной экспрессии, указывает наличие различных малораспространенных посторонних веществ. Эти фрагменты, очевидно, имеют отношение к самому продукту, а все посторонние вещества массой более 70 кДа, содержали, как минимум, один антисвязывающий агент (Fab-фрагмент), как показано блотом активности (фиг.3В). Природа и количество относящихся к продукту посторонних веществ, присутствующих в экстрактах растения, аналогичны тем, что наблюдались в системах продуцирования клеток млекопитающих. Поэтому процедура очистки, обычно используемая для обработки лечебных антител, (например, анионный обмен, аффинность, катионный обмен,) легко обеспечивает требуемую распорядительными органами степень чистоты белка, используемого для лечебных нужд.
В настоящем изобретении предлагается способ синтезирования целевого белка в растениях, характеризующегося наличием модифицированного паттерна гликозилирования. Способ включает в себя коэкспрессию целевого белка с нуклеотидной последовательностью, кодирующей бета-1,4 галактозилтрансферазу (GalT; SEQ ID NO: 14), например, но, не ограничиваясь этим, GalT млекопитающего или GalT человека, однако, может также быть использована GalT, полученная от другого источника. Каталитический домен GalT (например, нуклеотиды 370-1194 последовательности SEQ ID NO: 14, выделена полужирным шрифтом на фиг.5b, или нуклеотиды 238-1062 последовательности SEQ ID NO: 17, выделена полужирным шрифтом на фиг.5d) может также быть слит с CTS доменом (то есть цитоплазматический концевой сегмент, трансмембранный домен, стволовая область) N-ацетилглюкозаминил трансферазы (GNT1: например, содержащая нуклеотиды 34-87 последовательности SEQ ID NO: 17; фиг.5d) и кодирующая аминокислотную последовательность, содержащую аминокислоты 12-29 последовательности SEQ ID NO: 18 (фиг.5е), для образования гибридного энзима GNT1-GalT, а гибридный энзим коэкспрессирует с целевым белком. Способ также включает в себя коэкспрессию целевого белка с нуклеотидной последовательностью, кодирующую N-ацетилглюкозаминилтрансферазу III (GnT-III; SEQ ID NO: 16; фиг.5j), например, но, не ограничиваясь этим, GnT-III млекопитающего или GnT-III человека, однако, может также быть использована GnT-III, полученная от другого источника. Кроме того, гибридный энзим GNT1-GnT-III (SEQ ID NO: 26); фиг.5d), содержащий цитоплазматический концевой сегмент GNT1, слитый с GnT-III, может также быть использован, а его описание приводится ниже.
Альтернативные способы прикрепления нуклеотидной последовательности, кодирующей галактозилтрансферазу mGalT или hGalT, или GalT от других источников, включают в себя присоединение GalT к последовательностям HDEL, KDEL (обе являются последовательностями удержания эндоплазматического ретикулома), цитоплазматический концевой сегмент (CTS) белка, участвующего в биосинтезе N-гликопротеина, например, но, не ограничиваясь этим, CTS глюкозидазы I, ксилозилтрансферазы CTS глюкозидазы II, CTS маннозидазы I, CTS бета-1,2 ксилозилтрансферазы, CTS альфа-1,2 фукозилтрансферазы. Каталитический домен GalT может также быть присоединен к последовательностям HDEL, KDEL (обе являются последовательностями удержания эндоплазматического ретикулома) цитоплазматических концевых сегментов, т.е. CTS глюкозидазы I, CTS глюкозидазы II, CTS маннозидазы I, CTS маннозидазы II, CTS бета-1,2 ксилозилтрансферазы, CTS альфа-1,2 фукозилтрансферазы.
Использование гибридного энзима, содержащего либо последовательность GNT1-GalT, либо последовательность GNT1-GnT-III, помещает каталитический домен GalT или GnT-III в аппарат цис-Гольджи, где возникают ранние стадии сложного процесса созревания N-гликанов. Проверка теории практикой показала, что блокирование активности GalT на ранней стадии созревания гликанов может привести к присоединению β1,4 галактозы к созревающим гликанам, а также к эффективному ингибированию фукозилирования и ксилозилирования белка, которое в ином случае могло бы произойти в растении. Аналогичным образом, блокирование активности GnT-III на ранней стадии созревания гликанов может привести к присоединению остатков GlcNAc к бета-версии маннозы для образования делящегося GlnAc, а также привести к эффективному ингибированию фукозилирования и ксилозилирования белка, которое в ином случае могло бы произойти в растении. Например, целевой белок может быть коэкспрессирован с гибридным энзимом, содержащим CTS домен, слитым с каталитическим доменом GalT, например GNT1-GalT (R621; фиг.5а, 5d) или GNT1-GnT-III (SEQ ID NO: 26; фиг.5h). Если целевой белок имеет пониженные уровни фукозилирования, в то время как требуются ксилозилированные и галактозилированные белки, то вместе с целевым белком может быть экспрессирована немодифицированная (нативная) GalT. Если требуется целевой белок, имеющий модифицированное гликозилирование, содержащий делящиеся остатки GlnAc, то вместе с целевым белком может быть экспрессирована немодифицированная (нативная) GnT-III. Для специалиста в данной области знаний должно быть очевидным, что оптимизированная последовательность нуклеиновой кислоты растения может быть использована для получения немодифицированного или нативного энзима GalT или GnT-III.
Таким образом, предлагается нуклеотидная последовательность, содержащая нуклеотиды 1-10662 последовательности SEQ ED NO: 17 (GNT1-GalT) или содержащая нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-102 последовательности SEQ ID NO: 17, где нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка. Указанная последовательность может быть оптимизирована на растении. Также предлагается нуклеотидная последовательность, которая содержит последовательность нуклеиновой кислоты, имеющую нуклеотиды 1-1224 последовательности SEQ ID NO: 14 (GalT), или содержащая нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-1224 последовательности SEQ ID NO: 14, где нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка. Указанная последовательность может быть оптимизирована на растении. Идентичность последовательностей определяется при использовании следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11.
Также в описании представлена аминокислотная последовательность, показанная в последовательности SEQ ID NO: 18 (GNT1-GalT; фиг.5е) или SEQ ID NO: 15 (GalT; фиг.5 с).
Предлагается нуклеиновая кислота, имеющая нуклеотидную последовательность, содержащую нуклеотиды 1 1641 последовательности SEQ ID NO: 26; (GNT1-GnT-III), или содержащая нуклеотидную последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 1-1641 последовательности SEQ ID NO: 26, где нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка. Указанная последовательность может быть оптимизирована на растении. Также представлена нуклеотидная последовательность, которая содержит последовательность нуклеиновой кислоты, имеющую нуклеотиды 232-1641 последовательности SEQ ID NO: 26 (GnT-III; или нуклеотиды 1-1460 последовательности SEQ ID NO: 16), или содержащая последовательность, демонстрирующую от 80 до 100% идентичность с нуклеотидами 232-1641 последовательности SEQ ID NO: 26 (или нуклеотидами 1-1460 последовательности SEQ ID NO: 16), где последовательность нуклеиновой кислоты кодирует белок, который модифицирует гликозилирование целевого белка. Указанная последовательность может быть оптимизирована на растении. Идентичность последовательностей определяется при использовании следующих параметров: Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11, указанная, нуклеотидная последовательность кодирует белок, который модифицирует гликозилирование целевого белка.
Также в описании представлена аминокислотная последовательность, показанная в последовательности SEQ ID NO: 20 (GNT1-GnT-III; фиг.5i) или SEQ ID NO: 19 (GnT-III; фиг.5k).
Термин «модифицированное гликозилирование» белка означает, что профиль N-гликана целевого белка, содержащего модифицированное гликозилирование (например, как пояснено выше), отличается от профиля N-гликана целевого белка, полученного из дикого растения. Модификация гликозирования может включать уменьшение или увеличение целевого белка в одном и более чем в одном гликане, или деление GlnAc пополам. Например, целевой белок может показать пониженное ксилозилирование, пониженное фукозилирование, или одновременно пониженное ксилозилирование и пониженное фукозилирование. В альтернативном варианте профиль N-гликана целевого белка может быть модифицирован таким образом, что объем гликозилирования увеличивается, а в ряде случаев, объем ксилозирования, фукозилирования, или того и другого одновременно, может уменьшаться. Кроме того, может продуцироваться деленный пополам GlnAc, что может привести к уменьшению объема фукозилирования и ксилозилирования белка.
Термины «пониженное ксилозилирование» и «пониженное фукозилирование» целевого белка означают, что объем ксилозилирования, фукозилирования, или ксилозилирования и фукозилирования одновременно, и N-гликанов, обнаруживаемых на представляющем интерес белке, на 10% меньше, чем объем ксилозилирования, фукозилирования, или ксилозилирования и фукозилирования одновременно, которые обнаруживаются на представляющем интерес белке, продуцированном в диком растении, где изолирован целевой белок и где определено ксилозирование или фукозилирование при использовании аналогичного способа. Например, целевой белок может содержать менее 5% остатков N-гликана, подвергшихся фукозилированию, ксилозилированию или тому и другому одновременно, менее 1% остатков N-гликана, обнаруживаемых на представляющем интерес белке, могут быть подвергнуты фукозилированию, ксилозилированию или тому и другому одновременно, от примерно 0,1 до примерно 2% остатков N-гликана, обнаруживаемых на представляющем интерес белке, могут быть подвергнуты фукозилированию, ксилозилированию или тому и другому одновременно, от примерно 0,5 до примерно 1,5% остатков N-гликана фукозилированы и ксилозилированы, или от примерно 0,7 до примерно 1,0% остатков N-гликана фукозилированы и ксилозилированы, при сравнении с целевым белком, полученным в диком растении.
Как показано на фиг.6 и 7, при использовании изложенного в описании способа может быть произведен целевой белок, демонстрирующий модифицированный профиль гликозилирования. Например, был получен целевой белок с иммунологически необнаружимыми остатками фукозы и ксилозы, в то время как целевой белок коэкспрессирует с GNT1-GalT. MALDI-TOF анализ эпитопа целевого белка показывает, что может быть получен целевой белок с модифицированным паттерном гликозилирования в то время, когда целевой белок коэкспрессирует либо с GalT, либо с GNT1-GalT. (cм. фиг, 7А-С, вкладыш С). Например, на фиг.7А показан профиль гликозилирования эпитопа целевого белка, экспрессированного в диком растении. Целевой белок содержит несколько ксилозилированных и фукозилированных остатков (пики Н и J на, соответственно, фиг.7А). Данные остатки уменьшены или отсутствуют, когда целевой белок коэкспрессируется с GalT (фиг.7В). Более того, наблюдаются новые ксилозилированные остатки (пик F), а также увеличение остатков гликозилирования в представляющем интерес белке при коэкспрессии с GalT (cм. пики С, F, K, фиг.7В). Коэкспрессия целевого белка с GNT1-GalT ведет к образованию профиля N-гликана, характеризуемого наличием менее 1% ксилозилированных и фукозилированных остатков (см. фиг.7С, вкладыш), а также увеличением остатков гликозилирования (пик K, фиг.7С).
Таким образом, в настоящем изобретении предлагается способ (способ А) синтезирования целевого белка с модифицированным N-гликозилирования, предоставляющий растение, содержащее нуклеотидную последовательность, кодирующую первую нуклеотидную последовательность, кодирующую бета-1,4 галактозилтрансферазу человека, указанная первая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой и второй нуклеотидных последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозилирование. Коэкспрессия первой последовательности, кодирующей GalT, наряду со второй последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым снижая фукозилирование, ксилозилирование гликанов целевого белка или то и другое одновременно. Более того, с использованием данного способа степень галактозилирования целевого белка может быть повышена по сравнению с объемом галактозилирования целевого белка, полученного из дикого растения, которое не экспрессирует GalT.
Также предлагается способ (способ В) синтезирования целевого белка с модифицированным N-гликозилирования, который включает в себя экспрессию в транзиентном виде в пределах растения или части растения, нуклеотидной последовательности, кодирующей первую нуклеотидную последовательность, кодирующую бета 1,4 галактозилтрансферазу человека (GalT; SEQ ID NO: 14; фиг.5b), указанная первая нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, и экспрессию первой и второй нуклеотидных последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным N-гликозилированием. Коэкспрессия первой последовательности, кодирующей GalT, наряду со второй последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым снижая фукозилирование. ксилозилирование гликанов целевого белка или то и другое одновременно. Более того, степень галактозилирования целевого белка может быть повышена по сравнению с объемом галактозилирования целевого белка, полученного из дикого растения, которое не экспрессирует GalT. Шаг экспрессии может также включать в себя транзиентную коэкспрессию первой и второй нуклеотидных последовательностей или стабильную коэкспрессию первой и второй нуклеотидных последовательностей.
В настоящем изобретении предлагается альтернативный способ (способ С) синтезирования целевого белка с модифицированным N-гликозилирования, предоставляющий растение, содержащее нуклеотидную последовательность, кодирующую первую гибридную нуклеотидную последовательность, кодирующую первый составной белок, содержащий CTS домен составной белок, содержащий CTS домен. N-ацетил глгокозаминил трансферазы (GNT1), слитый с каталитическим доменом GalT (бета 1,4 галактозилтрансфераза человека; GNT1-GalT; SEQ ID NO: 17; фиг.5d), указанная первая гибридная нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность, кодирующую целевой белок, указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой гибридной и второй нуклеотидной последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозилирование. Коэкспрессия первой гибридной последовательности, кодирующей GNT1-GalT, наряду со второй нуклеотидной последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым, снижая фукозилирование. ксилозилирование гликанов целевого белка. Например, степень фукозилирования, ксилозилирования или того и другого одновременно, может быть снижена от примерно 0,5 до примерно 5% или от примерно 0,5 до примерно 2% объема при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GNT1-GalT.
Предлагается дополнительный альтернативный способ (способ D) синтезирования целевого белка с модифицированным N-гликозилирования, который включает в себя экспрессию в транзиентном виде в пределах растения или части растения, нуклеотидной последовательности, кодирующей первую гибридную нуклеотидную последовательность, кодирующую GNT1-GalT, указанная первая гибридная нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, и экспрессию первой и второй нуклеотидных последовательностей на синтезирование целевого белка, содержащего гликаны с модифицированным N-гликозилированием. Коэкспрессия первой гибридной последовательности, кодирующей GNT1-GalT, наряду со второй последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым снижая фукозилирование и ксилозилирование гликанов целевого белка. Например, степень фукозилирования, ксилозилирования или того и другого одновременно может быть снижена от примерно 0,5 до примерно 5%, или от примерно 0,5 до примерно 2% объема при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GNT1-GalT. Шаг экспрессии может также включать в себя транзиентную коэкспрессию первой и второй нуклеотидных последовательностей или стабильную коэкспрессию первой и второй нуклеотидных последовательностей.
В настоящем изобретении предлагается дополнительный альтернативный способ (способ Е) синтезирования целевого белка с модифицированным N-гликозилирования, который включает в себя предоставление растения, содержащего нуклеотидную последовательность, кодирующую первую нуклеотидную последовательность, кодирующую бета 1,4 галактозилтрансферазу человека (GalT), указанная первая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, и третью нуклеотидную последовательность для кодирования суппрессора сайленсинга гена, например HcPro, указанная третья нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой, второй и третьей нуклеотидных последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозилирование. Коэкспрессия первой последовательности, кодирующей GalT, наряду со второй нуклеотидной последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым снижая фукозилирование и ксилозилирование гликанов целевого белка, при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GalT. Степень галактозилирования целевого белка может быть увеличена при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GalT. Экспрессия третьей последовательности, кодирующей суппрессор сайленсинга, обеспечивает высокий выход галактозилтрансферазы и целевого белка.
Кроме того, предлагается способ синтезирования целевого белка (способ Е) с модифицированным N-гликозилирования, который включает в себя экспрессию в транзиентном виде в пределах растения или части растения, нуклеотидной последовательности, кодирующей первую нуклеотидную последовательность, кодирующую бета 1,4 галактозилтрансферазу человека (GalT), указанная первая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, и третью нуклеотидную последовательность для кодирования суппрессора сайленсинга гена, например HcPro, указанная третья нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой, второй и третьей нуклеотидных последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозилирование. Коэкспрессия первой последовательности, кодирующей GalT, наряду со второй нуклеотидной последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4 галактозы к созревающим гликанам целевого белка, тем самым снижая фукозилирование и ксилозилирование гликанов целевого белка. Степень галактозилирования целевого белка может быть увеличена при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GalT. Экспрессия третьей последовательности, кодирующей суппрессор сайленсинга, обеспечивает высокий выход галактозилтрансферазы и целевого белка. Шаг экспрессии может включать в себя транзиентную коэкспрессию первой и второй нуклеотидных последовательностей или стабильную коэкспрессию первой и второй нуклеотидных последовательностей.
В этой связи в настоящем изобретении предлагается способ (способ Е) синтезирования целевого белка с модифицированным N-гликозилирования, который включает в себя предоставление растения, содержащего нуклеотидную последовательность, кодирующую первую нуклеотидную последовательность, кодирующую N-ацетилглюкозаминилтрансферазу III (GnT-III), указанная первая нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении; а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой гибридной и второй нуклеотидной последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозиллирование. Коэкспрессия первой последовательности, кодирующей GnT-III, наряду со второй нуклеотидной последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4-связанных остатков N-ацетилглюкозамина (GlnAc) к бета-связанной маннозе (делящегося на два GlnAc) на созревающих гликанах целевого белка, тем самым снижая фукозилирование, ксилозилирование гликанов целевого белка или то и другое одновременно по сравнению с целевым белком, продуцированным в диком растении, не экспрессирующем GnT-III. Последовательность, кодирующая: GnT-III (первая нуклеотидная последовательность), целевой белок (вторая нуклеотидная последовательность) или первая и вторая нуклеотидные последовательности вместе могут быть транзиентно экспрессированы. Если последовательности экпрессируются транзиентно, то может быть также использована третья нуклеотидная последовательность для кодирования суппрессора сайленсинга гена, например HcPro, функционально связанная с регуляторной областью, являющейся активной в растении, а первая, вторая и третья последовательности экспрессируются на продуцирование целевого белка, содержащего модифицированное гликозилирование.
В настоящем изобретении также предлагается альтернативный способ (способ Н) синтезирования целевого белка с модифицированным N-гликозилированием, который включает в себя предоставление растения, содержащего первую гибридную нуклеотидную последовательность, кодирующую первый составной белок, кодирующий CTS домен. N-ацетилглюкозаминилтрансферазы (GNT1), слитый с каталитическим доменом GnT-III (N-ацетилглюкозаминилтрансфераза; GNT1-GnT-III SEQ ID NO: 20), указанная первая гибридная нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении; а также вторую нуклеотидную последовательность для кодирования целевого белка, указанная вторая нуклеотидная последовательность функционально связана с регуляторной областью, являющейся активной в растении, выращивание растения, а также экспрессия первой гибридной и второй нуклеотидной последовательностей на синтезирование целевого белка, содержащего модифицированное N-гликозилирование. Коэкспрессия первой последовательности, кодирующей GNT1-GnT-III, наряду со второй нуклеотидной последовательностью, кодирующей представляющий интерес белок, приводит к присоединению бета-1,4-связанных остатков N-ацетилглюкозамина (GlnAc) к бета-связанной маннозе (делящегося на два GlnAc) на созревающих гликанах целевого белка, тем самым снижая фукозилирование и ксилозилирование гликанов целевого белка. Например, степень фукозилирования, ксилозилирования или того и другого одновременно может быть снижена от примерно 0,5 до примерно 5% или от примерно 0,5 до примерно 2% объема при сравнении с целевым белком, полученным из дикого растения, которое не экспрессирует GNT1-GnT-III. Последовательность, кодирующая: GNT1-GnT-III (первая нуклеотидная последовательность), целевой белок (вторая нуклеотидная последовательность) или первая и вторая нуклеотидные последовательности вместе могут быть транзиентно экспрессированы. Если последовательности экпрессируются транзиентно, то может быть также использована третья нуклеотидная последовательность для кодирования суппрессора сайленсинга гена, например, HcPro, функционально связанная с регуляторной областью, являющейся активной в растении, а первая, вторая и третья последовательности экспрессируются на продуцирование целевого белка, содержащего модифицированное гликозилирование.
Дополнительные модификации к нуклеотидной последовательности, кодирующей целевой белок, могут быть произведены для обеспечения высокого выхода продукта. Например, вторая последовательность, кодирующая целевой белок, может быть также слита с последовательностью, кодирующей последовательность, являющейся активной в удержании белка в пределах эндоплазматического ретикулома (ЭР), например, но, не ограничиваясь этим, последовательность KDEL (Lys-Asp-Glu-Leu) или другие последовательности ЭР-удержания, например HDEL или KKSS.
Кроме того, при продуцировании сложного целевого белка вторая нуклеотидная последовательность, используемая в любом из способов А - И, как рассматривалось выше, может кодировать более одного пептида или домена сложного белка. Например, в случае, когда белком является антитело, вторая нуклеотидная последовательность может содержать две нуклеотидные последовательности 2А и 2В, каждая из них кодирует часть антитела, например, нуклеотид 2А может кодировать легкую цепь, а последовательность 2В может кодировать тяжелую цепь антитела. Неограничительные примеры таких структур представлены на фиг.1, где структура каждой из R216 и R610 содержит две вторые нуклеотидные последовательности 2А, кодирующие легкую цепь антитела С5-1 (С5-1 LC), функционально связанную с регуляторной областью, являющейся активной в растении, например, но, не ограничиваясь этим, с промотором пластоцианина и последовательностью 2 В, кодирующей тяжелую цепь антитела С5-1 (С5-1 НС), функционально связанную с регуляторной областью, являющейся активной в растении, например, но, не ограничиваясь этим, с промотором пластоцианина, содержащего нуклеотиды 556-999 на фиг.1b или SEQ ID NO: 23; US7125978, включенный в настоящее описание путем ссылки). Как показано на фиг.1 и со ссылкой на R610, последовательность KDEL может быть слита с c-концевой областью одного из пептидов 2А и 2В, который, например, не должен считаться ограничительным, последовательность KDEL может быть слита с тяжелой цепью антитела с целью обеспечения удержания с ЭР.
Каждый белок, кодируемый второй нуклеотидной последовательностью, может быть гликозилированным.
Целевой белок, полученный таким образом при использовании способов А - Н, может быть извлечен из растения. Более того, целевой белок может быть частично очищен или очищен с использованием стандартных методов, как это должно быть известно специалисту в данной области знаний.
В тех случаях, когда нуклеотидные последовательности экспрессируют в самом растении, каждая из необходимых нуклеотидных последовательностей может быть введена в растение с использованием стандартных методов трансформации, методов транзиентной трансформации; два и более растений, каждое экпрессирующее одну и более из требуемых нуклеотидных последовательностей могут быть скрещены для получения растения, которое коэкспрессирует требуемую комбинацию нуклеотидных последовательностей, или комбинация вышеуказанных методов может быть объединена. Например, транзиентная экспрессия может быть выполнена при использовании устойчиво трансформированного растения, экспрессирующего последовательность, кодирующую GalT, GNT1-GalT, GalT и GNT1-GalT, GnT-III, GNT1-GnT-III, GnT-III и GNT1-GnT-III, или комбинацию из них.
В связи с этим, в настоящем изобретении также предложен способ (способ I) продуцирования растения, которое может быть использовано в качестве платформы для продуцирования целевого белка с модифицированным N-гликозилированием. Указанный способ включает в себя предоставление растения, которое экспрессирует одну или более чем одну первую нуклеотидную последовательность, кодирующую GalT, GNT1-GalT, или совместно GalT и GNT1-GalT, а также экспрессию одной и более нуклеотидных последовательностей. Для получения целевого белка любая вторая нуклеотидная последовательность, кодирующая целевой белок, вводится в растение-платформу с применением стандартных методов, использующих или стабильной (устойчивой) трансформации, или транзиентной (неустойчивой) трансформации, а вторая нуклеотидная последовательность экспрессирует так, что полученный целевой белок содержит гликаны с модифицированным N-гликозилированием, или растение, экспрессирующее первую нуклеотидную последовательность, скрещивается со вторым растением, экспрессирующим вторую нуклеотидную последовательность, и таким образом полученный целевой белок содержит гликаны с модифицированным N-гликозилированием. Целевой белок может быть извлечен из растения и, при необходимости, целевой белок может быть выделен и очищен с использованием стандартных способов.
В связи с этим, в настоящем изобретении также предложен способ (способ J) продуцирования растения, которое может быть использовано в качестве платформы для продуцирования целевого белка с модифицированным N-гликозилированием. Указанный способ включает в себя предоставление растения, которое экспрессирует одну или более чем одну первую нуклеотидную последовательность, кодирующую GnT-III, GNT1-GnT-III, или совместно GnT-III и GNT1-GnT-III, а также экспрессию одной и более нуклеотидных последовательностей. Для получения целевого белка любая вторая нуклеотидная последовательность, кодирующая целевой белок, вводится в растение-платформу с применением стандартных методов, использующих или стабильной (устойчивой) трансформации, или транзиентной (неустойчивой) трансформации, а вторая нуклеотидная последовательность экспрессирует так, что полученный целевой белок содержит гликаны с модифицированным N-гликозилированием, или растение, экспрессирующее первую нуклеотидную последовательность, скрещивается со вторым растением, экспрессирующим вторую нуклеотидную последовательность, и таким образом, полученный целевой белок содержит гликаны с модифицированным N-гликозилированием. Целевой белок может быть извлечен из растения и, при необходимости, целевой белок может быть выделен и очищен с использованием стандартных способов.
В связи с этим, в настоящем изобретении также предложен способ (способ K) продуцирования растения, которое может быть использовано в качестве платформы для продуцирования целевого белка с модифицированным N-гликозилированием. Указанный способ включает в себя предоставление растения, которое экспрессирует одну или более чем одну первую нуклеотидную последовательность, кодирующую GalT, GNT1-GalT, GalT и GNT1-GalT, GnT-III, GNT1-GnT-III, GnT-III и GNT1-GnT-III, или комбинацию из них, а также экспрессию одной и более нуклеотидных последовательностей. Для получения целевого белка любая вторая нуклеотидная последовательность, кодирующая целевой белок, вводится в растение-платформу с применением стандартных методов, использующих или стабильной (устойчивой) трансформации, или транзиентной (неустойчивой) трансформации, а вторая нуклеотидная последовательность экспрессирует так, что полученный целевой белок содержит гликаны с модифицированным N-гликозилированием, или растение, экспрессирующее первую нуклеотидную последовательность, скрещивается со вторым растением, экспрессирующим вторую нуклеотидную последовательность, и таким образом, полученный целевой белок содержит гликаны с модифицированным N-гликозилированием. Целевой белок может быть извлечен из растения и, при необходимости, целевой белок может быть выделен и очищен с использованием стандартных способов.
Нуклеотидная последовательность, кодирующая GalT, GNT1-GalT, GnT-III, GNT1-GnT-III, целевой белок, или комбинацию из них, можетт иметь оптимизированный кодон с целью повышения уровня экспрессии в растении. Под оптимизацией кодонов понимается выбор подходящих нуклеотидов ДНК для синтеза блоков построения олигонуклеотидов структурного гена ил его фрагмента, с их последующей энзиматической сборкой, с целью достижения использования кодонов в растении.
Для оптимизации экспрессии чужеродной последовательности в растении нуклеотидная последовательность, которая может быть дикого типа или синтетической последовательностью, может быть использована или изменена, как требуется, так, что соответствующий белок, например GalT, GNT1-GalT, GnT-III, GNT1-GnT-III, целевой белок, или их комбинация, продуцируется с более высоким уровнем выхода продукта, чем мог бы быть уровень его продуцирования, при кодировании белка при немодифицированной нуклеотидной последовательности. Например, и это не следует считать ограничительным условием, последовательность может быть синтетической последовательностью, которая оптимизирована для использования кодонов в растении, имеющей приблизительно 80% идентичность последовательностью дикого типа, как это определено с использованием сравнительных методик, например, но, не ограничиваясь этим, методика BLAST (доступная через GenBank; при использовании default параметров). Существует предположение, что фрагменты или части последовательности, кодирующей целевой белок, или его производные, который демонстрирует полезные биологические свойства, например, но, не ограничиваясь этим, антигенные свойства, могут быть экспрессированы в ткани растения.
Для достижения максимальных уровней экспрессии и продуцирования трансгенным растением белка GalT, GNT1-GalT, GnT-III, GNT1-GnT-III, а также целевого белка, последовательность нуклеиновой кислоты может быть проверена, а область кодирования модифицирована с целью оптимизации для экспрессии генов в растении, используя процедуру, аналогичную представленной Sandra et al. (Plant Cell Reports [Отчеты по растительным клеткам] 15:677-681; 1996). Таблица использования кодонов из генов высокой экспрессии двудольных растений имеется во многих источниках, в том числе Murray et al (Nuc Acids Res. [Исследов. нукл. кислот] 17:447-498; 1989). Кроме того, оптимизация последовательности может также включать уменьшением тандемных дубликаций кодонов, ликвидацию скрытых участков сплайсинга, уменьшение повторных последовательностей (включая инвертированные повторы), и может быть определена с использованием, например, программы Leto 1,0 (Entelechon, Германия).
В этой связи, в настоящем изобретении предлагается способ (L) синтезирования целевого белка с модифицированным N-гликозилированием, как изложено в одном из вышеуказанных способов (способы А - К), где одна или более чем одна нуклеотидная последовательность, кодирующая GalT, GNT1-GalT, GnT-III, GNT1-GnT-III, целевой белок или их комбинацию, оптимизируется для экспрессии в растении.
Таким образом, настоящее изобретение имеет отношение к растению, растительной клетке или семени, которые содержат нуклеотидную последовательность, кодирующую GalT, GNT1-GalT, GnT-III, GNT1-GnT-III, целевой белок или их комбинация, каждая из последовательностей функционально связана с регуляторной областью, являющейся активной в растении. Растение, растительная клетка или семя могут также содержать вторую нуклеотидную последовательность, кодирующую один или более чем один целевой белок, указанная нуклеотидная последовательность функционально связана с одной или более чем одной второй регуляторной областью, являющейся активной в растении. Первая нуклеотидная последовательность, вторая нуклеотидная последовательность, а также первая нуклеотидная последовательность вместе со второй нуклеотидной последовательностью могут быть оптимизированы для экспрессии кодонов в растении, растительной клетке или семени растения.
Термин «функционально связана» означает, что конкретные последовательности взаимодействуют как напрямую, так и косвенно для выполнения предназначенной функции, например посредничество в экспрессии генов или ее модуляция. Взаимодействие функционально связанных последовательностей может, например, проходить при посредничестве белков, которые взаимодействуют с функционально связанными последовательностями. Транскрипционная регуляторная область и представляющая интерес последовательность функционально связаны, когда последовательности функционально связаны так, чтобы разрешить транскрипцию представляющей интерес последовательности, подлежащей вовлечению транскрипционной регуляторной областью в посредничество или модуляцию.
Термин «часть растения» означает любую часть, полученную из растения, включая само растение, ткань, взятую из растения, например, но, не ограничиваясь этим, листья, листва и стебель, корни, надземная часть вместе с листвой, стебель и дополнительно цветковая часть растения, клетки и протопласты, полученные из растения.
Под термином «растительный материал» понимается любой материал, полученный из растения. Растительный материал может представлять собой все растение, его ткань, клетки или любую его фракцию. Кроме того, растительный материал может содержать внутриклеточные растительные компоненты, внеклеточные растительные компоненты, жидкие или твердые экстракты из растений или их комбинации. Более того, растительный материал может содержать растения, растительные клетки, ткань, жидкий экстракт или их комбинацию, из листьев растения, стеблей, плодов, корней или их комбинации. Растительный материал может содержать растение или его часть, которая не была подвергнута каким-либо операциям обработки. Однако также предполагается, что растительный материал может быть подвергнут минимальной обработке, как это описано ниже, или он прошел более тщательную обработку, включая частичную или тщательную очистку с использованием общеизвестной в данной области знаний методики, включая, но, не ограничиваясь этим, хроматографию, электрофорез и т.п.
Под термином «минимальная обработка» понимается растительный материал, например растение или его часть, содержащая целевой белок, прошедший частичную очистку для получения растительного экстракта, гомогенат, фракцию растительного гомогената и т.п. Частичная очистка может включать, но, не ограничивается этим, разрушение клеточных структур растения и создание тем самым состава, содержащего растворимые растительные компоненты и нерастворимые растительные компоненты, которые могут быть отделены, например, но, не ограничиваясь этим, центрифугированием, фильтрованием или тем и другим одновременно. В этой связи белки, выделяемые во внеклеточном пространстве листа или других тканей, могли бы быть легко получены при помощи вакуума или экстракции на центрифуге, или же ткани могут быть отделены под давлением путем пропускания через валки, или измельчения и т.п. с целью выдавливания или высвобождения белка из внеклеточного пространства. Минимальная обработка также может включать подготовку препаратов суммарных экстрактов растворимых белков, поскольку эти препараты должны иметь ничтожное загрязнение вторичными растительными продуктами. Кроме того, минимальная обработка может включать водную экстракцию растворимых белков из листьев, за которой следует осаждение (преципитация) с любой подходящей солью. Другие способы могут включать обширную мацерацию и экстракцию сока для обеспечения прямого использования экстракта.
Растительный материал в виде растительного вещества или ткани может приниматься пациентом перорально. Растительный материал может вводиться в организм как часть пищевой добавки, вместе с пищей или в капсулах. Растительный материал или ткань могут быть приготовлены в концентрированной форме с целью улучшения или увеличения приятного вкуса или представлены вместе с другими веществами, ингредиентами или фармацевтическими наполнителями, если в этом возникает необходимость.
Предполагается, что растение, содержащее целевой белок, может быть назначено для введения пациенту, например животному или человеку различными путями, в зависимости от потребности и ситуации. Например, целевой белок, полученный из растения, может быть выделен перед его использованием в неочищенной, наполовину очищенной или очищенной форме. Если белок подлежит очистке, то он может быть продуцирован либо в съедобных, либо в несъедобных растениях. Кроме того, если белок вводится перорально, растительная ткань может быть собрана и напрямую скормлена пациенту, или же собранная растительная ткань может быть высушена перед скармливанием, или животному разрешают щипать растения на выгуле без какого-либо предварительного его сбора. В пределах объема настоящего изобретения также учитывается возможность использования собранной растительной ткани в качестве пищевой добавки в корм животных. Если растительная ткань скармливается животному с малой обработкой или без дальнейшей обработки, предпочтительно, чтобы вводимая растительная ткань была съедобной.
Как подробно рассматривается в Примерах, GalT, GNT1-GalT, а также целевой белок были введены в растения транзиентным способом. Иммунологический анализ с применением соответствующих антител показал, что белок с MB, равным 150 кДа, присутствовал в трансформированных клетках (фиг.2, 3А и 3В). Кроме того, GalT или GNT1-GalT была обнаружена в экстрактах, полученных из растений, экспрессирующих любую конструкцию, а измененное N-гликозилирование целевого наблюдалось при экспрессировании GNT1-GalT в растении (фиг.6). Таким образом, рекомбинантно экспрессированная GalT или GNT1-GalT является активной in planta.
GalT-FLAG или GNT1-GalT-FLAG (т.е. GalT или GNT1-GalT, маркированной на С-конце FLAG-эпитопом) для возможности проведения иммунологического анализа рекомбинантного белка в трансформантах были введены в растения. Иммуноблотинг с использованием анти-FLAG-антитела может быть использован для демонстрации того, что соответствующий белок присутствует в трансформированных клетках.
Термин «аналог» или «производное» включает замещение, удаление или присоединение к нуклеотидной последовательности, кодирующей GalT (SEQ ID NO: 14), каталитический домен GalT (нуклеотиды 368-1198 последовательности SEQ ID NO: 14; кодирующую выделенную полужирным шрифтом на фиг 5b) или GNT1-GalT (нуклеотиды 248-1077 последовательности SEQ ID NO: 17; кодирующую выделенную полужирным шрифтом на фиг 5d) при условии, что последовательность кодирует белок, который модифицирует, или при слиянии с цитоплазматическим концевым сегментом (CTS) GalT, модифицирует профиль гликозилирования целевого белка при экспрессии в растении, например уменьшение фукозилирования, ксилозилирования или того и другого одновременно, гликанов целевого белка, или увеличение гликозилирования целевого белка при сравнении с профилем гликозилирования целевого белка в растении, в условиях отсутствия эктопически экспрессированного GalT (SEQ ID NO: 14) или GNT1-GalT (SEQ ID NO: 17). Например, протеин, кодируемый последовательностью, может присоединять концевую галактозу в процессе созревания N-гликанов. Производные или аналоги последовательностей нуклеиновой кислоты обычно демонстрируют более чем 80% идентичность с последовательностью нуклеиновой кислоты, например от 80 до 100% идентичность последовательностей, или 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100% идентичность. Идентичность последовательностей может быть определена при использовании алгоритма BLAST (GenBank: ncbi.nlm.nih.gov/cgi-bin/BLAST/) с установленными по умолчанию параметрами (Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11). Аналоги или их производные также включают те нуклеотидные последовательности, которые скрещиваются в жестких условия гибридизации, см. Маниатис с соавт. (Maniatis с соавт. в публикациях Molecular Cloning [молекулярное клонирование] Рекомендации по проведению работ в лаборатории), лаборатория Cold Spring Harbor, 1982, стр.387-389 или Аусубел с соавт. (Ausubel с соавт. (eds), 1989, Current Protocols in Molecular Biology [Существующие протоколы в молекулярной биологии], том 1, Green Publishing Associates, Inc. и John Wiley & Sons, Inc., New York, в п.2.10.3) с любой из последовательностей GalT (SEQ ID NO: 14), GNT1-GalT (SEQ ID NO: 18), рассмотренных в настоящем описании при условии, что указанная последовательность кодирует белок, который модифицирует профиль гликозилирования целевого белка, например, уменьшая фукозилирование, ксилозилирование или то и другое одновременно, гликанов целевого белка, или увеличивая гликозилирование целевого белка при сравнении с профилем гликозилирования целевого белка в растении, продуцированного в отсутствии GalT (SEQ ID NO: 14) или GNT1-GalT (SEQ ID NO: 17). Например, протеин, кодируемый последовательностью, может присоединять концевую галактозу в процессе созревания N-гликанов. Примером таких жестких условий гибридизации с подходящим зондом, например, но, не ограничиваясь этим [гамма 32Р]АТФ-зависимый меченый зонд длительностью 16-20 ч при 65°С в 7% ДСН, 1 мМ ЭДТК, 0,5М Na2HPO4, pH 7,2. Затем производилось промывание в течение 30 минут при 65°С в 5% ДСН, 1 мМ ЭДТК, 40 mM Na2HPO4, pH 7,2 и промывание при 65°С в 1% ДСН, 1 мМ ЭДТК, 40-мМ Na2HPO4 pH 7,2. Промывание в этом буфере может быть повторено для снижения фона.
В аналогичном варианте, настоящее изобретение включает в себя модифицирование нуклеотидной последовательности, кодирующей GnT-III (SEQ ID NO: 16), каталитический домен GnT-III или GNT1-GnT-III (SEQ ID NO: 20) при условии, что последовательность кодирует белок, который модифицирует, или при слиянии с цитоплазматическим концевым сегментом (CTS) GnT-III, модифицирует профиль гликозилирования целевого белка при экспрессии в растении, например, деление пополам GlnAc, уменьшение фукозилирования, ксилозилирования или того и другого одновременно, гликанов целевого белка, или увеличение гликозилирования целевого белка при сравнении с профилем гликозилирования целевого белка в растении, в условиях отсутствия эктопически экспрессированного GnT-III (SEQ ID NO: 16) или GNT1- GnT-III (SEQ ID NO: 26). Производные или аналоги последовательностей нуклеиновой кислоты обычно демонстрируют более чем 80% идентичность с последовательностью нуклеиновой кислоты, например от 80 до 100% идентичность последовательностей, или 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100% идентичность. Идентичность последовательностей может быть определена при использовании алгоритма BLAST (GenBank: ncbi.nlm.nih.gov/cgi-bin/BLAST/) с установленными по умолчанию параметрами (Программа: blastn; База данных: номер; Expect 10; фильтр: малой сложности; Расположение: парами; Размер слова: 11). Аналоги или их производные также включают те нуклеотидные последовательности, которые скрещиваются в жестких условия гибридизации, см. Маниатис с соавт. (Maniatis с соавт. в публикациях Molecular Cloning [молекулярное клонирование] Рекомендации по проведению работ в лаборатории), лаборатория Cold Spring Harbor, 1982, стр.387-389 или Аусубел с соавт. (Ausubel с соавт. (eds), 1989, Current Protocols in Molecular Biology [Существующие протоколы в молекулярной биологии}, том 1, Green Publishing Associates, Inc. и John Wiley & Sons, Inc., New York, в п.2.10.3) с любой из последовательностей GnT-III (SEQ ID NO: 16), GNT1-GnT-III (SEQ ID NO: 26), рассмотренных в настоящем описании при условии, что указанная последовательность кодирует белок, который модифицирует профиль гликозилирования целевого белка, например, уменьшая фукозилирование, ксилозилирование или то и другое одновременно, гликанов целевого белка, или увеличивая гликозилирование целевого белка при сравнении с профилем гликозилирования целевого белка в растении, продуцированного в отсутствии GnT-III (SEQ ID NO: 16) или GNT1-GnT-III (SEQ ID NO: 26). Примером таких жестких условий гибридизации с подходящим зондом, например, помимо прочего [гамма 32Р] АТФ-зависимый меченый зонд длительностью 16-20 ч при 65°С в 7% ДСН, 1 мМ ЭДТК, 0,5М Na2HPO4, pH 7,2. Затем производилось промывание в течение 30 минут при 65°С в 5% ДСН, 1 мМ ЭДТК, 40 мM Na2HPO4, pH 7,2 и промывание при 65°С в 1% ДСН, 1 мМ ЭДТК, 40-мМ Na2HPO4, pH 7,2. Промывание в этом буфере может быть повторено для снижения фона.
Под «регуляторной областью», «регуляторным элементом» или «промотором» понимается часть нуклеиновой кислоты, обычно, но не всегда расположенной перед областью кодирования белка гена, которая может состоять либо из ДНК, либо из РНК, или из ДНК и РНК одновременно. Когда регуляторная область является активной и находится в функциональном взаимодействии или функционально связана с целевым геном, это может привести к экспрессии целевого гена. Регуляторный элемент может обладать способностью опосредования органной специфичности или контролирования эволюционной или временной активации гена. «Регуляторная область» включает в себя элементы промотора, элементы активной зоны промотора, демонстрирующие базовую активность промотора, элементы, индуцируемые в ответ на внешние раздражители, элементы, которые способствуют активности промотора, например отрицательные регуляторные элементы или транскрипционные ген-усилители. Используемая в настоящем описании «регуляторная область» также включает в себя элементы, являющиеся активными, следуя за транскрипцией, например регуляторные элементы, модулирующие экспрессию генов, например трансляционные и транскрипционные ген-усилители, трансляционные и транскрипционные ген-репрессоры, вышележащие активирующие последовательности, а также детерминанты нестабильности мРНК. Последние из указанных элементов могут быть расположены близко к области кодирования.
В контексте настоящего описания термин «регуляторный элемент» или «регуляторная область» обычно относится к последовательности ДНК, чаще, не всегда, расположенной перед (5'-концом) кодирующей последовательностью структурного гена, контролирующего экспрессию области кодирования путем обеспечения распознавания полимеразы РНК и/или другие факторы, необходимые для инициирования транскрипции в конкретном сайте. Однако следует понимать, что другие нуклеотидные последовательности, расположенные внутри интронов или 3'-конца последовательности, могут также участвовать в регулировании экспрессии кодирующей области, представляющей интерес. Примером регуляторного элемента, обеспечивающего распознавание полимеразы РНК или прочих транскрипционных факторов с целью инициирования конкретного сайта, является элемент промотора. Большинство, не все, эукариотные элементы промотора, содержат ТАТА-бокс, т.е. консервативную последовательность нуклеиновой кислоты, состоящей из пар нуклеотидов аденозин и тимидин, обычно расположенную на удалении приблизительно в 25 пар нуклеотидов перед сайтом инициирования транскрипции. Элемент промотора содержит основной элемент промотора, отвечающего за инициацию транскрипции, а также прочие регуляторные элементы (перечислены выше), модифицирующие экспрессию генов.
Существует несколько типов регуляторных областей, включая регулируемые эволюционно, индуцированные или конститутивные. Регуляторная область, регулируемая эволюционно или контролирующая дифференциальную экспрессию контролируемого гена, активируется внутри определенных органов или тканей органа в конкретные промежутки времени в период развития указанного органа или ткани. Однако некоторые регуляторные области, которые регулируются эволюционно, могут в предпочтительном случае быть активными в определенных органах или тканях на конкретных стадиях развития. Они могут быть также активными в режиме регулирования эволюционно или также на основном уровне в других органах или тканях растения. Примеры тканеспецифичных регуляторных областей, для примера смотри конкретную регуляторную область, включают в себя промотор напина, а также промотер круциферина (Rask с соавт., 1998, J.Plant Physiol. 152; 595-599; Bilodeau с соавт., 1994, Plant Cell [] 14; 125-130). Специфичный к листьям промотор включает в себя промотер пластоцианина (US 7125978, включенный в настоящее описание путем ссылки; SEQ ID NO: 23; фиг 1b).
Индуцированной регуляторной областью является область, способная напрямую или косвенно активировать транскрипцию одной или более последовательностей ДНК или генов в ответ на индуктор. При отсутствии индуктор последовательности считывание ДНК или генов не будет происходить. Обычно фактор белка, присоединяющийся конкретно к индуцируемой регуляторной области для активирования транскрипции, может присутствовать в неактивной форме, которая может быть прямо или косвенно преобразована индуктором в активную форму. Однако фактор протеина может тоже отсутствовать. Индуктором может выступать химическое вещество, например белок, метаболит, регулятор роста, гербицид, или фенольное соединение, или же физиологический стресс, вызванный непосредственно теплом, холодом, солью или токсичными элементами, или косвенно, через воздействие патогенным или болезнетворным веществом, например вирусом. Растительная клетка, содержащая индуцированную регуляторную область, может попасть под воздействие индуктора при внешнем приложении индуктора к клетке или растению, например, опрыскиванием, увлажнением, нагревом или иными способами. Индуцируемые регуляторные элементы могут быть получены из генов как растительного, так и нерастительного происхождения (например, Gatz С.и Lenk, I.R.P., 1998, Trends Plant Cell. [Отбор растений, имеющих изменения] 3, 352-358, включенный в настоящее описание путем ссылки). Примеры потенциальных индуцированных промоторов включают пример, но, не ограничиваясь этим, индуцируемый тетрациклином промотер (Gatz С., 1997, Ann. Rev. Plant Physiol. Plant Mol. Biol. 48, 89-108; включенный в настоящее описание путем ссылки), индуцируемый стероидом промотор (Aoyama, Т, и Chua, N.H., 1997, Plant J. 2, 397-404; включенный в настоящее описание путем ссылки) и индуцируемый этанолом промотор (Salter, M.G., с соавт., 1998, Plant Journal 16, 127-132; Caddick, M.X., с соавт., 1998, Nature Biotech. 16, 177-180, включенные в настоящее описание путем ссылки), индуцированные цитокинином гены IB6 и CKI1 (Brandstatter, I., и Kieber J.J., 1998, Plant Cell 10, 1009-1019; Kakimoto, Т., 1996, Science 274, 982-985; включенные в настоящее описание путем ссылки), и, наконец, индуцированный ауксином элемент, DR5 (Ulmasov, Т., с соавт., 1997, Plant Cell 19, 1963-1971; включенные в настоящее описание путем ссылки).
Конститутивная регуляторная область направляет экспрессию генов через различные части растения и непрерывно в течение всего развития растения. Примеры конститутивных регуляторных элементов включают промоторы, связанные с транскриптом вируса мозаики цветной капусты CaMV 35S (Odell с соавт., 1985, Nature, 313; 810-812), актин риса 1 (Zhang с соавт., 1991, Plant Cell, 3; 1155-1165), актин 2 (An с соавт., 1996, Plant J., 10: 107-121), или триметилсилил 2 (тмс 2) (U.S. 5,428,147, включенный в настоящее описание путем ссылки), и гены триозефосфатизомеразы 1 (Xu с соавт., 1994, Plant Physiol. 106; 469-467), ген убиквитина кукурузы 1 (Cormejo с соавт., 1993, Plant Mol. Biol. 29; 637-646), гены убиквитина 1 и 6 Arabidopsis (Holtorf at al., 1995, Plant Mol. Biol. 29; 637-646), ген фактора 4А инициирования трансляции табака (Mandel at al., 1995, Plant Mol. Biol. 29; 995-1004). Термин «конститутивная», как он используется в настоящем описании, не обязательно означает, что контролируемый ген конститутивной регуляторной области экспрессируется на одном уровне во всех типах клетки, но, что ген экспрессируется в широком диапазоне типов клетки, даже, несмотря на то, что часто наблюдается изменение численности.
Одна и более чем одна нуклеотидная последовательность по настоящему изобретению может быть экспрессирована в любом подходящем растении-хозяине, которое трансформировано при помощи указанной нуклеотидной последовательности, или структур или векторов настоящего изобретения. Примеры подходящих «хозяев» включают, но не ограничиваются этим, сельскохозяйственные культуры, среди них: люцерна, рапс, дикая горчица, кукуруза, табак, альфальфа (люцерна полевая), картофель, женьшень, горох, овес, рис, соя, пшеница, ячмень, подсолнечник и хлопок.
Одна и более химерических генетических конструкций в соответствии с настоящим изобретением могут дополнительно содержать 3'-нетранслируемую область. Указанная 3'-нетранслируемая область относится к части гена, содержащей сегмент ДНК, в котором имеется сигнал полиаденилирования и любые другие регуляторные сигналы, способные осуществлять процессинг мРНК или экспрессию гена. Сигнал полиаденилирования обычно характеризуется выполнением присоединения следов полиадениловой кислоты к 3'-концу прекурсора мРНК. Сигналы полиаденилирования обычно распознаются по присутствию гомологии к канонической форме 5' ААТААА-3', хотя вариации не являются обычным явлением. Одна и более химерических генетических конструкций по настоящему изобретению могут также включать дополнительные энхенсеры (усилители), усилители трансляции или транскрипции, как может потребоваться. Эти области усиления хорошо известны специалистам в данной области знаний, и они могут включать кодон инициирования АТГ и прилегающие последовательности. Кодон инициирования должен совпадать по фазе с рамкой считывания кодирующей последовательности для обеспечения трансляции всей последовательности.
Неограничительными примерами подходящих 3' областей являются 3' транскрибированные нетранслируемые области, содержащие сигнал полиаденилирования опухоли агробактерии Agrobacterium, индуцирующей (Ti) плазмидные гены, например наполин синтаза (ген NO-синтазы), и гены растения, например гены белка хранения сои и малая субединица гена рибулозо-1,5-бифосфат карбоксилазы (ssRUBISCO).
Для облегчения выявления трансформированных растительных клеток конструкции настоящего изобретения могут подвергаться дополнительному воздействию для введения селектируемых растением маркеров. Полезные селективные маркеры включают энзимы, которые обеспечивают сопротивляемость к химическим веществам, таким как антибиотики, например гентамицин, гигромицин, канамицин, или гербициды, например фосфинотрицин, глифосат, хлорсульфурон и т.п. Аналогичным образом могут быть использованы энзимы, обеспечивающие продуцирование соединения, определяемого по изменению цвета, например, бета-глюкуронидаза (GUS), или по свечению, например люцифераза или зеленый флуоресцентный белок (GFP).
Также следует принять во внимание часть изобретения, касающуюся трансгенных растений, растительных клеток и семян, содержащих конструкцию химерного гена в соответствии с настоящим изобретением. Способы регенерации целых растений из растительных клеток также известны из существующего уровня техники. В целом, трансформированные растительные клетки культивируются в соответствующей среде, которая может содержать отборные агенты, например антибиотики, в которых используются селективные маркеры для облегчения идентификации трансформированных растительных клеток. После образования каллюса формирование отростков может быть вызвано путем использования соответствующих растительных гормонов в соответствии с известными способами, а отростки помещаются в корнеобразующую среду для регенерации растений. Полученные растения могут быть использованы для создания повторных генераций либо из семян, либо путем использования методов вегетативного размножения. Трансгенные растения могут также быть выращены без использования тканевых культур.
Регуляторные элементы в соответствии с настоящим изобретением также могут быть объединены с представляющей интерес областью кодирования, для экспрессии в пределах организмов-хозяев, которые поддаются трансформации или транзиентной экспрессии. Такие организмы включают, но не ограничиваются этим, растения как однодольные, так и двудольные, например, но, не ограничиваясь этим, зерновые, злаковые растения, пшеница, ячмень, овес, табак, горчица, соя, фасоль, горох, люцерна, картофель, помидоры, женьшень и арабидопсис.
Способы стабильной трансформации и регенерации этих организмов существуют в области техники и известны специалисту в данной области знаний. Способ получения трансформированных и регенерированных растений не является существенным для настоящего изобретения.
Термин «трансформация» подразумевает межвидовой перенос генетической информации (нуклеотидной последовательности), что проявляется генотипически, фенотипически или тем и другим типом одновременно. Межвидовой перенос генетической информации от химерной конструкции к хозяину может быть наследственным, а перенос генетической информации считаться стабильным, или перенос может быть транзиентным, а перенос генетической информации не являться наследственным.
Настоящее изобретение также включает подходящий вектор, содержащий химерную конструкцию, удобную для использования с системами либо стабильной, либо транзиентной экспрессии. Генетическая информация также может быть представлена в одной конструкции и более. Например, нуклеотидная последовательность, кодирующая целевой белок, может быть введена в одну конструкцию, а вторая нуклеотидная последовательность, кодирующая белок, модифицирующий гликозилирование целевого белка, может быть введена с использованием отдельной конструкции. Указанные нуклеотидные последовательности затем могут быть коэкспрессированы внутри растения. Однако может быть также использована конструкция, содержащая нуклеотидную последовательность, кодирующую как целевой белок, так и белок, модифицирующий профиль гликозилирования целевого белка. В этом случае нуклеотидная последовательность должна была бы содержать первую последовательность, включающую в себя первую последовательность нуклеиновой кислоты, кодирующую целевой белок, и функционально связанную с промотором или регуляторной областью, а также вторую последовательность, содержащую вторую последовательность нуклеиновой кислоты, кодирующую белок, модифицирующий профиль гликозилирования целевого белка, указанная последовательность функционально связана с промотором или регуляторной областью.
Термин «коэкспрессированные» подразумевает, что две нуклеотидные последовательности и более экспрессируют почти одновременно внутри растения и внутри одной ткани растения. Однако нет необходимости в том, чтобы указанные нуклеотидные последовательности экспрессировали точно в одно и то же время. Предпочтительнее, чтобы две нуклеотидные последовательности и более экспрессировали так, что у кодированных продуктов была возможность для взаимодействия. Например, белок, модифицирующий гликозилирование целевого белка, может быть экспрессирован до или в течение периода экспрессии целевого белка так, что происходит модификация гликозилирования целевого белка. Две нуклеотидные последовательности и более могут быть коэкспрессированы с использованием системы транзиентной экспрессии, в которой две последовательности и более вводятся в растение почти одновременно в условиях, при которых происходит экспрессия обеих последовательностей. В альтернативном варианте растение-платформа, содержащее одну из нуклеотидных последовательностей, например последовательность, кодирующую белок, модифицирующий профиль гликозилирования целевого белка, может быть трансформирован либо транзиентно, либо стабильно с дополнительной последовательностью, кодирующей целевой белок. В этом случае последовательность, кодирующая белок, модифицирующий гликозилирование целевого белка, может быть экспрессирована в требуемой ткани на требуемой стадии развития, или его экспрессия может быть индуцирована при помощи индуцибельного промотора, а дополнительная последовательность, кодирующая целевой белок, может быть экспрессирована в аналогичных условиях и в той же ткани с целью обеспечения коэкспрессии нуклеотидных последовательностей.
Конструкции в соответствии с настоящим изобретением могут быть введены в клетки растения с использованием Ti-плазмид, Ri-плазмид, векторов вирусов растений, прямой трансформации ДНК, микроинъекции, электропорации и т.п. Для ознакомления с этими методами, см., например, Weissbach и Weissbach, Methods for Plant Molecular Biology, Academy Press, New York VIII, pp.421-463 (1988); Geierson и Corey, Plant Molecular Biology, 2d Ed. (1988); и Miki и lyer, Fundamentals of Gene Transfer in Plants. В Plant Metabolism, 2d Ed. DT. Dennis, DH Turpinm DD Leferbve, DB Layzell (eds), Addison Wesly, Langmans Ltd London, pp.561-579 (1997). Другие методы включают прямое усвоение ДНК, использование липосом, электропорации, например использование протопластов, микроинъекции, микроснарядов, а также вакуумной инфильтрации. Смотри, например, Bilang с соавт. (Gene 100: 247-250 (1991), Scheid с соавт. (Mol. Gen. Genet. 228: 104-112, 1991), Guerche с соавт. (Plant Science 52: 111-116, 1987), Neuhause с соавт. (Theor. Appl Genet. 75: 30-36, 1987), Klein с соавт., Nature 327: 70-73 (1987); Howell с соавт. (Science 208: 1265, 1980), Horsch с соавт. (Science 227: 1229-1231, 1985), De Block с соавт., Plant Physiology 91: 693-701, 1989)), Methods for Plant Molecular Biology (Weissbach и Weissbach, Academy Press Inc., (1988), Methods for Plant Molecular Biology (Schuler и Zielinski, eds, Academic Press Inc., 1989), Liu и Lomonossoff (J. Virol Meth, 105: 343-348, 2002), патенты США №№4945050; 5036006 и 5100792, заявки на патент США рег. №№08/438666, подана 10 мая 1995 г. и 07/951715, подана 25 сентября (все включены в описание в виде ссылок).
Как приведено в описании ниже, методы транзиентной экспрессии могут быть использованы для экспрессии конструкций в соответствии с настоящим изобретением (см. Liu и Lomonossoff, 2002, Journal of Virological Methods, 105: 343-348); включенные в настоящее описание в виде ссылки). В альтернативном варианте могут быть использованы методы транзиентной экспрессии, базирующейся на вакууме, как это изложено Kapila с соавт., 1997, включенные в настоящее описание в виде ссылки). Эти методы могут включать, например, но, не ограничиваясь этим, метод агроинокуляции или агроинфильтрации, однако, как было отмечено выше, также могут быть применены другие транзиентные методы. При помощи агроинокуляции или агроинфильтрации смесь агробактерий (Agrobacteria), содержащая искомую нуклеиновую кислоту, проникает в межклеточные пространства ткани, например, листья, надземная часть растения (включая стебель, листья и цветок), другие части растения (стебель, корень, цветок) или все растение. После преодоления эпидермиса агробактерий заражают и передают копии Т-ДНК в клетки. Т-ДНК эписомально транскрибируется, а мРНК транслируется, вызывая продуцирование целевого белка в зараженных клетках, проникновение Т-ДНК внутрь ядра является временным (транзиентным).
Термины «искомый ген», «целевая нуклеотидная последовательность», или «целевая кодирующая область» подразумевают любой ген, любую нуклеотидную последовательность, или кодирующую область, которые должны быть экспрессированы в организме-хозяине, например в растении. Эти термины являются взаимозаменяемыми. Такая целевая нуклеотидная последовательность включает, но, не ограничивается этим, ген или кодирующую область, продуктом которых является целевой белок. Примеры целевого белка включают, например, но не ограничиваясь этим, промышленный энзим, белковую добавку, нутрицевтик, продукт с добавленной стоимостью или их фрагменты для использования в кормах, продуктах питания или в тех и других одновременно, фармацевтически активный белок, например, но не ограничивается этим, факторы роста, регуляторы роста, антитела, антигены и их фрагменты или их производные, пригодные для иммунизации или вакцинации и т.п. Дополнительный целевой белок может включать, но не ограничиваясь этим, интерлейкины, например один и более ИЛ1 - ИЛ24, ИЛ-26 и ИЛ-27, цитокины, эритропоэтин (ЕРО), инсулин, факторы Г-КСФ, ГМКСФ, ГГЧ-КСФ, М-КСФ или их комбинации, интерфероны, например альфа-интерферон, бета-интерферон, гамма-интерферон, показатели свертываемости крови, например, фактор VIII, фактор IX, или тАП (тканевый активатор плазмиогена), ГРЧ (гормон роста человека), рецепторы, агонисты рецепторов, антитела, нейро-полипептиды, инсулин, нейро-полипептиды, вакцины, факторы роста, например, но, не ограничиваясь этим, кератиноцитарный фактор роста, трансформационный фактор роста, регуляторы роста, антигены, автоантигены, их фрагменты или их комбинации.
Если целевая нуклеотидная последовательность кодирует продукт, являющийся напрямую или косвенно токсичным по отношению к растению, то путем использования метода в соответствии с настоящим изобретением такая токсичность может быть снижена во всем растении путем селективной экспрессии целевого гена в пределах требуемой ткани или на требуемой стадии развития растения. Кроме того, ограниченный период экспрессии, обусловленный транзиентной экспрессией, может уменьшить эффект при продуцировании токсичного продукта в растении.
Целевая кодирующая область или целевая нуклеотидная последовательность может быть экспрессирована в любом растении-хозяине, которое является либо трансформированным, либо содержит нуклеотидные последовательности, либо молекулы нуклеиновой кислоты, либо генетические конструкции, либо векторы в соответствии с настоящим изобретением. Примеры подходящих хозяев включают, но, не ограничиваясь этим, арабидопсис, сельскохозяйственные культуры, включая, например, канолу (разновидность рапса), разновидность капусты, кукурузу, табак, люцерну, картофель, женьшень, горох, овес, рис, сою, пшеницу, ячмень, подсолнечник и хлопок.
Как подробно изложено в примерах, приведенных ниже, синтез целевого белка, например, но не ограничиваясь антителом, С5-1, с модифицированным N-гликозилированием, был получен в растении коэкспрессирующем либо GalT, либо GNT1-GalT.
Перечень последовательностей
ность
Примеры
Пример 1. Сборка полигенных экспрессирующих кластеров R610, R612 (Фиг.1a), R621 и R622 (Фиг.5а)
Все манипуляции были выполнены при использовании общих протоколов молекулярной биологии по Сэмбруку и Расселу (2001 г.).
R610, R612 (Фиг.1а)
Примененные олигонуклеотиды (праймеры) указаны ниже:



Первый шаг клонирования состоял из сборки плазмиды рецептора, содержащей расположенные выше и ниже регуляторные элементы гена пластоцианина люцерны. Промотор пластоцианина (Патент США 7125978, включенный в настоящее описание в виде ссылки) и последовательности 5'-НТО были амплифицированы из геномной ДНК люцерны при помощи олигонуклеотидных праймеров Xmal-pPlas.c (SEQ ID NO: 1) и Sacl-ATG-pPlas.r (SEQ ID NO: 2). Полученный продукт амплификации был обработан при помощи Xmal и Sacl и затем пришит в pCAMBLA.2300, ранее обработанный при помощи этих же энзимов, для создания pCAMBIA-PromoPlasto. Аналогичным образом последовательности 3'-НТО и терминатор гена пластоцианина (фиг.1с; нуклеотиды 1-399 последовательности SEQ ID NO: 24) были амплифицированы от геномной ДНК люцерны при помощи следующих праймеров: Sacl-PlasTer.c (SEQ ID NO: 3) и EcoRI-PlasTer.r (SEQ ID NO: 4), а продукт был обработан при помощи Sad и EcoRI перед их внесением в те же сайты pCAMBIA-PromoPlasta для создания pCAMBIAPlasto.
Плазмиды R610, R612 были подготовлены так, чтобы содержать последовательности, кодирующие легкую цепь антитела С5-1 и тяжелую цепь антитела С5-1 под промотором пластоцианина люцерны в качестве тандемной конструкции; R610 была создана для возможности удержания в ЭР собранного ИГГ и содержала последовательность KDEL, объединенную с концом тяжелой цепи антитела С5-1, а R612 была создана для обеспечения секреции.
Сборка полигонов С5-1 экспрессирующих кластеров была выполнена с использованием метода ПЦР-опосредованного лидирования (сшивания), описанного Darveau с соавт. (1995). Для сборки последовательностей, кодирующих легкую цепь, расположенную ниже промотора пластоцианина, первый шаг состоял в усилении первых 443 основных пар (bp) промотора пластоцианина люцерны (нуклеотиды 556-999 на фиг 1b или SEQ ID NO: 23), описано D'Aoust с соавт. (патент США 7125978, включенный в настоящее описание в виде ссылки), ниже по отношению к исходному АТГ, методом ПЦР с использованием pCAMBIAPlasto в качестве матрицы и следующих праймеров:
Plasto 443с (SEQ ID NO: 5) и Plas+LC-C51.r (SEQ ID NO: 6; перекрытие подчеркнуто, вверху).
Параллельно с этим, последовательность, кодирующая легкую цепь, была ПЦР-амплифицирована от Плазмиды pGA643-kappa (Khoudi с соавт., 1999) при помощи следующих праймеров:
LC-C51.C (SEQ ID NO: 7) и LC-C51XhoSac.r. (SEQ ID NO: 8; перекрытие подчеркнуто, вверху).
Полученные в результате амплификации два продукта были смешаны и использованы в качестве матрицы в третьей ПЦР-реакции с использованием праймеров Plasto-443c (SEQ ID NO: 5) и LC-C51XhoSac.r. (SEQ ID NO: 8). Перекрытие между праймерами Plas+LC-C51.r (SEQ ID NO: 6) и LC-C51.C (SEQ ID NO: 7), использованными в первых реакциях, привело к сборке продуктов амплификации в ходе третьей реакции. Собранный продукт, полученный в результате третьей ПЦР-реакции, был обработан с применением DraIII и SacI и введен в сайт pCAMBIAPlasto, обработанный с применением DraIII и Sad, для формирования плазмиды R540/
Последовательность, кодирующая тяжелую цепь, была слита с верхним регуляторным элементом пластоцианина путем амплифицирования 443 базовых пар выше исходного АТГ пластоцианина, нуклеотиды 556-999 (фиг.1b; SEQ ID NO: 23) при помощи ПЦР с использованием сайта pCAMBIAPlasto в качестве матрицы и следующими праймерами:
Plasto 443 с (SEQ ID NO: 5) и НС-С51.r (SEQ ID NO: 9; перекрытие подчеркнуто, вверху).
Продукты указанных реакций были смешаны и собраны в третьей ПЦР-реакции с использованием праймеров Plasto 443 с (SEQ ID NO: 5) и HC-C51XhoSac.r (SEQ ГО NO: 11). Полученный в результате этого фрагмент был обработан с применением DraIII и Sad и введен в pCAMBIAPlasto между сайтами DraIII и SacI. Полученная в результате этого плазмида была названа R541.
KDEL-маркер был присоединен к С-концу последовательности, кодирующей тяжелую цепь, путем ПЦР-амплификации с применением праймеров Plasto 443 с (SEQ ID NO: 8) и НС-С51 KDEL (Sacl).r (SEQ ID NO: 12), используя плазмиду R541 в качестве матрицы. Полученный в результате этого фрагмент был обработан с применением DraIII и SacI, клонированных в аналогичные сайты pCAMBIAPlasto, создающие плазмиду R550.
Сборка полигонов экспрессирующих кластеров легкой и тяжелой цепей на аналогичной бинарной плазмиде была выполнена следующим образом: R541 и R550 были обработаны при помощи EcoR1, дифосфорилированы («затуплены на концах»), обработаны при помощи эндонуклеазы рестрикции HindIII и лигированы в HindIII и Smal рецепторных зонах плазмиды R540 для создания R610 (с KDEL) и R612 (без KDEL, см. фиг.1).
R610, R612 (Фиг.5а) - Примененные олигонуклеотиды (праймеры) указаны ниже:

Плазмиды для экспрессии GalT и GNTIGalT были собраны из pBLTI121 (Pagny с соавт., 2003). Человеческий ген β(1,4)-галактозилтрансферазы (hGalT) (УДФ-галактоза; β-N-ацетилглюкозаминид; β(1,4)-галактозилтрансфераза; ЕС 2.4.1.22) был изолирован от pUC19-hGalT (Watzele с соавт.. 1991) с обработкой EcoRI. После обработки по Кленову 1,2-килобазовый фрагмент GalT был клонирован в pBLTI221 на сайтах Sma I, в результате образовалась плазмида pBLTI221 GalT. Флаг-маркер был прикреплен к С-концевой области кодирующей области при помощи ПЦР с использованием праймеров FGalT (SEQ ID NO: 27) и RGalTFlagStu (SEQ ID NO: 28) для амплификации. Затем была продуцирована плазмида R622 путем клонирования этот XbaI-StuI фрагмент в бинарный вектор pBLTI121. Первые 77 а.а. из N-ацитил глюкозаминил трансферазы I (GNTI), соответствующие трансмембранному домену, были амплифицированы ПЦР с использованием кДНК табака, кодирующей N-GNTI как матрицу (Strasser с соавт., 1999), а также FGNT (SEQ ID NO: 29) и RGNTSpe (SEQ ID NO: 30) в качестве праймеров. Продукт амплифицирования сначала был клонирован в вектор pGEM-T, a полученная плазмида была обработана при помощи ApaI и BamHI, и связана с pBLTI221, продуцирующим плазмиду, именуемую pBLTI221-GNTI. Каталитический домен hGalT был получен путем ПЦР-амплификации на pBLTI221 hGalT, с использованием праймеров FGalTSpe (SEQ ID NO: 25) и RGalTFlagStu (SEQ ID NO: 28), с образованием сайтов SpeI и StuI на 5'-конце 3'-конце, соответственно. Затем фрагмент SpeI/StuI hGalT был клонирован в pBLTI221-GNTI с использованием тех же самых (SpeI и StuI) сайтов, с созданием pBLTI221-GNTIGalT. Наконец, сайт pBLTI221-GNTIGalT был обработан при помощи XbaI и StuI с отделением GNTIGalT кодирующей последовательности (фиг.5d; SEQ ID NO: 17), a R621 была получена путем клонирования указанного фрагмента в бинарный вектор pBLTI121.
Все клоны были организованы в последовательности с целью подтверждения целостности конструкций. Плазмиды были использованы для трансформирования опухолеобразующих бактерий (Agrobacterium tumefaciens) (AGL 1; ATCC, Manassas, VA 20108, USA) методом электропорации (Hofgen и Willmitzer, 1988) с использованием прибора Gene Pulser II (Biorad, Hercules, CA. USA) для трансформации кишечной палочки (W.S. Dower, Electroporation of bacteria, in "Genetic Engineering", Volume 12, Plenum Press, New York, 1990, J.K. Setlow eds.). Целостность всех штаммов А. tumefaciens была подтверждена рестрикционным картированием.
Конструкция HcPro была подготовлена в соответствии с описанием в Hamilton с соавт. (2002).
Пример 2. Подготовка растительной биомассы, инокулята, агроинфильтрация, сбор продукта
Растения табака были выращены из семян в плоских поддонах, заполненных имеющейся в продаже подложкой из торфяного мха. Растения росли в теплице при световом периоде 16/8 и температурном режиме: 25°С днем/ 20°С ночью. По истечении трех недель после высева семян отдельные ростки были собраны, пересажены в горшочки и оставлены расти в теплице еще три недели при тех же условиях окружающей среды.
Штаммы агробактерий R612, R610, R621, R622 или 35S HcPro были выращены в среде YEB, дополненной 10 мМ 2-[N-морфолино]этансульфоновой (МЭС) кислоты, 20 мкМ ацетосирингона, 50 мкг/мл канамицина и 25 мкг/мл карбенициллина, рН 5,6, до момента, когда они достигают плотности клеток OD600 в пределах от 0,6 до 1,6. Перед использованием взвеси агробактерий подвергались центрифугованию, а затем были ресуспендированы в среде инфильтрата (10 мМ MgCl2 и 10 мМ МЭС, рН 5,6).
Инфильтрация при помощи шприца была выполнена, как описано Liu и Lomonossoff (2002, Journal of Virological Methods, 105: 343-348)
Для инфильтрации под вакуумом взвеси бактерий A, tumefaciens подвергались центрифугованию, были ресуспендированы в среде инфильтрата и помещены на хранение ночью при температуре 4°С. В день выполнения инфильтрации образцы культур были разбавлены до 2,5 объемов культуры, а затем подогревались перед использованием. Все растения табака были помещены на 2 минуты в перевернутом положении (вверх корнями) во взвесь с бактериями в герметичном резервуаре из нержавеющей стали под вакуумом 20-40 Торр. После выполнения инфильтрации при помощи шприца или под вакуумом растения возвращали в теплицу на период инкубирования в течение 4-5 дней перед сбором урожая.
Отбор листьев и полное извлечение белка
Вслед за инкубацией надземная часть растений была собрана, заморожена при температуре -80°С, раздроблена на кусочки и разделены на части массой от 1,5 до 7,5 грамм. Общий растворимый белок был извлечен методом гомогенизации (Политрон) каждой части замороженного и раздробленного растительного материала в трех объемах холодных 50 мМ Трис-растворе рН 7,4, 0,15 М NaCl, 0,1% Тритон Х-100, 1 мМ фенилметансульфонилфторида и 10 мкМ химостатина. После гемогенизирования кашица была подвергнута центрифугованию на уровне 20000 об/мин в течение 20 минут при 4°С, очищенный суммарный экстракт (супернатант) сохранялся для анализа. Общее содержание белка в очищенном суммарном экстракте было определено при помощи анализа Брэдфорда (Bio-Red, Hercules, CA) с использованием альбумина бычьей сыворотки в качестве стандартного образца.
Пример 3. Анализ белка, иммуноблотинг и ELISA (иммуноферментный анализ)
С5-1 - это антииммуноглобулин человека/мыши, поэтому его обнаружение и количественный анализ могут быть выполнены путем использования либо его аффинности (сродства) с ИгГ человека (блот-анализ активности), либо его иммунореактивности относительно антииммуноглобулина мыши.
Белок из полных суммарных экстрактов или очищенное антитело были отделены при помощи SDS PAGE и либо окрашен по классу «Кумасси-синий» R-250 или G-250, либо электроперенесен на мембраны из поливенилен-фторида (Roche Diagnostics Corporation, Indianopolos, IN) для иммунодетекции. Перед проведением иммуноблотинга мембраны были блокированы 5% снятым молоком и 0,1% Tween-20 в Трис-буферном растворе солей (TBS-T) в течение 16-18 ч при 4°С.
Иммуноблотинг выполнялся путем инкубирования при помощи следующих антител: конъюгированное с пероксидазой антитело K03S против ИгГ мыши (H+L) (Jackson ImmunoResearch, West Grove, PA, Cat# 115-035-146) (0,04 мкг/мл в 2% снятом молоке в растворе TBS-T), конъюгированное с пероксидазой антитело ИгГ из биоматериала человека (Gumunex ® Bayer Corp., Elkart, IN) (0,2 мкг/мл в 2% снятом молоке в растворе TBS-T) или поликлональное козье антитело против иммуноглобулина мыши (специфичное к тяжелой цепи) (Sigma-Aldrich, St-Louis, МО) (0,25 мкг/мл в 2% снятом молоке в растворе TBS-T). Конъюгированное с пероксидазой антитело из биоматериала осла против иммуноглобулина Г из биоматериала козы (Jackson ImmunoResearch) (0,04 мкг/мл в 2% снятом молоке в растворе TBS-T) было использовано как вспомогательное антитело для мембран, обработанных антителом, специфичным к тяжелой цепи. Иммунореактивные комплексы были обнаружены при помощи хемилюминесценции с использованием люминола в качестве субстрата (Roche Diagnostics Corporation). Конъюгирование с пероксидазой-энзимом хрена антитела ИгГ из биоматериала человека было выполнено с использованием набора конъюгирования с EZ-Link Plus ® - активированной пероксидазой (Pierce, Rockford, IL).
Количественный анализ ELISA (иммуноферментный анализ)
Многолуночные планшеты (Immunol 2HB, ThermoLab System, Franklin, MA) были покрыты 2,5 мкг/мл антитела козы против ИгГ мыши, специфичного тяжелой цепью ИгГ (Sigma M8770), в 50 мМ карбонатного буфера (рН 9,0) при 4°С в течение 16-18 ч. Затем многолуночные планшеты были блокированы посредством одночасовой инкубации в 1% казеине в солевом растворе с фосфатным буфером (PBS) (Pierce Biotechnology, Rockford, II) при 37°С. Была построена калибровочная кривая контроля титрования растворов очищенного ИгГ1 мыши (Sigma M9269). При выполнении иммуноанализов разбавления (контрольные и проб) осуществлялись в растительном экстракте, полученном из растительной ткани, инфильтрированной и инкубированной с ложным инокуломом так, чтобы исключить любое воздействие матрицы. Планшет был инкубирован с образцами белка с выполнением калибровочной кривой титрования в течение одного часа при 37°С. После трех промываний 0,1% Tween-20 в растворе PBS (PBS-Т) планшеты были инкубированы с конъюгированным с пероксидазой антителом козы против иммуноглобулина мыши Г (H+L) (Jackson ImmunoResearch, 115-035-146) (0,04 мкг/мл) в течение одного часа при 37°С. Промывания раствором PBS были повторены, и планшеты были инкубированы с подложкой 3,3'. 5,5'-тетраметилбензидина (ТМБ) Sure Blue пироксидазы (KPL, Gaithersburg, MD). Реакция была остановлена добавлением IN HC1, а поглощение было считано при 450 нм. Каждый образец был трижды проанализирован, и концентрации были интерполированы на прямолинейный участок калибровочной кривой.
Пример 4. Очистка ИгГ
Очистка С5-1 от остатков листьев включала отбор замороженных листьев табака N. benthamiana (100-150 г), добавление 20 мМ фосфата натрия, 150 мМ NaCl и 2 мМ пиросульфита натрия при рН 5,8-6,0, а также их смешивание при помощи доступного в продаже блендера в течение 2-3 минут при комнатной температуре. Нерастворимые волокна удалялись путем грубой фильтрации на материале Miracloth (Calbiochem, San Diego, CA), а затем к фильтрату были добавлены 10 мМ фенилметансульфонил фторида (ФМСФ). Экстракт был доведен до рН 4,8±0,1 добавлением 1 М HCL и осветлен путем центрифугованием со скоростью 18000 об/мин в течение 15 минут при 2-8°С. Осветленный супернатант был доведен до рН 8,0±0,1 добавлением 2 М раствора TRIS (гидроксиметиламинометана), снова осветлен путем центрифугованием со скоростью 18000 об/мин в течение 15 минут при 2-8°С, а затем отфильтрован на последовательно установленных мембранах 0,8 и 0,2 мкм (Pall Corporation, Canada). Отфильтрованный материал был подвергнут концентрированию посредством проточной фильтрации в направлении потока с использованием ультрафильтрационной мембраны, имеющей эффективную площадь 0,2 кв. фута, и улавливающей частицы с молекулярным весом 100 кДа (GE Healthcare Biosciences, Canada) с целью уменьшения объема осветленного материала в 5-10 раз. Концентрированные образцы были применены к колонках, размерами 5 мм x 5 см и объемом 1 мл, с быстрым потоком сефарозы G белка (Sigma-Aldrich, St-Louis, МО, Cat. # Р4691). Колонку промывали 5 раз в полном ее объеме раствором 20 мМ TRIS-HC1, 150 мМ NaCl с рН 7,5. Антитело было извлечено с использованием 100 мМ Глицина с рН 2,9-3,0 и сразу же доведен до нейтрального значения рН путем сбора в трубочки, содержащие расчетные объемы раствора 1 М TRIS-HCl с рН 7,5. Объединенные фракции антитела были подвергнуты центрифугованию со скоростью 21000 об/мин в течение 15 минут при 2-8°С и помещены на хранение при -80°С до проведения анализа. Колонка для аффинной хроматографии была очищена и помещена на хранение в соответствии с указаниями изготовителя. Такая хроматографическая среда может быть использована для нескольких операций очистки без значительных изменений характеристик очистки (проведено тестирование до 10 циклов).
Пример 5. Анализ N-гликозилирования
Образцы, содержащие антитело С5-1 (50 мкг), были подвергнуты анализу методом электрофореза в полиакриламидном геле (SDS-PAGE). Тяжелая и легкая цепи были выявлены методом окрашивания по классу «Кумасси-синий», а область локализации белка, соответствующая тяжелой цепи была извлечена и разделена на мелкие фрагменты. Фрагменты были промыты трижды 600 мкл раствора 0,1 М NH4HCO3/CH3CN каждый раз в течение 15 минут с последующей сушкой.
Уменьшение дисульфидных связей произошло путем инкубирования остатков геля в 600 мкл раствора 0,1 М ДДТ в 0,1 М NH4HCO3 при 56°С в течение 45 минут. Алкилирование осуществлялось добавлением 600 мкл раствора йодоацетамида 55 мМ в 0,1 М NH4HCO3 при комнатной температуре в течение 30 минут. Супернатанты были удалены, а полиамидные остатки были смыты в еще раз в растворе NH4HCO3 0,1 M/CH3CN (1/1).
Затем белки были обработаны с использованием 7,5 мкг трипсина (Promega) в 600 мкл 0,05 М NH4HCO3 при 37°С в течение 16 часов. Были добавлены 200 мкл CH3CN, и был собран супернатант. После этого остатки геля были смыты с использованием 200 мкл 0,1 М NH4HCO3/CH3CN, затем с использованием 200 мкл CH3CN еще раз, и, наконец, с использованием 5% муравьиной кислоты. Супернатанты были объединены и лиофилизированы
Сепарация пептидов путем ВЭЖХ выполнялась на колонке с обращенной фазой С 18 (4,5x250 мм) с линейным градиентом CH3CN в 0,1% ТФА. Фракции были собраны и лиофилизированы, а затем проанализированы при помощи MALDI-TOF масс-спектрометрии на приборе Voyager DE-Pro MALDI-TOF (Applied Biosystems, USA), оборудованном 337-мм азотным лазером. Масс-спектрометрия была выполнена в режиме замедленной экстракции рефлектора с использованием в качестве матрицы альфа-циано-4-гидроксицинамнной кислоты (Sigma-Aldrich).
Пример 6. Количественный анализ транзиентной экспрессии ИгГ в агроинфильтрованных листьях табака Nicotiana benthaniana
Для тестовой проверки способности прочных, базирующихся на пластоцианине полигенных экспрессирующих кластеров управлять большим накоплением полностью собранных ИгГ кодирующие последовательности легкой и тяжелой цепей антитела С5-1 иммуноглобулины мыши против ИгГ человека (Khoudi с соавт., 1997) были собраны в тандемные конструкции, расположенные ниже промотора пластоцианина и 5' нетранслированных последовательностей и ограниченные по бокам 3' нетранслированными и терминирующими транскрипцию последовательностями на одном и том же сегменте Т-ДНК бинарной плазмиде pCambia, как показано на фиг.1.
В обоих полигенных экспрессирующих кластерах R612 и R610 (см. Пример 1) последовательности, кодирующие легкую и тяжелую цепи, содержали нативные сигнальные пептиды из С5-1 (Khoudi с соавт., 1999), однако, в R610 кодирующая последовательность пептида KDEL была присоединена на С-конце тяжелой цепи для ограничения собранного ИгГ к аппарату Гольджи.
Вслед за шагами клонирования и переноса плазмид в агробактериях Agrobacterium tumefaciens (AGL1) каждый лист трех растений табака Nicotiana benthamiana был инфильтрован при помощи шприца штаммами Agrobacterium tumefaciens, трансформированными с плазмидами R612 и R610, и инкубирован в тепличных условиях на 6 дней перед проведением анализа, как это описано в Примере 2. После инкубационного периода листья каждого растения (примерно 20 г биомассы) были заморожены, измельчены, а замороженный порошок был перемешен с целью образования однородного образца, из которого две части, массой 1,5 г, были взяты для экстракции (от каждого растения, Пример 3). Содержимое в С5-1 было проанализировано на количество экстрактов суммарного белка из каждого образца при помощи твердофазного иммуноферментного анализа (ELISA) тяжелой цепи поликлонального иммуноглобулина козы против ИгП мыши для захвата и конъюгированный с пероксидазой козий иммуноглобулин против ИгГ мыши (H+L) для обнаружения (см. Пример 3).
Как показано на фиг.2, агроинфильтрация R512 привела к накоплению 106 мг антитела на 1 кг сырой массы, в то время как ЭР-удержанная форма антитела (R610) достигла 211 мг/кг сырой массы в одинаковых условиях.
Поскольку посттранскрипционный сайленсинг генов (ПТСГ) был показан для ограничения экспрессии трансгенов в агроинфильтрованных растениях табака Nicotiana benthamiana, а также для демонстрации противодействия коэкспрессии суппрессора сайленсинга HcPro из вируса картофеля Y противодействовала специфичному разрушению трансгена иРНК (Brigneti с соавт., 1998), коинфильтрация конструкции HcPro (Hamilton с соавт., 2002) была проверена на эффективность при увеличенной экспрессией С5-1. Коэкспрессия R612 и R610 с HcPro увеличила уровни накопления в 5,3 и 3,6 раза, соответственно, по сравнению с тем, что наблюдалось в отсутствии HcPro. В случае присутствия HcPro, контролируемая пластоцинином экспрессия С5-1 достигла средних значений 558 мг/кг сырой массы с R612 и 757 мг/кг сырой массы с R610 (фиг.2). Максимальные уровни экспрессии С5-1 превысили 1,5 г/кг сырой массы (25% суммарного растворимого белка) в некоторых формах листьев, инфильтрованных как R612, так и R610.
Для оценки масштабируемости системы экспрессии после агроинфильтрации накопление С5-1 было подвергнуто количественному анализу после проведения процедуры инфильтрации под вакуумом, заимствованной от Kapila с соавт. (1997). В этой серии экспериментов надземная часть всех растений была инфильтрована под вакуумом с использованием R612+HcPro или R610+HcPro, после этого растения возвратили в теплицу на 6 дней до сбора урожая. С целью обеспечения данных для получения представления о крупномасштабной системе производства, партии листьев/стебельков массой примерно 250 г от нескольких растений были заморожены, измельчены в однородные образцы, и три части по 7,5 г материала на каждую партию были отобраны для анализа. Как показали результаты иммуноферментного анализа (ELISA), средние уровни накопления С5-1 достигали 238 и 328 мг/кг сырой массы для инфильтраций с использованием R612 и R610 соответственно (фиг.2).
Пример 7. Характеристика полученного антитела
Блот-анализы белка (см. Пример 3) были использованы для выявления уровня сборки и фрагментирования антитела С5-1 ИгГ в растениях, продуцирующих секретируемую (R612) и ЭР-удерживающую (R610) формы белка в результате проведения экспериментов с применением вакуумной инфильтрации и введением в образцы шприцем. Вестерн блотинг с зондированием при помощи H+L конъюгированного с пероксидазой иммуноглобулина козы против ИгГ мыши был в первую очередь использован для выявления наличия максимального количества фрагментов антитела, независимо от их происхождения, на молекуле С5-1. Как показано на фиг.3А, все экстракты белка содержали фрагменты одинакового молекулярного размера и имели одинаковую относительную распространенность независимо от стратегии внутриклеточного указания целей или используемого способа инфильтрацию. В каждом случае большая группа (>85%), соответствующая полному антителу при примерно 150 кДа, была отображена с двумя малыми группами при молекулярной массе примерно 135 кДа и примерно 100 кДа, указывая на то, что антитело аккумулировалось в его полностью собранной форме (H2L2). Интересно отметить, что фрагменты одинаковой электрофорезной подвижности также присутствовали в контрольном ИгГ1, рафинированном из линии опухолевых клеток мыши (МОРС-21; Sigma #M9269), при предположении, что фрагменты, продуцированные в растении, и линия клеток млекопитающих были идентичны и, возможно, возникли в результате общей протеолитической активности. Аналогичные результаты были получены при использовании анти-антитела мыши, специфичного наличием тяжелой цепи, для детекции.
Для проверки идентичности фрагментов антитела, присутствующих в экстрактах, был применен блот-анализ их активности, в ходе которого полученные промоканием реплики белков зондируются с использованием конъюгированного с пероксидазой ИгГ1 человека, антиген антитела С5-1. Идентичность полностью собранного антитела массой примерно 150 кДа можно увидеть на фиг.3В. Кроме того, паттерн фрагментации, наблюдавшийся в вестерн блот-анализах, за исключением диапазона с массой 100 кДа (см. фиг.3А), виден в блот-анализах активности (фиг.3В). Без привязки к теории, данный результат дает основание полагать, что фрагмент массой 100 кДа не содержит Fab-областей антитела С5-1, и он может состоять, по крайней мере, частично, из димеров тяжелых цепей, промежуточный продукт цельного антитела.
Пример 8. Очистка антитела и характеристика очищенного продукта
Антитело было очищено от биомассы посредством единственной операции хроматографического анализа аффинности G-белка, а полученный продукт был проанализирован методом SDS-ПААГ (см. Пример 4). Окрашенный по классу «Кумасси» гель на фиг.4а показывает большую группу при молекулярной массе 150 кДа в извлеченной из G-белка фракции. Эта группа представляет более чем 85% очищенного продукта как в секретированной, так и ЭР-удержанной формах, а содержание загрязнений в обеих формах одинаковое (фиг.4А, дорожки 4 и 5). Вестерн блот-анализ с зондированием поликлональным анти-ИгГ мыши показал, что источником большинства загрязнений в рафинированных фракций С5-1 является мышиный ИгГ (данные не показаны). В восстановительных условиях были обнаружены два основных продукта при молекулярной массе примерно 25 кДа и примерно 55 кДа, соответственно, что соответствует молекулярному весу легкой и тяжелой цепей соответственно (фиг.4В, дорожка 2). Тяжелая цепь ЭР-удержанного антитела продемонстрировала более высокую подвижность, чем тяжелая цепь апопластического антитела (фиг.4В, дорожка 3), что интерпретируется как объединенный результат добавления аминокислот последовательности KDEL, присутствующих на С-концах и различий N-гликозилирования из-за удержания в ЭР. На фиг.4С показано, что очищенные антитела (150 кДа) связываются с человеческим ИгГ, как это делают и загрязняющие фрагменты массой 75, 90, 100 и 120 кДа, указывая на присутствие, как минимум, одного Fab-сегмента в этих фрагментах. Присутствие Fab-сегмента во фрагменте массой 100 кДа контрастировало результатом, полученным в ходе анализа суммарного экстракта, в котором группа с массой 100 кДа не связывалась с ИгГ человека. Предполагается, что либо количество содержащих Fab фрагментов, мигрирующих в суммарном экстракте при массе 100 кДа, был слишком мал для обнаружения в ходе указанного блот-анализа активности, либо, что фрагмент, мигрирующий при массе 100 кДа, состоял из двух различных молекул, одна из них, являющаяся димерами тяжелой цепи (без Fab-сегмента), а другая, содержащая области связи с антигеном.
Репродуктивность данной системы по продуцированию антитела была оценена при непосредственном сравнении рафинированных продуктов из двух различных инфильтрованных партий и трех групп особой очистки из каждой партии. Анализ SDS-PAGE с окрашиванием по классу «Кумасси» очищенных групп показал наличие идентичных полосок во всех группах и значительную похожесть относительного распространения (фиг.4D).
Пример 9. Модификация N-гликозилирования антитела коэкспрессией галактозилтрансферазы человека
Для исследования возможности применения транзиентной коэкспрессии для контроля гликозилирования белков, образующихся в процессе транзиентной экспрессии, были приготовлены полигенные экспрессирующие кластеры для пластоцианина, содержащие нативную β1,4 галактозилтрансферазу (GalT). R622 содержала GalT (фиг.5В), а R622 содержала каталитический домен GalT, связанный с CTS доменом N-ацетилглюкозаминил трансферазы (GNTI; GNTIGalT (фиг.5А). CTS домен N-ацетилглюкозаминил трансферазы (GNTI) был выбран в качестве «якоря» мембраны для каталитического домена GalT человека, в то время как GNTI действует на ранней стадии синтеза комплексного N-гликана в ЭР и аппарате цис-Гольджи (Saint-Jore-Dupas с соавт., 2006). Во избежание ограничения теорией, секвестрация активности GalT на ранней стадии созревания белка может выразиться в присоединении β1,4-галактозы на созревающие гликаны и эффективном ингибировании фукозилирования и ксилозилирования ядра. Эти конструкции были коинфильтрованы в растениях при помощи С5-1.
Растение табака Nicotiana benthamiana были подвергнуты инфильтрации (см. Пример 2) с использованием R612 (секретированная форма С5-1), R612+R621 (GNT1GalT) или R612+R622 (GalT) в присутствии HcPro. На фиг.6 показан иммунологический анализ С5-1, очищенного от этих образцов биомассы.
Галактозилирование антитела было определено путем обнаружения аффинности при помощи агглютинина Erithrina cristagali (ECA), конкретно связывающегося с β1,4 галактозой. Как ожидалось, галактоза не обнаруживалась, когда С5-1 экспрессировал в одиночку (R612, фиг.6). Галактозилирование наблюдалось в С5-1, очищенном от коинфильтратов с R512+R622 (GalT), но не от коинфильтратов с R612+R621 (GNTIGalT, фиг.6). Вестерн-блотинг, выполненный с использованием антител анти-α1,3 фукозы, выявил фукозилирование N-гликана на контрольном С5-1, экспрессированный без галактозилтрансферазы. Фукозилирование N-гликана не было обнаружено на антителе коэкспрессированном с GNTIGalT, без относительно к способу агроинфильтрации, в то время как коэкспрессия с нативным GalT не привела к детектируемому уменьшению фукозилирования антитела (фиг.6). Аналогичные результаты были получены с антителами, специфичными к анти-β1,2-ксилозе, что показало полное отсутствие специфичных к ксилозе иммуносигналов на С5-1, коэкспрессированном с GNTIGalT, и их присутствие, когда С5-1 было коэкспрессировано с GalT (фиг.6).
Окрашенный по классу «Кумасси» гель для прямого визуального определения полностью сконструированного ИгГ, а вестерн блот-анализ и блот-анализ активности были выполнены на тех же экстрактах. Основываясь на данных, система экспрессии антитела, как было описано, объемов в 1,5 г/кг сырой массы с более 85% продукта, состоящего из полноразмерного тетрамерного ИгГ, массой примерно 150 кДа, в суммарных экстрактах.
Присоединение KDEL пептида к С-концу тяжелой цепи было ранее применено для увеличения (2-10Х) накопления антитела, содействуя извлечению антитела из аппарата Гольджи с возвратом в ЭР (Schillberg с соавт., 2003). С использованием рассмотренной в настоящем описании системы экспрессии присоединение KDEL пептида к тяжелой цепи удваивало объем С5-1 на выходе, когда не использовался суппрессор сайленсинга HcPro. Различие в объеме С5-1 на выходе в случаях присутствия или отсутствия KDEL пептида было в значительной степени уменьшено, когда HcPro использовался для уменьшения сайленсинга. ЭР-удержание не влияло на качество, поскольку фрагменты, которые наблюдались в суммарных экстрактах из растений, продуцирующих ЭР-удерживаемые и секретируемые формы антитела, имели идентичные размеры и относительное распространение.
Антитело С5-1 было выделено на препаративном ВЭЖХ, а профиль N-гликана триптического гликопептида EEQNFSTER (SEQ ID NO: 13) антитела С5-1 был подвергнут анализу при помощи MALDI-TOF масс-спектрометрии. Как показано на фиг.7А, во время экспрессии С5-1 в одиночку, его популяция N-гликанов была представлена в основном комплексными формами, включая ионы, состоящие из фукозилированных и ксилозилированных олигосахаридов, как это происходили во время наблюдения стабильности экспрессии (Bardor с соавт., 2003). Наличие незрелых ЭР-специфичных гликанов, например, Man-8 и Man-9 может быть связано с фракцией белков "en route", как ранее докладывалось в отчетах в отношении антител, полученных из растений путем транзиентной экспрессии (Sriraman, с соавт., 2004).
Коэкспрессия С5-1 с нативным GalT привела к значительной модификации структуры N-гликана, несмотря на то, что ионы, соответствующие высокоманнозным N-гликанам, оставались в избытке. Основная часть комплексных фукозилированных и ксилозилированных N-гликанов (J) исчезла, и были обнаружены новые, частично галактозилированные олигосахариды, некоторые из них расположились как в специфичных для растения созреваниях, так и удлинение галактозы, например, GalGlcNAcMan3(Xy)GlcNAc2 (фиг.7В). Тем самым было продемонстрировано, что коэкспрессия С5-1 с человеческой р1,4 галактозилтрансферазой вызвала эффективную глико-инженерию получения антитела из растений.
Коэкспрессия С5-1 с GNTIGalT выдала на выходе очищенный препарат С5-1, в котором N-гликозилирование значительно отличалось от того, что было продемонстрировано GalT/C5-1. Как показано на фиг.7С, галактозилированные и негалактозилированные гибриды (GalGlcNAcMan5GlcNAc2 (K) и GalGlcNAcMan5GlcNAc2 (G) присутствовали совместно с N-гликанами незрелой олигоманнозы. Без необходимости привязки к теории, как предполагается Bakker, с соавт. (2006), GalGlcNAcMan5GlcNAc2 (G) и Man5GlcNAc2 (В) могут быть фрагментами, полученными в результате разрушения гибрида GalGlcNAcMan5GlcNAc2 эндогенными гликозидазами, а не промежуточными видами зрелой формации N-гликана. Эффект якоря мембраны GNTI был ошеломляющим, антитело С5-1, рафинированное из растений, в которых синтетический энзим GNTIGalT был транзиентно коэкспрессирован с С5-1, не содержало следов (≤99%) гликанов, расположившихся в специфичных для растения α1,3 фукозе и β1,2-ксилозе, демонстрируя, что полная модификация фукозилирования и ксилозилирования была достигнута в ходе транзиентной коэкспрессии.
Все противопоставленные в описании материалы включены в него в виде ссылки.
Описание настоящего изобретения было дано с привлечением одного или более вариантов его осуществления. Однако для специалиста в данной области знаний будет очевидным, что могут быть выполнены различные изменения и модификации изобретения без выхода за пределы объема изобретения, охарактеризованного пунктами формулы изобретения.
Литература
Bakker, H. et al. An antibody produced in tobacco expressing a hybrid beta-1, 4-galactosyltransferase is essentially devoid of plant carbohydrate epitopes. Proc. Natl. Acad. Sci. U.S.A. 103, 7577-7582 (2006).
Boisson, M, et al. Arabidopsis glucosidase I mutants reveal a critical role of N-glycan trimming in seed development. EMBO J. 20, 1010-1019 (2001).
Brigneti, G. et al. Viral pathogenicity determinants are suppressors of transgene silencing in Nicotiana benthamiana. EMBO J. 17, 6739-6746 (1998).
Chua, Y.L., Watson, L.A., & Gray, J.C. The transcriptional enhancer of the pea plastocyanin gene associates with the nuclear matrix and regulates gene expression through histone acetylation. Plant Cell 15, 1468-1479 (2003).
Сох, K.М., et al. Glycan optimization of a human monoclonal antibody in the aquatic plant Lemna minor. Nat. Biotechnol. 24, 1591-1597 (2006).
D'Aoust, M. A. et al. Efficient and reliable production of pharmaceuticals in alfalfa. Molecular Farming, pp 1-12. Rainer Fischer and Stefan Schillberg (eds.), Wiley-VCH, Weinheim, Germany (2004).
Darveau, A., Pelletier, A. & Perreault, J. PCR-mediated synthesis of chimeric molecules. Methods Neurosc. 26, 77-85 (1995).
Elmayan, Т. & Vaucheret, H. Expression of single copies of a strongly expressed 35S transgene can be silenced post-transcriptionally. Plant J. 9, 787-797 (1996).
Fischer, R. et al. Towards molecular farming in the future: transient protein expression in plants. Biotechnol. Appl. Biochem. 30, 113-116 (1999).
Fischer, R., Drossard, J., Commandeur, U., Schillberg, S. & Emans, N. Towards molecular farming in the future: moving from diagnostic protein and antibody production in microbes to plants. Biotechnol. Appl. Biochem. 30, 101-108 (1999).
Giritch, A, et al. Rapid high-yield expression of full-size IgG antibodies in plants coinfected with noncompeting viral vectors. Proc. Natl. Acad. Sci. U.S.A. 103, 14701-14706 (2006).
Gomord, V., Chamberlain, P., Jefferis, R. & Faye, L. Biopharmaceutical production in plants: problems, solutions and opportunities. Trends Biotechnol. 23, 559-565 (2005).
Hamilton, A., Voinnet, 0., Chappell, L. & Baulcombe, D. Two classes of short interfering RNA in RNA silencing. EMBO J. 21, 4671-4679 (2002).
Hiatt, A., Cafferkey, R. & Bowdish, K. Production of antibodies in transgenic plants. Nature 2>42, 76-78 (1989).
Hiatt, A. & Pauly, M. Monoclonal antibodies from plants: a new speed record. Proc. Natl. Acad. Sci. U.S.A. 103,14645-14646 (2006).
Hibino, Y., Ohzeki, H., Sugano, N. & Hiraga, K. Transcription modulation by a rat nuclear scaffold protein, PI30, and a rat highly repetitive DNA component or various types of animal and plant matrix or scaffold attachment regions. Biochem. Biophys. Res. Commun. 279, 282-287 (2000).
Hofgen, R. & Willmitzer, L. Storage of competent cells for Agrobacterium transformation. Nucleic Acid Res. 16, 9877 (1988).
Hull, A. K. et al. Human-derived, plant-produced monoclonal antibody for the treatment of anthrax. Vaccine 23, 2082-2086 (2005).
Kapila, J., De Rycke, R., Van Montagu, M. & Angenon, G. An Agrobacterium- mediated transient gene expression system for intact leaves. Plant Sci. 122, 101-108 (1997).
Kathuria, S.R. et al. Functional recombinant antibodies against human chorionic gonadotropin expressed in plants. Curr. Sci. 82, 1452-1456 (2002).
Ko, K. et al. Function and glycosylation of plant-derived antiviral monoclonal antibody. Proc. Natl. Acad. Sci. U.S.A. 100, 8013-8018 (2003).
Ko, K. & Koprowski, H. Plant biopharming of monoclonal antibodies. Virus Res. Ill, 93-100 (2005).
Koprivova, A. et al. Targeted knockouts of physcomitrella lacking plant-specific immunogenic N-glycans. Plant Biotechnol. J. 2, 517-523 (2004).
Khoudi, H. et al. Production of a diagnostic monoclonal antibody in perennial alfalfa plants. Biotechnol. Bioeng. 64, 135-143 (1999).
Liu, L & Lomonossoff, G.P. Agroinfection as a rapid method for propagating Cowpea mosaic virus-based constructs. J. Virol. Methods 105, 343-348 (2002).
Ma, J. K-C, Drake, P.M.W., Chargelegue, D., Obregon, P. & Prada, A. Antibody processing and engineering in plants, and new strategies for vaccine production. Vaccine 23, 1814-1818 (2005).
Misaki, R., Fujiyama, K. & Seki, T. Expression of human CMP-N-acetylneuraminic acid synthetase and CMP-sialic acid transporter in tobacco suspension-cultured cell. Biochem. Biophys. Res Corn. 339, 1184-1189 (2004).
Paccalet et al. Engineering of a sialic acid synthesis pathway in transgenic plants by expression of bacterial Neu5Ac-synthesizing enzymes. Plant Biotech. J. 5 (2007).
Pagny, S. et al. Protein recycling from the Golgi to the endoplasmic reticulum is very active in plants but has a minor contribution to calreticulin retention. Plant Cell 12, 739-752 (2000).
Pagny, S. et al. Structural requirements for Arabidopsis 61, 2-xylosyltransferase activity and targeting to the Golgi. Plant J. 33, 189-203 (2003).
Peterson, E., Owens, S.M. & Henry, R. L, Monoclonal antibody form and function: manufacturing the right antibodies for treating drug abuse. AAPS J. 8, E383-E390 (2006).
Petrucelli, S. et al. A KDEL-tagged monoclonal antibody is efficiently retained in the endoplasmic reticulum in leaves, but is both partially secreted and sorted to protein storage vacuoles in seeds. Plant Biotechnol. J. 4, 511-527 (2006).
Pwee, K-H. & Gray, J.C. The pea plastocyanin promoter directs cell-specific but not full light-regulated expression in transgenic tobacco plants. Plant J. 3, 437-449 (1993).
Rodriguez, M. et al. Transient expression in tobacco leaves of an aglycosylated recombinant antibody against the epidermal growth factor receptor. Biotechnol. Bioeng. 89, 188-194 (2005).
Rouwendal, G.J.A. et al. Efficient introduction of a bisecting GlnAc residue in tobacco N-glycans by expression of the gene encoding human N-acetylglucosaminyltrasnferase in. Glycobiology 17, 334-344 (2007).
Saint-Jore-Dupas, С.et al. Plant N-glycan processing enzymes employ different targeting mechanisms for their spatial arrangement along the secretory pathway. Plant Cell 18, 3182-3200 (2006).
Sambrook J., and Russell, D.W., Molecular Cloning: A Laboratory Manual. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York. (2001).
Sandhu, J.S., Webster, C.I., & Gray, J.C. А/T-rich sequences act as quantitative enhancers of gene expression in transgenic tobacco and potato plants. Plant Mol. Biol. 37, 885-896 (1998).
Schillberg, S., Fischer, R. & Emans, N. Molecular farming of recombinant antibodies in plants. Cell. Mol. Life Sci. 60, 433-445 (2003).
Sharp, J. M. & Doran, P. M. Characterization of monoclonal antibody fragments produced by plant cells. Biotechnol. Bioeng. 73, 338-346 (2001).
Sriraman, R. et al. Recombinant anti-hCG antibodies retained in the endoplasmic reticulum of transformed plants lack core-xylose and core-a(1-3)-fucose residues. Plant Biotechnol. J. 2, 279-287 (2004).
Strasser, R., Altmann, F., Mach, L., Glossl, J. & Steinkellner, H. Generation of Arabidopsis thaliana plants with complex N-glycans lacking 131, 2 linked xylose and core al, 3-linked fucose. FEBS Lett. 561, 132-136 (2004).
Szittya, G. et al. Low temperature inhibits RNA silencing-mediated defense by the control of siRNA generation. EMBO J. 22, 633-640 (2003).
Verch, Т, Yusibov, V. & Koprowski, H. Expression and assembly of a full-length monoclonal antibody in plants using a plant virus vector. J. Immunol. Methods 220, 69-75 (1998).
Watzele, G., Bachofner, R. & Berger, E.G.. Immunocytochemical localization of the Golgi apparatus using protein-specific antibodies to galactosyltransferase. Eur. J. Cell. Biol. 56, 451-458 (1991).
Yusibov, V., Rabindran, S., Commandeur, U. Twyman, R.M. & Fischer, R. The potential of plant virus vectors for vaccine production. Drugs R.D. 1, 203-217 (2006).
| название | год | авторы | номер документа |
|---|---|---|---|
| Получение вирусоподобной частицы вируса бешенства в растениях | 2012 |
|
RU2655433C2 |
| ХИМЕРНЫЕ ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ, СОДЕРЖАЩИЕ ГЕМАГГЛЮТИНИН, СХОДНЫЕ С ЧАСТИЦАМИ ВИРУСА ГРИППА | 2010 |
|
RU2569195C9 |
| ПОВЫШЕНИЕ ВЫХОДА ВИРУСОПОДОБНЫХ ЧАСТИЦ В РАСТЕНИЯХ | 2012 |
|
RU2682752C2 |
| ПОЛУЧЕНИЕ ВИРУСОПОДОБНЫХ ЧАСТИЦ В РАСТЕНИЯХ | 2011 |
|
RU2655431C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ | 2010 |
|
RU2567012C2 |
| ПОЛУЧЕНИЕ ВИРУСОПОДОБНЫХ ЧАСТИЦ ВИРУСА ГРИППА В РАСТЕНИЯХ | 2014 |
|
RU2742607C1 |
| ИММУНОГЕННЫЙ ЭПИТОП ВИРУСА ГРИППА | 2009 |
|
RU2546872C2 |
| ПОЛУЧЕНИЕ ВИРУСОПОДОБНЫХ ЧАСТИЦ ВИРУСА ГРИППА В РАСТЕНИЯХ | 2014 |
|
RU2705555C2 |
| ПРОДУКЦИЯ ГЛИКОПРОТЕИНОВ С МОДИФИЦИРОВАННЫМ ФУКОЗИЛИРОВАНИЕМ | 2008 |
|
RU2479629C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ РЕКОМБИНАНТНЫХ ГЛИКОПРОТЕИНОВ С МОДИФИЦИРОВАННЫМ ГЛИКОЗИЛИРОВАНИЕМ | 2015 |
|
RU2704830C2 |

















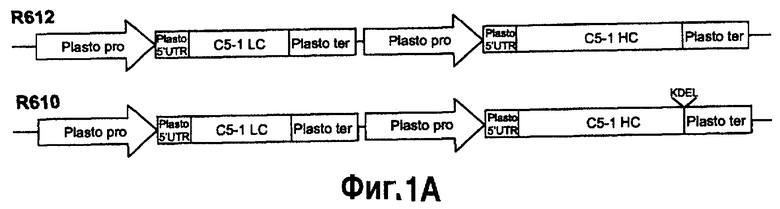

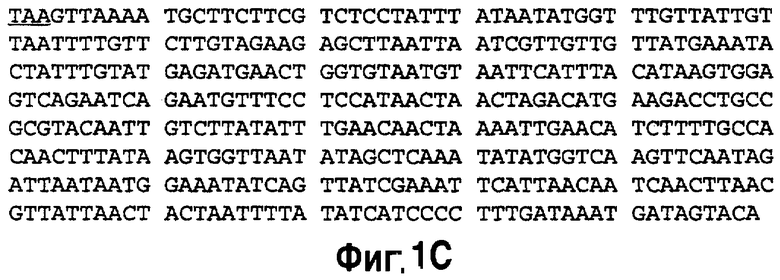
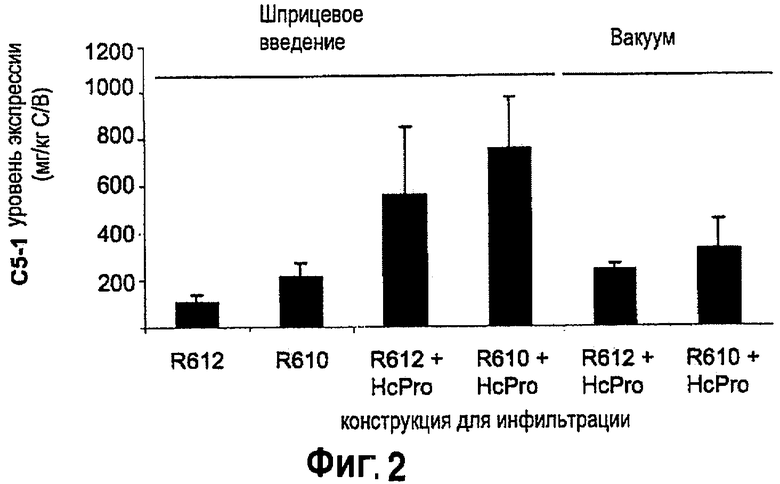
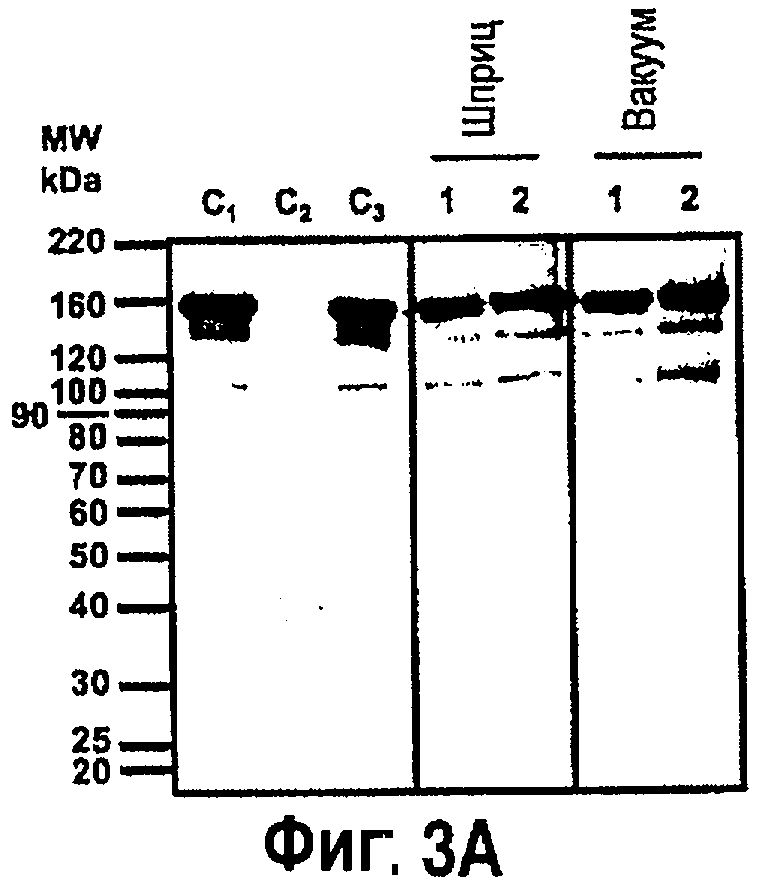
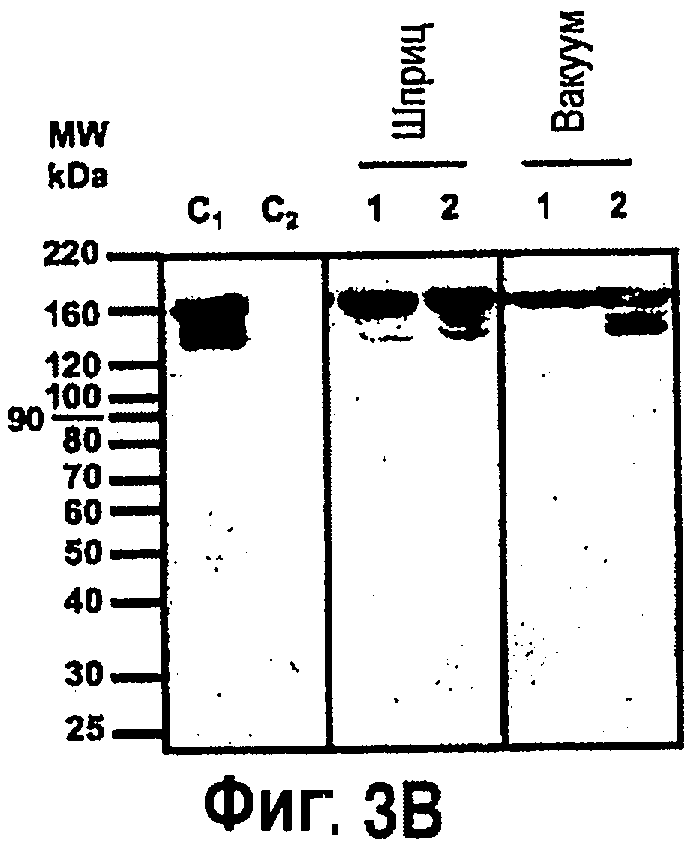
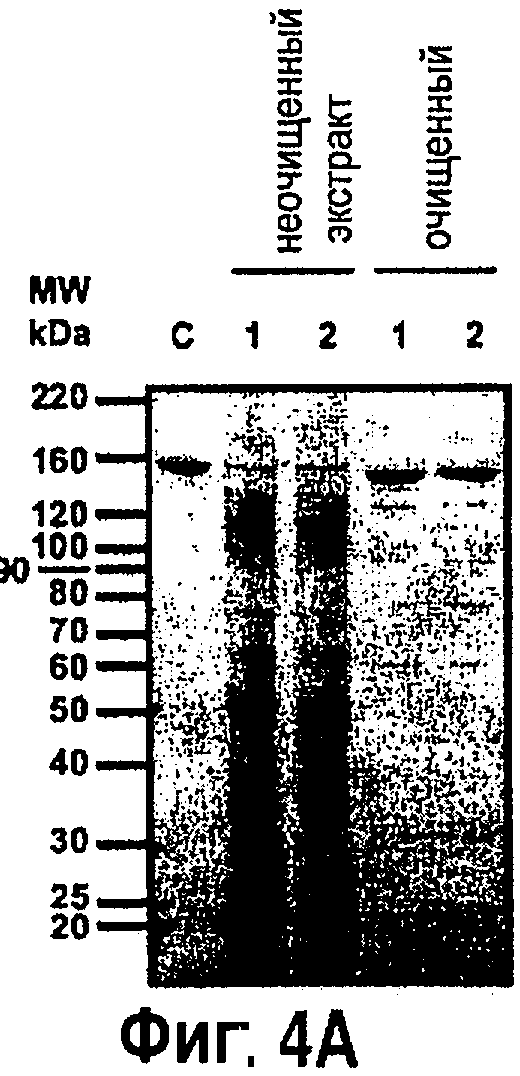

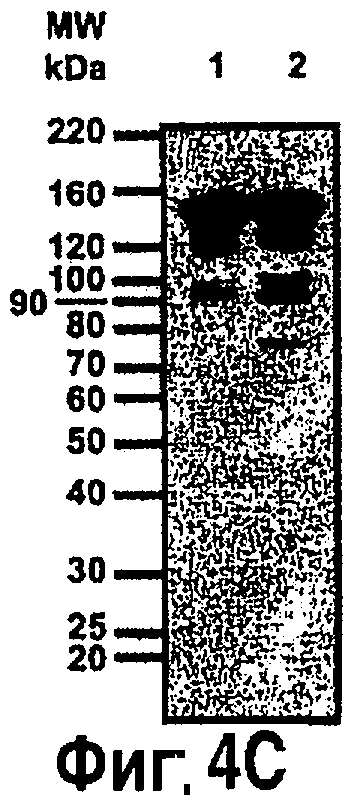
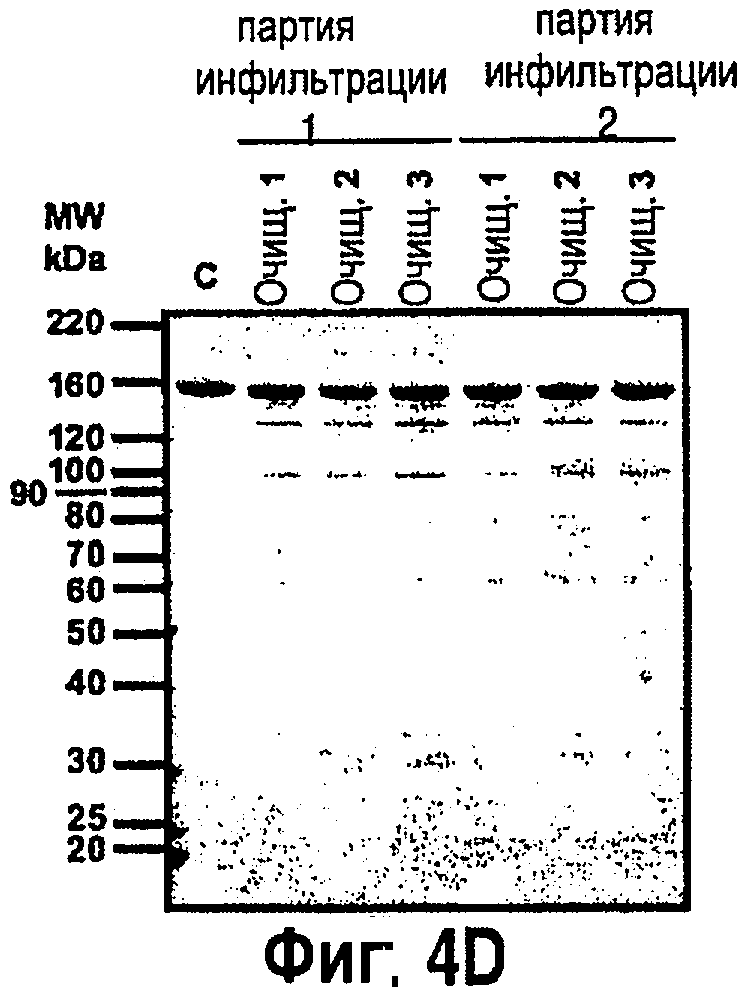
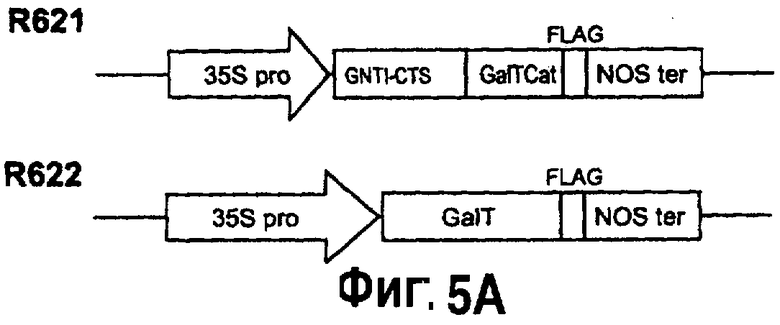
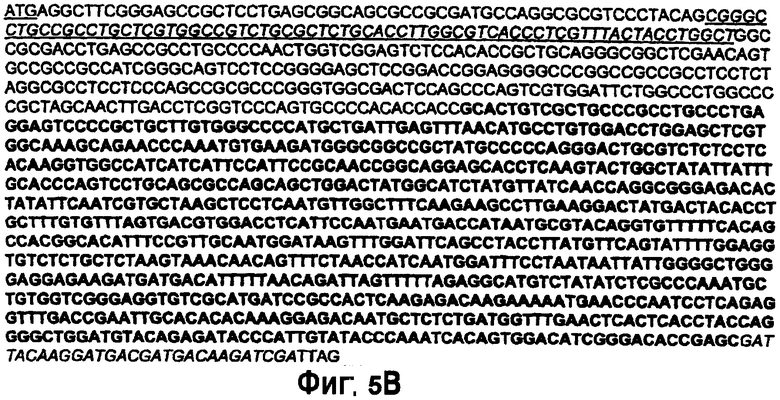

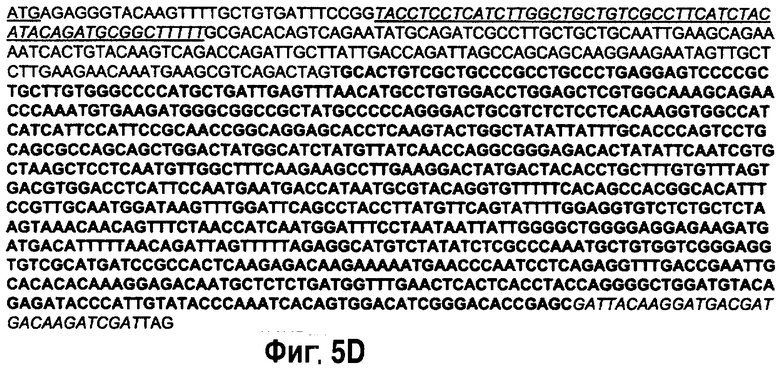



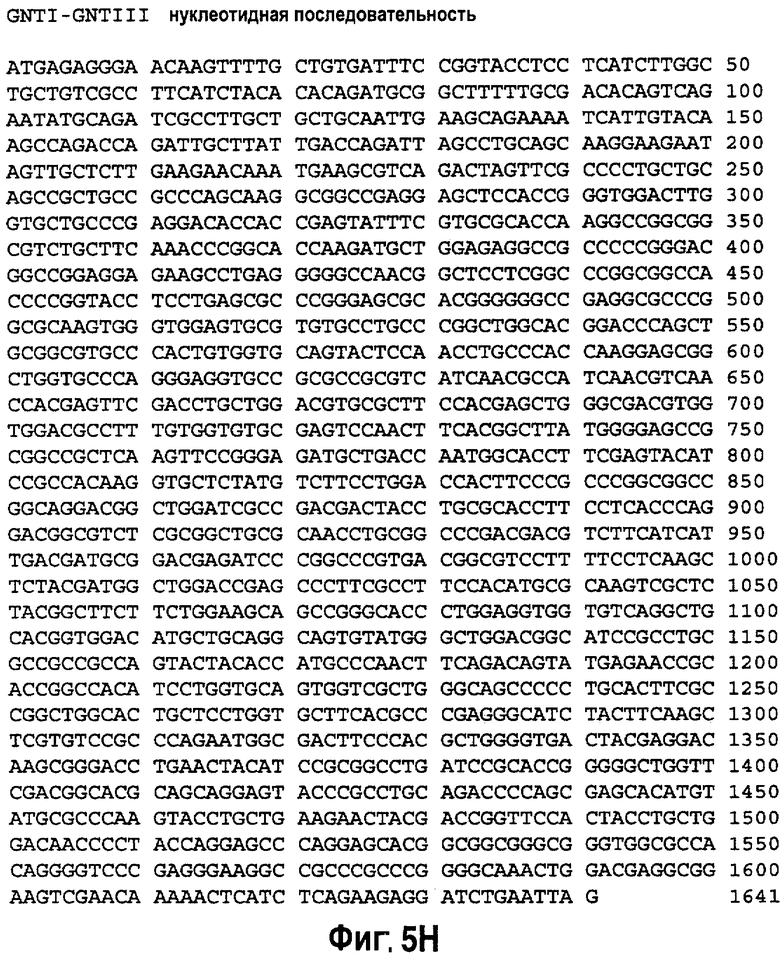


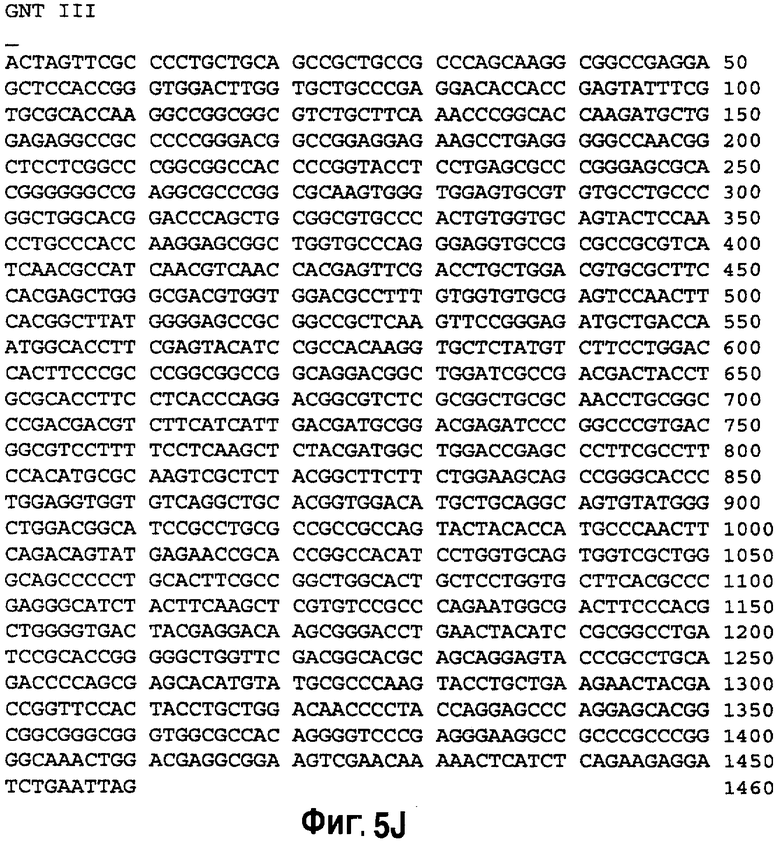
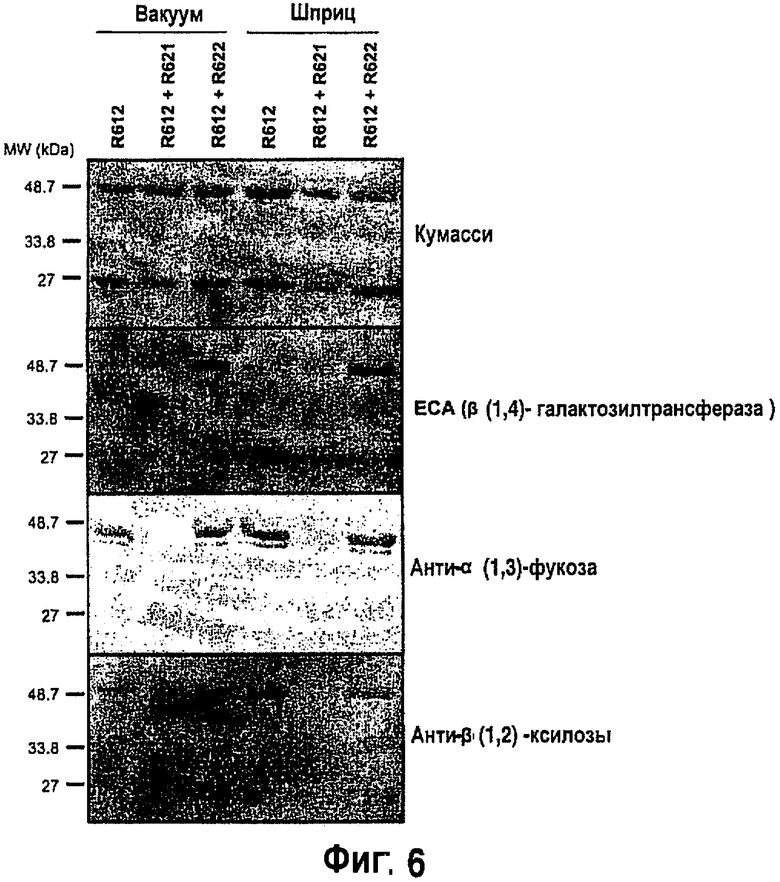
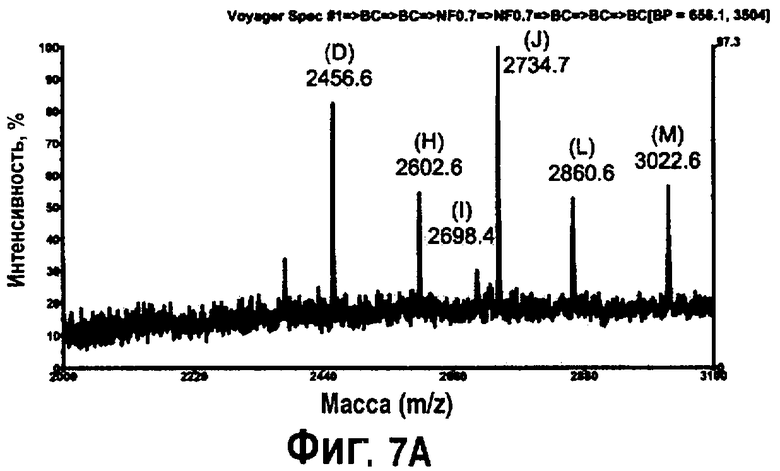
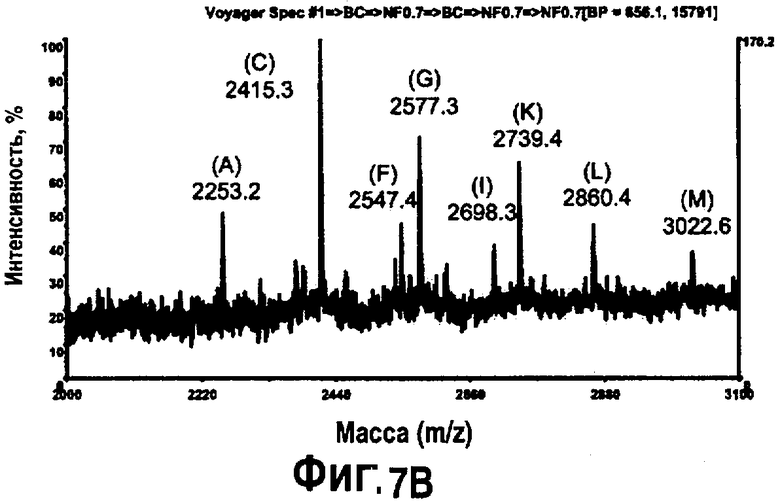
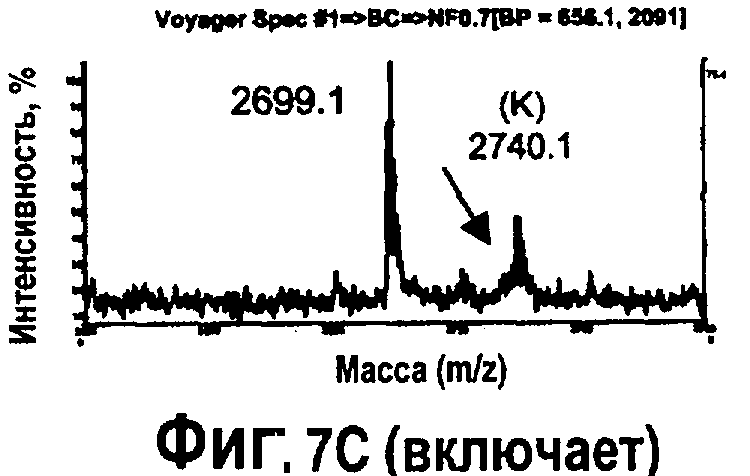
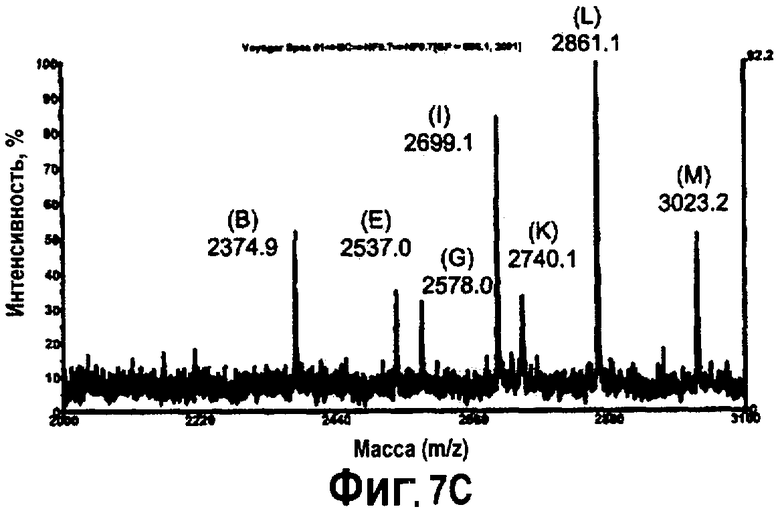
Изобретение относится к области биохимии, в частности к способу синтеза целевого белка с пониженным ксилозилированием, пониженным фукозилированием или их комбинацией. Способ включает в себя введение в растение, часть растения или растительную клетку нуклеотидной последовательности на 80-100 % идентичной нуклеотидной последовательности, определенной в SEQ ID NO: 17, и кодирующей составной белок, содержащий цитоплазматический концевой сегмент, трансмембранный домен, стволовую область (CTS домен) N-ацетилглюкозаминилтрансферазы (GNT1), слитую с каталитическим доменом бета-1,4-галактозилтрансферазы (GalT), причем указанная первая нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении; и второй нуклеотидной последовательностью для кодирования целевого белка, причем указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, а также транзиентную коэкспрессию первой и второй нуклеотидных последовательностей с синтезом целевого белка, содержащего гликаны, с пониженным ксилозилированием, пониженным фукозилированием или их комбинацией при сравнении с таким же целевым белком, полученным из дикого растения. Раскрыты нуклеиновая кислота, кодирующая белок, модифицирующий гликозилирование целевого белка, составной белок для модификации гликозилирования целевого белка, нуклеиновая кислота, его кодирующая, а также растение, растительная клетка и семя, содержащие указанную нуклеиновую кислоту или указанный составной белок. Изобретение позволяет эффективно получать целевой белок с пониженным ксилозилированием, пониженным фукозилированием или их комбинацией. 7 н. и 13 з.п. ф-лы, 7 ил., 9 пр.
1. Способ синтеза целевого белка с пониженным ксилозилированием, пониженным фукозилированием или их комбинацией, включающий в себя введение в растение, часть растения или растительную клетку нуклеотидной последовательности на 80-100 % идентичной нуклеотидной последовательности, определенной в SEQ ID NO: 17, и кодирующей составной белок, содержащий цитоплазматический концевой сегмент, трансмембранный домен, стволовую область (CTS домен) N-ацетилглюкозаминилтрансферазы (GNT1), слитую с каталитическим доменом бета-1,4-галактозилтрансферазы (GalT), причем указанная первая нуклеотидная последовательность функционально связана с первой регуляторной областью, являющейся активной в растении; и второй нуклеотидной последовательности для кодирования целевого белка, причем указанная вторая нуклеотидная последовательность функционально связана со второй регуляторной областью, являющейся активной в растении, а также транзиентную коэкспрессию первой и второй нуклеотидных последовательностей с синтезом целевого белка, содержащего гликаны, с пониженным ксилозилированием, пониженным фукозилированием или их комбинацией при сравнении с таким же целевым белком, полученным из дикого растения.
2. Способ по п.1, в котором первая регуляторная область является первым промотором пластоцианина или первым промотором 35S, а вторая регуляторная область является вторым промотором пластоцианина или вторым промотором 35S.
3. Способ по п.1, в котором дополнительно третья нуклеотидная последовательность вводится в растение, причем третья нуклеотидная последовательность кодирует суппрессор сайленсинга и функционально связана с третьей регуляторной областью, являющейся активной в растении.
4. Способ по п.3, в котором третья регуляторная область является промотором пластоцианина или промотором 35S.
5. Способ по п.2, в котором дополнительно третья нуклеотидная последовательность вводится в растение, причем третья нуклеотидная последовательность кодирует суппрессор сайленсинга и функционально связана с третьей регуляторной областью, являющейся активной в растении.
6. Способ по п.5, в котором третий промотор регуляторной области является промотором пластоцианина или промотором 35S.
7. Способ по п.1, в котором целевой белок - это антитело или антиген.
8. Способ по п.7, в котором вторая нуклеотидная последовательность, кодирующая целевой белок, содержит нуклеотидную последовательность, кодирующую легкую цепь, функционально связанную с регуляторной областью, которая является активной в пределах растения, и нуклеотидную последовательность, кодирующую тяжелую цепь, функционально связанную с регуляторной областью, которая является активной в растении, и продукт нуклеотидной последовательности, кодирующей легкую цепь, и нуклеотидной последовательности, кодирующей тяжелую цепь, объединяются с образованием антитела.
9. Способ по п.8, в котором регуляторная область является промотором пластоцианина.
10. Нуклеиновая кислота, по существу, состоящая из нуклеотидной последовательности с 1 по 1062, представленной в SEQ ID NO: 17 (GNT1-GalT), или, по существу, состоящая из нуклеотидной последовательности, которая демонстрирует от 80 до 100% идентичность с нуклеотидами с 1 по 1062 последовательности SEQ ID NO: 17, и где нуклеотидная последовательность кодирует белок, модифицирующий гликозилирование целевого белка.
11. Составной белок GNT1-GalT, предназначенный для модификации гликозилирования целевого белка, содержащий CTS домен N-ацетилглюкозаминилтрансферазы, слитый с каталитическим доменом бета-1,4-галактозилтрансферазы, причем составной белок содержит аминокислоты с 1 по 354 последовательности SEQ ID NO: 18.
12. Нуклеиновая кислота, кодирующая составной белок по п.11.
13. Растение, предназначенное для экспрессии белка, модифицирующего гликозилирование целевого белка, содержащее нуклеиновую кислоту по пп.10, 12 или белок по п.11.
14. Растительная клетка, предназначенная для экспрессии белка, модифицирующего гликозилирование целевого белка, содержащая нуклеиновую кислоту по пп.10, 12 или белок по п.11.
15. Семя, предназначенное для экспрессии белка, модифицирующего гликозилирование целевого белка, содержащее нуклеиновую кислоту по пп.10, 12 или белок по п.11.
16. Способ по п.3, в котором целевой белок является антителом и синтезирован в количестве вплоть до 1,5 г на килограмм массы необработанных листьев.
17. Способ по п.1, в котором синтезированный целевой белок не является фукозилированным и/или ксилозилированным.
18. Способ по п.1, в котором синтезированный целевой белок является на 5% менее фукозилированным и ксилозилированным по сравнению с таким же белком, полученным в растении дикого типа.
19. Способ по п.1, в котором синтезированный целевой белок является на 2% менее фукозилированным и ксилозилированным по сравнению с таким же белком, полученным в растении дикого типа.
20. Способ по п.1, в котором первая нуклеотидная последовательность включает нуклеотиды 1-1062 последовательности SEQ ID NO: 17 (GNT1-GalT).
| WO 03078637 А2, 25.09.2003 | |||
| WO 2004065540 A2, 05.08.2004 | |||
| US 6998267 В1, 14.02.2006 | |||
| RU 2004106559 A, 10.05.2005. |
Авторы
Даты
2013-11-20—Публикация
2008-06-13—Подача