Изобретение относится к области медицины и может быть использовано при кардиохирургических операциях с изоляцией сердца от задней поверхности грудины.
Известен ряд работ, посвященных послеоперационному спаечному процессу в брюшной полости. Согласно данным по источникам информации у 55-70% пациентов после абдоминального хирургического вмешательства развивается спаечный процесс, который способен привести к такому осложнению, как острая спаечная кишечная непроходимость см. Суфияров И.Ф. Система комплексной интраоперационной профилактики спаечной болезни брюшины: автореферат докторской диссертации. Послеоперационная летальность при неблагоприятном течении острой спаечной кишечной непроходимости достигает 16-25%. см. Спаечная болезнь брюшины / И.А. Чекмазов. М., 2008. С.18.
В кардиохирургии спаечный процесс также является серьезным послеоперационным осложнением, увеличивающим риск повторных операций, госпитальная летальность при которых может достигать 14-15%, а в экстренных случаях 43% см. BauemschmittR. // Interact. Cardiovasc.Sarg. 2007. V.6. S.277.
Изоляция сердца и крупных сосудов от экстраперикардиального спаечного процесса в переднем средостении, который развивается в послеоперационном периоде у больных после стернотомии имеет очень важное значение. Образование спаек является прямым результатом травмы, коагуляции и снижения фибринолитической активности крови. Хирургическая травма париетальной плевры и перикардиального мезотелия приводит к полимеризации фибрина, образованию фибриновых спаек между противоположными поверхностями, снижению фибринолитической активности, которая, в итоге, осложняет рассасывание полимеризованного фибрина и фибриновых спаек. Фибробласты разрастаются и мигрируют к месту вмешательства, перемещаются к фибриновым спайкам, где откладывается коллаген. В результате формируются обширные, плотные спайки в местах соединения противоположных поверхностей. Возможность полного разъединения или полной изоляции сердца от задней поверхности грудины не всегда представляется возможной. Постинфарктный кардиосклероз, дилатация с увеличением диастолического и систолического объемов приводит к расширению полостей сердца, возникает, так называемый, «дефицит перикарда». Возникает это по причине того, что объем сердца занимает значительную часть полости перикарда в норме. Сведение краев перикарда и изоляция зоны операции, без оставления неприкрытого миокарда, с которым впоследствии будет интимно спаяна задняя поверхность грудины весьма сомнительна. Сведение краев перикарда в такой ситуации приводит к сдавлению в первую очередь правых отделов сердца, снижению сердечного выброса, что может привести к неблагоприятным последствиям. В случае неполного разобщения зоны операции от задней поверхности грудины, в спаечный процесс вовлекаются неприкрытый миокард, что значительно увеличивает травматичность рестернотомии и последующего кардиолиза при реоперациях.
Известен способ изоляции легкого при котором используется аутоплевра - собственная плевра пациента, при котором париетальную плевру отслаивают от грудной стенки в виде полосок, и укладывают на линию резекции легкого, далее подшивают к легкому сшивающим аппаратом или ручным швом. Известный способ проведения операции имеет существенный недостаток - после отслаивания париетальной плевры возникает обильное капиллярное кровотечение с грудной стенки. [Мясникова М.Н. Хирургические методы в комплексной терапии эмфиземы легких. // Автореф дисс. д-ра мед. наук. Москва, 1968 - стр.16-17].
Традиционный способ изоляции сердца от задней поверхности грудины на конечных этапах операции перикардом - не всегда выполним. См. «Искусство коронарной хирургии» Ю.В. Белов 2009 г. Часть VI, стр.180-181 - прототип. Известный способ предусматривает изоляцию сердца при помощи сшивания краев собственного перикарда, вверху над аортой с клетчаткой вилочковой железы, в средней части между собой и внизу с диафрагмой.
К недостаткам известного традиционного способа можно отнести частичную изоляцию сердца, приводящую к сращению передней поверхности правого желудочка к задней поверхности грудины и увеличению риска разрыва сердца и крупных сосудов при проведении повторных операций.
Известны различные виды материалов, используемые для закрытия места операции это - тахокомб представляющий собой коллагеновую пластину, покрытую с одной стороны компонентами, способствующими свертыванию крови. Покрывающий слой состоит из высококонцентрированных фибриногена, тромбина и апротинина. На край резецированного легкого укладывают пластины тахокомба, увлажненные физиологическим раствором в течении 3-5 минут происходит адгезия тахокомба к легочной ткани. Тахокомб обладает хорошими гемостатическими свойствами, но и посредственными аэростатическими. Существенным недостатоком тахокомба является формирование в плевральной полости массивного спаечного процесса. [Hollaus, P. The use of Tachocomb in thoracic surgery / P. Hollaus, N. Pridun // J. Cardiovasc. Surg. - 1994. - P.169-170].
Задачей предполагаемого изобретения является разработка способа изоляции сердца от задней поверхности грудины, предупреждение образования спаек и снижения риска повторных операций.
Поставленная изобретением задача достигается сочетанием использования известных признаков, включающих стандартную предоперационную подготовку, инструментальное обследование сердечнососудистой системы, постановку диагноза, рассечение грудины, передней поверхности перикарда в месте соединения правой и левой средостенных частей медиастенальной плевры и проведение операции и новых признаков, заключающихся в том, что в качестве материала для изоляции сердца в переднем средостении от задней поверхности грудины в условиях дефицита перикарда используют медиастенальную плевру пациента, отпрепарированную от левой средостенной части перикарда, которую частично с двух сторон отделяют вверху от грудинно-перикардиальной связки, внизу вдоль диафрагмального нерва не травмируя его, до середины длинной оси сердца, одной стороной сохраняющей свою целостность и кровоснабжение с диафрагмальной частью медиастенальной плевры, после чего отпрепарированным лоскутом, накрывают сердце и сосуды и накладывают швы с отсеченной грудинно-перикардиальной связкой и с правой средостенной частью перикарда до дифрагмы.
Поверхности рассечения медиастенальной плевры коагулируют режимом «спрей» при помощи коагулятора ERBE ICC 350.
Накладываемые при сшивке плевры швы выполняют с шириной шага в три-четыре сантиметра.
Новизной предложенного способа является использование в качестве материала для изоляции сердца в переднем средостении от задней поверхности грудины в условиях дефицита перикарда собственной медиастенальной плевры пациента, отпрепарированной от левой средостенной части перикарда, которую с двух сторон отделяют вверху от грудинно-перикардиальной связки, внизу вдоль диафрагмального нерва, не травмируя его, до середины длинной оси сердца, с сохранением целостности и кровоснабжения с диафрагмальной частью медиастенальной плевры с диафрагмальной частью медиастенальной плевры, после чего отпрепарированным лоскутом, накрывают сердце и сосуды и накладывают швы последовательно в направлении от края отсеченной грудинно-перикардиальной связки с правой средостенной частью перикарда и вниз до дифрагмы.
Так, сохранение целостности отпрепарированного медиастенального лоскута с диафрагмальной частью медиастенальной плевры позволяет сохранить в лоскуте плевры хорошее кровообращение и высокую приживаемость к операционным поверхностям.
Признаки коагуляции поверхностей рассечения медиастенальной плевры режимом «спрей» при помощи коагулятора ERBE ICC 350 и выполнение накладываемых при сшивке плевры швов с шириной шага в три-четыре сантиметра - являются дополнительными признаками, раскрывающими конкретное выполнение основных признаков способа, которые направлены на достижение поставленной изобретением задачи изоляции сердца от задней поверхности грудины и профилактики плотного сращения сердца с грудиной и предупреждения риска повторных операций.
Согласно проведенного патентно-информационного поиска сочетания известных и новых признаков не обнаружено, следовательно указанное сочетание признаков можно отнести к новому. Указанные признаки не вытекают явным образом из уровня техники и не очевидны для специалиста. Описание предложенного способа с использованием указанных признаков являются промышленно выполнимым.
На фиг.1. показано сердце и крупные сосуды с выделенным лоскутом из медиастенальной плевры.
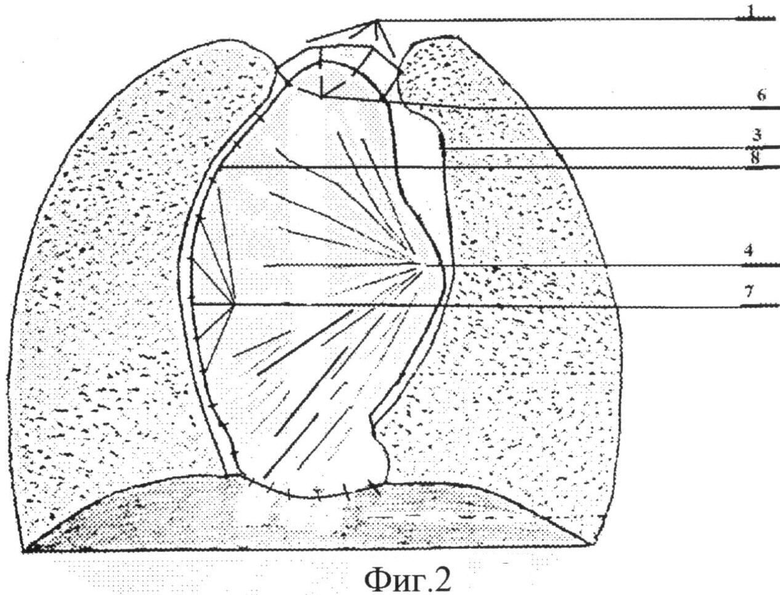
На фиг.2 показан внешний вид изоляции сердца, сосудов и шунтов.
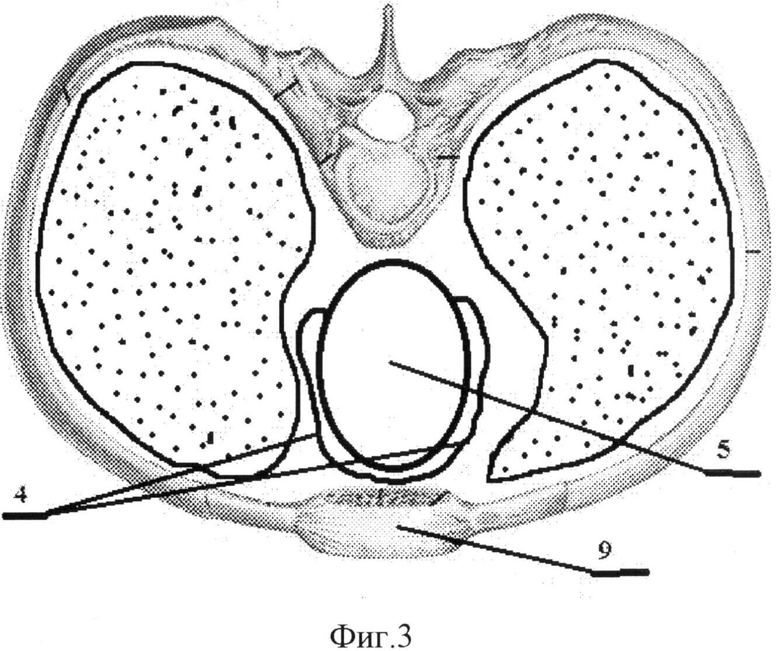
На фиг.3 показано сердце и грудина в поперечном сечении.
На изображенных графических материалах показан отсеченный от грудинно-перикардиальной связки 1 и вдоль левого диафрагмального нерва 2, отпрепарированный от левой средостенной части перикарда 3 лоскут 4 из медиастенальной плевры. Сердце 5 накрывают лоскутом 4 плевры и накладывают швы 6 - с отсеченной грудинно-перикардиальной связкой 1 и 7 - с правой средостенной частью перикарда 8. Между сердцем 5 и грудиной 9 расположен лоскут 4 медиастенальной плевры.
Предлагаемый способ изоляции сердца от задней поверхности грудины проводится в условиях дефицита перикарда и осуществляется следующим образом:
После предоперационной подготовки, заключающейся в инструментальном обследовании сердечно-сосудистой системы, постановке диагноза, больному проводят оперативное лечение в условиях эндотрахеального наркоза. Производят продольное рассечение грудины 9 и перикарда с последующим подключением искусственного кровообращения или без него. После выполнения основного этапа операции включающего, например, протезирование клапана, наложение коронарных шунтов, коррекцию врожденных пороков и др. и восстановления самостоятельной сердечной деятельности, осуществляют изоляцию сердца 5 от задней поверхности грудины 9 путем накрывания сердца 5 и сосудов лоскутом 4 отпрепарированной медиастенальной плевры. При этом тщательным препарированием отделяется медиастенальная плевра от левой средостенной части перикарда 3 и отсекается вверху от грудинно-перикардиальной связки 1 и вдоль левого диафрагмального нерва 2 не травмируя его, преимущественно до середины длинной оси сердца 5. Получается лоскут 4 из медиастенальной плевры, отсеченный с трех сторон, сохраняющий в основании свою целостность и кровоснабжение с диафрагмальной частью медиастенальной плевры. Поверхности отсечения плевры коагулируются режимом «спрей» при помощи коагулятора.
Медиастенальная плевра, имея в своем составе эластичные волокна, имеет свойство к значительному растяжению. Изоляция сердца, крупных сосудов на конечном этапе оперативного лечения начинается с шовной фиксации медиастенальной плевры. Первые швы 6 фиксируют медиастенальный лоскут 4 с отсеченной грудинно-перикардиальной связкой 1. Последующие швы 7 накладываются последовательно - сверху вниз с шириной шага в три-четыре сантиметра с правой средостенной частью перикарда 8. Затем разведенные края грудины 9 сшивают. При этом изоляция сердца 5, крупных сосудов от задней поверхности грудины 9 производится полностью. Сдавление сердца и сосудов не происходит из-за способности медиастенальной плевры к растяжению.
Пример осуществления предлагаемого способа.
Больной М. 54 лет (№ИБ 7815) поступил в Алтайский краевой кардиологический диспансер 22.10.12 г. с диагнозом: Ишемическая болезнь сердца. Стенокардия напряжения 111 ФК. Атеросклероз коронарных сосудов. Принято решение о проведении коронарного шунтирования. 24.10.12 г в условиях искусственного кровообращения произведено маммарокоронарное и аортокоронарное шунтирование с изоляцией сердца медиастенальной плеврой.
После предоперационной подготовки, заключающейся в инструментальном обследовании сердечно-сосудистой системы, постановке диагноза, больному провели эндотрахеальный наркоз. Затем провели продольное рассечение грудины 9 и перикарда и подключили искусственное кровообращение при помощи аппарата Jostra. После выполнения основного этапа операции наложения коронарных шунтов, восстановили самостоятельную сердечную деятельность пациента и осуществили изоляцию сердца 5 от задней поверхности грудины 9 путем накрывания сердца 5 и сосудов лоскутом 4 отпрепарированной медиастенальной плевры. Поверхности отсечения плевры коагулировали режимом «спрей» при помощи коагулятора ERBE ICC 350. Растянутым лоскутом медиастенальной плевры полностью накрыли сердце и крупные сосуды (аорту и легочной ствол) и осуществили сшивание плевры с отсеченной грудинно-перикардиальной связкой вверху, с правой средостенной частью перикарда и диафрагмой. Первые швы 6 зафиксировали медиастенальный лоскут 4 с отсеченной грудинно-перикардиальной связкой 1. Последующие швы 7 фиксировали последовательно - сверху вниз с шириной шага в три-четыре сантиметра с правой средостенной частью перикарда 8. Затем разведенные края грудины 9 сшили. При этом изоляция сердца 5, крупных сосудов от задней поверхности грудины 9 произведена полностью. Сдавления сердца и сосудов медиастенальной плеврой не происходило.
Второй конкретный пример осуществления предлагаемого способа.
Больной Г., 73 лет (№ ИБ 7301) поступил в Алтайский краевой кардиологический диспансер 06.10.12 г. с диагнозом: Ишемическая болезнь сердца. Стенокардия напряжения 111 ФК. Хроническая аневризма левого желудочка. Постинфарктный кардиосклероз (август 2012 г.). Атеросклероз коронарных сосудов. Принято решение о проведении коронарного шунтирования и пластики левого желудочка. 08.10.12 г в условиях искусственного кровообращения произведено маммарокоронарное шунтирование и эндовентрикулопластика левого желудочка с изоляцией сердца медиастенальной плеврой. После предоперационной подготовки, заключающейся в инструментальном обследовании сердечно-сосудистой системы, постановке диагноза, больному провели эндотрахеальный наркоз. Затем провели продольное рассечение грудины 9 и перикарда и подключили искусственное кровообращение при помощи аппарата Jostra. После выполнения основного этапа операции наложения коронарных шунтов и проведения пластики левого желудочка, восстановили самостоятельную сердечную деятельность пациента и осуществили изоляцию сердца 5 от задней поверхности грудины 9 путем накрывания сердца 5 и сосудов лоскутом 4 отпрепарированной медиастенальной плевры. Поверхности отсечения плевры коагулировали режимом «спрей» при помощи коагулятора ERBE ICC 350. Растянутым лоскутом медиастенальной плевры полностью накрыли сердце и крупные сосуды (аорту и легочной ствол) и осуществили сшивание плевры с отсеченной грудинно-перикардиальной связкой вверху, с правой средостенной частью перикарда и диафрагмой. Первые швы 6 зафиксировали медиастенальный лоскут 4 с отсеченной грудинно-перикардиальной связкой 1. Последующие швы 7 фиксировалипоследовательно - сверху вниз с шириной шага в три-четыре сантиметра с правой средостенной частью перикарда 8. Затем разведенные края грудины 9 сшили. При этом изоляция сердца 5, крупных сосудов от задней поверхности грудины 9 произведена полностью. Сдавления сердца и сосудов медиастенальной плеврой не происходило.
С 2006 по ноябрь2012 года, в Алтайском краевом кардиологическом диспансере, с использованием предложенного способа изоляции сердца собственной медиастенальной плеврой пациента, прооперированно 150 больных. Такая изоляция сердца применялась в случае, когда объема собственного перикарда не было достаточно для полного разобщения сердца от задней поверхности грудины.
Использование предлагаемого способа позволяет полностью изолировать сердце, крупные сосуды от экстраперикардиального спаечного процесса, что является ключевым моментом снижения риска реопераций, уменьшения травматичности рестернотомии и последующего кардиолиза с опасностью повреждения различных структур в грудной клетке. Являясь аутогенным материалом медиастенальная плевра исключает использование различных барьерных мембран, являющимися чужеродными для организма человека материалами, способными вызвать нежелательные реакции воспалительного типа. При этом предотвращается деформация аутовенозных и аутоартериальных шунтов, предотвращается нарушение реваскуляризации ишемизированного миокарда. Выделенный из медиастенальной плевры лоскут сохраняет свое кровоснабжение, остается жизнеспособным и не теряет способность плевры к всасыванию жидкости и формированию вновь образованных сосудов с эпикардом. Использование лоскута из собственной медиастенальной плевры пациента оправдано и с экономической точки зрения.
Принято решение предлагаемый способ после проведения экспертизы по существу использовать в практической деятельности кардиохирургическими центрами РФ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ТРАВМЫ СЕРДЦА ПРИ РЕСТЕРНОТОМИИ | 2015 |
|
RU2613079C1 |
| СПОСОБ УШИВАНИЯ ПЕРИКАРДА ПРИ ОПЕРАЦИИ АОРТОКОРОНАРНОГО ШУНТИРОВАНИЯ | 2020 |
|
RU2733505C1 |
| СПОСОБ ОПЕРАТИВНОГО ДОСТУПА КО ВСЕЙ НИСХОДЯЩЕЙ АОРТЕ | 2011 |
|
RU2463970C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ТРАХЕАЛЬНО-ЛЕГОЧНОГО КОМПЛЕКСА В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2541827C1 |
| ОПЕРАЦИОННЫЙ ДОСТУП К ПРОКСИМАЛЬНОМУ ОТДЕЛУ ЖЕЛУДКА ДЛЯ ЕГО РЕЗЕКЦИИ | 2000 |
|
RU2200474C2 |
| СПОСОБ ОПЕРАТИВНОГО ДОСТУПА КО ВСЕЙ АОРТЕ | 2011 |
|
RU2466684C1 |
| Способ мобилизации сердца | 2016 |
|
RU2624815C1 |
| СПОСОБ СОЗДАНИЯ СЕРДЕЧНОЙ СОРОЧКИ В.М. КАМАШЕВА ПОСЛЕ УДАЛЕНИЯ ЛЕВОГО ЛЕГКОГО | 2008 |
|
RU2380044C1 |
| Способ хирургического лечения сердечной недостаточности | 1990 |
|
SU1711844A1 |
| СПОСОБ ОБНАЖЕНИЯ ЗАДНЕГО СРЕДОСТЕНИЯ ПЕРЕДНИМ НАДДИАФРАГМАЛЬНЫМ ВНЕПЛЕВРАЛЬНЫМ ДОСТУПОМ | 1998 |
|
RU2167614C2 |
Изобретение относится к области медицины и может быть использовано в кардиохирургии. Выполняют стандартную предоперационную подготовку, инструментальное обследование сердечно-сосудистой системы. Осуществляют рассечение грудины, передней поверхности перикарда в месте соединения правой и левой средостенных частей медиастенальной плевры для проведения операции на сердце. При этом в качестве материала для изоляции сердца в переднем средостении от задней поверхности грудины в условиях дефицита перикарда используют медиастенальную плевру пациента. Отпрепарированную от левой средостенной части перикарда медиастенальную плевру частично с двух сторон отделяют вверху от грудинно-перикардиальной связки, внизу вдоль диафрагмального нерва, не травмируя его, до середины длинной оси сердца. При этом плевру отсепаровывают таким образом, чтобы с одной стороны она сохранила свою целостность и кровоснабжение с диафрагмальной частью медиастенальной плевры. Затем отпрепарированным лоскутом накрывают сердце и сосуды и накладывают швы последовательно в направлении от края отсеченной грудинно-перикардиальной связки с правой средостенной частью перикарда и вниз до дифрагмы. Способ позволяет полностью изолировать сердце, крупные сосуды и шунты от экстраперикардиального спаечного процесса, что способствует снижению риска реопераций, уменьшению травматичности рестернотомии и последующего кардиолиза с опасностью повреждения различных структур в грудной клетке. 2 з.п.ф-лы, 3 ил., 2 пр.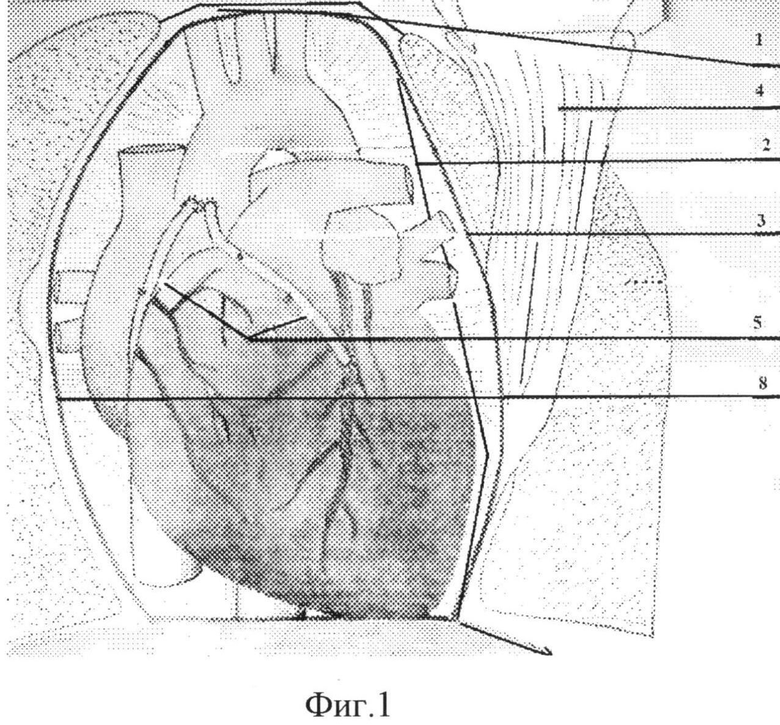
1. Способ изоляции сердца от задней поверхности грудины, включающий стандартную предоперационную подготовку, инструментальное обследование сердечно-сосудистой системы, постановку диагноза, рассечение грудины, передней поверхности перикарда в месте соединения правой и левой средостенных частей медиастенальной плевры и проведение операции, отличающийся тем, что в качестве материала для изоляции сердца в переднем средостении от задней поверхности грудины в условиях дефицита перикарда используют медиастенальную плевру пациента, отпрепарированную от левой средостенной части перикарда, которую частично с двух сторон отделяют вверху от грудинно-перикардиальной связки, внизу вдоль диафрагмального нерва, не травмируя его, до середины длинной оси сердца, одной стороной сохраняющей свою целостность и кровоснабжение с диафрагмальной частью медиастенальной плевры, после чего отпрепарированным лоскутом накрывают сердце и сосуды и накладывают швы с отсеченной грудинно-перикардиальной связкой и с правой средостенной частью перикарда до дифрагмы.
2. Способ по п.1, отличающийся тем, что поверхности рассечения медиастенальной плевры коагулируют режимом «спрей» при помощи коагулятора ERBE ICC 350.
3. Способ по п.1, отличающийся тем, что накладываемые при сшивке плевры швы выполняют с шириной шага в три-четыре сантиметра.
| Белов Ю.В | |||
| Искусство коронарной хирургии, 2009, Часть VI, с.180-181 | |||
| СПОСОБ РЕСТЕРНОТОМИИ ПРИ ПОВТОРНЫХ ОПЕРАЦИЯХ НА ОРГАНАХ ПЕРЕДНЕГО СРЕДОСТЕНИЯ | 2006 |
|
RU2322206C1 |
| КУДРЯВЦЕВА А.Ю | |||
| и др | |||
| Послеоперационные спайки в кардиохирургии: проблемы и решения | |||
| - Патология кровообращения и кардиохирургия, 2011, №1, с.100-104 | |||
| Hollaus, P | |||
| et al, The use of Tachocomb in thoracic surgery, J | |||
| Cardiovasc | |||
| Surg., 1994., - P.169-170. | |||
Авторы
Даты
2014-01-10—Публикация
2012-12-04—Подача