Область техники изобретения
Настоящее изобретение относится к лекарственному средству для лечения окклюзионного и/или ишемического поражения сосудов, особенно окклюзионного заболевания периферических артерий и/или острого расстройства мозгового кровообращения (инсульта). Точнее, изобретение относится к лекарственному средству для лечения окклюзионного заболевания периферических артерий и/или острого расстройства мозгового кровообращения, которое включает производное карбостирила формулы (1):

где А означает низшую алкиленовую группу, R означает циклоалкильную группу, связь между 3- и 4-положениями скелета карбостирила является простой связью или двойной связью, или его соль; и карнитин или его соль.
Уровень техники в данной области
Производные карбостирила формулы (1) или их соли и способы их получения описаны в японских патентах JP-63-20235-B и JP-55-35019-A. Известно, что производные карбостирила (1) проявляют способность ингибировать агрегацию тромбоцитов, ингибировать активность фосфодиэстеразы (PDE), обладают противоязвенной активностью, гипотензивным действием и противовоспалительным действием и являются пригодными в качестве антитромботического средства, лекарственного средства для улучшения мозгового кровообращения, противовоспалительного средства, противоязвенного лекарственного средства, антигипертензивного средства, противоастматического средства, ингибитора фосфодиэстеразы и т.д. Производное карбостирила описанной выше формулы (1), особенно 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил (цилостазол), имеется в продаже, который проявляет эффективность в лечении различных ишемических заболеваний, таких как язва, боль и охлаждение, которые являются симптомами, основанными на хронической окклюзии артерии.
Карнитины также называют витамином ВТ, которые образуются в процессе биосинтеза из незаменимых аминокислот: лизина и метионина в печени/почке. Карнитины могут проникать через клеточные мембраны со сравнительной легкостью, и поэтому они разносятся к любому органу и также выводятся с мочой. Хорошо известными карнитинами являются L-карнитин, хлорид карнитина, хлорид левокарнитина, ацетилкарнитин и т.д. В частности, хлорид левокарнитина имеется в продаже (коммерческое название: L-картин, таблетки), препарат с эффективностью восполняет дефицит левокарнитина при пропионовой ацидемии или метилмалоновой ацидемии, и также показано, что хлорид левокарнитина может быть пригоден для корректировки недостаточности кровообращения в нижних конечностях. Кроме того, L-карнитин также используется в качестве питательного вещества.
Окклюзионное заболевание периферических артерий включает острое окклюзионное заболевание артерий, облитерирующий тромбангиит, облитерирующий атеросклероз, спинальный стеноз поясничного отдела, перемежающуюся хромоту и тому подобное.
Острое окклюзионное заболевание артерий представляет собой заболевание, при котором артерия быстро закупоривается по каким-либо причинам, и симптом заболевания включает внезапную боль, холод, бледность, онемение и т.д.
Облитерирующий тромбангиит представляет собой васкулит в периферической артерии конечности, который часто возникает в ногах, и он известен как болезнь Бюргера, которая является хронической окклюзией артерии. Кроме того, облитерирующий тромбангиит охарактеризован министерством здравоохранения и социального обеспечения Японии как специфическое редкое заболевание.
Облитерирующий атеросклероз является заболеванием, при котором артерия конечности подвергается склерозу с образованием стеноза/окклюзии и, наконец, возникает недостаточность кровообращения.
Спинальный стеноз поясничного отдела является заболеванием, при котором спинномозговой канал поясничного отдела позвоночника сужается по некоторым причинам, и нервная ткань при этом сдавливается.
Перемежающаяся хромота является самым общим симптомом заболевания периферической артерии, которое вызывается постепенным сужением артерии ног. Симптом заболевания включает боль, судорогу и мышечную слабость, которая возникает в регулярные интервалы во время движения. Боль прекращается при остановке и, следовательно, после паузы появляется возможность продолжить ходьбу вновь, однако боль возникает опять при ходьбе на такое же расстояние, как до паузы. Перемежающаяся хромота может часто возникать в результате острого окклюзионного заболевания артерии, облитерирующего тромбангиита, облитерирующего атеросклероза и спинального стеноза поясничного отдела позвоночника.
Причина острого расстройства мозгового кровообращения заключается в том, что какое-либо повреждение, которое случается с кровеносным сосудом головного мозга (кровоток), может привести к последующему кровоизлиянию, вызывающему воспаление/выключение сосудистого русла, или последующей ишемии, вызывающей поражение ткани мозга. Расстройство мозгового кровообращения включает острый церебральный инфаркт, хронический церебральный инфаркт, преходящее ишемическое нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральную гематому, цереброкортикальное расстройство, отмирание черепно-мозговых нервных клеток и т.д. Кроме того, церебральный инфаркт означает, что ткань мозга омертвела или почти омертвела в результате окклюзии/стеноза в артерии и последующей ишемии.
Описание изобретения
Как описано выше, хотя производное карбостирила представленной выше формулы (1) (например, цилостазол как типичное соединение) широко используется в качестве лекарственного средства для лечения окклюзионного заболевания периферических артерий и лекарственного средства, предотвращающего от рецидива церебрального инфаркта, тем не менее авторы настоящего изобретения до сих пор проводят исследования с целью разработать более эффективное лекарственное средство.
Авторы настоящего изобретения тщательно изучали новое лекарственное средство и обнаружили, что комбинация или лекарственная комбинация производного карбостирила представленной выше формулы (1), особенно 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила (цилостазол) или его соли, и карнитина или его соли намного усиливает действие, направленное на лечение окклюзионного заболевания периферических артерий, и на основании полученных результатов настоящее изобретение было выполнено. В частности, заявителями было обнаружено, что комбинация согласно настоящему изобретению может проявлять усиленное действие, благодаря синергическому эффекту, по сравнению с цитостазолом, как единственно вводимым препаратом. Кроме того, было обнаружено, что комбинация или комбинация лекарственных средств является быстродействующей и обладает меньшей токсичностью и, следовательно, может быть введена в течение длительного периода времени. Поэтому, настоящее изобретение относится к пригодному с точки зрения безопасности лекарственному средству для лечения заболевания периферических артерий.
Кроме того, заявители обнаружили, что комбинация или лекарственная комбинация производного карбостирила представленной выше формулы (1), особенно 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила (цилостазол) или его соли, и карнитина и его соли намного усиливает действие, направленное на лечение острого расстройства мозгового кровообращения, и на основании полученных результатов настоящее изобретение было завершено. Авторами настоящего изобретения было обнаружено, что комбинация согласно настоящему изобретению может проявлять усиленное действие, благодаря синергическому эффекту, по сравнению с цитостазолом, как единственно вводимым препаратом. В частности, было найдено, что комбинация или комбинация лекарственных средств может усилить церебропротективную активность путем снижения окислительного стресса, увеличения числа олигодендроцитов и повышения уровня апоптоза, и, следовательно, она может эффективно действовать на проведение лечения острого расстройства мозгового кровообращения. Кроме того, было найдено, что комбинация или комбинация лекарственных средств является быстродействующей, обладает меньшей токсичностью и, следовательно, может быть введена в течение длительного периода времени. Поэтому настоящее изобретение относится к пригодному с точки зрения безопасности лекарственному средству для лечения острого расстройства мозгового кровообращения.
Кроме того, о введении комбинации или комбинации лекарственных средств 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила (цилостазол) или его соли и карнитина или его соли ранее не было известно.
Настоящее изобретение представляет комбинацию, включающую в качестве активных ингредиентов производное карбостирила общей формулы:

где А означает низшую алкиленовую группу, R означает циклоалкильную группу, связь между 3- и 4-положениями скелета карбостирила является простой связью или двойной связью, или его соль; и карнитин или его соль.
Настоящее изобретение также представляет комбинацию, включающую 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил или его соль и карнитин или его соль.
Настоящее изобретение также представляет лекарственное средство для лечения окклюзионного заболевания периферических артерий и/или острого расстройства мозгового кровообращения, включающее производное карбостирила общей формулы:

где А означает низшую алкиленовую группу, R означает циклоалкильную группу, связь между 3- и 4-положениями скелета карбостирила является простой связью или двойной связью, или его соль; и карнитин или его соль в качестве активных ингредиентов.
Настоящее изобретение также представляет лекарственное средство для лечения окклюзионного заболевания периферических артерий и/или острого расстройства мозгового кровообращения, включающее 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил или его соль и карнитин или его соль в качестве активных ингредиентов.
Настоящее изобретение представляет способ лечения окклюзионного заболевания периферических артерий и/или острого расстройства мозгового кровообращения, включающий введение больному по необходимости терапевтически эффективного количества описанной выше комбинации.
Настоящее изобретение относится к использованию описанной выше комбинации для производства лекарственного средства, описанного выше.
Кроме того, настоящее изобретение также представляет описанное выше лекарственное средство или способ, где окклюзионным заболеванием периферических артерий является острое окклюзионное заболевание артерий, облитерирующий тромбангиит, облитерирующий атеросклероз, спинальный стеноз поясничного отдела или перемежающаяся хромота и тому подобное. Кроме того, настоящее изобретение также представляет описанное выше лекарственное средство, где окклюзионным заболеванием периферических артерий является перемежающаяся хромота.
Кроме того, настоящее изобретение также представляет описанное выше лекарственное средство или способ, где острое нарушение мозгового кровообращения включает острый церебральный инфаркт, хронический церебральный инфаркт, преходящее ишемическое нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральную гематому, цереброкортикальное расстройство или отмирание черепно-мозговых нервных клеток.
Настоящее изобретение представляет композицию для лечения заболевания периферических артерий и/или острого расстройства мозгового кровообращения, содержащую комбинацию.
Согласно настоящему изобретению комбинация производного карбостирила (1), особенно 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила, или его соли и карнитина или его соли проявляет эффективное терапевтическое и профилактическое действия в отношении заболевания периферических артерий и эффективное терапевтическое, профилактическое и вторичное профилактическое действия в отношении острого расстройства мозгового кровообращения и, следовательно, имеет широкий спектр церебропротективного действия.
Краткое описание чертежей
На фиг.1 представлены результаты измерения того расстояния, которое крыса пробегает до начала многократного введения лекарственного средства (день 0), и расстояния на день 7, 14, 21 и 28 после начала многократного введения, при этом крысы пробегают по бегущей “дорожке” до появления какого-либо нарушения походки, на которое воздействовали введением цилостазола, L-карнитина и их комбинации. Значок ** означает существенное различие при множественном сравнении методом Бонферрони (<0,01).
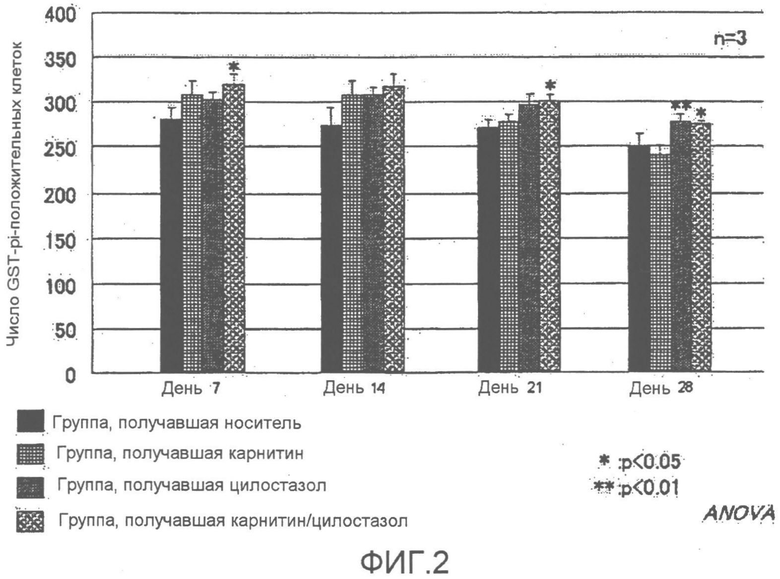
На фиг.2 представлены результаты зависимого от времени изменения числа GST-pi-положительных клеток (GST-pi окрашивание: 0,25 см2) в каждой группе.
На фиг.3 представлены результаты зависимого от времени изменения числа 8-OHdG-положительных клеток (8-OHdG окрашивание) в каждой группе.
На фиг.4 представлены результаты зависимого от времени изменения числа HNE-положительных клеток (HNE окрашивание) в каждой группе.
На фиг.5 представлены результаты зависимого от времени изменения числа ss-DNA-положительных клеток (ss-DNA окрашивание) в каждой группе.
Лучший способ осуществления изобретения
Производным карбостирила, которое включено в комбинацию лекарственных средств или используется в качестве комбинации с карнитином или его солью, является производное тетразолилалкоксидигидрокарбостирила формулы:

где А означает низшую алкиленовую группу, R означает циклоалкильную группу, связь между 3- и 4-положениями скелета карбостирила является простой связью или двойной связью, или его соль.
В описанной выше формуле (1), циклоалкильная группа включает С3-С8 циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Предпочтительной циклоалкильной группой является циклогексил. Низшая алкиленовая группа включает С1-С6 алкиленовые группы, такие как метилен, этилен, пропилен, тетраметилен, бутилен и пентилен, среди которых предпочтительной группой является тетраметилен.
Предпочтительным производным карбостирила является 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил, который был выпущен в продажу под торговым названием цилостазол в качестве антитромбоцитарного средства.
Производное карбостирила (1) может быть легко превращено в его соль путем обработки его фармацевтически приемлемой кислотой. Кислота включает, например, неорганические кислоты, такие как хлористоводородная кислота, серная кислота, фосфорная кислота и бромистоводородная кислота; и органические кислоты, такие как щавелевая кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота и бензойная кислота.
Указанные производные карбостирила (1) и их соли и способы их получения описаны в патенте Японии JP-55-35019-A (имеющем отношение к патенту США 4277479).
Карнитин, являющийся другим активным ингредиентом, включает L-карнитин, хлорид карнитина, хлорид левокарнитина, ацетилкарнитин и тому подобное, особенно L-карнитин и хлорид левокарнитина являются предпочтительными. Карнитин согласно настоящему изобретению может быть легко превращен в солевую форму путем обработки фармацевтически приемлемой кислотой. Кислота включает, например, неорганические кислоты, такие как хлористоводородная кислота, серная кислота, фосфорная кислота и бромистоводородная кислота; и органические кислоты, такие как щавелевая кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота и бензойная кислота.
Активные ингредиенты, указанные выше: производное карбостирила (1) или его соль и карнитин или его соль, могут быть введены вместе или раздельно, в одно и то же время или в разное время. Данные ингредиенты, большей частью, могут быть использованы в стандартной фармацевтической композиции. В таком случае указанные ингредиенты могут быть приготовлены в одной стандартной лекарственной форме или в раздельных дозированных формах.
Лекарственное средство согласно настоящему изобретению, содержащее производное карбостирила представленной выше формулы (1) или его соль и карнитин или его соль, проявляет пригодный терапевтический эффект в отношении окклюзионного заболевания периферических артерий, например острого окклюзионного заболевания артерий, облитерирующего тромбангиита, облитерирующего атеросклероза, спинального стеноза поясничного отдела или перемежающейся хромоты и тому подобное, и особенно проявляет эффективное действие в лечении перемежающейся хромоты.
Лекарственное средство согласно настоящему изобретению, содержащее производное карбостирила представленной выше формулы (1) или его соль и карнитин или его соль, также проявляет пригодный терапевтический эффект в отношении острого расстройства мозгового кровообращения, например острого церебрального инфаркта, хронического церебрального инфаркта, преходящего ишемического нарушения мозгового кровообращения, внутримозгового кровоизлияния, субарахноидального кровоизлияния, субдуральной гематомы, цереброкортикального расстройства или отмирания черепно-мозговых нервных клеток, и, следовательно, указанное лекарственное средство имеет широкий спектр церебропротективного действия.
Острое расстройство мозгового кровообращения (инсульт) включает острый церебральный инфаркт, хронический церебральный инфаркт, преходящее ишемическое нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральную гематому, цереброкортикальное расстройство или отмирание черепно-мозговых нервных клеток и тому подобное. Церебральный инфаркт означает некроз или состояние омертвения ткани мозга по причине окклюзии/стеноза артерии с последующей ишемией. В острой фазе церебрального инфаркта возникает наиболее серьезный симптом и имеется сообщение о том, что предотвращение образования свободного радикала может влиять на улучшение прогноза заболевания. Кроме того, вероятность возврата болезни у персоны, страдавшей от церебрального инфаркта прежде, является высокой. Преходящее ишемическое нарушение мозгового кровообращения представляет собой приступ, который является временно развивающимся локальным проявлением расстройства мозга вследствие сердечно-сосудистой патологии мозга, и поэтому симптом часто может возвращаться в течение несколько минут до нескольких часов. Внутримозговое кровоизлияние означает состояние кровотечения в мозге, вызванное разрывом сосуда по некоторым причинам. Субарахноидальное кровоизлияние вызывается геморрагией в спинномозговую жидкость, и данное заболевание отличается очень высокой смертностью. Субдуральная гематома означает гематому, вызванную скоплением крови в щели между веществом головного мозга и мембраной наружной твердой оболочки мозга, которая прилегает изнутри к костям черепа. Цереброкортикальное расстройство вызывает дисфункцию коры головного мозга, и впоследствии может развиться деменция или когнитивное нарушение. Причиной отмирания черепно-мозговых нервных клеток является амиотрофический боковой склероз (ALS), болезнь Паркинсона, возрастное нарушение функции мозга, такое как болезнь Альцгеймера, и связанное с возрастом ухудшение памяти, а также отмирание черепно-мозговых нервных клеток, возникающее в процессе ишемического церебрального поражения, такого как церебральный инфаркт.
Доза указанных выше активных ингредиентов не ограничивается конкретным диапазоном. Производные карбостирила (1) или их соли могут быть использованы в количестве от 50 до 200 мг/день для взрослого (50 кг массы тела), которое вводится один раз в день или от двух до нескольких раз в день. Карнитин может быть использован в количестве от 500 до 1000 мг/день для взрослого (50 кг массы тела), которое обычно вводят от одного до трех раз в день. В случае приготовления указанных ингредиентов в одной дозированной лекарственной форме, они включены в отношении от 0,1 до 100 частей масс., предпочтительно от 1 до 20 частей масс. карнитина на 1 часть масс. производного карбостирила (1) или его соли. Кроме того, комбинация лекарственных средств может включать сумму ингредиентов в диапазоне 0,1-70% (масс./масс.) на препарат, но не ограничивается указанным диапазоном.
Любая дозированная форма, используемая для комбинации лекарственных средств или комбинации в настоящем изобретении, включает, например, дозированные формы, приведенные в патенте Японии JP-10-175864-A, и, большей частью, включает пероральную твердую дозированную форму, такую как таблетки и капсулы, пероральную жидкую дозированную форму, такую как сиропы и эликсиры, парентеральную дозированную форму, такую как инъекции, и лекарственную форму для ингаляции.
Препараты согласно изобретению, такие как таблетки, капсулы, жидкость для перорального введения, могут быть приготовлены обычными способами. Таблетки могут быть приготовлены смешиванием активного ингредиента(ов) со стандартными фармацевтическими носителями, такими как желатин, крахмалы, лактоза, стеарат магния, тальк, аравийская камедь и тому подобное. Капсулы могут быть приготовлены путем смешивания активного ингредиента(ов) с инертными фармацевтическими наполнителями или разбавителями и наполнения твердых желатиновых капсул или мягких капсул смесью. Пероральные жидкие препараты, такие как сиропы или эликсиры, приготовляют смешиванием активного ингредиента(ов) с подсластителями (например, сахарозой), консервантами (например, метилпарабеном, пропилпарабеном), красителями, ароматизаторами и тому подобное. Препараты для парентерального введения также могут быть приготовлены обычным способом, например путем растворения активного ингредиента(ов) согласно настоящему изобретению в стерилизованном водном носителе, предпочтительно воде или физиологическом растворе. Предпочтительный жидкий препарат, подходящий для парентерального введения, приготовляют путем растворения суточной дозы активных ингредиентов, как описано выше, в воде и органическом растворителе и, кроме того, в полиэтиленгликоле молекулярной массы от 300 до 5000, в который предпочтительно смазывающее вещество, такое как карбоксиметилцеллюлоза натрия, метилцеллюлоза, поливинлпирролидон и поливиниловый спирт, включено. Предпочтительно, когда описанные выше жидкие препараты также могут содержать дезинфицирующее средство (например, бензиловый спирт, фенол, тимеросал), фунгицид и необязательно изотоничное средство (например, сахароза, хлорид натрия), местный анестетик, стабилизирующее средство, буфер и тому подобное. В связи с поддержанием устойчивости препарат для парентерального введения может быть помещен в капсулы с последующим удалением водной среды путем обычной лиофилизации. Препарат может быть превращен в жидкий препарат путем растворения его в водной среде при использовании. Лекарственные формы для ингаляции могут быть приготовлены обычным способом. То есть лекарственные формы для ингаляции могут быть приготовлены путем доведения активного соединения до порошкообразного или жидкого состояния, смешивания его с пропеллантами и/или носителями для ингаляционного средства и заправки соответствующего аэрозольного аппарата смесью. Большей частью, механический порошковый аэрозольный аппарат может быть использован, когда активное соединение представлено в виде порошка, и аэрозольный аппарат, такой как небулайзер, может быть использован, когда соединение находится в жидком состоянии. Кроме того, лекарственная форма для ингаляции необязательно может включать поверхностно-активное вещество, масло, ароматизатор, циклодекстрин или его производное, которые используются по необходимости.
Примеры описанных выше вспомогательных веществ, способов или других деталей включают, но не ограничиваются ими, такие, которые описаны в патенте Японии JP-10-175964-A.
ПРИМЕР
Положительное влияние комбинации цилостазола и L-карнитина на недостаточность кровообращения в конечностях, изученное на модели крыс с перемежающейся хромотой
Положительное влияние на недостаточность кровообращения в конечностях комбинации цилостазола и L-карнитина изучали, достигая усиления положительного влияния комбинации на перемежающуюся хромоту на модели крыс в качестве показательного примера, по сравнению с введением любого одного из обоих лекарственных средств.
Способ
(1) Приготовление раствора лекарственного средства
Цилостазол, представленный Otsuka Pharmaceutical, суспендировали в 5% аравийской камеди так, что концентрация его должна была составлять 6 мг/мл, и затем суспензию цилостазола вводили крысам в количестве 5 мл/кг. L-Карнитин HCl (Sigma) растворяли в очищенной воде так, что концентрация его должна была составлять 300 мг/мл, и затем раствор L-карнитина вводили крысам в количестве 1 мл/кг.
(2) Тестирование на бегущей дорожке
Эксперимент осуществляли согласно методу Orito et al. (J. Pharmacol. Toxicol. Methods 49, 25-29, 2004). То есть крыс самцов SD (возраст 9 недель, SLC) приучали в течение 4 дней постоянно бегать по движущейся дорожке. На 6-й день брюшную полость вскрывали под эфирным наркозом и левую подвздошную артерию перевязывали у дистального сегмента. Через три дня после перевязывания артерии крыс заставляли бегать на движущейся дорожке в течение 4 дней и затем расстояние, которое крысы пробегали до появления какого-либо нарушения походки, измеряли. На основании данных, полученных на последний день (4-й день), когда крыс заставляли бегать по бегущей дорожке, крыс разделяли на следующие четыре группы случайным образом. Крысам в каждой группе было сделано любое определенное многократное введение. Число экспериментальных крыс составляло девять на группу.
1-я группа: пероральное введение (дважды/день) 5% аравийской камеди, 5 мл/кг (контроль).
2-я группа: пероральное введение (дважды/день) цилостазола, 30 мг/кг.
3-я группа: пероральное введение (дважды/день) L-карнитина, 300 мг/кг.
4-я группа: пероральное введение (дважды/день) цилостазола, 30 мг/кг + L-карнитина, 300 мг/кг.
Через три дня после начала введения тестирование на бегущей дорожке постоянно осуществляли в течение 5 дней, и далее только введение было сделано в течение 2 дней. Кроме того, после этого введение и тестирование на бегущей дорожке (непрерывно 5 дней) + только введение (непрерывно 2 дня) повторяли. В итоге опыт был проведен в течение 4 недель полностью. Тестирование на бегущей дорожке было проведено приблизительно через один час после введения, и расстояние, которое крысы пробегали на бегущей дорожке до появления какого-либо нарушения походки, измеряли.
Статистика
В эксперименте использовали крыс до начала многократного введения (день 0) и крыс на дни 7, 14, 21 и 28 после начала многократного введения, расстояние, которое крысы пробегали до появления какого-либо нарушения походки, измеряли, и результаты анализировали относительно разницы между каждой группой согласно множественному сравнению методом Бонферрони. Было установлено по показателю Р<0,05, что результаты показали значимое различие.
Результат и обсуждение
Что касается крыс на дни 0, 7 и 14, значительной разницы между каждой группой не наблюдали. Однако на день 21, расстояние, которое крысы в группе, получавшей комбинацию цилостазол+L-карнитин, пробегали до появления какого-либо нарушения походки, существенно увеличивалось по сравнению с контрольной группой (фиг.1). Кроме того, на день 21 после начала многократного введения расстояние, которое пробегали крысы в группе, получавшей комбинацию лекарственных средств, существенно увеличивалось по сравнению не только с контрольной группой, но также с группой, получавшей только цилостазол, и группой, получавшей только L-карнитин (фиг.1).
Описанные выше результаты свидетельствуют о том, что комбинация цилостазола и L-карнитина может интенсифицировать положительное воздействие на ишемию на/после 21 дня, по меньшей мере, по сравнению с введением только цилостазола.
Полагают, что перемежающаяся хромота вызывается сочетанием метаболического нарушения в мышце конечности и ишемии. Из экспериментальных результатов следует, что карнитин оказывает воздействие на первое, т.е. метаболическое нарушение в мышце конечности, в то время как цилостазол оказывает воздействие на последнее, т.е. на ишемию. Отсюда, полагают, что комбинация указанных двух лекарственных средств оказывает синергическое действие на перемежающуюся хромоту. Особенно следует отметить, что воздействие является синергическим положительным эффектом, который достигается после длительного введения, и, кроме того, эффект оказывается очень сильным и намного большим, чем ожидаемый эффект.
Изучение церебропротективного действия цилостазола на модель животных с хронической ишемией
Церебропротективное действие цилостазола на воспалительную реакцию в результате окислительного стресса и активации глиальной клетки изучали на модели крыс с хронической ишемией мозга в качестве модели животных с деменцией.
Модель крыс с хронической церебральной ишемией получали методом Wakita et al. (Acta Neuropathol. (Berl). 87, 484-492, 1993), используя крыс Wistar (самцы, возраст 7-8 недель, массы тела 150-200 г), т.е. путем двойного перевязывания обеих внутренних сонных артерий крыс. В качестве физиологической оценки температуру тела и жидкость тела крыс до/после получения модели ишемии измеряли и мозговой кровоток оценивали посредством аппарата Доплера. Крысам каждой группы, которым вводили носитель, L-карнитин, цилостазол и комбинацию L-карнитин/цилостазол, любое определенное введение делали каждый день путем естественного проглатывания со дня, когда модель ишемии была готова к исследованию, до последнего дня эксперимента. На дни 7, 14, 21 и 30 после начала ишемии крыс каждой группы, которым вводили указанные выше средства, подвергали перфузии-фиксации 4% PFA и проводили гистологическое (иммуногистологическое) исследование. После того как паренхиму головного мозга крыс разрезали на кусочки размером 20 мкм, осуществляли их окрашивание НЕ и КВ и производили несколько иммуноокрашиваний. Дозировка для каждого испытания составляла 600 мг/кг/день L-карнитина и 50 мг/кг/день цилостазола.
Что касается глиальной клетки, астроцит оценивали посредством антитела к GFAP, и микроглию оценивали посредством антитела к Iba-1, олигодендроцит оценивали посредством антитела к глутатион-S-трансферазе р+ (GST-pi). Кроме того, окислительный стресс оценивали посредством антитела против анти 4-гидрокси-2-ноненаля (HNE).
Каждую группу оценивали методом Morris (227. R.G.M. Morris, Spatial localization does not require the presence of local cues. Learn. Motiv. 12 pp. 239-260, (1981)), который представляет собой количественную оценку пространственной памяти и пространственного обучения.
Результат
Как показано на фиг.2, число GST-pi-положительных олигодендроцитов в мозолистом теле имело тенденцию увеличиваться от дня 7 до дня 14 после перевязывания обеих общих сонных артерий (LBCCA) и количество данных клеток уменьшалось после дня 14. Число олигодендроцитов в группах, получавших карнитин и цилостазол, увеличивалось в большей степени по сравнению с группой, получавшей носитель, особенно группа, получавшая комбинацию карнитин/цилостазол, показала значительную разницу в количестве клеток по сравнению с группой, получавшей носитель, на дни 7 и 21 (Р<0,05).
Как показано на фиг.3, 8-гидроксидезоксигуанозин (8-OHdG)-положительные клетки, которые являются признаком клеточной дисфункции в результате пероксидирования, имели тенденцию к зависимому от времени увеличению числа клеток в группе, получавшей носитель, от дня 7 до дня 28 после LBCCA, в то время как число положительных клеток в каждой из групп, получавших карнитин, цилостазол и комбинацию карнитин/цилостазол, существенно уменьшалось (Р<0,01).
Как показано на фиг.4, при HNE-окрашивании, которое указывает на выход продукции перекисного окисления, число положительных клеток в группах, получавших карнитин, цилостазол и комбинацию карнитин/цилостазол, имело тенденцию существенно уменьшаться по сравнению с группой, получавшей носитель (Р<0,01). На дни 14 и 21, в группе, получавшей комбинацию карнитин/цилостазол, число клеток было ниже, чем в группе, получавшей карнитин Р<0,05).
На фиг.5 представлены результаты ss-DNA-окрашивания как маркера апоптоза. Относительно окрашивания клеток в группе, получавшей карнитин, на день 14, окрашивания клеток в группе, получавшей цилостазол на дни 14, 21 и 28, и окрашивания клеток в группе, получавшей комбинацию карнитин/цилостазол, на дни 7, 14, 21 и 28, число положительных клеток существенно уменьшалось по сравнению с группой, получавшей носитель (Р<0,01). Кроме того, относительно сравнения между группами, число клеток в группе, получавшей комбинацию карнитин/цилостазол, уменьшалось на дни 14 и 21 по сравнению с группой, получавшей карнитин, и дополнительно уменьшалось на дни 21 и 28 по сравнению с группой, получавшей цилостазол (Р<0,05).




Изобретение относится к лекарственному средству для лечения заболевания периферических артерий или расстройства мозгового кровообращения. Заявленное лекарственное средство включает комбинацию 6-[4-(1-циклогексил-1H-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила или его соли и L-карнитина или его соли или левокарнитина хлорида. Изобретение также относится к способу лечения окклюзионного заболевания периферических артерий или расстройства мозгового кровообращения, который включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества указанной комбинации. 3 н. и 7 з.п. ф-лы, 5 ил., 1 пр.
1. Лекарственное средство для лечения окклюзионного заболевания периферических артерий или расстройства мозгового кровообращения, включающее комбинацию 6-[4-(1-циклогексил-1H-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила или его соли и L-карнитина или его соли или левокарнитина хлорида.
2. Лекарственное средство по п.1, где окклюзионным заболеванием периферических артерий является острое окклюзионное заболевание артерий, облитерирующий тромбангиит, облитерирующий атеросклероз, спинальный стеноз поясничного отдела или перемежающаяся хромота.
3. Лекарственное средство по п.2, где окклюзионным заболеванием периферических артерий является перемежающаяся хромота.
4. Лекарственное средство по п.1, где расстройством мозгового кровообращения является острый церебральный инфаркт, хронический церебральный инфаркт, преходящее нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральная гематома, цереброкортикальное расстройство или отмирание черепно-мозговых нервных клеток.
5. Применение комбинации по п.1 для изготовления лекарственного средства для лечения окклюзионного заболевания периферических артерий или расстройства мозгового кровообращения.
6. Применение по п.5, где окклюзионное заболевание периферических артерий представляет собой острое окклюзионное заболевание артерий, облитерирующий тромбангиит, облитерирующий атеросклероз, спинальный стеноз поясничного отдела или перемежающуюся хромоту.
7. Применение по п.5, где расстройством мозгового кровообращения является острый церебральный инфаркт, хронический церебральный инфаркт, преходящее нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральная гематома, цереброкортикальное расстройство или отмирание черепно-мозговых нервных клеток.
8. Способ лечения окклюзионного заболевания периферических артерий или расстройства мозгового кровообращения, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества комбинации по п.1.
9. Способ по п.8, где окклюзионным заболеванием периферических артерий является острое окклюзионное заболевание артерий, облитерирующий тромбангиит, облитерирующий атеросклероз, спинальный стеноз поясничного отдела или перемежающаяся хромота.
10. Способ по п.8, где расстройством мозгового кровообращения является острый церебральный инфаркт, хронический церебральный инфаркт, преходящее нарушение мозгового кровообращения, внутримозговое кровоизлияние, субарахноидальное кровоизлияние, субдуральная гематома, цереброкортикальное расстройство или отмирание черепно-мозговых нервных клеток.
| WO 2007032557 A1, 22.03.2007 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| US 4968719 A1, 06.11.1990 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| АЛЯУТДИН Р.Н | |||
| Фармакология, 2-е изд-е | |||
| - М., 2004 | |||
| A.J | |||
| LIEDTKE: "Effects of carnitine isomers on fatty acid metabolism in ischemic swine hearts." / CIRCULATION RESEARCH, 1981, VOL | |||
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2014-02-20—Публикация
2009-03-13—Подача