ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на новые способы применения парацетамолсодержащих составов, которые предоставляют быстрое растворение активного вещества с последующим улучшенным поглощением у пациентов с замедленным желудочным освобождением.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение представляет собой применение состава парацетамола, который, как неожиданно было показано, обладает улучшенными фармакокинетическими профилями у пациентов с нарушением моторики желудка или гастропарезом. Исторически было показано, что у пациентов с диабетом моторика желудка (гастропарез) уменьшается на 50% по сравнению с индивидуумами, не страдающими диабетом.
Причастность вегетативной нервной системы у пациента с сахарным диабетом включает желудочную энтеропатию, характеризующуюся нарушением моторики желудочно-кишечного тракта. Bassotti, G., Recenti Prog Med. 82: 334-337 (1991). Продолжительный сахарный диабет может уменьшать желудочное освобождение у 50% пациентов. O'Mahony et al., Drugs Aging, 19: 515-527 (2002). Воздействие различных возрастных болезней на желудочно-кишечную подвижность у пожилых людей может также включать пожилых пациентов с депрессией, которая значительно продлевает время прохождения через весь кишечник, гипотиреозом, хронической почечной недостаточностью и идиопатической болезнью Паркинсона. Часто лекарственные препараты, такие как антихолинергические средства, опиатные болеутоляющие средства и антагонисты кальция, могут вызывать у пожилых людей расстройство желудочно-кишечной моторики.
Важность нарушения моторики у пациентов, особенно пожилых, может приводить к серьезным клиническим последствиям в случаях, где клинический ответ на лечение отсрочен, таких как при отсроченном всасывании леводопы или с мочегонными средствами. Поскольку опиаты и антихолинергические средства уже оказывают ингибирующие действия на желудочное освобождение, это может задержать поглощение других лекарств. Следовательно, в такой популяции пациентов существует очень большая потребность в постоянной, низкой внутрииндивидуальной вариабельности в поглощении лекарств, таких как болеутоляющие средства.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому способу уменьшения внутрииндивидуальной вариабельности у фармацевтически активного вещества, которое соответственно не всасывается желудком, такого как составы, содержащие парацетамол, у пациентов, обладающих нарушением моторики желудка, и настоящее изобретение направлено на способ улучшения обезболивания у диабетического пациента, или улучшения всасывания активного вещества у пациента с нарушением моторики желудка, способы, каждый из которых включает пероральное введение нуждающемуся в этом пациенту фармацевтической лекарственной формы, содержащей первое активное вещество, соответственно парацетамол, карбонат кальция, по меньшей мере, одно первое связующее вещество, и, по меньшей мере, одно дезинтегрирующее вещество в качестве внутригранулярных компонентов в форме гранулята, и в качестве внегранулярного компонента, по меньшей мере, один гидрофильный коллоид, необязательно второе связующее вещество, карбонат кальция, дезинтегрирующее вещество высшего качества и второе активное вещество.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому способу улучшения вариабельности поглощения активного вещества между пациентами, которые обладают нарушением моторики желудка. Нарушение моторики желудка также известно как гипокинезия желудка. Гипокинезия желудка у пациентов, нормальных в других отношениях, может быть вызвана разнообразием экологических, фармакологических и физиологических факторов. Важно, что замедленное желудочное освобождение может иметь вредное воздействие на поглощение лекарств, таких как парацетамол, которые всасываются, главным образом, в тонкой кишке. Это может привести к замедленным и неустойчивым уровням лекарства в плазме, и может вызвать дискомфорт в случае, когда специфическое лекарство представляет собой обезболивающее лекарство, такое как парацетамол.
Для целей здесь активное вещество, соответственно, не является активным веществом, которое всасывается в желудке. Настоящий состав предназначен для введения активного вещества в двенадцатиперстную кишку с увеличенной скоростью по сравнению со стандартным составом активного вещества. Поэтому любое активное вещество, которое всасывается, главным образом, после пилорического сфинктера (например, у основания желудка), а не в самом желудке, покажет, как ожидается, более быстрый и более подходящий фармакокинетический профиль. Как будет описано здесь более подробно, активное вещество - парацетамол - было выбрано здесь, чтобы описать изобретение. Было показано, что парацетамол в стандартной лекарственной форме не вносит свой вклад в скорость освобождения препарата из желудка.
Парацетамол представляет собой болеутоляющий и жаропонижающий лекарственный препарат, эффективный для облегчения несильной или умеренной боли. Рекомендованная терапевтическая доза в Великобритании составляет 500-1000 миллиграммов (мг) каждые 4-6 часов (час) вплоть до максимума в 4000 мг ежедневно. Абсолютное бионакопление при пероральном способе введения составляет приблизительно 80% и является независимым от дозы в диапазоне 5-20 мг/кг. Пиковые уровни в плазме достигаются через 0,5-3 часов после дозы в зависимости от состава.
Парацетамол обладает средним временем полужизни в плазме 2,4 часа у взрослых с диапазоном от 1,5 до 3,0 часов. Это значение несильно варьирует между индивидуумами, и не распространяется в клинически существенной степени на крайности возраста. Это в любом случае не связано с белком плазмы, и объем распределения составляет приблизительно 0,9 литра/килограмм (л/кг) массы тела.
Вводимый перорально парацетамол всасывается прежде всего в верхнем отделе тонкого кишечника, и для стандартных твердых дозированных таблетированных составов скорость всасывания ограничена i) процессом дезинтеграции/рассасывания таблетки и ii) желудочным опорожнением из желудка в верхний отдел тонкого кишечника.
Сахарный диабет (2-го типа) представляет собой наиболее общую причину ослабления желудочно-кишечной моторики у пожилых. Желудочное освобождение может быть анормальным у этой группы населения и, вследствие этого, может воздействовать на профиль поглощения активного вещества, такого как парацетамол. В настоящем изобретении был исследован профиль поглощения парацетамола при стандартной лекарственной форме и при гранулированной лекарственной форме парацетамола и карбоната кальция, и было установлено, что относительное различие в профилях поглощения, наблюдаемое у здоровых добровольцев, изменялось в случае диабетических пациентов, в качестве модели нарушения моторики желудка.
Один вариант осуществления настоящего изобретения относится к применению гранулированного состава парацетамола, как будет описано здесь далее, который, как теперь показано, обеспечивает значительно большее поглощение за 30 минут, и обладает статистически достоверными уровнями в плазме Cmax за 30 минут по сравнению со стандартными парацетамолсодержащими составами у пациентов с нарушением моторики желудка. В одном варианте осуществления изобретения те пациенты, которые обладают нарушением моторики желудка, представляют собой диабетических пациентов.
Также показало, что настоящее изобретение обеспечивает значительно большее поглощение за 60 минут по сравнению со стандартными парацетамолсодержащими составами у пациента с нарушением моторики желудка.
Несмотря на то, что также было показано, что настоящее изобретение обладает более коротким временем достижения максимальной концентрации (Tmax) по сравнению со стандартным парацетамолом, тем не менее различие не было статистически значимым. В целом диабетическое население демонстрирует более медленное поглощение парацетамола при обоих лечениях по сравнению с результатами, наблюдаемыми на здоровых добровольцах, и это частично могло было быть приписано желудочной энтеропатии, которая, как известно, имеет место при сахарном диабете. Поэтому пациенты с диабетом 2-го типа представляют собой подходящую модель нарушения моторики, которая может использоваться при оценке фармакокинетического профиля парацетамола для двух различных составов.
Парацетамолсодержащая лекарственная форма включает парацетамол, карбонат кальция, по меньшей мере, одно связывающее вещество и, по меньшей мере, одно дезинтегрирующее вещество, в качестве внутригранулярных компонентов в форме гранулята и в качестве внегранулярного компонента гидрофильный коллоид, необязательно связующее вещество, карбонат кальция, дезинтегрирующее вещество высшего качества и/или дополнительный парацетамол. Формула, включающая такие наполнители, была описана в WO 2007/118063, поданной 3 апреля 2007 г., чье раскрытие включено здесь в качестве ссылки в полном объеме.
В то же время, не желая ограничиваться такой лекарственной формой, также полагают, что парацетамолсодержащие лекарственные формы, как описано в Roberts et al. патенте США 2007/0141144, опубликованном 21 июня 2007 г., или в более ранней, но связанной WO-публикацией, WO 2005/15344, опубликованной 8 декабря 2005 г., чьи раскрытия включены здесь в качестве ссылки, также являются приемлемыми для применения в способах, описанных здесь.
Композиция с быстрым высвобождением по данному изобретению дезинтегрируется и быстро растворяется в желудке с тем, чтобы облегчить быстрое поглощение активного вещества в системе кровообращения. Как используют здесь, «быстрое высвобождение» означает, что, по меньшей мере, 60% активного вещества растворилось из композиции за 180 секунд, как определено описанным здесь способом проверки растворения. В другом варианте осуществления, соответственно, растворилось, по меньшей мере, 70% активного вещества. В другом варианте осуществления, соответственно, растворилось, по меньшей мере, 80% и в еще одном варианте осуществления, по меньшей мере, 90% активного вещества растворилось из композиции за 180 секунд. В подходящем способе проверки растворения для этой цели используют те же условия, как раскрыто в WO 02/100391, а именно лопастной прибор USP, вращающийся со скоростью 30 оборотов в минуту, с использованием 900 мл 0,05M HCl при 37°C в качестве растворяющей среды. В этой ссылке процент растворенного парацетамола определяли за пятнадцать минут, а не за 180 секунд, как описано в патенте США 2007/0141144. В качестве подходящих отмечают также описанные способы растворения за 5, 10, 15, 20, 25 и 30 минут в Rostami-Hodjegan et al., Drug Development and Industrial Pharmacy, 28(5), pp 533-5439 (2002).
Несмотря на то, что скорости высвобождения парацетамола были определены для множества коммерчески доступных парацетамолсодержащих продуктов и составили, как выяснилось, значения в пределах диапазона приблизительно от 12% до приблизительно 32%, быстрое высвобождение активного вещества представляет собой только часть настоящего изобретения. Мало того, что активное вещество должно быть высвобождено из своей лекарственной формы, активное вещество также должно освобождаться из желудка в двенадцатиперстную кишку со скоростью, которая является постоянной от пациента к пациенту, и в особенности у пациентов с ослабленной моторикой желудка освобождаться настолько близко к норме, насколько возможно.
Соответственно, один аспект изобретения предоставляет фармацевтический состав, включающий активное вещество, карбонат кальция, по меньшей мере, одно связывающее вещество и, по меньшей мере, одно дезинтегрирующее вещество, в качестве внутригранулярных компонентов в форме гранулята. Гранулят можно необязательно объединять с одним или несколькими подходящими внегранулярными компонентами, и он может быть в виде «таблетки», которая может включать таблетку любой формы, и включать кеплеты, которые представляют собой таблетки в форме капсул. Состав может быть помещен в капсулы, или может быть доступен в пакетиках с единичными дозами.
В случае единичной лекарственной формы состав по изобретению включает терапевтически эффективное количество активного вещества. В одном варианте осуществления активное вещество представляет собой парацетамол, под которым подразумевается количество парацетамола, достаточное для достижения терапевтической пользы. Соответственно, такое количество находится в диапазоне от 250 мг до 1000 мг на единичную лекарственную форму (например, на таблетку) и, как правило, составляет либо 325 мг, либо 500 мг.
В то время как активное вещество присутствует в качестве внутригранулярного компонента, признается, что ограниченное количество того же самого или отличного активного вещества может также присутствовать внегранулярно. Несмотря на то, что это не было подготовлено и проверено, другой вариант осуществления изобретения включает состав, в котором активное вещество распределено по составу исключительно в качестве внегранулярного компонента.
Фармацевтическая композиция по изобретению включает внутригранулярный карбонат кальция. Соответственно, содержание карбоната кальция в грануляте не превышает 20,0% по массе от массы композиции и, например, в одном варианте осуществления присутствует в количестве от приблизительно 5,0% до приблизительно 20,0% от массы, соответственно, от приблизительно 5,0% до приблизительно 15,0% по массе от массы композиции. В альтернативном варианте осуществления содержание карбоната кальция составляет от приблизительно 8,0% до приблизительно 15,0% по массе от массы композиции.
В одном варианте осуществления по изобретению содержание парацетамола в грануляте находится в диапазоне от 60% до 80% по массе, и карбонат кальция присутствует в количестве от 5% до 20% по массе.
В одном варианте осуществления по изобретению содержание парацетамола в грануляте находится в диапазоне от 70,0 до 80,0% по массе от массы композиции, и карбонат кальция в грануляте содержится в диапазоне от 8,0% до 15,0% по массе от массы композиции. Например, композиция с 500 мг парацетамола может включать от 30 мг до 110 мг внутригранулярного карбоната кальция, а композиция с 325 мг парацетамола может включать от 20 мг до 72 мг внутригранулярного карбоната кальция.
Несмотря на то, что карбонат кальция присутствует в качестве внутригранулярного компонента, признается, что ограниченное количество карбоната кальция, например, до приблизительно дополнительных 25,0% по массе от содержания внутригранулярного карбоната кальция в композиции может также присутствовать внегранулярно. В одном варианте осуществления композиция по изобретению включает, в качестве внегранулярного компонента, карбонат кальция в количестве в пределах приблизительно от 0,1% до приблизительно 10,0% по массе от количества находящегося там внутригранулярного карбоната кальция.
Состав по изобретению внутригранулярно включает компонент, который функционирует как связующее вещество, такое как один или несколько связующих агентов. Соответственно, связующее вещество может содержать первое связующее вещество и второе связующее вещество. Подходящие связующие вещества для использования здесь включают общераспространенные в области связующие вещества, такие как крахмалы, полимеры и производные целлюлозы или их комбинации.
Если связующее вещество включает крахмал, он, соответственно, является веществом растительного происхождения, таким как зерновой (или кукурузный) крахмал, модифицированный зерновой крахмал, пшеничный крахмал, модифицированный пшеничный крахмал, картофельный крахмал или желатинированный крахмал, например, коммерчески доступный как Starch 1500 G или Prejel; или комбинацией из двух или более из указанных веществ.
Комбинации крахмала с другими связующими веществами, такими как описанные здесь, также предусмотрены в рамках изобретения. В одном варианте осуществления, соответственно, крахмал представляет собой желатинированный крахмал, где он представляет собой единственное или первое связующее вещество. Желатинированный крахмал представляет собой крахмал, который был химически и/или механически обработан. Как правило, желатинированный крахмал содержит 5% свободной амилозы, 15% свободного амилопектина и 80% немодифицированного крахмала. Желатинированный крахмал может быть получен из зернового (или кукурузного), картофельного или рисового крахмала. Было обнаружено, что на скорость растворения парацетамола оказывается неблагоприятное воздействие в композиции, включающей, в качестве внутригранулярных компонентов: парацетамол, карбонат кальция, кукурузный крахмал, желатинированный крахмал, повидон K25 и калийсорбат, где массовое соотношение желатинированного крахмала к кукурузному крахмалу составляет приблизительно 2,3:1. Соответственно, если связующее вещество включает смесь зернового (или кукурузного) крахмала и желатинированного крахмала, то массовое соотношение желатинированного крахмала к зерновому (или кукурузному) крахмалу составляет, по меньшей мере, 3,0:1,0. В одном варианте осуществления этого изобретения массовое отношение желатинированного крахмала к зерновому (или кукурузному) крахмалу составляет, по меньшей мере, 5,0:1,0.
Соответственно, в случае присутствия в композиции по изобретению, крахмал присутствует в грануляте в количестве приблизительно от 1,0% до приблизительно 30,0% по массе от массы композиции, как правило, приблизительно от 5,0% до приблизительно 20,0%, например приблизительно от 8,0% до приблизительно 15,0% по массе от массы композиции.
Если связующее вещество включает полимер, то он, соответственно, представляет собой поливинилпирролидон или повидон (PVP), поливиниловый спирт (ПВА), полиэтиленоксид, полоксамер, полиметакрилат, например карбомер, полиэтиленгликоль (ПЭГ), такой как ПЭГ 3350, и поликарбофил кальция; или комбинацию двух или нескольких из этого. Комбинации полимера с другими связующими веществами, такими как описанные здесь, также предусмотрены в рамках изобретения. В случае, если полимер включает PVP, он должен, соответственно, обладать молекулярной массой приблизительно 30000, как, например, коммерчески доступный PVP K25. Соответственно, в случае присутствия в композиции по изобретению полимер присутствует в грануляте в количестве приблизительно от 1,0% до приблизительно 10,0% по массе от массы композиции, как правило, приблизительно от 1,5% до приблизительно 5,0% по массе от массы композиции.
В одном варианте осуществления полимер, такой как PVP, присутствует в качестве второго связующего вещества. В одном варианте осуществления крахмал, такой как желатинированный крахмал, присутствует в качестве первого связующего вещества, в количестве в пределах от приблизительно 10,0% до приблизительно 15,0% по массе от массы композиции, и полимер, такой как PVP, присутствует в качестве второго связующего вещества в количестве в пределах от приблизительно 1,5% до приблизительно 5,0% по массе от массы композиции. Соответственно, такой вариант осуществления в существенной степени не содержит зернового (или кукурузного) крахмала, например, включая не больше, чем количество в пределах от приблизительно 0,0% до приблизительно 1,0% зернового (или кукурузного) крахмала.
Если связующее вещество включает производное целлюлозы, соответственно, оно включает, по меньшей мере, одно из гидроксипропилцеллюлозы (HPC) (вариант вязкости от низкой к средней), например, которая может быть доступна коммерчески под фирменным знаком Klucel® от отделения Aqualon Hercules Inc., Dow Chemical Company, например Klucel GF, Klucel JF, Klucel LF и Klucel EF; гидроксипропилметилцеллюлозы (HPMC) (вариант вязкости от низкой к средней), которая, например, может быть коммерчески доступна под фирменным знаком Methocel® от Dow Chemical Company, например Methocel E15Premium, Methocel E3Premium LV, Methocel K100LV; микрокристаллической целлюлозы (MCC), карбоксиметилцеллюлозы (MC), натрийкарбоксиметилцеллюлозы; или комбинации из двух или более указанных веществ. Комбинации производной целлюлозы с другими связующими веществами, отмеченными выше, также предусмотрены в рамках изобретения.
Термин вязкость «от низкой до средней», как используется здесь, означает вязкость в диапазоне от приблизительно 15 до приблизительно 1000 мПа·с. В данной области признано, что определение вязкости производных целлюлозы основано на стандартных способах и градуировании, например, для HPMC можно определить вязкость 2%-ного раствора при 20°C с использованием вискозиметра Ubbelohde, или для HPC можно определить вязкость 2-10%-ного раствора при 25°C с использованием вискозиметра Brookfield LVF. Как правило, производное целлюлозы присутствует в грануляте в количестве в пределах от приблизительно 0,5% до приблизительно 5,0% по массе от массы композиции. В данной области признано, что определенные производные целлюлозы, такие как HPMC, должны иметь различные роли в составе, в зависимости от используемого количества. Например, HPMC (вязкость от низкой до средней) может функционировать как связующее вещество, покрывающее вещество или как вещество, образующее матрицу. Было обнаружено, что в случае, когда HPMC (вязкость от низкой до средней) используется при приблизительно 10,0% по массе от массы композиции, скорость растворения парацетамола замедляется, вероятно, вследствие свойств HPMC по замедлению высвобождения. В соответствии с настоящим изобретением в случае использования в качестве связующего вещества HPMC присутствует в количестве, как правило, не больше чем 2,5% по массе от массы композиции, например, в количестве приблизительно от 1,0% до приблизительно 2,5% по массе от массы композиции.
Общее количество присутствующего внутригранулярно связующего вещества в композиции по изобретению находится, соответственно, в количестве в пределах от приблизительно 1,0% до приблизительно 30,0% по массе от массы композиции, например, приблизительно от 2,0% до приблизительно 25,0% по массе от массы композиции, или альтернативно, приблизительно от 5,0% до приблизительно 20,0% по массе от массы композиции.
Несмотря на то, что связующее вещество присутствует в качестве внутригранулярного компонента, признано, что небольшое количество связующего вещества, например, вплоть до приблизительно дополнительных 5,0%-10,0% по массе от содержания внутригранулярного связующего вещества композиции, может также присутствовать внегранулярно. В одном варианте осуществления композиция по изобретению включает, в качестве внегранулярного компонента, связующее вещество в количестве в пределах от приблизительно 0,1% до приблизительно 10,0% по массе от присутствующего там внутригранулярного количества связующего вещества.
Композиция по изобретению включает, в качестве внутригранулярного компонента, по меньшей мере, один компонент, который функционирует как агент, вызывающий дезинтеграцию, и может включать, по меньшей мере, два дезинтегрирующих вещества. Подходящие дезинтегрирующие вещества включают дезинтегрирующие вещества невысшего качества, дезинтегрирующие вещества высшего качества или комбинацию обоих. Подходящие дезинтегрирующие вещества невысшего качества включают обычные дезинтегрирующие вещества, такие как крахмал (зерновой или кукурузный), желатинированный крахмал, например, Starch 1500 G, глины (Veegum или Bentonite), микрокристаллическую целлюлозу, целлюлозу или порошковую целлюлозу. В данной области признано, что некоторые наполнители могут выполнять больше чем одну роль в данном фармацевтическом составе. Например, определенные наполнители, например крахмалы, включая желатинированный крахмал, и микрокристаллическая целлюлоза (идентифицированные выше как связующие вещества) функционируют как связующие, так и как дезинтегрирующие вещества. Соответственно, следует понимать, что тот же самый наполнитель может действовать и как связующее вещество, и как дезинтегрирующее вещество. В таких случаях включение дезинтегрирующего вещества в дополнение к связующему веществу является совершенно необязательным. В равной степени, в таких случаях включение связующего вещества в дополнение к дезинтегрирующему веществу является абсолютно обязательным.
Один вариант осуществления изобретения предоставляет, в качестве внутригранулярных компонентов, парацетамол и карбонат кальция и, по меньшей мере, одно связующее вещество, которое является микрокристаллической целлюлозой или крахмалом, где крахмал представляет собой зерновой (или кукурузный) крахмал, модифицированный зерновой крахмал, пшеничный крахмал, модифицированный пшеничный крахмал, картофельный крахмал, желатинированный крахмал или комбинацию двух или нескольких таких крахмалов, при условии, что, если связующее вещество включает смесь зернового (или кукурузного) крахмала и желатинированного крахмала, то массовое отношение желатинированного крахмала к зерновому (или кукурузному) крахмалу составляет более чем приблизительно от 3,0 до 1,0; и необязательно дезинтегрирующее вещество; и один или несколько фармацевтически приемлемых компонентов в качестве внегранулярных компонентов.
Композиции здесь могут включать дезинтегрирующее вещество невысшего качества, которое может присутствовать внутригранулярно, внегранулярно или и внутригранулярно, и внегранулярно. В случае, когда дезинтегрирующее вещество высшего качества или отсутствует в составе, или присутствует только внегранулярно, дезинтегрирующее вещество должно соответственно включать дезинтегрирующее вещество высшего качества, присутствующее внутригранулярно.
Соответственно, дезинтегрирующее вещество невысшего качества должно присутствовать внутригранулярно в количестве в пределах приблизительно от 5,0% до приблизительно 30,0% по массе от массы композиции, соответственно, приблизительно от 5,0% до приблизительно 20,0% по массе от массы композиции. В случае присутствия внегранулярно, дезинтегрирующее вещество невысшего качества может также присутствовать в количестве, например, вплоть до приблизительно дополнительных 5,0%-10,0% по массе от содержания в композиции дезинтегрирующего вещества невысшего качества.
При использовании дезинтегрирующее вещество высшего качества может присутствовать внутригранулярно, внегранулярно или и внутригранулярно, и внегранулярно. Признано, что в случае, когда дезинтегрирующее вещество высшего качества или отсутствует в составе, или присутствует только внегранулярно, дезинтегрирующее вещество должно включать дезинтегрирующее вещество невысшего качества, присутствующее внутригранулярно. Дезинтегрирующее вещество высшего качества может использоваться внутригранулярно или внегранулярно в количестве в пределах от приблизительно 0,5% до приблизительно 5,0% по массе от массы композиции. Общая сумма дезинтегрирующего вещества высшего качества может быть в количестве в пределах от приблизительно 0,5% до приблизительно 10,0% по массе от массы композиции.
«Дезинтегрирующие вещества высшего качества» представляют класс дезинтегрирующих веществ, которые, как правило, могут использоваться в уменьшенных количествах в фармацевтических препаратах по сравнению с обычными дезинтегрирующими веществами. Примеры дезинтегрирующих веществ высшего качества включают натрийкрахмалгликолят, натриевую соль карбоксиметилкрахмала, модифицированную целлюлозу и поперечно сшитый поливинилпирролидон. Натрийкрахмалгликолят доступен коммерчески под торговыми марками Explotab® (Edward Mendell Co.), Primojel® (Корпорация Generichem) и Tablo® (Blanver, Бразилия). Пример модифицированной целлюлозы включает кроскармелозу, натриевую соль карбоксиметилцеллюлозы. Кроскармелоза доступна коммерчески под торговыми марками AcDiSol® (Корпорация FMC), Nymcel ZSX® (Nyma, Нидерланды), Primellose® (Avebe, Нидерланды), Solutab® (Blanver, Бразилия). Пример поперечно сшитого поливинилпирролидона включает кросповидон, который коммерчески доступен под торговыми марками Kollidon CL® или Kollidon CL-М (Корпорация Basf), и Polyplasdone XL® (Корпорация ISP). Соответственно, дезинтегрирующее вещество включает поперечно сшитый поливинилпирролидон.
Композиция по изобретению также может необязательно содержать дополнительные фармацевтически приемлемые внегранулярные компоненты. Например, композиция по изобретению может включать гидрофильный коллоид, такой как альгиновая кислота, карагенан, геллан, пектин и/или агар, в качестве внегранулярного компонента. Соответственно, гидрофильный коллоид представляет собой альгиновую кислоту. В случае наличия гидрофильный коллоид присутствует в количестве в пределах от приблизительно 1,0% до приблизительно 5,0% по массе от массы композиции.
В одном аспекте композиция по изобретению включает альгиновую кислоту в качестве внегранулярного компонента.
Другие фармацевтически приемлемые внегранулярные компоненты включают, в качестве неограничивающих примеров, антибактериальное вещество, например сорбат калия или парааминобензойную кислоту, а именно, один или несколько эфиров гидроксибензойных кислот, например метиловый, этиловый, пропиловый или бутиловый, соответственно, по отдельности или в качестве смеси. В одном варианте осуществления изобретения используют парааминобензойную кислоту.
В одном варианте осуществления композиция включает парацетамол, карбонат кальция, желатинированный крахмал и повидон в качестве внутригранулярных компонентов, а в качестве внегранулярных компонентов - альгиновую кислоту и кросповидон, и необязательно другие внегранулярные компоненты, предпочтительно спрессованные в таблетку. Соответственно, альгиновая кислота присутствует в количестве в пределах от приблизительно 1,0% до приблизительно 5,0% по массе от массы композиции.
Дополнительные фармацевтически приемлемые внегранулярные компоненты включают краситель; окрашивающее вещество; ароматизатор; вещество, способствующее компрессии; консервант; увлажняющее вещество; вещество-наполнитель; связующее вещество; подслащивающее вещество; смазывающее вещество, такое как стеарат магния, стеарат кальция, стеарат натрия, стеариновая кислота или тальк, и смазывающее или скользящее вещество, такое как коллоидный диоксид кремния (Cab-O-Sil, SyloidTM). Соответственно, при наличии смазывающего или скользящего вещества каждое используют в количестве в пределах от 0,1% до 5,0% по массе от массы композиции. Признано, что дополнительные фармацевтически приемлемые компоненты могут присутствовать в качестве внутригранулярных компонентов, так же как и внегранулярных компонентов.
В дополнение к парацетамолу композиции по изобретению могут также содержать другие фармацевтически активные вещества, например другие болеутоляющие средства, такие как кодеин, гидрокодон, оксикодон, трамадол и пропоксифен; противовоспалительные болеутоляющие средства, такие как средства нестероидной противовоспалительной терапии, например аспирин и ибупрофен; противозастойные или противоотечные средства, такие как псевдоэфедрин и фенилэфрин; средства против кашля, такие как фолькодин и декстрометорфан; отхаркивающие средства, такие как гуаифенезин и бромгексин; мочегонные средства, такие как памабром; неседативные и седативные антигистаминовые препараты, такие как дифенгидрамин, доксиламин и мепирамин; желудочно-кишечные вещества, такие как метоклопрамид; триптаны, такие как суматриптан; и мышечные релаксанты, такие как метокарбамол; и адъюванты, например кофеин. Как предварительно отмечено, фармацевтически активные вещества и адъюванты могут присутствовать внутригранулярно, внегранулярно или и внутригранулярно, и внегранулярно.
В другом аспекте предоставляется композиция, включающая кофеин внутригранулярно, внегранулярно или и внутригранулярно, и внегранулярно. Соответственно, кофеин присутствует внегранулярно. В одном варианте осуществления кофеин является дополнением к внутригранулярному парацетамолсодержащему составу.
Как используется здесь, термин «фармацевтически активное вещество» включает, в качестве неограничивающих примеров, лекарственные препараты, диетические добавки, витамины, микроэлементы, нутрицевтики и ветеринарные вещества. Этот термин включает биологически активные вещества, активные вещества, терапевтические вещества или лекарственный препарат(ы), как определено здесь, и следует рекомендациям Руководства Европейского Сообщества по Правилам организации производства и контроля качества лекарственных препаратов. Такие вещества предназначены для обеспечения фармакологической активности или другого прямого эффекта при лечении, смягчении, обработке, или предотвращении болезни или воздействия на структуру и функцию организма. Фармакологическая активность может являться профилактической или для лечения болезненного состояния.
Лекарственные субстанции включают субстанции, предназначенные для перорального введения. Описание этих классов лекарств и перечисление видов в пределах каждого класса может быть найдено в Martindale, The Extra Pharmacopoeia, Twenty-ninth Edition, The Pharmaceutical Press, London, 1989. Лекарственные вещества коммерчески доступны и/или могут быть подготовлены способами, известными в данной области.
Изобретение далее будет описано путем ссылки на следующие биологические примеры, которые являются просто иллюстративными и не должны рассматриваться к качестве ограничивающих возможности настоящего изобретения.
ПРИМЕР 1
Фармакокинетический профиль у пациентов с нарушением моторики желудка
Продолжительный диабет может ослабить перистальтику желудка вплоть до 50%. Поэтому пациенты с диабетом 2-го типа были выбраны в качестве модели с нарушением моторики для оценки фармакокинетического профиля парацетамола в двух различных составах. Это исследование представляло собой исследование с единым центром, двумя экспериментальными линиями, открытой индикацией, рандомизированное, с однократной дозой, с перекрестной фармакокинетикой. Субъекты получали единичную 1 г-дозу состава для перорального введения по изобретению или стандартного состава с парацетамолом, спустя 2 часа после стандартного приема пищи, со случайно выбранными пациентами, имеющими 24 часа перерыва между дозированием. 21 пациент завершил протокол, 18 мужчин и 3 женщины. Образцы крови были взяты через 4 часа после получения дозы для фармакокинетических исследований.
Первичная цель исследования состояла в том, чтобы сравнить ранние выдержки, как оценено по скорости всасывания (область под кривой [AUC]0-30минут). Другие вариации ранних выдержек включали время достижения максимальной концентрации (Tmax) и вариабельность между пациентами (коэффициент вариаций (CV)) в AUC0-30минут, AUC0-60минут и плазменной концентрации (Cплазма) за 30 минут.
Стандартные таблетки Панадол представляют собой покрытые пленкой таблетки, содержащие 500 мг парацетамола, и содержат в качестве наполнителей желатинированный крахмал, кукурузный крахмал, тальк, стеариновую кислоту, повидон, сорбат калия, гипромеллозу и триацетатглицерин.
Используемый здесь состав карбоната кальция/парацетамола содержит 500 мг парацетамола и подобен описанному в примере 6 из WO 2007/118063.
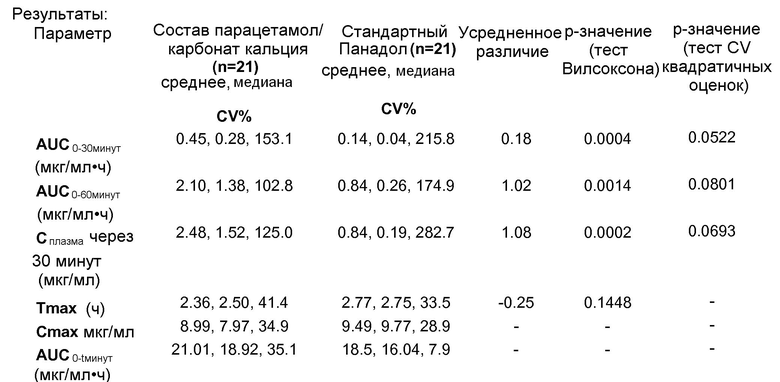
AUC0-30минут (первичная цель) было статистически существенно больше для состава, содержащего парацетамол/карбонат кальция, чем для стандартного парацетамола (p=0,0004).
AUC0-60минут и Cплазма за 30 минут были статистически существенно больше (p=0,0014) и выше (p=0,0002), соответственно, для состава, содержащего парацетамол/карбонат кальция, по сравнению со стандартным парацетамолом.
Время до максимальной концентрации (Tmax) было меньше для состава, содержащего парацетамол/карбонат кальция, по сравнению со стандартным парацетамолом, но различие не было статистически существенным (p=0,1448).
Была тенденция к статистической значимости для сравнения CV для AUC0-30минут (p=0,0522), AUC0-60минут (p=0,0801) и Cплазма за 30 минут (p=0,0693) в пользу состава, содержащего парацетамол/карбонат кальция.
Состав, содержащий парацетамол/карбонат кальция, всасывался быстрее, чем таблетки стандартного парацетамола, и демонстрировал тенденцию к меньшей вариабельности между пациентами (основанной на коэффициенте вариации) у этой группы диабетических пациентов.
Запланированный размер образца был меньше желаемого, и это может объяснить, почему имел место недостаток статистической значимости для полученного сравнения Tmax. Проверенное население (диабетики) в целом в этом исследовании показало более медленное поглощение парацетамола от обоих лечений по сравнению с результатами, наблюдаемыми на здоровых добровольцах, и это могло быть частично приписано желудочной энтеропатии, которая, как известно, происходит при сахарном диабете. Однако состав, содержащий парацетамол/карбонат кальция, по-видимому, поддерживает преимущества быстрого и постоянного всасывания, продемонстрированного прежде на здоровых добровольцах, даже у пациентов с сахарным диабетом.
ПРИМЕР 2
Исследование фармакокинетических параметров
Предварительно в клиническом исследовании было определено, что состав, содержащий парацетамол/карбонат кальция (как описано выше), освобождается из желудка быстрее, чем стандартный таблетированный состав парацетамола (SP). В нижеприведенном исследовании сравниваются фармакокинетические параметры PK состава, содержащего парацетамол/карбонат кальция, и стандартной таблетки с парацетамолом, и оценивается их вариабельность, так как они могут влиять на эффективность обезболивания и скорость реакции.
Способы:
В общей сложности 76 здоровых добровольцев были задействованы в исследовании с открытой индикацией, рандомизированном, с 8 экспериментальными линиями, перекрестном. Каждый состав вводили в повторностях, с однократной 1 г-дозой, принимаемой спустя 2 часа после стандартного приема пищи в 4 отдельных дня. Образцы крови были взяты спустя 10 часов после начальной дозы и спустя 4 часа после повторных доз для фармакокинетического (PK) анализа.
Первоначальные цели представляли собой: ранняя выдержка (скорость всасывания, AUC0-30мин, после и начального, и повторного дозирования), вариация среди (между) субъектов (среди-CV%, после начальной дозы) и внутрисубъектная вариация (внутри-CV%, после повторного дозирования). Вторичные цели включали AUC0-60мин, концентрацию в плазме через 30 минут (Cpl30мин) и процент всасывания препарата (PDA) через 30 и 60 минут (определенный способом анализа обращения свертки, вариация, измеренная только для начальной дозы).
Результаты:
AUC0-30мин как для начальной дозы, так и после повторного дозирования, были весьма значительно выше для состава, содержащего парацетамол/карбонат кальция по сравнению со стандартным составом парацетамола (начальная доза: 0,98 против 0,10 мкг·ч/мл [срединное различие 0,77, 95% CI 0,53-1,01, p<0,0001]; повторное дозирование: 1,23 против 0,15 мкг·ч/мл [срединное различие 0,99, 95% CI 0,81-1,19, p<0,0001]).
Среди-CV% для этого параметра был значительно ниже для состава, содержащего парацетамол/карбонат кальция, против стандартного состава парацетамола (84,4% против 192%, p<0,0001).
Сходным образом, наблюдалось существенное различие для внутри-CV% для AUC0-30мин (60,6% против 116%, p<0,0001). Подобные снижения в между-CV% и внутри-CV% наблюдали для AUC0-60мин и Cpl30мин наряду с между-CV% для PDA30мин и PDA60мин.
Заключения:
Эти данные ясно показывают, что поглощение парацетамола для состава, содержащего парацетамол/карбонат кальция, происходит значительно быстрее, чем поглощение со стандартным таблетированным составом парацетамола. Важно, что поглощение для состава, содержащего парацетамол/карбонат кальция, также показывает значительно меньшую межсубъектную и внутрисубъектную вариабельность. Взятые вместе, эти данные имеют ясные клинические проявления на примере популяции пациентов, получающих быстрое и стойкое облегчение боли при помощи этой ценной первичной обезболивающей терапии и поэтому избегающих потенциальных проблем побочного эффекта от последующих лечений, таких как с использованием средства нестероидной противовоспалительной терапии.
ПРИМЕР 3
ДЕЗИНТЕГРАЦИЯ И ЖЕЛУДОЧНОЕ ОСВОБОЖДЕНИЕ
Дезинтеграция и растворение таблеток представляют собой ключевые факторы скорости всасывания in vivo и последующих фармакокинетических параметров. С использованием состава, содержащего парацетамол/карбонат кальция, проводилось гамма исследование in vivo сцинтиграфии дезинтеграции таблетки и желудочного освобождения (GE).
Способы:
В это перекрестное исследование с единичной дозой было вовлечено 24 здоровых добровольца. Все участники съели стандартный радиоактивно меченый завтрак за 2 часа (ч) перед принятием изучаемого лекарственного средства (1 г парацетамола в виде либо состава, содержащего парацетамол/карбонат кальция (описан выше), либо стандартного таблетированного состава парацетамола, описанного выше (SP) [таблетка, меченая 111индий-DTPA]).
Скорость дезинтеграции определяли с использованием гамма-сцинтиграфии после определения участка желудка в качестве области интереса. Данные были проанализированы с использованием программы анализа изображения WebLink®. Начало и завершение дезинтеграции таблетки определяли путем качественной оценки сцинтиграфических изображений. Желудочное освобождение таблетки выявляли путем определения количества активного начала, остающегося в желудке в ряду временных точек. Для оценки GE использовались два параметра: время до 50%-ного освобождения (T50) и время до 90%-ного освобождения (T90). Начало GE определяли путем качественной оценки сцинтиграфических изображений.
Результаты:
Время как начала, так и завершения дезинтеграции было значительно меньше для состава, содержащего парацетамол/карбонат кальция, чем для стандартного состава парацетамола (6,4±4,3 против 46,7±20,5 минуты, p<0,0001 и 12,9±26,4 против 69,6±30,2 минуты, p<0,0001). Сходным образом, для GE время начала (41,9±28,8 против 85,0±28,2, p<0,0001), T50 (72,4±36,4 против 100,7±30,6, p=0,0013) и T90 (128,4±41,2 против 142±33,8, p=0,10) было меньше для состава, содержащего парацетамол/карбонат кальция, чем для стандартного состава парацетамола. Время для GE стандартной пищи для состава, содержащего парацетамол/карбонат кальция, и для стандартного состава парацетамола не отличалось между собой. Кроме того, в то время как 75% субъектов, принимающих состав, содержащий парацетамол/карбонат кальция, показали начало дезинтеграции/растворения в пределах 5 минут, ни один из стандартной группы не продемонстрировал начало в этой временной точке.
Заключения:
В этом сцинтиграфическом исследовании состав, содержащий парацетамол/карбонат кальция, обладал очень существенным преимуществом в плане дезинтеграции таблеток in vivo по сравнению со стандартным составом парацетамола. Это коррелирует с увеличением GE для состава, содержащего парацетамол/карбонат кальция, по сравнению со стандартным составом парацетамола.
Все публикации, включая, в качестве неограничивающих примеров, патенты и патентные заявки, процитированные в этой спецификации, включены здесь в качестве ссылки, как если бы каждая индивидуальная публикация была определенно и индивидуально обозначена для включения здесь в качестве ссылки, как если бы полностью были изложены.
Вышеприведенное описание полностью раскрывает изобретение, включая предпочтительные варианты его осуществления. Модификации и усовершенствования вариантов осуществления, специфически раскрытых здесь, находятся в границах следующих пунктов формулы изобретения. В случае отсутствия дополнительного уточнения предполагается, что любой специалист в данной области, используя предыдущее описание, может использовать настоящее изобретение во всей его полноте. Поэтому приведенные здесь примеры следует рассматривать просто в качестве иллюстративных и не ограничивающих никоим образом объема настоящего изобретения. Варианты осуществления изобретения, в которых требуется исключительное право собственности или привилегия, определены следующим образом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДОЗИРОВАННАЯ ФОРМА С НЕМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ | 2020 |
|
RU2795085C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ГЛЮКОЗАМИНА | 2011 |
|
RU2521231C2 |
| ТВЕРДЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИНГИБИТОР ИНТЕГРАЗЫ | 2010 |
|
RU2602865C2 |
| ПРЕПАРАТ NSAID, СОДЕРЖАЩИЙ ГРАНУЛИРОВАННУЮ КОМПОЗИЦИЮ И ВНЕГРАНУЛЯРНУЮ КОМПОЗИЦИЮ | 2002 |
|
RU2298404C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ АКОТИАМИДА И ИНГИБИТОРА ПРОТОННОЙ ПОМПЫ | 2019 |
|
RU2820820C2 |
| АНТИСМЫСЛОВЫЕ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2009 |
|
RU2593939C2 |
| КОМПОЗИЦИИ ЦЕНИКРИВИРОКА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2014 |
|
RU2633069C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ДОРАВИРИН, ТЕНОФОВИРА ДИЗОПРОКСИЛА ФУМАРАТ И ЛАМИВУДИН | 2016 |
|
RU2736941C2 |
| АНТИСМЫСЛОВЫЕ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2009 |
|
RU2739302C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АГОНИСТА РЕЦЕПТОРА S1P ДЛЯ ЛЕЧЕНИЯ ДЕМИЕЛИНИЗАЦИОННЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2530626C1 |
Настоящее изобретение относится к применению фармацевтической лекарственной формы для перорального введения для уменьшения межиндивидуальной вариабельности в парацетамолсодержащих составах у диабетического пациента, обладающего нарушением моторики желудка. Указанная лекарственная форма содержит в виде гранулята: парацетамол в количестве 60-80% по массе, карбонат кальция в количестве 5-20% по массе, по меньшей мере, одно первое связующее вещество и, по меньшей мере, одно дезинтегрирующее вещество, а также, по меньшей мере, один гидрофильный коллоид в качестве внегранулярного компонента. Заявленное изобретение обеспечивает улучшение всасывания активного вещества у пациента с нарушением моторики желудка. 12 з.п. ф-лы, 1 табл., 3 пр.
1. Применение фармацевтической лекарственной формы для перорального введения для уменьшения межиндивидуальной вариабельности, в парацетамолсодержащих составах у диабетического пациента, обладающего нарушением моторики желудка, где фармацевтическая лекарственная форма содержит внутригранулярные компоненты в виде гранулята,
парацетамол присутствует в количестве от 60% до 80% по массе,
карбонат кальция присутствует в количестве от 5% до 20% по массе,
по меньшей мере, одно первое связующее вещество и, по меньшей мере, одно дезинтегрирующее вещество, и
в качестве внегранулярного компонента, по меньшей мере, один гидрофильный коллоид.
2. Применение по п.1, где первое активное вещество представляет собой парацетамол, и где внегранулярный компонент содержит второе связующее вещество, присутствующее в количестве в пределах от 0,1% до 10,0% по массе от количества внутригранулярного связующего вещества.
3. Применение по п.2, где внегранулярный компонент содержит дополнительное количество карбоната кальция, присутствующего в количестве в пределах от 0,1% до 10,0% по массе от количества внутригранулярного карбоната кальция.
4. Применение по п.3, где внегранулярный компонент включает второе активное вещество, которое представляет собой парацетамол, в количестве в пределах от 0,1% до 10,0% по массе от массы внутригранулярного первого активного вещества, которое является парацетамолом.
5. Применение по п.3, где внегранулярный компонент включает супердезинтегрант, присутствующий в количестве в пределах от 0,5% до 5,0% по массе от массы композиции.
6. Применение по п.5, где гидрофильный коллоид выбран из альгиновой кислоты, каррагенана, геллана, пектина, агара или комбинации из двух или более веществ.
7. Применение по п.6, где гидрофильный коллоид включает альгиновую кислоту.
8. Применение по п.7, где гидрофильный коллоид присутствует в количестве в пределах от 1,0% до 5,0% по массе от массы композиции.
9. Применение по п.8, где лекарственная форма также включает в качестве внегранулярного компонента краситель, окрашивающее вещество, ароматизатор, подслащивающее вещество, смазывающее вещество или скользящее вещество или комбинацию из двух или более веществ.
10. Применение по п.1, где лекарственная форма является таблеткой для глотания, содержащей парацетамол, карбонат кальция, желатинированный крахмал и любые другие необязательные внутригранулярные компоненты, объединенные вместе в процессе гранулирования для образования гранулята, и затем с примешиванием альгиновой кислоты и любых других дополнительных внегранулярных компонентов для образования смеси, и затем сжатой, чтобы сформировать таблетку.
11. Применение по п.1, где лекарственная форма представляет собой таблетку для глотания, включающую гранулят, содержащий в качестве внутригранулярных компонентов парацетамол, карбонат кальция и, по меньшей мере, одно связующее вещество, которое представляет собой микрокристаллическую целлюлозу или крахмал, и где крахмал выбран из группы, состоящей из зернового крахмала, модифицированного кукурузного крахмала, пшеничного крахмала, модифицированного пшеничного крахмала, картофельного крахмала, желатинированного крахмала или комбинации двух или более, при условии, что в случае, если связующее вещество включает смесь зернового крахмала и желатинированного крахмала, то массовое отношение желатинированного крахмала к зерновому крахмалу составляет более чем от 3,0 до 1,0; и необязательно дезинтегрирующее вещество, объединенные вместе в процессе гранулирования для образования гранулята; и содержащиеся в качестве внегранулярных компонентов гидрофильный коллоид, выбранный из альгиновой кислоты, каррагенана, геллана, пектина, агара или комбинации двух или более веществ; и необязательно, по меньшей мере, один внегранулярный наполнитель, который является вторым активным веществом, дополнительное количество карбоната кальция, второе дезинтегрирующее вещество, второе связующее вещество, краситель, окрашивающее вещество, ароматизатор, подслащивающее вещество, смазывающее вещество или скользящее вещество, или комбинация двух или более веществ, и компоненты, спрессованные в таблетку.
12. Применение по п.1 для применения в целях улучшения обезболивания у диабетического пациента.
13. Применение по п.1 для применения в целях улучшения поглощения парацетамола у пациента с нарушением моторики желудка.
| WO 2007118063 A1 18.10.2007 | |||
| WO 2006049978 A1 11.05.2006 | |||
| HOROWITZ M | |||
| ET AL., "Gastric and oasophageal emplyting in patients with type 2 (non-insulin-dependent) diabetes mellitus", vol.32, N3, стр.151 | |||
| ЗАЙКО Н | |||
| Н | |||
| и др.: "Патологическая физиология (учебник для студентов мед | |||
| вузов)", Киев, 1996, стр.483-484 |
Авторы
Даты
2014-05-27—Публикация
2009-07-29—Подача