Изобретение относится к медицине, в частности к фармакологии, и касается антидепрессанта, представляющего собой глицин, иммобилизованный на частицах детонационного наноалмаза.
Депрессия - одно из наиболее частых психических заболеваний. В каждый момент времени около 5-6% людей находится в состоянии депрессии, а у 10% депрессия возникает в какой-либо период их жизни [1]. Депрессия представляет собой гетерогенное заболевание, имеющее различные проявления. Антидепрессивной активностью обладают вещества разной химической структуры. Их количество постоянно растет, но ни одна из групп таких веществ - антидепрессантов - не имеет неоспоримых преимуществ [1]. Все существующие в настоящее время антидепрессанты рассматриваются как влияющие на метаболизм или обратный захват серотонина, норадреналина или обоих аминов одновременно или действующие как их селективные антагонисты. Несмотря на интенсивные исследования, механизмы их действия пока недостаточно определены [1].
Основное показание к применению антидепрессантов - лечение депрессии, но международный клинический опыт дает обоснование их использования при панических состояниях, обсессивно-компульсивных нарушениях, энурезе, хронических болевых синдромах, расстройствах аппетита, булимии, дефиците внимания и генерализованных тревожных состояниях [2].
Известно, что современные антидепрессивные средства не удовлетворяют в полной мере требованиям клиники и имеют много побочных эффектов. В частности, они нередко вызывают усиление тревоги, возникновение кардиотоксических и антихолинергических эффектов [3]. Известно, что отдельные проявления психической патологии редко бывают изолированными и большинство психических расстройств невротического уровня представлены в виде композиции различных психопатологических синдромов, в частности коморбидными, депрессивными, тревожными, аффективными и когнитивными нарушениями [4]. Лечение таких расстройств представляет серьезную проблему в связи с недостаточностью применения отдельных лекарственных препаратов из разных групп и риском усиления их побочных эффектов, обусловленных механизмами взаимодействия при комбинированной терапии. Все вышеуказанное определяет актуальность поиска и изучения лекарственных средств, обладающих антидепрессивным действием, которые могут быть перспективными в качестве средств терапии депрессивных и невротических расстройств.
Известно, что заменимая аминокислота глицин (NH2CH2COOH), являясь центральным нейромедиатором тормозного типа действия, проявляет седативную активность и улучшает метаболические процессы в тканях мозга [5]. В современной терапевтической практике глицин применяют как средство, ослабляющее влечение к алкоголю, уменьшающее явления абстиненции, депрессивные нарушения, повышенную раздражительность, нормализующее сон, а также в комплексном лечении нарушений мозгового кровообращения [5]. В основе фармакологического действия глицина лежит эффект амплификации метаболических и нейротрансмиттерных процессов, возникающих за счет усиления его эндогенного синтеза. Увеличить внутриклеточный синтез глицина можно, только используя пути передачи сигнала, обусловленные взаимодействием с рецепторными системами. Его взаимодействие с глициновыми рецепторами приводит к открытию хлорных каналов, гиперполяризации мембраны и распространению торможения.
Наряду с этим глицин способен выступать в роли аллостерического коагониста глутаматных рецепторов. Связываясь в специфическом сайте, он усиливает способность глутамата и N-метил-D-аспарата (NMDA) открывать катионный канал [6, 7].
Применяемый фармакопейный глицин назначают в виде таблеток (по 0,1 г) под язык 3-4 раза в день.
Известен глицин, иммобилизованный на частицах детонационного наноалмаза с размером 2-10 нм, применяемый в качестве связующего компонента в полимерных композитах [8, 9]. Способ его получения заключается в следующем [9]. Навеску наноалмаза помещают в реактор в постоянном токе гелия и отжигают при температуре 150-470°С в течение 3-4 ч. Далее проводят фторирование образцов наноалмаза при температуре 50-500°С в течение 1-24 ч контактированием со смесью газообразных фтора и водорода. Для получения глицина, иммобилизованного на частицах наноалмаза, фторированный наноалмаз обрабатывают ультразвуком в о-дихлорбензоле в течение 20-30 мин, добавляют гидрохлорид этилового эфира глицина (NH2CH2COOCH2CH3·HCl) и несколько капель пиридина. Полученную смесь перемешивают при температуре 130-140°С в течение 8-12ч. Образовавшийся продукт фильтруют, промывают этанолом и сушат под вакуумом при 70°С.
Дополнительной характеристикой этого вещества является размер его частиц в суспензии, равный, по данным динамического рассеяния света (ДРС), 310 нм [9].
Особенностью данного вещества является наличие на поверхности частиц наноалмаза помимо молекул глицина также атомов фтора. Хотя их количество авторами декларируется менее 1 % ат., в действительности экспериментально установлено, что концентрация фтора на поверхности наноалмаза может достигать 14 % ат. и более. Это обусловлено тем, что связь C-F (Eсв.=115 ккал/г-атом) является прочной и фторпроизводные углерода инертны по отношению ко многим веществам. Поэтому при химической иммобилизации глицина на поверхность наноалмаза, содержащего атомы фтора, молекулы глицина замещаются на атомы фтора лишь частично. При этом известно, что присутствие в органическом веществе фтора и его производных повышает его токсичность и может изменять показатели микросомальной системы биотрансформации ксенобиотиков в печени [10]. Так, наличие атомов фтора в ближайшем наноструктурном аналоге наноалмаза - фуллерене (C60) - повышает его общую токсичность в 2, 4-5 раз [11]. Кроме того, фтор и его соединения способны накапливаться в различных объектах окружающей среды и присутствовать в них в различных количествах [12]. Поэтому глицин, иммобилизованный на частицах наноалмаза, которые содержат атомы фтора, нежелательно использовать в медицинской практике в качестве лекарственного средства.
Получение антидепрессанта, представляющего собой глицин, иммобилизованный на частицах детонационного наноалмаза, не содержащих атомов фтора, с повышенной дисперсностью в суспензии, применяемого в качестве лекарственного средства, а также снижение уровня экологической и эндоэкологической опасности, упрощение и удешевление его способа получения представляют собой актуальную и практически значимую задачу.
Использование глицина, иммобилизованного на частицах детонационного наноалмаза, как антидепрессанта в научной и патентной литературе не описано.
Целью изобретения является повышение эффективности антидепрессивного действия глицина без проявления каких-либо токсических воздействий и расширение номенклатуры антидепрессантов.
Поставленная цель решается с помощью применения описываемого в соответствии с изобретением средства с антидепрессивным действием, представляющего собой глицин, иммобилизованный на частицах детонационного наноалмаза размером 2-10 нм, не содержащих атомов фтора и имеющих оболочку толщиной до 1 нм, с содержанием глицина до 21 ± 3% масс., и способа его получения.
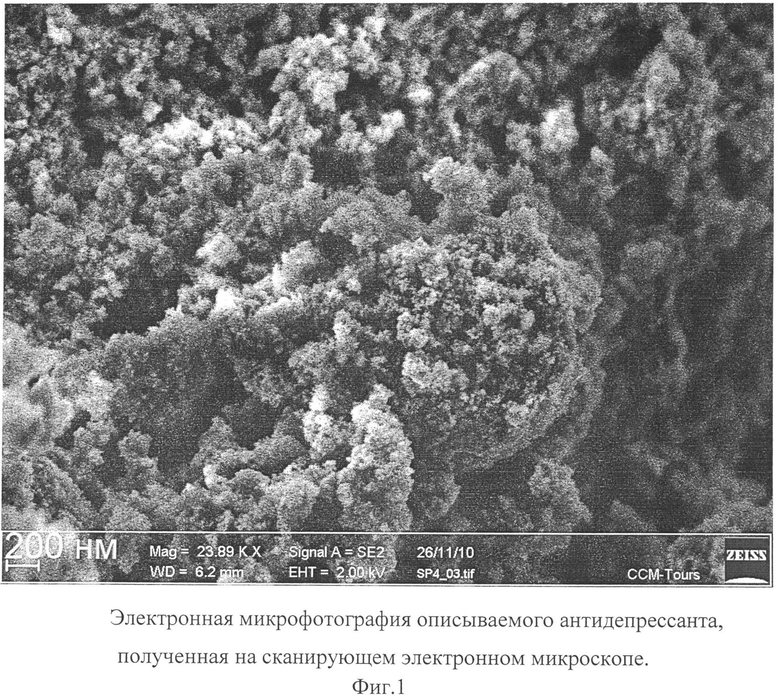
Описываемый антидепрессант в виде глицина, иммобилизованного на частицах детонационного наноалмаза, не содержащих на своей поверхности атомов фтора, представляет собой ультрадисперсный порошок (Фиг.1) темно-серого цвета или темно-серого цвета с зеленоватым или темно-синим оттенками с размером частиц от 2 до 10 нм, имеющих оболочку толщиной до 1 нм (Фиг.2), размером агрегатов в водной суспензии до 100 нм (Фиг.3) и содержанием глицина до 21±3 % масс., входящего в состав поверхностной оболочки.
На Фиг.1 отчетливо видно наличие у описываемого антидепрессанта ультрадисперсной структуры из частиц с размером, меньшим разрешающей способности использованного прибора (от 20 нм).
Микрофотография частиц описываемого антидепрессанта получена на автоэмиссионном сканирующем электронном микроскопе сверхвысокого разрешения Zeiss Ultra Plus (Carl Zeiss, Германия).
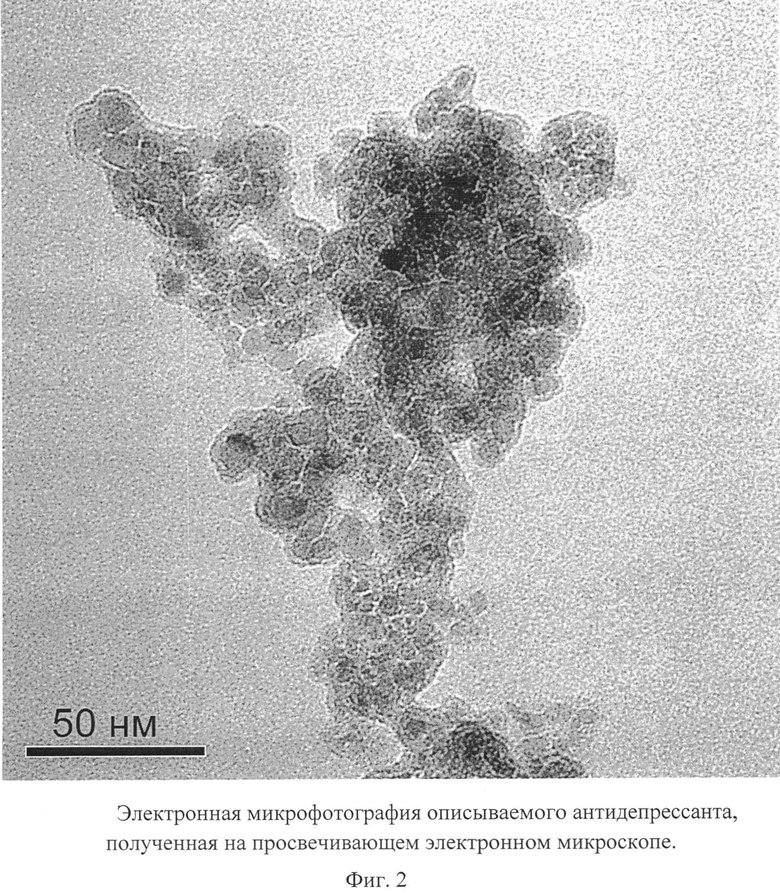
На Фиг.2 видно, что размер частиц описываемого антидепрессанта, покрытых оболочкой толщиной до 1 нм, равен 2-10 нм.
Микрофотография частиц описываемого антидепрессанта получена на просвечивающем электронном микроскопе Jeol 1011 (JEOL, Япония).
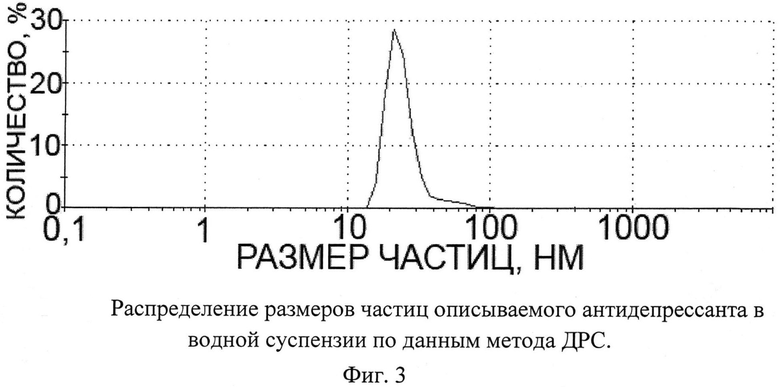
На Фиг.3. приведена кривая распределения размеров частиц в суспензии описываемого антидепрессанта, из которой следует, что размеры частиц в суспензии не превышают 100 нм.
Измерение распределения размера частиц описываемого антидепрессанта в суспензии проводили методом ДРС на приборе ZetaSizer (Malvem Instruments, США). По оси абсцисс отложена логарифмическая шкала размера частиц в нм. По оси ординат - процентное содержание частиц с определенными размерами.
Элементный состав поверхности частиц описываемого антидепрессанта по данным рентгенофотоэлектронной спектроскопии (РФЭС) приведен в табл.1.
Исследование поверхности описываемого антидепрессанта проводили на приборе LAS-3000 (Riber, Франция), оснащенном полусферическим анализатором ОРХ-150. Для возбуждения фотоэлектронов использовали немонохроматизированное рентгеновское излучение алюминиевого анода (AIKα=1486,6 эВ) при напряжении на трубке 12 кВ и токе эмиссии 20 мА. Калибровку фотоэлектронных пиков проводили по линии углерода C 1s с энергией связи 285 эВ. Вакуум в рабочей камере составлял 6,7·10-8 Па. Для получения высокого вакуума был использован ионный насос.
Количество глицина в описываемом антидепрессанте определяют следующим образом. Готовят смеси наноалмаза с разным содержанием глицина. Берут навески каждой смеси равной массы. Регистрируют их ИК-спектры, выбирают на них наиболее интенсивные характеристические сигналы, которые соотносят с полосами ИК-спектра исходного глицина. Затем строят калибровочные кривые зависимости интенсивности сигнала в ИК-спектре от содержания глицина в навеске. Далее по интенсивности выбранных характеристических полос исследуемого антидепрессанта по калибровочным кривым определяют количественное содержание в нем глицина. По полученным данным определяют среднее значение величины содержания глицина в описываемом антидепрессанте.
Описываемый способ получения антидепрессанта заключается в следующем. Детонационный наноалмаз отжигают в токе газообразного водорода при температуре 500-1200°С в течение 1-8 ч, затем подвергают жидкофазному хлорированию молекулярным хлором при фотохимическом воздействии видимым светом при температуре 50-70°С в течение 36-60 ч с последующей промывкой четыреххлористым углеродом, центрифугированием и сушкой под вакуумом. Модифицированный хлором наноалмаз растворяют в полярном растворителе с образованием суспензии. Добавляют третичный амин и глицин и обрабатывают полученную смесь ультразвуком в течение 5-60 мин с последующим выдерживанием при 50-80°С в течение 12-48 ч, центрифугированием, промывкой растворителем и сушкой. Обработку ультразвуком ведут в течение 5-60 мин, в качестве третичного амина используют триэтиламин и в качестве полярного растворителя применяют пиридин, низший алифатический спирт, водно-спиртовую смесь или воду.
Описываемый антидепрессант не содержит атомов фтора (табл.1), а также атомов других галогенов, в количестве, превышающем ошибку прибора (0,1 % ат.), так как в процессе получения антидепрессанта все атомы хлора заменяются на молекулы глицина и уходят с поверхности наноалмаза в виде молекул HCl.
В процессе фармакологических исследований была проведена работа по изучению специфического антидепрессивного действия описываемого лекарственного средства и его безвредности в сравнении с фармакопейным глицином.
Исследование антидепрессивной активности веществ было проведено согласно «Методическим указаниям по изучению активности веществ, обладающих антидепрессивной активностью» [13]. Для моделирования депрессивно-подобного состояние было использовано два базисных теста: поведенческое отчаяние мышей по Porsolt [14] и поведенческая беспомощность крыс по Nomura [15, 16], которые широко используются при поиске и изучении веществ с антидепрессивной активностью как в России, так и за рубежом.
Исследование антидепрессивной активности по методике Porsolt было выполнено на белых беспородных половозрелых мышах самцах массой 25-28 г (4 группы по 10 мышей).
Животное помещали в сосуд с водой таким образом, чтобы оно не могло выбраться или найти в нем опору. Попадая в воду, животные проявляли активность, направленную на поиск выхода из аверсивной стрессорной ситуации, но затем оставляли эти попытки и зависали в воде в характерной позе, оставаясь или неподвижными или совершая незначительные движения, необходимые для поддержания морды над поверхностью воды. Такое поведение расценивалось как проявление депрессивного состояния - отчаяния и подавленности. Показателем выраженности депрессивно-подобного состояния по данному тесту являлась длительность неподвижности (иммобилизация) в течение 6 мин. Воздействие веществ с антидепрессивной активностью уменьшает длительность иммобилизации и увеличивает время активного плавания.
Описываемый антидепрессант в дозах 0,5 и 1 мг/кг статистически достоверно уменьшал в 1,55 раза время иммобилизации и увеличивал время активного плавания (табл.3), что свидетельствует о наличии у описываемого антидепрессанта отчетливого антидепрессивного действия. В свою очередь фармакопейный глицин в дозе 1 мг/кг на уровне тенденции уменьшал время иммобилизации и увеличивал время активного плавания, однако изменение показателей было статистически недостоверным (табл.3).
Таким образом, в тесте поведенческого отчаяния по Porsolt описываемый антидепрессант оказывал отчетливый антидепрессивный эффект, превосходящий антидепрессивную активность фармакопейного глицина.
Исследование антидепрессивной активности по методике Nomura проводили на белых беспородных крысах самцах массой 270-290 г (5 групп по 10 крыс).
В сосуд с водой, снабженный колесами, помещали животное, которое старалось выбраться с помощью колес. Количество оборотов колес является объективной мерой активности животных. Поскольку колеса вращались свободно, эти попытки оставались бесуспешными, и у животных развивалось депрессивно-подобное состояние, которое выражалось в отказе от борьбы. Вещества с антидепрессивной активностью облегчают это состояния, повышая число оборотов колес. Чем ниже число оборотов колес, тем более выраженнее депрессивно-подобное состояние. Число оборотов колес регистрировали в течение 5 мин.
Установлено, что описываемый антидепрессант в дозе 1 мг/кг проявлял отчетливую антидепрессивную активность, о чем свидетельствовало статистически достоверное увеличение (в 1,6 раза) числа оборотов колес по сравнению с показателями контрольных животных (табл.4). Фармакопейный глицин в дозе 1 мг/кг не вызывал увеличения оборотов колес, что свидетельствует об отсутствии у него антидепрессивного действия. Амитриптилин в дозе 10 мг/кг достоверно увеличивал число оборотов колес в 1,5 раза. Флуоксетин в дозе 20 мг/кг достоверно увеличивал число оборотов колес в 1,3 раза по сравнению с контролем (табл.4).
Таким образом, описываемый антидепрессант в дозе 1 мг/кг обладает достоверным отчетливым антидепрессивным эффектом в тесте поведенческой беспомощности (вынужденного плавания) в сосуде с вращающимися колесами по Nomura и в существенно меньшей дозировке не уступает по глубине эффекта эталонным препаратам - амитриптилину в дозе 10 мг/кг и флуоксетину в дозе 20 мг/кг.
Исследование острой токсичности описываемого антиоксиданта было проведено согласно Методическим указаниям по изучению острой токсичности, изложенным в [15].
При проведении эксперимента регистрировались следующие показатели: характер шерстяного покрова, изменение состояния слизистых оболочек, птоз верхнего века, повышенная уринация, повышенная дефекация, повышенная саливация, пилоэрекция, вокализация, боковое положение, ритм и глубина дыхательных движений, агрессивность, пугливость, тремор, судороги, изменение порогов болевой реакции, изменение позы, каталепсия, нарушение координации движений в тесте вращающегося стержня, удерживание в течение 5 с на перевернутой сетчатой платформе, перелезание с перевернутой сетчатой платформы наверх, наличие пинеального, роговичного рефлексов, седации, стереотипии и груминга, гибель животного.
Статистическая обработка результатов была осуществлена с помощью статистических пакетов "BioStat" для Windows. Рассчитывали средние показатели по группе и стандартные ошибки показателей.
Полученные результаты убедительно показывают, что описываемый антидепрессант при внутрибрюшинном введении мышам в дозах 75, 150 и 225 мг/кг, так же как и фармакопейный глицин, не вызывает признаков интоксикации и гибели животных на протяжении 14 сут наблюдения.
Краткое описание чертежей
Фиг.1 - электронная микрофотография описываемого антидепрессанта, полученная на сканирующем электронном микроскопе.
Фиг.2 - электронная микрофотография описываемого антидепрессанта, полученная на просвечивающем электронном микроскопе.
Фиг.3 - распределение размеров частиц описываемого антидепрессанта в водной суспензии по данным метода ДРС.
Фиг.4 - ИК-спектры смесей наноалмаза с глицином, используемых для построения калибровочных кривых. I, II, III - спектры смесей с содержанием глицина 1:1,75:2,5 соответственно. В рамках выделены характеристические пики.
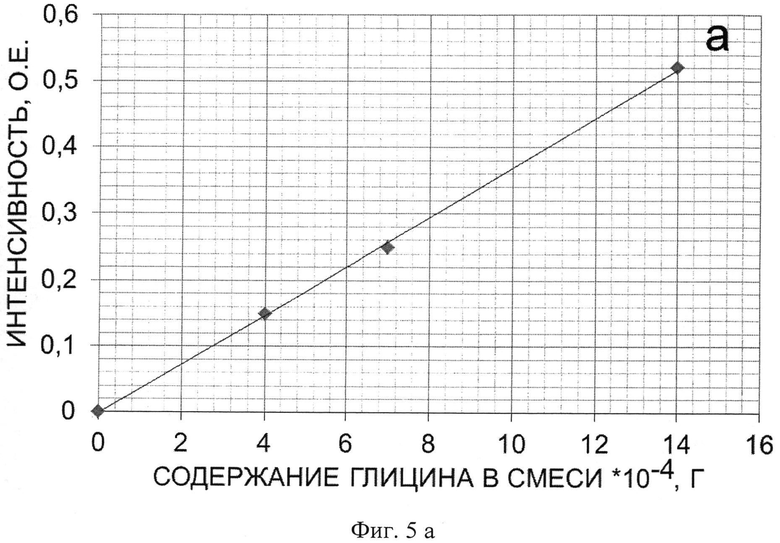
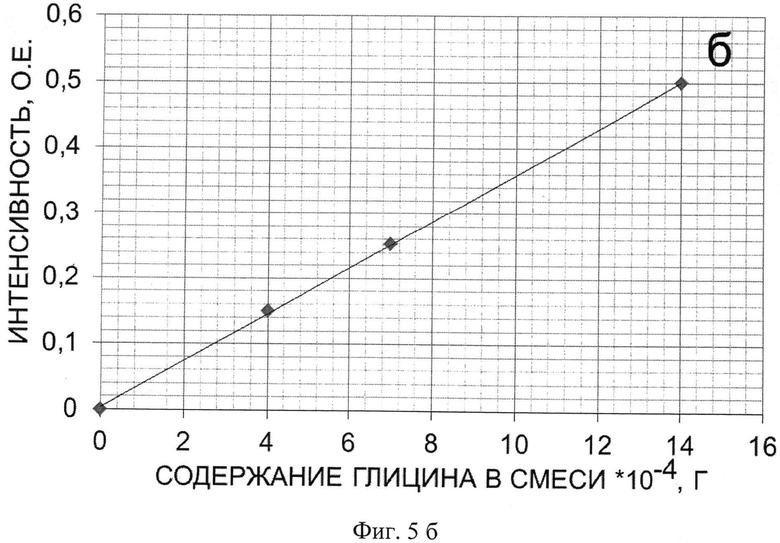
Фиг.5 - калибровочные кривые для каждой характеристической полосы ИК-спектра смеси наноалмаза с глицином, а, б, в - калибровочные кривые для полос 1407, 1332 и 504 см-1 соответственно.
Изобретение иллюстрируется следующими примерами.
Пример 1
300 мг исходного детонационного наноалмаза отжигают в токе газообразного водорода со скоростью 3,0 л/ч при температуре 1000°С в течение 6 ч. Затем отожженный наноалмаз подвергают жидкофазному хлорированию молекулярным хлором, растворенным в 40 мл CCl4 до 6% масс. Cl2. Реакцию хлорирования проводят при фотохимическом воздействии видимым светом в течение 60 ч при температуре 60°С. Затем образец промывают CCl4 с центрифугированием суспензии при 6000 об/мин и высушивают под давлением 0,1 мм рт.ст. до постоянного веса. Затем из хлорированного наноалмаза получают суспензию, используя 40 мл водно-спиртовой смеси (вода:метанол=1:1), в которую вносят 300 мг глицина в виде свободной аминокислоты (NH2CH2COOH) с добавлением 1 мл триэтиламина. Полученную смесь обрабатывают ультразвуком (50 Вт) в течение 60 мин и выдерживают при постоянном перемешивании при температуре при 65°С в течение 30 ч. Полученный продукт промывают большим количеством этанола, центрифугируют и высушивают под вакуумом при 70°С в течение всей ночи. Остаточная влажность продукта составляет 2,2%. Выход целевого продукта составляет 279 мг (93 %). Продукт представляет собой темно-серый с синеватым оттенком ультрадисперсный порошок (Фиг.1) с размерами первичных частиц 2-10 нм (Фиг.2), имеющих оболочку поверхностного слоя до 1 нм. В суспензии размер частиц порошка не превышает 100 нм (Фиг.3). Элементный состав поверхности частиц полученного продукта приведен в табл.2.
Для определения массовой доли глицина в полученном продукте готовят 3 смеси наноалмаза с глицином, с содержанием последнего 1:1,75:3,5 соответственно. Для каждой смеси берут навеску массой 0,0035 г и тщательно перетирают в ступке с 0,090 г KBr. 0,070 г полученной смеси прессуют в таблетку и снимают ее ИК-спектр (Фиг.4). Характеристические полосы выбирают при 1407, 1332 и 504 см-1 соответственно и строят для них калибровочные графики (Фиг.5). Интенсивность соответствующих характеристических полос на ИК-спектре полученного образца массой 0,0035 г составила 0,23, 0,22 и 0,10 о.е. соответственно. Из калибровочных кривых а, б, в на Фиг.5 определяют величину содержания глицина в полученном образце, которая составляет 0,00057±8-10-5 г. Следовательно, массовая доля глицина в навеске образца составляет 21±3% масс.
Пример 2
Изучение специфического фармакологического действия описываемого антидепрессанта
Исследования было выполнены на белых беспородных половозрелых мышах самцах массой 25-28 г, разделенных на 4 группы по 10 животных (по методике Porsolt), и белых беспородных крысах самцах массой 270-290 г, разделенных на 5 групп по 10 животных (по методике Nomura). Всего в эксперименте участвовало 90 животных.
Животных получали из Центрального питомника лабораторных животных «Столбовая», Московская область. Содержание животных соответствовало правилам лабораторной практики при проведении доклинических исследований в РФ (ГОСТ 3 51000.3-96 и 51000.4-96), нормативному документу «Санитарные правила по устройству, оборудованию и содержанию вивариев», утвержденных Главным Государственным санитарным врачом 06.04.1973 г. №1045-73, и Приказу МЗ РФ №267 от 19.06.2003 г. «Об утверждении правил лабораторной практики» (GLP) с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997 г.). Животные содержались в виварии при температурном режиме 20-22°С, при световом цикле - 12 часов светлый и 12 часов темный периоды, в пластмассовых клетках Т/4А размером 580×375×200 мм с верхней крышкой из нержавеющей стали и подстилкой обеспыленной из деревянной стружки. Животные содержались при постоянном доступе к корму и воде с использованием полного рациона экструдированного брикетированного корма (ГОСТ на корм Р 50258-92) и питьевой воды. При проведении экспериментов учитывались требования Комиссии по проблеме этики отношения к животным Российского национального Комитета по биоэтике при Российской академии наук и этические нормы, изложенные в «Международных рекомендациях по проведению медико-биологических исследований с использованием животных» (1985 г.). Опыты проводили в первую половину дня.
В тесте по Portsol установка для создания депрессивно-подобного состояния (поведенческого отчаяния) у мышей представляла собой сосуд цилиндрической формы диаметром 10 см и высотой 30 см. Сосуд наполняли водой с поддерживаемой температурой 27°С до уровня высоты 18 см. Животное помещали в сосуд с водой таким образом, что оно не могло ни выбраться из сосуда, ни найти в нем опору. Попадая в воду, животное начинало проявлять бурную двигательную активность, направленную на поиск выхода из аверсивной стрессорной ситуации, но затем оставляло эти попытки и зависало в воде в характерной позе, оставаясь полностью неподвижными или совершая незначительные движения, необходимые для поддержания морды над поверхностью воды. Это поведение расценивалось как проявление отчаяния, подавленности, депрессивного состояния. Показателем выраженности депрессивно-подобного состояния по данному тесту являлась длительность неподвижности (иммобилизации) в течение 6 мин. Вещества с антидепрессивной активностью уменьшают длительность иммобилизации и увеличивают время активного плавания.
Описываемый антидепрессант исследовали в сравнении с фармакопейным глицином. Вещества вводили внутрибрюшинно однократно в объеме 0,1 мл на 10 г веса мыши за 30 мин до эксперимента. Животным контрольной группы вводили дистиллированную воду. Статистическая обработка результатов была осуществлена с помощью статистических пакетов "BioStat" для Windows. Рассчитывали средние показатели по группе и стандартные ошибки показателей.
Установлено, что контрольные крысы при помещении их в сосуд с водой сначала начинали совершать активные плавательные движения для того, чтобы выбраться из сосуда, а затем их прекращали и начинали зависать в воде, совершая незначительные гребущие движения для поддержания головы над поверхностью воды. Период иммобилизации (неподвижности) у контрольных животных составил в среднем 283,4 с, а время активного плавания - 58,3 с (табл. 3).
∗ - р<0,05 достоверность различий по критерию Манна-Уитни в сравнении с группой контроля.
Описываемый антидепрессант в дозах 0,5 и 1 мг/кг статистически достоверно уменьшал в 1,55 раза время иммобилизации и увеличивал время активного плавания (табл.3), что свидетельствует о наличии у него отчетливого антидепрессивного действия.
Фармакопейный глицин в дозе 1 мг/кг на уровне тенденции уменьшал время иммобилизации и увеличивал время активного плавания, однако изменение показателей было статистически недостоверным (табл.3).
Таким образом, в тесте поведенческого отчаяния по Portsol описываемый антидепрессант проявляет отчетливый антидепрессивный эффект, тогда как фармакопейный глицин не оказывает достоверного антидепрессивного эффекта.
Для оценки антидепрессивного эффекта описывемого антидепрессанта по методике Nomura для неизбегаемого вынужденного плавания использовали сосуд с вращающимися колесами. Установка представляла собой сосуд размером 64×30×42 см, разделенный на 4 равных отсека. В каждом отсеке находятся колеса диаметром 10 см и шириной 11 см, имеющие 12 лопастей шириной 2 см. На краях каждого колеса укреплены магниты, а над колесами - герконы, которые срабатывают каждый раз, когда магнит проходит под ними и, таким образом, происходит автоматическая регистрация оборотов колес, которая является объективной мерой активности животных. Сосуд заполняли водой с температурой 25°С до середины колес.
Крыс помещали в сосуд с водой в каждый отсек мордой от колеса, с помощью которого животные старались выбраться из воды. Поскольку колеса вращались свободно, эти попытки оставались безуспешными, и у животных развивалось депрессивно-подобное состояние, которое выражалось в отказе от борьбы. Мерой депрессивно-подобного состояния являлось число оборотов колеса (чем ниже число оборотов, тем более выражено это состояние). Число оборотов колес регистрировали в течение 5 мин с помощью специальных герконовых электромеханических датчиков.
Описываемый антидепрессант исследовали в сравнении с фармакопейным глицином и эталонными антидепрессантами -амитриптилином и флуоксетином. Вещества вводили внутрибрюшинно однократно в объеме 0,1 мл на 10 г веса мыши за 30 мин до эксперимента. Животным контрольной группы вводили дистиллированную воду. Статистическая обработка результатов была осуществлена с помощью статистических пакетов "BioStat" для Windows. Рассчитывали средние показатели по группе и стандартные ошибки показателей.
Установлено, что контрольные крысы совершали в среднем 52 оборота колес за 5 мин регистрации (табл.4). Описываемый антидепрессант в дозе 1 мг/кг проявлял отчетливую антидепрессивную активность, о чем свидетельствовало статистически достоверное увеличение в 1,6 раза числа оборотов колес по сравнению с показателями контрольных животных (табл. 4).
Фармакопейный глицин в дозе 1 мг/кг не вызывал увеличения оборотов колес, что свидетельствует об отсутствии у него антидепрессивного действия. Амитриптилин в дозе 10 мг/кг достоверно увеличивал число оборотов колес в 1,5 раза. Флуоксетин в дозе 20 мг/кг достоверно увеличивал число оборотов колес в 1,3 раза по сравнению с контролем (табл. 4).
Таким образом, описываемый антидепрессант в дозе 1 мг/кг (внутрибрюшинно, однократно) обладает достоверным отчетливым антидепрессивным эффектом в тесте поведенческой беспомощности (вынужденного плавания) в сосуде с вращающимися колесами по Nomura и в существенно меньшей дозе не уступает по глубине эффекта эталонным препаратам - амитриптилину в дозе 10 мг/кг и флуоксетину в дозе 20 мг/кг. При этом фармакопейный глицин в дозе 1 мг/кг не обладает антидепрессивным эффектом в тесте по Nomura.
Пример 3
Изучение побочных эффектов и токсического действия описываемого антидепрессанта
Исследование проводили на белых беспородных половозрелых мышах-самцах массой 20-24 г возрастом 2-3 месяца. Всего использовалось 42 животных - 7 групп по 6 мышей.
Регистрацию возможных побочных эффектов, признаков интоксикации и гибели животных проводили через 1 ч-14 сут после внутрибрюшинного введения описываемого антидепрессанта в сравнении с фармакопейным глицином в тех же дозах.
В результате исследования было установлено, что описываемый антидепрессант при внутрибрюшинном введении мышам в дозах 75, 150 и 225 мг/кг не вызывал признаков интоксикации и гибели животных на протяжении 14 сут (табл.5-7). При этом описываемый антидепрессант также не вызывал у мышей изменения шерстяного покрова, состояния слизистых оболочек. Также отсутствовали птоз верхнего века, повышенная уринация, дефекация, саливация, пилоэрекция, вокализация, боковое положение. В пределах нормы были ритм и глубина дыхательных движений, отсутствовали агрессивность, пугливость, тремор, судороги, каталепсия, стереотипия и груминг. Не наблюдалось изменения позы. У животных были сохранены пинеальный, роговичный и болевой рефлексы. На протяжении всех 14 сут наблюдения животные удерживались на перевернутой сетчатой платформе в течение 5 с (табл.5-7).
Список литературы
1. У.З. Поттер, Л.Е. Холлистер. Антидепрессанты. В кн. Б.Г. Катцунг. Базисная и клиническая фармакология: В 2 т. T.1 / Пер. с англ. 2-е изд. перераб. и доп. - М., СПб.: Из-во Бином, Изд-во «Диалект». 2007 С.578-593.
2. С.Н. Мосолов, А.Б. Смулевич, Ю.Л. Нуллер и др. Новые достижения в терапии психических заболеваний / Под ред. С.Н. Мосолова. - М.: Изд-во Бином, 2002. 451 с.
3. С.Б. Середенин, Т.А. Воронина, Г. Г. Незнамов, В.П. Жердев. Феназепам: 25 лет в медицинской практике. М.: Медицина, 2007. 382 с.
4. Депрессии и коморбидные расстройства / Под ред. А.Б. Смулевича. - М.: Медицина, 1997. 308 с.
5. М.Д. Машковский. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна: Издатель Умеренков, 2012. С.661.
6. И.А. Комиссарова, Я.Р. Нарциссов. Молекулярные механизмы действия лекарственного препарата «Глицин» // Terra medica. 2001. №1. С.23-25.
7. А.Ю. Беспалов, Э.Э. Звартау. Нейропсихофармакология антагонистов NMDA-рецепторов. - СПб.: Невский Диалект, 2000. 297 с.
8. US Pat 7820130 B2. 24.11.2004.
9. Y. Liu, Zh. Gu, J.L. Margrave, V.N. Khabashesku. Functionalization of Nanoscale Diamond Powder: Fluoro-, Alkyl-, Amino-, and Amino Acid-Nanodiamond Derivatives // Chem. Mater. 2004. V.16. P.3924-3930.
10. Российская энциклопедия по охране труда. В 3 т. 2-е изд., перераб. и доп. Т.3. - М.: Изд-во. НЦ ЭНАС. 2007. С.181.
11. Н.Н. Каркищенко. Биомедицина, 2009. № 2. С.5-26.
12. Т.И. Шалина, Л.С. Васильева. Общие вопросы токсического действия фтора // Сибирский медицинский журнал. 2009. №5. С.5-9.
13. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ/ Под ред. Р.У. Хабриева - М.: Изд-во Медицина, 2005. С.244-253.
14. Porsolt R.D., Anton G., Blavet N. et al. Behavioral despair in rats: a new model sensitive to anti depressant treatment. // Europ. J. Pharmacol. 1978, 47, 379-391.
15. Г.М. Молодавкин, Т.А. Воронина, А.Л. Мдзинаришвили. Особенности влияния фармакологических веществ разных классов на вынужденное плавание у крыс // Эксперим. и клин. фармакология. 1994. Т.57. № 1. С.3-5.
16. S. Nomura, J. Shimizu, М. Kinjo et al. A new behavioral test for antidepressant drugs // Eur. J. Pharmacol. 1982. V.83. № 3-4. P.171-175.
17. Руководство по проведению доклинических исследований лекарственных средств 4.1. ФГБУ «НЦЭМСП». - М.: Изд-во Гриф и К, 2012. 244 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ АЛКОГОЛИЗМА | 2014 |
|
RU2574001C1 |
| АНКСИОЛИТИК И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2519755C1 |
| ПРОТИВОСУДОРОЖНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2508098C1 |
| СЕДАТИВНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2506075C1 |
| АНТИГИПОКСАНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2506074C1 |
| АНТИПСИХОТИЧЕСКОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2519761C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ НАРУШЕНИЙ СНА | 2014 |
|
RU2566713C1 |
| АНТИОКСИДАНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2519760C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ РАССТРОЙСТВ АУТИСТИЧЕСКОГО СПЕКТРА | 2015 |
|
RU2608444C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОИНСУЛИТНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2521404C1 |



Изобретение относится к области медицины, в частности к фармакологии и фармацевтике, и касается антидепрессанта, представляющего собой аминокислоту глицин, иммобилизованную на частицах детонационного наноалмаза размером 2-10 нм, и способа его получения. Антидепрессант обладает повышенной эффективностью. 2 н. и 2 з.п. ф-лы, 7 ил., 7 табл., 2 пр.
1. Антидепрессант, представляющий собой глицин, иммобилизованный на частицах детонационного наноалмаза размером 2-10 нм, имеющих оболочку толщиной до 1 нм, с содержанием глицина до 21±3% масс.
2. Способ получения антидепрессанта по п.1, характеризующийся тем, что детонационный наноалмаз отжигают в токе газообразного водорода при температуре 500-1200°С в течение 1-8 ч, подвергают жидкофазному хлорированию молекулярным хлором при фотохимическом воздействии видимым светом при температуре 50-70°С в течение 36-60 ч с последующей промывкой четыреххлористым углеродом, центрифугированием и сушкой, полученный модифицированный хлором наноалмаз растворяют в полярном растворителе с образованием суспензии, добавляют третичный амин и глицин, полученную смесь обрабатывают ультразвуком с последующим выдерживанием при 50-80°С, центрифугированием, промывкой растворителем и сушкой.
3. Способ по п.2, где обработку ультразвуком ведут в течение 5-60 мин и выдерживание при 50-80°С осуществляют в течение от 12 до 48 ч.
4. Способ по п.2 или 3, где в качестве третичного амина используют триэтиламин и в качестве полярного растворителя используют пиридин, низший алифатический спирт, водно-спиртовую смесь или воду.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ НА ОСНОВЕ ГЛИЦИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2457835C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИСТРЕССОВЫМ, СТРЕССПРОТЕКТОРНЫМ, НООТРОПНЫМ, АНТИАЛКОГОЛЬНЫМ И АНТИНАРКОТИЧЕСКИМ ДЕЙСТВИЕМ, СПОСОБЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ С ЕГО ИСПОЛЬЗОВАНИЕМ | 1994 |
|
RU2099078C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-ГЛИЦИНА ИЗ РАСТВОРОВ | 2011 |
|
RU2471372C1 |
Авторы
Даты
2014-06-20—Публикация
2013-01-25—Подача