Перекрестные ссылки
В данной заявке на изобретение заявлен приоритет предварительной заявки на патент США №61/134510, поданной 10 июля 2008 года, полное описание которой включено здесь путем специфической ссылки.
Предшествующий уровень техники
1. Область техники
Изобретение относится к способу лечения глазных и/или кожных заболеваний и состояний при помощи новых производных циклоспорина. В частности, настоящее изобретение относится к способу лечения вододефицитного состояния "сухого глаза", факоанафилактического эндофтальмита и увеита с использованием некоторых новых циклоспориновых производных.
2. Описание родственной области техники
Открытая часть нормального глаза покрыта тонкой слезной пленкой. Присутствие непрерывной слезной пленки важно для нормального состояния роговицы и конъюнктивального эпителия и придает роговице поверхность с оптически высоким качеством. Дополнительно, водная часть слезной пленки действует в качестве смазки век во время моргания. Кроме того, известно, что некоторые ферменты, содержащиеся в слезной жидкости, например, иммуноглобулин A, лизоцим и бета-лизин, обладают бактериостатическими свойствами.
Здоровая лакримальная система функционирует с образованием и поддержанием правильным образом структурированной непрерывной слезной пленки. Слезный орган состоит из секреторной системы (источник), системы распределения и системы секреции (сток). В секреторной системе водянистые слезы выделяются основными и вспомогательными слезными железами.
Основная масса слезной пленки образована такими водянистыми слезами. Непрерывная продукция и отвод водянистой слезы важны для поддержания эпителия роговицы и конъюнктивы во влажном состоянии, поступления питательных веществ для эпителиального дыхания, поступления бактериостатических агентов и очистке глазной поверхности благодаря промывающему действию движения слезы.
Аномалии слезной пленки включают абсолютный или частичный дефицит продукции водянистой слезы (сухой кератоконъюнктивит или СКК).
В относительно слабых случаях главный симптом СКК представляет собой ощущение инородного тела или слабое царапанье. Последнее может прогрессировать, становясь постоянным, интенсивным жжением или раздражающим ощущением, которое может быть изнурительным для пациента.
Более тяжелые формы могут прогрессировать до развития филаментозного кератита, представляющего собой болезненное состояние, характеризующееся появлением многочисленных нитей или филаментов, присоединенных к поверхности роговицы. Данные свидетельствуют о том, что эти филаменты представляют разрывы в непрерывности нормальных эпителиальных клеток роговицы. Сдвиг, создаваемый движением век, тянет эти филаменты, причиняя боль. Лечение этой стадии СКК является очень трудным.
Частое осложнение СКК представляет собой вторичную инфекцию. По-видимому, возникает несколько расстройств в нормальных защитных механизмах глаза, возможно относящихся к уменьшению в концентрации антибактериального лизоцима в водянистых слезах пациента, страдающего от СКК.
Хотя СКК может развиться в отсутствие любой другой выраженной системной аномалии, существует частая ассоциация СКК с системным заболеванием. СКК может возникнуть как часть большей системной вовлеченности, известной как синдром Шегрена. Он классически состоит из сухости глаз, сухости во рту и артрита.
Гистологически, при СКК (как часть синдрома Шегрена или самостоятельно) начальные изменения, обнаруженные в слезных железах, представляют собой изменения фокальных лимфоцитарных и инфильтратов клеток плазмы крови, ассоциирующиеся с дегенерацией железистой ткани. Эти изменения напоминают изменения, обнаруженные при аутоиммунном заболевании в другой ткани, давая начало предположению о том, что у СКК есть аутоиммунная основа.
Синдром Шегрена рассматривают как дисфункцию экзокринной железы. Характерно, что слезные железы демонстрируют инфильтрацию одноядерных клеток, которая в конечном счете приводит к разрушению железистой структуры.
Традиционное лечение СКК является симптоматическим. Обычно, состояния сухости глаз с водным дефицитом лечат путем дополнения слез искусственными заменителями слез. Тем не менее, облегчение ограничивается временем удерживания вводимого в глаз искусственного раствора слезы. Как правило, действие искусственного раствора слезы, вводимого в глаз, угасает в течение приблизительно от тридцати до сорока пяти минут. Таким образом, действие таких продуктов, будучи исходно мягким, не длится достаточно долго. Пациенту причиняет беспокойство необходимость повторного введения искусственного раствора слезы в глаз, что необходимо для дополнения нормальных слез. Кроме того, такое лечение просто действует для облегчения симптомов состояния сухости глаз и не вылечивает какие-либо лежащие в основе расстройства или причины состояния сухости глаз.
Гистологические исследования слезных желез у пациентов, страдающих от синдрома Шегрена, продемонстрировали некоторое доказательство воспаления слезной железы. Такое воспаление может произойти просто из-за естественного старения пациента. Предположили, что использование противовоспалительных средств могло бы служить для уменьшения железистого воспаления. Системное использование кортикостероидов пропагандировали при этих состояниях. Тем не менее, положительный эффект системных кортикостероидов в состояниях сухости глаз не был доказан. В большинстве случаев сухости глаз опасности длительного использования противовоспалительных средств, по-видимому, перевешивают их возможное достоинство.
Для лечения состояний сухости глаз также предлагались операции. В случае существенного разрушения конъюнктивы, пропагандировались трансплантации слизистой оболочки. Также предположили, что трансплантация протока околоушной (слюнной) железы могла быть полезной для лечения сухости глаз. Тем не менее, хирургические изменения для борьбы с состояниями сухости глаз представляют собой исключительное средство и, любая польза, возникающая в результате этих изменений, является сомнительной.
Было также предложено вводить перорально разведенный раствор пилокарпина для стимулирования автономной нервной системы, чтобы осуществить увеличенную продукцию водянистой слезы. Этот способ лечения не является универсальным из-за множества неприятных побочных действий пилокарпина после его проглатывания.
Модели синдрома Шегрена у животных были определяющими для основного офтальмологического исследования. Болезнь, подобная синдрому Шегрена, обнаружена у собак с системным люперитематозом. Это заболевание, которая может упоминаться как собачий СКК, является общим, хроническим, прогрессирующим и потенциально приводящим к слепоте заболеванием. Множество поражений роговицы и повреждений конъюнктивы является результатом состояния сухости глаз. Причина собачьего СКК часто не идентифицируется. Обычно собачий СКК представляет собой не отдельное офтальмологическое заболевание. В Kaswan et al., Am. J. Vet. Res. 46, 376-383 (1985) обсуждается, что большинство случаев собачьего СКК протекает через аутоиммунные механизмы.
Другие болезни глаза включают факоанафилактический эндофтальмит и увеит. Эти болезни могут быть локализованы по всему глазу в задней и передней камерах глаза, а также как в стекловидном теле.
Увеит, представляющий собой воспаление сосудистой оболочки глаза, ответственен приблизительно за 10% нарушения зрения в Соединенных Штатах. Факоанафилактический эндофтальмит представляет собой аутоиммунное заболевание у людей.
Панувеит относится к воспалению всего увеального (сосудистого) слоя глаза. Увеит задней камеры глаза, как правило, относится к хориоретиниту, а увеит передней камеры глаза относится к иридоциклиту. Воспалительные продукты (то есть клетки, фибрины, избыточные белки) этих воспалений, как правило, обнаруживаются в жидких пространствах в глазу, то есть передней камере глаза, задней камере глаза и стекловидном теле, а также проникая в ткань, тесно вовлеченную в воспалительный ответ. Увеит может возникать после хирургического или травматического повреждения глаза; как компонент аутоиммунного расстройства, то есть ревматоидного артрита, болезни Бехчета, анкилозирующего спондилита, саркоидоза; в виде отдельного опосредованного иммунной системой глазного расстройства, то есть промежуточного увеита, иридоцистита и т.д., не связанного с известными этиологиями; и после некоторые системных заболеваний, которые вызывают отложение комплексов антитела-антигена в увеальных тканях. Вместе эти расстройства представляют собой неинфекционные увеиты.
Нормальный глаз защищен от иммунного контроля кровяными барьерами, которые не дают возможность для свободной миграции клеток или белков в глаз. Когда глаз поврежден или когда возникает васкулит, тогда внутренние глазные структуры подвергаются воздействию общей иммунной системы и часто вызывают аутоиммунные ответы.
Соединения по этому изобретению также полезны при лечении кожных заболеваний и состояний. Обнаружено, что соединения по данному изобретению могут быть использованы для лечения баланита, например неспецифического воспалительного рецидивирующего баланита. См. "Pimecrolimus 1% Cream in Non-Specific Inflammatory Recurrent Balanitis" by S.Georgala et al., Dermatology 2007;215:209-212. Соединения по данному изобретению могут быть использованы для лечения псориаза и атопического дерматита (см. "Cyclosporin Greatly Improves the Quality of Life of Adults with Severe Atopic Dermatitis. A Randomized, Double-Bind, Placebo Controlled Trial" by MS Salek et al., Br J Dermatol 1993:129:422-430 и Physicians' Desk Reference: PDR-Gengraf Capsules (Abbot) соответственно).
Факоанафилаксия представляет собой тяжелую форму увеита, при котором хрусталик представляет собой вызывающий антиген. Белки хрусталика в норме отделены капсулой хрусталика до рождения. Когда эти белки высвобождаются в глаз при повреждении или хирургическом вмешательстве, или изредка при развитии катаракты, они могут стать сильно антигенными и вызвать аутоиммунный ответ. Если ответ умеренный, то он обнаруживается как хронический увеит. Если он очень быстро прогрессирует, то глаз становится сильно воспаленным во всех сегментах. Этот последний ответ называют факоанафилаксией.
Метилтиозамещенный циклоспорин A и другие алкилтиозамещенные производные циклоспорина А описаны в заявке РСТ №98-379455, 98-379456 и 98-379457 и, как обнаружили, являются активными против некоторых ретровирусов, в частности СПИД (синдром приобретенного иммуннодефицита) и ССК (связанный со СПИДОм комплекс) при введении перорально, парентерально, ректально или путем ингаляции.
Дополнительно, в общем обнаружено, что они обладают только очень слабым иммуносупрессирующим действием и демонстрируют антиретровирусную активность при не цитотоксических и не цитостатических концентрациях. Заявлено, что эти соединения обладают синергистическим действием с другими агентами, активными против ретровируса (такими как ингибиторы обратной транскриптазы, протеазы, интегразы, репликации HIV и нуклеокапсида).
Эти соединения также заявлены для применения при лечении глазных заболеваний и состояний в патентах США №№6350442 и 6254860.
Одна из задач данного изобретения заключается в том, чтобы предложить новые производные циклоспорина A для лечения глазных заболеваний и состояний, такие как сухость глаза.
Еще одна задача изобретения заключается в том, чтобы предложить новые производные циклоспорина A.
Еще одна задача изобретения представляет собой лечение кожных заболеваний и/или состояний, таких как баланит.
Еще одна задача изобретения представляет собой лечение кожных состояний, таких как псориаз и атопический дерматит.
Другие задачи данного изобретения станут очевидными из чтения настоящего описания изобретения.
Краткое описание изобретения
В настоящем изобретении предложен способ лечения глазного расстройства или состояния глаза, например, вододефицитного состояния сухого глаза, увеита или факоанафилактического эндофтальмита, включающий стадию введения в глаз терапевтически эффективного количества соединения, выбранного из группы, состоящей из производных циклоспорина A, имеющих нижеописанную формулу. В настоящем изобретении предложен способ лечения кожного расстройства или кожного состояния, например баланита или псориаза, или атопического дерматита, включающего стадию введения в глаз терапевтически эффективного количества соединения, выбранного из группы, состоящей из производных циклоспорина A. Производные циклоспорина A, использованные в способе(ах) по настоящему изобретению, представлены формулой
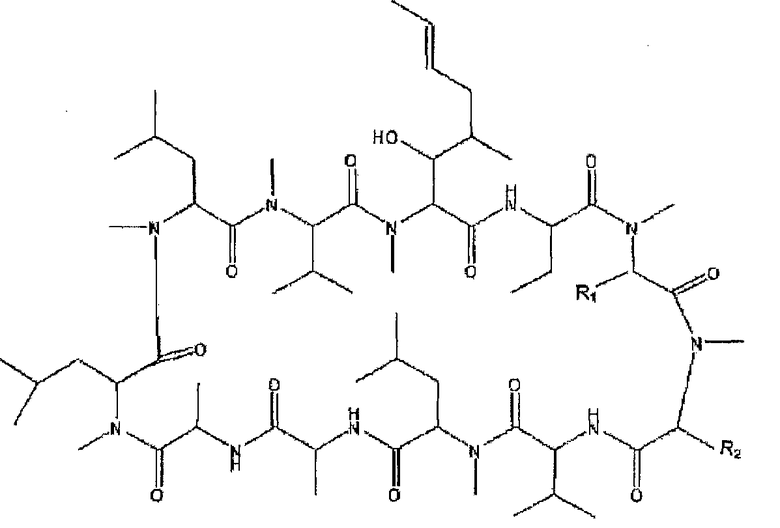
где R1 представляет собой S-Alk-R, где Alk представляет собой алкиленовую связь, предпочтительно метиленовую или полиметиленовую связь, например C2-C6 полиметиленовую связь или полиалкениленовую связь, например C3-C6 алкениленильную связь и R представляет собой -N=C(NR3R4)(NR5R6) или
-NR7[(NR3R4)C=NR5], т.е. гуанидины или -N=C(R8)(NR9R10), т.е. амидины, где R3-R10 представляет собой H, Alk, Ar или (CH2)nAr, где Ar представляет собой арильную группу, и n представляет собой целое число от 1 до 13, или R3 и R4, или R4 и R5, или R5 и R7, или R3 и R7, или R9 и R10, или R8 и R9 вместе могут представлять собой -(CH2)x-, где x представляет собой целое число от 2 до 5, например -СН2-CH2- или -СН2-СН2-CH2-, и R2 выбран из группы, состоящей из гидроксила, низшего алкила и замещенного гидроксилом низшего алкила. Например, R1 может представлять собой -S(CH2)2N=C(NH2)2 и R2 может представлять собой -СН2СН(СН3)2, -СН2С(OH)(CH3)2, -CH(СН3)2 или -СН(CH3)СН2СН3.
Подробное описание изобретения
В настоящем изобретении предложен способ лечения увеита и факоанафилактического эндофтальмита у страдающего от них пациента, а также вододефицитного состояния сухого глаза путем местного нанесения на пораженный глаз производного циклоспорина, представленного нижеприведенной формулой
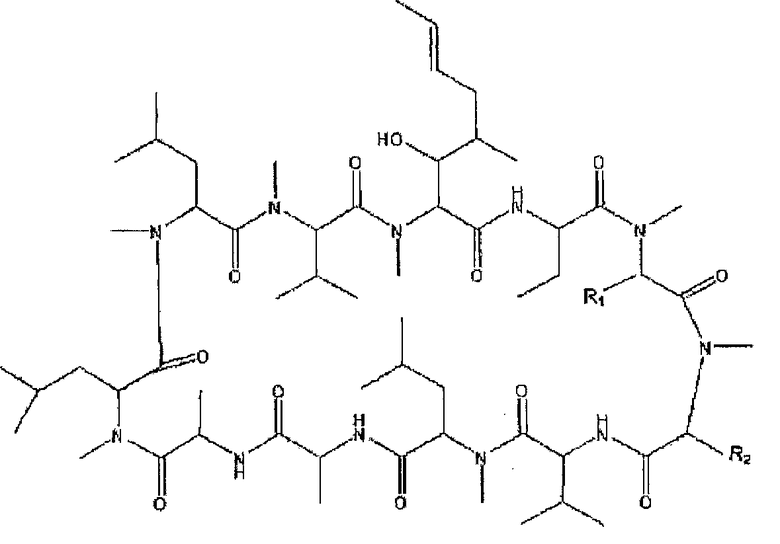
где R1 представляет собой S-Alk-R, где Alk представляет собой алкиленовую связь, предпочтительно метиленовую или полиметиленовую связь, например C2-C6 полиметиленовую связь или полиалкениленовую связь, например C3-C6 алкениленильную связь и R представляет собой -N=C(NR3R4)(NR5R6) или -NR7[(NR3R4)C=NR5], т.е. гуанидины или -N=C(R8)(NR9R10), т.е. амидины, где R3-R10 представляет собой H, Alk, Ar или (CH2)nAr, где Ar представляет собой арильную группу, и n представляет собой целое число от 1 до 13, или R3 и R4, или R4 и R5, или R5 и R7, или R3 и R7, или R9 и R10, вместе могут представлять собой -СН2-CH2- или -CH2-СН2-CH2- и R2 выбран из группы, состоящей из гидроксила, низшего алкила и замещенного гидроксилом низшего алкила. R представляет собой -N=C(NR3R4)(NR5R6) или -NR7C(NR3)(C=NR5), где R3-R7 представляет собой H, Alk, Ar или (СН2)nAr, где Ar представляет собой арильную группу, например, карбоциклический арил или гетероциклический арил, и n представляет собой целое число от 1 до 13, например целое число от 1 до 4, или R3 и R4, или R4 и R5, или R5 и R7(или R3 и R7, или R9 и R10, или R8 и R9 вместе, могут представлять собой -(CH2)x-, где x представляет собой целое число от 2 до 5, например -СН2-CH2- или -СН2-СН2-CH2-, и R2 выбран из группы, состоящей из гидрокси и низшего алкила.
Для целей описания и составления формулы настоящего изобретения следующие термины имеют следующие значения.
"Алкил" относится к прямоцепочечному, имеющему разветвленную цепь или циклическому насыщенному алифатическому углеводороду. Предпочтительно алкильная группа имеет от 1 до 12 атомов углерода. Более предпочтительно она представляет собой низший алкил, имеющий от 1 до 7 атомов углерода, наиболее предпочтительно от 1 до 4 атомов углерода. Типичные алкильные группы включают метил, этил, пропил, изопропил, бутил, изобутил, третичный бутил, пентил, гексил и т.п. Алкильная группа может необязательно быть замещена одним или более чем одним заместителем, выбранным из группы, состоящей из гидроксила, цианогруппы, алкокси, =O, =S, NO2, галогена, диметиламиногрупп и SH.
"Алкенил" относится к прямоцепочечной, имеющей разветвленную цепь или циклической ненасыщенной углеводородной группе, содержащей по меньшей мере одну углерод-углеродную двойную связь. Предпочтительно алкенильная группа имеет от 2 до 12 атомов углерода. Более предпочтительно она представляет собой низший алкенил, имеющий от 2 до 7 атомов углерода, наиболее предпочтительно от 2 до 4 атомов углерода. Алкенильная группа может необязательно быть замещена одним или более чем одним заместителем, выбранным из группы, состоящей из гидроксила, циано, алкокси, O, S, NO2, галогена, диметиламино и SH.
"Арил" относится к ароматической группе, которая имеет по меньшей мере одно кольцо, имеющее конъюгированную пи-электронную систему, и включает карбоциклические арильные, гетероциклические арильные и биарильные группы. Арильная группа может необязательно быть замещена одним или более чем одним заместителем, выбранным из группы, состоящей из галогена, тригалогенометила, гидроксила, SH, OH, NO2, амина, тиоэфира, цианогруппы, алкокси, алкила и аминогруппы.
"Алкарил" относится к алкилу, который ковалентно связан с арильной группой. Предпочтительно алкил представляет собой низший алкил.
"Алкокси" относится к "О-алкильной" группе.
"tBoc" относится к трет-бутилоксикарбонильной защитной группе.
"Карбоциклический арил" относится к арильной группе, где кольцевые атомы представляют собой углерод.
"Гетероциклический арил" относится к арильной группе, имеющей от 1 до 3 гетероатомов в виде кольцевых атомов, оставшиеся кольцевые атомы представляют собой атомы углерода. Гетероатомы включают кислород, серу и азот.
Производные циклоспорина A, используемые в способе по данному изобретению, получают следующим образом.
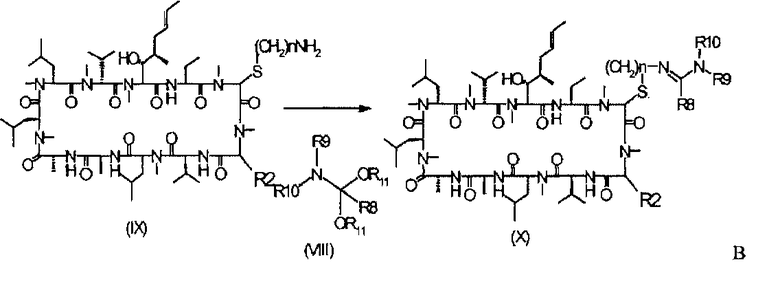
Соединения, где R4, R5 и R6 представляют собой водород и R7 представляют собой водород, алкил, замещенный алкил или арил, могут быть получены путем взаимодействия соединения формулы (I), где X представляет собой уходящую группу и Р представляет собой защитную группу, с соединением формулы (II) в подходящем растворителе, таком как метанол, с получением соединений формулы (III). Для соединений формулы I типичные примеры защитной группы представляют собой примеры, где X=хлор, MeS, MeSO2, 1-имидазолил и, в частности, 1-пиразолил. Защитные группы Р предпочтительно представляют собой третичные бутилоксикарбонильные группы (tBoc).
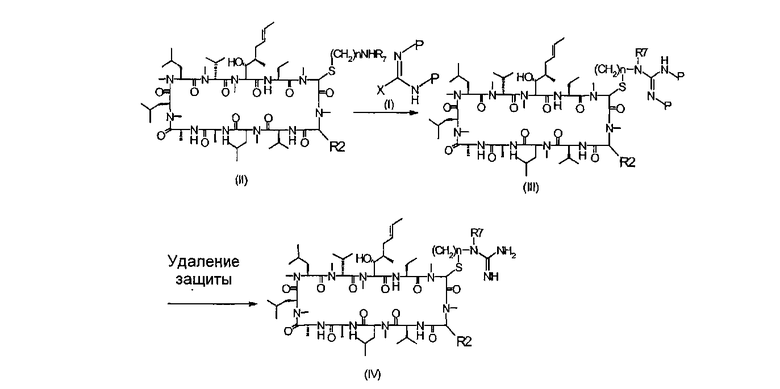
Защита с соединений формулы (III) может быть удалена путем применения различных условий с получением соединений формулы (IV). Например, когда P=третичные бутилоксикарбонильные группы (tBoc), они могут быть удалены в кислых условиях среды с использованием кислот, таких как метансульфоновая кислота.
Соединения формулы (V), где R7 представляет собой водород, алкил, замещенный алкил или арил; R3 представляет собой алкил, замещенный алкил или арил, могут быть получены путем взаимодействия соединения формулы (VI), где X представляет собой уходящую группу и Р представляет собой защитную группу, с соединением формулы (II) в подходящем растворителе, таком как метанол, с получением соединений формулы (VII).
Для соединений формулы (VI), типичные примеры защитной группы представляют собой примеры, где X=хлор, MeS, MeSO2, 1-имидазолил и, в частности, 1-пиразолил. Защитные группы Р предпочтительно представляют собой третичные бутилоксикарбоксильные группы (tBoc).
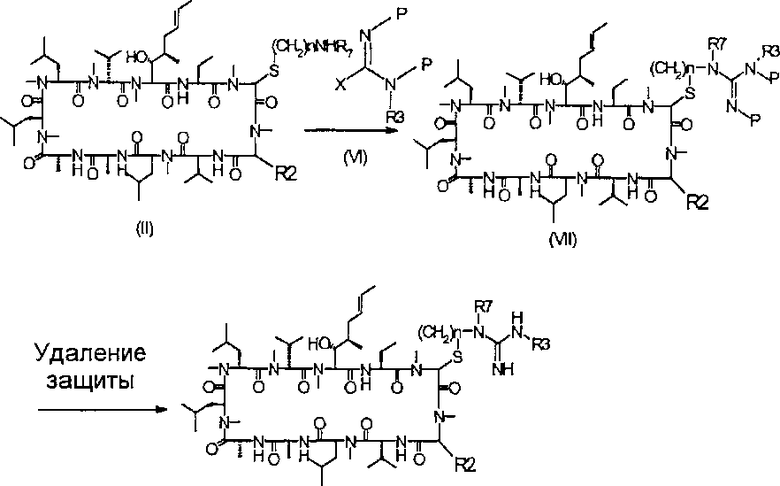
Например, в WO/2003/051797 N'/N'-ди-tBoc-N-метил-1H-пиразол-1-карбоксамид использовали для получения N-метилгуанина в неродственном химическом семействе.
Другие соединения по изобретению могут быть получены по аналогии с использованием родственных синтетических способов, если приемлемо, то с подходящими защитными группами, совместимыми с методикой синтеза.
Соединения формулы (X), где R представляет собой -N=C(R9)-NR9R10 (амидины), где R8 представляет собой водород, алкил, замещенный алкил или арил, и R9 и R10 могут представлять собой алкил, замещенный алкил или арил, или R9 и R10 могут образовывать кольцо, могут быть получены путем взаимодействия соединения формулы (VIII) с соединением формулы (IX) с получением соединений формулы (X). R11 предпочтительно представляет собой низший алкил и типичные примеры соединения (VIII) представляют собой диметилформамид диметилацеталь (ДМФ ДМА) и диметилацетамид диметилацеталь (ДМА ДМА).
Ниже приведены конкретные примеры получения некоторых соединений по изобретению при помощи вышеприведенных общих способов.
Гуанидиновые и амидиновые аналоги 3-[(2-аминоэтилтио]-циклоспорина A
Пример 1.
3-[(2-Гуанидил)-этилтио]-циклоспорин A (III)
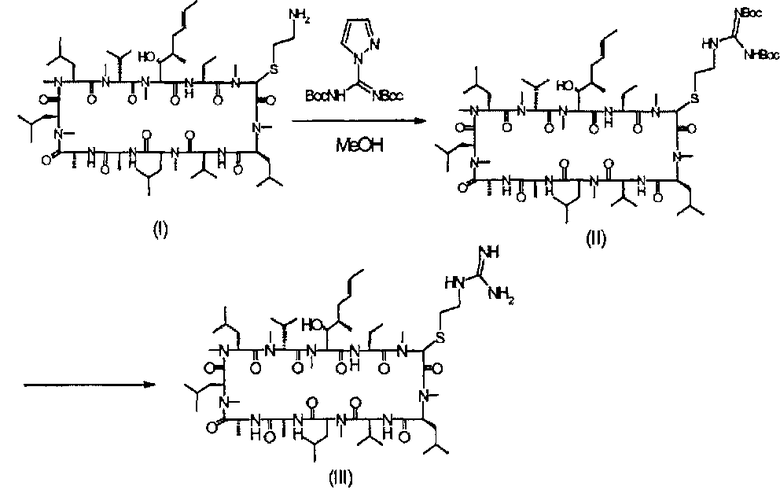
К раствору 3-[(2-аминоэтилтио]-циклоспорина A*-(I)) (200 мг, 0,16 ммоль) в метаноле (20 мл) добавляли ди-tBoc-пиразол карбоксамидин (250 мг, 0,8 ммоль) и реагенты перемешивали вместе в течение 18 ч. После этого добавляли еще одну порцию ди-Tt-пиразол карбоксамидина (100 мг, 0,32 ммоль) и реакционную смесь перемешивали в течение еще 3 ч. Реакционную смесь затем упаривали в вакууме, перерастворяли в дихлорметане, промывали 0,5М лимонной кислотой и органический слой сушили над MgSO4 и упаривали в вакууме. Продукт затем очищали при помощи хроматографической колонки на картридже 10 г SPE (для твердофазной экстракции) с элюцией диэтиловым эфиром для выделения 90 мг (40%) желемого продукта (II).
В качестве первого члена синтезированных гуанидиновых и амидиновых примеров и ввиду сложностей, с которыми сталкиваются при описании конечного продукта (III), решили полностью и широко охарактеризовать ди-tBoc защищенный гуанидин (II) на этой стадии и затем превратить это вещество в свободный гуанидин (III) путем кислотного гидролиза. Последующие аналоги в этом гуанидиновом и амидиновом подклассе, полученные из 3-[(2-аминоэтилтио]-циклоспорина A, затем охарактеризовывали в основном путем MS (масс-спектрометрии).
Соединение (II) анализировали при помощи 1Н, 13С, ЯМР метода неискаженного усиления поляризационным переносом (DEPT - Distortionless Enhancement by Polarization Transfer, ЯМР ядерный магнитный резонанс) и затем при помощи серий 2-D NMR экспериментов, HMQC (гетероядерная многоквантовая корреляция), НМВС (гетероядерная многополосная корреляция) и DEPT-HMQC.
Присутствие 3-[(2-гуанидил)-этилтиоловой] боковой цепи подтверждалось при помощи ID & 2D NMR. Анализ осуществляли в растворе CDCl3 при 300 K на спектрометре Bruker DRX500.
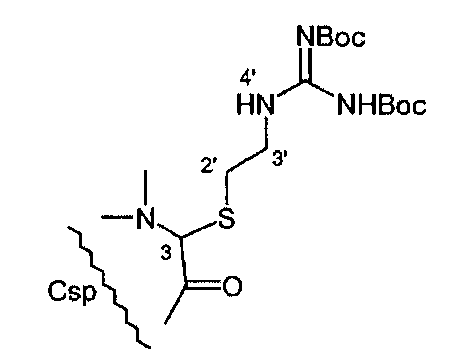
1H NMR ключевые резонансы:
δ=1.50, 1.51 млн-1 (2 синглета, 2 xBoc, 18H, 6xCH3)
δ=5.89 млн-1, (синглет, саркозин, 1H)
2D Спектры
С использованием экспериментов 1H детектируемой гетероядерной многоквантовой корреляции (HMQC), гетероядерной многополосной корреляции (НМВС) и скорректированной гетероядерной одноквантовой корреляции (DEPT-HSQC) могут быть оценены наличие связей и интерпретация, подтверждающие присутствие 3-[(2-гуанидил)-этилтио] боковой цепи.
H(3)-2' (мультиплет, 1H 2,84 млн-1, 2H).
2'-3' (мультиплет, 1H 3,67 млн-1, 2H).
3'-NH4' (триплет JHH 5,8 Гц, 1Н 8,67 млн-1, 1H).
К раствору di-tBoc защищенного 3-[(2-гуанидил)-этилтио]-циклоспорина A (II) (21 мг, 0,0138 ммоль) в дихлорметане (0,3 мл) добавляли трифторуксусную кислоту (0,3 мл) и раствор перемешивали при комнатной температуре в течение 1 часа. Раствор концентрировали с получением продукта (III) в виде белого твердого вещества (20 мг; 100%).
Анализ при помощи MS (E+) продемонстрировал массу 1320,2 (M+H), согласуемую с предлагаемой структурой
Пример 2
3-[(2-М, г>1-диметилформамидинил)-1-тиоэтил]-циклоспорин A (III)
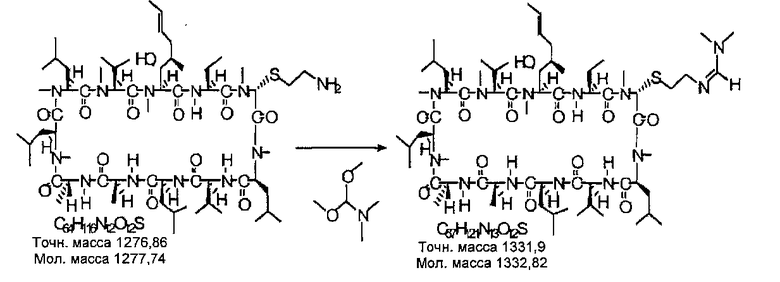
Смешанный раствор 3-(1-тиоэтиламин)циклоспорина A (0,64 г, 0,5 ммоль) и N,N-диметилформамид диметилацеталя в 20 мл ТГФ кипятили с обратным холодильником в течение двух часов. После удаления растворителя в вакууме остаток подвергали хроматографии на колонке силикагеля с использованием метилена/метанола (10:1) в качестве элюентов, получали 300 мг чистого продукта (выход: 45,0%).
MS (Е+) продемонстрировала массу 1332,82 (М+H+), согласующуюся с предлагаемой структурой.
Другие способы понятны специалистам-химикам, также как и способы получения исходных веществ и промежуточных соединений и т.д.
В соответствии с настоящим изобретением производные циклоспорина A могут быть нанесены на пораженный глаз в любой эффективной концентрации, например от 0,01 до насыщения (например, больше, чем 20 масс.%) в фармацевтически приемлемом эксципиенте. Может быть использовано от 0,01 до 50 масс.%, предпочтительно от 0,1 до 20 масс.% производных циклоспорина A в фармацевтически приемлемом эксципиенте. Такие фармацевтически приемлемые эксципиенты представляют собой, например, животное масло, растительное масло, подходящий органический или водный растворитель, искусственный раствор слезы, природный или синтетический полимер подходящую мембрану для инкапсуляции производного цикоспорина А.
Специфические примеры этих фармацевтически приемлемых эксципиентов представляют собой оливковое масло, арахисовое масло, касторовое масло, минеральное масло, вазелиновое масло, диметилсульфоксид, хремофор, Miglyol 182 (имеющийся в продаже от Dynamit Nobel Kay-Fries Chemical Company, Mont Vale, N.J.), спирт (например, этанол, н-пропиловый спирт или изопропиловый спирт), липосомы или липосомоподобные продукты или силиконовое масло. Предпочтительные эксципиенты представляют собой диметилсульфоксид и оливковое масло. Могут быть использованы смеси по меньшей мере двух любых подходящих эксципиентов.
Примеры искусственных эксципиентов слез, которые могут быть преимущественно использованы при практическом применении данного изобретения, представляют собой изотонический хлорид натрия, эфиры целлюлозы, такие как гидроксипропилметилцеллюлоза и гидроксиэтилцеллюлоза, поливиниловый спирт и доступные искусственные растворы чая.
Пример полезного полимерного эксципиента представляет собой полиоксиэтилированное касторовое масло.
Примеры фармацевтически приемлемых мембран, которые преимущественно могут быть использованы при практической реализации данного изобретения, представляют собой микродон, представляющий собой искусственную липидную мембрану, поливиниловый спирт или метилцеллюлозу.
Производные циклоспорина А преимущественно вводят местно в виде офтальмологических капель (раствор или суспензия) или офтальмологической мази, содержащей эффективное количество производного. Концентрации от 0,01 до 50 масс.%, предпочтительно от 0,1 до 20 масс.% производных циклоспорина A используются при практической реализации данного изобретения.
В соответствии со способом по настоящему изобретению по меньшей мере одно из производных циклоспорина А вводят местно в любом количестве, требующемся для обеспечения необходимой степени лечения. Например, благоприятно используют от 5 микролитров до 1 миллилитра раствора, суспензии или мази, содержащей эффективное количество производного циклоспорина A, такое как от 0,01 до 50 масс.%, предпочтительно от 0,1 до 20 масс.% производного циклоспорина А.
Многочисленные преимущества добавляются при практической реализации настоящего изобретения. Способ по настоящему изобретению полезен тем, что он может локально предотвратить активацию досистемного ответа. Местное введение производных циклоспорина A в глаза пациента, страдающие от дефицита слез, увеличивает продукцию слез в глазу. Таким образом, такое лечение дополнительно служит для коррекции расстройств роговицы и конъюнктивы, обостренных дефицитом слез и СКК, таких как рубцевание роговицы, изъязвление роговицы, воспаление роговицы или конъюнктивы, филаментозный кератит, слизисто-гнойный секрет и васкуляризация роговицы. Кроме того, производные циклоспорина A непосредственно ослабляют иммунный ответ и грануляцию и неоваскуляризацию.
Дополнительные задачи данного изобретения вместе с дополнительными особенностями, вносящими вклад в изобретение, и преимуществами, возникающими из него, понятны из следующих примеров изобретения.
Предшествующее описание приводит подробную информацию о специфических способах и композициях, которые могут быть использованы для практической реализации настоящего изобретения, и представляет наилучший предлагаемый способ. Таким образом, хотя в вышеприведенном тексте может появиться подробное описание, его не следует рассматривать как ограничивающее общий объем изобретения; скорее, объем настоящего изобретения должен определяться только правомерной конструкцией формулы изобретения. В частности, хотя способ по настоящему изобретению описан с применением конкретных производных циклоспорина A вышеприведенной формулы, новые циклоспориновые производные, которые могут быть использованы в способе по настоящему изобретению, дополнительно включают 3-замещенные иминоалкилтиопроизводные циклоспорина A, предпочтительно 3-замещенные диаминоиминоалкилтиопроизводные циклоспорина A, например, производные ((R)-(диамино)иминоалкилтио-Sar)3-(4'-гидрокси-MeLeu)4 циклоспорин A, ((R)-(алкил)(диалкиламино)иминоалкилтио-Sar)3--(4'-гидрокси-MeLeu)4-циклоспорин A, ((R)-(алкил)(диалкиламино)иминоалкилтио-Sar)3-циклоспорин A и производные ((R)-(диамино)иминоалкилтио-Sar)3-циклоспорина A.
Изобретение относится к соединению, выбранному из группы, состоящей из соединений, представленных формулой
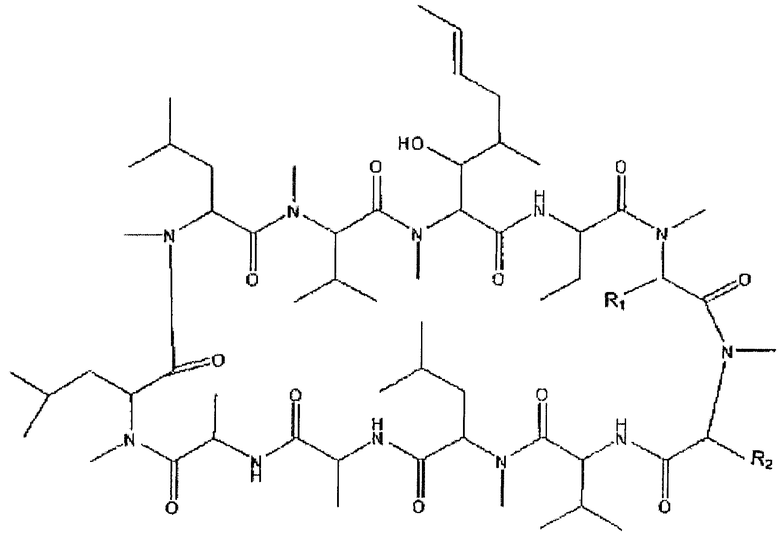
В указанной формуле R1 представляет собой S-Alk-R, где Alk представляет собой метилен, C2-C6 полиметиленовую связь или C3-C6 алкениленильную связь, R представляет собой -N=C(NR3R4)(NR5R6) или -NR7[(NR3R4)C=NR5], или -N=C(R8)(NR9R10), где R3-R10 представляет собой H, Alk, Ar или (CH2)nAr, где Ar представляет собой арильную группу, и n представляет собой целое число от 1 до 13, или R3 и R4, или R4 и R5, или R5 и R7, или R3 и R7, или R9 и R10, или R8 и R9 вместе могут представлять собой -(CH2)x-, где x представляет собой целое число от 2 до 5, и R2 выбран из группы, состоящей из гидроксила, алкила, имеющего от 1 до 7 атомов углерода, и замещенного гидроксилом алкила, имеющего от 1 до 7 атомов углерода. 4 з.п. ф-лы, 2 пр.
1. Соединение, выбранное из группы, состоящей из соединений, представленных формулой

где R1 представляет собой S-Alk-R, где Alk представляет собой метилен, C2-C6 полиметиленовую связь или C3-C6 алкениленильную связь, R представляет собой -N=C(NR3R4)(NR5R6) или -NR7[(NR3R4)C=NR5], или -N=C(R8)(NR9R10), где R3-R10 представляет собой H, Alk, Ar или (CH2)nAr, где Ar представляет собой арильную группу, и n представляет собой целое число от 1 до 13, или R3 и R4, или R4 и R5, или R5 и R7, или R3 и R7, или R9 и R10, или R8 и R9 вместе могут представлять собой -(CH2)x-, где x представляет собой целое число от 2 до 5, и R2 выбран из группы, состоящей из гидроксила, алкила, имеющего от 1 до 7 атомов углерода, и замещенного гидроксилом алкила, имеющего от 1 до 7 атомов углерода.
2. Соединение по п.1, где R представляет собой -N=C(NR3R4)(NR5R6) или -NR7C(NR3)(C=NR5), где R3-R7 представляет собой H, Alk, Ar или (CH2)nAr, где Ar представляет собой арильную группу и n представляет собой целое число от 1 до 13 или R3 и R4 или R4 и R5, или R5 и R7, или R3 и R7 вместе могут представлять собой -CH2-CH2- или -CH2-CH2-CH2-.
3. Соединение по п.1, представляющее собой 3-замещенное производное диаминоиминоалкилтиоциклоспорина A.
4. Соединение по п.1, выбранное из группы, состоящей из производных ((R)-(диамино)иминоалкилтио-Sar)3-(4′-гидрокси-MeLeu)4циклоспорина A, ((R)-(алкил)(диалкиламино)миноалкилтио-Sar)3(4′-гидрокси-MeLeu)4-циклоспорина A, производных ((R)-алкил)(диалкиламино)иминоалкилтио-Sar)3-циклоспорина А и производных ((R)-диамино)иминоалкилтио-Sar)3-циклоспорина A.
5. Соединение по п.1, где R1 представляет собой -S(CH2)2N=C(NH2)2 и R2 представляет собой -CH2CH(CH3)2, -CH2C(OH)(CH3)2, -CH(СН3)2 или -СН(CH3)СН2СН3.
| WO 00/61168 A1 19.10.00ДАЙСОН Г., МЕЙ П | |||
| «Химия синтетических лекарственных веществ», пер | |||
| с англ | |||
| М.:–«Мир», 1964 |
Авторы
Даты
2014-06-27—Публикация
2009-07-09—Подача