Изобретение относится к области медицины, в частности к неврологии, и может быть использовано для восстановления двигательных функций у больных, перенесших ишемический инсульт и имеющих грубые двигательные нарушения.
Известно, что повторяющиеся активные целенаправленные движения значительно способствуют восстановлению двигательных функций. У больных, перенесших инсульт, помимо лечебной физкультуры этот подход в течение последних 10 лет реализован в таких методах, как тренировка в условиях виртуальной реальности, когда пациенты обучаются движениям по обратной связи, и тренировка в условиях, когда движения облегчаются роботом (Черникова Л.А. Пластичность мозга и современные реабилитационные технологии. Анналы клинической и экспериментальной неврологии, 2007, 1(2):40-47).
Эти методы требуют сохранения возможности совершать активные движения парализованной конечностью и, следовательно, требуют частичного сохранения двигательных функций. В случае грубого пареза или плегии перспективным методом стимулирования пластичности мозга является воображение движений. Физиологические механизмы, лежащие в основе процесса воображения движения, во многом сходны с механизмами двигательного контроля и поэтому могут стимулировать те же пластические механизмы мозга, что и реальное исполнение движения (Neuper С, Scherer R., Reiner М., Pfurtscheller G. Imagery of motor actions: differential effects of kinesthetic and visual-motor mode of imagery in single-trial EEG. Cogn. Brain Res. 2005. 25(3): 668-677).
На сегодняшний день известен способ реабилитации больных, перенесших инсульт, путем обучения пациента «точностному схвату» с помощью биоуправления с обратной связью по электромиограмме (ЭМГ). Для тренировки точностного схвата используют аппаратно-программный комплекс «Бослаб» (г. Новосибирск). Электромиографические электроды накладывают на мышцы возвышения большого пальца. Пациент сжимает большим и указательным пальцами небольшой предмет и обучается поддерживать заданный уровень активности мышц в 20, 40 или 60% от уровня максимального сокращения. На экране монитора пациент видит заданный уровень ЭМГ в виде коридора, а также изменения своей интегрированной ЭМГ. Задача состоит в совмещении уровня ЭМГ с заданным коридором и удержании уровня мышечного напряжения в течение 30 с. После каждой пробы пациент максимально расслабляет мышцы под зрительным контролем (тренировка преодоления спастичности), а затем пытается воспроизвести необходимый уровень ЭМГ по памяти, не видя ЭМГ на экране, т.е. без зрительного контроля. Продолжительность сеанса составляет 20-25 мин. Курс обучения состоит из 10 ежедневных сеансов. (Черникова Л.А., Иоффе М.Е., Бушенева С.Н., Шестакова М.В., Билименко А.Е. Электромиографическое биоуправление и функциональная магнитно-резонансная томография в постинсультной реабилитации (на примере обучения точностному схвату). Бюллетень сибирской медицины, 2010, №2, с.12-16).
Это позволяет активно включать в программы двигательной реабилитации биоуправление, организованное по электромиограмме и направленное на выработку точностных движений пальцев кисти у больных с легкими и умеренными парезами и нарушением мелкой моторики руки, однако не обеспечивает полноценную реабилитацию у пациентов, имеющих грубые двигательные нарушения.
Технический результат заключается в повышении эффективности реабилитации у пациентов, перенесших инсульт и имеющих грубые двигательные нарушения, за счет влияния тренировки воображения движения на нейрофизиологию корковых моторных представительств, что обеспечивает увеличение возбудимости двигательной коры.
Технический результат достигается тем, что реабилитацию больных, перенесших инсульт, осуществляют путем проведения тренировок паретичной конечности, при этом тренировку проводят, предъявляя больному задание по воображению движения паретичной конечностью с последующим контролем воображения движения больным, основанным на анализе паттернов электроэнцефалограммы (ЭЭГ), возникающих при воображении движения паретичной конечностью, причем регистрацию ЭЭГ сигналов мозга осуществляют с системы активных электродов энцефалографа, размешенных на поверхности головы, и передачу этих данных в компьютер для их синхронной обработки и выделения сигналов, ответственных за воображение движения с помощью классификатора паттернов ЭЭГ по методу Байеса, результаты распознавания выполняемого ментального задания предъявляют больному по зрительной обратной связи с подтверждением правильности выполнения задания на экране монитора, причем задание по воображению движения предъявляют в течение 10 секунд, курс тренировки паретичной конечности составляет 6-12 дней, по одной тренировки в день, длительностью 20-30 минут с интервалами между тренировками от 1 до 4 дней.
Способ осуществляется следующим образом.
Для реабилитации больного, перенесшего инсульт, используют технологию с обратной связью - интерфейс мозг - компьютер (ИМК). Пациент в режиме реального времени получает визуальную информацию об активности своего головного мозга.
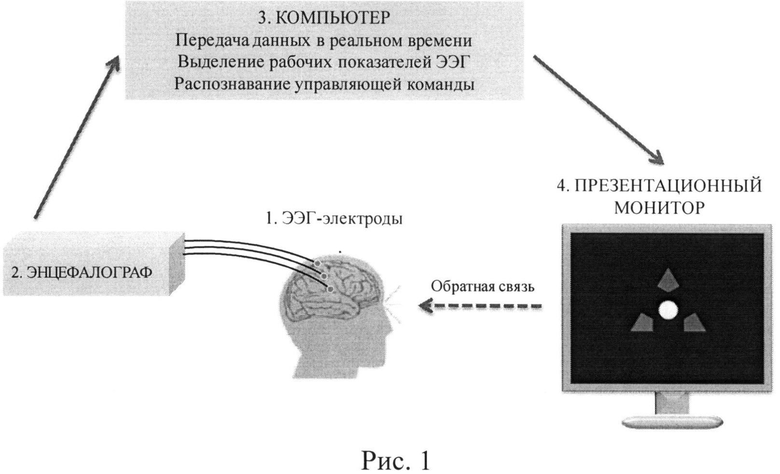
ИМК состоит из следующих элементов (рис.1): системы активных электродов ActiCap фирмы Brain Products (Германия) для регистрации электроэнцефалограммы (ЭЭГ) (1), энцефалографического аналого-цифрового преобразователя (АЦП) NBL640 производства ООО «НейроБиоЛаб» (2), персонального компьютера (операционная система Windows 7) для синхронной передачи данных, выделения рабочих показателей ЭЭГ и классификации сигналов для распознавания управляющей команды в реальном времени (3) (Бобров П.Д., Коршаков А.В., и др. Байесовский подход к реализации интерфейса мозг -компьютер, основанного на представлении движений. Журнал Высшей Нервной Деятельности и Нейрофизиологии, 2012, 62(1):89-100).
Во время сеанса тренинга пациент сидит в удобном кресле так, что голова находится на расстоянии 1 метра от компьютерного монитора, на котором ему предъявляют визуальные задания и обратную связь (информацию о правильности выполнения задания). В центре экрана монитора имеется кружок, служащий для фиксации взгляда, и расположенные вокруг него 3 ромбовидные стрелки, которые указаны на блок-схеме макета ИМК, применяемого в данном процессе реабилитации (рис.1). Пациент во время тренинга выполняет одно из трех заданий: расслабиться (когда загорается верхняя стрелка), представить движение левой или правой руки (когда загорается соответствующая левая или правая стрелка). В качестве представления движения руки предлагают воображать медленное сжатие кисти в кулак. По заданию расслабиться (покой) пациент должен спокойно сидеть и смотреть в центр экрана. Задания предъявляют в случайном порядке, каждое в течение 10 секунд. Результаты распознавания выполняемой ментальной задачи предъявляют пациенту по зрительной обратной связи: метка в середине экрана, фиксирующая взор, принимает зеленый цвет, если классификатор распознает задачу, соответствующую предъявляемому заданию движения, и остается белой, если задача не была распознана.
Регистрацию ЭЭГ проводят с помощью 30 электродов, расположенных на поверхности головы пациента, по схеме 10-20 (Зенков Л.Р. Клиническая электроэнцефалография (с элементами эпилептологии). Руководство для врачей. 3-е изд., М: МЕДпрессинформ, 2004, 368 с.). Под каждый электрод наносят специальный гель для улучшения контакта с поверхностью головы пациента. Сигналы ЭЭГ фильтруют в полосе частот от 5 до 30 Гц. В данной методике применялся классификатор паттернов ЭЭГ, основанный на методе Байеса (Бобров П.Д., Коршаков А.В. и др. Байесовский подход к реализации интерфейса мозг - компьютер, основанного на представлении движений. Журнал Высшей Нервной Деятельности и Нейрофизиологии, 2012, 62(1): 89-100). В качестве показателя точности классификации используют индекс «каппа Коэна» (при идеальном распознавании к=1, при случайном распознавании к=0) (Kohavi, R., Provost F. Glossary of terms. Machine Learning - Special Issue of Applications of Machine Learning and the Knowledge Discovery Process, 1998, 30: 271-274) и процент правильных ответов классификатора (распознавание выше случайного при > 35%). Определение источников активности, наиболее значимых для функционирования ИМК, проводилось с помощью метода независимых компонент (ICA, Independent Component Analysis) (Frolov A., Husek D. et al. Comparison of four classification methods for brain computer interface, Neural Network World, 2011, 21(2): 101-111).
С каждым пациентом реабилитацию проводят в течение 6-12 дней по одному тренингу в день, длительностью 20-30 минут. Интервалы между тренингами составляют от 1 до 4 дней.
Проведено исследование с целью сравнить качество управления ИМК у пациентов с очаговым повреждением головного мозга и у здоровых людей, а также с целью оценки эффективности данной методики для реабилитации пациентов, перенесших инсульт .В исследовании участвовало 36 пациентов с гемипарезами центрального генеза, из них 26 мужчин и 10 женщин, в возрасте от 34 до 70 лет, с давностью заболевания (инсульта или травмы головного мозга) от 1 месяца до 8 лет (медиана давности заболевания составила 11,5 [3; 21,5] месяцев). В раннем восстановительном периоде находились 14 пациентов, в позднем и резидуальном - 22 пациента. У всех пациентов в клинической картине наблюдался очень грубый парез или плегия в руке, медиана по шкале ARAT=0 [0; 4]. 16 пациентов составили основную группу, в комплексное лечение которых были включены тренировки ИМК, и группу сравнения, состоящую из 20 пациентов, которые получали только традиционную комплексную терапию. Основная группа и группа сравнения были сопоставимы по возрасту, давности инсульта и степени неврологического дефицита. Кроме того, в исследовании участвовали 7 здоровых добровольцев в возрасте от 24 до 68 лет, 6 мужчин и 1 женщина. Все испытуемые - правши (согласно Эдинбургскому опроснику мануальной асимметрии: R > 40%).
Тринадцать пациентов основной группы (3 пациента выбыло после первого сеанса по собственному желанию) и все здоровые испытуемые прошли курс ИМК-тренинга, в котором задание по воображению движения предъявляли в течение 10 секунд и проводили по одной тренировки в день, длительностью 20-30 минут с интервалами между тренировками от 1 до 4 дней. Достигнутые результаты управления ИМК для обученных пациентов обеих групп представлены в таблице 1 (данные представлены в виде медианы и 25%, 75% процентилей).
По показателям качества управления интерфейсом (каппа Коэна и процент распознавания) отличия между группами не выявлено (Р>0,05). Это позволяет сделать вывод о том, что пациенты с очаговым повреждением головного мозга в состоянии овладеть управлением ИМК с тем же качеством, что и люди без неврологических нарушений.
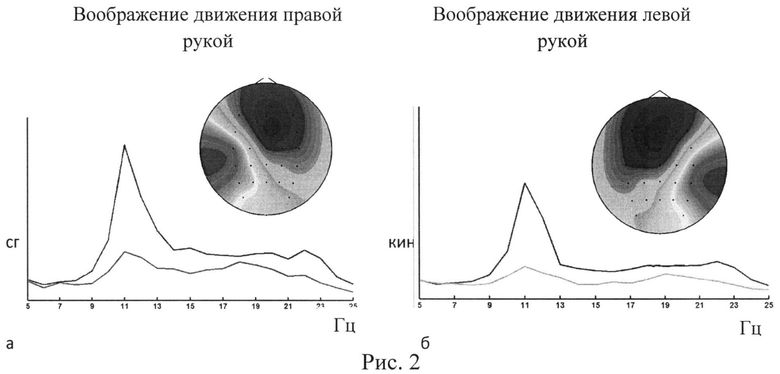
На рис. 2 представлены распределение вклада компонент в потенциалы, регистрируемые на поверхности головы (топографическое распределение), и спектральные плотности активности для этих компонент (для одного из здоровых испытуемых). Топографические распределения значимых для управления ИМК компонент и их спектральные плотности при трех ментальных состояниях - «норма». По оси абсцисс - частота в герцах, по оси ординат - спектральная плотность, нормированная на максимальное значение. Пик спектральной плотности для этих компонент соответствует диапазону сенсомоторного ритма (мю-ритма). Во время воображения движения происходит реакция десинхронизации сенсомоторного ритма в соответствующем полушарии (нижняя кривая на графике спектральной плотности).
Такое распределение потенциалов и изменение мю-ритма во время воображения движения наблюдалось у здоровых испытуемых и было принято за «норму».
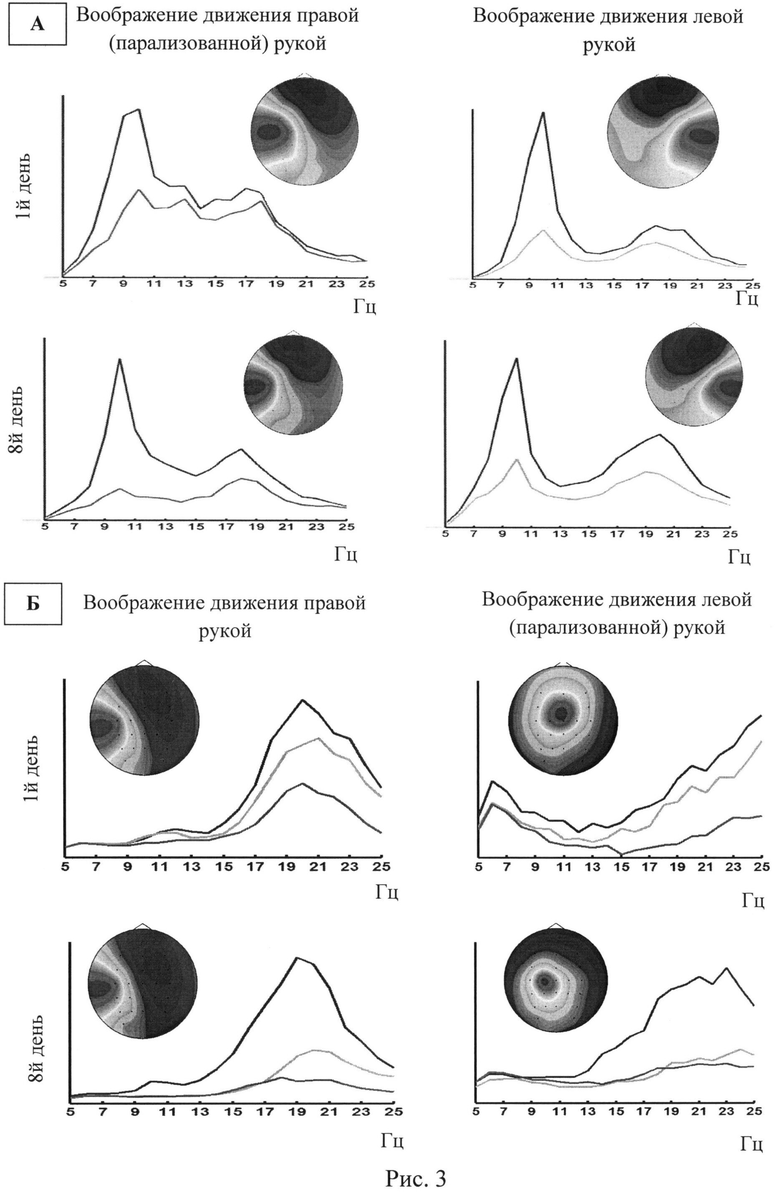
На рис. 3 представлены топографические распределения значимых компонент и спектральные плотности их интенсивности при трех ментальных состояниях (покой, воображение движения левой рукой и воображение правой рукой): А) у пациента с подкорковым повреждением головного мозга; Б) у пациента с повреждением двигательной коры. Среди пациентов встречались следующие варианты распределения вклада компонент в потенциалы в зависимости от локализации инсульта: при подкорковой локализации очага поражения наблюдалась картина, аналогичная «норме» (рис.3А), а при повреждении двигательной коры наблюдалось нетипичное распределение вклада компонент в поврежденном полушарии: в обоих случаях источник сигнала локализовался ближе к зоне проекции CZ при стандартном расположении ЭЭГ-электродов по системе 10-20 (рис.3Б). Значимые для управления ИМК компоненты, так же как и у здоровых испытуемых, были связаны с реакцией десинхронизации в диапазоне мю-ритма (10 пациентов), и бета-ритма (1 пациент, рис.3Б), или мю- и частично бета-ритма (1 пациент, рис.3А) во время воображения движения.
Среди испытуемых обеих групп встречались следующие варианты изменения активности мозга, с которыми было связано улучшение качества управления ИМК (овладение навыком управления ИМК): а) выделение значимых компонент с первых дней и усиление реакции десинхронизации в процессе тренировки; б) отсутствие значимых компонент в первые дни и появление их в процессе тренировки с последующим усилением реакции десинхронизации. Топографическое распределение не менялось для каждой из двух компонент в результате тренировки.
Для оценки клинической эффективности восстановительной реабилитации у больных с центральным парезом руки был проведен сравнительный анализ восстановления двигательной функции в основной группе (13 пациентов) и группе сравнения (20 пациентов). Следует отметить, что в данное исследование, как в основную группу, так и в группу сравнения были включены больные только с плегией или очень грубым парезом кисти с плохим прогнозом на восстановление движений.
У пациентов основной группы после проведенных реабилитационных мероприятий выявлено статистически значимое улучшение двигательной функции руки (по шкале ARAT). В группе сравнения значимого улучшения нарушенных двигательных функций не наблюдалось. Различие в улучшении функции руки между группами статистически значимо (р=0,02). Результаты оценки двигательной функции руки в динамике у пациентов основной группы и группы сравнения представлены в таблице 2.
Таким образом, полученные данные позволяют сделать вывод, что не только у здоровых, но и у пациентов с повреждением головного мозга при воображении движения как здоровой, так и паретичной руки выявляется реакция десинхронизации в соответствующем полушарии головного мозга. При этом впервые в проведенном исследовании было показано, что топографическое распределение компонент у тренированных здоровых испытуемых и пациентов с подкорковым инсультом соответствовало расположению представительства руки в первичных сенсомоторных областях центральной борозды, в то же время у больных с обширным повреждением коры при воображении движения паретичной руки наблюдалось смещение локализации источника активности в область расположения Cz электрода.
В результате была выявлена закономерность, свидетельствующую о том, что пациенты с очаговым повреждением головного мозга в состоянии овладеть управлением ИМК с тем же качеством, что и испытуемые без неврологических нарушений. При этом не было обнаружено зависимости качества управления ИМК от степени, локализации или давности поражения мозга.
Кроме того, у 42% больных с плегией и грубым парезом кисти после курса обучения наблюдался положительный эффект при использовании ИМК-тренинга, выражающийся в достоверном улучшении функции паретичной кисти. Следовательно, данный метод реабилитации позволит ускорить темп и сделать более полным восстановление нарушенных функций, предотвратить развитие вторичных осложнений (тромбофлебитов, контрактур, пролежней, застойной пневмонии и т.д.) у больных с разной тяжестью поражения головного мозга.
Примеры осуществления способа
Пример 1
Пациентка А., 70 лет, ишемический инсульт, давность заболевания 1,5 месяца, очаг инсульта по МРТ: в левом полушарии головного мозга в заднелатеральном отделе лентикулярного ядра с переходом на лучистый венец и заднее бедро внутренней капсулы. Грубый парез руки (7 баллов по шкале ARAT).
Проведен курс тренингов из 8 сеансов по 20 минут с интервалами между тренировками 1 день. Задание по воображению движения предъявляли в течение 10 секунд. Достигнутые показатели качества управления ИМК к 8 дню тренировки: каппа Коэна=0,42; процент распознавания=70%. Управление ИМК осуществлялось за счет реакции десинхронизации сенсомоторного ритма в области центральной борозды транслатерального полушария при воображении движения. После проведенной реабилитации наблюдалось клинически значимое улучшение функции кисти (на 11 баллов по шкале ARAT, таблица 4). Пациентка самостоятельно берет предметы со стола, открывает дверную ручку.
Пример 2
Пациентка В., 40 лет, ишемический инсульт, давность заболевания 21 месяц, очаг инсульта по МРТ: в левом полушарии головного мозга в лентикулярном ядре с распространением на заднее бедро внутренней капсулы, верхние отделы гиппокампальной извилины. Грубый парез руки (4 балла по ARAT).
Проведен курс тренингов из 12 сеансов, по одной тренировки в день, длительностью 30 минут с интервалами между тренировками 4 дня. Задание по воображению движения предъявляли в течение 10 секунд. Достигнутые показатели качества управления ИМК к 12 дню тренировки: каппа Коэна=0,30; процент распознавания=50%. Управление ИМК осуществлялось за счет реакции десинхронизации сенсомоторного ритма в области центральной борозды транслатерального полушария при воображении движения. После проведенной реабилитации наблюдалось улучшение функции руки, в том числе кисти (на 13 баллов по шкале ARAT, таблица 5). Пациентка может брать некоторые предметы со стола.
Таким образом, предложенный способ реабилитации пациентов, перенесших инсульт, обеспечивает повышение ее эффективности за счет влияния тренировки воображения движения на нейрофизиологию корковых моторных представительств. Это увеличивает возбудимость двигательной коры. Разработанный нами курс ИМК- тренинга улучшает точность произвольной активности мышц конечностей у больных с грубыми двигательными нарушениями после обучения с помощью зрительной обратной связи. Это позволяет активно включать в программы двигательной реабилитации курс ИМК-тренинга, организованный по электроэнцефалограмме и направленный на выработку восстановления двигательной функции, особенно у больных, перенесших ишемический инсульт и имеющих грубые двигательные нарушения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ ПОСЛЕ ИНСУЛЬТА ИЛИ ТРАВМЫ С ИСПОЛЬЗОВАНИЕМ РОБОТИЗИРОВАННОГО КОМПЛЕКСА, ВКЛЮЧАЮЩЕГО ЭКЗОСКЕЛЕТ КОНЕЧНОСТИ ЧЕЛОВЕКА, УПРАВЛЯЕМЫЙ ЧЕРЕЗ ИНТЕРФЕЙС МОЗГ-КОМПЬЮТЕР ПОСРЕДСТВОМ ВООБРАЖЕНИЯ ДВИЖЕНИЙ | 2015 |
|
RU2622206C2 |
| Способ стимуляции головного мозга | 2023 |
|
RU2822811C1 |
| Способ мультимодальной коррекции двигательных и когнитивных нарушений у пациентов, перенесших ишемический инсульт | 2023 |
|
RU2813807C1 |
| Способ реабилитации больных, перенесших инсульт | 2020 |
|
RU2742071C1 |
| Способ проведения тренировки с использованием виртуальной реальности в рамках реабилитации пациентов с заболеваниями, сопровождающимися парезом конечностей | 2021 |
|
RU2786990C1 |
| Способ реабилитации пациентов с нарушением двигательной активности с использованием персонифицированного контента клипов виртуальной реальности | 2024 |
|
RU2830938C1 |
| СПОСОБ КОМПЛЕКСНОЙ РЕАБИЛИТАЦИИ ДВИГАТЕЛЬНОЙ ФУНКЦИИ ВЕРХНЕЙ КОНЕЧНОСТИ У БОЛЬНЫХ ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ | 2020 |
|
RU2741221C1 |
| СПОСОБ КОМПЛЕКСНОЙ РЕАБИЛИТАЦИИ ДВИГАТЕЛЬНОЙ ФУНКЦИИ ВЕРХНЕЙ КОНЕЧНОСТИ У БОЛЬНЫХ ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ | 2023 |
|
RU2810440C1 |
| Способ реабилитации двигательных нарушений в виртуальной среде с выполнением нескольких задач одновременно у пациентов, перенесших ишемический инсульт | 2023 |
|
RU2823137C1 |
| Способ реабилитации пациентов с неврологическими нарушениями после ишемического инсульта | 2023 |
|
RU2829423C2 |
Изобретение относится к области медицины, в частности к неврологии. Проводят тренировку, предъявляя больному задание по воображению движения паретичной конечностью с последующим контролем воображаемого движения. При этом регистрируют ЭЭГ, передают полученные данные в компьютер для их синхронной обработки и выделяют сигналы реакции десинхронизации сенсомоторного ритма, ответственные за воображаемое движение, с помощью классификатора паттернов ЭЭГ по методу Байеса. Результаты распознавания выполняемого ментального задания предъявляют больному по зрительной обратной связи в виде метки на экране монитора. По изменению положения метки определяют правильность выполнения задания. Задание по воображению движения предъявляют в течение 10 секунд. Курс тренировки составляет 6-12 дней, по одной тренировки в день, длительностью 20-30 минут с интервалами между тренировками от 1 до 4 дней. Способ позволяет повысить эффективность реабилитации, что достигается за счет проведения тренировки с использованием обратной связи, в условиях, позволяющих больному визуально контролировать выполнение воображаемого движения паретичной конечностью. 3 ил., 4 табл., 2 пр.
Способ реабилитации больных, перенесших инсульт, путем проведения тренировок паретичной конечности, отличающийся тем, что тренировку проводят, предъявляя больному задание по воображению движения паретичной конечностью с последующим контролем воображения движения больным, основанным на анализе паттернов электроэнцефалограммы (ЭЭГ), возникающих при воображении движения паретичной конечностью, при этом регистрацию ЭЭГ сигналов мозга осуществляют с системы активных электродов энцефалографа, размешенных на поверхности головы, и передачу этих данных в компьютер для их синхронной обработки и выделения сигналов, ответственных за воображение движения с помощью классификатора паттернов ЭЭГ по методу Байеса, результаты распознавания выполняемого ментального задания предъявляют больному по зрительной обратной связи в виде метки на экране монитора, по изменению которой определяют правильность выполнения задания, установленную путем сравнения параметров реакции десинхронизации сенсомоторного ритма с таковыми у здоровых испытуемых, в соответствующем полушарии во время воображения движения, причем задание по воображению движения предъявляют в течение 10 секунд, курс тренировки паретичной конечности составляет 6-12 дней, по одной тренировки в день, длительностью 20-30 минут с интервалами между тренировками от 1 до 4 дней.
| ЧЕРНИКОВА Л.А | |||
| и др | |||
| Электромиографическое биоуправление и функциональная магнитно-резонансная томография в постинсультной реабилитации | |||
| Бюллетень сибирской медицины, 2010, 2, с | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ В ОСТРОЙ СТАДИИ ИНСУЛЬТА С ИСПОЛЬЗОВАНИЕМ БИОЛОГИЧЕСКОЙ ОБРАТНОЙ СВЯЗИ И ВИРТУАЛЬНОЙ РЕАЛЬНОСТИ | 2010 |
|
RU2432971C1 |
| US 2008021342 A1, 24.01.2008 | |||
| ЧЕРНИКОВА Л.А | |||
| и др | |||
| Применение технологии виртуальной реальности при восстановлении движений в паретичной | |||
Авторы
Даты
2014-07-20—Публикация
2013-04-11—Подача