Настоящее изобретение относится к способу лечения органов, которые являются дегенерировавшими и/или находятся в патологическом состоянии, посредством использования клеток, которые являются фенотипически стабильно дифференцирующимися или дифференцированными, но не обязательно окончательно детерминированными в отношении развития, из органа-донора, выбранного согласно принципам программы противоположной дифференцировки клеток (ППДК), и также к применению клеток этого типа для лечения или для производства лекарственного средства для лечения этих органов. Кроме того, настоящее изобретение относится к фармацевтическим агентам, содержащим подходящие фенотипически стабильные клетки.
В настоящее время большинство широко распространенных в западном мире дегенеративных заболеваний находится в центре внимания клеточных терапий (Slack JMW. Metaplasia and transdifferentiation: from pure biology to the clinic. Nature Rev. 2007; 8: 369-378). Эти заболевания включают нейродегенеративные заболевания (Альцгеймера, Паркинсона, Хантингтона и т.д.), хронические заболевания печени (гепатит, фиброз и цирроз), диабетические заболевания, сердечные заболевания, артрит и многие другие. Фундаментальной концепцией этих клеточных терапий является замена клеток, которые повреждены и ограничены в своих способностях или потеряли свою способность к регенерации, или содействие их замене посредством трофических факторов, которые продуцируются трансплантированными естественными или биотехнологически модифицированными клетками (Slack JMW. Metaplasia and transdifferentiation: from pure biology to the clinic, Nature Rev. 2007; 8:369-378).
В качестве подходящих клеток для возможного терапевтического успеха обсуждаются эмбриональные стволовые клетки, стволовые клетки взрослых, трансдифференцировка клеток (например, гемопоэтических стволовых клеток до клеток соответствующего органа), а также длительное или кратковременное применение клеток, которые стимулируют регенерацию в органах-реципиентах путем продукции цитокинов и ростовых факторов (Slack JMW. Metaplasia and transdifferentiation: from pure biology to the clinic, Nature Rev. 2007; 8: 369-378).
Первые экспериментальные, а также клинические испытания в этом направлении дали неудовлетворительные результаты (Jeffrey DR Failure of allogenic bone marrow transplantation to arrest disease activity in multiple sclerosis. Mult. Scler. 2007; July 10 (Epub ahead of print)) и одновременно выявили внутренние недостатки этого терапевтического подхода.
Концепция «программы противоположной дифференцировки клеток» (ППДК) согласно данному изобретению выходит за пределы ранее упомянутых терапевтических подходов, разработанных для замены клеток, и следует другой стратегии.
Современные способы клеточной терапии хронически больных органов основаны на применении:
1. стволовых клеток различного происхождения со способностью к дифференцировке в клетки больного органа и/или
2. клеток, в частности клеток, подвергнувшихся генетическим манипуляциям, которые обладают свойствами (например, продукции трофических факторов), посредством которых можно оказать положительное влияние на регенерацию больного органа.
Каждый из этих способов обещал радикальный прогресс в отношении терапевтических возможностей хронически больных органов или уже достигал его, но в то же самое время вызывал ряд существенных и неразрешенных недостатков.
В случае терапии стволовыми клетками используют плюри- или мультипотентные (недифференцированные) клетки-доноры (эмбриональные стволовые клетки (СК) или стволовые клетки взрослых), мезенхимные или эпителиальные гемопоэтические СК, клетки костного мозга, стволовые клетки из жировой ткани и кожи или из корней волос и из других органов) (Wobus AM, Boheler KR. Embryonic Stem Cells: prospects for developmental biology and cell therapy. Physol. Rev. 2005; 85: 635-678). Это применение основано на обнаружении того, что недифференцированные стволовые клетки имеют способность превращаться при ограниченном числе клеточных делений в разные органоспецифичные дифференцированные клетки. Примерами этого является превращение стволовых клеток в остеобласты, хондроциты, адипоциты, антигенпрезентирующие дендритные клетки. Однако также обсуждается возможность превращения дифференцированных клеток органа посредством подходящих мер, например путем трансфекции генов транскрипционных факторов, в другие дифференцированные клетки органа (трансдифференцировка; Slack JMW. Metaplasia and transdifferentiation: from pure biology to the clinic. Nature Rev. 2007; 8: 369-378). Основываясь на их фенотипической гибкости (плюри- или мультипотентности), полагают, что стволовые клетки могли бы быть имплантированы практически во все органы для того, чтобы заменить там клетки органа, выполняющие функции. Применение стволовых клеток или трансдифференцировки, однако, включает следующие недостатки:
- канцерогенные свойства (особенно в случае эмбриональных стволовых клеток);
- повышенный потенциал к дедифференцировке (со стволовыми клетками взрослых, генерацией опухолевых стволовых клеток);
- трансформация в чужеродные для органа клетки в культуре клеток и после трансплантации;
- дегенерация клеток или потеря ими незаменимой способности и/или регулируемости средой на основе генетической манипуляции;
- ограниченное число получаемых стволовых клеток;
- низкая скорость пролиферации взрослых или уже почти дифференцированных стволовых клеток;
- этические сомнения (в случае эмбриональных и фетальных стволовых клеток).
Предыдущая стратегия клеточной терапии (хронических) дегенеративных заболеваний основана на применении стволовых клеток или других клеток с терапевтическим потенциалом на поздней стадии заболевания, когда спонтанная или фармакологически индуцибельная защита и регенерация внутренних функциональных клеток тела не справляются. Хронический характер заболевания, таким образом, означает то, что в контексте органа преобладают (патологические) регуляторные системы, которые вызывают неизбежное принуждение поддерживать данную патологию. Непрерывное воздействие патогенных факторов на нервную ткань и ткань, не являющуюся нервной, запускает органоспецифичный гомеостаз и нарушает как метаболические пути, так и пути трансдукции сигнала, которые обеспечивают или контролируют компенсацию повреждения в здоровом контексте. Эти принуждения предотвращают (блокируют) не только внутреннюю регенерацию организма, но также заставляют трансплантированные клетки изменяться в патологическом направлении. Кроме того, патологическое окружение может ускорять дифференцировку и, следовательно, старение и происходящую из-за него потерю функции имплантированных стволовых клеток. Чем выше фенотипическая гибкость используемых стволовых клеток, тем легче они будут поддаваться патологическому давлению, тем больше, например, угроза ошибочной дифференцировки, неопластического нарушения или устранения этих клеток посредством гибели клеток.
Цель достижения стабильного, постоянно функционального фенотипа клеток-доноров, которые являются устойчивыми к дегенеративному окружению, к настоящему времени не была достигнута посредством применения стволовых клеток. Следовательно, цель настоящего изобретения заключается в том, чтобы избежать известные недостатки, возникающие из-за применения генетически модифицированных клеток, а также стволовых клеток различного происхождения в случае клеточной терапии. Эта цель достигается при помощи данных способов, а также фармацевтических агентов согласно настоящим независимым пунктам формулы изобретения. Полезные воплощения указаны в зависимых пунктах формулы изобретения.
Достижение этой цели заключается в применении концепции программы противоположной дифференцировки клеток (ППДК). ППДК исходит из двух основных предпосылок, которые не принимаются во внимание во всех других подходах клеточной терапии. Одной основной предпосылкой является существование в разных органах популяций клеток (типов клеток), которые в отношении конкретного набора экспрессируемых генов или в отношении конкретного набора фенотипических свойств, потенциально имеют обратные (противоположные) или реципрокные свойства и/или контрольные механизмы. В качестве примера следует упомянуть, например, популяции клеток, которые выполняют незаменимую функцию в отношении поддержания тканевого гомеостаза, переноса вещества между разными компартментами (примеры: кровь/ткань; воздух/ткань), детоксикации и регенерации (сокращенно именуемые "GPC" (клетки, продуцирующие глиальный белок), клетки продуцирующие GFAP (глиальный фибриллярный кислый белок) (Danielyan L, Tolstonog G, Traub P, Salvetter J, Gleiter CH, Reisig D, Gebhardt R, Buniatian GH. 4.6 Colocalization of glial fibrillary acidic protein, metallothionein, and MHC II in human, rat NOD/SCID, and nude mouse skin keratinocytes and fibroblasts. J Invest Dermatol. 2007 Mar.; 127 (3): 555-63). Второй предпосылкой является знание того, что эти клетки присутствуют в разных органах в состояниях активации или в состояниях регуляции, отличных от тех, которые доминируют в соответствующем типе ткани, которые в случае заболевания обычно, хотя и не обязательно, принимают точно противоположное состояние активации (или состояние дифференцировки) или состояние регуляции в отношении особенно важных функциональных белков и/или механизмов регуляции (Buniatian G.H., H-J Hartmann, P. Traub, U. Weser, H. Wiesinger, R. Gebhardt (2001). Acquisition of blood-tissue barrier supporting features by hepatic stellate cells and astrocytes of myofibroblastic phenotype. Inverse dynamics of metallothionein and glial fibrillary acidic protein expression. Neurochem. Int. 38, 373-383; Buniatian G.H., Hartmann H.-J., Traub P., Wiesinger H., Albinus M., Nagel W., Shoeman R., Mecke D., Weser U. (2002). Glial Fibrillary Acidic Protein-Positive Cells of the Kidney are Capable of Raising a Protective Biochemical Barrier Similar to Astrocytes: Expression of Metallothionein in Podocytes. Anat. Rec. 267, 296-306). Новым и неожиданным способом концепция ППДК теперь исходит из того факта, что трансплантация клеток, направленная на терапию больной ткани, является особенно успешной, когда трансплантируются представители популяции клеток, природное состояние активации или фенотип которых в отношении упомянутых важных антигенов (белков) или механизмов регуляции в органе-доноре являются противоположными фенотипу «родственных» клеток в органе-реципиенте. Таким образом, не важно, имеет ли популяция трансплантированных, естественных клеток свойства стволовых клеток, служит ли она источником трофических факторов или имеет другие свойства, которые стимулируют регенерацию органа-рецептора. В основе программы противоположной дифференцировки клеток лежит тот факт, что во многих (если не во всех) органах существуют «родственные» клетки, состояние дифференцировки которых варьирует таким образом, что существуют группы из пар органов, в которых это состояние дифференцировки соответствующих родственных клеток можно назвать обратным или противоположным. «Родственные» клетки в этом контексте не обязательно означает родственные в смысле того же самого происхождения, но также может просто означать то, что эти клетки имеют ограниченный набор тех же самых экспрессируемых генов А, В, С,… так, что эти клетки в одном органе могут характеризоваться, например, свойством: «ген А имеет высокий уровень экспрессии, ген В экспрессируется в меньшей степени», и в другом - «противоположным» свойством: «ген А экспрессируется в меньшей степени, ген В имеет высокий уровень экспрессии». Это следует вновь прояснить со ссылкой на два следующих примера, не ограничивая данное изобретение ими:
А) В каждом органе существует популяция клеток, которая выполняет незаменимую функцию в отношении поддержания тканевого гомеостаза, переноса вещества между разными компартментами (примеры: кровь/ткань; воздух/ткань), детоксикации и регенерации (например, клетки, продуцирующие GFAP). Помимо белка промежуточных филаментов GFAP (глиальный фибриллярный кислый белок), эти клетки в то же самое время могут продуцировать другие белки цитоскелета, например, SMAA (альфа-актин гладких мышц), белок микрофиламентов. Данные последних нескольких лет показали, что эти клетки присутствуют в различных органах в разных состояниях активации, которые доминируют в соответствующем типе ткани. Таким образом, например, астроциты в нормальном мозге характеризуются высокой экспрессией SMAA и низкой экспрессией GFAP, тогда как звездчатые клетки печени (HSC) - высокой экспрессией GFAP и низкой экспрессией SMAA. Этот варьирующий тип экспрессии генов связан с такой ситуацией, что нормальные астроциты участвуют в постройке малопроницаемого гематоэнцефалического барьера, тогда как HSC в печени способствуют постройке высокопроницаемой поверхности между кровью и тканью печени или определяют ее. В случае заболевания это состояние экспрессии изменяется на противоположное соответствующим образом, а также, следовательно, и проницаемость пораженной ткани гематоэнцефалического барьера, как и другие свойства, имеющие отношение к поддержанию тканевого гомеостаза, детоксикации и регенерации. Это означает то, что в дегенерировавшей зоне мозга в астроцитах снижается высокая экспрессия SMAA и возрастает экспрессия GFAP, тогда как в HSC в печени снижается экспрессия GFAP и возрастает экспрессия SMAA. Характеристика клеток с фенотипом, который является противоположным в нормальном состоянии, следовательно, не ограничивается примером белков GFAP и SMAA. На терапевтические свойства GPC также могут указывать другие паттерны экспрессии, например, экспрессия глутаминсинтетазы, металлотионеина или молекул МНС (главный комплекс гистосовместимости) II класса, и они могут определять противоположный фенотип. В этом случае реакции детоксикации находятся на переднем плане функции ткани.
Б) Второй пример в большей степени выдвигает на передний план регуляторный аспект. Во многих (если не во всех) тканях взрослых дуализм трансдукции сигнала hedgehog- и Wnt/β-катенина является особенно важным при субструктурировании тканей: часть клеток в большей степени подвержена влиянию hedgehog, другая - в большей степени влиянию Wnt/β-катенина. Примером этого может быть кишечник, в криптах которого преобладает влияние Wnt/β-катенина, тогда как влияние hedgehog является доминирующим на кончиках ворсинок. Такой дуализм применим даже к печени. Без постоянного антагонизма этих противоположных сигнальных путей, обеспечивающего определенный тканеспецифичный метаболический баланс, ткань подвергается различным типам патологии, включая образование опухоли. Наоборот, в случае патологии влияние одного из этих сигнальных путей усиливается за счет другого и, следовательно, аналогично примеру с GPC, процитированному выше, индуцируется противоположный или реципрокный фенотип клеток, который, однако, является значительно менее стабильным, чем соответствующий природный фенотип.
ППДК, следовательно, делает возможной и/или предполагает идентификацию подходящих клеток, которые оцениваются конкретно для трансплантации: прежде всего, определяют, какой тип клеток преимущественно поврежден или изменен в патологическом органе или который исходно играет более важную роль для патологии. Можно предположить, что патологический фенотип в отношении существенных свойств ведет себя противоположно нормальному фенотипу. Это конечно не применимо глобально, т.е. в отношении всего протеома этих клеток, но только в отношении существенных свойств в вышеуказанном смысле. На втором этапе идентифицируют орган, который содержит «родственный» тип клеток, который соответствует патологическому фенотипу в отношении существенных свойств и, если необходимо, показывает противоположный паттерн дифференцировки относительно нормального типа клеток патологического органа. Дифференцирующаяся или дифференцированная клетка-донор (с противоположными характеристиками дифференцировки) должна происходить из здорового органа-донора с противоположными физиологическими функциями и характеристиками поверхностей кровь-ткань, например, из печени и мозга. Благодаря опыту и памяти (Ghazarian A, Garner WL, Ehrlich HP. Memory of past exposure to the chemokine IL-8 inhibits the contraction of fibroblast-populated collagen lattices. Exp Mol Pathol. 2000 Dec; 69(3):242-7; Huang C, Kirn Y, Caramori ML, Moore JH, Rich SS, Mychaleckyj JC, Walker PC, Mauer M. Diabetic nephropathy is associated with gene expression levels of oxidative phosphorylation and related pathways. Diabetes. 2006 Jun; 55(6): 1826-31), которые клетка-донор приобретает на протяжении жизненного цикла в органе-доноре, после трансплантации этого типа клетки она может лучше соответствовать ее патологическому окружению и также лучше сопротивляется его патогенному давлению. Следовательно, регенерация может быть введена этим типом клеток более эффективно. Таким образом, не важно, имеет ли этот тип клеток специфические свойства мультипотентных стволовых клеток (например, свойство трансформироваться в родственные типы клеток органа-реципиента) или просто имеет свойства, стимулирующие регенерацию, и влияет, например, на экспрессию трофических факторов.
В случае GPS, например, имеет место следующая ситуация: в дегенерировавшем мозге и в случае нормального старения в клеточной структуре астроциты, которые оказывают в мозге сильный защитный эффект в отношении вредных агентов самых разных типов, теряют их активированный сократительный фенотип и все в большей степени приобретают расширенный фенотип с пониженной функциональностью. Эта патологическая ситуация в мозге улучшается введением фенотипически стабильно дифференцирующихся или дифференцированных активированных звездчатых клеток печени (HSC) из печени или мезангиальных клеток (МС) из почки.
Например, HSC и МС запрограммированы к приобретению активированного и сократительного фенотипа и ко все возрастающему усилению этого фенотипа в ходе их дифференцировки (т.е. свойств функциональных астроцитов). В результате многообразия защитных факторов, которые продуцируются фенотипически стабильно дифференцирующимися или дифференцированными активированными HSC и МС (эритропоэтин и/или BDNF (нейротрофический фактор головного мозга), и/или металлотионеины, и/или глутаминсинтетаза, и/или NGF (фактор роста нервов), и/или коллаген типа 1, и/или GPR 49 (связанный с G-белком рецептор 49) и другие), эти клетки могут улучшить нарушенный гомеостаз и выживание, а также функциональность клеток органа-реципиента (в случае мозга). Кроме того, HSC/MC аналогично стволовым клеткам в условиях культуры могут приобретать свойства нейронов (образование синапсов, продукция нейроноспецифичных маркеров, нейромедиаторов и ферментов, которые участвуют в образовании нейромедиаторов). По этой причине HSC/MC (в отличие от их улучшающего гомеостаз и защитного влияния на нейроны и астроциты) могут замещать функции потерянных и дегенерировавших нейронов в случае имплантации в дегенерировавший мозг. Таблица 1 просто в качестве примера показывает уровень экспрессии выбранных факторов как функцию состояний дифференцировки соответствующих типов клеток.
Из-за анатомического и функционального соответствия («аффинности») астроцитов звездчатых клеток печени (HSC) и мезангиальных клеток (МС), которые относятся к GFAP-позитивным околососудистым клеткам мозга, печени и почки, последние имеют аналогичные защитные механизмы против сигналов, происходящих из крови. Главными признаками дегенеративных заболеваний мозга являются потеря нейронов и глубокие изменения в специфичном для мозга гомеостазе, причем последний регулируется астроцитами. Особенностью HSC и МС для клеточной терапии нейродегенеративных заболеваний является то, что эти GFAP-PC, не являющиеся нервными, естественно запрограммированы для приобретения и усиления в ходе их дифференцировки (активации) характерных свойств молодых астроцитов (антицитотоксическая функция), нервных SC (продукция нестина) и нейронов (P-III тубулин, нейромедиаторы, нейротрофные факторы). Они быстро пролиферируют in vitro и in vivo и стабильно поддерживаются в больной ткани органа-реципиента из-за их дифференцированного фенотипа. Точно противоположно идущая программа дифференцировки астроцитов и HSC/MC обеспечивает применение фенотипически стабильных дифференцирующихся или дифференцированных HSC/MC для лечения нейродегенеративных заболеваний.
Стабильно дифференцирующиеся или дифференцированные HSC, которые используют для клеточной терапии нейродегенеративных заболеваний, продуцируют ЕРО (эритропоэтин), GS (глутаминсинтетазу) и МТ (металлотионеин). Их цитоскелет поддерживается нестином, бета-тубулином, десмином и SMAA. В случае этих клеток GFAP, который экспрессируется околоядерно или в ядре (но не в выпячиваниях), может присутствовать в малых количествах.
Следовательно, HSC и/или МС можно использовать для клеточной терапии при ряде нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона, рассеянный склероз, инсульт и другие заболевания, характеризующиеся потерей числа и функциональности нейронов и нарушением гомеостаза, специфичного для мозга.
В случае HSC/MC (или другого типа клеток с аналогичной программой дифференцировки) данные клетки доставляют в больной мозг посредством имплантации, внутривенного введения или других типов введения. Имплантацию HSC, следовательно, можно осуществлять даже у пациентов с поздними стадиями вышеупомянутых заболеваний. Имплантация HSC и/или МС предназначена для:
1) постоянного улучшения специфичного для мозга гомеостаза в поврежденной ткани за счет их отчетливой детоксифицирующей функции (продукция глутаминсинтетазы, эритропоэтина, металлотионеина),
2) увеличения коэффициента выживаемости собственных нейронов реципиента, а также их регенерации (например, аксональной регенерации),
3) улучшения нейропередачи путем превращения HSC/MC в клетки типа нейронов, которые могут продуцировать функциональные белки (например, ацетилхолин, тирозингидроксилазу),
4) улучшения функциональности клеток в органе-реципиенте (присутствие HSC/MC индуцирует продукцию ацетилхолина, тирозингидроксилазы в астроцитах/нейронах),
5) увеличения числа нейронов согласно (2), (3), (4).
В дифференцированном и активированном состоянии HSC экспрессирует белки МНС II класса, и, соответственно, они имеют антигенпрезентирующую функцию, варьирующую от очень слабой до едва присутствующей. Следовательно, в случае имплантации HSC проблемы реакции отторжения, которая присутствует со стволовыми клетками, и плохого коэффициента выживаемости имплантов устраняются или уменьшаются.
Дегенерация печени характеризуется потерей гепатоцитов, следовательно, сниженной функцией детоксикации, осуществляемой гепатоцитами, и глубокими изменениями специфичного для печени гомеостаза, контролируемого покоящимися HSC, и структурной модификацией синусоидов печени, осуществляемой активированными HSC. Покоящиеся HSC активно экспрессируют GFAP, белок промежуточных филаментов, поддерживающий продукцию ферментов, деградирующих внеклеточный матрикс, что поддерживает облегченный обмен кровь-печень посредством фенестрации в капилляре печени. Покоящиеся HSC, запасающие витамин А, продуцируют комплекс антигенов МНС II класса, важный для презентирования антигенов лимфоцитам хоуминга. Также эта функция осуществляется посредством фенестрации печени, размер которых контролируется покоящимися HSC. Фиброз печени характеризуется активацией HSC, проявляющейся в виде потери GFAP, ослабленного расщепления белков ЕСМ (внеклеточный матрикс) и развитием непрерывных, свойственных мозгу капилляров сосудистого типа.
Напротив, созревание и дифференцировка астроцитов приводит к накоплению больших количеств GFAP, MHC-II и металлопротеиназ или же к приобретению свойств, характерных для недифференцированных HSC в здоровой печени и почке и аналогичных клеток в других органах, не являющихся органами нервной системы. Этот набор антигенов был показан во время нейродегенеративных заболеваний (Markowitz СЕ. Interferon-beta: mechanism of action and dosing issues. Neurology. 2007 Jun 12:68 (24 Suppl 4):S8-11.). Частое появление ямок и полостей в стенках сосудов при болезни Альцгеймера (Scheibel AB, Duong Т. On the possible relationship of cortical microvascular pathology to blood brain barrier changes in Alzheimer's disease. Neurobiol Aging. 1988 Jan-Feb;9(1):41-2.) демонстрирует универсальность механизмов, обеспечивающих облегченное взаимодействие кровь-ткань, и способность околососудистых клеток, обогащенных GFAP, к поддержке открытия трансклеточных путей. Дифференцировка астроцитов заканчивается либо в мозге взрослого, либо она может достигаться в культуре нервных клеток.
Согласно данному изобретению дифференцирующиеся и фенотипически стабильные дифференцированные астроциты можно использовать для лечения органов, не являющихся органами нервной системы, пораженных фиброзом или другим заболеванием, которое по существу вызвано данным расстройством. Примерами этого являются цирроз печени и фиброз почек.
Дифференцированные астроциты (или другой тип клеток с аналогичной программой дифференцировки) поставляют в орган, не являющийся органом нервной системы (например, в печень в случае фиброза печени, цирроза печени). Также возможно применение фенотипически стабильно дифференцирующихся астроцитов.
В отличие от терапии стволовыми клетками и генотерапии, терапии нейродегенеративных заболеваний на основе HSC/MC и терапии фиброзных заболеваний органов, не являющихся органами нервной системы (печень, почка), на основе глии предлагают ряд преимуществ.
1) Фенотипическая стабильность трансплантированных клеток и их устойчивость к патологическим состояниям, которые преобладают в органе-реципиенте. Дифференцированные HSC/MC могут предпочтительно трансдифференцироваться в нейроно- и глиоподобные типы клеток после имплантации в мозг и, следовательно, оставаться фенотипически стабильными в отличие от стволовых клеток. Это дает решающее преимущество во время имплантации в болезненное окружение: трансплантированные клетки не будут принимать фенотип дегенерировавших клеток; и б) в результате их естественного программирования и сильной детоксифицирующей функции не только будут выживать в токсических условиях, но также будут улучшать гомеостаз.
2) Освобождение от этических сомнений (в отличие от эмбриональных стволовых клеток) и малая сложность способа выделения. Например, HSC/MC можно получать из собственной (аутологичной) печени или почки реципиента в больших количествах, чем в случае со стволовыми клетками взрослого, и можно размножать в культуре клеток путем индукции пролиферации. Другой возможностью является их получение из мезенхимных стволовых клеток, происходящих из крови, т.е., для индукции превращения мезенхимных стволовых клеток в HSC и МС.
3) Количество клеток, подлежащих трансплантации, не ограничено (из-за их высокой способности к пролиферации и возможности получения этих клеток из органа-донора).
4) Очень хорошая выживаемость имплантированных HSC/MC клеток в ткани-реципиенте из-за их гипоиммуногенности. Они имеют лишь слабовыраженную (по меньшей мере в условиях культуры клеток) антигенпрезентирующую функцию, так как они едва ли экспрессируют какие-либо белки МНС II класса.
Итак, стабильно дифференцирующиеся или дифференцированные околососудистые GFAP-позитивные клетки (HSC, МС и астроциты), соответственно, могут давать большую выживаемость имплантата в органе-реципиенте, улучшение гомеостаза, фенотипическую стабильность в органе-реципиенте и легкость получения и манипуляции с этими клетками до имплантации.
Кроме того, в качестве дополнительного примера применения ППДК можно упомянуть взаимную замену гломерулярных подоцитов и кератиноцитов кожи.
Применение фенотипически стабильно дифференцирующихся или дифференцированных клеток осуществляется известным способом. Например, их можно вводить или имплантировать внутривенно, интратекально (спинально), интракраниально, в спинномозговую жидкость, интраперитонеально, внутримышечно и/или подкожно.
Вводимые количества преимущественно составляют от 5×103 до 1×1010 клеток. Данное количество, соответственно, может зависеть от: 1) стадии заболевания; 2) возраста пациента; 3) типа заболевания; 4) пути введения (внутривенное, интраперитонеальное и т.д.); 5) длительности введения (постоянно, один или несколько раз); 6) предшествующих и/или сопутствующих заболеваний.
Показателями введения преимущественно являются однократное введение, инфузия с разными скоростями и продолжительностью инфузии, многократное или постоянное введение.
В настоящем изобретении далее заявлено применение фенотипически стабильно дифференцирующихся или дифференцированных клеток в качестве клеток-доноров (первых клеток) для производства лекарственного средства для лечения второго органа организма, который является дегенерировавшим и/или находится в патологическом состоянии, со вторыми клетками, которые являются дегенерировавшими и/или находятся в патологическом состоянии, причем используемые в качестве клеток-доноров клетки первого органа, который отличается от второго органа в отношении типа органа, при нормальном физиологическом состоянии имеют противоположные свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств относительно вторых клеток в нормальном физиологическом состоянии.
Указанное применение может далее характеризоваться тем, что вторые клетки в дегенерировавшем и/или в патологическом состоянии имеют противоположные свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств по сравнению с их нормальным физиологическим состоянием.
Указанное применение может далее характеризоваться тем, что клетки-доноры в их нормальном физиологическом состоянии являются эквивалентными в отношении заданного набора экспрессируемых генов и/или фенотипических свойств клеткам, которые являются дегенерировавшими и/или находятся в патологическом состоянии, и/или имеют те же самые свойства.
Указанное применение может далее характеризоваться тем, что клетки-доноры по сравнению со вторыми клетками в отношении заданного набора экспрессируемых генов и/или фенотипических свойств имеют противоположную программу дифференцировки в дегенерировавшем и/или в патологическом состоянии в отличие от нормального физиологического состояния.
В настоящем изобретении далее заявлено применение фенотипически стабильно дифференцирующихся или дифференцированных клеток специфического первого типа клеток организма для производства лекарственного средства для защиты и/или регенерации клеток специфического второго типа клеток организма, которые являются дегенерировавшими и/или находятся в патологическом состоянии, причем клетки первого типа клеток в нормальном физиологическом состоянии имеют противоположные свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств относительно клеток второго типа клеток в нормальном физиологическом состоянии.
В настоящем изобретении далее заявлено применение фенотипически стабильно дифференцирующихся или дифференцированных клеток специфического первого типа клеток организма для защиты и/или регенерации клеток специфического второго типа клеток организма, которые являются дегенерировавшими и/или находятся в патологическом состоянии, причем клетки первого типа клеток в нормальном физиологическом состоянии имеют противоположные свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств относительно клеток второго типа клеток в нормальном физиологическом состоянии.
Указанные выше применения могут далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки находятся в нормальном физиологическом состоянии.
Указанные выше применения могут далее характеризоваться тем, что клетки второго типа клеток в дегенерировавшем и/или в патологическом состоянии имеют противоположные свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств по сравнению с их нормальным физиологическим состоянием.
Указанные выше применения могут далее характеризоваться тем, что клетки первого типа клеток в нормальном физиологическом состоянии являются эквивалентными клеткам второго типа клеток, которые являются дегенерировавшими и/или находятся в патологическом состоянии, и/или имеют те же самые свойства в отношении заданного набора экспрессируемых генов и/или фенотипических свойств.
Указанные выше применения могут далее характеризоваться тем, что клетки первого типа клеток в нормальном физиологическом состоянии имеют обратные и/или противоположные состояния активации, регуляции и/или дифференцировки относительно клеток второго типа клеток, которые являются дегенерировавшими и/или находятся в патологическом состоянии, в отношении заданного набора экспрессируемых генов и/или фенотипических свойств.
Указанные выше применения могут далее характеризоваться тем, что степень активации, регуляции и/или дифференцировки клеток первого типа клеток в нормальном физиологическом состоянии являются противоположными степени активации, регуляции и/или дифференцировки клеток второго типа клеток, которые являются дегенерировавшими и/или находятся в патологическом состоянии, в отношении заданного набора экспрессируемых генов и/или фенотипических свойств.
Указанные выше применения могут далее характеризоваться тем, что как вторые клетки, так и клетки-доноры или клетки как первого типа клеток, так и второго типа клеток в их соответствующем органе имеют функции гомеостаза ткани органа, переноса вещества между разными компартментами органа, детоксикации органа и/или регенерации органа.
Указанные выше применения могут далее характеризоваться тем, что экспрессируемые гены и/или фенотипические свойства данного заданного набора выполняют функции в рамках гомеостаза ткани органа, переноса вещества между разными компартментами органа, детоксикации органа и/или регенерации органа.
Указанные выше применения могут далее характеризоваться тем, что по меньшей мере одна или более чем одна из заданных функций и/или свойств клеток органа, который является дегенерировавшим и/или находится в патологическом состоянии, или клеток второго типа является ослабленной и/или отсутствует.
Указанные выше применения могут далее характеризоваться тем, что организм является позвоночным и/или млекопитающим.
Указанные выше применения могут далее характеризоваться тем, что организм представляет собой человека.
Указанные выше применения могут далее характеризоваться тем, что клетки-доноры или клетки первого типа клеток продуцируют защитные факторы в виде заданных клеточных свойств и/или функций.
Указанные выше применения могут далее характеризоваться тем, что клетки-доноры или клетки первого типа клеток продуцируют один или более чем один фактор, который является специфичным для вторых клеток или клеток второго типа и стимулирует рост и/или регенерацию, причем указанные факторы не продуцируются или недостаточно продуцируются вторыми клетками или клетками второго типа клеток.
Указанные выше применения могут далее характеризоваться тем, что используют/вводят GFAP (глиальный фибриллярный кислый белок)-позитивные клетки, в частности околососудистые GFAP-позитивные клетки.
Указанные выше применения могут далее характеризоваться тем, что используемые/вводимые клетки продуцируют эритропоэтин, и/или BDNF (нейротрофический фактор головного мозга), и/или металлотионеин, и/или глутаминсинтетазу, и/или NGF (фактор роста нервов), и/или коллаген типа 1, и/или GPR 49 (связанный с G-белком рецептор 49), и/или другие защитные факторы.
Указанные выше применения могут далее характеризоваться тем, что используют/вводят глиальные клетки.
Указанные выше применения могут далее использоваться для лечения фиброзных заболеваний органа, не являющегося органом нервной системы, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные астроциты или клетки, имеющие аналогичную программу дифференцировки.
Указанные выше применения могут далее использоваться для лечения цирроза печени, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные астроциты или клетки, имеющие аналогичную программу дифференцировки.
Указанные выше применения могут далее использоваться для лечения фиброза почки, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные астроциты или клетки, имеющие аналогичную программу дифференцировки.
Указанные выше применения могут далее использоваться для лечения нейродегенеративных заболеваний, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени и/или мезангиальные клетки, или клетки, имеющие аналогичную программу дифференцировки.
Указанные выше применения могут далее использоваться для лечения заболеваний, характеризующихся потерей нейронов и/или их функциональности, и/или расстройством орган-специфичного гомеостаза, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
Указанные выше применения могут далее использоваться для лечения болезни Альцгеймера, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
Указанные выше применения могут далее использоваться для лечения рассеянного склероза, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
Указанные выше применения могут далее использоваться для лечения болезни Паркинсона, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
Указанные выше применения могут далее использоваться для лечения инсульта, где используют/вводят фенотипически стабильно дифференцирующиеся или дифференцированные звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
В настоящем изобретении далее заявлен фармацевтический агент, характеризующийся тем, что он содержит фенотипически стабильно дифференцирующиеся или дифференцированные клетки в отношении по меньшей мере одного или более чем одного заданного свойства и/или функции клетки.
Указанный фармацевтический агент может далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки продуцируют защитные факторы в виде заданных свойств и/или функций клетки.
Указанный фармацевтический агент может далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки являются GFAP-позитивными клетками, в частности околососудистыми GFAP-позитивными клетками.
Указанный фармацевтический агент может далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки являются глиальными клетками.
Указанный фармацевтический агент может далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки являются астроцитами или клетками, имеющими аналогичную программу дифференцировки.
Указанный фармацевтический агент может далее характеризоваться тем, что фенотипически стабильно дифференцирующиеся или дифференцированные клетки являются звездчатыми клетками печени, мезангиальными клетками, звездчатыми клетками поджелудочной железы, дендритными клетками селезенки и/или фибробластами кожи.
Следующие примеры объясняют данное изобретение без какого-либо ограничения.
1. Тесты in vitro
Далее используются следующие сокращения: HSC - звездчатые клетки печени; МС - мезангиальные клетки; GFAP-PC - околососудистые клетки, позитивные по глиальному фибриллярному кислому белку; АР - астроглиальная первичная культура; Р - пассаж; ЕРО - эритропоэтин; GS - глутаминсинтетаза; МТ - металлотионеин; PCNA - ядерный антиген пролиферирующей клетки; ППДК - программа противоположной дифференцировки клеток.
Защитные свойства HSC, линии клеток HSC-T6 и МС охарактеризовали в индивидуальных монокультурах и в сокультурах с астроглиальными первичными культурами из крыс посредством иммуноцитохимических анализов разных маркерных белков, специфичных для функции и типа клеток. Эффективность лечения посредством ППДК оценивали в моделях in vitro из сокультур высокодифференцированных первичных культур из мозга и GFAP-PC, не являющихся нервными. GFAP-PC, не являющиеся нервными, включают следующие (клетки):
1. мезангиальные клетки из почек взрослых и из почек новорожденных крыс,
2. активированные HSC взрослых (первичная культура),
3. линия клеток HSC-T6 (линия активированных клеток HSC).
Все эти типы клеток анализировали индивидуально и в сокультурах с астроглиальными клетками при разном возрасте культуры (вплоть до 150 суток в культуре) и при разных количественных условиях относительно друг друга и при разных плотностях клеток.
Нейронспецифичные морфологические и антигенные свойства дифференцированных GFAP-PC, не являющихся нервными, т.е. активированных HSC и МС, достигнутые посредством дифференцировки, показаны далее.
Свойства GFAP-PC клеток (HSC и МС), специфичные для нейронов и стволовых клеток
В случае МС от новорожденных крыс в культурах разного возраста (сутки 7; сутки 14 и сутки 21), а также HSC и МС взрослых в разных пассажах в МС можно наблюдать постепенное снижение GFAP и возрастающую высокорегулируемую экспрессию бета-III тубулина, маркера нейронов. Кроме того, сильно экспрессируется нестин, маркер стволовых клеток. МС и HSC взрослых также экспрессируют нестин и -III тубулин в значительной степени. В МС можно наблюдать то, что экспрессия бета-III тубулина после 3 пассажей в культуре клеток регулируется очень сильно.
Экспрессия белков с детоксифицирующими и защитными функциями (GS, МТ, ЕРО) и белков, которые участвуют в нейропередаче (синапсин и синаптофизин), и ацетилхолина в GFAP-PC).
Взрослые активированные HSC из крыс и МС в высокой степени экспрессируют GS, фермент, который превращает избыток глутамата и NHs в глутамин. Металлотионеин (МТ), который известен своей функцией «ловушки» в отношении свободных радикалов, наблюдается в GS-позитивных МС. Кроме того, взрослые дифференцированные HSC коэкспрессируют GS и ЕРО. GS и ЕРО также экспрессируются в активированных МС. Взрослые активированные МС показывают высокую пролиферативную способность даже после 9-го пассажа. Это показано по экспрессии PCNA (ядерный антиген пролиферирующих клеток). Активированные МС также экспрессируют маркеры функционально активных нейронов: ацетилхолин, синапсин и синаптофизин.
Нейроноподобная морфология HSC и МС
Луковицы синаптических окончаний в том виде, в котором они являются типичными для нейронов, также были обнаружены в МС и HSC. Из МС и HSC также образуются длинные аксоноподобные выпячивания, типичные для нейронов. Кроме того, двойное окрашивание на ЕРО и GS показало образование в HSC дендритных шипиков.
Экспрессия нейрональных маркеров (бета-III тубулина) и GFAP в сокультурах HSP-T6 (линия клеток HSC) с астроглиальными первичными культурами от крысы
Для того чтобы показать эффективность терапии на основе ППДК в дегенерировавшей ткани ЦНС (центральная нервная система), использовали in vitro модель нейродегенерации астроглиальной первичной культуры, которая главным образом содержит астроциты и имеет очень небольшое число нейронов. Эта модель отражает условия в больном мозге, в котором число нейронов радикально снижается, и число астроцитов возрастает. Поскольку астроциты в специфических зонах мозга имеют свойства клеток-предшественников и могут служить в качестве источника новых популяций клеток, включая нейроны, использовали культуры клеток разного возраста. Помимо молодых 7-суточных клеток и астроцитов среднего возраста (14 суток в культуре) также использовали старые астроциты (30, 48, 90-суточные культуры), которые теряют их исходные свойства.
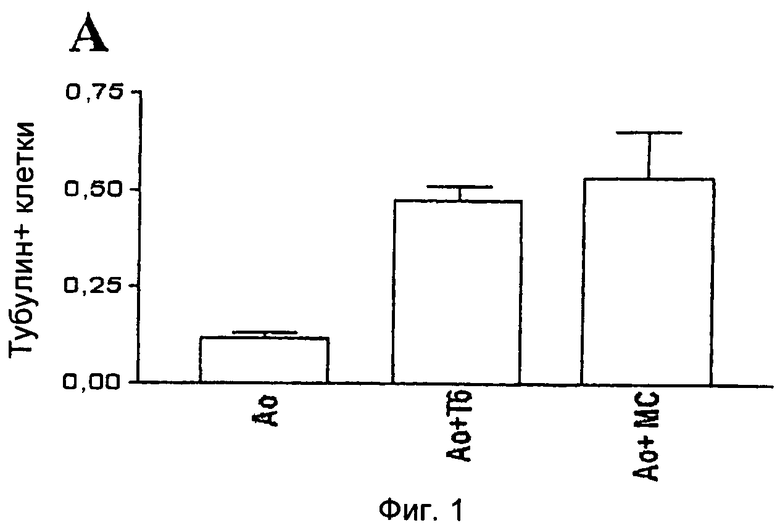
На Фиг.1 показаны изменения числа бета-III тубулин-позитивных клеток в 14-суточных астроглиальных культурах после совместного культивирования с линией клеток HSC-T6 или с первичными МС. Из данной диаграммы очевидно, что 14-суточное совместное культивирование астроглиальных клеток (Ао) с HSC-T6 (Ао+Т6) или с МС (Ао+МС) вызывает почти трехкратное увеличение бета-III тубулин-позитивных клеток по сравнению с астроглиальными контрольными культурами (Ао 14 сут). На сутки 28 астроглиальные культуры содержали лишь несколько бета-III тубулин-позитивных клеток. Введение 5×104 HSC-T6 клеток в 14-суточные астроглиальные культуры приводило к огромному увеличению популяции бета-III тубулин-позитивных клеток после 7-суточного совместного культивирования. После 14 суток в сокультуре наблюдали резкое и значительное увеличение числа бета-III тубулин-позитивных клеток. Из этих бета-III тубулин-позитивных клеток большое число показывало нейрональную морфологию, т.е. отдельные вытянутые аксоноподобные выпячивания и многочисленные короткие дендриты, окружающие тело клетки. Этот эффект наблюдали в культурах с плотностью клеток, меньшей в 5 раз. Бета-III тубулин-позитивные клетки были организованы в сеть. Эти клетки экспрессировали бета-III тубулин на очень высоком уровне и GFAP на очень низком уровне.
Экспрессия нейронального маркера (бета-III тубулина) и GFAP в сокультурах МС с астроглиальными первичными культурами из новорожденных крыс
Астроглиальные клетки культивировали совместно с МС из новорожденных крыс:
1. 14-суточные астроглиальные клетки с МС клетками, свежевыделенными из новорожденных крыс, и последующее совместное культивирование в течение 14 суток.
2. 14-суточные МС с астроглиальными клетками, свежевыделенными из новорожденных крыс, и последующее совместное культивирование в течение 14 суток.
3. 14-суточные МС с 14-суточными астроглиальными клетками из новорожденных крыс после пассажа в культуре и последующее совместное культивирование в течение 14 суток.
4. 21-суточные астроглиальные культуры с 21-суточными МС из новорожденных крыс после пассажа в культуре и последующее совместное культивирование в течение 14 суток.
5. 46-суточные астроглиальные клетки с 31-суточными МС клетками в пассаже 1 и последующее совместное культивирование в течение 14 суток.
Во всех 5 вышеперечисленных условиях сокультуры число бета-III тубулин-позитивных клеток значительно увеличивалось. Кроме того, число покоящихся клеток, которые можно определить только окрашиванием ядра, при контрольных условиях в 60-суточных астроглиальных культурах значительно выше, чем в сокультурах. Поскольку число бета-III тубулин-позитивных клеток в сокультурах значительно возрастает, можно предположить, что эти покоящиеся клетки превращаются в нейроны.
Экспрессия бета-III тубулина в сокультурах 140-суточных астроглиальных культур клеток и взрослых HSC или МС от крыс
В этой серии экспериментов более чем 140-суточные астроглиальные культуры наблюдали в качестве контроля. 28-суточное совместное культивирование 149-суточных астроглиальных клеток (АР1) со взрослыми МС из 8-го пассажа или со взрослыми активированными HSC из 7-го пассажа приводило к значительному увеличению (числа) бета-III тубулин-позитивных клеток по сравнению с контрольной культурой. Совместное культивирование АР1- и линии клеток HSC-T6 приводило к резкому и значительному отделению клеток от основания чашек Петри. Остающаяся популяция прикрепленных клеток, однако, показывала большее число бета-III тубулин-позитивных клеток, чем в контрольной культуре.
Антицитотоксические свойства HSC-T6
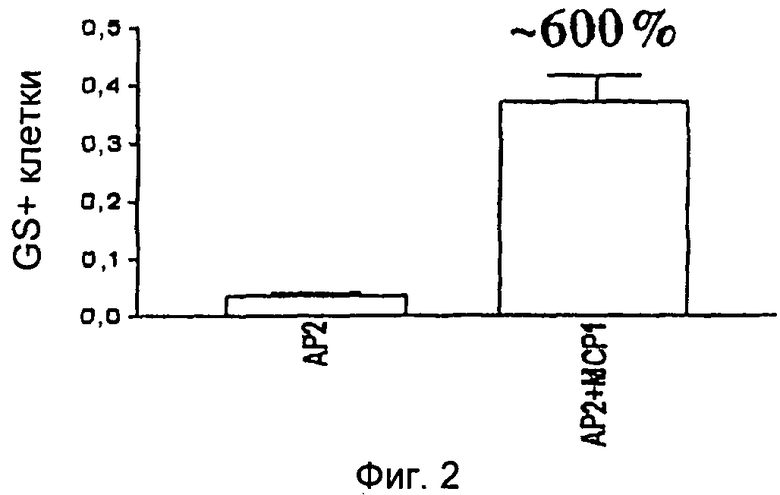
На Фиг.2 показано 600% увеличение числа GS-позитивных клеток в сокультуре астроглиальных клеток после пассажа (Р2) с МС (АР2 + МС Р1) после пассажа (Р1) по сравнению с монокультурой 56-суточных астроглиальных клеток (АР2). Кроме того, на этой Фиг. представлены результаты сравнительного исследования экспрессии GS и МТ в астроглиальных культурах с и без добавления HSC-T6 (клеточная линия активированных HSC). Добавление HSC-T6 к 52-суточным астроглиальным культурам приводило к резкому и значительному увеличению GS, МТ и десмина. Данные клетки формировали нейроноподобную сеть с сильно выраженными выпячиваниями, в которых имела место сильная экспрессия GS, МТ и десмина.
Антицитотоксические свойства МС
Экспрессия и, соответственно, активность GS в 58-суточных астроглиальных культурах резко и значительно возрастает при добавлении МС из новорожденных крыс в 14-суточные сокультуры.
Развитие нейронспецифичных функций в астроглиальных сокультурах с HSC или МС
Экспрессия тирозингидроксилазы (ТН)
На 28-е сутки большое число астроцитов в гомогенной культуре экспрессировало ТН. После 14 суток в сокультуре со взрослыми дифференцированными (активированными) МС из первичных культур из крыс или со взрослыми дифференцированными HSC и МС в 7-ом-8-ом пассаже число ТН-позитивных клеток оставалось приблизительно тем же самым по сравнению с астроглиальными контрольными культурами.
Экспрессия ТН после достаточно длительного времени культивирования
На 40-е сутки в астроглиальных первичных культурах число ТН-позитивных клеток было слегка сниженным в культуре по сравнению с 28-ми сутками. Интенсивность ТН окрашивания и число ТН-экспрессирующих клеток снижалось даже более значительно от 40-ых до 52-ых суток. Совместное культивирование 40-суточных астроглиальных культур со взрослыми активированными МС от крыс или со взрослыми активированными крысиными HSC, или с клеточной линией активированных HSC-T6 давало значительное увеличение экспрессии ТН по сравнению с 52-суточными астроглиальными контрольными культурами.
Экспрессия белка нейрофиламентов (NF)
Добавление 20000 HSC-T6 клеток в 14-суточные астроглиальные культуры приводило к небольшому увеличению числа NF-экспрессирующих клеток по сравнению с астроглиальными контрольными культурами. 10-кратное увеличение числа HSC-T6 клеток приводило к значительному увеличению числа и интенсивности (окрашивания) NF-позитивных клеток в 14-суточных сокультурах из АР (первичная культура астроцитов) и HSC-T6.
Экспрессия ядерного антигена пролиферирующих клеток (PCNA) в сокультурах астроглиальных клеток (пассаж 2, АР2) и линии клеток HSC-T6
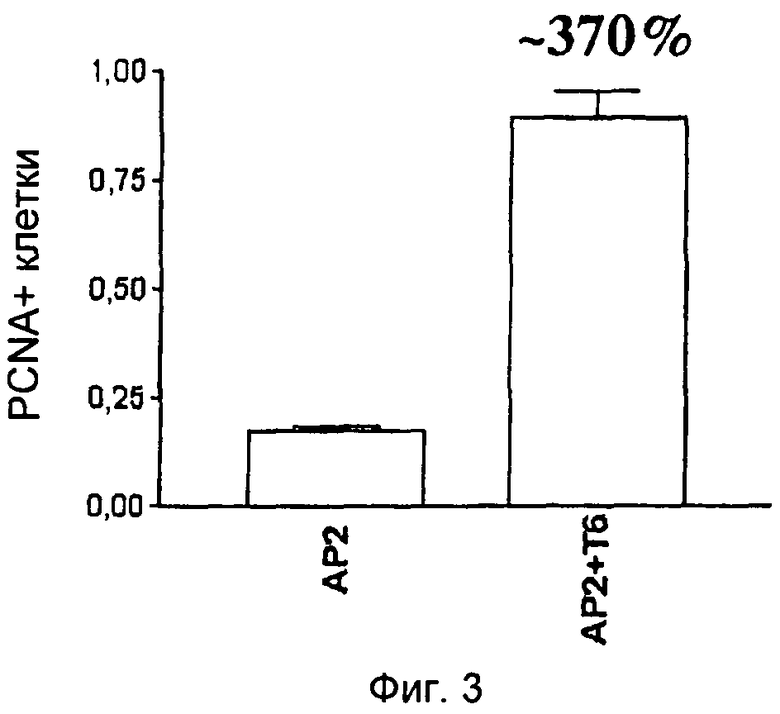
На Фиг.3 показано 370% увеличение (числа) PCNA-позитивных клеток в сокультурах астроглиальных клеток и 52-суточных астроглиальных культур.
Пролиферативная активность 31-суточных астроглиальных клеток в пассаже 2 (АР2) была слегка снижена по сравнению с первичной культурой без пассажа (видимая посредством экспрессии PCNA). Пролиферация значительно усиливалась добавлением HSC-T6 клеток в АР2 и дальнейшим совместным культивированием в течение 14 суток. Эффект HSC-T6 был даже большим, если последние смешивали с АР2 в суспензии клеток и одновременно культивировали на чашке Петри. Сильная пролиферация в смешанных культурах давала массовое отделение клеток от основания чашки (определяемое посредством больших зон густо растущих клеток, смежных с областями очень густых или очень разреженных распределений клеток). Тем не менее, в сокультуре даже в зонах с разреженным распределением клеток число PCNA-позитивных клеток было большим, чем в астроглиальной культуре без HSC.
Эффект HSC-T6 на процесс старения астроглиальных клеток
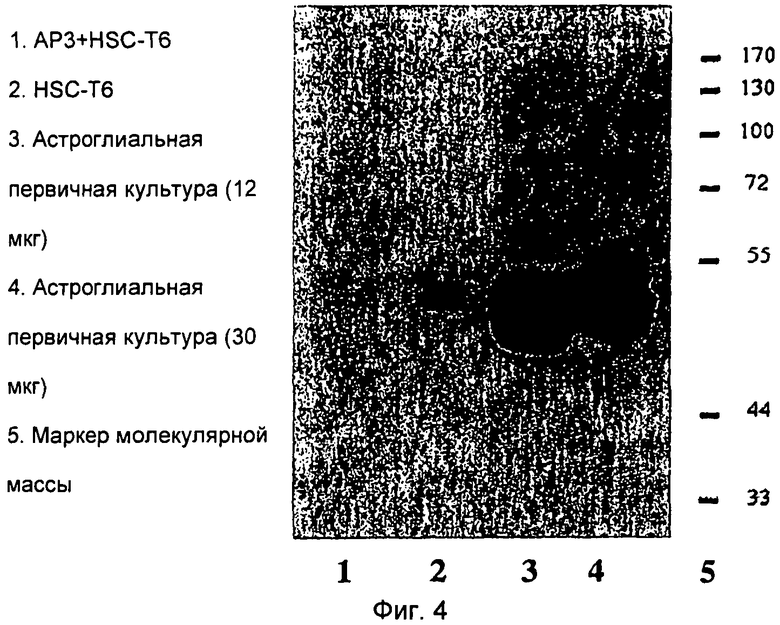
Для того чтобы выяснить этот эффект, проанализировали экспрессию GFAP в одних астроглиальных культурах и в сокультуре с HSC-T6 посредством вестерн-блоттинга. На Фиг.4 показана едва присутствующая экспрессия GFAP в сокультуре астроглиальных клеток с HSC-T6 (полоса 1 на Фиг.4) по сравнению с экспрессией GFAP в индивидуальных культурах HSC-T6 (полоса 2) или астроглиальных первичных культурах (полоса 3 и 4). Это указывает на очень сильную дифференцировку и, следовательно, на эффект задержки старения астроглиальных клеток посредством HSC.
Устойчивость к гипоксии астроглии и HSC-T6 клеток в сокультуре
В этой серии экспериментов астроглиальные клетки подвергали следующим условиям:
1. Только 43-суточные культуры из первого пассажа (Р1) культивировали при нормоксических условиях (NC). Нормоксический контроль.
2. 43-суточные культуры астроглиальных клеток из первого пассажа (Р1) культивировали в течение еще 10 суток при NC и затем переносили еще на 48 ч в гипоксические условия (НС) (1% O2, 10% СO2, 89% N3). Гипоксический контроль.
3. К 31-суточной астроглиальной культуре в Р1 добавляли 150000 HSC-T6 клеток и культивировали совместно при NC в течение еще 12 суток.
4. К 31-суточной астроглиальной культуре в Р1 добавляли 150000 HSC-T6 клеток и культивировали совместно в течение еще 10 суток при NC. Затем данную сокультуру подвергали НС в течение еще 48 ч.
Экспрессия нестина
Умеренную экспрессию нестина в GFAP-позитивных астроглиальных клетках наблюдали в первом пассаже (АР1) при нормоксических условиях. В этих культурах экспрессия нестина значительно снижалась при гипоксических условиях. После 12 суток сокультуры с HSC-T6 при NC скорость экспрессии нестина значительно возрастала. В 50% всей клеточной популяции интенсивность экспрессии нестина была больше, чем экспрессия GFAP. При НС интенсивность окрашивания нестина была даже выше, чем в контрольных культурах астроглиальных клеток без HSC при NC. В сокультуре клеток АР1 и HSC-T6 способность экспрессировать ацетилхолин поддерживалась даже при гипоксических условиях.
Экспрессия бета-III тубулина
Одновременное окрашивание бета-III тубулина и GFAP и отдельное окрашивание моноклональным антителом против бета-III тубулина показало только отдельные бета-III тубулин-позитивные клетки в АР1 при нормоксических и гипоксических условиях. После 12 суток в сокультуре с HSC-T6 число бета-III тубулин-позитивных клеток значительно возрастало как при NC, так и при НС. Некоторые из этих клеток показывали типично нейрональный фенотип (видимый за счет присутствия бета-III тубулина и отсутствия GFAP). При НС интенсивность окрашивания бета-III тубулина и число бета-III тубулин-позитивных клеток было аналогичным при NC и НС, но значительно большим, чем в монокультурах АР1 при NC.
Коэкспрессия глутаминсинтетазы (GS) и металлотионеина (МТ)
Клетки при NC в монокультуре АР1 слабо экспрессировали GS и почти не экспрессировали МТ как при NC, так и при НС. После 12 суток в сокультуре с HSC-T6 при NC, GS и МТ подвергались сильной регуляции. Большинство клеток коэкспрессировали GS и МТ. Во многих клетках преобладала экспрессия GS или МТ. При НС интенсивность окрашивания МТ в сокультурах была немного меньше, чем в сокультурах при NC. Тем не менее экспрессия GS и МТ в сокультурах при НС была значительно больше, чем в астроглиальной монокультуре при нормоксических условиях.
Коэкспрессия PCNA и каспазы 3
Лишь немного клеток в 43-суточных астроглиальных культурах в первом пассаже (АР1) экспрессировали PCNA при нормоксических условиях (NC). Большинство клеток также не содержало каспазу 3. Число клеток АР1 культур и интенсивность PCNA дополнительно снижались при гипоксических условиях. Совместное культивирование АР1 с HSC-T6 приводило к массовому увеличению (числа) PCNA-позитивных клеток при нормоксических и гипоксических условиях по сравнению с АР1 культурой при NC и НС. Усиление пролиферации в сокультурах давало массовое отделение клеток от основания чашки Петри, которое заметно по существованию больших конгломератов PCNA-позитивных клеток и прилегающих разреженных отдельно растущих клеток. В некоторых конгломератах экспрессия каспазы 3 практически полностью отсутствовала. В других, с другой стороны, была выявлена сильная экспрессия каспазы и PCNA. Это указывает на продукцию новых популяций клеток, способных к пролиферации, которая нейтрализуется апоптозом.
Настоящие результаты подтверждают защитные свойства линий клеток HSC, HSC-T6 и МС на астроглиальные первичные культуры. Эти свойства оценивали посредством следующих параметров:
1. увеличенное число нейронов (250-300% увеличение (числа) бета-III-тубулин-позитивных нейронов) в сокультурах;
2. активация покоящихся клеток;
3. повышенная экспрессия тирозин-гидроксилазы;
4. повышенная экспрессия GS и МТ, т.е. антицитотоксическая функция;
5. усиленная пролиферация клеток;
6. регенерация популяции астроцитов (наблюдаемая посредством увеличения интенсивности окрашивания нестина и 300% увеличения (числа) нестин-позитивных клеток);
7. увеличение нейрональной сети в сокультурах;
8. повышенная устойчивость к гипоксическим условиям, которая возникает из-за следующих эффектов:
а) усиленной пролиферации клеток при гипоксических условиях;
б) регенерации астроглиальных культур (более чем 300% увеличение (числа) нестин-позитивных клеток при нормоксии и гипокисии по сравнению с монокультурами);
в) повышенной экспрессии GS и МТ;
г) увеличенного числа нейронов (наблюдаемого посредством 300% увеличения бета-III тубулин-позитивных клеток).
Эти защитные свойства GFAP-позитивных клеток, не являющихся нервными, основаны на их долговременном эффекте на клетки ЦНС посредством:
1. продуцирования веществ, которые являются важными для дифференцировки и генерации нейронов;
2. эффектов задержки дифференцировки на астроциты, так как они принимают функцию дифференцированных астроцитов;
3. регенерации популяций нервных клеток посредством пролиферации;
4. собственной способности превращаться в нейроноподобные клетки.
2. Тесты in vivo
Защитный эффект линии клеток HSC-T6 для лечения рассеянного склероза
План теста:
Человеческий MOG (гликопротеин миелиновых олигодендроцитов) вводят внутривенно в концентрации 50 мкг/животное 18 крысам GA в возрасте приблизительно 1 месяц. Через 24 ч животных делили на 2 группы: группа 1 получала 5000000 клеток внутривенно (в растворе PBS (фосфатно-солевой буферный раствор)), причем в случае 2 животных из этой группы вводили флуоресцентно меченые клетки; группа 2 (контрольная группа) внутривенно получала только PBS. Звездчатые клетки печени в форме линии клеток HSC-T6 использовали в качестве клеток, соответствующих ППДК. В случае 2 животных из группы 1 флуоресцентно меченые клетки вводили внутривенно для того, чтобы определить доступность и стойкость введенных клеток в ЦНС. Этих животных препарировали через 11 суток. Кроме того, в случае 2 нормальных (наивных) крыс, у которых не была проведена индукция ЕАЕ (экспериментальный аутоиммунный энцефаломиелит) посредством MOG, внутривенно вводили то же самое количество флуоресцентно меченых клеток. Эти контрольные животные должны иметь меньшую популяцию HSC-T6 в ЦНС, так как гематоэнцефалический барьер у этих животных оставался интактным. Животных, обработанных MOG, наблюдали ежесуточно согласно последующей неврологической «оценке в баллах».
Результаты
Животных ежесуточно тестировали на экстраординарные моторные характеристики согласно следующим критериям:
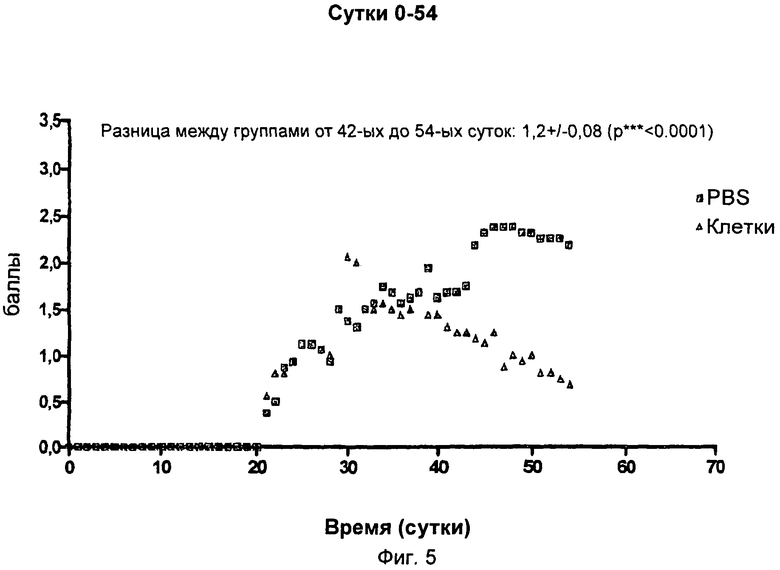
Промежуточное состояние неврологического статуса перечислено на Фиг.5.
Целиком заболевание развивалось у большей части популяции животных на 10-ой неделе после введения MOG. Начиная с этого времени группа с введением клеток показывала значительное улучшение неврологического статуса (баллы) в дальнейшем курсе (от суток 42 до 54). Группа с обработкой клетками (зеленая кривая на Фиг.5) имела средний балл 0,9±0,05 (n=8), тогда как группа, обработанная PBS (красная кривая на Фиг.1), показывала средний балл 2,21±0,06 (n=8). Следовательно, средняя разница между группой 1 («клетки» на Фиг.5) и группой 2 («PBS») составляла балл 1,2±0,08, который подразумевал значительное улучшение неврологических симптомов.
Идентификация HSC-T6, меченых CGDA, в разных областях мозга MS крыс и наивных необработанных животных
Для того чтобы доказать стойкость HSC-T6 в разных областях мозга в случае внутривенного введения 5000000 клеток, готовили последовательные срезы мозга животных, которые получали меченые CFDA флуоресцентные клетки HSC-T6, и тестировали флуоресцентной микроскопией.
Многочисленные популяции клеток идентифицировали в мозжечке (Фиг.6А), префронтальной коре (Фиг.6Б) и в гиппокампе (Фиг.6В) у MS животных, тогда как в случае наивных крыс (без введения MOG) были обнаружены только отдельные клетки исключительно в гиппокампе (Фиг.6Г).
Проиллюстрированные выше результаты недвусмысленно подтверждают преимущества, достигнутые настоящим изобретением, в частности:
1. Введение HSC-T6 клеток, которые имеют стабильный дифференцированный фенотип, приводит к значительному улучшению неврологических симптомов у животного-экспериментальной модели рассеянного склероза (MS);
2. Обогащение HSC-T6 посредством внутривенного введения значительно отличается случае MS животных и наивных животных с неповрежденным гематоэнцефалическим барьером и показывает, что только в случае запущенного заболевания, при котором поврежден гематоэнцефалический барьер, большое число клеток в самом деле мигрирует в ЦНС, тогда как только отдельные клетки могут достичь ЦНС у здоровых животных.
3. Животные, которым вводили клетки, не показали дополнительной токсической или канцерогенной реакции на введение клеток (ни здоровые наивные крысы, ни MS животные), так что применение данных клеток может считаться безопасным с токсикологической точки зрения.
Длительная культура
Кратковременная культура
Кратковременная культура
Длительная культура

Настоящая группа изобретений относится к медицине, а именно к неврологии, и касается лечения дегенерировавших органов в патологическом состоянии, в частности нейродегенеративных заболеваний. Для этого вводят лекарственное средство, содержащее фенотипически стабильно дифференцирующиеся или дифференцированные GFAP-положительные клетки, имеющие признаки дифференцирования, противоположные астроцитам в отношении по меньшей мере одного экспрессируемого гена. Это обеспечивает эффективное лечение нейродегенеративных заболеваний за счет экспрессии указанными клетками нейронспецифичных белков, обладающих детоксикационным действием и улучшающих нейропередачу. 2 н. и 3 з.п. ф-лы, 1 табл., 6 ил.
1. Применение фенотипически стабильно дифференцирующихся или дифференцированных GFAP (глиальный фибриллярный кислый белок)-позитивных клеток, имеющих признаки дифференцирования, противоположные астроцитам, так что степень активации, регуляции и/или дифференцировки GFAP-положительных клеток является противоположной степени активации, регуляции и/или дифференцировки астроцитов в отношении по меньшей мере одного экспрессируемого гена, для производства лекарственного средства для лечения нейродегенеративного заболевания, и/или для лечения заболевания, характеризующегося потерей нейронов, и/или для лечения заболевания, характеризующегося потерей нейрональной функциональности.
2. Применение по п.1, где указанные клетки представляют собой клетки печени и/или клетки почки.
3. Применение по любому из пп.1 или 2, где клетки представляют собой звездчатые клетки печени, мезангиальные клетки, звездчатые клетки поджелудочной железы, дендритные клетки селезенки и/или фибробласты кожи.
4. Применение по п.1, где заболевание представляет собой болезнь Альцгеймера, рассеянный склероз и/или болезнь Паркинсона.
5. Фармацевтический агент, полученный путем применения фенотипически стабильно дифференцирующихся или дифференцированных клеток по любому из пп.1-4.
| RU 2005131581 A 27.04.2006 | |||
| WO2004020601 A2 11.03.2004 | |||
| DANIELYAN L | |||
| et al | |||
| "Colocalization of glial fibrillary acidic protein, metallothionein, and MHC II in human,rat,NOD/SCID, and mouse skin keratinocytes and fibroblasts" | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| BUNIATIAN GH | |||
| Et | |||
Авторы
Даты
2014-09-10—Публикация
2008-04-18—Подача